Заміщені тіофени, спосіб їх одержання, їх застосування як ліків або діагностичних реагентів та ліки, що їх вміщують
Номер патенту: 77551
Опубліковано: 15.12.2006
Автори: Бляйх Маркус, Хайнельт Уве, Гекле Міхель, Ланг Ханс-Йохен, Вірт Клаус, Хофмайстер Армін
Формула / Реферат
1. Сполуки формули (І):
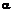
де
R1 і R2, незалежно один від одного, означають Н, F, Сl, Br, I, CN, NO2, -(X)n-CqH2q-Z, циклоалкіл з 3, 4, 5 або 6 атомами вуглецю, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл або алкілалкініл з 3 або 4 атомами вуглецю;
n означає нуль або 1;
Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k;
k означає нуль, 1 або 2;
q означає нуль, 1, 2, 3, 4, 5 або 6;
Ζ означає атом водню або CmF2m+1;
m означає нуль, 1, 2, 3 або 4;
R3 означає атом водню, метил, F, Сl, Br, І, CN, S(O)k-CH3, -NO2 або -O-СН3;
k означає нуль, 1 або 2;
R4 означає атом водню, циклоалкіл з 3, 4, 5 або 6 атомами вуглецю, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл або алкілалкініл з 3 або 4 атомами вуглецю або -CrH2r-Y;
r означає нуль, 1, 2, 3 або 4;
Υ означає атом водню або трифторметил;
R5 і R6 означають атом водню або разом означають зв'язок;
R7 і R8, незалежно один від одного, означають (С3-С5)-алкіл-, (С2-С5)-алкеніл, (С2-С5)-алкініл, (С3-С6)-циклоалкіл або (С4-С6)-циклоалкеніл;
або
R7 і R8 разом означають алкіленовий ланцюг, що складається з 3-8 атомів вуглецю, причому його атоми водню можуть бути не заміщені, частково або повністю заміщені атомами фтору;
або
R7 і R8 разом означають залишок
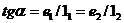 ,
,
причому R5 і R6 разом утворюють зв'язок;
R10 і R11, незалежно один від одного, означають атом водню, фтору, хлору, брому, метил, CN, ОН, -O-СН3, NO2, NH2 або -СF3;
R9 і R12 означають атом водню або F;
або
один із замісників R9 і R12 означає атом водню, а інший означає F, Сl, Вг, І, CN, NO2, СООН, CO-NR13R14, SO2-NR13R14, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл, алкілалкініл з 3 або 4 атомами вуглецю або -(X)n-CqH2q-Z;
R13 і R14, однакові або різні, означають атом водню або алкіл з 1, 2, 3 або 4 атомами вуглецю;
або
R13 і R14 разом з атомом азоту, з яким вони зв'язані, утворюють насичений 5-, 6- або 7-членний цикл;
n означає нуль або 1;
Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k;
k означає нуль, 1 або 2;
q означає нуль, 1, 2, 3, 4, 5 або 6;
і
Ζ означає атом водню або СmF2m+1;
m означає нуль, 1, 2, 3 або 4;
а також їх фармацевтично прийнятні солі, а також їх солі трифтороцтової кислоти.
2. Сполуки за п. 1, в яких
R1 і R2, незалежно один від одного, означають Н, F, Сl, Вr, СН3, СF3, SO2СН3 або SO2NH2, причому, щонайбільше один із замісників R1 і R2 означає атом водню;
R3 означає атом водню, F або Сl;
R4 означає атом водню, алкіл з 1, 2, 3 або 4 атомами вуглецю або циклопропіл;
R5 і R6 означають атом водню або разом означають зв'язок;
R7 і R8 разом означають алкіленовий ланцюг, що складається з 3, 4, 5, 6, 7 або 8 атомів вуглецю;
або
R7 і R8 разом означають залишок
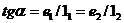 ,
,
причому R5 і R6 разом утворюють зв'язок;
R10 і R11, незалежно один від одного, означають атом водню, ОН, атом фтору або хлору;
R9 і R12 означають атом водню;
або
один із замісників R9 і R12 означає атом водню, а інший означає F, Сl, Br, CN, СООН, CO-NR13R14, SO2-NR13R14 або -(X)n-CqH2q-Z;
R13 і R14, однакові або різні, означають атом водню або метил;
n означає нуль або 1;
Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k;
k означає нуль, 1 або 2;
q означає нуль, 1, 2, 3 або 4;
Ζ означає атом водню або СF3;
а також їх фармацевтично прийнятні солі, а також їх солі трифтороцтової кислоти.
3. Сполуки за п. 1 і/або 2, в яких
R1 і R2, незалежно один від одного, означають F, Сl, Br, СН3 або СF3;
R3 означає атом водню;
R4 означає атом водню, метил або етил;
R5 і R6 означають атом водню або разом означають зв'язок;
R7 і R8 разом означають алкіленовий ланцюг, що складається з 3, 4, 5, 6, 7 або 8 атомів вуглецю;
або
R7 і R8 разом означають залишок
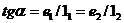 ,
,
причому R5 і R6 разом утворюють зв'язок;
R10 і R11, незалежно один від одного, означають атом водню, ОН або атом фтору;
R9 і R12 означають атом водню;
або
один із замісників R9 і R12 означає атом водню, а інший означає F, Сl, Вr або -(X)n-CqH2q-Z;
n означає нуль або 1;
Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k;
k означає нуль, 1 або 2;
q означає нуль або 1;
Ζ означає атом водню або СF3;
а також їх фармацевтично прийнятні солі, а також їх солі трифтороцтової кислоти.
4. Сполуки формули (І) за одним або декількома з пп. 1, 2 і 3, вибрані з групи, що включає
транс-R,R-2-хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-4-метил-3-тієніламін;
транс-R,R-2-бром-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-4-метил-3-тієніламін;
2-хлор-3N-(2-бензімідазоліл)-4-метил-3-тієніламін;
2-бром-3N-(2-бензімідазоліл)-4-метил-3-тієніламін;
2-хлор-3N-(4-метил-2-бензімідазоліл)-4-метил-3-тієніламін;
2-хлор-3N-(5-фтор-2-бензімідазоліл)-4-метил-3-тієніламін;
2-хлор-3N-(4-хлор-2-бензімідазоліламіно)-4-метилтіофен;
2-бром-3N-(4-хлор-2-бензімідазоліламіно)-4-метилтіофен;
2-бром-3N-(4-фтор-2-бензімідазоліламіно)-4-метилтіофен;
2-хлор-3N-(4-фтор-2-бензімідазоліламіно)-4-метилтіофен;
2-хлор-3N-(4-гідрокси-2-бензімідазоліламіно)-4-метилтіофен;
(1Н-бензімідазол-2-іл)-(2-хлор-4-метилтіофен-3-іл)метиламін;
(2-бром-4-метилтіофен-3-іл)-(5-фтор-1Н-бензімідазол-2-іл)амін;
2-хлор-3N-(2-бензімідазоліламіно)-4-метилтіофен;
2,4-дихлор-3N-(2-бензімідазоліламіно)тіофен;
2-бром-4-хлор-3N-(2-бензімідазоліламіно)тіофен;
2,4-дихлор-3N-(4-метил-2-бензімідазоліламіно)тіофен;
транс-R,R-2,4-дихлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-3-тієніламін і
2,4-дихлор-3N-(4-хлор-2-бензімідазоліламіно)тіофен;
а також їх фармацевтично прийнятні солі.
5. Сполуки формули (І) і/або їх фармацевтично прийнятні солі за одним або декількома з пп. 1-4, придатні як лікарський засіб.
6. Застосування сполуки формули (І) і/або її фармацевтично прийнятних солей за одним або декількома з пп. 1-4 для отримання лікарського засобу для лікування або профілактики порушень дихального імпульсу, особливо зумовлених сном порушень дихання, таких як зупинки дихання увісні, або хропіння; для лікування або профілактики гострих і хронічних захворювань нирок, особливо гострої ниркової недостатності або хронічної ниркової недостатності, або порушень функції кишечнику; для лікування або профілактики високого кров'яного тиску, особливо есенціальної гіпертонії, захворювань центральної нервової системи, особливо захворювань, які є результатом підвищеної збудливості центральної нервової системи, таких як епілепсія або судоми, що провокуються центральною нервовою системою, і захворювань центральної нервової системи, особливо станів страху, депресій і психозів; для лікування або профілактики гострих і хронічних ушкоджень, захворювань і опосередкованих подальших захворювань органів або тканин, зумовлених явищами ішемії або реперфузії, аритмій, атеросклерозу, гіперхолестеринемії, захворювань, первинною або вторинною причиною яких є проліферація клітин раку, гіпертрофії або гіперплазії простати, фіброзних захворювань внутрішніх органів, серцевої недостатності або застійної серцевої недостатності, тромбозів, порушень функції жовчного міхура, ураження ектопаразитами, захворювань внаслідок ендотеліальної дисфункції, синдрому Шарко, протозойних захворювань, особливо малярії; для лікування станів шоку, діабету і діабетичних пізніх ушкоджень, гострих або хронічних запальних захворювань; а також для отримання лікарського засобу для консервації і зберігання трансплантатів для хірургічних заходів, для отримання лікарського засобу для використання при хірургічних операціях і трансплантаціях органів; для отримання лікарського засобу для запобігання зумовленій старінням зміні тканин, для збереження здоров'я і збільшення тривалості життя, для зменшення цитотоксичних ефектів або для застосування як діагностичні засоби.
7. Застосування за п. 6 сполуки формули (І) і/або її фармацевтично прийнятних солей для отримання лікарського засобу для лікування або профілактики порушень дихального імпульсу, особливо зумовлених сном порушень дихання, таких як зупинки дихання увісні.
8. Застосування за п. 6 сполуки формули (І) і/або її фармацевтично прийнятних солей для отримання лікарського засобу для лікування або профілактики хропіння.
9. Застосування за п. 6 сполуки формули (І) і/або її фармацевтично прийнятних солей для отримання лікарського засобу для лікування або профілактики гострих і хронічних захворювань нирок, особливо гострої ниркової недостатності або хронічної ниркової недостатності.
10. Застосування за п. 6 сполуки формули (І) і/або її фармацевтично прийнятних солей для отримання лікарського засобу для лікування або профілактики порушень функцій кишечнику.
11. Застосування сполуки формули (І) і/або її фармацевтично прийнятних солей за одним або декількома з пп.1-4 в комбінації з іншими лікарськими засобами або біологічно активними речовинами для отримання лікарського засобу для лікування або профілактики порушень дихального імпульсу, особливо зумовлених сном порушень дихання, таких як зупинки дихання увісні, або хропіння; для лікування або профілактики гострих і хронічних захворювань нирок, особливо гострої ниркової недостатності або хронічної ниркової недостатності, або порушень функції кишечнику; для лікування або профілактики високого кров'яного тиску, особливо есенціальної гіпертонії, захворювань центральної нервової системи, особливо захворювань, які є результатом підвищеної збудливості центральної нервової системи, таких як епілепсія або судоми, що провокуються центральною нервовою системою, і захворювань центральної нервової системи, особливо станів страху, депресій і психозів; для лікування або профілактики гострих і хронічних ушкоджень, захворювань і опосередкованих подальших захворювань органів або тканин, зумовлених явищами ішемії або реперфузії, аритмій, атеросклерозу, гіперхолестеринемії, захворювань, первинною або вторинною причиною яких є проліферація клітин раку, гіпертрофії або гіперплазії простати, фіброзних захворювань внутрішніх органів, серцевої недостатності або застійної серцевої недостатності, тромбозів, порушень функції жовчного міхура, ураження ектопаразитами, захворювань внаслідок ендотеліальної дисфункції, синдрома Шарко, протозойних захворювань, особливо малярії; для лікування станів шоку, діабету і діабетичних пізніх ушкоджень, гострих або хронічних запальних захворювань; або для отримання лікарського засобу для консервації і зберігання трансплантатів для хірургічних заходів, для отримання лікарського засобу для використання при хірургічних операціях і трансплантаціях органів; для отримання лікарського засобу для запобігання зумовленій старінням зміні тканин, для збереження здоров'я і збільшення тривалості життя і для зменшення цитотоксичних ефектів.
12. Застосування за п. 11 сполуки формули (І) і/або її фармацевтично прийнятних солей в комбінації з іншими лікарськими засобами або біологічно активними речовинами для отримання лікарського засобу для лікування або профілактики порушень дихального імпульсу, особливо зумовлених сном порушень дихання, таких як зупинки дихання увісні.
13. Застосування за п. 11 сполуки формули (І) і/або її фармацевтично прийнятних солей в комбінації з іншими лікарськими засобами або біологічно активними речовинами для отримання лікарського засобу для лікування або профілактики хропіння.
14. Застосування за п. 11 сполуки формули (І) і/або її фармацевтично прийнятних солей в комбінації з іншими лікарськими засобами або біологічно активними речовинами для отримання лікарського засобу для лікування або профілактики гострих і хронічних захворювань нирок, особливо гострої ниркової недостатності або хронічної ниркової недостатності.
15. Застосування за п. 11 сполуки формули (І) і/або її фармацевтично прийнятних солей в комбінації з іншими лікарськими засобами або біологічно активними речовинами для отримання лікарського засобу для лікування або профілактики порушень функції кишечнику.
16. Лікарський засіб, призначений для людини, тварини або для фітозахисту, що містить ефективну кількість сполуки формули (І) і/або її фармацевтично прийнятної солі за одним або декількома з пп. 1-4 разом з фармацевтично прийнятними носіями і домішками.
17. Лікарський засіб за п. 16, який відрізняється тим, що містить ефективну кількість сполуки формули (І) і/або її фармацевтично прийнятної солі за одним або декількома з пп. 1-4 разом з фармацевтично прийнятними носіями і домішками в комбінації з іншими фармакологічними біологічно активними речовинами або лікарськими засобами.
Текст
1. Сполуки формули (І): 2 (19) 1 C2 (54) ЗАМІЩЕНІ ТІОФЕНИ, СПОСІБ ЇХ ОДЕРЖАННЯ, ЇХ ЗАСТОСУВАННЯ ЯК ЛІКІВ АБО ДІАГНОСТИЧНИХ РЕАГЕНТІВ ТА ЛІКИ, ЩО ЇХ ВМІЩУЮТЬ 3 77551 4 або один із замісників R9 і R12 означає атом водню, а R7 і R8 разом означають алкіленовий ланцюг, що інший означає F, Сl, Br, CN, СООН, CO-NR13R14, складається з 3-8 атомів вуглецю, причому його SO2-NR13R14 або -(X)n-CqH2q-Z; атоми водню можуть бути не заміщені, частково R13 і R14, однакові або різні, означають атом водабо повністю заміщені атомами фтору; ню або метил; або n означає нуль або 1; R7 і R8 разом означають залишок Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k; R12 R11 k означає нуль, 1 або 2; q означає нуль, 1, 2, 3 або 4; Ζ означає атом водню або СF3; R10 а також їх фармацевтично прийнятні солі, а також їх солі трифтороцтової кислоти. R9 3. Сполуки за п. 1 і/або 2, в яких , R1 і R2, незалежно один від одного, означають F, причому R5 і R6 разом утворюють зв'язок; Сl, Br, СН3 або СF3; R10 і R11, незалежно один від одного, означають R3 означає атом водню; атом водню, фтору, хлору, брому, метил, CN, ОН, R4 означає атом водню, метил або етил; -O-СН3, NO2, NH2 або -СF3; R5 і R6 означають атом водню або разом означаR9 і R12 означають атом водню або F; ють зв'язок; або R7 і R8 разом означають алкіленовий ланцюг, що один із замісників R9 і R12 означає атом водню, а складається з 3, 4, 5, 6, 7 або 8 атомів вуглецю; інший означає F, Сl, Вг, І, CN, NO2, СООН, COабо NR13R14, SO2-NR13R14, алкеніл з 2, 3 або 4 атоR7 і R8 разом означають залишок мами вуглецю, алкенілалкіл з 3 або 4 атомами R12 R11 вуглецю, етиніл, алкілалкініл з 3 або 4 атомами вуглецю або -(X)n-CqH2q-Z; R13 і R14, однакові або різні, означають атом водR10 ню або алкіл з 1, 2, 3 або 4 атомами вуглецю; або R9 R13 і R14 разом з атомом азоту, з яким вони зв'я, зані, утворюють насичений 5-, 6- або 7-членний причому R5 і R6 разом утворюють зв'язок; цикл; R10 і R11, незалежно один від одного, означають n означає нуль або 1; атом водню, ОН або атом фтору; Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k; R9 і R12 означають атом водню; k означає нуль, 1 або 2; або q означає нуль, 1, 2, 3, 4, 5 або 6; один із замісників R9 і R12 означає атом водню, а і інший означає F, Сl, Вr або -(X)n-CqH2q-Z; Ζ означає атом водню або СmF2m+1; n означає нуль або 1; m означає нуль, 1, 2, 3 або 4; Χ означає атом кисню, ΝΗ, N-СН3 або S(O)k; а також їх фармацевтично прийнятні солі, а також k означає нуль, 1 або 2; їх солі трифтороцтової кислоти. q означає нуль або 1; 2. Сполуки за п. 1, в яких Ζ означає атом водню або СF3; R1 і R2, незалежно один від одного, означають Н, а також їх фармацевтично прийнятні солі, а також F, Сl, Вr, СН3, СF3, SO2СН3 або SO2NH2, причому, їх солі трифтороцтової кислоти. щонайбільше один із замісників R1 і R2 означає 4. Сполуки формули (І) за одним або декількома з атом водню; пп. 1, 2 і 3, вибрані з групи, що включає R3 означає атом водню, F або Сl; транс-R,R-2-хлор-3N-(3а,4,5,6,7,7а-гексагідро-1НR4 означає атом водню, алкіл з 1, 2, 3 або 4 ато2-бензімідазоліл)-4-метил-3-тієніламін; мами вуглецю або циклопропіл; транс-R,R-2-бром-3N-(3а,4,5,6,7,7а-гексагідро-1НR5 і R6 означають атом водню або разом означа2-бензімідазоліл)-4-метил-3-тієніламін; ють зв'язок; 2-хлор-3N-(2-бензімідазоліл)-4-метил-3-тієніламін; R7 і R8 разом означають алкіленовий ланцюг, що 2-бром-3N-(2-бензімідазоліл)-4-метил-3-тієніламін; складається з 3, 4, 5, 6, 7 або 8 атомів вуглецю; 2-хлор-3N-(4-метил-2-бензімідазоліл)-4-метил-3або тієніламін; R7 і R8 разом означають залишок 2-хлор-3N-(5-фтор-2-бензімідазоліл)-4-метил-3R12 R11 тієніламін; 2-хлор-3N-(4-хлор-2-бензімідазоліламіно)-4метилтіофен; R10 2-бром-3N-(4-хлор-2-бензімідазоліламіно)-4метилтіофен; R9 2-бром-3N-(4-фтор-2-бензімідазоліламіно)-4, метилтіофен; причому R5 і R6 разом утворюють зв'язок; 2-хлор-3N-(4-фтор-2-бензімідазоліламіно)-4R10 і R11, незалежно один від одного, означають метилтіофен; атом водню, ОН, атом фтору або хлору; 2-хлор-3N-(4-гідрокси-2-бензімідазоліламіно)-4R9 і R12 означають атом водню; метилтіофен; або 5 77551 6 (1Н-бензімідазол-2-іл)-(2-хлор-4-метилтіофен-3влених сном порушень дихання, таких як зупинки іл)метиламін; дихання увісні. (2-бром-4-метилтіофен-3-іл)-(5-фтор-1Н8. Застосування за п. 6 сполуки формули (І) і/або її бензімідазол-2-іл)амін; фармацевтично прийнятних солей для отримання 2-хлор-3N-(2-бензімідазоліламіно)-4-метилтіофен; лікарського засобу для лікування або профілакти2,4-дихлор-3N-(2-бензімідазоліламіно)тіофен; ки хропіння. 2-бром-4-хлор-3N-(2-бензімідазоліламіно)тіофен; 9. Застосування за п. 6 сполуки формули (І) і/або її 2,4-дихлор-3N-(4-метил-2фармацевтично прийнятних солей для отримання бензімідазоліламіно)тіофен; лікарського засобу для лікування або профілактитранс-R,R-2,4-дихлор-3N-(3а,4,5,6,7,7а-гексагідроки гострих і хронічних захворювань нирок, особли1Н-2-бензімідазоліл)-3-тієніламін і во гострої ниркової недостатності або хронічної 2,4-дихлор-3N-(4-хлор-2ниркової недостатності. бензімідазоліламіно)тіофен; 10. Застосування за п. 6 сполуки формули (І) і/або а також їх фармацевтично прийнятні солі. її фармацевтично прийнятних солей для отриман5. Сполуки формули (І) і/або їх фармацевтично ня лікарського засобу для лікування або профілакприйнятні солі за одним або декількома з пп. 1-4, тики порушень функцій кишечнику. придатні як лікарський засіб. 11. Застосування сполуки формули (І) і/або її фа6. Застосування сполуки формули (І) і/або її фаррмацевтично прийнятних солей за одним або декімацевтично прийнятних солей за одним або декількома з пп.1-4 в комбінації з іншими лікарськими лькома з пп. 1-4 для отримання лікарського засобу засобами або біологічно активними речовинами для лікування або профілактики порушень дихадля отримання лікарського засобу для лікування льного імпульсу, особливо зумовлених сном поабо профілактики порушень дихального імпульсу, рушень дихання, таких як зупинки дихання увісні, особливо зумовлених сном порушень дихання, або хропіння; для лікування або профілактики гостаких як зупинки дихання увісні, або хропіння; для трих і хронічних захворювань нирок, особливо гослікування або профілактики гострих і хронічних трої ниркової недостатності або хронічної ниркової захворювань нирок, особливо гострої ниркової недостатності, або порушень функції кишечнику; недостатності або хронічної ниркової недостатносдля лікування або профілактики високого кров'яноті, або порушень функції кишечнику; для лікування го тиску, особливо есенціальної гіпертонії, захвоабо профілактики високого кров'яного тиску, особрювань центральної нервової системи, особливо ливо есенціальної гіпертонії, захворювань центразахворювань, які є результатом підвищеної збудльної нервової системи, особливо захворювань, ливості центральної нервової системи, таких як які є результатом підвищеної збудливості центраепілепсія або судоми, що провокуються центральльної нервової системи, таких як епілепсія або ною нервовою системою, і захворювань центральсудоми, що провокуються центральною нервовою ної нервової системи, особливо станів страху, десистемою, і захворювань центральної нервової пресій і психозів; для лікування або профілактики системи, особливо станів страху, депресій і психогострих і хронічних ушкоджень, захворювань і опозів; для лікування або профілактики гострих і хросередкованих подальших захворювань органів або нічних ушкоджень, захворювань і опосередкованих тканин, зумовлених явищами ішемії або реперфуподальших захворювань органів або тканин, зумозії, аритмій, атеросклерозу, гіперхолестеринемії, влених явищами ішемії або реперфузії, аритмій, захворювань, первинною або вторинною причиатеросклерозу, гіперхолестеринемії, захворювань, ною яких є проліферація клітин раку, гіпертрофії первинною або вторинною причиною яких є проабо гіперплазії простати, фіброзних захворювань ліферація клітин раку, гіпертрофії або гіперплазії внутрішніх органів, серцевої недостатності або простати, фіброзних захворювань внутрішніх оргазастійної серцевої недостатності, тромбозів, понів, серцевої недостатності або застійної серцевої рушень функції жовчного міхура, ураження ектонедостатності, тромбозів, порушень функції жовчпаразитами, захворювань внаслідок ендотеліального міхура, ураження ектопаразитами, захворюної дисфункції, синдрому Шарко, протозойних вань внаслідок ендотеліальної дисфункції, синдзахворювань, особливо малярії; для лікування рома Шарко, протозойних захворювань, особливо станів шоку, діабету і діабетичних пізніх ушкомалярії; для лікування станів шоку, діабету і діабеджень, гострих або хронічних запальних захворютичних пізніх ушкоджень, гострих або хронічних вань; а також для отримання лікарського засобу запальних захворювань; або для отримання лікардля консервації і зберігання трансплантатів для ського засобу для консервації і зберігання транспхірургічних заходів, для отримання лікарського лантатів для хірургічних заходів, для отримання засобу для використання при хірургічних операціях лікарського засобу для використання при хірургічі трансплантаціях органів; для отримання лікарсьних операціях і трансплантаціях органів; для кого засобу для запобігання зумовленій старінням отримання лікарського засобу для запобігання зміні тканин, для збереження здоров'я і збільшензумовленій старінням зміні тканин, для збереження тривалості життя, для зменшення цитотоксичня здоров'я і збільшення тривалості життя і для них ефектів або для застосування як діагностичні зменшення цитотоксичних ефектів. засоби. 12. Застосування за п. 11 сполуки формули (І) 7. Застосування за п. 6 сполуки формули (І) і/або її і/або її фармацевтично прийнятних солей в комбіфармацевтично прийнятних солей для отримання нації з іншими лікарськими засобами або біологічлікарського засобу для лікування або профілактино активними речовинами для отримання лікарськи порушень дихального імпульсу, особливо зумокого засобу для лікування або профілактики порушень дихального імпульсу, особливо зумов 7 77551 8 лених сном порушень дихання, таких як зупинки нації з іншими лікарськими засобами або біологічдихання увісні. но активними речовинами для отримання лікарсь13. Застосування за п. 11 сполуки формули (І) кого засобу для лікування або профілактики поруі/або її фармацевтично прийнятних солей в комбішень функції кишечнику. нації з іншими лікарськими засобами або біологіч16. Лікарський засіб, призначений для людини, но активними речовинами для отримання лікарсьтварини або для фітозахисту, що містить ефектикого засобу для лікування або профілактики вну кількість сполуки формули (І) і/або її фармацехропіння. втично прийнятної солі за одним або декількома з 14. Застосування за п. 11 сполуки формули (І) пп. 1-4 разом з фармацевтично прийнятними носіі/або її фармацевтично прийнятних солей в комбіями і домішками. 17. Лікарський засіб за п. 16, який відрізняється нації з іншими лікарськими засобами або біологічно активними речовинами для отримання лікарсьтим, що містить ефективну кількість сполуки форкого засобу для лікування або профілактики мули (І) і/або її фармацевтично прийнятної солі за гострих і хронічних захворювань нирок, особливо одним або декількома з пп. 1-4 разом з фармацевгострої ниркової недостатності або хронічної ниртично прийнятними носіями і домішками в комбікової недостатності. нації з іншими фармакологічними біологічно акти15. Застосування за п. 11 сполуки формули (І) вними речовинами або лікарськими засобами. і/або її фармацевтично прийнятних солей в комбі Винахід відноситься до сполук типу заміщених похідних тіофену формули (І). Лікарські засоби, що містять сполуки цього типу, корисні при попередженні або лікуванні різних захворювань. Так, сполуки можна застосовувати, зокрема, для лікування порушень дихання і хропіння, а також для поліпшення дихального імпульсу, для лікування гострих і хронічних захворювань, для лікування захворювань, що викликаються ішемічними і/або реперфузійними явищами, а також проліферативними або фіброзними явищами, для лікування або профілактики захворювань центральної нервової системи, жирового обміну і діабету, згортання крові і ураження паразитами. Винахід відноситься до сполук формули (І): , де R1 і R2, незалежно один від одного, означають Н, F, СІ, Br, I, CN, NO2, -(X)n-CqH2q-Z, циклоалкіл з 3, 4, 5 або 6 атомами вуглецю, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл або алкілалкініл з 3 або 4 атомами вуглецю; n означає нуль або 1; X означає атом кисню, NH, N-CH3, S(O)k; k означає нуль, 1 або 2; q означає нуль, 1, 2, 3, 4, 5 або 6; Ζ означає атом водню або CmF2m+1; m означає нуль, 1, 2, 3 або 4; R3 означає атом водню, метил, F, СІ, Br, I, CN, S(O)k-CH3, -NO2, -O-CH3; k означає нуль, 1 або 2; R4 означає атом водню, циклоалкіл з 3, 4, 5 або 6 атомами вуглецю, алкеніл з 2, 3 або 4 ато мами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл або алкілалкініл з 3 або 4 атомами вуглецю, -CrH2r-Y; r означає нуль, 1, 2, 3 або 4; Υ означає атом водню або трифторметил; R5 і R6 означають атом водню або разом означають зв'язок; R7 і R8, незалежно один від одного, означають (С3-С5)-алкіл, (С2-С5)-алкеніл, (С2-С5)-алкініл, (С3С6)-циклоалкіл або (С4-С6)-циклоалкеніл; або R7 і R8 разом означають алкіленовий ланцюг, що складається з 3-8 атомів вуглецю, причому атоми водню в ланцюгу можуть бути не заміщені, частково або повністю заміщені атомами фтору; або R7 і R8 разом означають залишок , причому R5 і R6 разом утворюють зв'язок; R10 і R11, незалежно один від одного, означають атом водню, фтору, хлору, брому, метил, CN, ОН, -О-СН3, ΝΟ2, ΝΗ2 або -CF3; R9 і R12 означають атом водню або F; або один із замісників R9 і R12 означає атом водню, а інший означає F, СІ, Вr, І, CN, NO2, СООН, CO-NR13R14, SO2-NR13R14, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл, алкілалкініл з 3 або 4 атомами вуглецю або -(X)n-CqH2q-Z; R13 і R14, однакові або різні, означають атом водню або алкіл з 1, 2, 3 або 4 атомами вуглецю; або R13 і R14 разом з атомом азоту, з яким вони пов'язані, утворюють насичений 5-, 6- або 7-членний цикл; 9 77551 10 n означає нуль або 1; n означає нуль або 1; X означає атом кисню, NH, N-CH3, S(O)k; X означає атом кисню, NH, N-CH3, S(O)k; k означає нуль, 1 або 2; k означає нуль, 1 або 2; q означає нуль, 1, 2, 3, 4, 5 або 6; q означає нуль, 1, 2, 3, 4, 5 або 6; і і Ζ означає атом водню або CmF2m+1; Ζ означає атом водню або CmF2m+1; m означає нуль, 1, 2, 3 або 4; m означає нуль, 1, 2, 3 або 4; а також до їх фармацевтично прийнятних соа також до їх фармацевтично прийнятних солей, як і до їх солей трифтороцтової кислоти. лей, як і до їх солей трифтороцтової кислоти. Один варіант здійснення відноситься до споПереважні сполуки формули (І), де лук формули (І), де R1 і R2, незалежно один від одного, означають R1 і R2, незалежно один від одного, означають Н, F, СІ, Вr, СH3, CF3, SO2CH3, SO2NH2, однак, щоН, F, СІ, Br, I, CN, NO2, -(X)n-CqH2q-Z, циклоалкіл з найбільше один із замісників R1 і R2 означає атом 3, 4, 5 або 6 атомами вуглецю, алкеніл з 2, 3 або 4 водню; атомами вуглецю, алкенілалкіл з 3 або 4 атомами R3 означає атом водню, F або СІ; вуглецю, етиніл або алкілалкініл з 3 або 4 атомами R4 означає атом водню, алкіл з 1, 2, 3 або 4 вуглецю; атомами вуглецю або циклопропіл; n означає нуль або 1; R5 і R6 означають атом водню або разом X означає атом кисню, NH, N-CH3, S(O)k; означають зв'язок; k означає нуль, 1 або 2; R7 і R8 разом означають алкіленовий ланцюг, q означає нуль, 1, 2, 3, 4, 5 або 6; що складається з 3, 4, 5, 6, 7 або 8 атомів вуглецю; Ζ означає атом водню або CmF2m+1; або m означає нуль, 1, 2, 3 або 4; R7 і R8 разом означають залишок R3 означає атом водню, метил, F, СІ, Br, I, CN, S(O)k-CH3, -NO2, -O-CH3; R4 означає атом водню, циклоалкіл з 3, 4, 5 або 6 атомами вуглецю, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл або алкілалкініл з 3 або 4 атомами вуглецю, -CqH2q-Z; q означає нуль, 1, 2, 3 або 4; причому R5 і R6 разом утворюють зв'язок; Ζ означає атом водню або трифторметил; R10 і R11, незалежно один від одного, ознаR5 і R6 означають атом водню або разом чають атом водню, ОН, атом фтору або хлору; означають зв'язок; R9 і R12 означають атом водню; R7 і R8, незалежно один від одного, означають або (С3-С5)-алкіл-, (С2-С5)-алкеніл, (С2-С5)-алкініл, (С3один із замісників R9 і R12 означає атом водС6)-циклоалкіл або (С4-С6)-циклоалкеніл; ню, а інший означає F, СІ, Br, CN, СООН, COабо NR13R14, SO2-NR13R14 або -(X)n-CqH2q-Z; R7 і R8 разом означають алкіленовий ланцюг, R13 і R14, однакові або різні, означають атом що складається з 3-8 атомів вуглецю, причому водню або метил; атоми водню можуть бути не заміщені, частково n означає нуль або 1; або повністю заміщені атомами фтору; X означає атом кисню, NH, N-CH3 або S(O)k; або k означає нуль, 1 або 2; R7 і R8 разом означають залишок q означає нуль, 1, 2, 3 або 4; , причому R5 і R6 разом утворюють зв'язок; R9, R10 і R11, незалежно один від одного, означають атом водню, фтору, хлору, брому, метил, CN, ОН, -О-СН3, NO2, NH2 або -CF3; R9 і R12 означають атом водню; або один із замісників R9 і R12 означає атом водню, а інший означає F, СІ, Вr, І, CN, NO2, СООН, CO-NR13R14, SO2-NR13R14, алкеніл з 2, 3 або 4 атомами вуглецю, алкенілалкіл з 3 або 4 атомами вуглецю, етиніл, алкілалкініл з 3 або 4 атомами вуглецю або -(X)n-CqH2q-Z; R13 і R14, однакові або різні, означають атом водню або алкіл з 1, 2, 3 або 4 атомами вуглецю; Ζ означає атом водню або CF3; а також їх фармацевтично прийнятні солі, як і їх солі трифтороцтової кислоти. Oсобливо переважні сполуки формули (І), де R1 і R2, незалежно один від одного, означають F, СІ, Вr, СН3 або CF3; R3 означає атом водню; R4 означає атом водню, метил, етил; R5 і R6 означають атом "водню або разом означають зв'язок; R7 і R8 разом означають алкіленовий ланцюг, що складається з 3, 4, 5, 6, 7 або 8 атомів вуглецю; або R7 і R8 разом означають залишок , причому R5 і R6 разом утворюють зв'язок; 11 77551 12 R10 і R11, незалежно один від одного, ознаЯкщо сполуки містять кислотну групу, вони можуть чають атом водню, ОН або атом фтору; утворювати солі з основами, наприклад, можуть R9 і R12 означають атом водню; бути у вигляді солей лужних металів, переважно або натрієвих або калієвих солей, або у вигляді амоніодин із замісників R9 і R12 означає атом водєвих солей, наприклад, у вигляді солей з аміаком ню, а інший означає F, СІ, Вг або -(X)n-CqH2q-Z; або органічними амінами або амінокислотами. n означає нуль або 1; Вони також можуть знаходитися у вигляді цвітерX означає атом кисню, NH, N-CH3 або S(O)k; іону. k означає нуль, 1 або 2; Якщо сполуки формули (І) містять один або q означає нуль або 1; декілька центрів асиметрії, то, незалежно один від Ζ означає атом водню або CF3; одного, вони можуть знаходитися як в S-, так і в Rа також їх фармацевтично прийнятні солі, як і конфігурації. Сполуки можуть знаходитися у виїх солі трифтороцтової кислоти. гляді оптичних ізомерів, діастереомерів, рацематів Особливо переважні наступні сполуки формуабо у вигляді їх сумішей. ли (І), вибрані з групи, що включає Сполуки формули (І), далі, можуть знаходититранс-R,R-2-хлор-3N-(3а,4,5,6,7,7а-гексагідрося у вигляді таутомерів або у вигляді суміші тау1Н-2-бензімідазоліл)-4-метил-3-тієніламін; томерних структур. При цьому, наприклад, мають транс-R,R-2-бром-3N-(3а,4,5,6,7,7а-гексагідрона увазі наступні таутомери: 1Н-2-бензімідазоліл)-4-метил-3-тієніламін; 2-хлор-3N-(2-бензімідазоліл)-4-метил-3тієніламін; 2-бром-3N-(2-бензімідазоліл)-4-метил-3тієніламін; 2-хлор-3N-(4-метил-2-бензімідазоліл)-4-метил3-тієніламін; 2-хлор-3N-(5-фтор-2-бензімідазоліл)-4-метилАлкільні залишки можуть бути лінійними або 3-тієніламін; розгалуженими. Це відноситься також до тих ви2-хлор-3N-(4-хлор-2-бензімідазоліламіно)-4падків, коли вони містять замісники або знахометилтіофен; дяться у вигляді замісників інших залишків, напри2-бром-3N-(4-хлор-2-бензімідазоліламіно)-4клад, у фторалкільних або алкоксильних метилтіофен; залишках. Прикладами алкільних залишків є ме2-бром-3N-(4-фтор-2-бензімідазоліламіно)-4тил, етил, н-пропіл, ізопропіл (= 1-метилетил), нметилтіофен; бутил, ізобутил (= 2-метилпропіл), втор-бутил (= 12-хлор-3N-(4-фтор-2-бензімідазоліламіно)-4метилпропіл), трет-бутил (= 1,1-диметилетил), нметилтіофен; пентил, ізопентил, трет-пентил, неопентил або 2-хлор-3N-(4-гідрокси-2-бензімідазоліламіно)гексил. Переважними алкільними залишками є 4-метилтіофен; метил, етил, н-пропіл, ізопропіл, н-бутил, трет(1Н-бензімідазол-2-іл)-(2-хлор-4-метилтіофенбутил, н-пентил, н-гексил. В алкільних залишках 3-іл)метиламін; один або декілька, наприклад, 1, 2, 3, 4, 5, 6, 7, 8 (2-бром-4-метилтіофен-3-іл)-(5-фтор-1Набо 9, атомів водню можуть бути заміщені атомабензімідазол-2-іл)амін; ми фтору. Прикладами таких фторалкільних за2-хлор-3N-(2-бензімідазоліламіно)-4лишків є трифторметил, 2,2,2-трифторетил, пенметилтіофен; тафторетил, гептафторізопропіл. Заміщені 2,4-дихлор-3N-(2-бензімідазоліламіно)тіофен; алкільні залишки можуть бути заміщені в будь2-бром-4-хлор-3N-(2яких положеннях. бензімідазоліламіно)тіофен; Алкенільні залишки можуть бути лінійними або 2,4-дихлор-3N-(4-метил-2розгалуженими. Це відноситься також до тих вибензімідазоліламіно)тіофен; падків, коли вони знаходяться як замісники, напритранс-R,R-2,4-дихлор-3N-(3а,4,5,6,7,7аклад, в алкенілалкіленах. Алкенільні залишки могексагідро-1Н-2-бензімідазоліл)-3-тієніламін; або жуть бути ненасиченими в різних положеннях. 2,4-дихлор-3N-(4-хлор-2Прикладами алкенільних залишків є етеніл, пробензімідазоліламіно)тіофен; пеніл або бутеніл. а також їх фармацевтично прийнятні солі, наАлкінільні залишки можуть бути лінійними або приклад, гідрохлорид або гідробромід або метанрозгалуженими. Це відноситься також до тих висульфонат кожної із сполук. падків, якщо вони знаходяться як замісники, наСполуки формули (І) можуть знаходитися в приклад, в алкінілалкіленах. Алкінільні залишки формі солей. Як адитивні солі кислот при цьому можуть бути ненасиченими в різних положеннях. можна використати солі всіх фармакологічно приПрикладами алкінільних залишків є етиніл, пропійнятних кислот, наприклад, галогеніди, особливо ніл або бутиніл. гідрохлориди, гідроброміди, лактати, сульфати, Прикладами циклоалкільних залишків є цитрати, тартрати, ацетати, фосфати, метилсульцикл.опропіл, циклобутил, циклопентил або циклофонати, бензолсульфонати, п-толуолсульфонати, гексил. Заміщені циклоалкільні залишки можуть адипінати, фумарати, глюконати, глутамати, гліцебути заміщені в будь-яких положеннях. Циклоалкіринфосфати, малеїнати, бензоати, оксалати і пальні залишки також можуть бути розгалуженими, моати. Ця група відповідає також фізіологічно прияк алкілциклоалкіл або циклоалкілалкіл. йнятним аніонам; однак, також трифторацетатам. Описуються також способи отримання сполук, 13 77551 14 що пропонуються згідно з винаходом. Так, сполуки він володіє відомою селективністю відносно NHE2 формули (І) можна отримувати відомим фахівцеві [J. Orlowski і інш., J. Biol. Chem., 268, 25-36]. Тому способом з вихідних ізотіоціанатів формули (II) і його, швидше, треба називати інгібітором NHE2. відповідних діамінів формули (III). Поряд зі слабким впливом на NHE клонідин володіє високою спорідненістю до адренергенного альфа2-рецептору і імідазолін-I1-рецептору, завдяки чому виникає сильна дія, що знижує кров'яний тиск [Ernsberger і інш., Eur. J. Pharmacol., 134, 1 (1987)]. Подібні до клонідину сполуки з тіофеновим циклом замість фенільного циклу відомі з [патенту ФРН 1941761]. Ці відомі сполуки відрізняються від описаних в даному контексті структур формули (І) Проміжне похідне тіосечовини, що утворюєтьзначно меншими залишками R7 і R8 і особливо ся при цьому, з допомогою метилйодиду тим, що R7 і R8 не можуть утворювати ніякого спі[Synthesis, 41-42 (1974)] або карбодііміду льного циклу. [Synthesis, 864-865 (1977)] або з допомогою хлоЗа рахунок цієї відмінності в замісниках R7 і рангідриду п-толуолсульфокислоти циклізують з R8 можна виключати описані, вище подібні до отриманням відповідної сполуки формули (І). Ізоклонідину, небажані, опосередковані альфатіоціанати формули (II), що використовуються при адренорецепторним впливом серцево-судинні цьому, якщо вони комерційно недоступні, можна ефекти цих похідних тіофену. Одночасно, внасліотримувати відомим з літератури способом з віддок цієї відмінності в заміщенні посилюються інгіповідних похідних амінотіофену відомими фахівбуючі NHE властивості описаних в даному концеві способами, наприклад, шляхом обробки тіотексті сполук аж до мікромолярної і фосгеном [J. Med. Chem., 18, 90-99 (1975)] або субмікромолярної ділянки, в той час як відомі з тіокарбонілдіімідазолом [Justus Liebigs Ann, Chem., [патенту ФРН 1941761] сполуки не виявляють або 657, 104 (1962)]. виявляють тільки дуже слабо виражені інгібуючі Поряд з вищезгаданими ізотіоціанатами форNHE ефекти. Так, основний представник згідно з мули (II) також ізоціанати формули (IV) [патентом ФРН 1941761], вибраний як розроблений препарат для зниження кров'яного тиску тіаменідин, в кількості, відповідно, 300мкмоль не володіє жодними інгібуючими впливами на досліджені підтипи NHE: NHE1, NHE2, NHE3 і NHE5. Сполуки формули (І) відрізняються інгібуванням натрій-протонного обміну і особливо інгібуюуспішно можна вводити у взаємодію з амінами чою NHE3 дією. типу амінів формули (III), отримуючи сполуки фоNHE3 в організмі різних видів відбувається в рмули (І). При цьому проміжне похідне сечовини, жовчі, кишечнику і в нирках [Larry Fliegel і інш., що утворюється, циклізують за допомогою оксихBiochem. Cell. Biol., 76, 735-741 (1998)], однак молориду фосфору з отриманням відповідних сполук же виявлятися також в головному мозку [Е. Ма і формули (І). інш., Neuroscience, 79, 591-603]. Згідно з даним винаходом несподівано було Завдяки інгібуючим NHE властивостям сполупоказано, що описані сполуки являють собою ки формули (І) придатні для попередження і лікуефективні інгібітори натрій/протонного обміну вання захворювань, які провокуються активацією (NHE), особливо натрій/протонного обміну підтипу NHE або, відповідно, активованим NHE, а також 3 (NHE3). виникаючих повторно захворювань, зумовлених Відомі досі інгібітори NHE3 є похідними сполук NHE порушеннями. типу ацилгуанідину [європейський патент 825178], Оскільки інгібітори NHE переважно діють четипу норборніламіну [патент ФРН 19960204], типу рез регуляцію значення рН в клітинах, їх можна 2-гуанідинхіназоліну [заявка WO 0179186] або типу сприятливим чином комбінувати з іншими, також бензамідину [заявки WO 0121582, WO 0172742]. регулююче внутрішньоклітинне значення рН споОписаний також як інгібітор NHE3 скваламін [М. луками, причому як компонент комбінації враховуDonowitz і інш., Am. J. Physiol., 276 (Cell Physiol. ють інгібітори ферментної групи карбоангідратаз, 45): C136-C144], згідно з рівнем техніки, діє не інгібітори транспортуючих бікарбонат-іони систем, безпосередньо, як сполука формули (І), а через як спільного натрій-бікарбонатного перенесення опосередкований механізм і, таким чином, досягає (NBC) або натрійзалежного хлорид-бікарбонатного своєї максимальної активності тільки через годину. обміну (NCBE), а також інгібітори NHE з інгібуючим Такі діючі по механізму іншого роду інгібітори впливом на інші підтипи NHE, оскільки за рахунок NHE3 придатні тому як компонент комбінації з них можна посилювати або модулювати фармакопредставленими згідно з винаходом сполуками. логічно релевантні, регулюючі значення рН ефекти Подібний описаним в даному контексті сполуописаних в даному контексті інгібіторів NHE. кам клонідин відомий як слабкий інгібітор NHE. Застосування сполук, що пропонуються згідно Правда, його вплив на NHE3 щура при напівмакз винаходом, відноситься до попередження і лікусимальній інгібуючій концентрації (ІС50), що склавання гострих і хронічних захворювань в медицині дає 620мкмоль, є надто посереднім. Замість цього людини і тварини. 15 77551 16 Фармакологічна дія сполук формули (І) відрізхірургічних втручань, при закупорці кишечнику або няється тим, що вони приводять до поліпшення при сильно зниженій діяльності кишечнику. дихального імпульсу. Тому їх можна використовуЗа допомогою сполук, що пропонуються згідно вати для лікування порушених станів дихання, які з винаходом, існує можливість запобігання утвоможуть виникати, наприклад, у випадку наступних ренню жовчних каменів. клінічних станів і захворювань: порушений Інгібітори NHE, що пропонуються згідно з вицентральний дихальний імпульс (наприклад, находом, придатні, загалом, для лікування захвоцентральна зупинка дихання у сні, раптова смерть рювань, що провокуються ішемією і реперфузією. дитини, постоперативна гіпоксія), м'язово обумовВнаслідок своїх фармакологічних властивослені порушення дихання, порушення дихання пістей сполуки, що пропонуються згідно з винаходом, ля тривалої штучної вентиляції легенів, порушення придатні як антиаритмічні лікарські засоби. дихання при адаптації у високогір'ї, обструктивна За рахунок свого кардіозахисного компонента або змішана форма зупинки дихання у сні, гострі і інгібітори NHE формули (І) чудово придатні для хронічні захворювання легенів з гіпоксією і гіперкапрофілактики інфаркту і лікування інфаркту, а тапнією. Додатково сполуки підвищують м'язовий кож для лікування стенокардії, причому вони також тонус верхніх дихальних шляхів, так що придушупрофілактично інгібують або сильно зменшують ється хропіння. Вказані сполуки тому знаходять патофізіологічні процеси при виникненні ішемічно переважно застосування для отримання лікарськоіндукованих ушкоджень, особливо при вияві ішеміго засобу для попередження і лікування зупинок чно індукованих аритмій серця. Через їх захищаюдихання у сні і м'язовообумовлених порушень дичу дію проти патологічних гіпоксичних і ішемічних хання, для отримання лікарського засобу для поситуацій сполуки формули (І), що використовуютьпередження і лікування хропіння. ся згідно з винаходом, внаслідок інгібування мехаМоже виявитися корисною комбінація інгібітонізму клітинного №+/Н+-обміну, можна застосовуру NHE формули (І) з інгібітором карбоангідрази вати як лікарські засоби для лікування всіх гострих (як, наприклад, ацетазоламід), причому останній або хронічних, провокованих ішемією ушкоджень викликає метаболічний ацидоз і завдяки цьому або індукованих за рахунок цього первинних або вже підвищує дихальну діяльність, так що можна повторних захворювань. Це стосується їх застосудосягати посиленої дії при зниженому введенні вання як лікарських засобів при хірургічних втрубіологічно активної речовини. чаннях. Так, сполуки, що пропонуються згідно з Сполуки, що пропонуються згідно з винаховинаходом, можна використовувати при транспладом, внаслідок їх інгібуючої NHE3 дії зберігають нтаціях органів, причому сполуки можна застосоклітинні енергоресурси, які швидко вичерпуються вувати як для захисту органів у донора до і під час при токсичних і патогенних явищах і, таким чином, вилучення, для захисту вилучених органів, наприприводять до ушкодження або загибелі клітини. клад, при обробці за допомогою фізіологічних розПри цьому енергоємної АТФ, що споживає резорчинів електролітів або при їх зберіганні в фізіологібції натрію в проксимальному канальці під впличних розчинах електролітів, так і при перенесенні в вом сполук формули (І), тимчасово не відбуваєтьзаздалегідь оброблений сполуками формули (І) ся і клітина, таким чином, може пережити гостру організм реципієнта. патогенну, ішемічну або токсичну ситуацію. СполуСполуки також являють собою цінні, протектики тому придатні, наприклад, як лікарські засоби вно діючі лікарські засоби при здійсненні ангіопладля лікування ішемічних патогенних факторів, настичних оперативних втручань, наприклад, у випаприклад, гострої ниркової недостатності. дку серця, а також у випадку периферичних Далі, сполуки також придатні для лікування органів і судин. всіх хронічних захворювань нирок і форм нефриту, Оскільки інгібітори NHE не тільки ефективно які внаслідок підвищеного виділення протеїнів захищають людську тканину і органи від" ушкоприводять до хронічної ниркової недостатності. джень, які провокуються ішемією і реперфузією, Відповідно цьому сполуки формули (І) придатні але і від цитотоксичної дії лікарських засобів, які для отримання лікарського засобу для лікування знаходять застосування, особливо, при терапії діабетичних пізніх ушкоджень, діабетичної нефрораку і аутоімунних захворювань, придатним є компатії і хронічних захворювань нирок, особливо всіх біноване введення разом із сполуками формули (І) запалень нирок (нефрити), які пов'язані з підвищедля зменшення або придушення цитотоксичних ним виділенням протеїну/альбуміну. ефектів терапії. За рахунок зменшення цитотоксиВиявлено, що сполуки, що використовуються чних ефектів, особливо кардіотоксичності, внаслізгідно з винаходом, володіють помірною послабдок спільної лікарської терапії за допомогою інгібілювальною дією і внаслідок цього також можуть торів NHE, крім того, можна підвищувати дозу переважно застосовуватися як проносний засіб цитотоксичного терапевтичного засобу і/або проабо при загрозливій закупорці кишечнику. довжувати лікарську терапію за допомогою таких Далі, сполуки, що пропонуються згідно з виналікарських засобів. Терапевтичну ефективність ходом, можна застосовувати переважно для попетакої цитотоксичної терапії можна значно підвищуредження і лікування гострих і хронічних захворювати за рахунок комбінації з інгібіторами NHE. вань кишечнику, наприклад, що провокуються Сполуки формули (І) особливо придатні для поішемічними станами в кишковій зоні і/або подальліпшення терапії за допомогою лікарських засобів, шою реперфузією або запальними станами і явищо володіють небажаним кардіотоксичним компощами. Такі ускладнення можливі, наприклад, за нентом. рахунок недостатньої перистальтики кишечнику, Відповідно до їх захисної дії проти ішемічно яку, наприклад, можна часто спостерігати після індукованих ушкоджень сполуки згідно з винахо 17 77551 18 дом також придатні як лікарські засоби для лікутому придатні для запобігання і для лікування севання ішемій нервової системи, особливо центрарцевої недостатності (застійна серцева недостатльної нервової системи, причому вони придатні, ність = CHF), а також при лікуванні і профілактиці наприклад, для лікування інсульту або набряку гіперплазії, відповідно, гіпертрофії простати. мозку. Сполуки формули (І) відрізняються, далі, споСполуки формули (І) придатні також для лікувільненням або запобіганням фіброзним захворювання і профілактики захворювань і порушень, що ванням. Вони придатні, таким чином, як засоби виникають за рахунок підвищеної збудливості для лікування фіброзів серця, а також фіброзу центральної нервової системи, особливо для лікулегенів, печінки, нирок і інших фіброзних захворювання захворювань групи епілептичних нозологічвань. них форм, центрально провокованих клонічних і Оскільки NHE в есенціальних гіпертоніків знатонічних спазмів, психічних депресивних станів, чно підвищений, сполуки формули (І) придатні для пов'язаних зі страхом захворювань і психозів. При попередження і лікування високого кров'яного тисцьому інгібітори NHE, що пропонуються згідно з ку і серцево-судинних захворювань. винаходом, можна використовувати індивідуально При цьому їх можна застосовувати індивідуаабо в комбінації з іншими антиепілептично діючильно або разом з придатним компонентом комбіми речовинами або антипсихотичними біологічно націй і препаративних форм для лікування високоактивними речовинами або інгібіторами карбоангіго кров'яного тиску і серцево-судинних дратази, наприклад, з ацетазоламідом, а також з захворювань. Так, наприклад, один або декілька іншими інгібіторами NHE або натрійзалежного тіазидоподібно діючих діуретиків, байпасних діурехлорид-бікарбонатного обміну (NCBE). тиків, антагоністів альдостерону і псевдоальдесБільше того, сполуки формули (І), що пропотерону, як гідрохлортіазид, індапамід, політіазид, нуються згідно з винаходом, також придатні для фуросемід, піретанід, торасемід, буметанід, амілікування форм шоку, як, наприклад, алергічного, лорид, триамтерен, спіронолактон або еплерон, кардіогенного, гіповолемічного і бактерійного шоку. можна комбінувати із сполуками формули (І). Далі, Сполуки формули (І) також можна використоінгібітори NHE згідно з винаходом, можна застосовувати для попередження і для лікування тромбовувати в комбінації з антагоністами кальцію, як тичних захворювань, оскільки вони як інгібітори верапаміл, дилтіазем, амлодипін або ніфедипін, а NHE можуть інгібувати навіть агрегацію тромбоцитакож з інгібіторами АСЕ, як, наприклад, раміприл, тів. Більше того, вони можуть інгібувати, відповіденалаприл, лізиноприл, фозиноприл або каптопно, запобігати тому, що відбувається після ішемії і рил. Іншими сприятливими компонентами комбіреперфузії вивільненню медіаторів запалення, що націй є також -блокатори, як метопролол, альбувідхиляється від встановленого значення і згортерол і т.д., антагоністи рецептора ангіотензину і тання, особливо фактора Віллебранда і тромбойого рецепторних підтипів, як лосартан, ірбесаргенних селектинових протеїнів. Тим самим можна тан, валсартан, омапатрилат, гемопатрилат, антазменшувати або виключати патогенний вплив гоністи ендотеліну, інгібітори реніну, агоністи ретромбогенних і істотних у випадку запалення факцептора аденозину, інгібітори і активатори торів. Інгібітори NHE згідно з даним винаходом калієвих каналів, як глібенкламід, глімепірид, діатому комбінують з іншими антикоагулятивними зоксид, кромокалим, міноксидил і його похідні, акі/або тромболітичними біологічно активними речотиватори мітохондріального АТФ-чутливого калієвинами, як, наприклад, з рекомбінантним або привого каналу (мітоК(АТФ)канал), інгібітори інших родним тканинним плазміногенним активатором, калієвих каналів, як Kvl.5, і т.д. стрептокіназою, урокіназою, ацетилсаліциловою Внаслідок їх протизапальної дії, інгібітори NHE кислотою, антагоністами тромбіну, антагоністами можна використовувати як протизапальні засоби. фактора Ха, фібринолітично діючими лікарськими З точки зору механізму при цьому виділяють інгіречовинами, антагоністами рецептора тромбоксабування вивільнення медіаторів запалення. Спону, інгібіторами фосфодіестерази, антагоністами луки, таким чином, можна використовувати індивіфактора VIla, клопідогрелем, тиклопідином і т.д. дуально або в комбінації з протизапальним Особливо сприятливе комбіноване застосування засобом для попередження або лікування хронічданих інгібіторів NHE з інгібіторами NCBE і/або з них і гострих запальних захворювань. Як компонеінгібіторами карбоангідратази, як, наприклад, з нти комбінації використовують переважно стероїдацетазоламідами. ні і нестероїдні протизапальні засоби. Більше того, сполуки формули (І), що пропоКрім того, показано, що сполуки формули (І) нуються згідно з винаходом, відрізняються сильвпливають сприятливим чином на сироваткові ним інгібуючим впливом відносно проліферації ліпопротеїни. Тому їх можна використовувати для клітин, наприклад, проліферації фібробластів або профілактики і регресії атеросклеротичних змін, проліферації гладком'язових судинних клітин. Тооскільки вони виключають каузальний фактор риму сполуки формули (І) розглядаються як цінні зику, до якого прираховують не тільки первинні терапевтичні засоби від захворювань, первинною гіперліпідемії, але і також відомі вторинні гіперліпіабо вторинною причиною яких є проліферація клідемії, які є, наприклад, при діабеті. Більше того, тин, і внаслідок цього їх можна застосовувати як сполуки формули (І) приводять до виразного зниантиатеросклеротичні засоби, засоби проти хроніження аномалій обміну речовин, що індукуються чної ниркової недостатності, онкологічних захвоза рахунок інфарктів і, особливо, до значного змерювань. Таким чином, їх можна використовувати ншення розміру інфаркту, що індукується, і міри для лікування гіпертрофії і гіперплазії органів, найого тяжкості. приклад, серця і простати. Сполуки формули (І) Вказані сполуки тому знаходять застосування 19 77551 20 переважно для отримання лікарського засобу для NIDDM антидіабетичними лікарськими засобами. лікування гіперхолестеринемії; для попередження При цьому особливе значення надають комбінації атерогенезу; для попередження і лікування атероз сприятливою формою введення інсуліну. склерозу; для попередження і лікування захворюІнгібітори NHE формули (І), що пропонуються вань, які провокуються підвищеним рівнем холесзгідно з винаходом, нарівні із захисними ефектами терину; для попередження і лікування проти гострих ішемічних виявів і подальших також захворювань, які провокуються ендотеліальною гострих загострюючих явищ реперфузії, також видисфункцією; для попередження і лікування гіперявляють ще прямі терапевтично придатні дії проти тонії, що індукується атеросклерозом; для поперезахворювань і порушень у випадку всього організдження і лікування тромбозів, що індукуються атему ссавця, які пов'язані з явищами хронічно протіросклерозом; для попередження і лікування каючого процесу старіння і які також незалежні від ішемічних ушкоджень і постішемічних реперфузійгострих ішемічних станів і також можуть виникати в них ушкоджень, що індукуються гіперхолестеринормальних неішемічних умовах. У випадку цих немією і ендотеліальною дисфункцією; для попепатологічних, виникаючих протягом тривалого чаредження і лікування кардіальних гіпертрофій і су старіння і зумовлених старінням явищ, як закардіоміопатій і застійної серцевої недостатності хворювання, ведуча до повного виснаження хво(CHF); для попередження і лікування коронарних роба і смерть, які віднедавна змогли стати спазмів судин і інфарктів міокарда, що індукуються доступними для лікування за допомогою інгібіторів гіперхолестеринемією і ендотеліальною дисфункNHE, мова йде про захворювання і порушення, які цією; для попередження і лікування вказаних хвозначною мірою провокуються зумовленими старінроб в комбінації зі знижуючими кров'яний тиск реням змінами життєво необхідних органів і їх функчовинами, переважно з інгібіторами ції і в старіючому організмі набувають зростаючого ангіотензинконвертуючих ферментів (АСЕ) і антазначення. Захворюваннями, які пов'язані із зумовгоністами рецептора ангіотензину. Комбінація інгіленим старінням порушенням функції, із зумовлебітору NHE формули (І) зі знижуючою кров'яний ними старінням явищами "зносу" органів, є, напритиск біологічно активною речовиною, переважно з клад, недостатня чутливість і реагування інгібітором HMG-CoA-редуктази (наприклад, як кровоносних судин по відношенню до скорочень і ловастатин або правастатин), причому останній реакцій релаксації. Це зумовлене старінням погірнадає гіполіпідемічну дію і завдяки цьому поліпшує шення реакції судин на стискаючі і релаксуючі погіполіпідемічні властивості інгібітору NHE формули дразнення, які являють собою есенціальний про(І), виявляється сприятливою комбінацією з посицес серцево-судинної системи і, таким чином, леною дією і зменшеним використанням біологічно погіршення якості життя і здоров'я, можна значною активної речовини. мірою загальмувати або зменшити за допомогою Таким чином, сполуки формули (І) приводять інгібіторів NHE. Важливою функцією і мірою підтдо ефективного захисту відносно ушкоджень енримання реагованості судин є блокада, відповідно, дотелію різного генезу. За рахунок захисту судин ретардація зумовленої старінням прогресуючої проти синдрому ендотеліальної дисфункції сполуендотеліальної дисфункції, яку можна значною ки формули (І) є цінними лікарськими засобами мірою ліквідувати за допомогою інгібіторів NHE. для попередження і лікування коронарних спазмів Сполуки формули (І), таким чином, придатні для судин, периферичних судинних захворювань, осолікування і попередження зумовленої старінням бливо синдрому Шарко, атерогенезу і атеросклепрогресуючої ендотеліальної дисфункції, особливо розу, лівошлуночкової гіпертрофії і дилатованої синдрому Шарко. Крім того, сполуки формули (І), кардіоміопатії, і тромботичних захворювань. таким чином, придатні для лікування і попереКрім того, інгібітори NHE формули (І) придатні дження серцевої недостатності, застійної серцевої для лікування інсуліннезалежного діабету недостатності (CHF), а також для лікування і, осо(NIDDM), при цьому, наприклад, придушується бливо для попередження зумовлених старінням резистентність до інсуліну. Для посилення антидіформ раку. абетичної ефективності і підвищення якості дії Крім того, можна використати комбінацію зі сполук, що пропонуються згідно з винаходом, мознижуючими кров'яний тиск лікарськими засобами, же виявитися сприятливим комбінування їх з бігуяк з інгібіторами АСЕ, антагоністами рецептора анідом, як метформін, з антидіабетичною сульфоангіотензину, діуретиками, антагоністами Са2+ і нілсечовиною, як глібурид, глімепірид, толбутамід і т.д., або з нормалізуючими обмін речовин лікарсьт.д., з інгібітором глюкозидази, агоністом PPAR, як кими засобами, як знижуючі рівень холестерину росіглітазон, піоглітазон і т.д., з інсуліновим препазасоби. Сполуки формули (І) придатні, таким чиратом різної форми введення, з інгібітором DB4, з ном, для попередження зумовлених старінням чутливим до інсуліну засобом або з меглітинідом. змін тканини і для продовження життя при досягНарівні з безпосередніми антидіабетичними ненні високої якості життя. ефектами сполуки формули (І) протидіють виникСполуки, що пропонуються згідно з винахоненню діабетичного пізнього ускладнення і тому їх дом, є ефективними інгібіторами клітинного натрійможна застосовувати як лікарські засоби для попротонного антипорту (Na/H-обмін), який у випадку передження і лікування діабетичних пізніх ушкочисленних захворювань (есенціальна гіпертонія, джень, як діабетичної нефропатії, діабетичної неватеросклероз, діабет і т.д.) підвищений також в ропатії, діабетичної ретинопатії, діабетичної таких клітинах, які легко доступні для вимірювань, кардіоміопатії і інших захворювань, які виникають як, наприклад, в еритроцитах, тромбоцитах або як наслідок діабету. При цьому їх можна переважлейкоцитах. Сполуки, що використовуються згідно но комбінувати з вказаними нижче при лікуванні з винаходом, придатні тому як чудові і прості нау 21 77551 22 кові засоби, наприклад, при їх застосуванні як діафосфат калію, молочний цукор, глюкозу або крохгностичні засоби для визначення і розпізнавання маль, особливо кукурудзяний крохмаль. При цьопевних форм гіпертонії, однак, також атеросклерому приготування здійснюють як у вигляді сухого зу, діабету і діабетичних пізніх ускладнень, пролігрануляту, так і у вигляді мокрого грануляту. Як феративних захворювань і т.д. масляні носії або як розчинники використовують, Далі, інгібітори NHE3 придатні для лікування наприклад, рослинні олії або тваринні масла, такі захворювань, що викликаються бактеріями, а таяк соняшникова олія або риб'ячий жир. кож найпростішими (у людини і тварини). У випадДля підшкірного, черезшкірного або внутрішку викликаних найпростішими захворювань особньовенного введення з активних сполук, що виколиво треба назвати малярійні захворювання ристовуються, в бажаному випадку, разом із звилюдини і курячий кокцидіоз. чайними для цієї мети речовинами, такими як Крім того, сполуки придатні як засоби для босприяючі розчиненню речовини, емульгатори або ротьби з сисними паразитами в медицині людини і інші допоміжні речовини, приготовляють розчин, тварини, а також при захисті рослин. При цьому в суспензію або емульсію. Як розчинники придатні, медицині і ветеринарії переважним є застосування наприклад, вода, фізіологічний розчин хлориду як засоби проти кровосисних паразитів. натрію або спирти, наприклад, етанол, пропанол, Сполуки формули (І), поряд зі своїми високими гліцерин, нарівні з ними також розчини цукрів, такі показниками відносно інгібування NHE, своїми як розчини глюкози і маніту, або також суміш з фармакологічними властивостями і відсутністю вказаних різних розчинників. небажаних біологічних дій, також відрізняються Як фармацевтична композиція для введення в сприятливими фармакокінетичними властивостяформі аерозолів або спреїв придатні, наприклад, ми, які дозволяють особливо сприятливо здійснюрозчини, суспензії або емульсії біологічно активної вати їх застосування як лікарських засобів. речовини формули (І) в фармацевтично безпечТаким чином, винахід відноситься до лікарсьному розчиннику, такому як, особливо, етанол або кого засобу для застосування в медицині людини, вода, або суміші таких розчинників. За необхідносветеринарії або для фітозахисного застосування, ті композиція також може містити ще інші фармащо містить ефективну кількість сполуки формули цевтичні допоміжні речовини, такі як поверхнево(І) і/або її фармацевтично прийнятних солей індиактивні речовини, емульгатори і стабілізатори, а відуально або в комбінації з іншими фармакологітакож пропелент. Такий препарат містить біологіччними біологічно активними речовинами або ліно активну речовину звичайно в концентрації від карськими засобами. приблизно 0,1%мас., до 10%мас., особливо від Лікарські засоби, що містять сполуки формули приблизно 0,3%мас. до 3%мас. (І), можна вводити, наприклад, перорально, паренДозування біологічно активної речовини фортерально, внутрішньом'язово, внутрішньовенно, мули (І), що вводиться, і частота введення залеректально, назально, шляхом інгаляції, підшкірно жать від сили і тривалості дії сполук, що викорисабо шляхом придатної черезшкірної форми вветовуються; крім того, від роду і інтенсивності дення, причому переважне введення залежить від захворювання, що лікується, а також від статі, віку, відповідної картини захворювання. Сполуки форваги і індивідуальної чутливості ссавця, що піддамули (І) при цьому можна застосовувати індивідується лікуванню. ально або разом з галеновими допоміжними речоУ середньому добова доза сполуки формули винами, а саме як у ветеринарії, так і в медицині (І) у випадку пацієнта вагою приблизно 75кг станолюдини і при захисті рослин. вить, щонайменше 0,001мг/кг, переважно 0,1мг/кг, Які допоміжні речовини придатні для бажаної аж до найбільше 30мг/кг, переважно 1мг/кг ваги готової лікарської форми, фахівцеві відомо на остіла. У гострих ситуаціях, наприклад, безпосереднові його спеціального знання. Нарівні з розчинниньо після перенесення станів зупинки дихання у ками, гелеутворювачами, основами супозиторіїв, високогір'ї, можуть також вимагатися ще більш допоміжними речовинами для таблеток і іншими високі дози. Особливо при внутрішньовенному носіями біологічно активних речовин можна застовведенні, наприклад, у випадку пацієнта з інфарксовувати, наприклад, антиоксиданти, диспергатотом у відділенні інтенсивної терапії, можуть вимари, емульгатори, антиспінювачі, поліпшуючі смак гатися аж до 200мг/кг на добу. Добову дозу можна речовини, консерванти, сприяючі розчиненню рерозділяти на одну або декілька, наприклад, аж до човини або барвники. 4 разових доз. Для пероральної форми введення активні Якщо мова йде про енантіомерні сполуки, то сполуки змішують з придатними для цієї мети довказується конфігурація і/або знак оптичного обермішками, такими як носії, стабілізатори або інертні тання. Якщо ці дані відсутні, то мова йде про рарозріджувачі, і звичайними способами доводять до цемати або оптично неактивні сполуки. придатних форм введення, таких як таблетки, Вказані нижче часи втримання (Rt) відносяться драже, роз'ємні капсули, водні, спиртові або масдо вимірювань шляхом мас-спектрометрії з рідинляні розчини. Як інертні носії можна використати, ною хроматографією (LCMS) з наступними паранаприклад, гуміарабік, магнезію, карбонат магнію, метрами: 23 Аналітичні методи: А нерухома фаза: рухома фаза: B нерухома фаза: рухома фаза: C нерухома фаза: рухома фаза: D нерухома фаза: рухома фаза: E нерухома фаза: рухома фаза: 77551 24 Merck Purospher, 3 мікрони, 2x55мм 95% Н2О (0,1% НСООН) 95% ацетонітрил (0,1% НСООН); 5хв. (0,1% НСООН); 2хв. 95% Н2О (0,1% НСООН); 1хв.; 0,45мл/хв. 95% ацетонітрил YMC J' sphere H80, приблизно 4 мікрони, 2,1x33мм 95% Н2О (0,1% НСООН) 95% ацетонітрил (0,08% НСООН); 2,5хв. 95% ацетонітрил (0,08% НСООН); 0,5хв. 95% Н2О (0,1% НСООН); 0,5мін; 1,3мл/хв. YMC J' sphere H80, 4 мікрони, 2,1x20мм 90% Н2О (0,05% ТФОК) 95% ацетонітрил; 1,9хв.; 95% ацетонітрил; 0,5хв.; 1мл/хв. Merck Purospher, 3 мікрони, 2x55мм 95% Н2О (0,1% НСООН) 95% ацетонітрил (0,1% НСООН); 3,4хв. (0,1% НСООН); 1хв. 95% Н2О (0,1% НСООН); 0,2мін; 0,75мл/хв. 95% ацетонітрил Merck Purospher, 3 мікрони, 2x55мм 95% Н2О (0,05% CF3COOH) 95% ацетонітрил (0,05% CF3COOH); 3,4хв. тонітрил (0,05% CF3COOH); 1хв.; 0,75мл/хв. 95% аце F нерухома фаза: YMC J' sphere H80, 4 мікрони, 2,1x20мм 96% Н2О (0,05% CF3COOH) 95% ацетонітрил; 2хв.; >95% ацетонітрил; 0,4хв.; рухома фаза: 1мл/хв. Препаративну високоефективну рідинну хроматографію (ВЕРХ) здійснюють в наступних умовах: Нерухома фаза: Merck Purospher RP18 (10мкМ) 250x25мм рухома фаза: 90% Н2О (0,05% ТФОК) 90% ацетонітрил; 40хв.; 25мл/хв. Приклад 1 3Н-(5-Фтор-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид а) 4-Метил-3-тієнілізотіоціанат 4-Метил-3-тієнілізотіоціанат отримують шляхом взаємодії еквімолярних кількостей 3-аміно-4метилтіофену і Ν,Ν'-тіокарбонілдіімідазолу в безводному тетрагідрофурані (ТГФ) шляхом перемішування реакційної суміші протягом 5 годин при кімнатній температурі і подальшого витримування протягом ночі при кімнатній температурі. Виділення 4-метил-3-тієнілізотіоціанату здійснюють шляхом відгонки розчинника при зниженому тиску в ротаційному випарнику, розчинення залишку в етилацетаті і багаторазової промивки органічної фази водою. Після висушування органічної фази над сульфатом натрію органічний розчинник відганяють в ротаційному випарнику при зниженому тиску і отримують 4-метил-3-тієнілізотіоціанат у вигляді маслянистого залишку коричневого кольору. Подальше застосування 4-метил-3тієнілізотіоціанату можна здійснювати без подальшого очищення. b) N-(2-Аміно-5-фторфеніл)-N'-(4-метил-3тієніл)тіосечовина До розчину 0,02моль 4-метил-3тієнілізотіоціанату в 60мл безводного тетрагідрофурану додають 0,02моль 4-фтор-1,2діамінобензолу. Після перемішування реакційної суміші протягом 2 годин при кімнатній температурі і витримування протягом ночі розчинник відганяють в ротаційному випарнику при зниженому тиску і маслянистий залишок очищають на колонці з силікагелем за допомогою суміші з рівних частин толуолу і етилацетату. Забарвлена в коричневий колір кристалічна тверда речовина: т.пл.: 180°С. с) 3М-(5-Фтор-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид 1,5г (0,0053моль) N-(2-аміно-5-фторфеніл)-N'(4-метил-3-тієніл)тіосечовини в 50мл безводного етанолу змішують з багаторазовою молярною кількістю (приблизно 1,5-4моль) метилйодиду і кип'ятять із зворотним холодильником протягом 5 годин. Після витримування протягом ночі при кімнатній температурі етанол відганяють в ротаційному випарнику при зниженому тиску, залишок змішують з водою і за допомогою насиченого водного розчину гідрокарбонату натрію встановлюють значення рН від 8 до 9. Екстрагують багато разів етилацетатом, органічну фазу промивають водою, сушать над сульфатом натрію, розчинник відганяють при зниженому тиску в ротаційному випарнику і залишок очищають колонковою хроматографією на силікагелі за допомогою суміші розчинників з рівними об'ємними частками етилацетату і толуолу (нижче позначають як "суміш 2") як елююючий засіб. Отриманий після відгонки органічного розчинника маслянистий продукт розчиняють в етилацетаті, сильно підкисляють за допомогою насиченого розчину хлороводню в безводному діетиловому ефірі і осад, що викристалізовується після тривалого витримання, відфільтровують. Кристалічна тверда речовина; т.пл.: 192°С±2°С. Приклад 2 25 77551 2-Хлор-3N-(5-фтор-2-бензімідазоліл)-4-метил3-тієніламінгідрохлорид і 2,5-дихлор-3N-(5-фтор-2бензімідазоліл)4-метил-3-тієніламінгідрохлорид До розчину з 0,5г (0,0018моль) 3N-(5-фтор-2бензімідазоліл)-4-метил-3-тієніламінгідрохлориду в 25мл крижаної оцтової кислоти додають по краплях розчин з 0,24г (0,0018моль) N-хлорсукциніміду в 15мл крижаної оцтової кислоти, реакційну суміш перемішують протягом приблизно 2-3 годин при кімнатній температурі і розчинник відганяють при зниженому тиску в ротаційному випарнику. Після змішання залишку з водою підлуговують за допомогою 2н розчину NaOH, екстрагують етилацетатом, органічну фазу промивають водою, сушать над сульфатом натрію і розчинник відганяють в ротаційному випарнику при зниженому тиску. Таким чином отриманий маслянистий залишок розділяють на колонці шляхом хроматографії середнього тиску і за допомогою суміші розчинників з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти (нижче позначають як "суміш 17") як елююючий засіб, і після обробки за допомогою розчину газоподібного хлороводню в діетиловому ефірі отримують: 2-хлор-3N-(5-фтор-2-бензімідазоліл)-4-метил3-тієніламінгідрохлорид з фракцій 1 і 2: безбарвний аж до злегка забарвленого в жовтий колір кристалічний продукт; т.пл.: 200-202°С; 2,5-дихлор-3N-(5-фтор-2-бензімідазоліл)-4метил-3-тієніламінгідрохлорид з фракції 3: безбарвний аж до злегка забарвленого в жовтий колір кристалічний продукт; т.пл.: 286-288°С. Приклад 3 3N-(5,6-Дихлор-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид а) N-(2-Аміно-4,5-дихлорфеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і 4,5-дихлор1,2-діамінобензолу. Кристалічна тверда речовина; т.пл.:310-320°С. b) 3N-(5,6-Дихлор-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці з N-(2-аміно-4,5-дихлорфеніл)-N'-(4метил-3-тієніл)тіосечовини і метилйодиду. Кристалічна тверда речовина; т.пл.: 290-294°С. Приклад 4 3N-(2-Бензімідазоліл)-4-метил-3тієніламінгідрохлорид 26 а) N-(2-Амінофеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і 1,2діамінобензолу. Кристалічна тверда речовина з (1) т.пл.: 177-182°С, після знову здійсненої кристалізації з (2) т.пл.: 285-290°С. b) 3N-(2-Бензімідазоліл)-4-метил-3тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці з N-(2-амінофеніл)-N'-(4-метил-3тієніл)тіосечовини і метилйодиду. Кристалічна тверда речовина після перекристалізації з суміші етилацетат/етанол/т.пл.: 194-200°С. Приклад 5 3N-(4-Фтор-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид a) 3-Фтор-1,2-діамінобензол Отримують у вигляді маслянистого аморфного продукту шляхом гідрування 3-фтор-2нітрофенілгідразину (отримують шляхом реакції 2,6-дифторнітробензолу з гідразингідратом) за допомогою водню і каталізатора 10%-і паладій-навугіллі в метанолі при кімнатній температурі і нормальному тиску. b) N-(2-Аміно-3-фторфеніл)-N'-(4-метил-3тієніл')тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і 3-фтор-1,2діамінобензолу. Кристалічна тверда речовина; температура розкладання >240°С. с) 3N-(4-Фтор-2-бензімідазоліл)-4-метил-3тієніл амінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці з N-(2-аміно-3-фторфеніл)-N'-(4-метил-3тієніл)тіосечовини і метилйодиду. Аморфний осад, який кристалізують з ацетону. Кристалічна тверда речовина; т.пл.: 220-230°С. Приклад 6 3N-(4,6-Дифтор-2-бензімідазоліл)-4-метил-3тієніл амінгідрохлорид а) N-(2-Аміно-3,5-дифторфеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціаната і 3,5 27 77551 28 дифтор-1,2-діамінобензолу. Кристалічна тверда речовина з (1) т.пл.: 178-182°С, після знову здійсненої кристалізації з (2) т.пл.: 299-301°С. b) 3N-(4,6-Дифтор-2-бензімідазоліл)-4-метил3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) а) транс-N-(2-Аміноциклогексил)-N'-(4-метил-3методиці з N-(2-аміно-3,5-дифторфеніл)-N'-(4тієніл)тіосечовина (рацемат) метил-3-тієніл)тіосечовини і метилйодиду. АморфОтримують аналогічно вказаній в прикладі 1b) ний осад, який кристалізують з етилацетату. Крисреакції з 4-метил-3-тієнілізотіоціанату і рацемічноталічна тверда речовина; т.пл.: 232-234°С. го транс-1,2-діаміноциклогексану. Кристалічна Приклад 7 тверда речовина; т.пл.: 205-210°С. 3N-(3,4,5,6-Тетрафтор-2-бензімідазоліл)-4b) транс-3N-(3а,4,5,6,7,7а-Гексагідро-1Н-2метил-3-тієніламінгідрохлорид бензімідазоліл)-4-метил-3-тієніламінгідрохлорид (рацемат) 0,6г рацемічної транс-N-(2-амiноциклогексил)N'-(4-метил-3-тiенiл)тіосечовини суспендують в 60мл толуолу і розчиняють шляхом нагрівання до температури 90°С. Залишають охолоджуватися до температури 70°С, додають по краплях розчин 0,376г дициклогексилкарбодііміду в 5мл безводноа) N-(2-Аміно-3,4,5,6-тетрафторфеніл)-N'-(4го толуолу, перемішують загалом протягом прибметил-3-тієніл)тіосечовина лизно 10 годин при температурі 70°С і протягом 2Отримують аналогічно вказаній в прикладі 1b) 3 днів при кімнатній температурі. Кристалічний реакції з 4-метил-3-тієнілізотіоціанату і 3,4,5,6осад відфільтровують, розчинник видаляють в тетрафтор-1,2-діамінобензолу. Кристалічна тверда ротаційному випарнику при зниженому тиску і таречовина; т.пл.: 286-290°С. ким чином отриманий маслянистий залишок розb) 3N-(3,4,5,6-Тетрафтор-2-бензімідазоліл)-4чиняють в невеликій кількості етилацетату. Після метил-3-тієніламінгідрохлорид додавання безводного розчину хлороводню в діеОтримують аналогічно вказаній в прикладі 1с) тиловому ефірі утворюється в'язкий осад, який методиці з N-(2-аміно-3,4,5,6-тетрафторфеніл)-N'після додавання невеликої кількості етанолу крис(4-метил-3-тієніл)тіосечовини і метилйодиду. Амоталізується. Кристалічна тверда речовина; т.пл.: рфний осад, який кристалізують з етилацетату. 261-264°С. Кристалічна тверда речовина; т.пл.: 225-228°С. Приклад 10 Приклад 8 Транс-R,R-3N-(3а,4,5,6,7,7а-Гексагідро-1Н-23N-(4-Метил-2-бензімідазоліл)-4-метил-3бензімідазоліл)-4-метил-3-тієніламінгідрохлорид тієніламінгідрохлорид a) N-(2-Аміно-3-метилфеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і 3-метил1,2-діамінобензолу. Кристалічна тверда речовина; т.пл.: 184-186°С. b) 3N-(4-Метил-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці з N-(2-аміно-3-метилфеніл)-N'-(4-метил3-тієніл)тіосечовини і метилйодиду. Аморфний осад, який кристалізують з ацетону. Кристалічна тверда речовина; температура розкладання: 320°С. Приклад 9 транс-3N-(3а,4,5,6,7,7а-Гексагідро-1Н-2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид (рацемат) а) Транс-R,R-N-(2-Аміноциклогексил)-N'-(4метил-3-тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і транс-R,R1,2-діаміноциклогексану шляхом розділення за допомогою колонкової хроматографії на силікагелі при елююванні сумішшю розчинників, що складається з 10 частин етилацетату, 5 частин н-гептану, 5 частин дихлорметану, 5 частин метанолу і 1 частини 26%-го водного розчину аміаку (надалі позначають як "суміш 4") у вигляді аморфного маслянистого продукту поряд з більш високомолекулярним кристалічним продуктом з т.пл. 94-100°С. Аморфний продукт піддають подальшому перетворенню без подальшого очищення. b) транс-R,R-3N-(3а,4,5,6,7,7а-Гексагідро-1Н-2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці шляхом введення у взаємодію R,R-N-(2аміноциоогексил)-N'-(4-метил-3-тієніл)тіосечовини і метилйодиду в безводному метанолі як розчиннику і реакційному середовищі. Аморфний осад, який піддають хроматографії на силікагелі за до 29 77551 помогою суміші 4 як елююючого засобу і кристалізують з ацетону. Кристалічна тверда речовина; т.пл.: 235-238°С. Приклад 11 транс-S,S-3N-(3а,4,5,6,7,7а-Гексагідро-1Н-2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид а)транс-S,S-3N-(2-Аміноциклогексил)-N'-(4метил-3-тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і транс-S,S1,2-діаміноциклогексану шляхом розділення за допомогою колонкової хроматографії на силікагелі при використанні суміші 4 як елююючого засобу у вигляді аморфного маслянистого продукту поряд з більш високомолекулярним продуктом з т.пл. 94102°С. Аморфний продукт піддають подальшому перетворенню без подальшого очищення. b) транс-S,S-3N-(3а,4,5,6,7,7а-Гексагідро-1Н-2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці шляхом введення у взаємодію S,S-N-(2аміноцшшогексил)-N'-(4-метил-3тієніл)тіосечовини і метилйодиду в безводному етанолі як розчиннику і реакційному середовищі. Аморфний осад, який піддають хроматографії на силікагелі за допомогою суміші 4 як елююючого засобу і кристалізують з ацетону. Кристалічна тверда речовина; т.пл.:225-230°С. Приклад 12 2-Хлор-3N-(2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид і 2,5-дихлор-3N-(2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(2-бензімідазоліл)-4-метил-3тієніламінгідрохлориду і N-хлорсукциніміду в крижаній оцтовій кислоті. Колонкова хроматографія на силікагелі за допомогою суміші 17 як елююючого засобу приводить до відділення 2,5-дихлор-3N(2-бензімідазоліл)-4-метил-3тієніламінгідрохлориду (безбарвна кристалічна сполука; т.пл.: 291°С) від 2-хлор-3N-(2бензімідазоліл)-4-метил-3-тієніламінгідрохлориду (безбарвна кристалічна сполука; т.пл.: 257-259°С). Приклад 13 2-Хлор-3N-(4-метил-2-бензімідазоліл)-4-метил3-тієніламінгідрохлорид 30 Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(4-метил-2-бензімідазоліл)-4-метил3-тієніламінгідрохлориду і N-хлорсукциніміду в крижаній оцтовій кислоті. Після колонкової хроматографії на силікагелі при використанні суміші 17 як елююючого засобу отримують 2-хлор-3N-(4метил-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид у вигляді безбарвного аж до забарвленого в слабо-жовтуватий колір кристалічного продукту, т.пл.: 255-259°С. Приклад 14 2-Хлор-3N-(4,5,6,7-тетрафтор-2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(4,5,6,7-тетрафтор-2бензімідазоліл)-4-метил-3-тієніламінгідрохлориду і N-хлорсукциніміду в крижаній оцтовій кислоті. Кристалічний продукт; т.пл.: 233-235°С. Приклад 15 транс-2-Хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н2-бензімідазоліл)-4-метил-3-тієніламінгідрохлорид (рацемат) Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(3a,4,5,6,7,7a-гексагідро-1Н-2бензімідазоліл)-4-метил-3-тієніламінгідрохлориду (рацемат) і N-хлорсукциніміду в крижаній оцтовій кислоті. Кристалічний продукт; т.пл.: 258-260°С. Приклад 16 Транс-R,R-2-Хлор-3N-(3а,4,5,6,7,7а-гексагідро1Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид ітранс-R,R-2,5-дихлор-3N(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-4метил-3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 2 методиці з Tpaнc-R,R-3N-(3а,4,5,6,7,7а-гексагідро1Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлориду і N-хлорсукциніміду в крижаній оцтовій кислоті після хроматографічного 31 77551 32 розділення обох кристалічних продуктів в нижченаведеній послідовності: a) Транс-R,R-2,5-дихлор-3N-(3а,4,5,6,7,7агексагідро-1Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид; розкладання при спіненні, починаючи з температури 80°С; Отримують аналогічно вказаній в прикладі 18 b) транс-R,R-2-хлор-3N-(3а,4,5,6,1,7аметодиці з транс-R,R-3N-(3а,4,5,6,7,7а-гексагідрогексагідро-1Н-2-бензімідазоліл)-4-метил-31Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид; кристалічний продукт; т.пл.: тієніламінгідрохлориду і N-бромсукциніміду в кри260-262°С. жаній оцтовій кислоті. Після колонкової хроматогПриклад 17 рафії на силікагелі при використанні суміші 1 як транс-S,S-2-Хлор-3N-(3а,4,5,6,7,7а-гексагідроелююючого засобу і обробки розчином газоподіб1Н-2-бензімідазоліл)-4-метил-3ного хлороводню в діетиловому ефірі, після фрактієніламінгідрохлорид ційної кристалізації з етилацетату, отримують: транс-R,R-2-бром-3N-(3а,4,5,6,7,7а-гексагідро1Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид; кристалічний продукт; т.пл.: 215-218°С; і транс-R,R-2,5-дибром-3N-(3а,4,5,6,7,7агексагідро-1Н-2-бензімідазоліл)-4-метил-3Отримують аналогічно вказаній в прикладі 2 тієніламінгідрохлорид; кристалічний продукт; т.пл.: методиці з Tpaнc-S,S-3N-(3а,4,5,6,1,7а-гексагідро218-220°С. 1Н-2-бензімідазоліл)-4-метил-3Приклад 20 тієніламінгідрохлориду і N-хлорсукциніміду в кри3N-(4-Хлор-2-бензімідазоліламіно)-4жаній оцтовій кислоті після хроматографічного метилтіофенгідрохлорид розділення. Безбарвний кристалічний продукт; т.пл.: 258-260°С. Приклад 18 2-Бром-3N-(2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид і 2,5-дибром-3N-(2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(2-бензімідазоліл)-4-метил-3тієніламінгідрохлориду і N-бромсукциніміду (замість N-хлорсукциніміду) в крижаній оцтовій кислоті. Після колонкової хроматографії на силікагелі при використанні суміші з 5 частин дихлорметану, 3 частин н-гептану, 1 частини крижаної оцтової кислоти і 1 частини етанолу (в подальшому позначають як "суміш 1") як елююючий засіб і обробка розчином газоподібного хлороводню в діетиловому ефірі отримують, шляхом фракційної кристалізації з етилацетату, 2-бром-3N-(2-бензімідазоліл)4-метил-3-тієніламінгідрохлорид, кристалічний продукт з т.пл.: 228-231°С, і 2,5-дибром-3N-(2бензімідазоліл)-4-метил-3-тієніламінгідрохлорид, кристалічний продукт з т.пл. 208-210°С. Приклад 19 транс-R,R-2-бром-3N-(3а,4,5,6,7,7а-гексагідро1Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид і транс-R,R-2,5-дибром-3N(3а,4,5,6,7,7а -гексагідро-1Н-2-бензімідазоліл)-4метил-3-тієніламінгідрохлорид а) N-(2-Аміно-3-хлорфеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 1b) реакції з 4-метил-3-тієнілізотіоціанату і 3-хлор-1,2діамінобензолу (отримують шляхом каталітичного гідрування 3-хлор-2-нітроаніліну за допомогою платини на активному вугіллі при нормальному тиску і при кімнатній температурі). Кристалічна тверда речовина; т.пл.: 298-305°С. b) 3N-(4-Хлор-2-бензімідазоліламіно)-4метилтіофенгідрохлорид Отримують аналогічно вказаній в прикладі 1с) методиці з N-(2-аміно-3-хлорфеніл)-N'-(4-метил-3тієніл)тіосечовини і метилйодиду. Аморфний осад, який кристалізують з етилацетату. Кристалічна тверда речовина; температура розкладання: 240245°С. Приклад 21 2-Хлор-3N-(4-хлор-2-бензімідазоліламіно)-4метилтіофенгідрохлорид Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(4-хлор-2-бензімідазоліл)-4-метил-3тієніламінгідрохлориду і N-хлорсукциніміду в крижаній оцтовій кислоті. Після колонкової хроматографії на силікагелі при використанні суміші з 10 33 77551 34 частин дихлорметану і 1 частини метанолу як 2-бензімідазоліламіно)-4-метилтіофенгідрохлорид елююючого засобу отримують 2-хлор-3N-(4-хлор2-бензімідазоліламіно)-4-метилтіофенгідрохлорид у вигляді безбарвної аж до забарвленої в слабожовтуватий колір твердої речовини після кристалізації з етилацетату; т.пл.: 270-272°С. Приклад 22 2-Бром-3N-(4-хлор-2-бенеімідазоліламіно)-4метилтіофенгідрохлорид До роздану з 0,214г 3N-(4-фтор-2 Отримують аналогічно вказаній в прикладі 2 методиці з 3N-(4-хлор-2-бензімідазоліламіно)-4метилтіофенгідрьхлориду і N-бромсукциніміду (замість N-хлорсукциніміду) в крижаній оцтовій кислоті. Після колонкової хроматографії на силікагелі при використанні суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти як елююючого засобу і обробки розчином газоподібного хлороводню в діетиловому ефірі, шляхом фракційної кристалізації з етилацетату в присутності насиченого хлороводнем діетилового ефіру, отримують 2-бром-3N-(4-хлор2-бензімідазоліламіно)-4-метилтіофенгідрохлорид. Кристалічний продукт з т.пл. 278-280°С. Приклад 23 (2-Бром-4-метилтіофен-3-іл)-(5-фтор-1Нбензімідазол-2-іл)амінгідрохлорид 300мг (5-Фтор-1Н-бензімідазол-2-іл)-(4метилтіофен-3-іл)аміну (приклад 1) розчиняють в 50мл крижаної оцтової кислоти. При кімнатній температурі і при інтенсивному перемішуванні повільно додають по краплях розчин 207мг Nбромсукциніміду в 10мл крижаної оцтової кислоти. По закінченні додання ще додатково перемішують протягом 10 хвилин, потім крижану оцтову кислоту відганяють у вакуумі, залишок розчиняють в етилацетаті і промивають насиченим розчином карбонату калію. Після висушування над сульфатом магнію відфільтровують і концентрують. Залишок очищають препаративною хроматографією, фракції, що містять продукт, об'єднують, видаляють ацетонітрил, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію і фільтрують. Після видалення розчинника залишок змішують з водою і 2н соляною кислотою і піддають сушінню виморожуванням. Отримують 245мг цільового продукту. LCMS, Rt (В): 0,95хв.; мас-спектрометрія (МС) (іонізація електронним розпиленням з утворенням позитивних іонів (ES+, М+Н+): 326,09. Приклад 24 2-Бром-3N-(4-фтор-2-бензімідазоліламіно)-4метилтіофенгідрохлорид і 2,5-дибром-3N-(4-фтор бензімідазоліламіно)-4-метилтіофенгідрохлориду в 6мл крижаної оцтової кислоти додають розчин 0,161г N-бромсукциніміду в 6мл крижаної оцтової кислоти і суміш перемішують протягом 30 хвилин при кімнатній температурі. Після відгонки розчинника залишок змішують з водою, підлуговують за допомогою 2н розчину NaOH і екстрагують етилацетатом. Органічні фази сушать, розчинник відганяють і залишок розділяють колонковою хроматографією на силікагелі при використанні суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти. Гідрохлориди обох сполук отримують шляхом відгонки розчинників з фракціонованих розчинів, розчинення в етилацетаті і осадження шляхом додання насиченого хлороводнем діетилового ефіру. При цьому кристалізацію прискорюють за рахунок здійснюваного нагрівання. Приклад 24а: 2-бром-3N-(4-фтор-2-бензімідазоліламіно)-4метилтіофенгідрохлорид: безбарвні кристали; т.пл.: 212°С (розкладання). Приклад 24b: 2,5-дибром-3N-(4-фтор-2бензімідазоліламіно)-4-метилтіофенгідрохлорид: безбарвні кристали; т.пл.: 242-244°С (розкладання). Приклад 25 3N-(5-Метокси-2-бензімідазоліламіно)-4метилтіофен a) N-(2-Аміно-4-метоксифеніл)-N'-(4-метил-3тієніл)тіосечовина Суміш з 5,89г 4-метилтіофен-3-ізотіоціанату і 5г 4-метокси-1,2-діамінобензолу в 60мл безводного тетрагідрофурану перемішують протягом 2 годин при кімнатній температурі і розчинник відганяють. Залишок змішують з водою, екстрагують етилацетатом, розчин темного кольору обробляють активним вугіллям і знов випаровують органічний розчинник. Залишок багато разів обробляють діізопропіловим ефіром злегка при нагріванні і відфільтровують тверду речовину. Забарвлена в коричневий колір кристалічна тверда речовина; т.пл.: 143-146°С. b) Суміш з 2,83г N-(2-аміно-4-метоксифеніл)N'-(4-метил-3-тієніл)тіосечовини, 8,5г метилйодиду і 100мл безводного етанолу кип'ятять із зворотним холодильником протягом 5 годин, потім розчинник відганяють і залишок змішують з водою. Підлуговують за допомогою 2н розчину гідроксиду натрію, 35 77551 36 екстрагують етилацетатом, органічну фазу обробкрижаної оцтової кислоти протягом приблизно 2ляють водою і потім активним вугіллям і очищають 2,5 годин при температурі 55°С отримують 2,5колонковою хроматографією на силікагелі при видихлор-3N-(5-метокси-2-бензімідазоліламіно)-4користанні елююючої суміші з 20 частин етилацеметилтіофен. Кристалічна тверда речовина; т.пл.: тату, 10 частин н-гептану і 3 частин крижаної оцто278-282°С. вої кислоти. Отримують 3N-(5-метокси-2Приклад 29 бензімідазоліламіно)-4-метилтіофен у вигляді 3N-(4-Метокси-2-бензімідазоліламіно)-4аморфного продукту. метилтіофенгідрохлорид Приклад 26 3N-(5-Метокси-2-бензімідазоліламіно)-4метилтіофенгідрохлорид Отримують шляхом осадження з розчину 0,2г 3N-(5-метокси-2-бензімідазоліламіно)-4метилтіофену (приклад 25) в 10мл етилацетату за допомогою насиченого розчину газоподібного хлороводню в діетиловому ефірі у вигляді кристалічного осаду; т.пл.: 222-225°С. Приклад 27 2-Хлор-3N-(5-метокси-2-бензімідазоліламіно)4-метилтіофенгідрохлорид Суміш з 0,519г 3N-(5-метокси-2бензімідазоліламіно)-4-метилтіофенгідрохлориду, 0,046г N-хлорсукциніміду і 10-15мл крижаної оцтової кислоти нагрівають при температурі 45°С протягом приблизно 2-2,5 годин. Потім відганяють крижану оцтову кислоту, до залишку додають воду і за допомогою 2н розчину NaOH встановлюють значення рН на рівні 9-10. Екстрагують етилацетатом, розчинник випаровують і залишок хроматографують на силікагелі при використанні колонки середнього тиску за допомогою суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти. Отриману після відгонки розчинника основу в етилацетаті за допомогою насиченого розчину хлороводню в діетиловому ефірі перетворюють в гідрохлорид і кристалізують з етилацетату. Кристалічна тверда речовина; т.пл.: 182-186°С. Приклад 28 2,5-Дихлор-3N-(5-метокси-2бензімідазоліламіно)-4-метилтіофенгідрохлорид При аналогічній обробці реакційної суміші з 3N-(5-метокси-2-бензімідазоліламіно)-4метилтіофенгідрохлориду, N-хлорсукциніміду і а) 3-Метокси-1,2-діамінобензол Отримують у вигляді коричневої олії шляхом гідрування 2-метокси-6-нітроаніліну за допомогою газоподібного водню і нікелю Ренея як каталізатора при кімнатній температурі і тиску 3бар. Продукт без подальшого очищення перетворюють в тіосечовину. b) N-(2-Аміно-3-метоксифеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно описаній в прикладі 25а) методиці з 3-метокси-1,2-діамінобензолу, 4метил-3-тієнілізотіоціанату в безводному тетрагідрофурані і шляхом подальшої хроматографії середнього тиску на силікагелі за допомогою суміші з 1 частини толуолу і 1 частини етилацетату. Кристалічна тверда речовина; т.пл.: 148-153°С. Затвердження розплаву і найближчої т.пл. при 260°С. с) 3N-(4-Метокси-2-бензімідазоліламіно)-4метилтіофенгідрохлорид Отримують аналогічно описаним в прикладах 25 і 26 методикам з N-(2-аміно-3-метоксифеніл)-N'(4-метил-3-тієніл)тіосечовини шляхом нагрівання з метилйодидом в тетрагідрофурані, аналогічної обробки і обробки бензімідазолу за допомогою НСI в діетиловому ефірі. Кристалічна тверда речовина; т.пл.: 230-235°С. Приклад 30 2-Хлор-3N-(4-метокси-2-бензімідазоліламіно)4-метилтіофенгідрохлорид Суміш з 0,1г 3N-(4-метокси-2бензімідазоліламіно)-4-метилтіофенгідрохлориду, 0,046г N-хлорсукциніміду і 10-15мл крижаної оцтової кислоти нагрівають при температурі 40°С протягом приблизно 2-2,5 годин. Потім відганяють крижану оцтову кислоту, до залишку додають воду і за допомогою 2н розчину NaOH встановлюють значення рН на рівні 9-10. Екстрагують етилацетатом, розчинник випаровують і залишок хроматографують на силікагелі при використанні колонки середнього тиску за допомогою суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин кри 37 77551 38 жаної оцтової кислоти. Таким чином отриману осня рН на рівні 9-10. Екстрагують етилацетатом, нову в етилацетаті за допомогою насиченого розрозчинник випаровують і залишок хроматографучину хлороводню в діетиловому ефірі перетворюють на силікагелі при використанні колонки середють в гідрохлорид. Безбарвна аж до забарвленої в нього тиску за допомогою суміші з рівних частин ясно-жовтий колір кристалічна тверда речовина; толуолу і етилацетату. Таким чином отриману піст.пл.: 248-250°С. ля відгонки розчинника основу в етилацетаті за Приклад 31 допомогою насиченого розчину хлороводню в діе3N-(4-Хлор-6-трифторметил-2тиловому ефірі перетворюють в гідрохлорид. Безбензімідазоліламіно)-4-метилтіофенгідрохлорид барвна аж до забарвленої в ясно-жовтий колір кристалічна тверда речовина; т.пл.: 247-250°С. Приклад 33 3N-(4-Карбокси-2-бензімідазоліламіно)-4метилтіофенгідрохлорид а) N-(2-Аміно-3-хлор-5-трифторметилфеніл)N'-(4-метил-3-тієніл)тіосечовина Отримують аналогічно описаній в прикладі 25а) методиці шляхом реакції 3-хлор-5трифторметил-1,2-діамінобензолу і 4-метил-3тієнілізотіоціанату в безводному тетрагідрофурані протягом 3 днів при кімнатній температурі. Після відгонки розчинника і додання до залишку води екстрагують етилацетатом, знов відганяють розчинник і аморфний залишок кристалізують з діізопропілового ефіру; т.пл.: >310°С. b) 3N-(4-Хлор-6-трифторметил-2бензімідазоліламіно)-4-метилтіофенгідрохлорид Отримують аналогічно описаним в прикладах 25 і 26 методикам з N-(2-аміно-3-хлор-5трифторметилфеніл)-N'-(4-метил-3тієніл)тіосечовини шляхом кип'ятіння із зворотним холодильником протягом 5 годин з метилйодидом в тетрагідрофурані, аналогічної обробки і очищення колонковою хроматографією середнього тиску на силікагелі за допомогою суміші з рівних об'ємних частин етилацетату і толуолу. Після випаровування розчинника залишок розчиняють в етилацетаті і шляхом додання насиченого розчину хлороводню в діетиловому ефірі отримують 3N-(4хлор-6-трифторметил-2-бензімідазоліламіно)-4метилтіофенгідрохлорид у вигляді кристалічного осаду; тверда речовина; т.пл.: 210-213°С. Приклад 32 2-Хлор-3N-(4-хлор-6-трифторметил-2бензімідазоліламіно)-4-метилтіофенгідрохлорид Суміш з 0,34г 3N-(4-метокси-2бензімідазоліламіно)-4-метилтіофенгідрохлориду, 0,151г N-хлорсукциніміду і 20мл крижаної оцтової кислоти витримують протягом 0,5 години при кімнатній температурі і нагрівають протягом години при температурі 60°С. Потім відганяють крижану оцтову кислоту, до залишку додають воду і за допомогою 2н розчину NaOH встановлюють значен а)-N-(2-Аміно-3-карбоксифеніл)-N'-(4-метил-3тієніл)тіосечовина Отримують аналогічно описаній в прикладі 25а) методиці з 3-карбокси-1,2-діамінобензолу, 4метил-3-тієнілізотіоціанату в безводному тетрагідрофурані і шляхом подальшої хроматографії середнього тиску на силікагелі за допомогою суміші з 12 частин дихлорметану і 1 частини метанолу. Аморфний продукт. b) 3N-(4-Карбокси-2-бензімідазоліламіно)-4метилтіофенгідрохлорид Отримують шляхом кип'ятіння із зворотним холодильником розчину з 1,12г N-(2-аміно-3карбоксифеніл)-N'-(4-метил-3-тієніл)тіосечовини і 3,1г метилйодиду в 60мл етанолу. Розчинник випаровують, залишок змішують з водою, за допомогою 2н соляної кислоти встановлюють значення рН на рівні 5 і осад відфільтровують. Кристалічна тверда речовина; температура розкладання: 265285°С. Приклад 34 2-Хлор-3N-(4-карбокси-2-бензімідазоліламіно)4-метилтіофенгідрохлорид Отримують аналогічно описаній в прикладі 32 методиці з 0,2г 3N-(4-карбокси-2бензімідазоліламіно)-4-метилтіофенгідрохлориду і 0,103г N-хлорсукциніміду в 20-25мл крижаної оцтової кислоти і осадження відповідного гідрохлориду в етилацетаті за допомогою насиченої НСI діетилового ефіру і подальшої кристалізації з діізопропілового ефіру і етилацетату. Температура розкладання: 170°С. Приклад 35 3N-[4-(1-Піперидинокарбоніл)-2бензімідазоліламіно]-4-метилтіофенгідрохлорид 39 До суміші з 0,330г 3N-(4-карбокси-2бензімідазоліламіно)-4-метилтіофенгідрохлориду, 30мл безводного тетрагідрофурану і 5мл безводного диметилацетаміду додають 0,215г Ν,Ν'карбонілдіімідазолу. Перемішують протягом приблизно 4 годин при кімнатній температурі, причому закінчується виділення діоксиду вуглецю, і після цього змішують з 0,411г піперидину. Розчин перемішують протягом 2 годин при кімнатній температурі і після подальшого втримання протягом ночі розчинник відганяють при зниженому тиску. Залишок перемішують з водою, тверду речовину відфільтровують, розчиняють її в етилацетаті, видаляють нерозчинну частину шляхом відфільтровування і розчинник відганяють при зниженому тиску. Пінистий аморфний продукт. Приклад 36 2-Хлор-4-метил-3N-[4-(1-піперидинокарбоніл)2-бензімідазоліламіно]тіофенгідрохлорид Суміш з 0,2г 3N-[4-(1-піперидинокарбоніл)-2бензімідазоліламіно]-4-метилтіофенгідрохлориду і 0,086г N-хлорсукциніміду приблизно в 20мл крижаної оцтової кислоти перемішують протягом 1,5 годин при кімнатній температурі і протягом приблизно 30 хвилин при температурі 35°С, розчинник відганяють і залишок після додання води підлуговують за допомогою 2н розчину NaOH. Після екстракції етилацетатом розчинник випаровують і залишок очищають хроматографією середнього тиску на колонці з силікагелем за допомогою сумішпз 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти. Розчинник відганяють, залишок розчиняють в етилацетаті і підкисляють за допомогою насиченого хлороводнем діетилового ефіру. Аморфний залишок кристалізують з суміші етилацетату з невеликою кількістю ацетону і невеликою кількістю етанолу. Аморфна тверда речовина; температура розкладання, починаючи з 100°С. Приклад 37 2-Хлор-3N-(4-фтор-2-бензімідазоліламіно)-4метилтіофенгідрохлорид 77551 40 0,234г 3N-(4-фтор-2-бензімідазоліламіно)-4метилтіофенгідрохлориду в приблизно 20мл крижаної оцтової кислоти змішують з 0,132г Nхлорсукциніміду, перемішують протягом 30 хвилин при кімнатній температурі і протягом наступних 1,5 годин при температурі 50-60°С. Після відгонки оцтової кислоти при зниженому тиску залишок змішують з водою і за допомогою 2н розчину NaOH встановлюють значення рН приблизно 10-11, екстрагують етилацетатом, який потім відганяють. Залишок хроматографують на силікагелі при використанні колонки в умовах середнього тиску за допомогою суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти. Після концентрування залишок розчиняють в невеликій кількості етилацетату і гідрохлорид осаджують шляхом додання насиченого хлороводнем діетилового ефіру. Безбарвна аж до забарвленої в ясно-жовтий колір кристалічна тверда речовина; т.пл.: 268-270°С. Приклад 38 2-Хлор-3N-(4-гідрокси-2-бензімідазоліламіно)4-метилтіофенгідрохлорид До суспензії 0,29г активного безводного хлориду алюмінію в 10мл безводного дихлорметану додають суспензію 0,13г 2-хлор-3N-(4-метокси-2бензімідазоліламіно)-4-метилтіофенгідрохігориду в приблизно 20мл безводного дихлорметану і реакційну суміш перемішують протягом 2 годин при температурі 55°С. Після охолоджування реакційну суміш виливають у воду з льодом, екстрагують етилацетатом, органічну фазу сушать над сульфатом натрію і розчинник відганяють. Залишок хроматографують на колонці з силікагелем в умовах середнього тиску за допомогою суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти і елюат випаровують при зниженому тиску. Залишок розчиняють в етилацетаті і гідрохлорид осаджують шляхом додання насиченого хлороводнем діетилового ефіру. Кристалічна тверда речовина; т.пл.: 246-248°С. Приклад 39 2-Хлор-3N-(2-бензімідазоліламіно)-4метилтіофен Отримують шляхом додання 2н розчину NaOH до розчину 3г 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофенгідрохлориду в 200мл води, встановлюючи значення рН аж до 10. Кристали відфільтровують і додатково промивають багато разів водою. Вихід: 2,52г. Безбарвний кристалічний порошок; т.пл.: 182-185°С. Приклад 40 41 2-Хлор-3N-(2-бензімідазоліламіно)-4метилтіофенгідробромід 0,25г 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофену розчиняють в 10мл етанолу, потім змішують з 0,1мл 48% НВr і короткочасно перемішують при кімнатній температурі. Розчинник відганяють і залишок піддають кристалізації з етилацетату. Вихід: 0,29г. Безбарвні кристали; температура розкладання: 252-254°С. Приклад 41 Сіль адипінової кислоти 2-хлор-3N-(2бензімідазоліламіно)-4-метилтіофену Отримують аналогічно описаній в прикладі 40 методиці з 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофену з одним еквівалентом адипінової кислоти. Безбарвні кристали; т. пл.: 155-157°С. Приклад 42 Сіль щавлевої кислоти 2-хлор-3N-(2бензімідазоліламіно)-4-метилтіофену Отримують аналогічно описаній в прикладі 40 методиці шляхом введення у взаємодію 2-хлор3N-(2-бензімідазоліламіно)-4-метилтіофену з одним еквівалентом щавлевої кислоти в етилацетаті. Безбарвні кристали; т.пл.: 220-222°С. Приклад 43 Сіль фосфорної кислоти 2-хлор-3N-(2бензімідазоліламіно)-4-метилтіофену Отримують аналогічно описаній в прикладі 40 методиці з 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофену з одним еквівалентом фосфорної кислоти. Безбарвні кристали; температура розкладання: 113-175°С. Приклад 44 (1Н-Бензімідазол-2-іл)-(2-хлор-4-метилтіофен3-іл)метиламін 77551 42 До розчину з 125мг 2-хлор-3N-(2бензімідазоліл)-4-метил-3-тієніламіну (з прикладу 39) і 20мл безводного метанолу додають 66мг порошкоподібного сухого карбонату калію. Потім за відсутності вологи і при інтенсивному перемішуванні додають по краплях 74мл метилйодиду і суміш кип'ятять із зворотним холодильником протягом трьох днів. Після видалення розчинника залишок розподіляють між етилацетатом і водою, етилацетатну фазу сушать над сульфатом магнію, сульфат магнію відфільтровують і фільтрат випаровують досуха. Після цього очищають за допомогою ВЕРХ. Фракції, що містять продукт, об'єднують і після видалення ацетонітрилу піддають сушінню виморожуванням. З метою подальшої обробки потім хроматографують на силікагелі за допомогою суміші етилацетату і гептану (в співвідношенні 1:4). Після об'єднання фракцій, що містять продукт, концентрують досуха, обробляють за допомогою НСI і піддають сушінню виморожуванням. Отримують 5мг твердої речовини. LCMS, Rt (А): 2,04хв.; МС (ES+, M+H+): 278,05. Приклад 45 Сіль трифтороцтової кислоти (5,6-дифтор-1Нбензімідазол-2-іл)-(4-метилтіофен-3-іл)аміну До розчину з 1г 1,2-діаміно-4,5-дифторбензолу в 20мл абсолютного тетрагідрофурану додають по краплях розчин 1,08г 3-ізотіоціанат-4метилтіофену в 30мл абсолютного тетрагідрофурану. Потім перемішують протягом 2 годин при кімнатній температурі і залишають стояти протягом ночі. Після додання 0,44мл метилйодиду перемішують протягом 8 годин і залишають стояти протягом ночі. Після цього тетрагідрофуран видаляють, залишок розподіляють між етилацетатом і водою, фази розділяють і етилацетатну фазу сушать над сульфатом магнію. Залишок наносять на силікагель і хроматографують шляхом пропущення через силікагель за допомогою суміші н-гептану і етилацетату в співвідношенні 1:1 як елююючий засіб. Отримують 229мг цільової сполуки у вигляді вільної основи. Забруднену фракцію, отриману в результаті вищезгаданої хроматографії, очищають за допомогою препаративної ВЕРХ. При цьому після сушіння виморожуванням виділяють 42,2мг цільової сполуки у вигляді солі трифтороцтової кислоти. LCMS, Rt (А): 1,98хв.; МС (ES+, M+H+): 266,13. Приклад 46 (2-Хлор-4-метилтіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл) амінгідрохлорид До розчину 225мг (5,6-дифтор-1Нбензімідазол-2-іл)-(4-метилтіофен-3-іл)аміну в 5мл 43 77551 44 крижаної оцтової кислоти при кімнатній темперадповідно до [патенту Великобританії 1131191]. турі додають по краплях розчин з 124,6мг NПри цьому 2-хлорциклогексанон вводять у взаєхлорсукииніміду в 5мл крижаної оцтової кислоти. модію з фталімідом, отримуючи 2-(2Потім перемішують протягом 3,5 годин при кімнатоксоциклогексил)ізоіндол-1,3-діон, який за допомоній температурі. Після цього крижану оцтову кисгою етиленгліколю в присутності плоту видаляють, залишок обробляють водою і за толуолсульфокислоти каталізують з отриманням допомогою 2Μ розчину гідроксиду натрію встанов2-(1,4-діоксаспіро[4,5]дец-6-ил)ізоіндол-1,3-діону. люють значення рН на рівні 10. Водну фазу екстПісля обробки гідразингідратом для відщеплення рагують три рази етилацетатом, об'єднані органічфталімідного залишку отримують вказаний в загоні фази сушать над сульфатом магнію і розчинник ловку 1,4-діоксаспіро[4,5]дец-6-ил амін. видаляють. Залишок очищають препаративною b) 1-(1,4-Діоксаспіро[4,5]дец-6-ил)-3-(4хроматографією, фракції, що містять продукт, метилтіофен-3-іл)тіосечовина об'єднують, ацетонітрил видаляють, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію, відфільтровують і концентрують. Залишок обробляють водою, підкисляють за допомогою 10%-ої соляної кислоти і піддають сушінню виморожуванням. Отримують 81мг цільового продукту у вигляді До розчину з 300мг 1,4-діоксаспіро[4,5]дец-6твердої речовини. иламіну в 10мл абсолютного тетрагідрофурану LCMS, Rt (А): 2,15хв.; МС (ES+, M+H+): 300,11. додають по краплях розчин з 296,2мг 3Приклад 47 ізотіоціанато-4-метилтіофену (див. приклад 1а) в (2-Бром-4-метилтіофен-3-іл)-(5,6-дифтор-1Н10мл абсолютного тетрагідрофурану, перемішубензімідазол-2-іл)амін ють протягом 2 годин при кімнатній температурі і потім розчинник видаляють. Залишок очищають препаративною хроматографією, фракції, що містять продукт, об'єднують, видаляють ацетонітрил, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію і фільтрують. Отримують 428мг цільового продукту. При кімнатній температурі, в реакційній посуLCMS, Rt (А): 3,57хв.; МС (ES+, M+H+): 313,19. дині, до розчину з 15мг солі трифтороцтової кисс) 1-(1,4-Діоксаспіро[4,5]дец-6-ил)-2-метил-3лоти (5,6-дифтор-1Н-бензімідазол-2-іл)-(4(4-метилтіофен-3-іл)ізотіосечовина метилтіофен-3-іл)аміну (приклад 45) в 0,5мл крижаної оцтової кислоти додають по краплях розчин з 8мг N-бромсукциніміду в 0,5мл крижаної оцтової кислоти і перемішують протягом 0,5 години при кімнатній температурі. Потім оцтову кислоту видаляють і залишок змішують з насиченим розчином карбонату калію і етилацетатом. Після відділення органічної фази екстрагують два рази етилацета393мг 1-(1,4-діоксаспіро[4,5]дец-6-ил)-3-(4том. Об'єднані органічні фази сушать над сульфаметилтіофен-3-іл)ізотіосечовини розчиняють в том магнію і потім осушувач відфільтровують. За8,5мл абсолютного тетрагідрофурану і змішують з лишок, що залишається післявидалення розчином з 179мг метилйодиду в 0,5мл абсолютрозчинника, очищають препаративною хроматогного тетрагідрофурану. Потім перемішують протярафією. Фракції, що містять продукт, об'єднують, гом 2 днів на піщаній бані при температурі 70°С. видаляють ацетонітрил, змішують з насиченим Після цього реакційну суміш змішують з етилацерозчином гідрокарбонату натрію і екстрагують три татом і промивають 2 рази водою. Органічну фазу рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію і після відфільтросушать над сульфатом магнію і фільтрують. Після вування видаляють розчинник. Залишок очищають видалення етилацетату залишок обробляють топрепаративною хроматографією, фракції, що міслуолом і потім висушують у високому вакуумі. тять продукт, об'єднують, ацетонітрил видаляють, Отримують 8,1мг цільової сполуки. + + підлуговують і екстрагують три рази етилацетатом. LCMS, Rt (D): 1,45хв.; МС (ES , M+H ): 343,96. Органічні фази об'єднують, сушать над сульфатом Приклад 48 магнію і фільтрують. Отримують 59мг цільового [(2-Хлор-4-метилтіофен-3-іл)-(4,5,6,7продукту, які використовують на найближчій стадії. тетрагідро-1Н-бензімідазол-2-іл)]амінгідрохлорид LCMS, Rt (С): 1,05хв.; МС (ES+, M+H+): 327,4. a) 1,4-Діоксаспіро[4,5]дец-6-иламін d) N-(1,4-Діоксаспіро[4,51дец-6-ил)-N'-(4метилтіофен-3-іл)гуанідин Необхідний як попередник амін отримують ві 45 У реакційній посудині 58,8мг 1-(1,4діоксаспіро[4,5]дец-6-ил)-2-метил-3-(4метилтіофен-3-іл)ізотіосечовини змішують з 2мл 7Μ розчину аміаку в метанолі і нагрівають протягом 16 годин при температурі приблизно 100°С на піщаній бані. Після видалення розчинника отримують 51мг маслянистого продукту, які прямо вводять у взаємодію далі. LCMS, Rt (С): 1,00хв.; МС (ES+, M+H+): 296,4. е) N-(2-Хлор-4-метилтіофен-3-іл)-N'-(1,4діоксаспіро[4,5]дец-6-ил)гуанідин 49мг N-(1,4-діоксастро[4,5]дец-6-ил)-N'-(4метилтіофен-3-іл)гуанідину розчиняють в 3мл крижаної оцтової кислоти і повільно змішують з розчином з 20,3мг N-хлорсукциніміду в 5мл крижаної оцтової кислоти. Після перемішування протягом декількох годин і витримування до кінця тижня при кімнатній температурі крижану оцтову кислоту видаляють, залишок обробляють водою і за допомогою 2н розчину гідроксиду натрію встановлюють значення рН на рівні 10. Лужну фазу екстрагують три рази етилацетатом, об'єднані органічні фази сушать над сульфатом магнію, фільтрують і концентрують. Залишок очищають препаративною хроматографією, фракції, що містять продукт, об'єднують, ацетонітрил видаляють, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію і фільтрують. Після видалення розчинника отримують 24мг цільового продукту, які прямо використовують на найближчій стадії. LCMS, Rt(C): 1,09хв; MC(ES+, M+H+): 330,4. f) (2-Хлор-4-метилтіофен-3-іл)-(4,5,6,7тетрагідро-1Н-бензімідазол-2-іл)амінгідрохлорид 24мг N-(2-хлор-4-метилтіофен-3-іл)-N'-(1,4діоксаспіро[4,5]дец-6-ил)гуанідину розчиняють в 1мл 2н соляної кислоти і переміїиують протягом 30 хвилин при кімйатній температурі. Потім додають 1мл концентрованої соляної кислоти і перемішують наступні дві години. Після цього розбавляють невеликою кількістю води і піддають сушінню виморожуванням. Залишок змішують з толуолом, який відганяють у вакуумі. Після того, як цей процес повторюють двічі, залишаються 22мг цільового продукту у вигляді твердої речовини. + + LCMS, Rt (В): 0,95хв.; МС (ES , M+H ): 268,07. Приклад 49 2-Хлор-3N-(2-бензімідазоліламіно)-4метилтіофенбензолсульфонат 77551 46 250мг 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофену розчиняють в 5мл тетрагідрофурану і при перемішуванні змішують з розчином 150мг бензолсульфокислоти в 5мл тетрагідрофурану. Після відфільтровування під вакуумом осаду і висушування при температурі 75°С у високому вакуумі отримують цільовий продукт. Безбарвні кристали; т.пл.: 235°С. Приклад 50 2-Хлор-3N-(2-бензімідазоліламіно)-4метилтіофенметансульфонат Отримують аналогічно описаній в прикладі 49 методиці з 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофену з одним еквівалентом метансульфокислоти. Безбарвні кристали; т.пл.: 227°С. Приклад 51 2-Хлор-3N-(2-бензімідазоліламіно)-4метилтіоФенбензоат Отримують аналогічно описаній в прикладі 49 методиці з 2-хлор-3N-(2-бензімідазоліламіно)-4метилтіофену з одним еквівалентом бензойної кислоти. Для виділення реакційну суміш концентрують до половини і потім змішують з 30мл діетилового ефіру. Безбарвні кристали; т.пл.: 198°С. Приклад 52 2,4-Дихлор-3N-(2бензімідазоліламіно)тіофенгідрохлорид a) Метиловий ефір 3-ацетиламінотіофен-2карбонової кислоти До суміші з 942г метилового ефіру 3амінотіофен-2-карбонової кислоти і 1000мл толуолу додають по краплях, при одночасному нагріванні на масляній бані, 567мл ацетангідриду, потім 47 77551 48 протягом 1,5 годин кип'ятять із зворотним холодиефіром і об'єднані органічні фази після екстракції в льником і після цього охолоджують на бані з льоділильній лійці промивають один раз водою. Оргадом до температури приблизно 0°С. Кристали вінічну фазу сушать, розчинник відганяють і маслядфільтровують, промивають 2 рази невеликою нисто-аморфний залишок хроматографують на кількістю холодного ізопропанолу і 2 рази діізопроколонці з силікагелем за допомогою суміші з 1 часпіловим ефіром. З фільтрату шляхом подальшого тини етилацетату і 1 частини толуолу. концентрування і кристалізації можна отримати f) 4-Хлор-3-тієнілізотіоиіанат метиловий ефір 3-ацетиламінотіофен-2До розчину з 1,1г 3-аміно-4-хлортіофену в карбонової кислоти. Т.пл.: 93-95°С. 20мл безводного тетрагідрофурану додають 1,46г b) Метиловий ефір 3-ацетиламіно-4,5тіокарбонілдіімідазолу і перемішують протягом дихлортіофен-2-карбонової кислоти однієї години при кімнатній температурі. РозчинДо розчину 19,9г метилового ефіру 3ник відганяють при зниженому тиску, залишок розацетиламінотіофен-2-карбонової кислоти в 100мл чиняють в етилацетаті, органічну фазу обробляхлороформу при перемішуванні магнітною мішалють два рази водою в ділильній лійці, сушать і кою і температурі реакції 20-30°С додають по крарозчинник знов відганяють у вакуумі. Отримують плях 17,9г сульфурилхлориду SO2CI2. Потім пере4-хлор-3-тієнілізотіоціанат у вигляді темної олії, мішують наступні 2 людини при температурі 40°С і яку потім без подальших операцій очищення ввокип'ятять із зворотним холодильником протягом дять у взаємодію далі. подальших 15 хвилин. Після відгонки розчинника g) N-(2-Амінофеніл)-N'-(4-хлор-3при зниженому тиску залишок змішують з етилатієніл)тіосечовина цетатом і після витримування при стоянні кристаДо розчину з 1,4г 4-хлор-3-тієнілізотіоціанату в ли відфільтровують. Т.пл.: 136-138°С. 40мл безводного тетрагідрофурану додають 0,86г c) Метиловий ефір 3-ацетиламіно-41,2-діамінобензолу (о-фенілендіамін), перемішухлортіофен-2-карбонової кислоти ють протягом приблизно 20 годин при кімнатній Суміш з 25г метилового ефіру 3-ацетиламінотемпературі і розчинник відганяють при зниженому 4,5-дихлортіофен-2-карбонової кислоти, приблизтиску. Залишок обробляють водою, екстрагують но 10г триетиламіну, 300мл метанолу і 1г паладіяетилацетатом, розчинник знов відганяють і залина-вугіллі гідрують при кімнатній температурі і ношок очищають при застосуванні колонкової хромармальному тиску аж до припинення поглинання тографії середнього тиску на силікагелі за допомоводню. Після відфільтровування каталізатора фігою суміші етилацетату і толуолу в співвідношенні льтрат концентрують шляхом відгонки при зниже1:1. Тверда речовина коричнювато-жовтого коному тиску аж до кристалізації, що починається, льору. потім змішують з водою і тверду речовину відфільh) 4-Хлор-3N-(2-бензімідазоліламіно)тіофен тровують. Безбарвні кристали з ізопропанолу. До розчину 0,5г N-(2-амінофеніл)-N'-(4-хлор-3Т.пл.: 142-147°С. тієніл)тіосечовини в 25мл безводного тетрагідроd) Метиловий ефір 3-аміно-4-хлортіофен-2фурану додають розчин 0,169г гідроксиду натрію в карбонової кислоти 5мл води і потім розчин 0,363г хлорангідриду п7г метилового ефіру 3-ацетиламіно-4толуолсульфокислоти в 10мл тетрагідрофурану. хлортіофен-2-карбонової кислоти в суміші з 50мл Перемішують протягом 3 годин при кімнатній темметанолу і 50мл концентрованої соляної кислоти пературі, потім відганяють розчинник при знижеперемішують протягом 4 годин при температурі ному тиску, залишок обробляють водою і екстра60°С, протягом 5 годин при кип'ятінні із зворотним гують етилацетатом. Після відгонки розчинника холодильником і протягом наступних 3 днів при продукт очищають хроматографією середнього кімнатній температурі. Відфільтровують осад, що тиску на силікагелі за допомогою суміші з 20 часможливо утворюється, і видаляють приблизно 1/3 тин етилацетату, 10 частин н-гептану і 3 частин об'єму розчинника шляхом відгонки при зниженокрижаної оцтової кислоти як елююючого засобу. му тиску. Після додання приблизно 100мл води Невелику частину 4-хлор-3N-(2перемішують подальші 15 хвилин при кімнатній бензімідазоліламіно)тіофену, з метою охараіігеритемпературі, безбарвні кристали відфільтровують і зовування, в етилацетаті за допомогою розчину висушують їх в струмі повітря. Т.пл.: 62-64°С. хлороводню в діетиловому ефірі переводять в 4e) 3-Аміно-4-хлортіофен хлор-3N-(2-бензімідазоліламіно)тіофенгідрохлорид 18,02г метилового ефіру 3-аміно-4і охарактеризовують. Безбарвні кристали; т.пл.:хлортіофен-2-карбонової кислоти додають до роз256-260°С. чину з 11,1г КОН і 160мл води, потім протягом 3 і) 2,4-Дихлор-3N-(2годин кип'ятять із зворотним холодильником і пісбензімідазоліламіно)тіофенгідрохлорид ля охолоджування додають по краплях до нагрітоРозчин 0,3г 4-хлор-3N-(2го до температури 60°С розчину з 15мл концентбензімідазоліламіно)тіофену в 10мл крижаної оцрованої соляної кислоти в 30мл води. При цьому тової кислоти змішують з розчином 0,16г Nприходять до виразного виділення СО2. Після похлорсукциніміду в 5мл крижаної оцтової кислоти. дальшого перемішування при температурі 60°С Реакційну суміш перемішують протягом 15 хвилин протягом приблизно 40 хвилин залишають охолопри температурі 40°С і протягом приблизно 4 годжуватися, потім наливають 50-100мл метил-третдин при кімнатній температурі, потім крижану оцбутилового ефіру і підлуговують за допомогою тову кислоту відганяють при зниженому тиску і концентрованого розчину гідроксиду натрію і водну залишок обробляють водою. Після підлуговування фазу відділяють в ділильній лійці. Водну фазу ексза допомогою розчину гідроксиду натрію екстрагутрагують подальші 2 рази метил-трет-бутиловим ють етилацетатом, промивають водою, органічну 49 77551 50 фазу сушать і розчинник відганяють при зниженоb) (4-Хлортіофен-3-іл)-(5-фтор-1Нму тиску. Залишок очищають колонковою хроматобензімідазол-2-іл)амін графією в умовах середнього тиску за допомогою суміші з 20 частин етилацетату, 10 частин нгептану і 3 частин крижаної оцтової кислоти як елююючого засобу і потім осаджують з етилацетату шляхом додання розчину хлороводню в діетиловому ефірі. Безбарвний кристалічний продукт; т.пл.: 264-268°С. 625мг 1-(2-аміно-4-фторфеніл)-3-(4Приклад 53 хлортіофен-3-іл)тіосечовини розчиняють в тетрагі2-Бром-4-хлор-3N-(2дрофурані і змішують з розчином з 0,207г NaOH в бенеімідазоліламіно)тіофенгідрохлорид 9мл води. Протягом 5 хвилин додають по краплях розчин з 0,395г хлорангідриду п-толуїлової кислоти в 10мл тетрагідрофурану. По закінченні додатки перемішують протягом години при кімнатній температурі. Для обробки реакційну суміш змішують з водою і етилацетатом і фази розділяють в ділильній лійці. Водну фазу екстрагують три рази етилацетатом, об'єднані етилацетатні фази сушать над До розчину з 0,5г 4-хлор-3N-(2сульфатом магнію, освітлюють вугіллям, фільтрубензімідазоліламіно)тіофену в 15мл крижаної оцють і концентрують. Отримують 135мг цільового тової кислоти по краплях додають розчин з 0,356г продукту. N-бромсукциніміду в 6мл крижаної оцтової кислоти LCMS, Rt (F): 0,90хв.; МС (ES+, M+H+): 268,0. і перемішують наступні 15 хвилин при кімнатній с) (2,4-Дихлортіофен-3-іл)-(5-Фтор-1Нтемпературі. Розчинник відганяють, залишок оббензімідазол-2-іл)амінгідрохлорид робляють водою і підлуговують за допомогою розчину гідроксиду натрію. Після екстракції етилацетатом органічну фазу промивають водою, сушать і випаровують при зниженому тиску. Залишок хроматографують в умовах середнього тиску на силікагелі за допомогою суміші з 20 частин етилацетату, 10 частин н-гептану і 3 частин крижаної оцтової кислоти як елююючого засобу. Після відгонки роз85мг (4-хлортіофен-3-іл)-(5-фтор-1Нчинника залишок обробляють етилацетатом і 2бензімідазол-2-іл)аміну розчиняють в 4мл крижабром-4-хлор-3N-(2ної оцтової кислоти і при кімнатній температурі і бензімідазоліламіно)тіофенгідрохлорид осаджують інтенсивному перемішуванні повільно змішують з шляхом додання розчину газоподібного хлороводрозчином 42мг N-хлорсукциніміду в 4мл крижаної ню в діетиловому ефірі. Безбарвний кристалічний оцтової кислоти. По закінченні додатки перемішупродукт; т.пл.: 264-266°С. ють протягом 45 хвилин при кімнатній температурі, Приклад 54 потім 5 годин при температурі 50°С. Після додання (2,4-Дихлортіофен-3-іл)-(5-фтор-1Ннаступних 4мг N-хлорсукциніміду перемішують ще бензімідазол-2-іл)амінгідрохлорид протягом години при температурі 50°С. Потім реаa) 1-(2-Аміно-4-фторфеніл)-3-(4-хлортіофен-3кційну суміш змішують з 20мл толуолу і крижану іл)тіосечовина оцтову кислоту відганяють. Залишок розчиняють в етилацетаті і елююють за допомогою насиченого розчину карбонату калію. Етилацетатну фазу сушать над сульфатом магнію, фільтрують і концентрують. Залишок очищають препаративною ВЕРХ, фракції, що містять продукт, об'єднують, ацетонітрил видаляють, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, 900мг 4-фтор-1,2-фенілендіаміну розчиняють сушать над сульфатом магнію і фільтрують. Після в 25мл тетрагідрофурану і при перемішуванні довидалення розчинника залишок змішують з водою дають по краплях розчин 4-хлор-3і 2н соляною кислотою і піддають сушінню вимотієнілізотіоціанату (приклад 52с) в 15мл тетрагідрожуванням. Отримують 17мг цільового продукту. рофурану. Розчин перемішують протягом приблиLCMS, Rt (Ε): 2,65хв.; МС (ES+, М+Н+): 301,93. зно 3 годин при кімнатній температурі і залишають Приклад 55 стояти протягом ночі. Потім реакційну суміш кон(2-Бром-4-хлортіофен-3-іл)-(5-фтор-1Нцентрують і залишок очищають препаративною бензімідазол-2-іл)амінгідрохлорид ВЕРХ. Фракції, що містять продукт, об'єднують, ацетонітрил видаляють, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію і фільтрують. Після видалення розчинника отримують 625мг цільового продукту. LCMS, Rt (F): 1,28хв.; МС (ES+, M+H+): 302,0. 51 50мг (4-Хлортіофен-3-іл)-(5-фтор-1Нбензімідазол-2-іл)аміну (приклад 54b) розчиняють в 4мл крижаної оцтової кислоти і при кімнатній температурі і інтенсивному перемішуванні повільно змішують з розчином 33мг N-бромсукциніміду в 4мл крижаної оцтової кислоти. По закінченні додатки перемішують протягом 45 хвилин при кімнатній температурі і потім реакційну суміш змішують з 20мл толуолу і крижану оцтову кислоту відганяють. Залишок розчиняють в етилацетаті і промивають насиченим розчином карбонату калію. Етил ацетатну фазу сушать над сульфатом магнію, фільтрують і концентрують. Залишок очищають препаративною хроматографією, фракції, що містять продукт, об'єднують, ацетонітрил видаляють, підлуговують і екстрагують три рази етилацетатом. Органічні фази об'єднують, сушать над сульфатом магнію і фільтрують. Після видалення розчинника залишок змішують з водою і 2н соляною кислотою і піддають сушінню виморожуванням. Отримують 27мг цільового продукту. LCMS, Rt (Ε): 2,29хв.; МС (ES+, M+H+): 347,87. Приклад 56 (2,4-Дихлортіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл)амінгідрохлорид a) 1-(2-Аміно-4,5-дифторфеніл)-3-(4хлортіофен-3-іл)тіосечовина 1,02г 1,2-діаміно-4,5-дифторбензолу вносять в 15мл абсолютного тетрагідрофурану і додають по краплях розчин 1,25г 4-хлор-3-тієнілізотіоціанату (приклад 52с) в 15мл абсолютного тетрагідрофурану. Подальше здійснення методики аналогічно прикладу 54а) приводить до отримання 773мг цільової сполуки. LCMS, Rt (F): 1,32хв.; МС (ES+, M+H+): 320,0. b) (4-Хлортіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл)амін 773мг 1-(2-аміно-4,5-дифторфеніл)-3-(4хлортіофен-3-іл)тіосечовини вносять в 20мл тетрагідрофурану і змішують з розчином 240мг NaOH в 9мл води і після цього додають розчин 528мг тозилхлориду в 10мл тетрагідрофурану. Подальше здійснення методики аналогічно прикладу 54b) приводить до отримання 275мг цільової сполуки. + + LCMS, Rt (F): 0,95хв.; МС (ES , M+H ): 286. c) (2,4-Дихлортіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл)амінгідрохлорид 77551 52 125мг (4-хлортіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл)аміну вносять в 8мл оцтової кислоти і додають по краплях розчин 59мг хлорсукциніміду в 2мл оцтової кислоти. Подальше здійснення методики аналогічно прикладу 54с) приводить до отримання 58мг цільового продукту. LCMS, Rt (Ε): 2,97хв.; МС (ES+, M+H+): 319,88. Приклад 57 (2-Бром-4-хлортіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл) амінгідрохлорид 125мг (4-хлортіофен-3-іл)-(5,6-дифтор-1Нбензімідазол-2-іл)аміну (приклад 55b) розчиняють в 8мл крижаної оцтової кислоти і при кімнатній температурі і інтенсивному перемішуванні повільно змішують з розчином 78мг N-бромсукциніміду в 2мл крижаної оцтової кислоти. Подальше здійснення методики аналогічно прикладу 55) приводить до отримання 77мг цільового продукту. LCMS, Rt (Ε): 2,39хв.; МС (ES+, M+H+): 365,86. Приклад 58 4-Хлор-3N-(4-метил-2бензімідазоліламіно)тіофенгідрохлорид а) N-(2-Аміно-3-метилфеніл)-N'-(4-хлор-3тієніл)тіосечовина Отримують аналогічно вказаній в прикладі 52g) методиці з 4-хлор-3-тієнілізотіоціанату і 1,2діаміно-3-метилбензолу і при застосуванні колонкової хроматографії середнього тиску на силікагелі за допомогою суміші з 20 частин етилацетату, 10 частин н-гептану і 1 частини етилацетату. Тверда речовина коричнювато-жовтого кольору; т.пл.: 193-196°С. b) 4-Хлор-3N-(4-метил-2бензімідазоліламіно)тіофен Отримують аналогічно вказаній в прикладі 52h) методиці з N-(2-аміно-3-метилфенілфеніл)-N'(4-хлор-3-тієніл)тіосечовини і при застосуванні колонкової хроматографії середнього тиску на силікагелі за допомогою суміші з 10 частин дихлорметану і 1 частини метанолу у вигляді аморфного пінистого продукту. Отримання 4-хлор-3N-(4метил-2-бензімідазоліламіно)тіофенгідрохлориду здійснюють в етилацетаті за допомогою насиченого газоподібним хлороводнем діетилового ефіру. Кристалічний продукт; т.пл.: 325-327°С. Приклад 59 53 2,4-Дихлор-3N-(4-метил-2бензімідазоліламіно)тioфенгідрохлорид 77551 54 реакції з 4-хлор-3-тієнілізотіоціанату і транс(1R,2R)-(-)-1,2-діаміноциклогексану шляхом подальшого виділення колонковою хроматографією на силікагелі за допомогою суміші з 10 частин етилацетату, 5 частин н-гептану, 5 частин дихлорметану, 5 частин метанолу і 1 частини 35-37%-го водного розчину аміаку у вигляді аморфного продукту темного кольору, який без подальшого очищення використовують далі. b) транс-(3аR,7аR)-4-Хлор-3N-(3а,4,5,6,7,7аОтримують аналогічно вказаній в прикладі гексагідро-1Н-2-бенеімідазоліл)-3-тієніламін 521) методиці з 4-хлор-3N-(4-метил-2Отримують аналогічно вказаній в прикладі бензімідазоліламіно)тіофену і N-хлорсукциніміду в 52h) методиці з транс-R,R-3N-(2крижаній оцтовій кислоті при аналогічній обробці. аміноциклогексил)-N'-(4-хлор-3-тієніл)тіосечовини, Кристалічний продукт; т.пл.: 296-298°С. хлорангідриду п-толуолсульфокислоти і шляхом Приклад 60 подальшого застосування колонкової хроматограTpaнс-(3aS, 7аS)-4-Хлор-3N-(3а,4,5,6,7,7афії середнього тиску на силікагелі за допомогою гексагідро-1Н-2-бензімідазоліл)-3суміші з 10 частин етилацетату, 5 частин нтієніламінгідрохлорид гептану, 5 частин дихлорметану, 5 частин метанолу і 1 частини 35-37%-го водного розчину аміаку у вигляді аморфного маслянистого продукту. Отримання транс-R,R-4-хлор-3N-(3а,4,5,6,7,7агексагідро-1Н-2-бензімідазоліл)-3тієніламінгідрохлориду здійснюють в етилацетаті і невеликій кількості етанолу за допомогою насичеа)транс-S,S-3N-(2-Аміноциклогексил)-N7-(4ного газоподібним хлороводнем діетилового ефіхлор-3-тієніл)тіосечовина ру. Кристалічний продукт; т.пл.: 240-244°С. Отримують аналогічно вказаній в прикладі 1b) Приклад 62 реакції з 4-хлор-3-тієнілізотіоціанату і транс-S,Sцис-4-Хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-21,2-діаміноциклогексану шляхом виділення колонбензімідазоліл)-3-тієніламінгідрохлорид ковою хроматографією на силікагелі за допомогою суміші з 10 частин етилацетату, 5 частин дихлорметану, 5 частин н-гептану, 5 частин метанолу і 1 частини 35-37%-го водного розчину аміаку у вигляді аморфного продукту темного кольору, який без подальшого очищення використовують далі. b) транс-(3аS,7аS)-4-Хлор-3N-(3а,4,5,6,7,7аa) цис-3N-(2-Аміноциклогексил)-N'-(4-хлор-3гексагідро-1Н-2-бензімідазоліл)-3-тієніламін тієніл)тіосечовина Отримують аналогічно вказаній в прикладі Отримують аналогічно вказаній в прикладі 1b) 52h) методиці з транс-S,S-3N-(2реакції з 4-хлор-3-тієнілізотіоціанату і цис-1,2аміноциклогексил)-N'-(4-хлор-3-тієніл)тіосечовини, діаміноциклогексану шляхом подальшого виділенхлорангідриду п-толуолсульфокислоти і шляхом ня колонковою хроматографією на силікагелі за подальшого застосування колонкової хроматоградопомогою суміші з 10 частин етилацетату, 5 часфії середнього тиску на силікагелі за допомогою тин н-гептану, 5 частин дихлорметану, 5 частин суміші з 10 частин дихлорметану і 1 частини метаметанолу і 1 частини 35-37%-го водного розчину нолу у вигляді аморфного пінистого продукту. аміаку у вигляді аморфного продукту темного коОтримання транс-S,S-4-хлор-3N-(3а,4,5,6,7,7альору, який без подальшого очищення використогексагідро-1Н-2-бензімідазоліл)-3вують далі. тієніламінгідрохлориду здійснюють в етилацетаті і b) цис-4-Хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Нневеликій кількості етанолу за допомогою насиче2-бензімідазоліл)-3-тієніламін ного газоподібним хлороводнем діетилового ефіОтримують аналогічно вказаній в прикладі ру. Кристалічний продукт; т.пл.: 196-200°С. 52h) методиці з цис-3N-(2-аміноциклогексил)-N'-(4Приклад 61 хлор-3-тієніл)тіосечовини, хлорангідриду птранс-(3аR,7аR)-4-Хлор-3N-(3а,4,5,6,7,7атолуолсульфокислоти і шляхом подальшого загексагідро-1Н-2-бензімідазоліл)-3стосування колонкової хроматографії середнього тієніламінгідрохлорид тиску на силікагелі за допомогою суміші з 10 частин етилацетату, 5 частин н-гептану, 5 частин дихлорметану, 5 частин метанолу і 1 частини 35-37%го водного розчину аміаку у вигляді маслянистого продукту коричневого кольору. Отримання 4-хлор3N-(цис-3а,4,5,6,7,7а-гексагідро-1Н-2бензімідазоліл)-3-тієніламінгідрохлориду здійснюа)транс-(1R,2R)-3N-(2-Аміноциклогексил)-N'-(4ють в етилацетаті і невеликій кількості етанолу за хлор-3-тієніл)тіосечовина допомогою насиченого газоподібним хлороводнем Отримують аналогічно вказаній в прикладі 1b) діетилового ефіру. Кристалічний продукт; т.пл.: 55 228-231°С. Приклад 63 транс-R,R-2,4-Дихлор-3N-(3а,4,5,6,7,7агексагідро-1Н-2-бензімідазоліл)-3тієніламінгідрохлорид Отримують аналогічно вказаній в прикладі 52і) методиці шляхом введення у взаємодію трансR,R-4-хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2бензімідазоліл)-3-тієніламіну з N-хлорсукцинімідом і аналогічної обробки. Кристалічний продукт. Спінення з сублімацією, починаючи з температури 165°С. Приклад 64 цис-2,4-Дихлор-3N-(3а,4,5,6,7,7а-гексагідро1Н-2-бензімідазоліл)-3-тієніламінгідрохлоридОтримують аналогічно вказаній в прикладі 52і) методиці шляхом введення у взаємодію цис-4хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2бензімідазоліл)-3-тієніламіну з N-хлорсукцинімідом і шляхом аналогічної обробки. Кристалічний продукт; т.пл.: 270-274°С. Приклад 65 4-Хлор-3N-(4-хлор-2бензімідазоліламіно)тіофенгідрохлорид а) 1-N-(2-Аміно-3-хлорфеніл)-3-Ν-(4-хлор-3тієніл)тіосечовина Отримують з 3-хлор-1,2-діамінобензолу і 4хлор-3-тієнілізотіоціанату аналогічно описаній в прикладі 1b) методиці і шляхом кристалізації з діізопропілового ефіру у вигляді твердої речовини з двома температурами плавлення: т.пл. 1: 152155°С при перекристалізації; т.пл. 2: >310°С. b) 4-Хлор-3N-(4-хлор-2бензімідазоліламіно)тіофен Отримують аналогічно описаній в прикладі 52h) методиці шляхом взаємодії 1-N-(2-аміно-3хлорфеніл)-3-N-(4-хлор-3-тієніл)тіосечовини з хлорангідридом п-толуолсульфокислоти і колонкової хроматографії на силікагелі за допомогою суміші з 3 частин толуолу і 1 частини етилацетату як елююючого засобу і подальшої відгонки розчинника при зниженому тиску у вигляді пінистого аморфного продукту, який потім перетворюють в гідрохлорид. c) 4-Хлор-3N-(4-хлор-2 77551 56 бензімідазоліламіно)тіофенгідрохлорид Отримують шляхом обробки розчину 4-хлор3N-(4-хлор-2-бензімідазоліламіно)тіофену в етилацетаті за допомогою насиченого розчину газоподібного хлороводню в діетиловому ефірі у вигляді кристалічного осаду. Т.пл.: 276-280°С. Приклад 66 2,4-Дихлор-3N-(4-хлор-2бензімідазоліламіно)тіофенгідрохлорид Отримують аналогічно вказаній в прикладі 52I) методиці з 4-хлор-3N-(4-метил-2бензімідазоліламіно)тіофену і N-хлорсукциніміду в крижаній оцтовій кислоті при аналогічній обробці. Кристалічний продукт; т.пл.: 294-297°С. Аналогічно вказаним в прикладах здійснення сполукам можна отримувати наступні похідні тіофену: 2-бром-4-хлор-3N-(4-метил-2бензімідазоліламіно)тіофенгідрохлорид; т.пл.: 284286°С; 2-бром-4-хлор-3N-(4-хлор-2бензімідазоліламіно)тіофенгідрохлорид; т.пл.: 304306°С; транс-R,R-2-бром-4-хлор-3N-(3а,4,5,6,7,7агексагідро-1Н-2-бензімідазоліл)-3тієніламінгідрохлорид; температура розкладання: 215°С; транс-(3аS,7аS)-2-бром-4-хлор-3N(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-3тієніламінгідрохлорид; т.пл.: 243-254°С; 2,4-дибром-3N-(2-бензімідазоліл)-3тієніламінгідрохлорид; 2,4-диметил-3N-(2-бензімідазоліл)-3тієніламінгідрохлорид; 2,4-диметил-3N-(4-метил-2-бензімідазоліл)-3тієніламінгідрохлорид; 2,4-диметил-3N-(5-фтор-2-бензімідазоліл)-3тієніламшгідрохлорид; 2-хлор-3N-(4-бутокси-2-бензімідазоліл)-4метил-3-тієніламінгідрохлорид; 2-хлор-3N-(4-трифторметил-2-бензімідазоліл)4-метил-3-тієніламінгідрохлорид; 2-хлор-3N-(4-метилсульфонил-2бензімідазоліл)-4-метил-3-тієніламін-гідрохлорид. Фармакологічні дані Опис тесту У цьому тесті визначали відновлення внутрішньоклітинного значення рН (рНi) після підкислення, яке застосовують у випадку нормально функціонуючого NHE також в умовах відсутності бікарбонатів. Для цього значення рНi визначали за допомогою чутливого до рН флуоресцентного барвника BCECF (2',7'-біс(2-карбоксіетил)-5,6карбоксифлуоресцеїн; Calbiochem; використовують у вигляді попередника BCECF-AM). Клітини спочатку навантажували з допомогою BCECF. Флуоресценцію BCECF визначали в "Ratio Fluorescence Spectrometer" (спектрометр для визначення міри флуоресценції) [Photon Technology 57 77551 58 International, South Brunswick, N.J., США] при довповного відновлення значення рН (100%) клітини жинах хвиль збудження 505нм і 440нм і довжині інкубували в буфері, що містить Na+ (133,8мМ хвилі емісії 535нм і перераховували на pHj за доNaCl, 4,7мМ КСI, 1,25мМ СаСI2, 1,25мМ MgCl2, помогою калібрувальних кривих. Клітини вже при 0,97мМ Na2HPO4, 0,23мМ NaH2PO4, 5мМ Hepes, навантаженні за допомогою BCECF інкубували в 5мМ глюкози; за допомогою 1Μ розчину NaOH NН4СI-буфері (рН 7,4) (NН4СI-буфер: 115мМ NaCl, встановлюють значення рН на рівні 7,0). Для ви20мМ NH4CI, 5мМ КСI, 1мМ СаСI2, 1мМ MgSO4, значення значення 0% клітини інкубували в буфе20мМ Hepes, 5мМ глюкози, 1мг/мл бичачого сирорі, що не містить Na+ (133,8мМ холінхлориду, ваткового альбуміну; за допомогою 1Μ розчину 4,7мМ КСI, 1,25мМ СаСI2, 1,25мМ MgCl2, 0,97мМ NaOH встановлюють значення рН на рівні 7,4). К2НРО4, 0,23мМ КН2РО4, 5мМ Hepes, 5мМ глюкоВнутрішньоклітинне підкислення індукували шлязи; за допомогою 1Μ розчину КОН встановлюють хом додання 975мкл буферу, що не містить NH4CI, значення рН на рівні 7,0). Речовини, що тестують(див. нижче) до аліквот 25мкл інкубованих в ся, вводили в буфер, що містить Na+. Відновлення NH4СI-буфері клітин. Подальшу швидкість відноввнутрішньоклітинного значення рН у випадку кожлення значення рН реєстрували у випадку NHE1 ної концентрації речовини, що тестується, вирапротягом двох хвилин, у випадку NHE2 протягом 5 жали в процентах від максимального відновлення. хвилин і у випадку NHE3 протягом трьох хвилин. З виражених в процентах значень відновлення Для розрахунку інгібуючої здатності речовин, що значення рН за допомогою програми Sigma-Plot тестуються, спочатку досліджували клітини в бурозраховували значення ІС50 відповідної речовини ферах, в яких відбувалося повне, або не відбувадля окремих підтипів NHE. лося взагалі ніякого відновлення значення рН. Для Результати Приклад 16 транс-R,R-2-хлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид 12 2-хлор-3N-(3-бензімідазоліл)-4-метил-3-тієніламінгідрохлорид 54 2-бром-4-хлор-3N-(2-бензімідазоліламіно) тіофенгідрохлорид 53 2,4-дихлор-3N-(2-бензімідазоліламіно) тіофенгідрохлорид 56 2,4-дихлор-3N-(4-метил-2-бензімідазоліламіно)тіофенгідрохлорид 60 транс-R,R-2,4-дихлор-3N-(3а,4,5,6,7,7а-гексагідро-1Н-2-бензімідазоліл)-3тієніламінгідрохлорид 63 2,4-дихлор-3N-(4-хлор-2-бензімідазоліламіно)тіофенгідрохлорид 38 2-хлор-3N-(4-гідрокси-2-бензімідазоліламіно)-4-метилтіофенгідрохлорид 18 2-бром-3N-(2-бензімідазоліл)-4-метил-3-тієніламінгідрохлорид 19 Tpaнс-R,R-2-бром-3N-(3a,4,5,6,7,7a-гексагідро-1H-2-бензімідазоліл)-4-метил-3тієніламінгідрохлорид 2 2-хлор-3N-(5-фтор-2-бензімідазоліл)-4-метил-3-тієніламінгідрохлорид 44 (1Н-бензімідазол-2-іл)-(2-хлор-4-метилтіофен-3-іл)метиламін Комп’ютерна верстка О. Гапоненко Підписне ІС50 [мкмоль] 0,27 (rNHE3) 0,12 (rNHE3) 0,22 (hNHE3) 0,14(hNHE3) 0,22 (hNHE3) 0,19 (hNHE3) 0,54 (hNHE3) 0,84 (hNHE3) 0,12 (hNHE3) 0,56 (hNHE3) 0,62 (hNHE3) 1,59 (hNHE3) Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted thiophene derivatives, method of production, their use as drugs or diagnostic reagents, pharmaceutical compositions
Автори англійськоюLang Hans-Jochen, Heinelt Uwe, Hofmeister Armin, Wirt Klaus, Bleich Markus
Назва патенту російськоюЗамещенные тиофены, способ их получения, их применение в качестве лекарств или диагностических реагентов и лекарственные средства, содержащие указанные соединения
Автори російськоюЛанг Ханс-Йохен, Хайнельт Уве, Хофмайстер Армин, Вирт Клаус, Бляйх Маркус
МПК / Мітки
МПК: A61K 31/454, A61P 9/04, A61P 9/10, A61P 33/06, A61P 13/12, A61K 31/4184, A61P 25/08, A61P 43/00, A61P 35/00, A61P 13/08, A61P 9/12, A61P 29/00, A61P 1/04, C07D 409/12, A61P 11/00, A61P 25/24, A61P 33/00, A61P 39/02, A61P 3/10, A61P 3/06, A61P 9/06, A61P 25/00, A61P 25/22
Мітки: реагентів, діагностичних, заміщені, вміщують, спосіб, тіофени, ліків, одержання, застосування, ліки
Код посилання
<a href="https://ua.patents.su/29-77551-zamishheni-tiofeni-sposib-kh-oderzhannya-kh-zastosuvannya-yak-likiv-abo-diagnostichnikh-reagentiv-ta-liki-shho-kh-vmishhuyut.html" target="_blank" rel="follow" title="База патентів України">Заміщені тіофени, спосіб їх одержання, їх застосування як ліків або діагностичних реагентів та ліки, що їх вміщують</a>
Попередній патент: Лайнер
Наступний патент: Шихта для виготовлення високовогнетривкого бетону
Випадковий патент: Живильник порошкоподібних та сипучих матеріалів












