Вагінальна таблетка, яка містить рифаксимін, спосіб її виготовлення та застосування для лікування вагінальних інфекцій
Номер патенту: 111972
Опубліковано: 11.07.2016
Автори: Кручані Федеріка, Маффеі Паола, Лауро Вітторіа, Віталі Беатріче, Каланні Фіорелла, Віскомі Джузеппе Клаудіо
Формула / Реферат
1. Вагінальна таблетка, яка містить:
(a) гранули рифаксиміну, які містять:
рифаксимін у кількості 2,5-200 мг, один або більше внутрішньогранулярних наповнювачів, які охоплюють принаймні один зв'язувач; та
(b) два або більше зовнішньогранулярних наповнювачів, які охоплюють принаймні два дезінтегранти, що являють собою суміш кросповідону та кальцію силікату.
2. Вагінальна таблетка за п. 1, яка покрита плівкою.
3. Вагінальна таблетка за п. 1, де рифаксимін міститься в кількості від 2,5 до 100 мг.
4. Вагінальна таблетка за п. 1, де дезінтегрант вибрано в групи, яка складається з наступного: натрію крохмаль гліколят, пептизований крохмаль, співполімер полівінілпіролідону (PPPV або кросповідон), натрійкарбоксиметилметилцелюлоза (натрійкармелоза), поперечно зв'язана карбоксиметилцелюлоза (натрійкроскармелоза), силікати лужних та лужноземельних металів (наприклад кальцію силікат) та їх суміш.
5. Вагінальна таблетка за п. 1, де внутрішньогранулярні наповнювачі додатково охоплюють принаймні один розріджувач та змащувач; зовнішньогранулярні наповнювачі додатково охоплюють принаймні один зв'язувач, розріджувач та змащувач, та необов'язково консерванти, біоадгезивні, буферувальні, антисептичні засоби та природний ароматизатор.
6. Вагінальна таблетка за п. 1, де розріджувач, вибраний з групи, що складається з наступного: целюлоза, мікрокристалічна целюлоза, гідроксипропілметилцелюлоза, кальцію фосфат, крохмаль, каолін, двогідратний кальцію сульфат, кальцію карбонат, безводна або гідратована лактоза, сахароза, манітол, полісахариди, глюкани, ксилоглюкан та їх суміш;
зв'язувач вибрано із групи, яка містить наступне: кукурудзяний крохмаль, пептизований крохмаль, гуміарабік, лактоза, мальтодекстрин, співполімер 1 вініл-2-піролідон та вінілацетат (коповідон), сахароза та їх суміші;
змащувач вибрано із групи, що складається з наступного: гліцерин дибегенат, кальцію або магнію стеарати, алюміній, натрію стеарилфумарат, гідрогенізовані олії, рослинні олії, пальмітинова кислота, спирт, крохмаль, мінеральні масла, поліетиленгліколь, натрію лаурилсульфат, тальк, гліцериди, натрію бензоат та їх суміш.
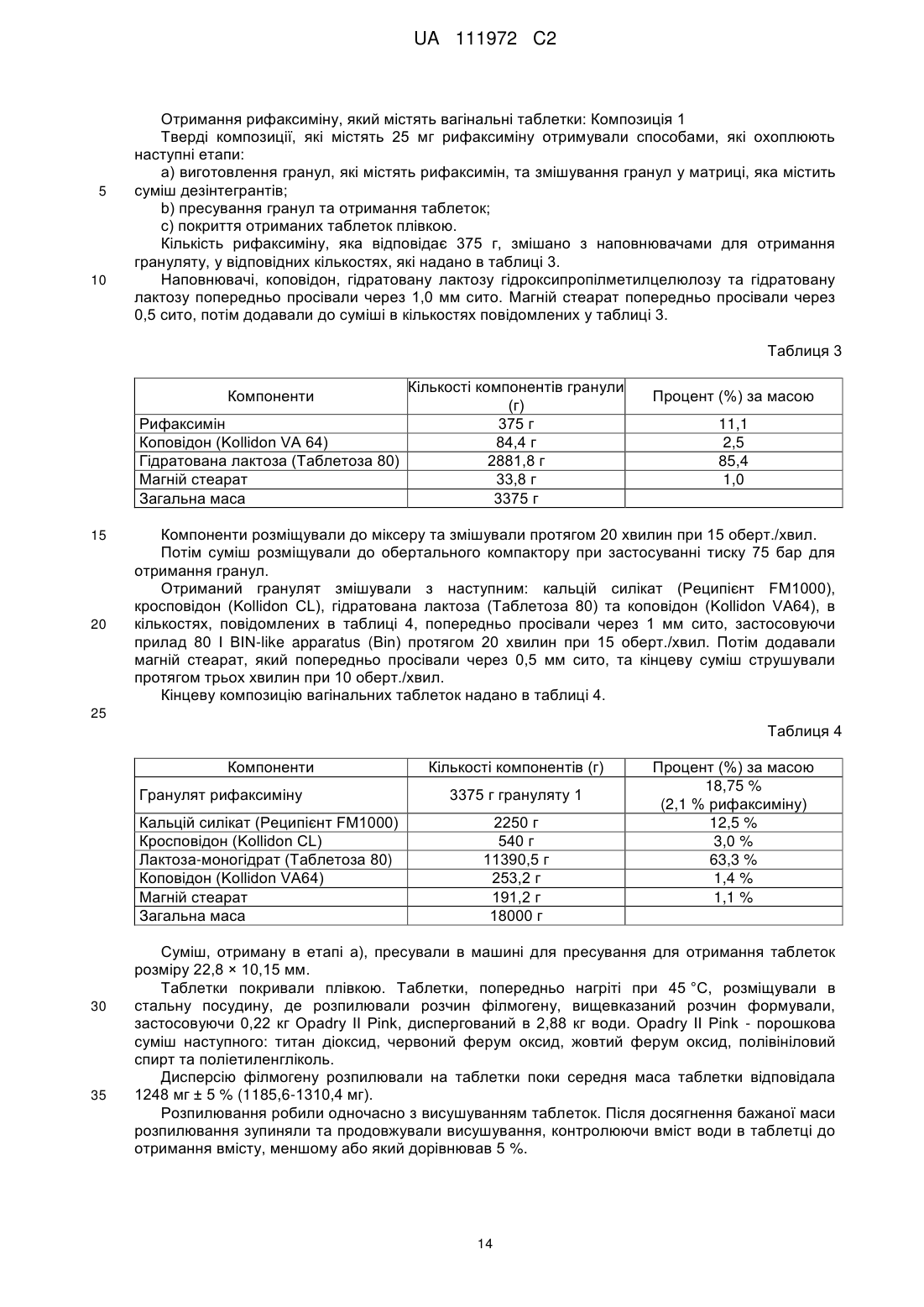
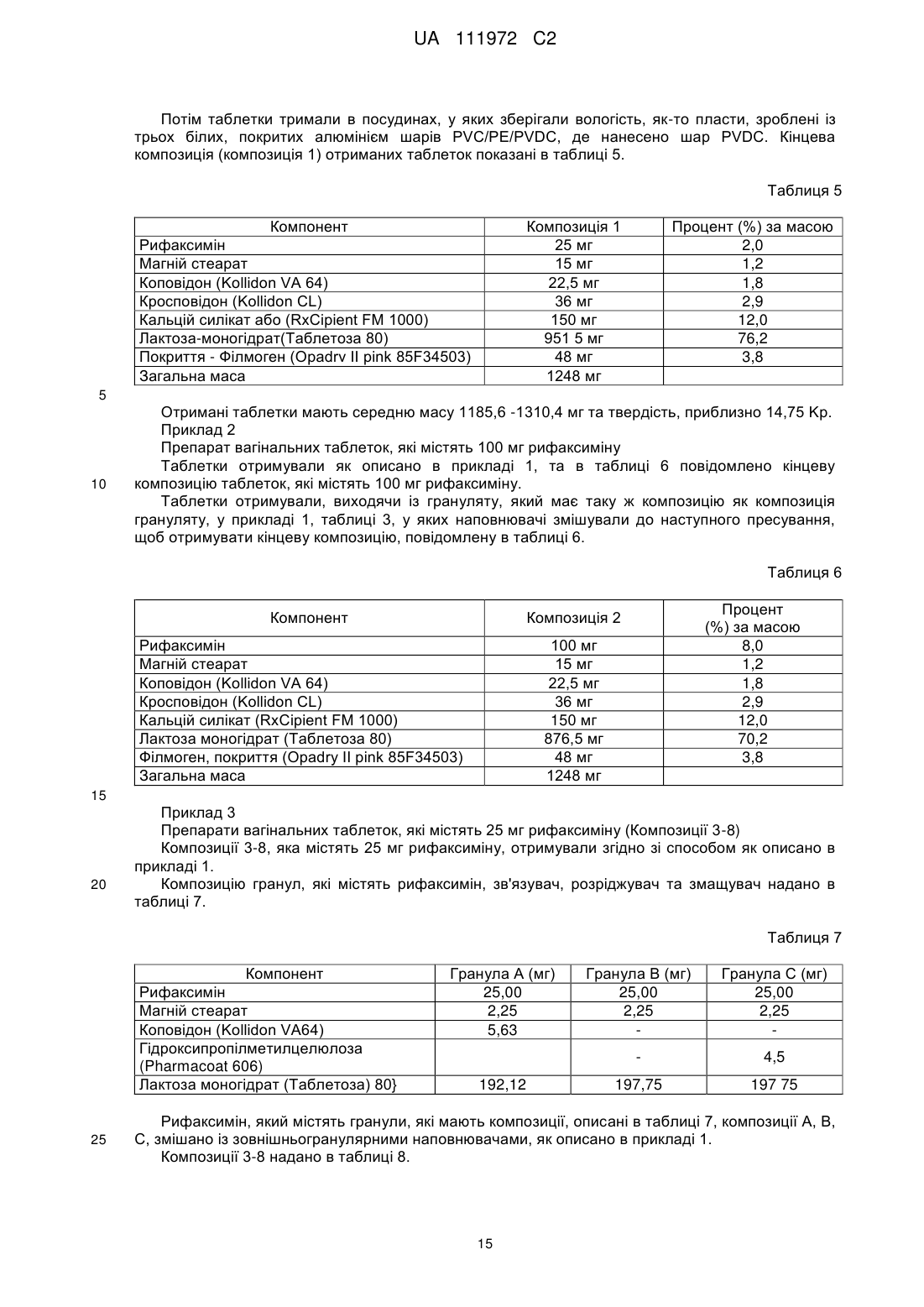
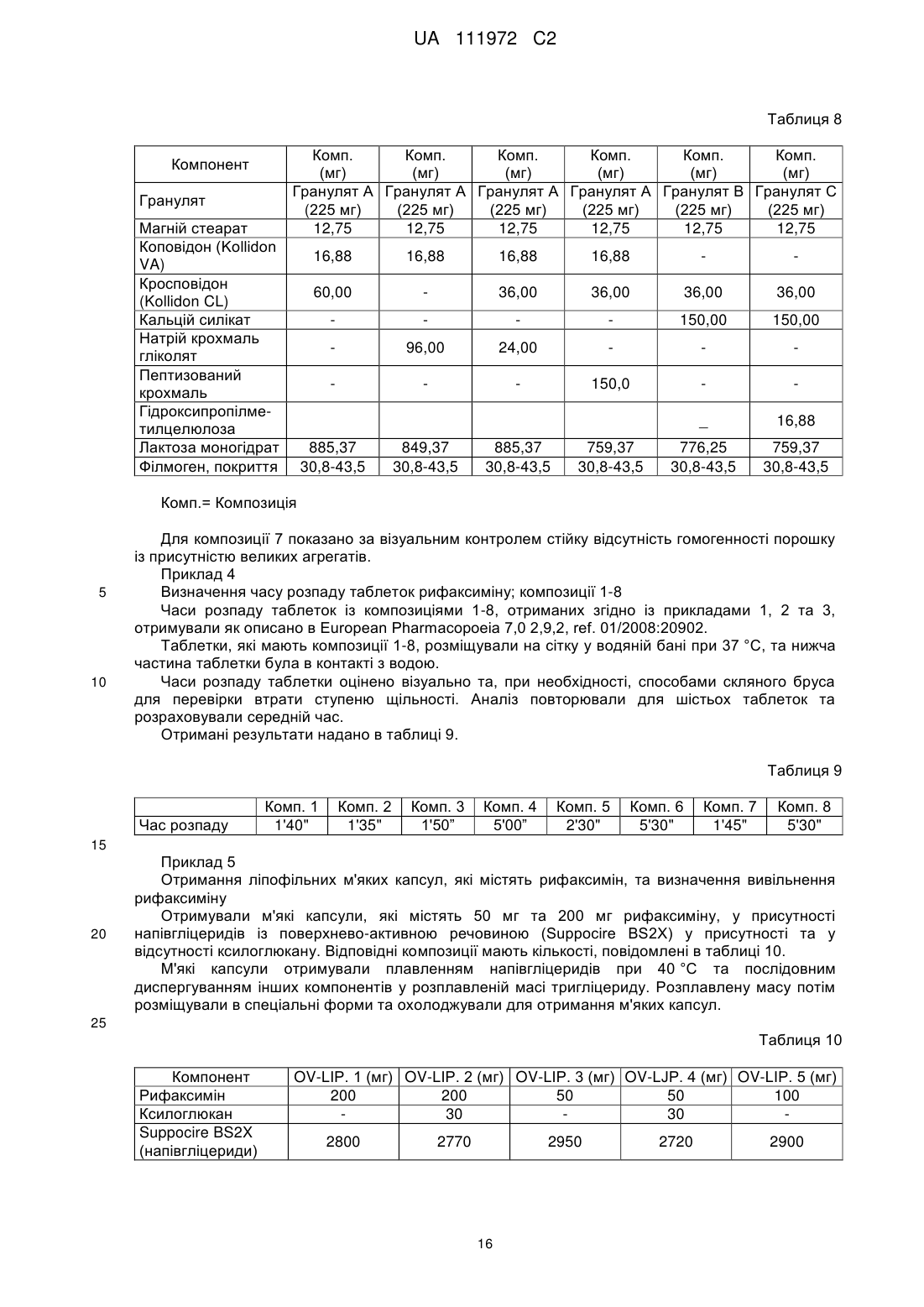
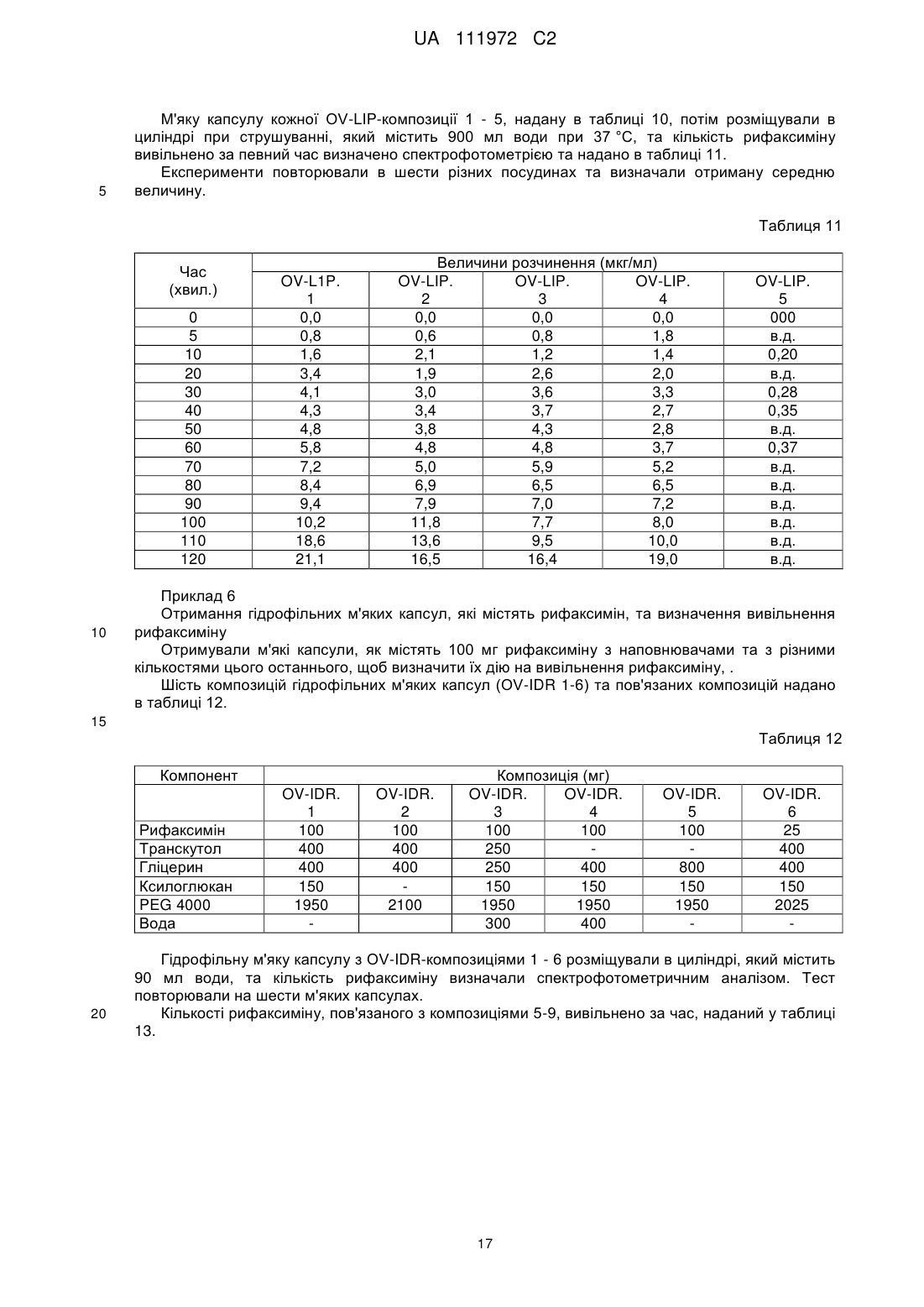
7. Вагінальна таблетка за п. 2, яка містить, мг:
рифаксимін
25
магнію стеарат
15
коповідон
22,5
кросповідон
36
кальцію силікат
150
лактоза
951,5
плівкоутворююче покриття
48.
8. Вагінальна таблетка за п. 2, яка містить, мг:
рифаксимін
100
магнію стеарат
15
коповідон
22,5
кросповідон
36
кальцію силікат
150
лактоза
876,5
плівкоутворююче покриття
48.
9. Вагінальна таблетка за п. 1, яка містить рифаксимін у поліморфній або аморфній формі.
10. Спосіб виготовлення вагінальної таблетки, яка містить рифаксимін у кількості 2,5-200 мг та один або більше внутрішньогранулярних наповнювачів, охоплюючи принаймні один зв'язувач, та два або більше зовнішньогранулярних наповнювачів, охоплюючи принаймні два дезінтегранти, які являють собою суміш кросповідону та кальцію силікату, де вищевказаний спосіб складається з наступних етапів:
формування гранул рифаксиміну сухим гранулюванням суміші рифаксиміну та одного або більше внутрішньогранулярних наповнювачів;
формування таблетки спочатку змішуванням та потім пресуванням гранул рифаксиміну з двома або більше зовнішньогранулярних наповнювачів, охоплюючи два або більше дезінтегранти.
11. Вагінальна таблетка за п. 1 для лікування або попередження бактеріальної вагінальної інфекції.
12. Вагінальна таблетка за п. 11, де вагінальну бактерію вибрано із групи, яка складається з наступного: Gardnerella vaginalis, Mycoplasma hominis, Bacteroides Atopobium vaginale, Peptostreptococcus, Mobiluncus, Prevotella, Veillonella та їх суміші.
13. Вагінальна таблетка за п. 11, придатна для зниження балів по шкалі Nugent та критеріїв Amsel у пацієнтів, уражених бактеріальним вагінозом.
14. Спосіб лікування бактеріального вагінозу, який охоплює етап введення вагінальної таблетки за будь-яким з пп. 1-9 суб'єкту при дозуванні рифаксиміну менше 200 мг/добу при курсі лікування менше тижня.
15. Спосіб за п.14, де загальна кількість рифаксиміну на курс лікування - менше 700 мг.
16. Спосіб за п. 14, де вагінальна таблетка містить кількість рифаксиміну від 12,5 до 100 мг та прийнятні наповнювачі, для лікування вагінальних інфекцій протягом часу лікування менше одного тижня.
Текст
Реферат: Винахід стосується вагінальної таблетки, яка містить гранули рифаксиміну та охарактеризована вивільненням рифаксиміну в піхві контрольованим шляхом, ефективна при лікуванні вагінальних інфекцій, зокрема бактеріального вагініту; та способу виготовлення вагінальної таблетки рифаксиміну та її застосування для лікування вагінальних інфекцій. UA 111972 C2 (12) UA 111972 C2 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 Заявлений винахід стосується композицій, які містіть гранули рифаксиміну разом із фармацевтично прийнятними наповнювачами, що призводить до контрольованого вивільнення композицій. У заявленому винаході також описано способи їх виготовлення та їх застосування для лікування вагінальних інфекцій, зокрема, бактеріального вагініту. Крім того, також у винаході описано дозування рифаксиміну, придатні та ефективні при видужанні від хвороби та попередженні будь-якого можливого рецидиву. Рифаксимін (INN, дивись The Merck Index, XIII ed., 8304, CAS No, 80621-81-4), номенклатура lUPAC 2S, 16Z, 18E, 20S, 21 S, 22R, 23R, 24R, 25S, 26S, 27S, 28E)-5,6,21, 23,25 пентагідрокси27-метокси-2,4,11,16,20, 22,24,26-октаметил-2,7-(епоксипентадека (1,11,13) триєнімін) бензофуро (4,5-e) піридо(1,2,-a бензімідазол-1,15(2H)діон, 25-ацетат) є напівсинтетичний антибіотичний медикамент, який належить до групи рифаміцину, точніше піридо-імідазорифаміцину, описаному в IT 1154655, оскільки EP 0 161 534 описує спосіб продукування, виходячи з Рифаміцину O (The Merck Index XIII ed., 8301). US 7,045,620, EP 1557421 B1, EP 1676847B1, EP 1676848B1, WO2005/044823, WO2006/094662 описують кристалічні форми α, β, γ, δ та ε рифаксиміну. WO2008/155728, US 2009/312357 та US2008/008253 описують способи отримання аморфних форм. WO2009/108730 описує поліморфні форми рифаксиміну, названі zeta, eta, α-dry, iota, β-1, β-2 та ε-dry. WO2011/153444 описує поліморфні форми κ та Θ, та WO 2011/156897 описує поліморфні форми, названі AO-1 та APO-2. Viscomi G. et al, Cryst. Eng Comm., 2008, 10 1074-1081 (2008) описує поліморфи α,β,γ, δ, ε, спосіб їх отримання та їх хімікофізичні та біологічні властивості. Рифаксимін - антибіотичний медикамент активний проти грампозитивних та грамнегативних бактерій, які мають низьку системну абсорбцію, незначну при застосуванні пероральним шляхом, як описано в Descombe J. J. et al. в Int. J. Clin. Pharmacol. Res., 14 (2), 51-56, (1994); відомо про його антибактеріальну активність, наприклад, проти бактерії, локалізованої в шлунково-кишковому тракті, яка спричиняє кишкові інфекції, діарею та синдром подразненої товстої кишки (IBS), бактеріальне зростання в тонкій кишці або "надмірний розвиток мікрофлори малого кишечнику " (SIBO), також відома пов'язаність із хворобою Крона (CD), недостатністю підшлункової залози, ентеритом, фіброміалгією. Щодо його особливості, рифаксимін грає доречну роль у лікуванні інфекційних та запальних хвороб кишечнику в гострій та в хронічній фазі. Різні форми рифаксиміну пов'язано з різними рівнями системної абсорбції. Рифаксимін тепер є дозволеним для лікування гострих та хронічних патологій, етіологія яких частково або повністю стосується грампозитивних та грамнегативних кишкових бактерій, як-то синдроми діареї, спричиненb [зміненим балансом бактеріальної флори кишечнику, як-то діарея влітку, дорожня діарея та ентероколіт. Рифаксимін є придатним для профілактики інфекційних ускладнень перед та після хірургічного втручання в шлунково-кишковий тракт як допоміжна речовина при лікуванні гіперамоніємії та для зниження ризику гострих приступів печінкової енцефалопатії. Рифаксимін також може бути придатним для лікування "синдрому "втомлених ніг"; для попередження спонтанного бактеріального перитоніту в пацієнтів, уражених печінковою недостатністю, та при інфекціях, спричинених постійним застосуванням інгібіторів протонного насосу. Крім того, той факт, що рифаксимін є погано системно абсорбованим, є сприятливим для раніше зазначених застосувань, оскільки рифаксимін є нетоксичним навіть при високих дозах та зменшує випадки небажаних побічних ефектів, як-то, наприклад, добір резистентних до антибіотика бактеріальних штамів та ризик можливих фармакологічних взаємодій. Особливості рифаксиміну роблять його сполукою, придатною для місцевих лікувань, як-то придатний для лікування вагінальних інфекцій, наприклад, бактеріального вагініту. Бактеріальний вагініт є надзвичайно частою патологією, яка складає 40-50 % від усіх вагінальних інфекцій. Коли він є симптоматичним та без ускладнень, бактеріальний вагініт охарактеризовано вагінальними виділеннями з неприємним запахом, не пов'язаним із запальною клінічною картиною хвороби (вагінітом), та це віднесено до альтерації вагінальної екосистеми. Нормальна вагінальна флора здорової жінки внаслідок переважаючої присутності Lactobacilli, зокрема, Lactobacillus crispatus та gasseri, продукує гідроген пероксид та підтримує кислий вагінальний pH, отже, інгібує зростання більшості патогенних мікроорганізмів. При бактеріальному вагініті бактерії Lactobacillus замінено надмірним зростанням, у тисячу разів вищим нормальної величини, факультативних анаеробних та аеробних бактерій, головним 1 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 чином, наступними: Gardnerella vaginalis, які присутні майже в усіх жінок, уражених бактеріальним вагінітом, Mycoplasma hominis, грамнегативні анаеробні бактерії, як-то Bacteroides та Prevotella, анаеробні, як-то Peptostreptococcus, анаеробні грампозитивні, як-то Mobiluncus, які присутні в 50 % випадків, та грампозитивні бацили, як-то Atopobium vaginale, які присутні в 95 % випадків бактеріального вагініту. Фактори, які привертають напад хвороби, переважно сформовані в дітородних жінок, які мають низький соціально-економічний рівень, які належать до чорної раси, при регулярному застосуванні вагінальних промивань, курінні та, які мають статеві стосунки з кількома різними партнерами. Із другого боку здається, що застосування естропрогестогенових ліків грають захисну роль. Також гормональна складова виключено є для введення в її етіопатогенез, оскільки цю патологію переважно знайдено в дітородних жінок. Бактеріальний вагініт може стосуватися кількох важливих гінекологічних та акушерських ускладнень, як-то, наприклад: тазова запальна хвороба, часта причина стерильності та позаматкова вагітність; інфекція хірургічного втручання після гінекологічної хірургії; передчасний розрив мембран у вагітних жінок; передчасні роди та аборт. Крім того, хоча це не розглядають як венеричну хворобу, бактеріальний вагініт пов'язано з підвищеним ризиком зараження статево переданих пандемічних хвороб, охоплюючи ВІЛвірусну інфекцію для невагітних та вагітних жінок. Останнім часом також визначено зростання ризику передачі ВІЛ-вірусу від матері до плоду. Діагноз бактеріального вагініту може спиратися на клінічні та/або мікробіологічні критерії. Клінічний діагноз зроблено згідно із клінічними критеріями Amsel, які описано в Amsel R. et al. в Am. J. Med. 1983; 74(1): 14-22. Діагноз є позитивним, коли, принаймні, повідомлено три із чотирьох наступних симптомів: 1) вагінальні виділення, які є гомогенними та прилипають до вагінальних стінок; 2) позитивний тест на слабкий запах (розвиток "аромату риби" після додавання 10 % калій гідроксиду до вагінального виділення); 3) вагінальне pH вище 4,5, та 4) кількість клубка клітин більше 20 % (вагінальні клітини лускатого епітелію, укриті бактеріями, ідентифіковані новим мікроскопічним дослідженням). Мікробіологічний діагноз базовано на обчисленні мітки Nugent, яка охоплює мікроскопічне дослідження вагінальних виділень способами фарбування по Граму. Визначено присутність та кількість трьох різних вагінальних бактеріальних різновидів. Зокрема, низьку мітку отримують, якщо концентрація Lactobacilli є високою, мітка зростає, якщо виявлено присутність Gardnerella та Bacteroidi, та мітка є вищою, якщо також установлено присутність мітки Mobiluncus. Мітка, отримана між 0 та 3, є характерною вагінальною флорою здорової жінки, мітка між 4 та 6 показує, що вагінальна флора початком зміни, та мітка між 7 та 10 показує впевнений діагноз бактеріального вагініту, як описано в Nugent RP et al. в J. Clin. Microbiol. 1991, 29(2), 297-301. Крім того, в останні роки розроблено діагностичні молекулярні способи, як-то PCR-DGGE та реальний час PCR, базовані на аналізі послідовності РНК, та які дозволяють ідентифікацію мікробної композиції вагінальної екосистеми, як описано Zhou X et al. в Microbiology 2004, 150 (Pt8), 2565-2573 та в Appl. Environ. Microbiol. 2004, 70(6), 3575-3581. Отже, ці способи можна безпосередньо застосовувати для визначення присутності патогенних агентів, які спричиняють хворобу, і також перевіряти дію лікування на них із кількісної точки зору. Хоч етіологія бактеріального вагініту не є цілком зрозумілою, лікування має мету застосовувати клінічне та мікробіологічне зцілення, та коли можливо - уникнення рецидивів хвороби. Отже, досконалому лікуванню слід бути ефективним при зниженні патогенних різновидів, та одночасно слід стимулювати відновлення та проліферацію захисних різновидів Lactobacillus із метою попередження можливих рецидивів хвороби. Нормативи Центру контролю хвороби (CDC), 2010, 59, NoRR-12 встановлюють, що всіх жінок, уражених клінічно вираженим бактеріальним вагінітом, та не вагітних жінок слід лікувати антибіотиком. Щодо цього, CDC пропонує, як перший терапевтичний підхід, лікування антибіотиком, як-то, наприклад, наступним: метронідазол, пероральні таблетки 500 мг, двічі за добу протягом 7 діб; або метронідазол, вагінальний гель, 0,75 %, аплікатор (5 г один раз на добу протягом 5 діб, або кліндаміцин, вагінальний крем, 2 %, аплікатор (5 г) один раз на добу протягом 7 діб. Метронідазол та кліндаміцин, застосовані системним шляхом (перорально) або локальним шляхом (вагінально), є ефективними при лікуванні бактеріального вагініту. Однак, інгібіторна дія обох проти захисної флори Lactobacillus, як описано Simoes JA et al вInfect. Dis. Obstet. Gynecol. 2001, 9(1), 41-45, обмежує їх ефективність при попередженні рецидивів. Крім того, обидва з вище вказаних антибіотиків, пов'язані із системними побічними ефектами, деякі з них конкретно обумовлюють, як-то, наприклад, метронідазол - неврологічні реакції, або кліндаміцин - псевдомембранні коліти навіть при застосуванні вагінальним шляхом. 2 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 Крім того, при повторному застосуванні метронідазол та кліндаміцин можуть спричиняти мікробіологічні резистентності не тільки на вагінальному рівні, але також на системному рівні, оскільки їх системно абсорбовано навіть після вагінального застосування. У EP 0547294 описано композиції, які містять кількості рифаксиміну між 50 та 500 мг, які, як установлено, придатні для лікування вагінальних інфекцій, спричинених мікроорганізмами, чутливими до рифаксиміну. Зокрема, в EP 0547294 описано клінічне випробування, зроблене із препаратом рифаксиміну, як вагінальна піна та крем, який містить 200 мг рифаксиміну, де встановлено вищу ефективність піни в порівнянні до крему. У цьому документі також описано композиції для лікування бактеріального вагініту, які містять рифаксимін у капсулах, м'яких капсулах та таблетках, також там описано антибактеріальну дію рифаксиміну проти бактерій звичайно присутніх у вагінальних виділеннях. У таблиці 1 з EP 0547294 описано, що рифаксимін виявляє важливу антибактеріальну активність проти патогенних бактерій, як-то Gardnerella vaginalis, Bacteroides bivious-disiens, Mobiluncus, і також проти непатогенних бактерій, як-то Lactobacilli. Інгібування Lactobacilli, чия присутність є благотворною для підтримання здорового вагінального середовища, слід уважати шкідливим стосовно терапевтичної ефективності. Дійсно, як уже встановлено, кисле середовище, генероване lactobacilli, є необхідною умовою для попередження колонізації патогенних бактерій. У таблиці 1 EP 0547292 також показано, що інгібіторна дія рифаксиміну (MIC50 та MIC90) проти Lactobacilli є рівною, або навіть вищою ніж його дія проти патогенних бактерій, як-то, наприклад, Gardnerella vaginalis, Mobiluncus spp, Bacteroides bivius-disiens. Отже, при застосуванні через вагінальний шлях рифаксимін неперебірливо діє на всю бактеріальну флору, включаючи Lactobacilli. Debbia A. et al. описує в J. Chemother. 20, (2), 186-194, 2008, що рифаксимін проявляє залежну від часу бактеріальну активність, отже, нові фармацевтичні композиції рифаксиміну є потрібними, бо вони є ефективними для лікування вагінальних інфекцій, що забезпечує відповідний період часу контакту рифаксимін із джерелом зараження та локальні концентрації рифаксиміну, придатні для лікування вагінальних інфекцій, як-то для бактеріального вагініту, та вони не знижують концентрацію Lactobacilli, що є важливим для попередження рецидиву вагінальних інфекцій. Крім того, важливо, що концентрації рифаксиміну, які постачає композиція, є ефективними без потреби високих доз рифаксиміну. Беручи до уваги, що інтенсивний колір рифаксиміну також є важливим, бо рифаксимін, який містять композиції, добре сприймали пацієнти без причин щодо знебарвлення, та найкраще, коли композиції були б у твердій формі дозування. Також важливо, що фармацевтичні композиції були б ефективними при знищенні хвороби (вагінальних інфекцій) та при зменшенні кількості рецидивів за короткі періоди лікування та зі зменшеними загальними кількостями застосованого рифаксиміну в порівнянні з описаним в EP 0547294. Метою заявленого винаходу, яка тепер несподівано досягнута, є тверді фармацевтичні композиції, зокрема, у формі вагінальних таблеток, конкретно - таблеток, сформованих пресуванням гранул рифаксиміну з екстрагранулярними наповнювачами. Гранули рифаксиміну відрізняються тим, що гранули рифаксиміну містять фармацевтично прийнятні наповнювачі, вибрані з наступного: розріджувач, зв'язувач та змащувач, де, принаймні, присутній зв'язувач. Екстрагранулярні наповнювачі характеризуються тим, що містять, принаймні, один дезінтегрант та необов'язково інші зовнішньогранулярні наповнювачі, вибрані з наступного: зв'язувач, розріджувач та змащувач. Фармацевтичні композиції заявленого винаходу характеризуються тим, що вони вивільнюють рифаксимін із гранул за короткий час, навіть в оточенні зниженими кількостями води, які фізіологічно присутні в піхві. Композиції достатньо дезінтегрують гранули в піхві та постачають рифаксимін в ефективних кількостях для лікування вагінальних інфекцій. Нові композиції можна отримувати з різними поліморфами рифаксиміну, уже відомими в рівні техніки, та придатними для лікування бактеріального вагініту та в попередженні рецидивів хвороби. Зокрема, нові композиції не зменшують концентрацію Lactobacilli, звичайно присутньої у вагінальній флорі, але несподівано сприяють їх збільшенню протягом курсу лікування. Згідно з метою заявленого винаходу запропоновано композиції, придатні для лікування вагінальних інфекцій, та, зокрема, бактеріального вагініту, при дозах менших 200 мг/добу, з курсом лікування менше тижня, та забезпечують видужання з нижчими кількостями рифаксиміну за більш короткий курс лікування ніж повідомлений у літературі, відомій експерту в рівні техніки, та в клінічній практиці, отже отримання видужання від хвороби при повному 3 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 застосуванні кількостей рифаксиміну, які, приблизно, у десять разів нижчі вказаних в патенті EP 0547294. Зокрема, згідно з винаходом запропоновано ефективні дози та курс лікування, придатні для отримання повного видужання, зокрема, у порівнянні із плацебо. Фармацевтичні композиції, які містять рифаксимін, згідно з метою заявленого винаходу, є ефективними при лікуванні вагінальних інфекцій, та, зокрема, бактеріального вагініту, при концентраціях, нижчих 200 мг/добу, при тривалості лікування менше тижня в порівнянні із плацебо. Окрім дози згідно із заявленим винаходом також вибрано тривалість лікування, придатну для отримання повного видужання. Знайдені композиції не розповсюджені, добре сприйнятливі та вільні від побічних дій. У прикладах описаних тут здійснень переборено описані вище недоліки традиційних композицій рифаксиміну передбаченням фармацевтичних композицій, які містять рифаксимін, ефективний при лікуванні вагінальних інфекцій, та, зокрема, бактеріального вагініту. Один аспект винаходу - фармацевтичні композиції, які містять гранули рифаксиміну, які мають рифаксимін в кількості меншій 500 мг, наприклад, меншій 200 мг, краще 2,5 - 100 мг, наприклад, 12,5, 25 мг, 50 мг та 100 мг, та один або більше екстрагранулярних наповнювачів, які містять, принаймні, один дезінтегрант; де вищевказана фармацевтична композиція має селективну активність проти вагінальних патогенних бактерій. Ще один аспект винаходу фармацевтична композиція, яка має селективну антибактеріальну дію, яка підтримує або збільшує кількість Lactobacilli після курсу лікування. Фармацевтична композиція може мати, принаймні, один екстрагранулярний дезінтегрант, присутній в кращій кількості 2 - 20 мас. % фармацевтичної композиції. Фармацевтична композиція може бути композицією контрольованого вивільнення та може бути у формі вагінальної таблетки або м'якої капсули. Краще, коли фармацевтична композиція є у формі вагінальної таблетки. Вагінальна таблетка може мати час розпаду менший п'яти хвилин, краще - менше двох хвилин. Також тепер описано нові способи: i) спосіб лікування вагінальної інфекції (наприклад, бактеріального вагініту) та ii) спосіб попередження рецидиву вагінальної інфекції (наприклад, бактеріального вагініту), способи, які полягають у вагінальному застосуванні терапевтично ефективної кількості описаної фармацевтичної композиції, де терапевтично ефективна кількість селективно зменшує кількість вагінальних патогенних бактерій, підтримуючи або збільшуючи кількість Lactobacilli за курс лікування. В одному аспекті розкритого тепер способу збільшено кількість Lactobacilli за курс лікування. В одному втіленні терапевтично ефективна кількість може бути добовою дозою рифаксиміну меншою 500 мг, краще - 200 мг, наприклад, меншою 100 мг. Краще, коли добова доза рифаксиміну дорівнює 100 мг, 50 мг або 25 мг. Кращим часом курсу лікування є десять діб або менше, наприклад, один тиждень або менше. Кількість рифаксиміну, застосованим за курс лікування, може дорівнювати 700 мг рифаксиміну або менше, наприклад, 500 мг рифаксиміну або менше. Терапевтично ефективна кількість рифаксиміну може дорівнювати 12,5 або 25 мг на добу, де курс лікування - 5 діб. Альтернативно, у ще одному втіленні терапевтично ефективна кількість рифаксиміну на добу може дорівнювати 100 мг, де курс лікування є 2 доби. В одному втіленні спосіб лікування вагінальної інфекції згідно із заявленим винаходом спричиняє зменшення мітки Nugent за 3 пунктами або більше після курсу лікування. Також тут описано спосіб створення фармацевтичної композиції, який охоплює етапи створення гранул рифаксиміну сухим гранулюванням суміші рифаксиміну та одного або більше наповнювачів, формування таблетки спочатку змішуванням, а потім пресуванням гранул рифаксиміну з одним або більше екстрагранулярними наповнювачами, охоплюючи, принаймні, один дезінтегрант. У переважному втіленні, при застосуванні розкритого способу, форма рифаксиміну перед етапом сухого гранулювання та форма рифаксиміну після етапу сухого гранулювання є однаковими. Заявлений винахід описує фармацевтичні композиції, які містять менше 200 мг рифаксиміну у твердій формі, зокрема, у формі таблеток, які вивільнюють рифаксимін контрольованим способом, забезпечуючи селективну бактерицидну активність проти патогенних бактерій. Фармацевтичні композиції заявленого винаходу містять гранули рифаксиміну та/або мікрогранули з екстрагранулярними наповнювачами. Гранули рифаксиміну містять наповнювачі, вибрані серед одного або більше розріджувачів, зв'язувачів та змащувачів; екстрагранулярні наповнювачі містять один або більше зв'язувачів, розріджувачів, змащувачів та дезінтегрантів. 4 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 Фармацевтичні композиції у твердій формі, зокрема, у формі таблеток, забезпечують швидкий розпад, наприклад, менший п'яти хвилин, та вивільнюють гранули рифаксиміну навіть у присутності низьких кількостей водної рідини, як-то вагінальної мукози. В одному втіленні фармацевтична композиція містить гранули рифаксиміну та/або мікрогранули, які містять менш 200 мг рифаксиміну, краще - менше 100 мг рифаксиміну. Нові композиції, крім того, містять один або більше внутрішньогранулярних наповнювачів та один або більше зовнішньогранулярних наповнювачів, які охоплюють, принаймні, один дезінтегрант. Внутрішньогранулярні наповнювачі вибрано із групи, яка складається з наступного: розріджувач, зв'язувач, змащувач та їх суміш. Зовнішньогранулярні наповнювачі містять, принаймні, один дезінтегрант та необов'язково додаткові зовнішньогранулярні наповнювачі, вибрані із групи, яка складається з наступного зв'язувачі, розріджувачі, змащувачі та їх суміші. Гранули, які містять рифаксимін, містять кількість рифаксиміну 1 - 80 % (мас. %), один або більше зв'язувачів в кількості 0,5 - 20 % (мас. %), один або більше розріджувачів в кількості 30 90 % (мас. %), один або більше змащувачів в кількості 0,1 - 5 % стосовно маси гранули. Згідно із переважним втіленням винаходу гранули рифаксиміну містять кількість рифаксиміну 5 - 30 % (мас. %), один або більше зв'язувачів в кількості 1 - 10 % (мас. %), один або більше розріджувачів в кількості 50 - 90 % (мас. %) та один або більше змащувачів в кількості 0,5 - 4 % (мас. %) стосовно маси гранули. Розріджувач, придатний для виготовлення гранул рифаксиміну, краще вибирати з наступного: целюлоза, мікрокристалічна целюлоза, гідроксипропілметилцелюлоза, кальцій фосфат, крохмаль, каолін, двогідратний кальцій сульфат, кальцій карбонат, безводна або гідратована лактоза, сахароза, манітол, полісахариди, глюкани, ксилоглюкан та їх суміш. Зв'язувач, придатний для виготовлення гранул рифаксиміну, вибрано із групи, яка містить наступне: зерновий крохмаль, пептизований крохмаль, гуміарабік, лактоза, мальтодекстрин, співполімер 1 вініл-2-піролідон та вінілацетат (коповідон), сахароза та їх суміші. Змащувач, придатний для виготовлення гранул рифаксиміну, вибрано із групи, яка містить наступне: гліцерин дибегенат, кальцій або магній стеарати, алюміній, натрій стеарилфумарат, гідрогенізовані олії, рослинні олії, пальмітинова кислота, спирт, крохмаль, мінеральні масла, поліетиленгліколь, натрій лаурилсульфат, тальк, гліцериди, натрій бензоат та їх суміш. Згідно з переважним втіленням заявленого винаходу, зв'язувач вибрано із групи, яка складається з наступного: коповідон та зерновий крохмаль. Найкращий зв'язувач - коповідон. Згідно з переважним втіленням заявленого винаходу розріджувач вибрано із групи, яка складається з наступного: моногідратна або негідратована лактоза, целюлоза та мікрокристалічна целюлоза, гідроксипропілметилцелюлоза. Найкращий розріджувач моногідратна або негідратна лактоза. Згідно з переважним втіленням заявленого винаходу змащувач вибрано із групи, яка складається з наступного: магній стеарат та гліцерин дибегенат. Найкращий змащувач - магній стеарат. Гранули рифаксиміну виготовлено способами сухого гранулювання, способом, де рифаксимін змішано з вибраними наповнювачами (внутрішньогранулярні наповнювачі), у вказаних вище кількостях, та все змішано для отримання гомогенної суміші. Суміш потім розміщують в ущільнювач для отримання гранул. Гранули рифаксиміну потім оброблюють та змішують із зовнішньогранулярними наповнювачами, охоплюючи, принаймні, один дезінтегрант із розкритих. Додаткові зовнішньогранулярні наповнювачі вибрано з наступної групи: зв'язувач, розріджувач та змащувач та їх комбінація. Згідно з переважним втіленням зв'язувач вибрано із групи, яка містить коповідон, пептизований крохмаль та зерновий крохмаль; розріджувач вибрано із групи, яка складається з наступного: лактоза, целюлоза, мікрокристалічна целюлоза та гідроксипропілметилцелюлоза; змащувач вибрано із групи, яка складається з наступного: магній стеарат та гліцерин дибегенат. Дезінтегрант, придатний для виготовлення композиції згідно із заявленим винаходом вибрано в групи, яка складається з наступного: натрій крохмаль гліколят, пептизований крохмаль, співполімер полівінілпіролідону (PPPV або кросповідон), натрійкарбоксиметилметилцелюлоза (натрійкармелоза), поперечно зв'язана карбоксиметилцелюлоза (натрійкроскармелоза), силікати лужних та лужноземельних металів (наприклад кальцій силікат) та їх суміш. Краще, коли зовнішньогранулярний дезінтегрант вибрано із групи, яка складається з наступного: кросповідон, натрій крохмаль гліколят, пептизований крохмаль, силікати лужних металів та їх суміш. 5 UA 111972 C2 5 Найкраще, коли зовнішньогранулярний дезінтегрант вибрано в групи, яка складається з наступного: кросповідон, кальцій силікат та їх суміш. Зокрема, та в запропонованому втіленні дезінтегрант - суміш кросповідону та кальцій силікату. Згідно із переважним втіленням заявленого винаходу тверда фармацевтична композиція, краще у формі таблеток, може містити гранули рифаксиміну в кількості 10 - 85 % (мас. %); дезінтегранти або їх суміш, де їх загальна кількість 2 - 20 % (мас. %), незалежно від їх відносних співвідношень; зв'язувач в кількості 0,5 та 5,0 % (мас. %) та змащувач в кількості 0,1 та 10,0 % (мас. %), стосовно кінцевої композиції яку надано в таблиці 1. Таблиця 1 Компонент Процент {%) за масою Гранули рифаксиміну 10-85 % Змащувач 0,1-10 % Зв'язувач 0,5-5 % Розріджувач 10-80 % Дезінтегрант 2-20 % 10 15 20 Згідно з переважним втіленням заявленого винаходу, зовнішньогранулярний розріджувач вибрано в групи, яка складається з наступного: безводна або моногідратна лактоза, зерновий крохмаль та кристалічна целюлоза; зовнішньогранулярний змащувач - магній стеарат, зв'язувач вибрано серед наступного: пептизований крохмаль та коповідон, гідроксипропілметилцелюлоза, та зовнішньогранулярний дезінтегрант вибрано серед наступного: кросповідон, пептизований крохмаль та кальцій силікат та їх суміш. Згідно з найкращим втіленням зовнішньогранулярний розріджувач вибрано із групи, яка складається з наступного: безводна або моногідратна лактоза; зовнішньогранулярний зв'язувач вибрано в групи, яка складається з наступного: коповідон та пептизований крохмаль; зовнішньогранулярний змащувач - магній стеарат; зовнішньогранулярний дезінтегрант вибрано в групи, яка складається з наступного: кросповідон, кальцій силікат, пептизований крохмаль та крохмаль гліколят. Згідно з найкращим втіленням композицію таблетки, яка містить рифаксимін, надано в таблиці 2. 25 Таблиця 2 Процент {%) за масою Гранули рифаксиміну 20-60 % Магній стеарат 0,1-10 % Коповідон 0,5-4 % Лактоза 10-80 % Кросповідон та кальцій силікат 2-20 % Компонент 30 35 40 Композиція таблетки може, крім того, містити таке покриття як філмоген. Тверда композиція у формі таблеток може містити кількість рифаксиміну 2,5 - 500 мг, краще - 2,5 - 100 мг, найкраще - 10 - 50 мг. Тверда композиція у формі таблеток також може містити рифаксимін у кількості краще - 0 100 мг, 10 - 50 мг та 10 - 25 мг, ще краще - 25 - 100 та 25 - 50 мг, та найкраще - 25 мг. Композиція згідно із заявленим винаходом, крім того, необов'язково може містити біоадгезивні засоби, консерванти, буфери, антисептичні засоби та ароматизатори. Коли присутній біоадгезивний засіб, композиція може мати біоадгезивні властивості, що означає, що гранули рифаксиміну можуть прилипати до вагінальної мукози. Прикладами полімерів та олігомерів або їх сумішей, як можна вводити в мікрогранули, є пектини, зеїни, казеїн, желатина, альбумін, колаген, кітосан, олігосахариди та полісахариди, якто, наприклад, целюлоза, декстран, полісахариди із зерен тамаринду, смола ксантану, гуміарабік, гіалуронова кислота, альгінова кислота, натрій альгінат. Коли біоадгезив - синтетичний полімер, полімер вибрано з наступного: поліаміди, полікарбонати, поліалкілени, поліалкіленгліколі, поліалкіленоксиди, поліалкілентерефталати, полівініловий спирт, полівінілетери, полівінілестери, полівінілпіролідон, полісилоксани, поліуретани, полістирени, полімери акрилової кислоти та метакрилат-естери, співполімер 6 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 метакрилової кислоти етилакрилату, поліактиди, полібарбітурові кислоти, поліангідриди, поліортоестери та їх суміші. Іншими придатними полімерами є метилцелюлоза, етилцелюлоза, гідроксипропілцелюлоза, гідроксибутилметилцелюлоза, целюлоза ацетат, целюлоза пропіонат, целюлоза ацетат бутират, карбоксиметилцелюлоза, целюлоза триацетат, сіль натрій сульфат целюлоза, поліметилметакрилат, поліізопропілметакрилат, поліізобутилакрилат, полі(октадецилакрилат), поліпропілен, поліетиленгліколь, поліетиленоксид, поліетилентерефталат, полівінілацетат, полівінілхлорид, полістирол, полівінілпіролідон, полівінілфенол та їх суміші. Ще одною групою полімерів, придатних для отримання біоадгезивності, є полімери, які мають групу розгалуження, яка містить, принаймні, одну зв'язану гідрофобну групу, де гідрофобні групи звичайно є неполярними групами. Приклади, але без обмеження, таких гідрофобних груп охоплюють алкіл, алкеніл та алкініл. Кращі гідрофобні групи вибрано для збільшення біоадгезивності полімерів. Інші полімери мають гідрофобне розгалуження, принаймні, з гідрофільною групою, як-то карбонові кислоти, сульфонові кислоти та фосфонові кислоти, нейтральні та позитивно заряджені аміни, аміди та іміни, де гідрофільні групи - такі, які підвищують біоадгезивність полімеру. Гранули рифаксиміну отримано способами сухого гранулювання, що дозволяє підтримувати вихідний кристалічний рифаксимін або аморфну форму без будь-яких поліморфних перетворень, які відбуваються як описано в літературі, у присутності води або органічних розчинників. Переважний спосіб отримання композиції охоплює вибрану поліморфну форму в рівні техніки, оскільки відомо, що поліморфні форми рифаксиміну мають різну розчинність та надають абсорбції в плазмі, які відмінні, принаймні, у два порядки. Термін "рифаксимін" застосовано в широкому сенсі та охоплює не тільки "рифаксимін", а також його фармацевтично прийнятні солі, сольвати, гідрати, вторинні енантіомери, поліморфи, аморфні форми, співкристали та фармацевтично прийнятні комплекси, але без обмеження. Предмет заявленого винаходу рифаксимін у фармацевтичних композиціях є переважним у слабко розчинній формі при його застосуванні для лікування бактеріального вагініту, щоб діяла локальна без системна абсорбції. Це дозволяє уникати на системному рівні потенційного ризику стійких до антибіотику бактеріальних штамів, як можуть виникати навіть при низьких концентраціях плазми. Вибором різних поліморфів рифаксиміну, які мають різне розчинення та абсорбцію, або їх сумішей, надана можливість отримувати композицію, та, зокрема, у формі таблеток, для лікування вагінальних інфекцій, та більше, зокрема, - для різних форм інфекції. Гранули рифаксиміну далі змішують у суміші, яка містить зовнішньогранулярні наповнювачі, які описано в таблиці 1; суміш пресують у пристрої для пресування, який відомий у рівні техніки, для отримання таблеток, краще покритих філмогеном. Зовнішньогранулярні компоненти, присутні у фармацевтичній композиції разом із гранулами рифаксиміну у формі таблеток у кількостях, описаних у заявленому винаході, дозволяють контрольоване вивільнення рифаксиміну. Гранули рифаксиміну вивільнено з таблеток навіть у середовищі зі зниженими кількостями водної рідини, як-то фізіологічне середовище, присутнє в піхві. Гранули рифаксиміну, вивільнені таблетками у вагінальній порожнині, здійснюють місцеву дію у вагінальній мукозі протягом належного періоду часу завдяки комбінованій дії швидкого розпаду таблетки та зниженій швидкості розчинення гранул. У заявленому винаході також описано застосування фармацевтичних композицій рифаксиміну для лікування вагінальних інфекцій, наприклад, конкретно - бактеріального вагініту. Згідно із заявленим винаходом також запропоновано спосіб лікування бактеріальної інфекції та спосіб попередження рецидиву бактеріальної інфекції застосуванням нової композиції. Зокрема, фармацевтичні композиції, які є метою заявленого винаходу, при застосуванні розкритим способом лікування не знижують концентрацію Lactobacilli, що є потрібним для підтримання вагінальної екосистеми, та вони придатні для попередження рецидивуінфекцій, подібно повідомленому стосовно композицій, відомих у рівні техніки. Тверді фармацевтичні композиції заявленого винаходу є терапевтично ефективними для лікування бактеріальних інфекцій при добових дозах рифаксиміну, нижчих 500 мг, краще менших 200 мг, найкраще - менших 100 мг та із повним застосованим рифаксиміном меншим 700 мг, найкраще - меншим 500 мг, для отримання повного видужання та попередження рецидиву в порівнянні з плацебо. 7 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 Зокрема, композиції у формі таблетки, які містять рифаксимін, є ефективними для лікування бактеріальних інфекцій, про що свідчить зменшення мітки Nugent та критеріїв Amsel, застосуванням терапевтично ефективних добових доз менших 500 мг, краще - менших 200 мг, та найкраще - менших 100 мг, наприклад, 100 мг, 50 мг, 25 мг 12,5 або 2,5 мг, при скороченому часі лікування менше десяти діб та, зокрема, менше одного тижня, в порівнянні з плацебо. Композиції таблеток можна застосовувати один раз або кілька разів на добу, краще - один раз на добу. Описані фармацевтичні композиції здійснюють селективну антибактеріальну дію, краще проти патогенних бактерій, краще ніж проти Lactobacilli. Композиція у формі таблеток, які містять рифаксимін, у кількостях менших 500 мг, конкретно, менших 200 мг та конкретніше, менших 100 мг, збільшують та зберігають високу концентрацію Lactobacilli навіть після кінця курсу лікування в порівнянні із плацебо. Згідно із ще одним аспектом заявленого винаходу запропоновано композицію та курс лікування, придатні для лікування вагінальних інфекцій, отриманні видужання та попередження рецидиву в пацієнтів, які потерпають від бактеріальних інфекцій. Конкретно, описані композиції підтримують видужання від хвороби протягом періоду часу тривалістю більше 30 діб при закінченні лікування при добових дозах менших 200 мг, краще менших 100 мг при часі застосування меншому одного тижня. Згідно із ще одним аспектом щодо нових фармацевтичних композицій, які містять кількість рифаксиміну 12,5 мг - 100 мг, вони є придатними для лікування вагінальних інфекцій із періодами лікування меншими одного тижня. Конкретніше, показано, що композиції, які містять 25 мг рифаксиміну, при лікуванні протягом п'яти діб є придатними для лікування бактеріальних інфекцій. Пацієнти яких лікували композиціями, які містять 25 мг рифаксиміну, які отримували таблетку один раз на добу протягом п'яти діб, показали більшу швидкість видужання (процент пацієнтів, які показали видужання в кінці курсу лікування) згідно з міткою Nugent та критеріями Amsel їх більше ніж пацієнтів, яких лікували плацебо. Конкретно, пацієнти, яких лікували композиціями, які містять 25 мг рифаксиміну протягом п'яти діб, показали більшу швидкість видужання, тобто, 48 %, у порівнянні, приблизно, зі швидкістю видужання пацієнтів 25,9 %, яких лікували 100 мг рифаксиміну протягом п'яти діб, приблизно, зі швидкістю видужання пацієнтів 36 %, яких лікували 100 мг/добу протягом двох діб, та приблизно, зі швидкістю видужання пацієнтів 19,2 %,, яких лікували плацебо, як надано в таблиці 8. Конкретніше, пацієнти, яких лікували композиціями, які містять 25 мг рифаксиміну, показали більшу швидкість видужання, згідно міткою Nugent, більшу ніж та, яку отримано іншими групами, яких лікували. Зокрема, більша швидкість видужання в 47 % у порівнянні зі швидкістю видужання пацієнтів, приблизно, 25 %, яких лікували 100 мг рифаксиміну протягом п'яти діб, зі швидкістю видужання пацієнтів, приблизно, 36 %, яких лікували протягом двох діб, та зі швидкістю видужання пацієнтів, приблизно, 19 % у пацієнтів, яких лікували плацебо. Згідно із ще одним аспектом заявленого винаходу композиції, які містять рифаксимін у вагінальних таблетках, призводять до зменшення на 3 пункти мітки Nugent в усіх пацієнтів, яких лікували, у порівнянні з пацієнтами, яких лікували плацебо. Конкретно, зменшення на 3 пункти мітки Nugent одержали, приблизно, більше 65 % пацієнтів, яких лікували композицією вагінальної таблетки, яка містить 25 мг рифаксиміну протягом п'яти діб; більше 50 % пацієнтів, яких лікували композицією, яка містить 100 мг рифаксиміну протягом п'яти діб; більше 30 % пацієнтів, яких лікували композицією в таблетці, яка містить 100 мг рифаксиміну протягом двох діб, у порівнянні, приблизно, з 18 % пацієнтів, яких лікували плацебо. Крім того, та конкретно, композиції вагінальної таблетки, які містять 25 мг рифаксиміну, при застосуванні до пацієнтів, уражених бактеріальним вагінітом, протягом курсу лікування п'ять діб призводить до зниження на п'ять пунктів мітки Nugent, приблизно, в 48 % пацієнтів, яких лікували, приблизно в 28 % пацієнтів, яких лікували 100 мг рифаксиміну, протягом п'яти діб, та, приблизно, в 26 % пацієнтів, яких лікували 10 мг протягом двох діб, у порівнянні, приблизно, з 0 % пацієнтів, яких лікували плацебо. Крім того, та конкретніше, композиції вагінальної таблетки, які містять 25 мг рифаксиміну, протягом курсу лікування п'ять діб призводить до зниження мітки Nugent більше ніж на 8-10 пунктів у порівнянні іншими групами лікування, які охоплено в цьому дослідженні. Описані фармацевтичні композиції внаслідок комбінації вибраних гранулярних та зовнішньогранулярних наповнювачів та способу отриманні, забезпечують контрольоване 8 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 вивільнення рифаксиміну в піхві при ефективності тільки при одному застосуванні дозування на добу. Описані фармацевтичні композиції є придатними та ефективними для лікування пацієнтів, уражених вагінальними інфекціями, конкретно, бактеріальним вагінітом, при добових дозах, нижчих 200 мг, та конкретно - при дозах, які містять 100 - 25 мг, наприклад, 100 мг, 50 мг 25 мг та 12,5 мг рифаксиміну, при часі лікування меншому одного тижня. Згідно із ще одним аспектом описаних композицій, які містять 25 мг рифаксиміну у формі вагінальних таблеток, композиції є придатними для лікування пацієнтів, уражених вагінальними інфекціями, конкретно, важким бактеріальним вагінітом, і мають високу мітку Nugent (> 6, краще > 7, або найкраще > 9, або згідно 3 з 4 факторів серед критеріїв Amsel). Згідно із ще одним аспектом заявленого винаходу є застосування композицій рифаксиміну, які містять рифаксимін при концентраціях менших 200 мг, та конкретно, 100 мг, 50 мг 25 мг та 12,5 мг, згідно з розкритим часом лікування, для лікування та попередження рецидиву бактеріального вагініту. Згідно із ще одним аспектом заявленого винаходу є фармацевтичні композиції, які містять рифаксимін, та є добре стерпними та безпечними при застосуванні, та конкретно, це призводить до зниженої системної абсорбції, що показано незначним рівнем рифаксиміну, визначеному в плазмі. Тверді фармацевтичні композиції у формі таблеток мають несподівану властивість вивільнювати гранули рифаксиміну у вагінальній мукозі навіть зі зниженими кількостями вагінальної рідини. Результати клінічного випробування заявленого винаходу показують, що вищевказані гранули здатні вивільнювати ефективні кількості рифаксиміну в пацієнтів, уражених бактеріальним вагінітом, навіть при лікуванні низькими дозами рифаксиміну, та при курсі лікування, наприклад, не більше десяти діб, та, конкретно, не більше п'яти діб, та здатні попереджувати рецидив інфекцій протягом чотирьох тижнів після закінчення курсу лікування. Крім того, конкретно дуже важливим є те, що композиція таблетки, яка містить кількості рифаксиміну нижчі 200 мг, та конкретно, нижчі 100 мг, збільшує та підтримує високі концентрації Lactobacilli навіть після завершенні лікування в порівнянні із плацебо. У прикладі 1 описано отримання гранул рифаксиміну та отримання вагінальних таблеток, які містять 25 мг рифаксиміну. Таблетки виготовлено змішуванням гранул рифаксиміну разом із зовнішньогранулярними наповнювачами. Отримані таблетки мають твердість, визначену як описано в European Pharmacopeia Ed. 7,0, Chapter 2,9,8, ref. 01/2008:20908, вищу 5 Kp, та вони мають час розпаду, приблизно, одну хвилину, в умовах, описаних в European Pharmacopeia Ed. 7,0, Chapter 2,9,2. ref. 01/2008:20902,. У прикладі 2 описано отримання 100 мг таблеток рифаксиміну, де гранули рифаксиміну змішано разом із зовнішньогранулярними наповнювачами, де показано гнучкість способу продукування таблетки, також спосіб, коли при змінних кількостях рифаксиміну не збільшено масу готової таблетки. У прикладі 3 описано отримання таблеток рифаксиміну щодо застосованих у прикладі 1, де гранули виготовлено з різними зв'язувачами, та їх змішано із зовнішньогранулярними наповнювачами. Конкретно, у прикладі 3 описано отримання композицій, де різні наповнювачі застосовано в порівнянні із прикладом 1 та 2. Конкретно, дезінтегрант вибрано з наступного: кальцій силікат, кросповідон, натрій крохмаль гліколят або їх суміш; зв'язувач - гідроксипропілметилцелюлоза та розріджувач - моногідрат лактоза. Композиція 7, де зв'язувач не присутній у зовнішньогранулярних наповнювачах, ілюструє проблему формування суміші, та за візуальним контролем суміш не є гомогенною при відсутності зв'язувачу. У прикладі 4 описано час розпаду таблеток рифаксиміну, згідно з European Pharmacopeia European Pharmacopoeia 7,0 2,9,2, ref. 01/2008:20902, в композиціях 1-8, отриманих згідно із прикладами 1, 2 та 3. Час розпаду змінюється, приблизно, між одною хвилиною та десятьма хвилинами, залежно від компонентів композицій; композиція без будьякого дезінтегранту (Комп. 4) надає час розпаду, приблизно, 5 хвилин, та коли присутній тільки кросповідон (Комп. 3, 5. та 6), час розпаду є між 1'30" та 5'30". Нижчий час розпаду композиції 3 відповідає композиції, де додано більшу кількість кросповідону. Менші часи розпаду, виявлені композицією 1, композицією 2 та композицією 7, є кращим, але композиція 7 тепер не є кращою для промислового масштабу. Композиція 1 та 2 відповідно до таблеток, які містять рифаксимін у кількості 25 та 100 мг, мають внутрішньогранулярний зв'язувач - коповідон, та зовнішньогранулярний дезінтегрант є a суміші кросповідону та кальцій силікату. Ці композиції здатні розпадатися протягом часу меншому 2 хвилин та вивільнюють рифаксимін на місці дії. 9 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 У прикладі 5 описано отримання ліпофільних м'яких капсул, де кількість рифаксиміну дорівнює 50 - 200 мг, у присутності напівгліцеридів, поверхнево-активних речовин та ксилоглюкану. Кількість рифаксиміну, вивільненого ліпофільними м'якими капсулами протягом, приблизно, двох годин, дорівнює 15 % - 25 % стосовно загального рифаксиміну, вміщеного в м'яких капсулах. У прикладі 6 описано отримання гідрофільних м'яких капсул, де кількість рифаксиміну дорівнює 25 - 100 мг у присутності наступного 2(2-етоксиетокси)-етанол, транскутол, гліцерин, поліетиленгліколь (PEG) та ксилоглюкан. Ці композиції мають швидке вивільнення рифаксиміну, та протягом 20 хвилин рифаксимін вивільнено більше 70 % (мас. %). У прикладі 7 описано вивільнення композицій у таблетках та вагінальних м'яких капсулах, отриманих як у прикладах 1-5, у розчині за умова об'єму та температури подібних вагінальним фізіологічним умовам. Різні композиції, які містять 25 - 100 мг рифаксиміну, є порівнянними з оцінкою вивільнення рифаксиміну в термостатованих умовах при 37 °C. Кількість рифаксиміну, вивільненого в 10 мл водного розчину, визначено спектрофотомерично. Описані експерименти показують, що таблетки, які містять 100 мг рифаксиміну, отримані як описано в прикладі 1, та які мають композицію описану в прикладі 2, вивільнюють за одну годину кількість рифаксиміну, приблизно, меншу 0,5 мг; гідрофільні м'які капсули, які містять 100 мг, рифаксимін вивільнюють за одну годину, приблизно, 8,5 мг рифаксиміну, гідрофільні м'які капсули, як містять 25 мг рифаксиміну, вивільнюють за одну годину, приблизно, 7 мг рифаксиміну, та ліпофільні м'які капсули, як містять приблизно 100 мг рифаксиміну, вивільнюють за одну годину, приблизно, 4 мг рифаксиміну. У прикладі 8 описано дослідження біонакопичення, зроблене з фармацевтичними композиціями в таблетках, описаних у цьому винаході, де таблетки та м'які капсули, які містять кількість рифаксиміну, яка відповідає 12,5 мг, отримані способами, ідентичними одному описаному в прикладах 1 та 4, застосовували до самиць білих специфічних вільних від патогену (SPF) кролів Нової Зеландії, які не народжували та не вагітніли. Протягом лікування тварин не спостерігали локальних клінічних ознак, жодних реакцій на лікування, ніяких змін маси тіла в порівнянні з контрольною групою. Концентрацію рифаксиміну в плазмі визначали обґрунтованим способом РХ-MС/MС, який має нижчу межу кількісного аналізу (LLOQ) 0,5 нг/мл. У таблиці 15 прикладу 8 повідомлено фармакокінетичні параметри рифаксиміну в кроля після застосування вагінальних таблеток та м'яких капсул. Тільки в деякі випадках фармакокінетичні параметри є злегка вищими LLOQ. Середнє значення величин максимальної концентрації плазми (Cмакс.) для м'яких капсул, приблизно, у чотири рази вище величини Cмакс. у таблеток, оскільки величина площі під кривою концентрація плазми стосовно часу (AUCO-t last) для м'яких капсул, приблизно, у дванадцять разів є більшою в порівнянні з одною з таблеток. Ці результати показують, що, при застосуванні однакового дозування рифаксиміну вагінальні таблетки надають нижчу плазмову абсорбцію в порівнянні з м'якими капсулами. Цей результат є у відповідності до профілів розчинення, показаних у прикладі 7. У прикладі 9 описано ефективність композицій рифаксиміну в м'яких капсулах та таблетках в експериментальних моделях на тваринах, де вагінальну інфекцію індукували способами щеплення Gardnerella vaginalis, виділених у самиць, уражених бактеріальним вагінітом. Кроля Нової Зеландії, який має масу 2 - 3 кг, заражали фізіологічним розчином, який містив кількість Gardnerella vaginalis більшу 105 та, щоб отримати стійку інфекцію, щеплення робили двічі або тричі. Через сім діб після щеплення тварин лікували композиціями рифаксиміну в таблетках та м'яких капсулах, які містять кількості рифаксиміну 1,5 - 12,5 мг, який отримували згідно із прикладом 1 та прикладом 4, де співвідношення наповнювачів пропорційно знижували для отримання композицій із різними кількостями рифаксиміну. Дози рифаксиміну 1,5 мг - 12,5 мг відповідають дозам, приблизно 12,5 мг - 100 мг в самиці, розрахованій згідно із площею поверхні тіла. Композиції не показали будь-якого шкідливого наслідку у тварин та виявили повідомлене в таблицях 16 та 17. Тестовані дозування рифаксиміну в таблетках та в м'яких капсулах призводить після кінця лікування до повного викоренення інфекції за сім діб. М'які капсули та композиції таблеток є ефективним та їх добре витримують тварини. Однак, оскільки таблетки мають нижчі рівні системної абсорбції ніж м'які капсули, як описано в прикладі 8, їх слід уважати більш придатним фармацевтичним препаратом для застосування до пацієнтів, уражених бактеріальним вагінітом. Клінічне дослідження, описане в прикладі 12, робили з таблетками, які містять 25 та 100 мг рифаксиміну, отриманого як описано в прикладах 1 та 2. 10 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 У прикладах 10 та 11 описано системну абсорбцію та терпимість щодо таблеток рифаксиміну в клінічному дослідженні на здорових волонтёрах. У прикладі показано, що концентрації рифаксиміну в плазмі після застосування внутрішньопіхвовим шляхом таблетки, яка містить 100 мг рифаксиміну, є неприйнятним, бо вони завжди нижче інструментального LLOQ 0,5 нг/мл. Ефективність композиції в таблетках для лікування бактеріального вагініту визначали способами клінічного дослідження, зробленого на 114 невагітних жінках віком 18 - 50 років, про що повідомлено в прикладі 12. Клінічні дослідження, описані в прикладі 12, робили з таблетками, які містять 25 та 100 мг рифаксиміну, який отримано як описано в прикладі 1 та 2. Первинним кінцевим пунктом цього випробування була оцінка видужання від бактеріального вагініту згідно з міткою Nugent та критеріями Amsel при першому контрольному візиті через (V3) 7-10 діб після кінця лікування. Вторинним кінцевим пунктом цього випробування було видужання від хвороби, що індивідуально оцінено згідно з міткою Nugent та критеріями Amsel, через 7-10 діб після кінця лікування, підтвердження видужання при другому контрольному візиті, приблизно, через один місяць після кінця лікування (V4) та визначення композиції вагінальної мікробіоти способами молекулярної техніки, як-то реальний час PCR- та PCR-DGGE (реакція ланцюг полімерaзи електрофорез градієнту денатурації гелю). Реальний час PCR- є кількісним способом, де кожний зразок ДНК підсилено різними гендер- та/або видо-специфічними праймерами, чия мішень є бактеріальний ген 16S rРНК або область 16S-23S rРНК; конкретно, специфічні зонди застосовували для Lactobacillus gender, для Gardnerella vaginalis, для Atopobium, для Prevotella та для Veillonella, оскільки вони відображають головні бактеріальні групи, які потерпають від змін при бактеріальному вагініті. З іншого боку, PCR-DGGE - якісний спосіб, внаслідок чого в цьому дослідженні робили підсилення універсальними праймерами зубактерії. Конкретно, пацієнтів, уражених бактеріальним вагінітом та не уражених сучасними вірусними, протозойними та грибковими вагінальними інфекціями, призначали до одної з наступних груп лікування, застосовуючи централізовану процедуру рандомізації та подвійний сліпий експериментальний проект: Група A: пацієнти, які отримували вагінальну таблетку рифаксиміну, як містить 100 мг рифаксиміну, отриманого згідно із прикладом 2, один раз на добу протягом п'яти діб увечері; Група B: пацієнти, які отримували вагінальну таблетку рифаксиміну, як містить 25 мг рифаксиміну, отриманого згідно із прикладом 1, один раз на добу протягом п'яти діб увечері; Група C: пацієнти, які отримували вагінальну таблетку рифаксиміну, як містить 100 мг рифаксиміну, отриманого згідно із прикладом 2, один раз на добу протягом двох діб увечері, плюс вагінальну таблетку плацебо, один раз на добу протягом інших трьох діб увечері; Група D: пацієнти, які отримували таблетку плацебо, отриману згідно із прикладом 1, де кількість рифаксиміну замінювали водною лактозою, один раз на добу протягом п'яти діб увечері. Діагноз бактеріального вагініту базували на критеріях Amsel (принаймні, три із чотирьох позитивних критеріїв) та на мітці Nugent (яка дорівнює або більше 4). Дослідження містить скринінг (V1), а потім - рандомізація через сім діб (V2), перший контрольний візит через 7-10 діб після кінця лікування (V3), та другий і останній контрольний візит через 28-35 діб після кінця лікування (V4). Визначення досягнення первинної кінцевої точки робили протягом візиту V3, та визначення досягнення вторинної кінцевої точки оцінювали протягом візиту V4. У таблиці 18 повідомлено величини проценту пацієнтів після лікування композицією, отриманою згідно із прикладом 1 та прикладом 2, у порівнянні з тим, як лікували плацебо. Клінічне випробування звертає увагу на те, що всі групи пацієнтів, яких лікували композиціями таблеток рифаксиміну, показали процент видужання більший ніж ті, яких лікували плацебо. Пацієнти, які належать до групи, яку лікували таблеткою, яка містить 25 мг рифаксиміну, отриманої згідно із прикладом 1, протягом п'яти діб показали процент видужання від хвороби більший ніж в інших групах. Конкретніше, пацієнт, які належить до групи, яку лікували таблеткою, яка містить 25 мг рифаксиміну (Група B), отриманого згідно із прикладом 1, протягом п'яти діб, показали процент видужання більший 40 %; ті, яких лікували таблеткою рифаксиміну, яка містить 100 мг рифаксиміну, протягом двох діб (Група C), показали процент видужання більший 30 %; ті. яких лікували таблеткою, яка містить 100 мг рифаксиміну, протягом п'яти діб (Група A), показали процент видужання більший 20 %. У групі, яку лікували плацебо (Група D), показано процент видужання, приблизно, 19 %. У таблиці 19 повідомлено величини проценту пацієнтів, розрахованих згідно із критеріями Amsel, через 7-10 діб після кінця лікування. Цей результат підтверджує, що в групі, яка 11 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 отримувала протягом п'яти діб композицію, яка містить 25 мг рифаксиміну, показано процент видужання більший ніж у групі, яку лікували плацебо. У таблиці 20 повідомлено, що згідно з міткою Nugent, при візиті V3 процент видужання від хвороби є більшим у пацієнтів, які належить до групи, яку лікували композицією, яка містить 25 мг рифаксиміну протягом п'яти діб, група B є більшою щодо інших груп та щодо групи, яку лікували плацебо. У цьому прикладі опису клінічного дослідження пацієнтів розподіляли наступним чином "пацієнт із рецидивом бактеріального вагініту" та "пацієнт із першим випадком бактеріального вагініту". Процент видужання від хвороби в усіх групах, яких лікували рифаксиміном, був більшим у пацієнтів, які потерпають від рецидиву бактеріального вагініту. Крім того, групу, яку лікували 25 мг рифаксиміну протягом п'яти діб, показала вищий процент видужання навіть у суб'єктів, які потерпають від першого випадку хвороби. Процент видужання від хвороби, розрахований згідно з міткою Nugent та критеріями Amsel, в усіх групах, яких лікували рифаксиміном, був вищим у пацієнтів, які потерпають від інфекції бактеріального вагініту в порівнянні з пацієнтами, які потерпають від першого випадку бактеріального вагініту. Крім того, група, яку лікували рифаксиміном 25 мг протягом п'яти діб, група B, показала вищий процент видужання також у суб'єктів, які потерпають від першого випадку хвороби, як надано в таблиці 23. Пацієнти, яких лікували 25 мг та 100 мг рифаксиміну у вагінальних таблетках, у клінічному дослідженні не показали будь-якого особливого шкідливого випадку, та жодна із груп, яких лікували, не показала протягом лікування будь-якого випадку пов'язаного з рифаксиміном вульвовагінального кандидамікозу. У повідомленому клінічному дослідженні показано, що лікування пацієнтів, уражених бактеріальним вагінітом, вагінальними таблетками контрольованого вивільнення, отриманих згідно із прикладом 1, та які містять 25 мг рифаксиміну, один раз на добу протягом п'яти діб, є більш ефективним при видужанні від хвороби. У прикладах 13-16 описано отримання видужання, згідно із критеріями Nugent, у чотирьох групах пацієнтів, зареєстрованих у клінічному дослідженні групи A, B, C та D. У прикладі 17 повідомлено про мікробіологічне дослідження, зроблене на вагінальних промиваннях пацієнтів, яких лікували 100 мг та 25 мг рифаксиміну протягом п'яти діб (групи A та B) та 100 мг рифаксиміну протягом двох діб (група C), застосовуючи молекулярні способи, реальний час PCR- та PCR-DGGE для визначення композиції вагінальної мікробіоти. У таблиці 28 прикладу 17 повідомлено результати, отримані реальним часом PCR, зображеним як "нг мішень ДНК/нг загальна геномна ДНК", для мікробних різновидів, аналізованих для групи пацієнтів, залучених до клінічного дослідження, візити V3 та V4, у порівнянні з даними, отриманими способами аналізу до лікування. Результати аналізу реального часу PCR показують збільшення Lactobacilli в усіх групах, яких лікували рифаксиміном, оскільки концентрації патогенних бактерій, як-то Gardnerella vaginalis, Atopopium та Prevotella, показали зниження в усіх групах, яких лікували рифаксиміном, у порівнянні із плацебо, отже, демонструючи ефективність композиції в таблетках. Конкретно, пацієнти, яких лікували рифаксиміном у таблетках, отриманих згідно із прикладом 1, та які містять 25 мг рифаксиміну, протягом п'яти діб, при візиті V3 показали підвищення Lactobacilli у порівнянні з іншими групам, яких лікували. Крім того, лікування таблетками контрольованого вивільнення, які містять 25 мг рифаксиміну при лікуванні протягом п'яти діб, є найбільш ефективним щодо їх активності проти анаеробних бактерій та для відновлення Lactobacilli, отже, сприяючи фізіологічному вагінальному мікросередовищу. Аналіз вагінальних зразків при візиті V4 підтверджували дані, отримані при візиті V3 у кінці лікування для пацієнтів, яких лікували композицією у вагінальних таблетках, які містять 25 мг рифаксиміну, отриманого згідно із прикладом 1, при лікуванні протягом п'яти діб, оскільки втримували концентрацію Lactobacilli, оскільки, крам того, знижували патогенні бактерії. Цей результат підтверджує селективну бактерицидну дію композиції, описаної в прикладі 1 та 2, щодо патогенних вагінальних бактерій та не проти Lactobacilli. Також група пацієнтів, яких лікували композицією в таблетках, які містять 100 мг, рифаксиміну, група A, протягом п'яти діб при візиті V4, зберігала швидкість, спостережену при третьому візиті через 7-10 діб після кінця лікування. Результати, отримані способом реального часу PCR, підтверджували даними PCR-DGGE, та повідомленими в прикладі 18, що показує ефективність лікування рифаксиміном при модулюванні композиції вагінальної мікробіоти. Також, згідно із цими способами, дозування рифаксиміну, які є найбільш ефективними при 12 UA 111972 C2 5 10 15 20 25 30 35 40 45 50 55 60 модулюванні вагінальної мікробіоти, є таким, який отримано при лікуванні таблетками, які містять 25 мг рифаксиміну один раз на добу протягом п'яти діб. У прикладі 8 описано дивний та несподіваний результат, наданий композиціями в таблетках, які містять рифаксимін, описаний у заявленому винаході, та результати щодо концентрацій вагінальної мікробіоти при візиті V4 надано в таблиці 29. Описана композиція у вагінальних таблетках, які містять рифаксимін при дозах лікування 100 мг/5 діб, 25 мг/5 діб та 100 мг/2 доби, є ефективними при підтриманні низьких концентрацій патогенних бактерій та збільшенні концентрації Lactobacilli у порівнянні із плацебо. Конкретно, згідно з лікуванням групи A, яка одержувала таблетку, яка містить 100 мг рифаксиміну протягом п'яти діб, показано збільшення в двадцять разів концентрації Lactobacilli; лікування групи B, яка одержувала таблетку, яка містить 25 мг рифаксиміну протягом п'яти діб, показало збільшення в сорок разів концентрації Lactobacilli, та лікування групи C, яка одержувала таблетку, яка містить 100 мг рифаксиміну протягом двох діб, показало збільшення у вісім разів концентрації Lactobacilli. Результати, повідомлені в таблиці 29, показують, що селективна дія цієї композиції рифаксиміну у формах таблеток, отриманих як у прикладах 1 та 2, сприяє колонізації Lactobacilli. Кількість Lactobacilli при візиті V4 груп B та C, та конкретно, у групі B, є переважною в порівнянні до патогенних різновидів, присутніх у пацієнтів, яких лікували рифаксиміном, тоді як це залишає меншість кількості Lactobacilli в пацієнтів, яких лікували плацебо, також у тих, хто показав видужання. Цей доказ підтримує гіпотезу, що пацієнти, яких лікували препаратами рифаксиміну можуть отримувати видужання, тоді як інші ймовірно потерпають від рецидиву. Описана композиція у вагінальних таблетках є придатною при видужанні від вагінальної інфекції, та конкретно, композиція, яка містить 25 мг рифаксиміну, застосована протягом п'яти діб, підтримує низьку концентрацію патогенних бактерій протягом, приблизно, одного місяця після кінця лікування та призводить до збільшення концентрації Lactobacilli в піхві. У прикладі 19 описано визначення профілів DGGE в жінки, яку лікували рифаксиміном, демонструючи менше число смуг, що вказує на присутність меншого числа патогенних різновидів у порівнянні з вихідними профілями. У таблиці 30 повідомлено процент жінок, які мають профілі "кластеризації", у яких цим підтверджено вищу внутрішню мінливість у жінок, яких лікували рифаксиміном у порівнянні з тими, яких лікували плацебо. Конкретно, спостережено, що лікування таблетками, які містять 25 мг рифаксиміну протягом п'яти діб має сильнішу дію на вагінальну мікробіоту, що призводить до меншої величини проценту ніж у інших груп, яких лікували. Щоб розрахувати фармакологічну дію дослідженої композиції рифаксиміну, різні групи лікування зіставляли способами, так званими "Similarity Indexes (SI)". У таблиці 31 повідомлено середні величини SI (Similarity Index), які підтверджують, що лікування рифаксиміном відновлює менший комплекс та більше фізіологічне вагінальне мікросередовище. Ще один критерій, застосований для оцінювання зразків, є так званий "Richness Index (Rl)". Цей критерій, базований на смугах кожного профілю DGGE, надає міру комплексності бактеріальної сукупності, яка є ознакою хвороби, для протистояння щодо нових патогенних різновидів. У таблиці 32 повідомлено середні величини Rl, визначені при візитах V1 та V3. Результати в таблиці 32 показують, що профілі вагінальної мікробіоти стають менш комплексними в групах, які лікували препаратами рифаксиміну в порівнянні групою, яку лікували плацебо. Згідно із заявленим винаходом розкрито фармацевтичні композиції в таблетках контрольованого вивільнення, які містять рифаксимін, придатний для лікування бактеріального вагініту з незначною системною абсорбцією, які здатні вивільнювати рифаксимін також у присутності малої кількості водних розчинів. Конкретно, описані композиції діють селективно проти фотогенних бактерій, підтримуючи та сприяючи зростанню Lactobacilli вагінальної флори. Крім того, композиції заявленого винаходу є ефективними в зменшенні фотогенних бактерій, сприянні Lactobacilli вагінальної флори тільки після єдиного добового дозування. Також тут запропоновано комплект, наприклад, комплект, який містить вагінальні таблетки, які мають ефективний уміст, який містить ефективну кількість рифаксиміну для лікування пацієнтів із вагінальними інфекціями, та інструкцію для застосування вищевказаних композицій. Повідомлено приклади щодо вагінальних таблеток, які містять різні кількості рифаксиміну та наповнювачів, способи їх отримання, дослідження на тваринах in vivo та на уражених вагінальними інфекціями жінках. Приклад 1 13 UA 111972 C2 5 10 Отримання рифаксиміну, який містять вагінальні таблетки: Композиція 1 Тверді композиції, які містять 25 мг рифаксиміну отримували способами, які охоплюють наступні етапи: a) виготовлення гранул, які містять рифаксимін, та змішування гранул у матриці, яка містить суміш дезінтегрантів; b) пресування гранул та отримання таблеток; c) покриття отриманих таблеток плівкою. Кількість рифаксиміну, яка відповідає 375 г, змішано з наповнювачами для отримання грануляту, у відповідних кількостях, які надано в таблиці 3. Наповнювачі, коповідон, гідратовану лактозу гідроксипропілметилцелюлозу та гідратовану лактозу попередньо просівали через 1,0 мм сито. Магній стеарат попередньо просівали через 0,5 сито, потім додавали до суміші в кількостях повідомлених у таблиці 3. Таблиця 3 Кількості компонентів гранули (г) Рифаксимін 375 г Коповідон (Kollidon VA 64) 84,4 г Гідратована лактоза (Таблетоза 80) 2881,8 г Магній стеарат 33,8 г Загальна маса 3375 г Компоненти 15 20 Процент (%) за масою 11,1 2,5 85,4 1,0 Компоненти розміщували до міксеру та змішували протягом 20 хвилин при 15 оберт./хвил. Потім суміш розміщували до обертального компактору при застосуванні тиску 75 бар для отримання гранул. Отриманий гранулят змішували з наступним: кальцій силікат (Реципієнт FM1000), кросповідон (Kollidon CL), гідратована лактоза (Таблетоза 80) та коповідон (Kollidon VA64), в кількостях, повідомлених в таблиці 4, попередньо просівали через 1 мм сито, застосовуючи прилад 80 I BIN-like apparatus (Bin) протягом 20 хвилин при 15 оберт./хвил. Потім додавали магній стеарат, який попередньо просівали через 0,5 мм сито, та кінцеву суміш струшували протягом трьох хвилин при 10 оберт./хвил. Кінцеву композицію вагінальних таблеток надано в таблиці 4. 25 Таблиця 4 Компоненти Гранулят рифаксиміну Кальцій силікат (Реципієнт FM1000) Кросповідон (Kollidon CL) Лактоза-моногідрат (Таблетоза 80) Коповідон (Kollidon VA64) Магній стеарат Загальна маса 30 35 Кількості компонентів (г) 3375 г грануляту 1 2250 г 540 г 11390,5 г 253,2 г 191,2 г 18000 г Процент (%) за масою 18,75 % (2,1 % рифаксиміну) 12,5 % 3,0 % 63,3 % 1,4 % 1,1 % Суміш, отриману в етапі a), пресували в машині для пресування для отримання таблеток розміру 22,8 × 10,15 мм. Таблетки покривали плівкою. Таблетки, попередньо нагріті при 45 °C, розміщували в стальну посудину, де розпилювали розчин філмогену, вищевказаний розчин формували, застосовуючи 0,22 кг Opadry II Pink, диспергований в 2,88 кг води. Opadry II Pink - порошкова суміш наступного: титан діоксид, червоний ферум оксид, жовтий ферум оксид, полівініловий спирт та поліетиленгліколь. Дисперсію філмогену розпилювали на таблетки поки середня маса таблетки відповідала 1248 мг ± 5 % (1185,6-1310,4 мг). Розпилювання робили одночасно з висушуванням таблеток. Після досягнення бажаної маси розпилювання зупиняли та продовжували висушування, контролюючи вміст води в таблетці до отримання вмісту, меншому або який дорівнював 5 %. 14 UA 111972 C2 Потім таблетки тримали в посудинах, у яких зберігали вологість, як-то пласти, зроблені із трьох білих, покритих алюмінієм шарів PVC/PE/PVDC, де нанесено шар PVDC. Кінцева композиція (композиція 1) отриманих таблеток показані в таблиці 5. Таблиця 5 Компонент Рифаксимін Магній стеарат Коповідон (Kollidon VA 64) Кросповідон (Kollidon CL) Кальцій силікат або (RxCipient FM 1000) Лактоза-моногідрат(Таблетоза 80) Покриття - Філмоген (Opadrv II pink 85F34503) Загальна маса Композиція 1 25 мг 15 мг 22,5 мг 36 мг 150 мг 951 5 мг 48 мг 1248 мг Процент (%) за масою 2,0 1,2 1,8 2,9 12,0 76,2 3,8 5 10 Отримані таблетки мають середню масу 1185,6 -1310,4 мг та твердість, приблизно 14,75 Kp. Приклад 2 Препарат вагінальних таблеток, які містять 100 мг рифаксиміну Таблетки отримували як описано в прикладі 1, та в таблиці 6 повідомлено кінцеву композицію таблеток, які містять 100 мг рифаксиміну. Таблетки отримували, виходячи із грануляту, який має таку ж композицію як композиція грануляту, у прикладі 1, таблиці 3, у яких наповнювачі змішували до наступного пресування, щоб отримувати кінцеву композицію, повідомлену в таблиці 6. Таблиця 6 Компонент Процент (%) за масою 8,0 1,2 1,8 2,9 12,0 70,2 3,8 Композиція 2 Рифаксимін Магній стеарат Коповідон (Kollidon VA 64) Кросповідон (Kollidon CL) Кальцій силікат (RxCipient FM 1000) Лактоза моногідрат (Таблетоза 80) Філмоген, покриття (Opadry II pink 85F34503) Загальна маса 100 мг 15 мг 22,5 мг 36 мг 150 мг 876,5 мг 48 мг 1248 мг 15 20 Приклад 3 Препарати вагінальних таблеток, які містять 25 мг рифаксиміну (Композиції 3-8) Композиції 3-8, яка містять 25 мг рифаксиміну, отримували згідно зі способом як описано в прикладі 1. Композицію гранул, які містять рифаксимін, зв'язувач, розріджувач та змащувач надано в таблиці 7. Таблиця 7 Компонент Рифаксимін Магній стеарат Коповідон (Kollidon VA64) Гідроксипропілметилцелюлоза (Pharmacoat 606) Лактоза моногідрат (Таблетоза) 80} 25 Гранула A (мг) 25,00 2,25 5,63 Гранула С (мг) 25,00 2,25 192,12 Гранула В (мг) 25,00 2,25 4,5 197,75 197 75 Рифаксимін, який містять гранули, які мають композиції, описані в таблиці 7, композиції A, B, C, змішано із зовнішньогранулярними наповнювачами, як описано в прикладі 1. Композиції 3-8 надано в таблиці 8. 15 UA 111972 C2 Таблиця 8 Компонент Гранулят Магній стеарат Коповідон (Kollidon VA) Кросповідон (Kollidon CL) Кальцій силікат Натрій крохмаль гліколят Пептизований крохмаль Гідроксипропілметилцелюлоза Лактоза моногідрат Філмоген, покриття Комп. Комп. Комп. Комп. Комп. Комп. (мг) (мг) (мг) (мг) (мг) (мг) Гранулят А Гранулят А Гранулят А Гранулят А Гранулят В Гранулят С (225 мг) (225 мг) (225 мг) (225 мг) (225 мг) (225 мг) 12,75 12,75 12,75 12,75 12,75 12,75 16,88 16,88 16,88 16,88 60,00 36,00 36,00 36,00 36,00 150,00 150,00 96,00 24,00 150,0 _ 16,88 776,25 30,8-43,5 759,37 30,8-43,5 885,37 30,8-43,5 849,37 30,8-43,5 885,37 30,8-43,5 759,37 30,8-43,5 Комп.= Композиція 5 10 Для композиції 7 показано за візуальним контролем стійку відсутність гомогенності порошку із присутністю великих агрегатів. Приклад 4 Визначення часу розпаду таблеток рифаксиміну; композиції 1-8 Часи розпаду таблеток із композиціями 1-8, отриманих згідно із прикладами 1, 2 та 3, отримували як описано в European Pharmacopoeia 7,0 2,9,2, ref. 01/2008:20902. Таблетки, які мають композиції 1-8, розміщували на сітку у водяній бані при 37 °C, та нижча частина таблетки була в контакті з водою. Часи розпаду таблетки оцінено візуально та, при необхідності, способами скляного бруса для перевірки втрати ступеню щільності. Аналіз повторювали для шістьох таблеток та розраховували середній час. Отримані результати надано в таблиці 9. Таблиця 9 Час розпаду Комп. 1 1'40" Комп. 2 1'35" Комп. 3 1'50” Комп. 4 5'00” Комп. 5 2'30" Комп. 6 5'30" Комп. 7 1'45" Комп. 8 5'30" 15 20 Приклад 5 Отримання ліпофільних м'яких капсул, які містять рифаксимін, та визначення вивільнення рифаксиміну Отримували м'які капсули, які містять 50 мг та 200 мг рифаксиміну, у присутності напівгліцеридів із поверхнево-активною речовиною (Suppocire BS2X) у присутності та у відсутності ксилоглюкану. Відповідні композиції мають кількості, повідомлені в таблиці 10. М'які капсули отримували плавленням напівгліцеридів при 40 °C та послідовним диспергуванням інших компонентів у розплавленій масі тригліцериду. Розплавлену масу потім розміщували в спеціальні форми та охолоджували для отримання м'яких капсул. 25 Таблиця 10 Компонент Рифаксимін Ксилоглюкан Suppocire BS2X (напівгліцериди) OV-LIP. 1 (мг) OV-LIP. 2 (мг) OV-LIP. 3 (мг) OV-LJP. 4 (мг) OV-LIP. 5 (мг) 200 200 50 50 100 30 30 2800 2770 2950 16 2720 2900 UA 111972 C2 5 М'яку капсулу кожної OV-LIP-композиції 1 - 5, надану в таблиці 10, потім розміщували в циліндрі при струшуванні, який містить 900 мл води при 37 °C, та кількість рифаксиміну вивільнено за певний час визначено спектрофотометрією та надано в таблиці 11. Експерименти повторювали в шести різних посудинах та визначали отриману середню величину. Таблиця 11 Час (хвил.) 0 5 10 20 30 40 50 60 70 80 90 100 110 120 10 OV-L1P. 1 0,0 0,8 1,6 3,4 4,1 4,3 4,8 5,8 7,2 8,4 9,4 10,2 18,6 21,1 Величини розчинення (мкг/мл) OV-LIP. OV-LIP. OV-LIP. 2 3 4 0,0 0,0 0,0 0,6 0,8 1,8 2,1 1,2 1,4 1,9 2,6 2,0 3,0 3,6 3,3 3,4 3,7 2,7 3,8 4,3 2,8 4,8 4,8 3,7 5,0 5,9 5,2 6,9 6,5 6,5 7,9 7,0 7,2 11,8 7,7 8,0 13,6 9,5 10,0 16,5 16,4 19,0 OV-LIP. 5 000 в.д. 0,20 в.д. 0,28 0,35 в.д. 0,37 в.д. в.д. в.д. в.д. в.д. в.д. Приклад 6 Отримання гідрофільних м'яких капсул, які містять рифаксимін, та визначення вивільнення рифаксиміну Отримували м'які капсули, як містять 100 мг рифаксиміну з наповнювачами та з різними кількостями цього останнього, щоб визначити їх дію на вивільнення рифаксиміну, . Шість композицій гідрофільних м'яких капсул (OV-IDR 1-6) та пов'язаних композицій надано в таблиці 12. 15 Таблиця 12 Компонент Рифаксимін Транскутол Гліцерин Ксилоглюкан PEG 4000 Вода 20 OV-IDR. 1 100 400 400 150 1950 OV-IDR. 2 100 400 400 2100 Композиція (мг) OV-IDR. OV-IDR. 3 4 100 100 250 250 400 150 150 1950 1950 300 400 OV-IDR. 5 100 800 150 1950 OV-IDR. 6 25 400 400 150 2025 Гідрофільну м'яку капсулу з OV-IDR-композиціями 1 - 6 розміщували в циліндрі, який містить 90 мл води, та кількість рифаксиміну визначали спектрофотометричним аналізом. Тест повторювали на шести м'яких капсулах. Кількості рифаксиміну, пов'язаного з композиціями 5-9, вивільнено за час, наданий у таблиці 13. 17 UA 111972 C2 Таблиця 13 Час (хвил.) 0 5 10 20 30 40 50 60 70 80 90 100 110 120 5 10 OV-IDR. 1 000 22,30 37,85 56,92 66,39 72,30 76,26 78,81 79,29 77,23 72,52 65,62 60,35 54,76 OV-IDR. 2 0,00 29,41 57,99 105,81 124,15 127,45 102,55 59,28 35,07 24,69 19,70 16,98 15,31 14,09 Величини розчинення (мкг/мл) OV-IDR. OV-IDR. OV-IDR. 3 4 5 0,00 0,00 0,00 3,16 1,35 25,72 6,33 2,64 49,15 12,07 3,38 91,60 15,23 3,62 112,72 16,63 3,72 115,00 17,16 3,72 101,45 17,27 3,76 78,08 17,32 3,77 53,12 17,29 3,76 35,28 15,93 3,77 16,12 15,86 3,77 12,42 20,74 3,77 10,35 23,73 4,87 0,00 OV-IDR. 6 0,00 в.д. в.д. 0,38 0,64 в.д. 0,60 0,70 в.д. в.д. в.д. в.д. в.д. в.д. Приклад 7 Порівняння вивільнення рифаксиміну з вагінальних таблеток, гідрофільних та ліпофільних м'яких капсул. Ліпофільну м'яку капсулу, як містить 100 мг рифаксиміну, отриманого згідно із прикладом 5, та гідрофільну м'яку капсулу, отриману згідно із прикладом 6, які містять, відповідно, 25 та 100 мг рифаксиміну, та таблетку, отриману згідно із прикладом 2, яка містить 100 мг рифаксиміну, розміщували в ємність, яка містить 10 мл води в середовищі, нагрітому до 37 °C. Кількість вивільненого рифаксиміну визначали при постійних інтервалах часу. Експеримент повторювали тричі для кожної композиції. Рифаксимін, вивільнений дослідженими композиціями, визначали в часі способами УФспектрофотометрії, та концентрації рифаксиміну надано в таблиці 14. Таблиця 14 Час (хвил.) 0 15 30 45 60 OV-IDR. 1 0,00 0,56 0,56 0,63 0,82 Величини розчинення (мг/мл) OV-IDR. OV-LIP. 6 5 0,00 0,00 0,38 0,21 0,64 0,28 0,61 0,40 0,70 0,37 Таблетки Композиція 2 0,00 0,06 0,07 0,11 0,05 15 20 25 OV-IDR, 1: отриманий як у прикладі 6 та, який містить 100 мг рифаксиміну; OV-IDR, 6: отриманий як у прикладі 6 та, який містить 25 мг рифаксиміну; OV-LIP, 5: отриманий як у прикладі 2 та, який містить 100 мг рифаксиміну. Приклад 8 Дослідження біонакопичення рифаксиміну в кролів інтравагінальним шляхом при застосовуванні у вагінальних таблетках та м'яких капсулах. Було дванадцять самиць кролів білих специфічних вільних від патогену (SPF) (SPF) з Нової Зеландії, які не народжували та не були вагітними (6 у кожній групі), яких лікували вагінальними таблетками та м'якими капсулами, які містять 12,5 мг рифаксиміну, отриманого як у прикладі 1 та 4, у єдиній дозі. Протягом лікування не спостерігали локальних клінічних ознак, реакції на лікування, зміни маси тіла у тварин, яких лікували в порівнянні з контрольною групою. Гепаринізовану кров відбирали з маргінальної вени вуха перед дозуванням та, приблизно, через 1, 2, 4, 6, та 24 години після застосування. Концентрацію рифаксиміну в плазмі визначали обґрунтованим способом РХ-МС/МС із LLOQ - 0,5 нг/мл. 18 UA 111972 C2 5 10 Фармакокінетичний аналіз робили згідно зі звичайним некомпартментним аналізом, та потім розраховували фармакокінетичні параметри: Cмакс.: максимальна концентрація визначена в плазмі t макс.: час, потрібний для досягнення максимальної концентрації плазми AUC(o-t останнє) - площа, обмежена кривою концентрації плазми стосовно часу від t=0 (перед дозуванням) до останнього часу (остання виміряна кількісна концентрація) AUC(нескінчен.): площа, обмежена кривою концентрації плазми стосовно часу від t=0 до t=нескінченність. У таблиці 15 повідомлено фармакокінетичні параметри після застосування вагінальних таблеток та м'яких капсул, які містять 12,5 мг рифаксиміну. Таблиця 15 Препарати М'які капсули Таблетки 15 20 25 30 35 40 45 50 tмакс. (годин) 2 1 Фармакокінетичні параметри Cмакс. AUC (0-t ост.) (нг/мл) (нг/мл) 6,06±5,38 26,74±28,31 1,48±0,8 2,12±1,08 AUC(нескінчен.} (нг/мл.г) 20,57 (n=2) N/C Приклад 9 Визначення ефективності композицій рифаксиміну в м'яких капсулах та вагінальних таблетках у моделі інфікованих тварин. Ефективність вагінальних композицій у таблетках та м'які капсулах, які містять рифаксимін, розраховано в моделі на тваринах при бактеріальному інфікуванні кроля. Модель вагінальної інфекції індукували щепленням Gardnerella vaginalis, виділеної в жінок, уражених бактеріальним вагінітом. Бактеріальні штами клітин червоних кров'яних тілець корови вирощували в агарі при 37 °C при додаванні доповнення DIFCO-C та тримали під контрольованою атмосферою 5 % CО2 протягом 24-48 годин. Для створення моделі тваринної інфекції застосовували кролів Нової Зеландії (Oryctolagus cunicolis), які мають масу 2 - 3 кг. Тварин анестезували внутрішньом'язовою ін'єкцією сумішшю кетаміну (30 мг/кг) та ксилазину (2 мг/кг) при часі щеплення та при часі застосування рифаксиміну в таблетках або м'яких капсулах. Перед інфікуванням тварин обробляли 10 % розчином 1 мл енрофлоксацину для зменшення ендогенного Lactobacilli та полегшення зростання патогенного засобу. Інфекцію індукували щепленням до піхви тварини 1 мл стерильного фізіологічного розчину, який містить 106-7 UFC (Unit Forming Colony) vaginalis Gardnerella, застосовуючи тефлоновий катетер 2224G. Присутність трихомоніазу G. у тварин перевіряли перед щепленням та через 24 та 48 годин після щеплення. Тварин щеплювали двічі та тричі при інтервалах часу три доби. Через 14 діб робили останнє щеплення всім тваринам 1 мл 10 % розчину енрофлоксацину для перевірки чутливості моделі до антибіотиків. Отже, догляд при одужанні від інфекції є підтвердженням, що цю модель можна застосовувати для оцінювання ефективності антибіотиків, застосованих інтравагінальним шляхом. Присутність трихомоніазу G. перевіряли вагінальним буфером 1, 2, 4, через 10 - 14 діб після останнього щеплення нанесенням вагінальних буферів у чашку с агаровим середовищем клітин червоних кров'яних тілець корови з доповненням DIFCO-C та зростанням при 37 °C протягом 48 годин. Присутність G-трихомоніази перевіряли способами морфологічної ідентифікації під мікроскопом (1000x) та з фарбуванням по Граму. Тварин зі стійкою інфекцію потім лікували таблетками та м'якими капсулами, які містять рифаксимін у кількостях 1,5, 3, 6 та 12,5 мг. Композиції у формі таблеток, які містять рифаксимін, для досліджень тварин отримували згідно із прикладом 1, де пропорцію наповнювачів пропорційно знижено, щоб отримувати композиції з різними кількостями рифаксиміну. М'які капсули для досліджень тварин отримували згідно із прикладом 5, композиція OV-2, де пропорцію наповнювачів пропорційно знижено, щоб отримувати композиції з різними кількостями Рифаксимін, який містить вагінальна м'яка капсула або таблетка, уводили в піхву, та, у випадку вагінальних таблеток, 1 мл фізіологічного розчин при 37 °C уводили для полегшення розпаду таблетки. Протягом лікування не спостерігали несприятливого випадку. 19 UA 111972 C2 5 Через три та сім діб після кінця лікування рифаксиміном розраховували присутність Gardnerella vaginalis способами з вагінальними буферами, як попередньо описано. Вагінальні буфери вважали позитивними, якщо нараховували 10 або більше колоній, та присутність смердючих вагінальних виділень, що було клінічною ознакою наявності інфекції. Ефективність вагінальних таблеток, отриманих як у прикладі 1 із різними дозами рифаксиміну, зображеною згідно із процентом викоренення інфекції в кроля, спричиненої Gardnerella, надано в таблиці 16. Таблиця 16 Число тварин 6 8 8 8 12 10 Викоренення (%.) Після 3 діб Після 7 діб 0 0 88 100 63 100 88 100 100 100 Доза рифаксиміну (мг) 0 1,5 3 6 12,5 Ефективність вагінальних м'яких капсул, отриманих як у прикладі 4, із різними дозами рифаксиміну при викорененні в кролів стійкої інфекції, спричиненої Gardnerella spp., надано як процент викоренення, та це надано в таблиці 17. Таблиця 17 Число тварин 6 8 8 8 12 15 20 25 30 35 40 Викоренення (%) Після 3 діб Після 7 діб 0 0 100 100 88 100 88 100 100 100 Доза рифаксиміну (мг) 0 1,5 3 6 12,5 Аналізи кролів, яких лікували рифаксиміном, був негативним протягом 7 діб після кінця лікування, тоді як кролі, яких не лікували (контрольні кролі), залишалися інфікованими. Після лікування також зникали всі клінічні симптоми. Приклад 10 Визначення системної абсорбції, локальної та системної терпимості фармакокінетичним дослідженням (клінічне випробування, Фаза I) вагінальних таблеток рифаксиміну. Фаза I, визначали на здорових волонтёрах, щоб оцінити можливу системну абсорбцію та локальну та системну терпимість вагінальних таблеток рифаксиміну після єдиного застосування вагінальним шляхом. Єдину дозу вагінальних таблеток рифаксиміну 100 мг, отриману як описано в прикладі 8, застосовували до 24 здорових волонтёрів, які мали вік 18 - 50 років. Зразки крові відбирали в кожного суб'єкта (S) перед застосуванням (час 0) та після застосування, тобто після 30 хвилин, 1, 1,5, 2, 3, 4, 6, 8, 10, 12, 16 та 24 годин після застосування єдиної дози вагінальних таблеток рифаксиміну 100 мг. Зразки аналізували рідинною хроматографією, яка діяла з детектором мас-спектрометрії, з нижчою межею дискретизації (LLOQ) концентрації рифаксиміну 0,5 нг/мл. Усі концентрації рифаксиміну плазми, при різних часах, в аналізованих суб'єктів були в межі аналітичного визначення. Приклад 11 Визначення терпимості після застосування вагінальних таблеток рифаксиміну У дослідженні Фази I на 24 здорових волонтёрах також розраховано локальну та системну терпимість після єдиного застосування вагінальної таблетки, яка містить 100 мг рифаксиміну. Відсутній суб'єкт, який показав свербіж або біль у різні часи після застосування, отже, підтверджено хорошу локальну терпимість. Тільки у волонтёра виявлено легкий вагінальний біль, мимовільно завершений пізніше через кілька годин. Для визначення системної терпимості спостерігали головні показники, як-то ECG, біохімічні параметри в крові та сечі та шкідливі наслідки, повідомлені волонтёрами. Відсутність виявлених 20 UA 111972 C2 5 10 15 20 25 30 35 системних концентрацій рифаксиміну та системних симптомів означають хорошу терпимість до вагінальної таблетки, яка містить 100 мг рифаксиміну. Приклад 12 Лікування бактеріального вагініту вагінальними таблетками рифаксиміну У прикладі описано клінічне випробування Фази II, зроблене на 114 пацієнтах, уражених бактеріальним вагінітом, не вагітних, віком 18 - 50 років. Діагноз бактеріального вагініту базували на критерії Amsel, де, принаймні, трьом критеріям із чотирьох слід бути позитивними, та на мітці Nugent, де мітка вище чотирьох указує на присутність патогенної вагінальної бактерії. Цілями випробування були визначення видужання від бактеріального вагініту згідно із критеріями Amsel (індекс Amsel < 3) та згідно з міткою Nugent (індекс Nugent 3 точок мітки Nugent при візиті V3 Група A Рифаксимін 1 таблетка 100 мг × 5 діб Застосована доза Пацієнти зі зменшеною міткою Nugent > 3 точок (%) 5 10 В Рифаксимін 1 таблетка 25 мг × 5 діб С Рифаксимін 1 таблетка 100 мг × 2 доби 52,4 65,2 36,9 D Плацебо 18-2 Приклад 14 Визначення кількості пацієнтів, які показують зниження більше або, яке дорівнює 3 точкам при візиті в кінці лікування (V3) у порівнянні з візитом до лікування (V1) Пацієнти, яких реєстрували в клінічних випробуваннях та які належить до груп лікування A, B, C та D, як описано в прикладі 12, показали при візиті до лікування величини мітки Nugent 7 10. У таблиці 25 повідомлено число та процент пацієнтів, які при візиті в кінці лікування показали зменшення мітки Nugent вище або, яке дорівнює 5 точкам. Таблиця 25 Зменшення > 5 точок мітки Nugent при візиті V3 Група A Рифаксимін 1 таблетка 100 мг × 5 діб Застосована доза Пацієнти зі зменшеною міткою Nugent > 5 точок (%) 15 20 В Рифаксимін 1 таблетка 25 мг × 5 діб С Рифаксимін 1 таблетка 100 мг × 2 доби 28,6 47,8 26,3 D Плацебо 0,1 Приклад 15 Визначення кількості пацієнтів, які показують зниження більше або, яке дорівнює 8 точкам при візиті в кінці лікування (V3) у порівнянні з візитом до лікування (V1) Пацієнти, яких реєстрували в клінічних випробуваннях та які належить до груп лікування A, B, C та D, як описано в прикладі 12, показали при візиті до лікування величини мітки Nugent 7 10. У таблиці 26 повідомлено число та процент пацієнтів, які при візиті в кінці лікування показали зменшення мітки Nugent вище або, яке дорівнює 8 точкам. Таблиця 26 Зменшення > 8 точок мітки Nugent при візиті V3 Група Застосована доза Пацієнти зі зменшеною міткою Nugent > 8 точок (%) 25 A Рифаксимін 1 таблетка 100 мг × 5 діб В Рифаксимін 1 таблетка 25 мг × 5 діб С Рифаксимін 1 таблетка 100 мг × 2 доби 14,29 17,39 15,79 D Плацебо 0 Приклад 16 Визначення пацієнтів, які не реагували на лікування вагінальними таблетками, які містять рифаксимін Пацієнти, яких реєстрували в клінічних випробуваннях та які належить до груп лікування A, B, C та D, як описано в прикладі 12, показали при візиті до лікування величини мітки Nugent 7 10. 24 UA 111972 C2 У таблиці 27 повідомлено число та процент пацієнтів, які при візиті в кінці лікування не реагували на лікування при реєстрації зменшення мітки Nugent на 0 точок, або показали погіршення хвороби, отже, реєструючи збільшення мітки Nugent. Таблиця 27 Зменшення на 0 точок мітки Nugent при візиті V3 Група A Рифаксимін 1 таблетка 100 мг × 5 діб Застосована доза Пацієнти зі зменшеною міткою Nugent 0 точок (%) В Рифаксимін 1 таблетка 25 мг × 5 діб С Рифаксимін 1 таблетка 100 мг × 2 доби 9,52 17,39 36,84 D Плацебо 68,18 5 10 15 20 Приклад 17 Визначення композиції вагінальної мікробіоти способом кількісного реального часу PCT, при візитах V1 та V3 Протягом клінічного випробування, описаного в прикладі 12, збирали зразки вагінальної чистки, та композицію вагінальної мікробіоти визначали способами кількісного реального часу PCR. З реальним часом PCR зразки ДНК підсилювали гендером-та/або різновидамиспецифічними праймерами, чиєю мішенню є бактеріальний ген 16S рРНК або область 16S-23 S рРНК. Конкретно, специфічні проби застосовували для Lactobacillus gender, для Gardnerella vaginalis, для Atopobium, для Prevotella та для Veillonella, оскільки вони є представниками головних бактеріальних груп, які потерпають від модифікацій при бактеріальному вагініті. У таблиці 28 повідомлено величини реального часу PCR, які стосуються бактеріальних родів та різновидів, виміряних у вагінальних чистках жінок, які належить до різних груп лікування, зображених як загальна мішень ДНК нг/ геномна ДНК мкг для мікробних різновидів, тестованих для кожної групи при візиті V3 у порівнянні з візитом V1. Таблиця 28 Група Доза Візит (і) А Рифаксимін 1 таблетка 100 мг × 5 діб V1 Рифаксимін 1 таблетка 25 мг × 5 діб V1 Рифаксимін 1 таблетка 100 мг × 2 доби V1 Плацебо V1 (і) V3 (іі) B (іі) V3 (ііі) С D (iii) V3 (іv) Мішень ДНК/геномна вагінальна ДНК (нг/мкг) (середнє ± SD) Gardnerella Laсtobacillus Atopobium Prevotella Veillonella vaginalis 1,683Е+01 3,492E+01 9,З07Е+01 1,880E+01 4,128E-02 ± ± ± ± ± 1,695Е+00 7,994Е+00 7,086E+00 3,182E+00 1,341E-02 2,009E+01 2,356E+01 6,146E+01 1,220E+01 7,807Е-03 ± ± ± ± ± 2,885E+00 3,386Е+00 3,623E+00 1,324E+00 4,069E-03 1,006E+01 1,194E+02 1,082E+02 1,847Е+01 3,492E-02 ± ± ± ± ± 6,863Е-01 1,393E+01 1,388E+01 1,308Е+00 1,118E-02 3,378Е+01 6,626Е+01 4,880E+01 3,712E+00 1,761E-02 ± ± ± ± ± 4,434E+00 1,312E+01 1,444E+01 8,556E-01 8,451Е-03 1,266E+01 6,674E+01 1,704E+02 1,791E+01 2,214E-01 ± ± ± ± ± 1,378E+00 9,774E+00 2,164E+01 2,802E+00 5,992E-02 2,536Е+01 2,944E+01 5,999Е+01 7,248E+00 5,642Е-03 ± ± ± ± ± 2,110E+00 6,199Е+00 1,260E+01 2,176E+00 2,001E-03 1,488E+01 1,272E+02 1,210E+02 1,729E+01 1,878E-02 ± ± ± ± ± 1,482E+00 1,406E+01 1,943E+01 3,359E+00 3,581E-03 25 UA 111972 C2 Таблиця 28 Група Доза Візит (іv) V3 5 10 15 20 Мішень ДНК/геномна вагінальна ДНК (нг/мкг) (середнє ± SD) Gardnerella Laсtobacillus Atopobium Prevotella Veillonella vaginalis 9,040Е+00 6,674Е+01 5,671E+01 1,292Е+01 4,826Е-02 ± ± ± ± ± 1,039E+00 8,032E+00 1,015E+01 2,537E+00 1,600E-02 (і) 27 пацієнтів; (ii) 25 пацієнтів; (iii) 25 пацієнтів; (iv) 25 пацієнтів Результати зіставлення величин при візиті V1 до величин при візиті V4, показують, що кількості всіх патогенних різновидів були зниженими, тоді як при такому ж зіставленні Lactobacilli була збільшеною. Конкретно, для Групи B ці відмінності були статистично видатними, за винятком Veillonella. Приклад 18 Визначення композиції вагінальної мікробіоти кількісним реальним часом PCR при візити V1 та V4 після лікування вагінальними таблетками рифаксиміну. Композицію вагінальної мікробіоти визначали способами кількісного реального часу PCR пацієнтів, підтримуючи їх видужання при візиті V4 через 30-40 діб після кінця лікування, та зразки ДНК, підсилені гендером-та/або різновидами-специфічними праймерами, розраховували способом реальний час PCR. Конкретно, застосовували специфічні проби для Lactobacillus gender, для Gardnerella vaginalis, для Atopobium, для Prevotella та для Veillonella, оскільки вони уособлюють головні бактеріальні групи, які потерпають від модифікацій при бактеріальному вагініті. У таблиці 29 повідомлено величини реального часу PCR, щодо мішені бактеріальних родів та визначених кількостей різновидів у вагінальному промиванні жінок, які належить до різних груп лікування, відображені як повна мішень ДНК нг/геномна ДНК мкг для мікробних різновидів, тестованих для кожної групи при візиті V4, коли в порівнянні з величини спостереженими при візиті V1 в усіх пацієнтів, яких лікували. Таблиця 29 Група Доза Візит V1 А Рифаксимін 1 таблетка 100 мг × 5 діб (і) (іі) V4 (ііі) В Рифаксимін 1 таблетка 25 мг × 5 діб V1 (iv) V4 (v) С Рифаксимін 1 таблетка 100 мг × 2 доби V1 (vi) V4 Мішень ДНК/геномна або вагінальна ДНК (нг/мкг) середнє ± SD) Gardnerella Lactobacillus Atopobium Prevotella Veillonella vaginalis 1,683E+01 3,492E+01 9,307E+01 1,880E+01 4,128E-02 ± ± ± ± ± 1,695E+00 7,994E+00 7,086Е+00 3,182E+00 1,341E-02 2,130E+01 3,067E+00 5,348E+00 4,296E-02 0,000E+00 ± ± ± ± ± 2,152E+00 2,904E-01 5,819E-01 1,232E-02 0,000E+00 1,006E+01 1,194E+02 1,082E+02 1,847E+01 3,492E-02 ± ± ± ± ± 6,863E-01 1,393E+01 1,388E+01 1,308E+00 1,118E-02 3,957Е+01 1,757E+01 2,825E+01 2,345E+00 0,000E+00 ± ± ± ± ± 9,400E+00 2,908E+00 2,719E+00 2,348E-01 0,000E+00 1,266E+01 6,674E+01 1,704E+02 1,791E+01 2,214E-01 ± ± ± ± ± 1,378E+00 9,774Е+00 2,164E+01 2,802E+00 5,992E-02 8,959E+00 7,509E+01 1,399Е+02 5,400E+01 2,748E-01 ± ± ± ± ± 1,725E+00 1,295E+01 1,708E+01 1,003E+01 1,020E-01 26 UA 111972 C2 Таблиця 29 Група Доза Візит (vii) V1 D Плацебо (viii) V4 5 10 15 20 Мішень ДНК/геномна або вагінальна ДНК (нг/мкг) середнє ± SD) Gardnerella Lactobacillus Atopobium Prevotella Veillonella vaginalis 1,488Е+01 1 272E+02 1,210E+02 1,729Е+01 1,878E-02 ± ± ± ± ± 1,482E+00 1,406E+01 1,943E+01 3,359E+00 3,581E-03 1,408E+01 6,095E+01 2,537E+01 1,444E-01 0,000E+00 ± ± ± ± ± 9,778E-01 4,117E+00 1,323E+00 3,709Е-02 0,000E+00 (i), 27 пацієнтів; (ii) 6 пацієнтів; (iii) 25 пацієнтів; (iv) 12 пацієнтів; (v) 25 пацієнтів; (vi) 9 пацієнтів; (vii) 9 пацієнтів; (viii) 4 пацієнтів. Приклад 19 Визначення композиції вагінальної мікробіоти з PCR-DGGE після лікування препаратами рифаксиміну Протягом клінічного випробування брали зразки вагінальних промивань, та композицію вагінальної мікробіоти визначали способом PCR-DGGE, дозволяючи ідентифікацію різних бактеріальних ДНК електрофоретичним способом, та ампліфікацію ДНК із універсальними праймерами для бактеріальної області 16S рРНК. Результатом цього способу була послідовність видимих смуг, названих кластерами, де кожна з них є характерною для ДНК бактеріальних різновидів, присутніх у розглянутому зразку. Аналіз кластерів профілів DGGE зразків, зроблений при застосуванні програмного забезпечення FPQuest software (Bio-Rad), надає інформацію стосовно подібності двох зразків. У конкретному випадку, де видужання означало зниження патогенних різновидів, позитивним є те, що зразок пацієнта після лікування є зовсім відмінним від зразку того ж пацієнта до лікування. Аналіз робили з вагінальними зразками при візити V1, V3 та V4 для чотирьох груп пацієнтів A, B, C та D, яких лікували. У таблиці 30 повідомлено процент пацієнтів з "кластеризованими" профілями. Таблиця 30 Процент пацієнтів із кластеризованими профілями Група Застосована доза V1 стосовно V3 (%) V1 стосовно V3 стосовно V4 (%) 25 30 35 A Рифаксимін 1 таблетка 100 мг × 5 діб 37 В Рифаксимін 1 таблетка 25 мг × 5 діб 24 С Рифаксимін 1 таблетка 100 мг × 2 доби 28 Плацебо 0 0 11 50 D 56 Результати, повідомлені в таблиці 30 показують, що існує висока варіабельність у бактеріальній популяції, ідентифікованій при V1, V3 та V4 у пацієнтів, яких лікували препаратами рифаксиміну, отже, це вказує, що вагінальна мікробіота була значно модифікована фармакологічною дією рифаксиміну при концентраціях, вивільнених застосованими препаратами. Конкретно, виявляється, що препарат, застосований до пацієнтів групи B є найбільш ефективним при візиті V3. Дію препаратів рифаксиміну далі підтвердили після візиту V4, де, конкретно, у групах A та B бактеріальну популяцію повністю модифіковано. Для того щоб оцінити фармакологічну дію досліджуваних препаратів рифаксиміну, різні групи лікування зіставляли через так званий індекс подібності Similarity Indexes (SI). Аналіз полягав в оцінюванні подібності електрофоретичних профілів, розрахованих на базі коефіцієнта кореляції Pearson. У дослідженому випадку SI показує процент подібності між двох або більше профілів DGGE, які належить одній і тій же жінці при різних візитах. 27 UA 111972 C2 Таблиця 31 Група Застосована доза V1-V3 V1-V4 V3-V4 V1-V3-V4 5 A Рифаксимін 1 таблетка 100 мг × 5 діб 61,6 52,1 66,8 50,8 Індекс подібності В Рифаксимін 1 таблетка 25 мг × 5 діб 48,4 40,0 62,1 36,4 С Рифаксимін 1 таблетка 100 мг × 2 доби 54,0 47,1 42,8 37,6 D Плацебо 75,4 57,6 58,7 56,7 Результати в таблиці 31 показують, що при порівнянні V1-V3 індекс подібності груп, яких лікували препаратами рифаксиміну, значно відрізняється від групи плацебо. Ще одним прийнятим критерієм визначення зразків є так званий індекс Richness Index (Rl). Цей критерій, базований на смугах кожного профілю DGGE, надає міру складності бактеріальної популяції, яка є ознакою хвороби у випадку нових патогенних різновидів. У таблиці 32 повідомлено середні величини Rl, виміряні при візитах V1 та V3. Таблиця 32 Група Застосована доза V1 V3 A Рифаксимін 1 таблетка 100 мг × 5 діб 13,5 10,9 Індекс Richness В Рифаксимін 1 таблетка 25 мг × 5 діб 14,0 10,7 С Рифаксимін 1 таблетка 100 мг × 2 доби 15,4 12,2 D Плацебо 13,3 13,9 10 Результати в таблиці 32 показують, що профілі вагінальної мікробіоти ставали менш комплексними в групах, яких лікували препаратами рифаксиміну в порівнянні із групою, яку лікували плацебо. 15 20 25 30 35 40 ФОРМУЛА ВИНАХОДУ 1. Вагінальна таблетка, яка містить: (a) гранули рифаксиміну, які містять: рифаксимін у кількості 2,5-200 мг, один або більше внутрішньогранулярних наповнювачів, які охоплюють принаймні один зв'язувач; та (b) два або більше зовнішньогранулярних наповнювачів, які охоплюють принаймні два дезінтегранти, що являють собою суміш кросповідону та кальцію силікату. 2. Вагінальна таблетка за п. 1, яка покрита плівкою. 3. Вагінальна таблетка за п. 1, де рифаксимін міститься в кількості від 2,5 до 100 мг. 4. Вагінальна таблетка за п. 1, де дезінтегрант вибрано в групи, яка складається з наступного: натрію крохмаль гліколят, пептизований крохмаль, співполімер полівінілпіролідону (PPPV або кросповідон), натрійкарбоксиметилметилцелюлоза (натрійкармелоза), поперечно зв'язана карбоксиметилцелюлоза (натрійкроскармелоза), силікати лужних та лужноземельних металів (наприклад кальцію силікат) та їх суміш. 5. Вагінальна таблетка за п. 1, де внутрішньогранулярні наповнювачі додатково охоплюють принаймні один розріджувач та змащувач; зовнішньогранулярні наповнювачі додатково охоплюють принаймні один зв'язувач, розріджувач та змащувач, та необов'язково консерванти, біоадгезивні, буферувальні, антисептичні засоби та природний ароматизатор. 6. Вагінальна таблетка за п. 1, де розріджувач, вибраний з групи, що складається з наступного: целюлоза, мікрокристалічна целюлоза, гідроксипропілметилцелюлоза, кальцію фосфат, крохмаль, каолін, двогідратний кальцію сульфат, кальцію карбонат, безводна або гідратована лактоза, сахароза, манітол, полісахариди, глюкани, ксилоглюкан та їх суміш; зв'язувач вибрано із групи, яка містить наступне: кукурудзяний крохмаль, пептизований крохмаль, гуміарабік, лактоза, мальтодекстрин, співполімер 1 вініл-2-піролідон та вінілацетат (коповідон), сахароза та їх суміші; 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical compositions comprising rifaximin, processes for their preparation and their use in the treatment of vaginal infections
Автори англійськоюViscomi, Giuseppe, Claudio, Maffei, Paola, Lauro, Vittoria, Calanni, Fiorella, Vitali, Beatrice, Cruciani, Federica
Автори російськоюВискоми Джузеппе Клаудио, Маффеи Паола, Лауро Витториа, Каланни Фиорелла, Витали Беатриче, Кручани Федерика
МПК / Мітки
МПК: A61K 9/00, A61K 9/20, A61K 9/02
Мітки: рифаксимін, спосіб, застосування, вагінальна, містить, виготовлення, вагінальних, таблетка, лікування, яка, інфекцій
Код посилання
<a href="https://ua.patents.su/31-111972-vaginalna-tabletka-yaka-mistit-rifaksimin-sposib-vigotovlennya-ta-zastosuvannya-dlya-likuvannya-vaginalnikh-infekcijj.html" target="_blank" rel="follow" title="База патентів України">Вагінальна таблетка, яка містить рифаксимін, спосіб її виготовлення та застосування для лікування вагінальних інфекцій</a>
Попередній патент: Вибір єдиних кандидатів режиму злиття і адаптивного режиму прогнозування вектора руху
Наступний патент: Провід для повітряних електромереж
Випадковий патент: Склад антимікробного конвеєрного мастила, що містить діамін ацетат, спосіб змащування і зниження концентрації мікроорганізмів на несучій поверхні конвеєра