Інгібітори 11-бета-гідроксистероїдної дегідрогенази 1, придатні для лікування цукрового діабету, ожиріння і дисліпідемії
Формула / Реферат
1. Сполука, представлена формулою І
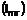 І,
І,
або її фармацевтично прийнятна сіль або сольват, де:
А і В разом являють собою (а) С1-4-алкілен, необов'язково заміщений 1-3 галогеновими групами і 1-2 Rа групами, де Rа являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10-ар-С1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами, або (b) С2-5-алкандіїл, так що вони утворюють з атомом вуглецю, до якого приєднані, 3-6-членний цикл, причому вказаний цикл необов'язково містить 1 подвійний зв'язок або 1-2 гетероатоми, вибрані з О, S і N, і вказаний 3-6-членний цикл є необов'язково заміщеним С1-4-алкіленом, оксо, етилендіокси або пропілендіокси і необов'язково додатково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4-алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6-алкіл-ОС(O)-, С2-4-алкенілу, С2-4-алкінілу, С1-3-алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси, фенілу, CN, OH, D, NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище;
кожний R1 являє собою Н або незалежно вибраний з групи, що включає ОН, галоген, С1-10-алкіл, С1-6-алкокси і С6-10-арил, причому вказані С1-10-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогеновими, ОН, ОС1-3алкільною, фенільною або нафтильною групами, і вказані феніл і нафтил є необов'язково заміщеними 1-3 замісниками, вибраними з галогену, ОСН3, ОСF3, СН3, СF3 і фенілу, де вказаний феніл є необов'язково заміщеним 1-3 галогеновими групами,
або дві R1 групи разом утворюють конденсований С5-6-алкільний або арильний цикл, який може бути необов'язково заміщеним 1-2 ОН або Ra групами, де Ra приймає значення, визначені вище;
R2 і R3 взяті разом або окремо;
коли взяті разом, R2 і R3 являють собою (а) С3-8-алкандіїл, що утворює конденсований 5-10-членний неароматичний цикл, який необов'язково містить 1-2 подвійних зв'язки і необов'язково містить 1-2 гетероатоми, вибрані з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу, причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-6 атомами галогенів і 1-4 групами, вибраними з ОН, С1-3-алкілу, ОС1-3-алкілу, галоген-С1-3-алкілу, галоген-С1-3-алкокси і фенілу, і вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, С1-3-алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеними 1-3 галогеновими групами;
коли взяті окремо,
R2 вибраний з групи, що включає (а) С1-14-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3-алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, ОСF3, СН3 і СF3, і вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогеновими, ОН або Ra групами, де Ra приймає значення, визначені вище; (с) С2-10-алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (d) СН2СO2Н; (е) СН2СO2-С1-6-алкіл; (f) CH2C(O)NHRa, де Ra приймає значення, визначені вище; (g) NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище;
і R3 вибраний з групи, що включає С1-14-алкіл, С2-10-алкеніл, SС1-6-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SС1-6-алкілу є необов'язково заміщеними (а) R; (b) 1-6 атомами галогенів і (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSО2- і (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і
R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С1-4-алкілу, С1-4-алкіл-S(O)х-, де х приймає значення, визначені вище, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSO2-, (С1-4-алкіл)2NSO2-, CN, ОН, ОС1-4-алкілу, і вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 атомами галогенів і 1 групою, вибраною з ОН і ОС1-3-алкілу.
2. Сполука за п. 1, де А і В взяті разом і являють собою С2-5-алкандіїл, так що з атомом вуглецю, до якого приєднані, вони утворюють 3-6-членний цикл, причому вказаний цикл необов'язково містить 1 подвійний зв'язок або 1-2 гетероатоми, вибрані з О, S і N, де вказаний 3-6-членний цикл є необов'язково заміщеним С1-4-алкіленом, оксо, етилендіокси або пропілендіокси і необов'язково додатково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4-алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6-алкіл-ОС(О)-, С2-4-алкенілу, С2-4-алкінілу, С1-3-алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси, фенілу, CN, OH, D, NH2, NHRa і N(Ra)2, де Ra являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10-ар-С1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами.
3. Сполука за п. 2, де А і В взяті разом і являють собою С2-4-членну алкандіїльну групу, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-5-членний цикл, необов'язково заміщений 1-2 групами, вибраними з галогену С1-4-алкілу, галоген-С1-4-алкілу, С1-3-алкокси, С1-3-алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси і фенілу.
4. Сполука за п. 3, де А і В взяті разом і являють собою С2-4-алкандіїльну групу, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-5-членний цикл, причому вказаний цикл є незаміщеним або заміщений 1-2 галогеновими групами.
5. Сполука за п. 4, де 1-2 галогенові групи являють собою атоми фтору.
6. Сполука за п. 1, де дві R1 групи являють собою Н і один R1 вибраний з групи, що включає ОН, галоген, С1-10-алкіл, С1-6-алкокси і С6-10-арил, причому вказані С1-10-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогеновою, ОН, ОС1-3алкільною, фенільною або нафтильною групами, і вказані феніл і нафтил є необов'язково заміщеними 1-3 замісниками, вибраними з галогену, ОСН3, ОСF3, СН3, СF3 і фенілу, де вказаний феніл є необов'язково заміщеним 1-3 галогеновими групами.
7. Сполука за п. 1, де одна R1 група являє собою Н і дві інші R1 групи вибрані з групи, що включає ОН, галоген, С1-10-алкіл і С1-6-алкокси, причому вказаний С1-10-алкіл і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогеновими групами.
8. Сполука за п. 7, де дві R1 групи являють собою галоген або метил.
9. Сполука за п. 1, де R2 взятий окремо від R3 і вибраний з групи, що включає (а) С1-14-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3-алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, ОСF3, СН3 і СF3, і вказана С1-3 алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогенами, ОН або Ra групами; (с) С2-10-алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (d) СН2СО2Н; (е) СН2СО2С1-6-алкіл; (f) CH2C(O)NHRa і (g) NH2, NHRa і N(Ra)2, і
Ra являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10-ар-С1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами.
10. Сполука за п. 1, де R2 взятий окремо від R3 і являє собою С1-14-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3-алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, ОСF3, СН3 і СF3, і алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами.
11. Сполука за п. 9, де R2 взятий окремо від R3 і являє собою метил або циклопропіл.
12. Сполука за п. 1, де R3 взятий окремо від R2 і вибраний з групи, що включає С1-14-алкіл, С2-10-алкеніл, SС1-6-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SС1-6-алкілу є необов'язково заміщеними (а) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSO2- і (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і
R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С1-4-алкілу, С1-4-алкіл-S(O)х-, де х приймає значення, визначені вище, С1-4-алкіл-SО2NН-, Н2NSО2-, С1-4-алкіл-NHSO2-, (С1-4-aлкіл)2NSO2-, CN, ОН, ОС1-4-алкілу, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 галогенами і 1 групою, вибраною з ОН і ОС1-3-алкілу.
13. Сполука за п. 12, де R3 взятий окремо від R2 і вибраний з групи, що включає С1-14-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані групи є необов'язково заміщеними (а) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SO2NH-, H2NSO2-, С1-4-алкіл-NHSO2-, (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами.
14. Сполука за п. 12, де R3 взятий окремо і вибраний з групи, що включає циклопропіл, необов'язково заміщений метилом або фенілом; феніл, необов'язково заміщений галогеном, ОН, ОСН3 або ОСF3; гетероарил, вибраний з бензімідазолілу, індолілу, бензофуранілу і дигідробензофуранілу, причому вказані гетероарильні групи є необов'язково заміщеними (а) R; (b) 1-6 галогеновими групами або (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SO2NH-, H2NSO2-, С1-4-алкіл-NНSO2-, (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і
R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С1-4-алкілу, ОН, ОС1-4-алкілу, і вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу.
15. Сполука за п. 1, де R2 і R3 взяті разом і являють собою (а) С3-8-алкандіїл, що утворює конденсований 5-10-членний неароматичний цикл, який необов'язково містить 1 подвійний зв'язок і необов'язково містить 1 гетероатом, вибраний з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу,
причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-3 атомами галогенів і 1-2 групами, вибраними з ОН, С1-3-алкілу, ОС1-3-алкілу, галоген-С1-3-алкілу, галоген-С1-3-алкокси і фенілу, і вказаний феніл є необов'язково заміщеним 1-2 групами, незалежно вибраними з галогену, С1-3-алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеними 1-3 галогеновими групами.
16. Сполука за п. 1, де R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 галогеновими групами і 1-2 групами, вибраними з С1-4-алкілу, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSO2-, (С1-4-алкіл)2NSО2-, CN, ОН і ОС1-4-алкілу, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-3 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу.
17. Сполука, вибрана з групи, що включає
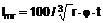 ,
, 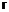 ,
,
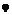 ,
, 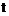 ,
,
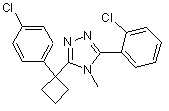 ,
, 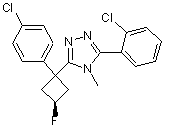 ,
,
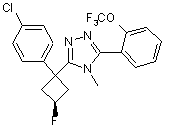 та
та 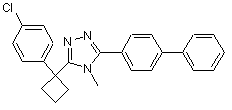 ,
,
або її фармацевтично прийнятна сіль або сольват.
18. Сполука за п. 17
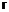
або її фармацевтично прийнятна сіль або сольват.
19. Сполука за п. 17 структурної формули:
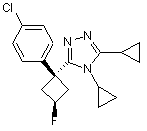
або її фармацевтично прийнятна сіль або сольват.
20. Сполука за п. 17 структурної формули:
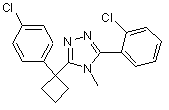
або її фармацевтично прийнятна сіль або сольват.
21. Сполука за п. 17 структурної формули:
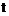
або її фармацевтично прийнятна сіль або сольват.
22. Фармацевтична композиція, що містить сполуку за п. 1 у поєднанні з фармацевтично прийнятним носієм.
23. Спосіб лікування гіперглікемії, цукрового діабету або інсулінорезистентності у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту ефективної кількості сполуки за п. 1.
24. Спосіб лікування інсуліннезалежного цукрового діабету у пацієнта-ссавця, який потребує такого лікування, що включає введення пацієнту сполуки за п. 1 у кількості, ефективній для лікування цукрового діабету.
25. Спосіб лікування ожиріння у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, ефективній для лікування ожиріння.
26. Спосіб лікування синдрому Х у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, яка ефективна для лікування синдрому X.
27. Спосіб лікування ліпідного розладу, вибраного з групи, що включає дисліпідемію, гіперліпідемію, гіпертригліцеридемію, гіперхолестеринемію, низький вміст HDL і високий вміст LDL у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, яка ефективна для лікування вказаного ліпідного розладу.
28. Спосіб лікування атеросклерозу у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, ефективній для лікування атеросклерозу.
Текст
1. Сполука, представлена формулою І 2 UA 1 (13) ДО ПАТЕНТУ НА ВИНАХІД C2 ОПИС (19) ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ 3 необов'язково додатково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6алкіл-ОС(O)-, С2-4-алкенілу, С2-4-алкінілу, С1-3алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси, фенілу, CN, OH, D, NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище; кожний R1 являє собою Н або незалежно вибраний з групи, що включає ОН, галоген, С1-10алкіл, С1-6-алкокси і С6-10-арил, причому вказані С110-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогеновими, ОН, ОС1-3алкільною, фенільною або нафтильною групами, і вказані феніл і нафтил є необов'язково заміщеними 1-3 замісниками, вибраними з галогену, ОСН3, ОСF3, СН3, СF3 і фенілу, де вказаний феніл є необов'язково заміщеним 1-3 галогеновими групами, або дві R1 групи разом утворюють конденсований С5-6-алкільний або арильний цикл, який може бути необов'язково заміщеним 1-2 ОН або Ra групами, де Ra приймає значення, визначені вище; R2 і R3 взяті разом або окремо; коли взяті разом, R2 і R3 являють собою (а) С3-8алкандіїл, що утворює конденсований 5-10членний неароматичний цикл, який необов'язково містить 1-2 подвійних зв'язки і необов'язково містить 1-2 гетероатоми, вибрані з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу, причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-6 атомами галогенів і 1-4 групами, вибраними з ОН, С1-3-алкілу, ОС1-3-алкілу, галоген-С1-3-алкілу, галоген-С1-3-алкокси і фенілу, і вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, С1-3-алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3-алкільна частина ОС1-3алкілу є необов'язково заміщеними 1-3 галогеновими групами; коли взяті окремо, R2 вибраний з групи, що включає (а) С1-14алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, ОСF3, СН3 і СF3, і вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогеновими, ОН або Ra групами, де Ra приймає значення, визначені вище; (с) С2-10алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 13 галогеновими групами; (d) СН2СO2Н; (е) СН2СO2С1-6-алкіл; (f) CH2C(O)NHRa, де Ra приймає значення, визначені вище; (g) NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище; і R3 вибраний з групи, що включає С1-14алкіл, С2-10-алкеніл, SС1-6-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SС1-6-алкілу є необов'язково заміщеними 81417 4 (а) R; (b) 1-6 атомами галогенів і (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSО2- і (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С14-алкілу, С1-4-алкіл-S(O)х-, де х приймає значення, визначені вище, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4алкіл-NНSO2-, (С1-4-алкіл)2NSO2-, CN, ОН, ОС1-4алкілу, і вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 атомами галогенів і 1 групою, вибраною з ОН і ОС1-3-алкілу. 2. Сполука за п. 1, де А і В взяті разом і являють собою С2-5-алкандіїл, так що з атомом вуглецю, до якого приєднані, вони утворюють 3-6членний цикл, причому вказаний цикл необов'язково містить 1 подвійний зв'язок або 1-2 гетероатоми, вибрані з О, S і N, де вказаний 3-6членний цикл є необов'язково заміщеним С1-4алкіленом, оксо, етилендіокси або пропілендіокси і необов'язково додатково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6алкіл-ОС(О)-, С2-4-алкенілу, С2-4-алкінілу, С1-3алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси, фенілу, CN, OH, D, NH2, NHRa і N(Ra)2, де Ra являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10-ар-С1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами. 3. Сполука за п. 2, де А і В взяті разом і являють собою С2-4-членну алкандіїльну групу, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-5-членний цикл, необов'язково заміщений 1-2 групами,вибраними з галогену С1-4алкілу, галоген-С1-4-алкілу, С1-3-алкокси, С1-3алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси і фенілу. 4. Сполука за п. 3, де А і В взяті разом і являють собою С2-4-алкандіїльну групу, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-5-членний цикл, причому вказаний цикл є незаміщеним або заміщений 1-2 галогеновими групами. 5. Сполука за п. 4, де 1-2 галогенові групи являють собою атоми фтору. 6. Сполука за п. 1, де дві R1 групи являють собою Н і один R1 вибраний з групи, що включає ОН, галоген, С1-10-алкіл, С1-6-алкокси і С6-10-арил, причому вказані С1-10-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогеновою, ОН, ОС1-3алкільною, фенільною або нафтильною групами, і вказані феніл і нафтил є необов'язково заміщеними 1-3 замісниками, вибраними з галогену, ОСН3, ОСF3, СН3, СF3 і фенілу, де вказаний феніл є необов'язково заміщеним 1-3 галогеновими групами. 7. Сполука за п. 1, де одна R1 група являє собою Н і дві інші R1 групи вибрані з групи, що включає ОН, галоген, С1-10-алкіл і С1-6-алкокси, 5 причому вказаний С1-10-алкіл і алкільна частина С1є необов'язково заміщеними 1-3 6-алкокси галогеновими групами. 8. Сполука за п. 7, де дві R1 групи являють собою галоген або метил. 9. Сполука за п. 1, де R2 взятий окремо від 3 R і вибраний з групи, що включає (а) С1-14-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, ОСF3, СН3 і СF3, і вказана С1-3 алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогенами, ОН або Ra групами; (с) С2-10-алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 13 галогеновими групами; (d) СН2СО2Н; (е) СН2СО2С1-6-алкіл; (f) CH2C(O)NHRa і (g) NH2, NHRa і N(Ra)2, і Ra являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10-ар-С16-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами. 10. Сполука за п. 1, де R2 взятий окремо від R3 і являє собою С1-14-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3-алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, ОСF3, СН3 і СF3, і алкільна частина ОС1-3-алкілу є необов'язково заміщеною 13 галогеновими групами. 11. Сполука за п. 9, де R2 взятий окремо 3 від R і являє собою метил або циклопропіл. 12. Сполука за п. 1, де R3 взятий окремо 2 від R і вибраний з групи, що включає С1-14-алкіл, С2-10-алкеніл, SС1-6-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SС1-6алкілу є необов'язково заміщеними (а) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSO2- і (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С14-алкілу, С1-4-алкіл-S(O)х-, де х приймає значення, визначені вище, С1-4-алкіл-SО2NН-, Н2NSО2-, С1-4алкіл-NHSO2-, (С1-4-aлкіл)2NSO2-, CN, ОН, ОС1-4алкілу, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 галогенами і 1 групою, вибраною з ОН і ОС1-3-алкілу. 13. Сполука за п. 12, де R3 взятий окремо 2 від R і вибраний з групи, що включає С1-14-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані групи є необов'язково заміщеними (а) R; 81417 6 (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SO2NH-, H2NSO2-, С1-4-алкіл-NHSO2-, (С1-4-алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами. 14. Сполука за п. 12, де R3 взятий окремо і вибраний з групи, що включає циклопропіл, необов'язково заміщений метилом або фенілом; феніл, необов'язково заміщений галогеном, ОН, ОСН3 або ОСF3; гетероарил, вибраний з бензімідазолілу, індолілу, бензофуранілу і дигідробензофуранілу, причому вказані гетероарильні групи є необов'язково заміщеними (а) R; (b) 1-6 галогеновими групами або (с) 1-3 групами, вибраними з ОН, NH2, NНС1-4-алкілу, N(С1-4-алкіл)2, С1-4-алкілу, ОС1-4алкілу, CN, С1-4алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкілSO2NH-, H2NSO2-, С1-4-алкіл-NНSO2-, (С1-4алкіл)2NSO2-, причому вказаний С1-4-алкіл і С1-4алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С14-алкілу, ОН, ОС1-4-алкілу, і вказаний С1-4-алкіл і С14-алкільні частини вказаних груп є необов'язково заміщеними 1-5 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу. 15. Сполука за п. 1, де R2 і R3 взяті разом і являють собою (а) С3-8-алкандіїл, що утворює конденсований 5-10-членний неароматичний цикл, який необов'язково містить 1 подвійний зв'язок і необов'язково містить 1 гетероатом, вибраний з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу, причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-3 атомами галогенів і 1-2 групами, вибраними з ОН, С1-3-алкілу, ОС1-3-алкілу, галогенС1-3-алкілу, галоген-С1-3-алкокси і фенілу, і вказаний феніл є необов'язково заміщеним 1-2 групами, незалежно вибраними з галогену, С1-3алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3алкільна частина ОС1-3-алкілу є необов'язково заміщеними 1-3 галогеновими групами. 16. Сполука за п. 1, де R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 галогеновими групами і 1-2 групами, вибраними з С1-4-алкілу, С1-4-алкіл-S(O)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкіл-NНSO2-, (С1-4-алкіл)2NSО2-, CN, ОН і ОС1-4-алкілу, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-3 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу. 17. Сполука, вибрана з групи, що включає 7 81417 Cl 8 Cl N N N N F3CO N N F F , та Cl Cl N N N N N N , або її фармацевтично прийнятна сіль або сольват. 18. Сполука за п. 17 Cl , Cl N N N N N N F , або її фармацевтично прийнятна сіль або сольват. 19. Сполука за п. 17 структурної формули: Cl Cl N N N N N N F , Cl F або її фармацевтично прийнятна сіль або сольват. 20. Сполука за п. 17 структурної формули: Cl Cl N N Cl N N N N , Cl Cl N або її фармацевтично прийнятна сіль або сольват. 21. Сполука за п. 17 структурної формули: Cl N N N F , N N F або її фармацевтично прийнятна сіль або сольват. 9 81417 10 22. Фармацевтична композиція, що містить сполуку за п. 1 у поєднанні з фармацевтично прийнятним носієм. 23. Спосіб лікування гіперглікемії, цукрового діабету або інсулінорезистентності у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту ефективної кількості сполуки за п. 1. 24. Спосіб лікування інсуліннезалежного цукрового діабету у пацієнта-ссавця, який потребує такого лікування, що включає введення пацієнту сполуки за п. 1 у кількості, ефективній для лікування цукрового діабету. 25. Спосіб лікування ожиріння у пацієнтассавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, ефективній для лікування ожиріння. 26. Спосіб лікування синдрому Х у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, яка ефективна для лікування синдрому X. 27. Спосіб лікування ліпідного розладу, вибраного з групи, що включає дисліпідемію, гіперліпідемію, гіпертригліцеридемію, гіперхолестеринемію, низький вміст HDL і високий вміст LDL у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, яка ефективна для лікування вказаного ліпідного розладу. 28. Спосіб лікування атеросклерозу у пацієнтассавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки за п. 1 у кількості, ефективній для лікування атеросклерозу. Даний винахід відноситься до інгібіторів ферменту 11-бета-гідроксистероїдної дегідрогенази І типу (11β-HSD-1 або HSD-1) і способів лікування, що використовують такі сполуки. Сполуки корисні для лікування цукрового діабету, такого як інсуліннезалежний цукровий діабет 2 типу (NIDDM), інсулінорезистентності, ожиріння, ліпідних розладів та інших захворювань і станів. Цукровий діабет обумовлений множиною факторів і найбільш просто характеризується підвищеними рівнями вмісту глюкози у плазмі (гіперглікемія) натщесерце. Звичайно розрізняють дві форми цукрового діабету: цукровий діабет 1 типу або інсулінзалежний діабет (IDDM), при якому у пацієнтів виробляється невелика кількість інсуліну або зовсім не виробляється інсулінгормон, що регулює споживання глюкози, і цукровий діабет 2 типу або інсуліннезалежний цукровий діабет (NIDDM), при якому інсулін у пацієнтів виробляється і навіть проявляється гіперінсулінемія (тобто рівні вмісту інсуліну у плазмі дорівнюють і навіть є підвищеними у порівнянні з суб'єктами, які не страждають діабетом), і у той же час спостерігається гіперглікемія. Цукровий діабет 1 типу звичайно лікується екзогенним введенням інсуліну за допомогою ін'єкції. Однак у пацієнтів з цукровим діабетом 2 типу часто розвивається "інсулінорезистентність", так що дія інсуліну у стимулюванні метаболізму глюкози і ліпідів в основних чутливих до інсуліну тканинах, а саме, м'язових тканинах, тканинах печінки і жирових тканинах, слабшає. У пацієнтів, які є інсулінорезистеними, але не хворі цукровим діабетом, спостерігаються підвищені рівні вмісту інсуліну, які компенсують їх інсулінорезистентність, тому рівні вмісту глюкози у плазмі не підвищені. У пацієнтів з NIDDM рівні вмісту інсуліну у плазмі, навіть коли вони підвищені, є недостатніми для подолання вираженої інсулінорезистентності, що приводить до гіперглікемії. Інсулінорезистентність обумовлена, передусім, порушенням рецепторного зв'язування, яке ще не повністю вивчене. Несприйнятливість до інсуліну приводить до недостатньої активації поглинання глюкози, зниженого окислення глюкози і накопичення глікогену у м'язі, неадекватної інсулінової репресії ліполізу у жировій тканині та неадекватного продукування і секреції глюкози печінкою. Тривала або неконтрольована гіперглікемія, яка має місце у хворих цукровим діабетом, пов'язана з підвищеною захворюваністю і передчасною смертністю. Аномальний гомеостаз глюкози також пов'язаний як прямо, так і опосередковано, з ожирінням, гіпертензією і порушеннями у ліпідному, ліпопротеїновому і аполіпопротеїновому метаболізмі. Хворі цукровим діабетом 2 типу є пацієнтами з підвищеним ризиком серцево-судинних ускладнень, таких як атеросклероз, коронарна хвороба серця, удар, захворювання периферичних судин, гіпертензія нефропатія, нейропатія і ретинопатія. Отже, терапевтичний контроль гомеостазу глюкози, метаболізму ліпідів, ожиріння і гіпертензії є особливо важливим для клінічного контролю і лікування цукрового діабету. Велика кількість пацієнтів з інсулінорезистентністю, у яких однак не спостерігається розвитку цукрового діабету 2 типу, також мають ризик розвитку симптомів, що називаються "синдромом X" або "метаболічним синдромом". Синдром X характеризується інсулінорезистентністю у поєднанні з патологічним ожирінням, гіперінсулінемією, високим кров'яним тиском, низьким рівнем HDL і високим рівнем VLDL. Такі пацієнти, не залежно від наявності або відсутності розвитку явного цукрового діабету, є пацієнтами з підвищеним ризиком розвитку серцево-судинних ускладнень, перерахованих вище. Лікування цукрового діабету 2 типу звичайно включає фізичне навантаження і дієту. Підвищення рівня вмісту інсуліну у плазмі 11 введенням сульфонілсечовин (наприклад, толбутаміду і гліпізиду) або меглітиніду, які стимулюють секрецію панкреатичними β-клітинами більшої кип кості інсуліну, і/або ін'єкцією інсуліну, коли сульфонілсечовини або меглітинід неефективні, може приводити до того, що концентрації інсуліну стають досить високими, щоб стимулювати інсулінорезистентні тканини. Однак у даному випадку можуть бути одержані небезпечно низькі рівні вмісту глюкози у плазмі і у кінцевому результаті може мати місце підвищений рівень інсулінорезистентності. Бігуаніди підвищують чутливість до інсуліну, приводячи до деякої корекції гіперглікемії. Однак багато бігуанідів, наприклад фенформін і метформін, викликають молочний ацидоз, нудоту і діарею. Глітазони (тобто 5-бензилтіазолідин-2,4-діони) складають більш новий клас сполук, які можуть полегшувати гіперглікемію та інші симптоми діабету 2 типу. Дані фармацевтичні засоби по суті підвищують чутливість до інсуліну у м'язовій, печінковій і жировій тканині, приводячи до часткової або повної корекції підвищених рівнів вмісту глюкози у плазмі по суті не викликаючи гіперглікемії. Глітазони, які у наш час надходять у продаж, є агоністами рецептора, що активується проліфератором піроксисоми (PPAR) гаммапідтипу. Вважається, що PPAR-g агонізм відповідальний за підвищення сенсибілізації до інсуліну, яка спостерігається при використанні глітазонів. Більш нові PPAR агоністи, які розроблені для лікування діабету 2 типу і/або дисліпідемії, є агоністами одного або декількох PPAR альфа-, гамма- і дельта-підтипів. У наш час зберігається потреба у нових способах лікування цукрового діабету і пов'язаних з ним станів. Даний винахід задовольняє ці та інші потреби. Даний винахід відноситься до сполуки, представленої формулою І або її фармацевтично прийнятної солі або сольватів, де: А і В можуть бути взяті окремо або разом, коли взяті окремо, А являє собою галоген, С1-6-алкіл, ОС1-6-алкіл або феніл, причому вказані алкіл, феніл або алкільна частина ОС1-6-алкілу є необов'язково заміщеними 1-3 галогеновими групами; і В являє собою Н, галоген, С1-6-алкіл, -ОС1-6алкіл, -SС1-6-алкіл, С2-6-алкеніл, феніл або нафтил, причому вказані алкіл, алкеніл-феніл, нафтил і алкільні частини -ОС1-6-алкілу і -SС1-6-алкілу є необов'язково заміщеними 1-3 групами, вибраними з галогену, ОН, СН3О, CF3 і OCF3; коли взяті разом, А і В разом являють собою (а) С1-4-алкілен, необов'язково заміщений 1-3 галогеновими групами і 1-2 Ra групами, де Ra являє собою С1-3 81417 12 алкіл, ОС1-3-алкіл, С6-10-арилС1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами, або (b) С2-5-алкандіїл, так що вони утворюють з атомом вуглецю, до якого приєднані, 3-6-членний цикл, причому вказаний цикл необов'язково містить 1 подвійний зв'язок або 1-2 гетероатоми, вибрані з О, S і N, і вказаний 3-6членний цикл є необов'язково заміщеним С1-4алкіленом, оксо, етилендіокси або пропілендіокси і необов'язково додатково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6алкіл-ОС(О)-, С2-4-алкенілу, С2-4-алкінілу, С1-3алкоксі-С1-3-алкілу. С1-3-алкокси-С1-3-алкокси, фенілу, CN, OH D, NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище; кожний R1 являє собою Η або незалежно вибраний з групи, що включає ОН, галоген, С1-10алкіл, С1-6-алкокси і С6-10-арил, причому вказані С110-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогенами, ОН, ОС1-3-алкільною, фенільною або нафтильною групами, і вказані феніл і нафтил є необов'язково заміщеними 1-3 замісниками, незалежно вибраними з галогену, ОСН3, OCF3, CH3, CF3 і фенілу, де вказаний феніл необов'язково заміщений 1-3 галогеновими групами, або дві R1 групи разом являють собою конденсований С5-6-алкільний або арильний цикл, який може бути необов'язково заміщеним 1-2 ОН або Ra групами, де Ra приймає значення, визначені вище; R2 і R3 взяті разом або окремо; коли взяті разом, R2 і R3 являють собою (а) С38-алкандіїл, що утворює конденсований 5-10членний неароматичний цикл, який необов'язково містить 1-2 подвійних зв'язки і необов'язково містить 1-2 гетероатоми, вибрані з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу, причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-6 атомами галогенів і 1-4 групами, вибраними з ОН, С1-3-алкілу, ОС С1-3-алкілу, галоген-С1-3-алкілу, галоген-С1-3-алкокси і фенілу, і вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, С1-3-алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3-алкільна частина ОС1-3алкілу є необов'язково заміщеними 1-3 галогеновими групами; коли взяті окремо, R2 вибраний з групи, що включає (а) С1-14алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, OCF3, CH3 і CF3, і вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогенами, ОН або Ra групами, де Ra приймає значення, визначені вище; (с) С2-10алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна 13 частина ОС1-3-алкілу є необов'язково заміщеною 13 галогеновими групами; (d) СН2СО2Н; (e) СН2СО2С1-6-алкіл; (f) CH2C(O)NHRa, де Ra приймає значення, визначені вище; (g) NH2; NHRa і N(Ra)2, де Ra приймає значення, визначені вище; і R3 вибраний з групи, що включає С1-4-алкіл, С2-10-алкеніл, SC1-6-алкіл, С6-10-арил, гетероцикліл і гетероарил, причому вказані алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SC1-6алкілу є необов'язково заміщеними (a) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NС1-4-алкілу, групи N(С1-4-алкіл)2, С1-4алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(O)x-, де x дорівнює 0, 1 або 2, C1-4-алкіл-SO2NH-, H2NSO2-, С1-4-алкіл-NHSO2 і (С1-4-алкіл)2NSО2-, причому вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, С14-алкілу, С1-4-алкіл-S(О)х-, де x приймає значення, визначені вище, C1-4-алкіл-SO2NH-, H2NSO2-, C1-4алкіл-NHSO2-, (С1-4-алкіл)2NSО2-, CN, ОН, ОС1-4алкілу, і вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 галогенами і 1 групою, вибраною з ОН і ОС1-3алкілу. Даний винахідвідноситься до сполуки, представленої формулою І: або її фармацевтично прийнятної солі або сольвату, де: А і В можуть бути взяті окремо або разом; коли взяті окремо, А являє собою галоген, С1-6-алкіл, ОС1-6-алкіл або феніл, причому вказані алкіл, феніл і алкільна частина ОС1-6-алкілу є необов'язково заміщеними 1-3 галогеновими групами; і В являє собою Н, галоген, С1-6-алкіл, -ОС1-6алкіл, -SС1-6-алкіл, С2-6-алкеніл, феніл або нафтил, причому вказані алкіл, алкеніл, феніл, нафтил і алкільні частини -ОС1-6-алкілу і -SС1-6-алкілу є необов'язково заміщеними 1-3 групами, вибраними з галогену, ОН, СН3О, CF3 і OCF3; і коли взяті разом, А і В разом являють собою (а) С1-4-алкілен, необов'язково заміщений 1-3 галогеновими групами і 1-2 Ra групами, де Ra являє собою С1-3алкіл, ОС1-3-алкіл, С6-10-ар-С1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами, або (b) С2-5-алкандіїл, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-6-членний цикл, причому вказаний цикл необов'язково містить 1 подвійний зв'язок або 1-2 гетероатоми, вибрані з О, S і N, і вказаний 3-6членний цикл є необов'язково заміщеним С1-4алкіленом, оксо, етилендіокси або пропілендіокси і необов'язково додатково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4 81417 14 алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6алкіл-ОС(О)-, С2-4-алкенілу, С2-4-алкінілу, С1-3алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси, фенілу, CN, OH, D, NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище; кожний R1 являє собою Η або незалежно вибраний з групи, що включає ОН, галоген, С1-10алкіл, С1-6-алкокси і С6-10-арил, причому вказані С110-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогенами, ОН, ОС1-3-алкільними, фенільними або нафтильними групами, і вказані феніл і нафтил є необов'язково заміщеними 1-3 замісниками, незалежно вибраними з галогену, ОСН3, OCF3, СН3, CF3 і фенілу, де вказаний феніл є необов'язково заміщеним 1-3 галогеновими групами, або дві R1 групи разом утворюють конденсований С5-6-алкільний або арильний цикл, який може бути необов'язково заміщеним 1-2 ОН або Ra групами, де Ra приймає значення, визначені вище; R2 і R3 взяті разом або окремо; коли взяті разом, R2 і R3 являють собою (а) С38-алкандіїл, що утворює конденсований 5-10членний неароматичний цикл, що необов'язково містить 1-2 подвійних зв'язки і необов'язково містить 1-2 гетероатоми, вибрані з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу, причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-6 атомами галогенів і 1-4 групами, вибраними з ОН, С1-3-алкілу, ОС1-3-алкілу, галоген-С1-3-алкілу, галоген-С1-3-алкокси і фенілу, і вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, С1-3-алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3-алкільна частина ОС1-3алкілу є необов'язково заміщеними 1-3 галогеновими групами; коли взяті окремо, R2 вибраний з групи, що включає: (а) С1-4алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3алкілу і фенілу, причому вказаний феніл необов'язково заміщений 1-4 групами, незалежно вибраними з галогену, ОСН3, OCF3, CH3 і CF3, і вказана С1-3-алкільна частина OС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогенами, ОН або Ra групами, де Ra приймає значення, визначені вище; (с) С2-10алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна частина ОС1-3-алкілу необов'язково заміщена 1-3 галогеновими групами; (d) CH2CO2H; (e) CH2CO2C1-6-алкіл; (f) CH2C(O)NHRa, де Ra приймає значення, визначені вище; (g) NH2, NHRa і N(Ra)2, де Ra приймає значення, визначені вище; і R3 вибраний з групи, що включає С1-14-алкіл, С2-10-алкеніл, SС1-6-алкіл, С6-10-арил, гетероцикліл і гетероарил, Причому вказані алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SС1-6алкілу є необов'язково заміщеними (a) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними 15 з ОН, NH2, NНСI-4-алкілу, N(C1-4-алкіл)2, С1-4-алкілу, ОС1-4-алкілу, CN, С1-4-алкіл-S(О)х-, де х дорівнює 0, 1 або 2, С1-4-алкіл-SО2NН-, H2NSO2-, С1-4-алкілNHSO2 і (С1-4-алкіл)2NSО2-, причому вказаний С1-4алкіл і С1-4-алкільні частини вказаних груп необов'язково заміщені фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група необов'язково заміщена 1-4 групами, вибраними з галогену, С1-4алкілу, С1-4-алкіл-С(О)Х-, де x приймає значення, визначені вище, С1-4-алкіл-SO2NH-, H2NSO2-; С1-4алкіл-NHSO2-, (С1-4-алкіл)2NSО2-, CN, ОН, ОС1-4алкілу, і вказаний С1-4-алкіл і С1-4-алкільні частини вказаних груп необов'язково заміщені 1-5 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу. У даному описі застосовні наступні визначення. Термін "Ас" означає ацетил, тобто групу СН3С(О)-. Термін "алкіл", а також префікс "алк" в інших групах, таких як алкокси і алканоїл, означає вуглецеві ланцюги, які можуть бути лінійними або розгалуженими, або їх поєднання, якщо вуглецевий ланцюг не визначений інакше. Приклади алкільних груп включають метил, етил, пропіл, ізопропіл, бутил, втор- і трет-бутил, пентил, гексил, гептил, октил, ноніл і т.п. Коли дозволяє вказана кількість атомів вуглецю, наприклад для С3-С10, термін "алкіл" включає також циклоалкільні групи і поєднання лінійних або розгалужених алкільних ланцюгів з циклоалкільними структурами. Коли кількість атомів вуглецю не вказана, мається на увазі С1-6. Термін "алкеніл" означає вуглецеві ланцюги, які містять, щонайменше, один вуглецьвуглецевий подвійний зв'язок і які можуть бути лінійними або розгалуженими, або їх поєднання, якщо вуглецевий ланцюг не визначений інакше. Приклади алкенілу включають вініл, аліл, ізопропеніл, пентеніл, гексеніл, гептеніл, 1пропеніл, 2-бутеніл, 2-метил-2-бутеніл і т.п. Коли вказана кількість атомів вуглецю дозволяє, наприклад для С5-С10, термін "алкеніл" включає також циклоалкенільні групи і поєднання лінійних, розгалужених і циклічних структур. Коли кількість атомів вуглецю не вказана, мається на увазі С2-6. Термін "алкініл" означає вуглецеві ланцюги", які містять, щонайменше, один вуглецьвуглецевий потрійний зв'язок і які можуть бути лінійними або розгалуженими або являти собою їх поєднання. Приклади алкінілу включають етиніл, пропаргіл, 3-метил-1-пентиніл, 2-гептиніл і т.п. Термін "алкандіїл" відноситься до вуглецевих ланцюгів, які є біфункціональними, такими як -СН2, -(СН2)2-, -(СН2)3- і т.п. Алкандіїльні групи є лінійними або розгалуженими, якщо не вказано інше. Для порівняння, алкільні групи є монофункціональними. Термін "алкілен" у даному описі відноситься до атома вуглецю або вуглецевого ланцюга, який приєднаний через подвійний зв'язок. Термін "циклоалкіл" відноситься до підгрупи алкілу і означає насичений карбоцикл, що містить 81417 16 вказану кількість атомів вуглецю. Приклади циклоалкілу включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і т.п. Циклоалкільна група звичайно є моноциклічною, якщо не вказано інше. Циклоалкільні групи є насиченими, якщо не вказано інше. Термін "арил" означає ароматичну моно- або поліциклічну систему, що містить у кільці атоми вуглецю. Переважними арилами є ароматичні моноциклічні або біциклічні 6-10-членні циклічні системи. Феніл і нафтил є переважними арилами. Найбільш переважним арилом є феніл. Терміни "гетероцикл" і "гетероцикліл" відносяться до насичених або ненасичених неароматичних циклів або циклічних систем, які містять, щонайменше, один гетероатом, вибраний з О, S і N, і додатково включають атом сірки в окислених формах, SO і SO2. Приклади гетероциклів включають тетрагідрофуран (ТГФ), дигідрофуран, 1,4-діоксан, морфолін, 1,4-дитіан, піперазин, піперидин, 1,3-діоксолан, імідазолідин, імідазолін, піролін, піролідин, тетрагідропіран, дигідропіран, оксатіолан, дитіолан, 1,3-діоксан, 1,3-дитіан, оксатіан, тіоморфолін і т.п. Термін "гетероарил" означає ароматичний або частково ароматичний гетероцикл, який містить у циклі, щонайменше, один гетероатом, вибраний з О, S і N (включаючи SO). Таким чином, гетероарили включають гетероарили, конденсовані з іншими видами циклів, такими як арили, циклоалкіли і гетероцикли, які є неароматичними. Приклади гетероарильних груп включають піроліл, ізЬксазоліл, ізотіазоліл, піразоліл, піридил, оксазоліл, оксадіазоліл, тіадіазоліл, тіазоліл, імідазоліл, триазоліл, тетразоліл, фурил, триазиніл, тієніл, піримідил, бензизоксазоліл, бензоксазоліл, бензотіазоліл, бензотіадіазоліл, дигідробензофураніл, індолініл, піридазиніл, індазоліл, ізоіндоліл, дигідробензотієніл, індолізиніл, хінолізиніл, цинолініл, фталазиніл, хіназолініл, нафтиридиніл, карбазоліл, бензодіоксоліл, хіноксалініл, пуриніл, фуразаніл, ізобензилфураніл, бензімідазоліл, бензофураніл, бензотієніл (включаючи S-оксид), хіноліл, індоліл, ізохіноліл, дибензофураніл, нафтиридил і т.п. Гетероциклільні і гетероарильні групи включають цикли і циклічні системи, що містять від 3 до 15 атомів, які утворюють 1-3 цикли. Термін "галоген" відноситься до фтору, хлору, брому і йоду. Хлор і фтор звичайно є переважними. Фтор є найбільш переважним, коли галогени заміщують алкільну або алкокси групу (наприклад, CF3O і CF3CH2O). Термін "фармацевтична композиція" означає препарат, що включає активний(і) інгредієнт(и) і носій, а також будь-який продукт, який утвориться у результаті, безпосередньо або опосередковано, поєднання, комплексоутворення або агрегації будь-яких двох або декількох інгредієнтів або внаслідок реакції дисоціації або реакції іншого типу одного або декількох інгредієнтів. Відповідно, фармацевтичні композиції даного винаходу включають композиції, одержані змішуванням 17 сполуки або сполук даного винаходу і фармацевтично прийнятного носія. Сполуки формули І можуть містити один або декілька асиметричних центрів і, отже, можуть існувати у вигляді рацематів або рацемічних сумішей, індивідуальних енантіомерів, діастереомерних сумішей та індивідуальних діастереомерів. Всі ці ізомерні форми включені у галузь даного винаходу. Деякі сполуки, описані у даному винаході, містять подвійні олефінові зв'язки. У галузь даного винаходу включені як Е, так і Ζ геометричні ізомери у чистій формі, а також у вигляді суміші. Деякі сполуки, описані у даному винаході, можуть існувати у вигляді таутомерів, які мають різні точки приєднання водню, що супроводжується зміщенням одного або декількох подвійних зв'язків. Наприклад, кетон і його енольна форма є кето-енольними таутомерами. Винахід включає як окремі таутомери, так і їх суміші. Якщо необхідно, рацемічні суміші сполук формули І можуть бути розділені з виділенням окремих енантіомерів. Розділення може проводитися способами, добре відомими у даній галузі техніки, такими як поєднання рацемічної суміші сполук формули І з енантіомерно чистою сполукою з утворенням діастереомерної суміші, яка потім піддається розділенню на окремі діастереомери стандартними методами, такими як фракційна кристалізація або хроматографія. Реакція поєднання часто є реакцією одержання солей з використанням енантіомерної чистої кислоти або основи. Діастереомерні похідні після цього можуть бути перетворені у, по суті, чисті енантіомери відщепленням приєднаного хірального залишку від діастереомерної сполуки. Рацемічна суміш сполук формули І також може розділятися безпосередньо хроматографічними методами з використанням хіральних нерухомих фаз, і ці методи добре відомі у даній галузі техніки. Альтернативно, енантіомери сполук загальної формули І можуть бути одержані стереоселективним синтезом з використанням оптично чистих вихідних речовин або реагентів. Один аспект даного винаходу, який представляє особливий інтерес, відноситься до сполуки формули І, де А і В взяті разом і являють собою С2-5-алкандіїл, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-6членний цикл, причому вказаний цикл необов'язково містить 1 подвійний зв'язок або 1-2 гетероатоми, вибрані з О, S і N, і вказаний 3-6членний цикл є необов'язково заміщеним С1-4алкіленом, оксо, етилендіокси або пропілендіокси і додатково необов'язково заміщеним 1-4 групами, вибраними з галогену, С1-4-алкілу, галоген-С1-4алкілу, С1-3-ацилу, С1-3-ацилокси, С1-3-алкокси, С1-6алкіл-ОС(О)-, С2-4-алкенілу, С2-4-алкінілу, С1-3алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси, фенілу, CN, OH, D, NH2, NHRa і N(Ra)2, де Ra являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10-ар-С1-6-алкілен або феніл, необов'язково заміщений 1-3 атомами галогену. У даний аспект винаходу включені всі 81417 18 інші змінні, які спочатку визначені відповідно до формули І. Іншим аспектом даного винаходу, який представляє ще більший інтерес, є сполука, описана вище, де А і В взяті разом і являють собою С2-4-членну алкандіїльну групу, так що разом з атомом вуглецю, до якого приєднані, Іони утворюють 3-5-членний цикл, необов'язково заміщений 1-2 групами, вибраними з галогену, С1галоген-С1-4-алкілу, С1-3-алкокси, С1-34-алкілу, алкоксі-С1-3-алкілу, С1-3-алкоксі-С1-3-алкокси і фенілу. У даний аспект включені всі інші змінні, які спочатку визначені відповідно до формули І. Ще більш точно, аспект винаходу, який представляє інтерес, відноситься до сполуки, описаної вище, де А і В взяті разом і являють собою С2-4-алкандіїльну групу, так що разом з атомом вуглецю, до якого приєднані, вони утворюють 3-5-членний цикл, причому вказаний цикл є незаміщеним або заміщений 1-2 галогеновими групами. У даний аспект включені всі змінні, які визначені відповідно до формули І. Ще більш точно, аспект даного винаходу, який представляє інтерес, відноситься до сполуки, описаної вище, де 1-2 галогенові групи являють собою атоми фтору. У даний аспект включені всі змінні, які визначені відповідно до формули І. В іншому аспекті даного винаходу, який представляє інтерес, розкрита сполука формули І, де дві групи R1 являють собою Η і одна група R1 вибрана з групи, що включає ОН, галоген, С1-10алкіл, С1-6-алкокси і С6-10-арил, причому вказані С110-алкіл, С6-10-арил і алкільна частина С1-6-алкокси є необов'язково заміщеними 1-3 галогенами, ОН, ОС1-3-алкільною, фенільною або нафтильною групами, і вказаний феніл і нафтил є необов'язково заміщеними 1-3 замісниками, вибраними з галогену, ОСН3, OCF3, CH3, CF3 і фенілу, де вказаний феніл необов'язково заміщений 1-3 галогеновими групами. У даний аспект включені всі інші змінні, які спочатку визначені відповідно до формули І. Більш точно, аспект даного винаходу, який представляє інтерес, відноситься до сполуки формули І, де одна група R1 являє собою Η і дві інші групи R1 вибрані з групи, що включає ОН, галоген, С1-10-алкіл і С1-6-алкокси, причому вказаний С1-10-алкіл і алкільна частина С1-6алкокси є необов'язково заміщеними 1-3 галогеновими групами. У даний аспект включені всі інші змінні, які спочатку визначені відповідно до формули І. Ще більш точно, аспект даного винаходу, який представляє інтерес, відноситься до сполуки формули І, де дві групи R1 являють собою галоген або метил. Даний аспект включає всі інші змінні, які спочатку визначені відповідно до формули І. В іншому аспекті даного винаходу розкрита сполука формули І, де R2 взятий окремо від R3 і вибраний з групи, що включає (а) С1-4-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, OCF3, CH3 і CF3, і 19 вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами; (b) феніл або піридил, необов'язково заміщений 1-3 галогеновими, ОН або Ra групами; (с) С2-10-алкеніл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогену, ОН і ОС1-3-алкілу, причому вказана С1-3-алкільна частина ОС1-3-алкілу є необов'язково заміщеною 13 галогеновими групами; (d) СН2СО2Н; (e) СН2СО2С1-6-алкіл; (f) CH2C(O)NHRa і (g) NH2, NHRa i N(Ra)2 і Ra являє собою С1-3-алкіл, ОС1-3-алкіл, С6-10арил-С1-6-алкілен або феніл, необов'язково заміщений 1-3 галогеновими групами. Даний аспект винаходу включає всі інші змінні, які спочатку визначені відповідно до формули І. Більш точно, у даному аспекті даного винаходу розкрита сполука формули І, де R2 взятий окремо від R3 і являє собою С1-4-алкіл, необов'язково заміщений 1-6 галогеновими групами і 1-3 замісниками, вибраними з ОН, ОС1-3алкілу і фенілу, причому вказаний феніл є необов'язково заміщеним 1-4 групами, незалежно вибраними з галогену, ОСН3, OCF3, CH3 і CF3, і алкільна частина ОС1-3-алкілу є необов'язково заміщеною 1-3 галогеновими групами. Даний аспект включає всі інші змінні, які спочатку визначені відповідно до формули І. Ще більш точно, аспект даного винаходу, який представляє особливий інтерес, відноситься до сполуки формули І, де R2 взятий окремо від R3 і являє собою метил або циклопропіл. Даний аспект включає всі інші змінні, які спочатку визначені відповідно до формули І. В іншому аспекті даного винаходу, сполука, яка представляє інтерес, визначена відповідно до формули І, де R взятий окремо від R і вибраний з групи, що включає С1-14-алкіл, С2-10-алкеніл, SС1-6алкіл, С6-10-арил, гетероцикліл і геретоарил, причому вказаний алкіл, алкеніл, арил, гетероцикліл, гетероарил і алкільна частина SC1-6алкілу є необов'язково заміщеними (a) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NHС1-4-алкілу, N(C1-4-алкіл)2, С1-4алкілу, ОС1-4-алкілу, CN, C1-4-алкіл-S(O)x-, де х дорівнює 0, 1 або 2, C1-4-алкіл-SO2NH-, H2NSO2-, C1-4-алкіл-NHSО2- і (C1-4-алкіл)2NSO2-, причому вказаний C1-4-алкіл і C1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, C1-4-алкілу, C1-4алкіл-S(О)х-, де x приймає значення, визначені вище, C1-4-алкіл-SO2NH-, H2NSO2-, C1-4-алкілNHSO2, (C1-4-алкіл)2NSO2-, CN, OH, ОC1-4-алкілу, причому вказаний C1-4-алкіл і C1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 атомами галогенів і 1 групою, вибраною з ОН і ОC1-3-алкілу. Даний аспект включає всі інші змінні, які спочатку визначені відповідно до формули І. Більш точно, сполука, яка представляє інтерес, визначена відповідно до формули І, де R3 взятий окремо від R2 і вибраний з групи, що включає C1-14-алкіл, С6-10-арил, гетероцикліл і 81417 20 гетероарил, причому вказані групи є необов'язково заміщеними (a) R; (b) 1-6 галогеновими групами і (с) 1-3 групами, вибраними з ОН, NH2, NHC1-4алкілу, N(C1-4-алкіл)2, C1-4-алкілу, ОC1-4-алкілу, CN, C1-4-алкіл-S(О)х-, де x дорівнює 0, 1 або 2, C1-4алкіл-SО2NH-, H2NSO2-, C1-4-алкіл-NHSO2, (C1-4алкіл)2NSO2-, причому вказаний C1-4-алкіл і C1-4алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 атомами галогенів. Даний аспект винаходу включає всі інші змінні, які спочатку визначені відповідно до формули І. Ще більш точно, сполука, яка представляє інтерес, визначена відповідно до формули І, де R взятий окремо і вибраний з групи, що включає циклопропіл, необов'язково заміщений метилом або фенілом; феніл, необов'язково заміщений галогеном, ОН, ОСН3 або OCF3; гетероарил, вибраний з бензімідазолілу, індолілу, бензофуранілу і дигідробензофуранілу, причому вказані гетероарильні групи є необов'язково заміщеними (a) R; (b) 1-6 галогеновими групами або (с) 1-3 групами, вибраними з ОН, NH2, NHC1-4алкілу, групи N(C1-4-алкіл)2, C1-4-алкілу, ОC1-4алкілу, CN, C1-4-алкіл-S(О)х-, де x дорівнює 0, 1 або 2, C1-4-алкіл-SО2NН-, H2NSO2-, C1-4-алкіл-NHSO2, (C1-4-алкіл)2NSО2-, причому вказаний C1-4-алкіл і C1-4-алкільні частини вказаних груп є необов'язково заміщеними фенілом і 1-3 галогеновими групами, і R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 групами, вибраними з галогену, C1-4-алкілу, ОН, ОC1-4-алкілу, і вказаний C1-4-алкіл і C1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-5 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу. Даний аспект винаходу включає всі інші змінні, які спочатку визначені відповідно до формули І. В іншому аспекті даного винаходу, який представляє інтерес, описана сполука формули І, де R2 і R3 взяті разом і являють собою (а) С3-8алкандіїл, що утворює конденсований 5-10членний неароматичний цикл, який необов'язково містить 1 подвійний зв'язок і необов'язково містить 1 гетероатом, вибраний з О, S і N; або (b) конденсовану 6-10-членну ароматичну моноциклічну або біциклічну групу, причому вказані алкандіїл і ароматична моноциклічна або біциклічна група є необов'язково заміщеними 1-3 атомами галогенів і 1-2 групами, вибраними з ОН, С1-3-алкілу, ОС1-3-алкілу, галогенС1-3-алкілу, галоген-С1-3-алкокси і фенілу, причому вказаний феніл є необов'язково заміщеним 1-2 групами, незалежно вибраними з галогену, С1-3алкілу, ОС1-3-алкілу, і вказаний С1-3-алкіл і С1-3алкільна частина ОС1-3-алкілу є необов'язково заміщеними 1-3 галогеновими групами. Даний аспект винаходу включає всі інші змінні, які спочатку визначені відповідно до формули І. Більш точно, аспект даного винаходу, який представляє інтерес, відноситься до сполуки формули І, де R вибраний з гетероциклілу, гетероарилу і арилу, причому вказана група є необов'язково заміщеною 1-4 галогеновими групами і 1-2 групами, вибраними з C1-4-алкілу, C1 21 4-алкіл-S(О)х-, де x дорівнює 0, 1 або 2, C1-4-алкілSО2NH-, H2NSO2-, C1-4-алкіл-NHSO2-, (C1-4алкіл)2NSO2-, CN, ОН і ОC1-4-алкілу, причому вказаний C1-4-алкіл і C1-4-алкільні частини вказаних груп є необов'язково заміщеними 1-3 галогеновими групами і 1 групою, вибраною з ОН і ОС1-3-алкілу. Даний аспект включає всі інші змінні, які спочатку визначені відповідно до формули І. Сполуки, які входять в об'єм даного винаходу, включають сполуки, описані у прикладах. Ілюстративними, але не обмежувальними, прикладами сполук даного винаходу є інгібітори 11β-HSD-1, що являють собою сполуки наступних структурних формул та їх фармацевтично прийнятні солі і сольвати. Ще один аспект даного винаходу відноситься до фармацевтичної композиції, яка включає сполуку відповідно до формули І або її сіль або гідрат у поєднанні з фармацевтично прийнятним носієм. Ще один аспект даного винаходу відноситься до способу лікування гіперглікемії, цукрового діабету або інсулінорезистентності у пацієнтассавця, який потребує такого лікування, що включає введення вказаному пацієнту ефективної кількості сполуки відповідно до формули І або її солі або сольвату. У ще одному аспекті даного винаходу розкритий спосіб лікування інсуліннезалежного цукрового діабету у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки відповідно до формули І у кількості, ефективній для лікування цукрового діабету. У ще одному аспекті даного винаходу описаний спосіб лікування ожиріння у пацієнта 81417 22 ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки відповідно до формули І у кількості, яка ефективна для лікування ожиріння. У ще одному аспекті даного винаходу описаний спосіб лікування синдрому X у пацієнтассавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки відповідно до формули І у кількості, яка ефективна для лікування синдрому X. У ще одному аспекті даного винаходу описанийспосіб лікування ліпідного розладу, вибраного з групи, що включає дисліпідемію, гіперліпідемію, гіпертригліцеридемію, гіперхолестеринемію, низький вміст HDL і високий вміст LDL, у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки відповідно до формули І у кількості, ефективній для лікування вказаного ліпідного розладу. У ще одному аспекті даного винаходу описаний спосіб лікування атеросклерозу у пацієнта-ссавця, який потребує такого лікування, що включає введення вказаному пацієнту сполуки відповідно до формули І у кількості, ефективній для лікування атеросклерозу. У ще одному аспекті даного винаходу розкритий спосіб лікування стану, вибраного з групи, що включає (1) гіперглікемію, (2) низьку толерантність до глюкози, (3) інсулінорезистентність, (4) ожиріння, (5) ліпідні розлади, (6) дисліпідемію, (7) гіперліпідемію, (8) гіпертригліцеридемію, (9) гіперхолестеринемію, (10) низькі рівні вмісту HDL, (11) високі рівні вмісту LDL, (12) атеросклероз і його наслідки, (13) судинний рестеноз, (14) панкреатит, (15) відкладення жирової тканини у ділянці очеревини, (16) нейродегенеративне захворювання, (17) ретинопатію, (18) нефропатію, (19) нейропатію, (20) синдром X та інші стани і розлади, компонентом яких є інсулінорезистентність, у пацієнта-ссавця, який потребує такого лікування, що включає введення пацієнту сполуки відповідно до формули І у кількості, ефективній для лікування вказаного стану. В іншому аспекті даного винаходу розкритий спосіб лікування стану, вибраного з групи, що включає (1) гіперглікемію, (2) низьку толерантність до глюкози, (3) інсулінорезистентність, (4) ожиріння, (5) ліпідні розлади, (6) дисліпідемію, (7) гіперліпідемію, (8) гіпертригліцеридемію, (9) гіперхолестеринемію, (10) низькі рівні вмісту HDL, (11) високі рівні вмісту LDL, (12) атеросклероз і його наслідки, (13) судинний рестеноз, (14) панкреатит, (15) відкладення жирової тканини у ділянці очеревини, (16) нейродегенеративне захворювання, (17) ретинопатію, (18) нефропатію, (19) нейропатію, (20) синдром X та інші стани і розлади, компонентом яких є інсулінорезистентність, у пацієнта-ссавця, який потребує такого лікування, що включає введення пацієнту ефективної кількості сполуки відповідно до формули І і сполуки, вибраної з групи що включає: (a) DP-IV інгібітори; 23 (b) сенсибілізатори інсуліну, вибрані з групи, що включає (і) PPAR агоністи і (іі) бігуаніди; (c) інсулін та імітатори інсуліну; (d) сульфонілсечовини та інші засоби, що посилюють секрецію інсуліну; (e) інгібітори а-глюкозидази; (і) антагоністи глюкогонового рецептора; (g) GLP-1, імітатори GLP-1 і агоністи GLP-1 рецептора; (h) GIP, імітатори GIP і агоністи GIP рецептора; (і) ΡАСАР, імітатори РАСАР і агоністи РАСАР рецептора 3; (j) засоби, що знижують вміст холестерину і вибрані з групи, що включає (і) інгібітори HMG-CoA редуктази, (іі) речовини, що посилюють екскрецію, (ііі) нікотиніловий спирт, нікотинову кислоту і їх солі, (iv) PPARα агоністи, (ν) подвійні PPARα/g агоністи, (vi) інгібітори абсорбції холестерину, (vii) інгібітори ацил-СоА:холестерин ацилтрансферази і (viii) антиоксиданти; (k) PPAR δ агоністи; (l) сполуки для лікування ожиріння; (m) інгібітор транспортера клубової жовчноїжислоти; (n) протизапальні засоби, відмінні від глюкокортикоїдів; (о) інгібітори протеїн-тирозин-фосфатази-ІВ (РТР-1В), причому вказані сполуки вводяться пацієнту у кількості, ефективній для лікування вказаного стану. В іншому аспекті даного винаходу розкритий спосіб лікування стану, вибраного з групи, що включає гіперхолестеринемію, атеросклероз, низькі рівні вмісту HDL, високі рівні вмісту LDL, гіперліпідемію, гіпертригліцеридемію і дисліпідемію, у пацієнта-ссавця, який потребує такого лікування, що включає введення пацієнту терапевтично ефективної кількості сполуки відповідно до формули І та інгібітору HMG-CoA редуктази. Більш точно, в іншому аспекті даного винаходу розкритий спосіб лікування стану, вибраного з групи, що включає гіперхолестеринемію, атеросклероз, низькі рівні вмісту HDL, високі рівні вмісту LDL, гіперліпідемію, гіпертригліцеридемію і дисліпідемію, у пацієнта-ссавця, який потребує такого лікування, де інгібітор HMG-CoA редуктази являє собою статин. Ще більш точно, в іншому аспекті винаходу описаний спосіб лікування стану, вибраного з групи, що включає гіперхолестеринемію, атеросклероз, низькі рівні вмісту HDL, високі рівні вмісту LDL, гіперліпідемію, гіпертригліцеридемію і дисліпідемію, у пацієнта-ссавця, який потребує такого лікування, де інгібітор HMG-CoA редуктази являє собою статин, вибраний з групи, що включає ловастатин, симвастатин, правастатин, флувастатин, аторвастатин, ітавастатин, ZD-4522 і ривастатин. В іншому аспекті даного винаходу розкритий спосіб лікування атеросклерозу у пацієнта людини, яка потребує такого лікування, де інгібітор HMG-CoA редуктази являє собою статин, який 81417 24 додатково включає введення інгібітору абсорбції холестерину. Більш точно, в іншому аспекті даного винаходу розкритий спосіб лікування атеросклерозу у пацієнта - людини, яка потребує такого лікування, де інгібітор HMG-CoA редуктази являє собою статин та інгібітор абсорбції холестерину являє собою езетиміб. В іншому аспекті даного винаходу розкрита фармацевтична композиція, яка включає (1) сполуку відповідно до формули І, (2) сполуку, вибрану з групи, що включає (a) DP-IV інгібітори; (b) сенсибілізатори інсуліну, вибрані з групи, що включає (і) PPAR агоністи і (іі) бігуаніди; (c) інсулін та імітатори інсуліну; (d) сульфонілсечовини та інші засоби, що посилюють секрецію інсуліну; (e) інгібітори а-глюкозидази; (f) антагоністи глюкагонового рецептора; (g) GLP-1, імітатори GLP-1 і агоністи GLP-1 рецептора; (h) GIP, імітатори GIP і агоністи GIP рецептора; (і) РАСАР, імітатори РАСАР і агоністи РАСАР рецептора 3; (j) засоби, що знижують вміст холестерину і вибрані з групи, що включає (і) інгібітори HMG-CoA редуктази, (іі) речовини, що посилюють екскрецію, (ііі) нікотиніловий спирт, нікотинову кислоту і їх солі, (iv) PPARα агоністи, (ν) подвійні PPARα/g агоністи, (vi) інгібітори абсорбції холестерину, (vii) інгібітори ацил-СоА:холестерин ацилтрансферази і (viii) антиоксиданти; (k) PPAR δ агоністи; (l) сполуки для лікування ожиріння; (m) інгібітор транспортера клубової жовчної кислоти; (n) протизапальні засоби, відмінні від глюкокортикоїдів; (о) інгібітори протеїн-тирозин-фосфатази-1В (РТР-1В); і (3) фармацевтично прийнятний носій. Термін "фармацевтично прийнятна сіль" відноситься до солей, одержаних з фармацевтично прийнятних основ або кислот, включаючи неорганічні або органічні основи і неорганічні або органічні кислоти. Солі, одержані з неорганічних основ, включають солі алюмінію, амонію, кальцію, міді, тривалентного заліза, двовалентного заліза, літію, магнію, тривалентного марганцю, двовалентного марганцю, калію, натрію, цинку і т.п. Особливо переважними є солі амонію, кальцію, магнію, калію і натрію. Солі у твердій формі можуть мати декілька·кристалічних структур, а також можуть існувати у формі гідратів і полігідратів. Солі, одержані з фармацевтично прийнятних органічних основ, включають солі первинних, вторинних і третинних амінів, заміщених амінів, у тому числі наявних у природі заміщених амінів, циклічних амінів, і основних іонно-обмінних смол, таких як аргінін, бетаїн, кофеїн, холін, Ν,Ν'дибензилетилендіамін, діетиламін, 2 25 діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидин, гідрабамін, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, поліамінові смоли, прокат, пурини, теобромін, триетиламін, триметиламін, трипропіламін, трометамін і т.п. Коли сполука даного винаходу є основною, солі можуть бути одержані з фармацевтично прийнятних кислот, включаючи неорганічні і органічні кислоти. Такі кислоти включають оцтову, бензолсульфонову, бензойну, камфорсульфонову, лимонну, етансульфонову, фумарову, глюконову, глутамінову, бромистоводневу, хлористоводневу, ізетіонову, молочну, малеїнову, яблучну, мигдалеву, метансульфонову, слизову, азотну, памову, пантотенову, фосфорну, бурштинову, сірчану, винну, п-толуолсульфонову кислоту і т.п. Особливо переважні фармацевтично прийнятні кислоти включають лимонну, бромистоводневу, хлористоводневу, малеїнову, фосфорну, сірчану і винну кислоти. У більшості випадків сполуки даного винаходу є основними, оскільки триазольний цикл є основним. Похідні триазолу даного винаходу також можуть бути одержані і оброблятися у вигляді фармацевтично не прийнятних солей (наприклад трифторацетатних солей) у процесі синтезу їх перед застосуванням для одержання фармацевтичних засобів. Буде зрозуміло, що посилання на сполуки формули І у даному винаході включають фармацевтично прийнятні солі, а також фармацевтично не прийнятні солі, коли вони використовуються як попередники вільних сполук або їх фармацевтично прийнятних солей або в інших синтетичних маніпуляціях. Сольвати і, зокрема, гідрати сполук формули І включені у галузь даного винаходу. Метаболіти сполук даного винаходу, які є терапевтично активними і які визначені формулою І, також включені у галузь даного винаходу. Проліки являють собою сполуки, які перетворюються у терапевтично активні сполуки при введенні пацієнту або після введення пацієнту. Сполуки, які самі по собі не володіють структурами, заявленими у даному винаході, але які перетворюються в активні сполуки, визначені формулою І у процесі або після введення ссавцеві - пацієнту, є проліками і сполуками даного винаходу, оскільки є їх активними метаболітами, які визначені формулою І. Сполуки, описані у даному винаході, є селективними інгібіторами 11β-HSD1 ферменту. Отже, даний винахід відноситься до застосування інгібітору 11β-HSD1 для інгібування редуктазної активності 11β-гідроксистероїдної дегідрогенази, яка відповідальна за перетворення кортизону у кортизол. Надмірний кортизол пов'язаний з рядом розладів, включаючи NIDDM, ожиріння, дисліпідемію, інсулінорезистентність і гіпертензію. Введення сполук знижує рівень вмісту кортизолу та інших 11β-гідроксистероїдів у тканинахмішенях, знижуючи, таким чином, ефекти надмірних кількостей кортизолу та інших 11 β 81417 26 гідроксистероїдів. Інгібування 11β-HSD1 може застосовуватися для лікування і контролю захворювань, що проводяться патологічно високими рівнями вмісту кортизолу та інших 11βгідроксистероїдів, такими як NIDDM, ожиріння, гіпертензія і дисліпідемія. Даний винахід включає застосування 11βHSD1 інгібітору для лікування, контролю, полегшення, профілактики, затримки атаки або зниження ризику розвитку захворювань і станів, які описані вище і які проводяться надмірними або неконтрольованими кількостями кортизолу і/або інших кортикостероїдів у пацієнта-ссавця, зокрема у людини, введенням ефективної кількості сполуки формули І або її фармацевтично прийнятної солі або сольвату. Інгібування 11β-HSD1 ферменту обмежує перетворення кортизону, який у нормальному стані є інертним, у кортизол, який може викликати симптоми або здійснити внесок у симптоми даних захворювань і станів, якщо присутній у надмірних кількостях. NIDDM і гіпертензія Сполуки даного винаходу є селективними інгібіторами 11β-HSD1 і не впливають на 11βHSD2. У той час як інгібування 11β-HSD1 корисне для зниження рівнів вмісту кортизолу і лікування станів, пов'язаних з ним, інгібування 11β-ΗSD2 пов'язане з серйозними побічними ефектами, такими як гіпертензія. Кортизол є важливим і широко відомим протизапальним гормоном, який також виступає як антагоніст дії інсуліну у печінці, так що чутливість до інсуліну знижується, приводячи до підвищеного глюконеогенезу і підвищених рівнів вмісту глюкози у печінці. Для пацієнтів з вже ослабленою толерантністю до глюкози характерна велика ймовірність розвитку цукрового діабету 2 типу у присутності патологічно високих рівнів вмісту кортизолу. Високі рівні вмісту кортизолу у тканинах, де присутній мінерало-кортикоідний рецептор, часто приводять до гіпертензії. Інгібування 11β-HSD1 зміщує співвідношення кортизолу і кортизону у специфічних тканинах у бік кортизону. Введення терапевтично ефективної кількості 11β-HSD1 інгібітору ефективне для лікування, контролю і полегшення симптомів NIDDM, і регулярне введення терапевтично ефективної кількості 11β-HSD1 інгібітору затримує або запобігає атаці NIDDM, особливо у людей. Ожиріння, метаболічний синдром, дисліпідемія Надмірні рівні вмісту кортизолу зв'язували з ожирінням, можливо, внаслідок підвищеного печінкового глюконеогенезу. Патологічне ожиріння тісно пов'язане з інтолерантністю до глюкози, гіперінсулінемією, гіпертригліцеридемією та іншими факторами синдрому X, такими як високий кров'яний тиск, підвищений вміст VLDL і знижений вміст HDL (Montague et al., Diabetes, 2000, 49: 883888). Таким чином, введення ефективної кількості 11β-HSD1 інгібітору корисне для лікування або контролю ожиріння. Тривале лікування 11β-HSD1 інгібітором також корисне для затримки або профілактики початку ожиріння, особливо якщо пацієнт використовує інгібітор 11β-HSD1 у 27 поєднанні з контрольованою дієтою та фізичним навантаженням. За допомогою зниження інсулінорезистентності і підтримки вмісту глюкози у плазмі на рівні нормальних концентрацій сполуки даного винаходу можуть застосовуватися для лікування і профілактики станів, які супроводжують цукровий діабет 2 типу та інсулінорезистентність, включаючи метаболічний синдром ("синдром X"), ожиріння, реактивну гіпоглікемію і діабетичну дисліпідемію. Атеросклероз Як описано вище, інгібування активності 11βHSD1 і зниження кількості кортизолу сприятливі для лікування і контролю гіпертензії. Оскільки гіпертензія і дисліпідемія сприяють розвитку атеросклерозу, введення терапевтично ефективної кількості інгібітору 11β-HSD1 даного винаходу може бути особливо корисне для лікування, контролю, затримки початку розвитку або профілактики атеросклерозу. Інші застосування При використанні для лікування сполук даного винаходу можна лікувати, контролювати, запобігати захворюванням, розладам або станам, перерахованим нижче, або можна сповільнювати їх розвиток: (1) гіперглікемія, (2) низька толерантність до глюкози, (3) інсулінорезистентність, (4) ожиріння, (5) ліпідні розлади, (6) дисліпідемія, (7) гіперліпідемія, (8) гіпертригліцеридемія, (9) гіперхолестеринемія, (10) низькі рівні вмісту HDL, (11) високі рівні вмісту LDL, (12) атеросклероз і його наслідки, (13) судинний рестеноз, (14) панкреатит, (15) патологічне ожиріння, (16) нейродегенеративне захворювання, (17) ретинопатія, (18) нефропатія, (19) нейропатія, (20) синдром X та інші розлади, компонентом яких є інсулінорезистентність. Перераховані вище захворювання і стани можна лікувати з використанням сполук формули І, або сполука може вводитися для профілактики або зниження ризику розвитку захворювань і станів, описаних вище. Оскільки конкурентне інгібування 11β-HSD2 може мати шкідливі побічні ефекти або може фактично підвищувати кількість кортизолу у тканині-мішені, де бажане зниження вмісту кортизолу, селективні інгібітори 11β-HSD1 з невеликим інгібуванням lip-HSD2 або без такого інгібування є бажаними. Інгібітори 11β-HSD1 формули І звичайно мають значення константи інгібування ІС50 менше приблизно 500нМ, переважно менше приблизно 100нМ. Звичайно співвідношення значення ІС50 11β-ΗSD2 до значення ІС50 11β-HSD1 дорівнює, щонайменше, приблизно двом або більше, переважно приблизно десяти або більше. Ще більш переважними є сполуки зі співвідношенням ІС5о для 11β-HDS1 і ІС50 для 11β-HDS2, що дорівнює приблизно 100 або більше. Наприклад, для сполук, які мають ІС50, сполуки ідеально показують константу інгібування 11β-HSD2 більше приблизно 500нМ, переважно більше 1000нМ. Сполуки формули І можуть використовуватися у поєднанні з одним або декількома " іншими лікарськими засобами для лікування, 81417 28 профілактики, пригнічення або полегшення перебігу захворювань або станів, для яких застосовні сполуки формули І або інші лікарські засоби. Звичайно поєднання лікарських засобів є більш надійним або більш ефективним, ніж застосування одного лікарського засобу, або поєднання є більш надійним або більш ефективним, ніж повинно було очікуватися на основі складання властивостей окремих лікарських засобів. Такий(і) інший(і) лікарський(і) засіб(оби) можуть вводитися способами та у кількості, які звичайно застосовуються, одночасно або послідовно зі сполукою формули І. Коли сполука формули І використовується одночасно з одним або декількома іншими лікарськими засобами, переважним є складний препарат, що містить такий(і) інший(і) лікарський(і) засіб(оби) і сполуку формули І. Однак комбінована терапія також включає терапевтичні лікування, при яких сполука формули І і один або декілька інших лікарських засобів вводяться за різними схемами лікування, що перекриваються. Це має на увазі, що при використанні у поєднанні з іншими активними інгредієнтами сполука даного винаходу або інший активний інгредієнт або обидва лікарських засоби можуть застосовуватися ефективно у більш низьких дозах, ніж при застосуванні кожного окремо. Відповідно, фармацевтичні композиції даного винаходу включають композиції, які на додаток до сполуки формули І містять один або декілька інших активних інгредієнтів. Приклади інших активних інгредієнтів, які можуть вводитися у поєднанні зі сполукою формули І і можуть вводитися окремо або разом в одній фармацевтичній композиції, включають, але без обмеження тільки ними: (a) інгібітори дипептидилпептидази IV (DP-IV); (b) сенсибілізатори інсуліну, включаючи (і) PPARg агоністи, такі як глітазони (наприклад, троглітазон, піоглітазон, енглітазон, МСС-555, розиглітазон і т.п.) та інші PPAR ліганди, включаючи подвійні агоністи PPARα/g, такі як KRP297, і PPARα агоністи, такі як гемфіброзил, клофібрат, фенофібрат і безафібрат, і (іі) бігуаніди, такі як метформін і фенформін; (c) інсулін та імітатори інсуліну; (d) сульфонілсечовини та інші засоби, що посилюють секрецію інсуліну, такі як толбутамід і гліпізид, меглітинід і аналогічні засоби; (e) інгібітори а-шюкозидази (такі як акарбоза); (f) антагоністи глюкогонового рецептора, такі як засоби, [описані у WO 98/04528, WO 99/01423, WO 00/39088 і WO 00/69810]; (g) GLP-1, імітатори GLP-1 і агоністи GLP-1 рецептора, такі як засоби, [описані у WO 00/42026 і WO 00/59887]; (h) GIP, імітатори GIP, такі як засоби, [описані у WO 00/58360], і агоністи GIP рецептора; (і) РАСАР, імітатори РАСАР і агоністи РАСАР рецептора 3, такі як засоби, [описані у WO 01/23420]; (j) засоби, що знижують вміст холестерину, такі як (і) інгібітори HMG-CoA редуктази (ловастатин, симвастатин, правастатин, 29 флувастатин, аторвастатин, ривастатин, ітавастатин, росувастатин та інші статини), (іі) речовини, що посилюють екскрецію (холестирамін, колестипол і діалкіламіноалкільні похідні зшитого декстрану), (ііі) нікотиніловий спирт, нікотинова кислота і їх солі, (iv) інгібітори абсорбції холестерину, такі як, наприклад, езетиміб і бетаситостерол, (ν) інгібітори ацил-СоА:холестерин ацилтрансферази, такі як, наприклад, авасиміб, (vi) антиоксиданти, такі як пробукол; (k) PPAR d агоністи, такі як засоби, [описані у WO 97/28149]; (l) сполуки для лікування ожиріння, такі як фенфлурамін, дексфенфлурамін, фентермін, сибутрамін, орлістат, нейропептидні Υ5 інгібітори, СВ1 рецепторні інверсні агоністи та антагоністи і b3 адренергічні рецепторні агоністи; (m) інгібітор транспортера клубової жовчної кислоти; (n) засоби, призначені для застосування при запальних станах і відмінні від глюкокортикоїдів, такі як аспірин, нестероїдні протизапальні лікарські засоби, азулфідин і селективні інгібітори циклооксигенази 2; (о) інгібітори протеїн-тирозин-фосфатази-1В (РТР-1В); Описані вище поєднання включають сполуку формули І або її фармацевтично прийнятну сіль, гідрат або сольват, не тільки з однією або декількома іншими активними сполуками. Приклади, що не обмежуються наведеним переліком включають поєднання сполук формули І з двома або декількома активними сполуками, вибраними з бігуанідів, сульфонілсечовин, інгібіторів HMG-CoA редуктази, PPAR агоністів, інгібіторів РТР-1В, інгібіторів DP-IV і сполук для лікування ожиріння. Для забезпечення ссавця, особливо людини, ефективною дозою сполуки даного винаходу може використовуватися будь-який придатний спосіб введення. Наприклад, можуть використовуватися пероральний, ректальний, місцевий, парентеральний, очний, легеневий, назальний способи введення. Лікарські форми включають таблетки, пастилки, дисперсії, суспензії, розчини, капсули, креми, мазі, аерозолі і т.п. Переважно, сполука формули вводиться перорально. Ефективна доза активного інгредієнта змінюється в залежності від конкретної застосовуваної сполуки, способу введення, стану, що підлягає лікуванню, і тяжкості стану. Такі дози можуть без великих зусиль визначатися кваліфікованим фахівцем. При лікуванні або для профілактики захворювань і станів, описаних у даному винаході, для яких показані сполуки формули І, задовільні результати одержані при введенні сполук даного винаходу у добовій дозі від приблизно 0,1 до приблизно 100 міліграмів на кілограм (мг/кг) маси тіла, переважно при прийомі у вигляді разової добової дози або у вигляді дози, поділеної приблизно на прийом від двох до шести разів на день. Таким чином, загальна добова доза знаходиться в інтервалі від приблизно 0,1мг до приблизно 1000мг, переважно від приблизно 1мг 81417 30 до приблизно 50мг. Для типового дорослого пацієнта з масою тіла 70кг загальна добова доза буде знаходитися в інтервалі від приблизно 7мг до приблизно 350мг. Дане дозування може коректуватися для забезпечення оптимального терапевтичного результату. Інший аспект даного винаходу відноситься до фармацевтичної композиції, яка включає сполуку формули І або її фармацевтично прийнятну сіль, гідрат або сольват у поєднанні з фармацевтично прийнятним носієм. Композиції включають композиції, придатні для перорального, ректального, місцевого, парентерального (включаючи підшкірне, внутрішньом'язове або внутрішньовенне), очного (офтальмологічне), черезшкірного, легеневого (назальну або трансбукальну інгаляцію) або назального введення, хоча найбільш придатний спосіб у будь-якому випадку буде залежати від природи і тяжкості стану, що підлягає лікуванню, і активного інгредієнта. Вони можуть традиційно постачатися у стандартній лікарській формі і можуть бути одержані будь-якими способами, добре відомими у фармацевтичній галузі. Сполука формули І може об'єднуватися з фармацевтичним носієм відповідно до традиційних фармацевтичних способів одержання сумішей. Носії приймають різноманітні форми. Зокрема, носії для рідких композицій для перорального введення включають, наприклад, воду, гліколі, масла, спирти, смакові агенти, консерванти, барвники та інші компоненти, що використовуються при одержанні рідких суспензій, еліксирів і розчинів для перорального введення. Для приготування твердих лікарських форм для перорального введення, наприклад, порошків, твердих і м'яких капсул і таблеток, використовуються такі носії як крохмаль, цукор і мікрокристалічна целюлоза, розріджувачі, гранулюючі агенти, змащувальні агенти, в'яжучі речовини, дезінтегруючі агенти і т.п. Тверді препарати для перорального введення переважні у порівнянні з рідкими препаратами для перорального введення. Тверді лікарські форми для перорального введення можуть також містити в'яжучу речовину, таку як трагакант, аравійська камедь, кукурудзяний крохмаль або желатин; наповнювачі, такі як гідрофосфат кальцію; дезінтегруючий агент, такий як кукурудзяний крохмаль, картопляний крохмаль, альгінова кислота; змащувальну речовину, таку як стеарат магнію; і підсолоджуючу речовину, таку як сахароза, лактоза або сахарин. Капсули можуть також містити рідкий носій, такий як жирне масло. Можуть бути присутніми й інші речовини для того, щоб виступати як покриття або для модифікації фізичної форми стандартної дози. Наприклад, таблетки можуть бути покриті шелаком, цукром або тим й іншим. Таблетки можуть бути покриті стандартними водними або неводними методами. Звичайний процентний вміст активного інгредієнта, звичайно, може змінюватися від приблизно 2 процентів до приблизно 60 процентів (мас/мас). Таким чином, таблетки містять сполуку формули І або її сіль або 31 гідрати у кількості в інтервалі від приблизно 0,1мг до приблизно 1,5г, переважно в інтервалі від приблизно 1,0мг до приблизно 500мг, і найбільш переважно, в інтервалі від приблизно 10мг до приблизно 100мг. Рідкі препарати для перорального введення, такі як сиропи або еліксири, можуть містити крім активного інгредієнта сахарозу як підсолоджуючу речовину, метил- і пропілпарабени як консерванти, барвник і смакову домішку, таку як вишнева або апельсинова смакова домішка. Препарати для парентерального введення, звичайно у формі розчину або суспензії, як правило одержують з водою, і вони необов'язково включають поверхнево-активну речовину, таку як гідроксипропілцелюлоза. Дисперсії можуть бути одержані у гліцерині, рідких поліетиленгліколях та їх сумішах у маслах. Звичайно препарати у розбавленій формі також містять консервант. Фармацевтичні лікарські форми для ін'єкцій, включаючи водні розчини і дисперсії і порошки для швидкого одержання розчинів або дисперсій для ін'єкцій, також є стерильними і повинні бути досить рідкими для можливості введення їх за допомогою шприца; вони повинні бути стабільними в умовах виробництва і зберігання і звичайно є консервованими. Отже, носій включає розчинник або дисперсійне середовище, що містить, наприклад, воду, етанол, багатоатомний спирт (наприклад, гліцерин, пропіленгліколь і рідкий поліетиленгліколь), їх відповідні суміші та рослинні олії. Біологічні випробування: визначення констант інгібування В умовах in vitro ферментативну активність випробовуваних сполук оцінюють за допомогою досліду сцинтиляційного наближення (Scintillation Proximity Assay - SPA). Коротко, субстрат тритованого кортизону, NADPH кофактор і титровану сполуку витримують з 11β-HSD1 ферментом при 37°С для створення умов протікання перетворення кортизолу. Після інкубації препарат SPA гранул, покритих білком А, заздалегідь змішаними з антикортизольним моноклональним антитілом і неспецифічним 11βHSD інгібітором, додають у кожну комірку. Суміш струшують при 15°С і потім зчитують за допомогою рідинного сцинтиляційного лічильника, придатного для застосування на 96-ямкових планшетах. Визначають процент інгібування у порівнянні з неінгібованою контрольною ямкою і будують графіки ІС50. Аналогічне випробування проводять з використанням 11β-HSD2, де тритований кортизол і NAD використовують як субстрат і кофактор, відповідно. Для початку досліду 40мкл субстрату (25нМ 3Н-кортизон +1,25мМ NADPH у 50мМ HEPES буфера, рН7,4) додають у підготовані ямки на 96-ямковому планшеті. Тверду сполуку розчиняють у ДМСО з концентрацією 10мМ з подальшим 50-разовим розбавленням у ДМСО. Розбавлений розчин потім титрують 4-разово 7 разів. 1мкл кожної титрованої сполуки потім двічі додають до субстрату. Для початку реакції 10мкл 11β-HSD1 мікросом з СНО трансфектантів додають у кожну ямку при 81417 32 відповідній концентрації для досягнення приблизно 10% конверсії вихідної речовини. Для остаточного підрахунку процента інгібування додають ряд ямок, які являють собою мінімум і максимум досліду: одна серія ямок містить субстрат без сполуки або ферменту (фоновий сигнал), інша серія ямок містить субстрат і фермент без якої-небудь сполуки (максимальний сигнал). Планшети протягом нетривалого періоду обертають з низькою швидкістю у центрифузі для об'єднання реагентів, герметично закривають клейкою стрічкою, обережно перемішують і витримують при 37°С протягом 2 годин. Після інкубування 45мкл SPA гранул, попередньо суспендованих з антикортизольним моноклональним антитілом і неспецифічним 11βHSD інгібітором, додають у кожну ямку. Планшети знову герметично закривають і обережно струшують протягом більше 1,5 години при 15°С. Дані планшета зчитують за допомогою рідинного сцинтиляційного лічильника, такого як Topcount. Для контролю для інгібування зв'язування антитіла проти кортизолу з кортизолом субстрат з 1,25нМ [3]Н кортизолу додають у вказані одиночні ямки. 1мкл 200мкМ сполуки додають у кожну з цих ямок разом з 10мкл буфера замість ферменту. Будь-яке обчислене інгібування обумовлене тим, що сполука втручається у процес зв'язування кортизолу з антитілом на SPA гранулах. Біологічні випробування: визначення інгібування in vivo Кажучи загалом, випробовувану сполуку дозовано перорально вводять ссавцеві і залишають її на деякий час, звичайно від 1 до 24 годин. Тритований кортизон вводять внутрішньовенно і через декілька хвилин проводять забір крові. З відділеної плазми екстрагують стероїди і аналізують за допомогою ВЕРХ. Відносні рівні вмісту 3Н-кортизону і продукту його відновлення, 3Н-кортизолу, визначають для групи, що приймає сполуки, і контрольної групи, що приймає дозування носія. З одержаних значень обчислюють абсолютну конверсію, а також процент інгібування. Більш точно, сполуки готують для перорального введення розчиненням їх у носії (5% (об./об.) гідроксипропіл-бета-циклодекстрин в Н2О або еквівалент) при потрібній концентрації для одержання дози звичайно 10 міліграмів на кілограм. Вранці натщесерце розчини вводять ICR мишам (які постачаються Charles River) через зонд живлення у дозі 0,5мл на тварину трьом тваринам у дослідній групі. Після закінчення потрібного часу, звичайно 1 години або 4 годин, 0,2мл 3мкМ 3H-кортизону у dPBS вводять ін'єкцією у хвостову вену. Тварину відсаджують у клітку на 2 хвилини і потім безболісно умертвляють у камері з СО2. Після експірації мишу видаляють і кров збирають серцевою пункцією. Кров вміщують у пробірку для відділення сироватки і витримують при кімнатній температурі не менше 30 хвилин для відповідної коагуляції. Після закінчення періоду інкубації кров розділяють на сироватку центрифугуванням при 3000g (4°С) протягом 10 хвилин. 33 Для аналізу стероїдів у сироватці їх спочатку екстрагують органічним розчинником. 0,2мл сироватки переносять у чисту пробірку мікроцентрифуги. Для цього додають 1,0мл етилацетату з подальшим енергійним збовтуванням протягом 1 хвилини. Швидке обертання на центрифузі приводить до утворення шару водних білків сироватки, і органічний супернатант стає прозорим. 0,85мл верхньої органічної фази переносять у чисту пробірку мікроцентрифуги і сушать. Висушений зразок знову суспендують у 0,250мл ДМСО з високою концентрацією кортизону і кортизолу для аналізу методом ВЕРХ. 0,200мл зразка впорскують у хроматографічну колонку Metachem Inertsil C-18, врівноважену 30% метанолом. Розділення цільових стероїдів проводять з невеликим лінійним градієнтом до 50% метанолу; одночасний контроль за допомогою УФ при 254нМ охолоджених стандартних розчинів у знову суспендованому розчині служить як внутрішній стандарт. Тритієвий сигнал одержують за допомогою радіохроматографічного детектора, який завантажує дані у програму для аналізу. Процент конверсії 3Н-кортизону у 3Н-кортизол обчислюють у вигляді співвідношення AUC для кортизолу до об'єднаного AUC для кортизону і кортизолу. Наведені далі приклади ілюструють даний винахід і не призначені для обмеження його галузі. Приклад 1 Загальна схема Описаний далі синтез одновимірного одиничного масиву чистих сполук проводять на системі марки Myriad Core System. Всі реактори перед застосуванням сушать у потоку азоту при 120°С протягом 12 годин. Розчинники сушать над ситами протягом, щонайменше, 12 годин перед застосуванням. Реагенти і допоміжні сполуки (карбонові кислоти і 8-метокси-2,3,4,5,6,7гексагідроазоцин (простий іміноефір А)) розчиняють у придатних розчинниках безпосередньо перед застосуванням. Синтез Карбонову кислоту, показану у таблиці нижче як вихідну речовину, додають у сухий реактор Myriad об'ємом 10мл зі скляною пористою перегородкою в атмосфері азоту (714мл, 0,1ммоль, 0,14Μ в Ν,Ν-диметилформаміді (ДМФА)). Гексафторфосфат фтор-Ν,Ν,Ν',Ν'тетраметилформамідію (TFFH) (200мкл, 0,1ммоль, 0,5Μ у ДМФА), потім триетиламін (400мкл, 0,2ммоль, 0,5Μ у ДМФА) і гідразин (240мкл, 81417 34 0,12ммоль, 0,5Μ у ДМФА) додають у реактор в атмосфері азоту. Реакційну суміш витримують протягом 1 години при 25°С з перемішуванням газом (1-секундний імпульс кожні 5 хвилин). 8Метокси-2,3,4,5,6,7-гексагідроазоцин (простий іміноефір А, 600мкл, 0,15ммоль, 0,25Μ у ДМФА) додають у реактор в атмосфері азоту. Реакційну суміш витримують протягом 12 годин при 120°С з перемішуванням газом (1-секундний імпульс кожні 5 хвилин) і потім охолоджують до кімнатної температури. Після охолоджування сиру реакційну суміш аналізують РХ-МС (метод 1). Сиру реакційну суміш очищають препаративною ВЕРХ з використанням мас-спектрометричного виявлення (метод 2). Чистоту зібраних фракцій аналізують РХ-МС (метод 1); фракції, які, як показує аналіз, мають чистоту більше 90%, об'єднують у зважених ЕРА пляшечках об'ємом 40мл та ліофілізують. Умови ВЕРХ Аналітична РХ - метод 1: Колонка: MetaChem Polaris C-18A, 30мм´4,6мм, 5,0мкм. Елюент А: 0,1% трифтороцтова кислота (ТФОК) у воді. Елюент В: 0,1% ТФОК в ацетонітрилі. Градієнт: від 5% В до 95% В протягом 3,3 хвилин, і зворотно до 5% В протягом 0,3 хвилини. Об'ємна 2,5мл/хв. витрата: Температура колонки: 50°С. Об'єм проби: 5мкл нерозбавленої неочищеної реакційної суміші або очищеної фракції. Детектування: УФ при 220 і 254нм. МС: API-ES режим іонізації, ділянка сканування маси (100-600 атомних одиниць маси) ELSD: детектор розсіювання світла. Препаративна РХ - метод 2: Колонка: MetaChem Polaris C-18A, 100мм´21,2мм, 10,0мкм. Елюент А: 0,1% ТФОК у воді. Елюент В: 0,1% ТФОК в ацетонітрилі. Врівноваження перед упорскуванням: 1,0 хвилина. Затримка після упорскування: 1,0 хвилина. Градієнт: від 10% В до 100% В протягом 6,0 хвилин, утримання 100% протягом додаткових 2,0 хвилин, і зворотно від 100% В до 10% В протягом 1,5 хвилини. Об'ємна 20мл/хв. витрата: Температура колонки: кімнатна температура. Об’єм проби: 1,5мл нерозбавленої неочищеної реакційної суміші. Детектування: МС: API-ES режим іонізації, ділянка сканування маси (100-600 атомних одиниць маси), збір фракцій починається детектування М+1. Параметри ліофілізації Встановлена вихідна замерзання: 1 година при -70°С температура 35 81417 Встановлена температура сушіння фазового конденсатора: -50°С Таблиця сушіння фаз Температура полиці (°С) -60 -40 5 20 Тривалість (хв.) 240 240 480 1000 Встановлений вакуум (мТор) 25 25 25 25 Вихідною речовиною для прикладу 1-1 є Приклад 2 Методика 2А Загальна схема Одержання 3-(1,1-дифенілпропіл)-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцину (2-1) 2,2-Дифенілбутанову кислоту (39,6мг, 0,166ммоль) розчиняють у ДМФА (0,33мл). До розчину додають гексафторфосфат фторΝ,Ν,Ν',Ν"-тетраметилформамідію (TFFH, 43,6мг) і безводний триетиламін (46,4мкл) і розчин охолоджують до 0°С. Через 10 хвилин, додають моногідрат гідразину (6,5мкл) Одержану реакційну суміш перемішують при кімнатній температурі протягом 30 хвилин, після чого ВЕРХ/МС показує повне перетворення у 2,2-дифенілбутангідразид. Додають 8-мегокси-2,3,4,5,6,7-гексагідроазоцин (38мл, 0,249ммоль) і розчин перемішують при 120°С протягом ночі. Суміш нагрівають до кімнатної температури, продукт очищають препаративною ВЕРХ і виділяють у вигляді солі трифтороцтової кислоти. Сіль додають у насичений розчин гідрокарбонату натрію і екстрагують етилацетатом з одержанням вільної основи. Екстракт сушать над сульфатом магнію, фільтрують та упарюють з одержанням очищеного триазолу (2-1) у вигляді твердої білої речовини; МС ESI (m/z) 346,3. 36 Сполуки 2-2 - 2-23 одержують по суті відповідно до цієї ж методики з використанням придатної карбонової кислоти (В.Р.). Утворення продукту контролюють ВЕРХ/МС. 37 81417 38 Методика 2В Загальна схема 39 Одержання 3-[1-(2-фторфеніл)циклобутил]5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцину (2-24) Стадія 1 Гідроксид калію (1,78г) розчиняють у диметилсульфоксиді (5,8мл) [1]. (2Фторфеніл)ацетонітрил (0,97г, 7,2ммоль) і 1,3дибромпропан (0,95мл, 9,3ммоль) розчиняють в етиловому ефірі (2мл), і одержану суміш по краплях при енергійному перемішуванні додають до розчину гідроксиду калію при кімнатній температурі. Суміш перемішують при кімнатній температурі протягом однієї години, потім реакцію гасять додаванням води (3,8мл), охолодженої льодом. Суміш фільтрують через пухкий шар целіту, який промивають ефіром (20мл). Фільтрат переносять у ділильну лійку і водний шар екстрагують ефіром (3´10мл). Органічні шари об'єднують, сушать над сульфатом магнію, фільтрують та упарюють до світло-жовтого масла (1,0г). Чистий 1-(2-фторфеніл)циклобутанкарбонітрил (0,45г) одержують після хроматографії на силікагелі. Стадія 2 1-(2-Фторфеніл)циклобутанкарбонітрил (0,21г, 1,15ммоль) і гідроксид калію (0,194г) розчиняють в етиленгліколі (2мл). Одержану суміш кип'ятять зі зворотним холодильником протягом 3 годин при 198°С, потім виливають у воду (5мл) і екстрагують ефіром (2´5мл). Видний розчин підкислюють НСI та екстрагують ефіром (3´5мл).Екстракти об'єднують, сушать над сульфатом магнію, фільтрують та упарюють з одержанням неочищеної карбонової кислоти. Стадія 3 1-(2-фторфеніл)циклобутанкарбонову кислоту (51,3мг, 0,264ммоль) розчиняють у ДМФА (0,52мл). До одержаного розчину при кімнатній температурі додають гексафторфосфат φτορΝ,Ν,Ν',Ν'-тетраметилформамідію (TFFH, 74,6мг, 0,282ммоль) і безводний триетиламін (71,0мкл, 0,509ммоль). Через 5 хвилин додають безводний гідразин (10мкл, 0,319ммоль). Суміш перемішують при кімнатній температурі протягом 30 хвилин, після чого ВЕРХ-МС показує утворення 1-(2фторфеніл)циклобутанкарбогідразиду з хорошим виходом. 8-Метокси-2,3,4,5,6,7-гексагідроазоцин (47мкл, 0,412ммоль) додають до розчину 1-(2фторфеніл)циклобутанкарбогідразиду і реакційну 81417 40 суміш перемішують при 120°С протягом ночі. Розчин охолоджують, концентрують і продукт очищають препаративною ВЕРХ з одержанням його у вигляді солі трифтороцтової кислоти. Сіль додають до насиченого розчину гідрокарбонату натрію і екстрагують етилацетатом з одержанням вільної основи. Екстракт сушать над сульфатом магнію, фільтрують та упарюють з одержанням очищеного триазолу (2-24) у вигляді твердої речовини. Сполуки 2-25 - 2-32 одержують, по суті, відповідно до цієї ж методики з використанням відповідного фенілацетонітрилу. Утворення продукту контролюють за допомогою ВЕРХ/МС. 41 81417 42 показує, що реакція завершена. Леткі розчинники видаляють у вакуумі і продукт розбавляють водою і промивають гексаном (3мл). Водний розчин підкислюють 6Ν водною хлористоводневою кислотою до рН2. Розчин екстрагують етилацетатом (3´20мл), об'єднані органічні шари промивають розчином солі (5мл), сушать над сульфатом магнію, фільтрують та упарюють з одержанням цільової карбонової кислоти (125мг). Стадія 3 Методика 2С Загальна схема Одержання 3-[1-(3,4дифторфеніл)циклобутил]-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцину (2-33) Стадія 1 (3,4-Дифторфеніл)ацетонітрил перетворюють у 1-(3,4-дифторфеніл)цикло-бутанкарбонітрил відповідно до способу, описаного у методиці 2В, стадія 1. Стадія 2 1-(3,4-Дифторфеніл)циклобутанкарбонітрил (384,5мг, 1,99ммоль) розчиняють у толуолі (30мл) і охолоджують до -78°С. До одержаного розчину по краплях додають гідрид діізобутилалюмінію (DIBAL-H) (1,0Μ розчин у гексанах) (3,98мл, 3,98ммоль). Суміш перемішують при -78°С протягом 30 хвилин, потім додають 5% сірчану кислоту (2мл). Реакційну суміш нагрівають до кімнатної температури, перемішують протягом 20 хвилин і фільтрують через пухкий шар целіту. Целіт промивають етилацетатом, весь фільтрат переносять у ділильну лійку і промивають водою. Органічний шар сушать над сульфатом натрію та упарюють з одержанням цільового альдегіду. 1-(3,4-Дифторфеніл)циклобутанкарбальдегід (240,0мг, 1,22ммоль) розчиняють у суміші третбутанол/тетрагідрофуран/2-метилбут-2-ен (3,0мл/1,0мл/1,0мл) і енергійно перемішують при кімнатній температурі. Хлорит натрію (243,4мг, 2,69ммоль) і дигідрофосфат натрію (370,4мг, 2,68ммоль) розчиняють у воді (1,2мл) і по краплях додають до одержаного раніше розчину. Суміш перемішують протягом години, після чого ТШХ 1-(3,4-Дифторфеніл)циклобутанкарбонову кислоту піддають перетворенню у 3-[1-(3,4дифторфеніл)циклобутил]-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин (2-33) відповідно до способу, описаного у методиці 2В, стадія 3; МС ESI (m/z) 318,2. Сполуки 2-34 - 2-38 одержують по суті відповідно до цієї ж методики, використовуючи відповідний дизаміщений фенілацетонітрил. Утворення продукту контролюють ВЕРХ/МС. 43 81417 44 50%; в інтервалі від 16 до 21 хвилини знову до 100% В і затримка 100% В протягом 2 хвилин; і від 100% В до 10% В протягом 1 хвилини. 20мл/хв. Методика 2D Загальна схема Одержання 3-(1-(4-хлорфеніл)циклогексил)5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцину (2-39) Метил 1-(4хлорфеніл)циклогексанкарбоксилат (277мг) і гідразингідрат (0,30мл) розчиняють в етиленгліколі (5мл), нагрівають до 150°С і витримують при цій температурі протягом 15 годин. Розчин охолоджують і додають воду (5мл). Осад, що утворюється, відфільтровують і сушать у вакуумі, одержуючи ацилгідразид (108мл) у вигляді твердої білої речовини. Безводний толуол додають до суміші 1-(4хлорфеніл)циклогексан-карбогідразиду (62мг) і 8метокси-2,3,4,5,6,7-гексагідроазоцину (40,1мг). Реактор нагрівають до 120°С і витримують при цій температурі протягом ночі, після чого охолоджують до кімнатної температури і розчинник випарюють. Неочищений продукт очищають колонковою хроматографією, одержуючи 3-(1-(4-хлорфеніл)циклогексил)5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3-а]азоцин (2-39) у вигляді твердої білої речовини. Метод препаративної РХ для прикладу 2: Колонка: YMC-PACK ODS, 100мм´20мм, 5,0мкм. Елюент А: 0,05% ТФОК у воді. Елюент В: 0,05% ТФОК в ацетонітрилі. Врівноваження перед упорскуванням: 1,0 хвилина. Затримка після 1,0 хвилина. упорскування: Градієнт: від 10% В до 100% В: в інтервалі від 1 до 16 хвилини зворотно до Об'ємна витрата: Температура кімнатна температура. колонки: Об'єм проби: 5,0мл. Детектор: Фотодіодна матриця. Аналітичний метод РХ для прикладу 2: Колонка: Waters-XTerra С-18А, 5мкм, 4,6мм´50мм. Елюент А: 0,60% ТФОК у воді. Елюент В: 0,50% ТФОК в ацетонітрилі. Градієнт: від 10% В до 90% В протягом 4,5 хвилин, затримка протягом 0,5 хвилини і зворотно до 10% В протягом 0,5 хвилини. Температура колонки: 30°С. Об'єм проби: 10мкл нерозбавленої неочищеної реакційної суміші. Детектування: DAD: 190-600нм. MC: API-Ε S режим позитивної іонізації, Змінний інтервал сканування маси: LCl-Xlo=50-500 атомних одиниць маси LCl-Low= 150-750 атомних одиниць маси LCl-Med=300-1000 атомних одиниць маси LCl-High=500-2000 атомних одиниць маси Приклад 3 Методика 3А Одержання хлорфеніл)циклобутанкарбогідразиду 1-(4 1-(4-Хлорфеніл)циклобутанкарбонову кислоту (10,0г) розчиняють у дихлорметані (150мл) і охолоджують до -10°С на бані із сумішшю лід/розчин солі. До одержаного розчину додають піридин (3,84мл) і потім ціанурфторид (8,9мл у 25мл дихлорметану). Суміш перемішують при кімнатній температурі протягом години, після чого ТШХ показує, що реакція завершена. Розчин переносять у ділильну лійку, що містить лід (150мл). Після енергійного струшування органічний шар видаляють, сушать над сульфатом магнію, фільтрують та упарюють з одержанням карбонілфториду. Безводний гідразин (2,02мл) розчиняють в ацетонітрилі (100мл) і охолоджують до 0°С. Додають триетиламін (12,8мл) і потім 1-(4хлорфеніл)циклобутанкарбонілхлорид (10г) в ацетонітрилі (25мл). Розчин перемішують при кімнатній температурі протягом години, після чого ацетонітрил видаляють випарюванням. Продукт одержують після хроматографії на силікагелі. Методика 3В 45 Одержання 1 хлорфеніл)циклопропанкарбогідразиду 81417 -(4 1-(4-Хлорфеніл)циклопропанкарбогідразид одержують відповідно до методики 3А, використовуючи 1-(4хлорфеніл)циклопропанкарбонову кислоту. Методика 3С Одержання 1-(4фторфеніл)циклобутанкарбогідразиду Стадія 1 Гідроксид калію (8,2г, 146,1ммоль) розчиняють у диметилсульфоксиді (100мл) [1]. (4Фторфеніл)ацетонітрил (6,87г, 50,8ммоль) і 1,3дибромпропан (56,4ммоль) розчиняють в етиловому ефірі (10мл) і одержану суміш при енергійному перемішуванні по краплях додають до розчину гідроксиду калію при кімнатній температурі. Суміш перемішують протягом двох годин, після чого реакцію гасять додаванням води (100мл), охолодженої льодом. Суміш фільтрують через пухкий шар целіту, який промивають ефіром (10мл). Фільтрат переносять у ділильну лійку і водний шар екстрагують ефіром (3´100мл). Органічні шари об'єднують, сушать над сульфатом магнію, фільтрують та упарюють, одержуючи продукт (8,85г) у вигляді блідо-жовтого масла. Стадія 2 Неочищений 1-(4фторфеніл)циклобутанкарбонітрил (8,85г, 50,5ммоль) розчиняють у безводному толуолі (100мл) і охолоджують до -78°С. До одержаного розчину по краплях додають гідрид діізобутилалюмінію (DIBAL-H) (1,0Μ розчин у гексанах, 60,6мл). Реакцію контролюють ТШХ (гексан:етилацетат 9:1). Суміш перемішують при 78°С протягом години, після чого додають 5% сірчану кислоту (20мл). Реакційну суміш нагрівають до кімнатної температури, перемішують протягом 20 хвилин і фільтрують через пухкий шар целіту. Целіт промивають етилацетатом, весь фільтрат переносять у ділильну лійку і промивають водою. Органічний шар сушать над сульфатом натрію, фільтрують та упарюють досуха, одержуючи цільовий-альдегід. 1-(4-Дифторфеніл)циклобутанкарбальдегід (8,8г, 49,4ммоль) розчиняють у трет-бутанолі (90мл), тетрагідрофурані (30мл) і 2-метилбут-2-ені (30мл) і енергійно перемішують при кімнатній температурі. Хлорит натрію (9,8г, 108,7ммоль) і дигідрофосфат натрію (15,0г, 108,7ммоль) розчиняють у воді (54мл) і по краплях додають до 46 одержаного раніше розчину. Суміш перемішують протягом години, після чого ТШХ показує, що реакція завершена. Леткі розчинники видаляють у вакуумі, продукт розбавляють водою і потім промивають гексаном (3мл). Водний розчин підкислюють 6N водною хлористоводневою кислотою до рН2. Розчин екстрагують етилацетатом (3´150мл), об'єднані органічні шари промивають розчином солі (20мл), сушать над сульфатом магнію, фільтрують та упарюють, одержуючи 1-(4-фторфеніл)циклобутанкарбонову кислоту (8,0г). Одержану карбонову кислоту піддають перетворенню в 1-(4-фторфеніл)циклобутанкарбогідразид відповідно до способу, описаного у методиці 3А. Методика 3D Одержання 1 -(4-фторфеніл )циклопропанкарбогідразиду 1-(4-Фторфеніл)ацетонітрил (3,77г, 27,9ммоль), 1-бром-2-хлоретан (5,0г, 34,9ммоль) і хлорид бензилтриетиламонію (ТЕВАС, 127,6мг, 0,56ммоль) додають у колбу і енергійно перемішують [2]. До одержаного розчину по краплях додають гідроксид калію (50% у воді, 195ммоль). Суміш перемішують при 40°С протягом 5 годин і протягом ночі при кімнатній температурі, реакційну суміш розбавляють водою і екстрагують дихлорметаном. Органічний шар відділяють, промивають 1N водною хлористоводневою кислотою, водою і сушать над сульфатом магнію. Одержаний розчин фільтрують і дихлорметан випарюють, одержуючи неочищений продукт (4,5г). 1-(4-Фторфеніл)циклопропанкарбонову кислоту одержують з неочищеного 1-(4фторфеніл)циклопропілкарбонітрилу відповідно до способу, описаного у методиці 3С, стадія 2. Одержану карбонову кислоту піддають перетворенню в 1-(4фторфеніл)циклопропанкарбогідразид відповідно до методики 3А. Методика 3Е Загальна схема Одержання 3,4-дициклопропіл-5-(1фенілциклобутил)-4Н-1,2,4-триазолу (3-1) 47 Метилтрифторметансульфонат (89,1мкл) додають до N-циклопропілциклопропанкарбоксаміду (98,6мг, 0,788ммоль). Одержану суміш перемішують протягом 30 хвилин при 60°С, після чого ЯМР чітко показує перетворення у метил Nциклопропілциклопропанкарбоксімідоат. Толуол (2мл), триетиламін (223мкл) і 1фенілциклобутанкарбогідразид (90мг) додають до метил N-циклопропілциклопропанкарбоксімідоату і перемішують при 60°С протягом 3 годин, потім при 110°С протягом 1 години. Суміш охолоджують та упарюють, залишок очищають препаративною ВЕРХ, одержуючи продукт у вигляді солі трифтороцтової кислоти. Сіль додають до насиченого розчину гідрокарбонату натрію та екстрагують етилацетатом, одержуючи вільну основу. Органічний екстракт сушать над сульфатом магнію, фільтрують та упарюють з одержанням 3,4-дициклопропіл-5-(1фенілциклобутил)-4Н-1,2,4-триазолу (3-1); МС ESI (m/z) 280,2. Іншу сполуку прикладу 3 одержують по суті відповідно до цієї ж методики, використовуючи відповідні карбоксамід і ацилгідразид. Як розчинник при одержанні 3-2 використовують ацетонітрил. Сполуки 3-19 виділяють як побічний продукт у синтезі 3-18. Метиламіди одержують з їх відповідних складних ^ метилових ефірів і метиламіну з використанням добре відомих методик. Інші аміди стандартно одержують з комерційно доступних карбонових кислот і амінів, використовуючи 1-(диметиламінопропіл)-3етилкарбодіімід гідрохлорид як реагент і методики, описані у літературі. Одержання ацилгідразидів описане у методиках 3А, 3В, 3С і 3D. 81417 48 49 81417 50 51 Метод препаративної ВЕРХ для прикладу 3: Використовують методику, описану у прикладі 2. Метод аналітичної РХ для прикладу 3: Використовують методики, ідентичні описаним у прикладі 2. Приклад 4 Методика 4А Одержання 3-[1-(4-хлорфеніл)-(Z)-3(метоксиметокси)циклобутил]-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцину (4-1) і 3-[1(4-хлорфеніл)-(Е)-3-(метоксиметокси)циклобутил]5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцину (4-2) 81417 52 Гідроксид калію (2,57г) розчиняють у диметилсульфоксиді (8,0мл). (4Хлорфеніл)ацетонітрил (1,58г, 10,4ммоль) і 1,3дихлор-2-(метокси-метокси)пропан (1,993г) розчиняють у діетиловому ефірі (3мл) і одержану суміш додають по краплях до розчину гідроксиду калію з енергійним перемішуванням при кімнатній температурі. Суміш перемішують при кімнатній температурі протягом години, після чого реакцію гасять додаванням води (5,5мл), охолодженої льодом. Суміш фільтрують через пухкий шар целіту, який промивають ефіром (30мл). Фільтрат переносять у ділильну лійку і водний шар екстрагують ефіром (3´15мл). Органічні шари об'єднують, сушать над сульфатом магнію, фільтрують та упарюють. Продукт очищають хроматографією на силікагелі, одержуючи 1-(4хлорфеніл)-3(метоксиметокси)циклобутанкарбонітрил (1,28г) у вигляді суміші ізомерів (-2:1). Нітрил (1,28г) і гідроксид калію (2,2г) розчиняють в етиленгліколі (13мл). Суміш витримують протягом шести годин при 198°С, після чого охолоджують до кімнатної температури, виливають у воду (15мл) і промивають ефіром (2´20мл). Водний розчин обережно підкислюють водною хлористоводневою кислотою і екстрагують ефіром (2´20мл). Органічні шари об'єднують, сушать над сульфатом магнію, фільтрують та упарюють, одержуючи продукт у вигляді коричневого масла (0,9068г). 1-(4-Хлорфеніл)-3(метоксиметокси)циклобутанкарбонову кислоту (0,9068г) і піридин (0,40мл) розчиняють у дихлорметані (12мл) і охолоджують до -10°С. Ціанурфторид (1,0мл) розчиняють у дихлорметані (2мл) і по краплях додають до реакційної суміші. Через 30 хвилин, реакційну суміш переносять у ділильну лійку, що містить лід (10мл). Після енергійного струшування дихлорметановий шар видаляють, сушать над сульфатом магнію, фільтрують та упарюють. Неочищений фторангідрид розчиняють в ацетонітрилі (3мл) і додають при перемішуванні до розчину безводного гідразину (140мкл), триетиламіну (1,0мл) і ацетонітрилу (15мл) при 0°С. Через 10 хвилин, реакцію завершують за допомогою ВЕРХ/МС і сушать у вакуумі. Частину неочищеного 1-(4-хлорфеніл)-3(метоксиметокси)циклобутан-карбогідразиду (456,1мг) розчиняють у безводному толуолі (7мл) і змішують з 8-метокси-2,3,4,5,6,7гексагідроазоцином (228мкл). Розчин нагрівають до 120°С і витримують при цій температурі протягом 3 годин, потім повільно охолоджують до 53 кімнатної температури. Продукт частково очищають хроматографією на силікагелі (100% етилацетат →5% метанол в етилацетаті →10% метанол в етилацетаті), одержуючи суміш 4-1 і 4-2 у співвідношенні 62:38, відповідно. Ізомери розділяють препаративною ВЕРХ і виділяють у вигляді їх солей трифтороцтової кислоти. Кожну сіль окремо додають до насиченого розчину гідрокарбонату натрію і екстрагують етилацетатом. Очищені вільні основи 3-[1-(4хлорфеніл)-цис-3-(метоксиметокси)циклобутил]-r5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-1) і 3-[1-(4-хлорфеніл)-транс-3(метоксиметокси)циклобутил]-r-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-2) сушать над сульфатом магнію, фільтрують і концентрують. Ізомери, 4-1 і 4-2, більш ефективно розділяють хіральною препаративною ВЕРХ (ChiralPak OD (Daicel Chemical Industries), колонка 2см´25см, 20% ізопропанол/гептан, 6мл/хв.), МС ESI (m/z) 376,2. Методика 4В Одержання 3-(4-хлорфеніл)-цис-3(5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцин-3-іл)циклобутан-r-олу (4-3) 3-[1-(4-Хл орфеніл)-цис-3(метоксиметокси)циклобутил]-r-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-1) (53мг) розчиняють у дихлорметані (1мл) і перемішують при кімнатній температурі. До одержаного розчину додають трифтороцтову кислоту (0,2мл) і розчин перемішують протягом ночі при кімнатній температурі. Леткі розчинники видаляють у вакуумі, і залишок очищають хроматографією на силікагелі, одержуючи 3-(4-хлорфеніл)-г/мс-3(5,6,7,8,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцин-3-іл)циклобутан-r-ол (4-3) у вигляді твердої білої речовини. 3-(4-Хлорфеиіл)-транс-3-(5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин-3іл)циклобутан-r-ол (4-4) одержують по суті відповідно до цієї ж методики, використовуючи епімерну вихідну речовину (4-2). 81417 54 Методика 4С Одержання 3-(4-хлорфеніл)-3-(5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин-3іл)циклобутанону (4-5) Суміш спиртів (4-3 і 4-4) (114,1мг) розчиняють у дихлорметані (5мл) і охолоджують до 0°С. До одержаного розчину додають перутенат тетрапропіламонію (ТРАР, 12,1мг) і 4метилморфолін N-оксид (60,4мг) і реакційну суміш перемішують при кімнатній температурі протягом трьох годин. Після цього неочищену реакційну суміш завантажують безпосередньо на колонку з силікагелем і очищають (100% дихлорметан →5% метанол у дихлорметані →10% метанол у дихлорметані), одержуючи 3-(4-хлорфеніл)-3(5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцин-3-іл)циклобутанон (4-5); МС ESI (m/z) 330,1. Методика 4D Одержання 3-[1-(4-хлорфеніл)-3метиленциклобутил]-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцину (4-6) 3-(4-Хлорфеніл)-3-(5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин-3іл)циклобутанон (4-5) (52мг) розчиняють у свіжоперегнаному тетрагідрофурані (2мл). До одержаного розчину додають бромід метилтрифенілфосфонію (281мг) і потім біс(триметилсиліл)амід калію (KHMDS, 0,5Μ у толуолі, 1,25мл). Реакційну суміш перемішують протягом 24 годин при кімнатній температурі, після чого неочищений продукт додають до насиченого розчину гідрокарбонату натрію і екстрагують 55 етилацетатом. Органічний шар збирають сушать над сульфатом магнію, .фільтрують і концентрують. Продукт очищають колонковою хроматографією на силікагелі, одержуючи 3-[1-(4хлорфеніл)-3-метилен-циклобутил]-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-6); МС ES (m/z) 328,2. Методика 4Е Одержання 3-[1-(4-хлорфеніл)-3,3Дифторциклобутил]-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцину (4-7) 3-(4-Хлорфеніл)-3-(5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин-3іл)циклобутанон (4-5) (11,4мг) розчиняють у дихлорметані (1мл). До одержаного розчину додають трифторид (діетиламіно)сірки (DAST, 73мкл) і розчин перемішують при кімнатній температурі протягом 24 годин. Розчин виливають у насичений водний розчин гідрокарбонату натрію і екстрагують дихлорметаном. Органічний шар сушать над сульфатом магнію, фільтрують і концентрують. Залишок очищають хроматографією на силікагелі (100% дихлорметан 1% метанол у дихлорметані 5% метанол у дихлорметані), одержуючи 3-[1-(4-хлорфеніл)-3,3дифторциклобутил]-5,б,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-7); МС ESI (m/z): 352,1. Методика 4F Одержання 3-[1-(4-хлорфеніл)-траис-3фторциклобутил]-r-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцину (4-8) 3-(4-Хлорфеніл)-цис-3-(5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин-3іл)циклобутан-r-ол (4-3) (21,3мг) розчиняють у безводному дихлорметані (1,5мл) і охолоджують до 0°С. До одержаного розчину додають трифторид (діетиламіно)сірки (DAST, 80мкл). Розчин нагрівають до кімнатної температури і перемішують протягом ночі. Продукт виливають у насичений водний розчин бікарбонату натрію і екстрагують дихлорметаном. Органічний шар сушать над сульфатом магнію, фільтрують і концентрують. Залишок очищають хроматографією на силікагелі (100% дихлорметан →1% метанол у дихлорметані →5% метанол у дихлорметані), одержуючи 3-[1-(4-хлорфеніл) 81417 56 трйнс-3-фторциклобутил]-r-(5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин(4-8). 3-[1-(4-Хлорфеніл)-транс-3-фторциклобутил]-r(5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-9) одержують, по суті, відповідно до цієї ж методики, використовуючи епімерну вихідну речовину (4-4). Методика 4G Одержання 3-(3-метил-1-фенілциклобутил)5,6,7,8,9,10-гекcагідро[1,2,4]триазоло[4,3а]азоцину (4-10) 2-Фенілацетогідразин (1,01г) додають до розчину безводного толуолу (11мл) і 8метокси~2,3,4,5,6,7-гексагідроазоцину (0,96мл). Суміш витримують при 60°С протягом 3 годин, потім при 110°С протягом ночі. Розчин охолоджують до кімнатної температури і концентрують. Залишок очищають хроматографією на силікагелі, одержуючи 3бензил-5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3а]азоцин у вигляді твердої білої речовини. 3-Бензил-5,6,7,8,9,10гексагідро[1,2,4]триазоло[4,3-а]азоцин (287,6мг) і 1-бром-3-хлор-2-метилпропан (140мкл) розчиняють у безводному тетрагідрофурані, вивільненому від кисню, і розчин охолоджують до 40°С в атмосфері аргону. До одержаного розчину по краплях додають біс(триметилсиліл)амід калію (KHMDS, 0,5Μ у толуолі, 2,5мл). Через 30 хвилин, додають другу аліквоту KHMDS (2,5мл). Ще через 30 хвилин знову додають KHMDS (2,15мл) і розчину дають можливість повільно нагрітися до кімнатної температури. Через одну годину, реакцію гасять водою і реакційну суміш додають у розчин солі. Суміш екстрагують етилацетатом, органічний шар сушать сульфатом магнію, фільтрують, упарюють і очищають хроматографією на силікагелі, одержуючи 3-[1-(4хлорфеніл)-(Z)-3-(метоксиметокси)циклобутил] 57 81417 58 5,6,7,8,9,10-гексагідро[1,2,4]триазоло[4,3-а]азоцин (4-10) у вигляді суміші ізомерів (~1,2:1); МС ESI (m/z): 296,2. Методика 4Н Одержання 1-(4-хлорфеніл)-транс-3фторциклобутан-r-карбогідразиду (4-Хлорфеніл)ацетонітрил (14,04г) розчиняють у свіжоперегнаному тетрагідрофурані (250мл) і перемішують при -78°С в атмосфері аргону [1]. До одержаного розчину по краплях додають метиллітій (LiBr-комплекс, 1,5Μ у діетиловому ефірі, 62мл, 1екв.) так, щоб температура реакції зберігалася на рівні нижче -66°С. Розчин перемішують протягом години при -78°С, при цьому колір розчину змінюється від жовтого до глибокого червоного. До розчину по краплях додають епібромгідрин і розчин перемішують протягом додаткових 90 хвилин. У розчин додають йодид метилмагнію (3,0М у діетиловому ефірі, 31мл), і розчин, який стає світло-коричневим при повільному нагріванні до кімнатної температури, перемішують протягом ночі. Реакцію гасять водою (75мл) і підкислюють до рН2 5N водною хлористоводневою кислотою (~30мл). Розчин солі додають доти, доки шари не розділяться. Органічний шар збирають, водний шар повторно екстрагують діетиловим ефіром (2´50мл). Органічні шари об'єднують, сушать сульфатом магнію, фільтрують і концентрують. Неочищений 1-(4-хлорфеніл)-3гідроксициклобутан-1-карбонітрил (суміш цис:транс ізомерів зі співвідношенням приблизно 4,2:1) розчиняють у дихлорметані (150мл) і перемішують при 0°С. До розчину додають піридин (11,3мл) і потім бензоїлхлорид (10,8мл), розчин нагрівають до кімнатної температури і перемішують протягом 2,5 годин. Потім додають додаткову кількість піридину (2мл) і бензоїлхлориду (2мл) і реакційну суміш перемішують при 30°С протягом ночі. Реакційний розчин додають до насиченого розчину гідрокарбонату натрію і екстрагують дихлорметаном. Органічний шар промивають насиченим хлоридом амонію, сушать над хлоридом магнію, фільтрують і концентрують, одержуючи масло червонуватого кольору. Два ізомери розділяють хроматографією на силікагелі (25% дихлорметан/гексани →33% дихлорметан/гексани →50% дихлорметан/гексани →100% дихлорметан), одержуючи цільовий 3-(4хлорфеніл)-цис-3-ціаноциклобугилбензоат (18,63г). 3-(4-Хлорфеніл)-цис-3ціаноциклобутилбензоат (6,42г) розчиняють у суміші метанол/тетрагідрофуран (10мл/20мл) і перемішують при кімнатній температурі. Гідроксид літію моногідрат (1,1г) розчиняють у воді (10мл) і додають у розчин бензоату. Через 10 хвилин, додають твердий хлорид амонію (~2г) і леткі розчинники випарюють. Водну суміш, що залишилася, екстрагують діетиловим ефіром, органічний шар сушать сульфатом магнію, фільтрують і концентрують, одержуючи цільовий циклобутанол. Наважку 1-(4-хлорфеніл)-цис-3гідроксициклобутан-r-карбонітрилу (1,13г) розчиняють у безводному дихлорметані і перемішують при 0°С. У розчин додають трифторид (діетиламіно)сірки (DAST, 1,43г), розчин нагрівають до 40°С і витримують при цій температурі протягом 10 годин. Додають додаткову кількість DAST (0,5мл) і реакційний розчин перемішують при 40°С протягом ночі. Розчин охолоджують, додають насичений водний розчин гідрокарбонату натрію і двічі екстрагують дихлорметаном. Органічні екстракти об'єднують, сушать сульфатом магнію, фільтрують і концентрують. Неочищений залишок обережно хроматографують на силікагелі (10% етилацетат/гексани →20% етилацетат/гексани →25% етилацетат/гексани), одержуючи 1-(4хлорфеніл)-транс-3-фторциклобутан-r-карбонітрил (1,024г). 1-(4-Хлорфеніл)-транс-3-фторциклобутан-rкарбонітрил (1,65г) розчиняють у безводному толуолі (30мл) і охолоджують до -78°С. Розчин гідриду діізобутилалюмінію (DIBAL, 1Μ у гексанах, 9,4мл) додають протягом 10 хвилин, і одержаний розчин перемішують протягом 30 хвилин. Реакцію гасять додаванням 5% сірчаної кислоти (2,5мл), і суміш нагрівають до кімнатної температури. Через 1 годину, суміш фільтрують через пухкий шар целіту. Целіт промивають етилацетатом і весь фільтрат виливають у воду (20мл). Шари розділяють, і водний розчин екстрагують етилацетатом. Органічні шари об'єднують, сушать над сульфатом магнію, фільтрують і концентрують. Неочищений альдегід розчиняють у суміші трет-бутанол/тетрагідрофуран/2-метилбут-2-ен (15мл/5мл/5мл) і одержаний розчин перемішують при кімнатній температурі. Хлорид натрію (1,56г) і 59 дигідрофосфат натрію (2,39г) розчиняють у воді (7мл) і додають до розчину при енергійному перемішуванні. Через 80 хвилин леткі розчинники видаляють у вакуумі і суміш підкислюють до рН2 водною 1N хлористоводневою кислотою. Продукт екстрагують етилацетатом (3´30мл). Екстракти об'єднують, сушать над сульфатом магнію, фільтрують та упарюють, одержуючи цільову карбонову кислоту. 1-(4-Хлорфеніл)-транс-3-фторциклобутан-rкарбонову кислоту (5,68г) розчиняють у суміші дихлорметан/метанол (40мл/10мл). До одержаного розчину додають (триметилсиліл)діазометан (15мл, 2,0Μ у гексанах) до одержання жовтого забарвлювання, що не зникає. Розчин перемішують при кімнатній температурі протягом 1 години, після чого ТШХ показує, що реакція завершена. Для гасіння (гриметилсиліл)діазометану додають оцтову кислоту (2мл) і розчин концентрують. одержуючи 1-(4-хлорфеніл)-транс-3-фторциклобутан-rкарбоксилат. Неочищений складний метиловий ефір (5,8г) розчиняють у толуолі (15мл). Додають безводний гідразин (3,1мл, 98,8ммоль) і реакційну суміш кип'ятять зі зворотним холодильником протягом двох днів. Розчин охолоджують до кімнатної температури і толуол видаляють у вакуумі, продукт очищають хроматографією на силікагелі (100% етилацетат), одержуючи 1-(4-хлорфеніл)транс-3-фторциклобутан-r-карбогідразид у вигляді твердої білої речовини (4,82г). Методика 41 Загальна схема 81417 60 годин. Розчин охолоджують, потім концентрують і залишок очищають хроматографією на силікагелі (100% етилацетат →1% метанол в етилацетаті 3% метанол в етилацетаті →5% метанол в етилацетаті), одержуючи очищений 3-[1-(4хлорфеніл)-транс-3-фторциклобутил]-4,5-дициклопропіл-r-4Н-1,2,4-триазол (4-11). Сполуки 4-12 - 4-15 одержують, по суті, відповідно до цієї ж методики, використовуючи відповідний карбоксамід як вихідну речовину і 1-(4хлорфеніл)-трднс-3-фторциклобутан-rкарбогідразид. Одержання 3-[1-(4-хлорфеніл)-транс-3фторциклобутил]-4,5-дициклопропіл-r-4Н-1,2,3триазолу (4-11) Метил трифторметансульфонат (84,1мкл) додають до N-циклопропілциклопропанкарбоксаміду (93,0мг). Суміш нагрівають до 65°С, витримують при цій температурі протягом 2 хвилин, потім охолоджують до кімнатної температури. Толуол (1мл), триетиламін (207мкл) і 1-(4-хлорфеніл)транс-3-фторциклобутан-r-карбогідразид (108мг) додають до метил N-циклопропілциклопропанкарбоксімідоату і одержану суміш перемішують при 60°С протягом ночі і при 115°С протягом 2 Метод препаративної ВЕРХ для прикладу 4: Використовують метод препаративної ВЕРХ, описаний у прикладі 2. Аналітичний метод РХ ідентичний методу, описаному у прикладі 2. У той час, як в описі наведені переважні втілення даного винаходу, мається на увазі, що множина альтернативних втілень також входить в об'єм, що визначається формулою винаходу. Отже, винахід визначений ширше, ніж окремі втілення, розкриті в описі.
ДивитисяДодаткова інформація
Назва патенту англійською11-beta-hydroxysteroid dehydrogenase 1 inhibitors useful for the treatment of diabetes, obesity and dyslipidemia
Автори англійськоюOlson Steven, Zhu Yuping
Назва патенту російськоюИнгибиторы 11-бета-гидроксистероидной дегидрогеназы 1, пригодные для лечения сахарного диабета, ожирения и дислипидемии
Автори російськоюОлсон Стивен, Зху Юпинг
МПК / Мітки
МПК: A61P 43/00, C07D 249/08, A61K 31/433, A61P 25/08, A61K 31/4196, A61P 3/10, C07D 487/04, A61P 9/10, A61P 9/14, A61P 3/08, A61P 13/12, C07D 417/04, A61P 27/02, A61P 5/50, A61P 3/06, C07D 403/04, A61P 1/18, C07D 405/04, A61P 3/04, A61P 5/48, A61P 9/12, A61P 25/00
Мітки: цукрового, 11-бета-гідроксистероїдної, інгібітори, дисліпідемії, ожиріння, придатні, діабету, лікування, дегідрогенази
Код посилання
<a href="https://ua.patents.su/31-81417-ingibitori-11-beta-gidroksisterodno-degidrogenazi-1-pridatni-dlya-likuvannya-cukrovogo-diabetu-ozhirinnya-i-dislipidemi.html" target="_blank" rel="follow" title="База патентів України">Інгібітори 11-бета-гідроксистероїдної дегідрогенази 1, придатні для лікування цукрового діабету, ожиріння і дисліпідемії</a>
Попередній патент: Спосіб визначення акумуляції нікелю рослинами
Наступний патент: Спосіб відновлення екологічного балансу водоймища
Випадковий патент: Спосіб відновлення порушень портопечінкової гемодинаміки у хворих з доброякісною обтураційною жовтяницею