Спосіб лікування колоректального раку або симптому колоректального раку комбінацією, яка містить афліберцепт, фолінову кислоту, 5-фторурацил і іринотекан
Формула / Реферат
1. Спосіб лікування колоректального раку (CRC) або симптому колоректального раку (CRC) у пацієнта, що цього потребує, де спосіб включає стадію на якій вводять вказаному пацієнту комбінацію, яка містить афліберцепт, фолінову кислоту, 5-фторурацилу (5-FU) і іринотекан, причому афліберцепт вводять в дозі від приблизно 1 мг/кг до приблизно 10 мг/кг, і фолінову кислоту, 5-фторурацил (5-FU) й іринотекан вводять у терапевтично ефективних кількостях.
2. Спосіб за п. 1, в якому вказаний пацієнт вже піддавався лікуванню у відношенні CRC або симптому CRC.
3. Спосіб за будь-яким з пп. 1-2, в якому вказаний пацієнт раніше піддавався лікуванню з використанням хіміотерапії, променевої терапії або хірургічного втручання.
4. Спосіб за будь-яким з пп. 1-3, в якому вказаний пацієнт раніше піддавався лікуванню з використанням терапії на основі оксаліплатину або бевацизумабу.
5. Спосіб за п. 1 або 2, в якому вказаний пацієнт дав незадовільний результат хіміотерапії, променевої терапії або хірургічного втручання.
6. Спосіб за будь-яким з пп. 1-5, в якому колоректальний рак являє собою метастатичний колоректальний рак (МCRC).
7. Спосіб за будь-яким з пп. 1-6, в якому афліберцепт, фолінову кислоту, 5-фторурацил (5-FU) й іринотекан вводять послідовно.
8. Спосіб за будь-яким з пп. 1-6, в якому афліберцепт, фолінову кислоту, 5-фторурацил (5-FU) й іринотекан вводять розтягнуто протягом періоду часу для отримання максимальної ефективності комбінації.
9. Спосіб за будь-яким з пп. 1-8, в якому пацієнту вводять фолінову кислоту в дозі від 200 мг/м2 до 600 мг/м2, 5-фторурацил (5-FU) в дозі від 2000 мг/м2 до 4000 мг/м2, іринотекан в дозі від 100 мг/м2 до 300 мг/м2 і афліберцепт в дозі від 1 мг/кг до 10 мг/кг.
10. Спосіб за будь-яким з пп. 1-9, в якому пацієнту вводять фолінову кислоту в дозі, що становить приблизно 400 мг/м2, 5-фторурацил (5-FU) в дозі, що становить приблизно 2800 мг/м2, іринотекан в дозі, що становить приблизно 180 мг/м2, і афліберцепт в дозі, що становить 4 мг/кг.
11. Спосіб за будь-яким з пп. 1-10, в якому фолінову кислоту вводять внутрішньовенно в дозі, що становить приблизно 400 мг/м2, 5-фторурацил (5-FU) вводять внутрішньовенно в дозі, що становить приблизно 2800 мг/м2, іринотекан вводять внутрішньовенно в дозі, що становить приблизно 180 мг/м2, афліберцепт вводять внутрішньовенно в дозі, що становить приблизно 4 мг/кг, і в якому комбінацію вводять кожні два тижні.
12. Спосіб за будь-яким з пп. 1-11, в якому фолінову кислоту, 5-фторурацил (5-FU), іринотекан і афліберцепт вводять внутрішньовенно кожні два тижні протягом періоду часу, що укладається між 9 і 18 тижнями.
13. Спосіб за будь-яким з пп. 1-12, в якому фолінову кислоту вводять внутрішньовенно відразу ж після введення афліберцепту.
14. Спосіб за будь-яким з пп. 1-13, в якому фолінову кислоту вводять внутрішньовенно відразу ж після введення афліберцепту протягом періоду часу, що складає приблизно 2 години.
15. Спосіб за будь-яким з пп. 1-14, в якому іринотекан вводять внутрішньовенно відразу ж після введення афліберцепту.
16. Спосіб за будь-яким з пп. 1-15, в якому іринотекан вводять внутрішньовенно відразу ж після введення афліберцепту протягом періоду часу, що складає приблизно 90 хвилин.
17. Спосіб за будь-яким з пп. 1-16, в якому 5-фторурацил (5-FU) вводять відразу ж після введення афліберцепту.
18. Спосіб за будь-яким з пп. 1-17, в якому першу частку 5-фторурацилу (5-FU) вводять внутрішньовенно відразу ж після введення афліберцепту, а другу частку 5-FU вводять внутрішньовенно після введення першої частки у вигляді безперервної інфузії.
19. Спосіб за будь-яким з пп. 1-18, в якому приблизно 400 мг/м2 5-фторурацилу (5-FU) вводять внутрішньовенно протягом періоду часу, що становить 2-4 хвилини, після введення афліберцепту, і в якому 2400 мг/м2 5-FU вводять внутрішньовенно протягом майже 46 годин після введення 400 мг/м2 у вигляді безперервної інфузії.
20. Спосіб за будь-яким з пп. 1-19, в якому пацієнт має метастази в печінці.
21. Спосіб за будь-яким з пп. 1-6, в якому афліберцепт, фолінову кислоту, 5-фторурацил (5-FU) й іринотекан вводять одночасно.
Текст
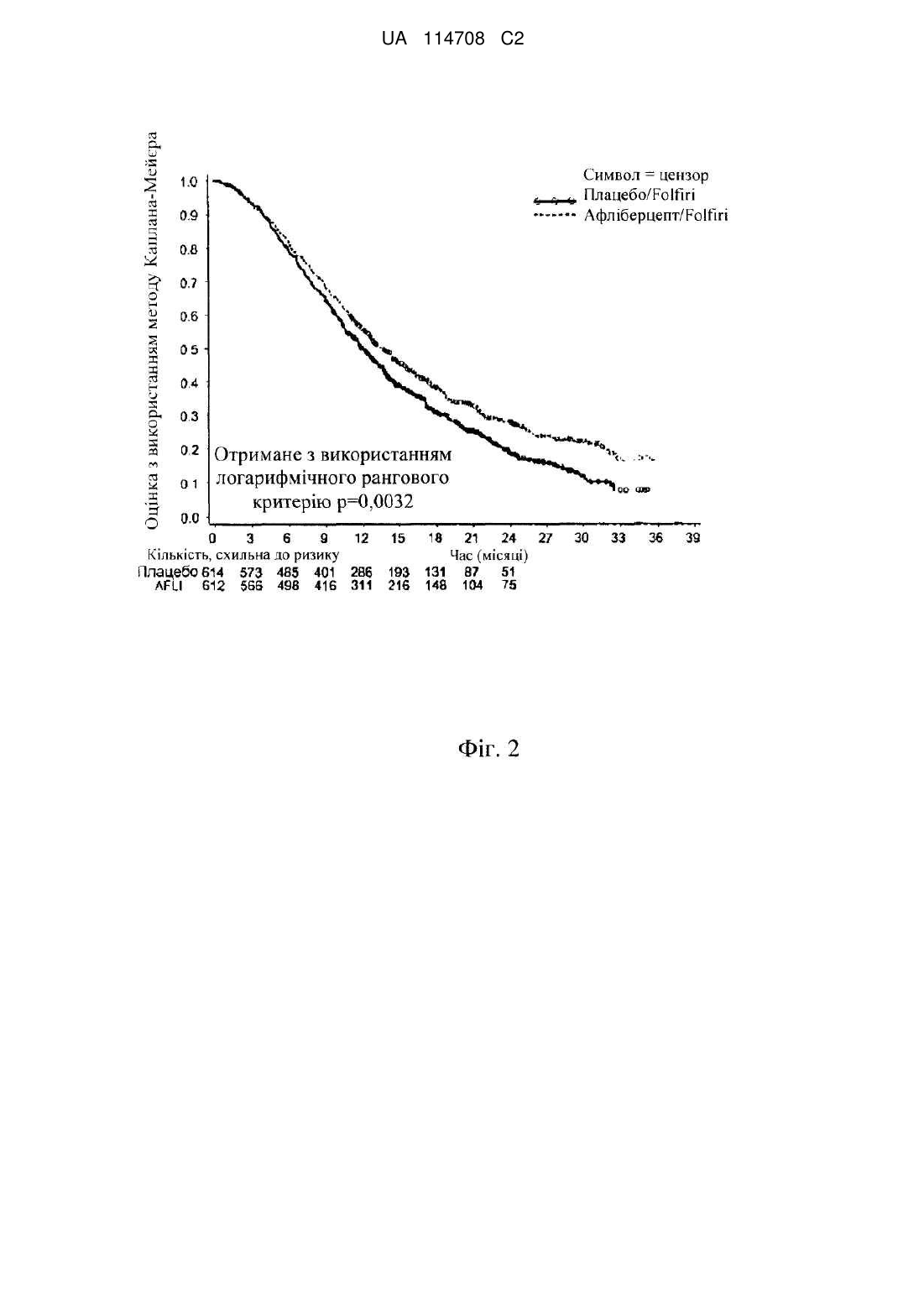
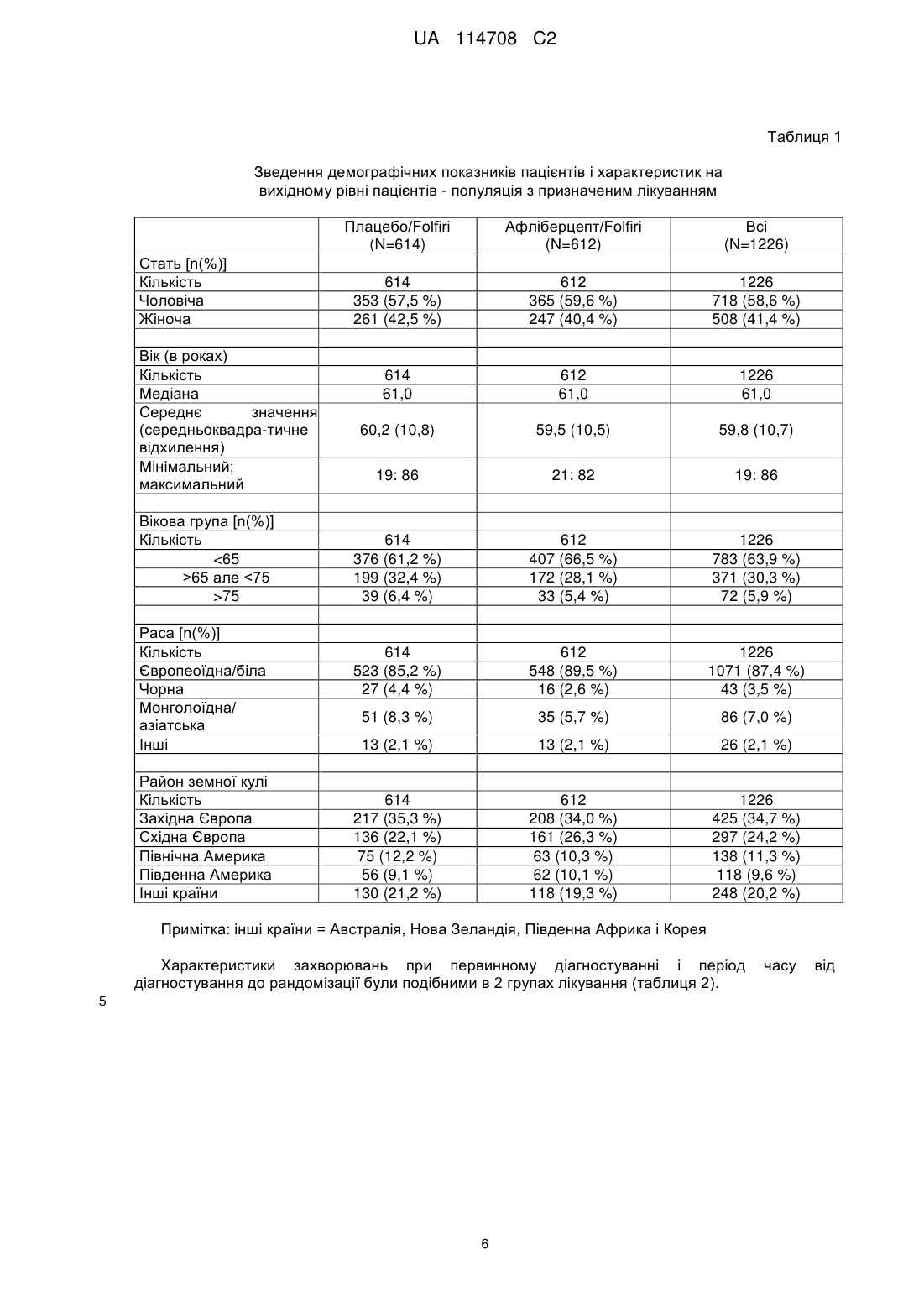
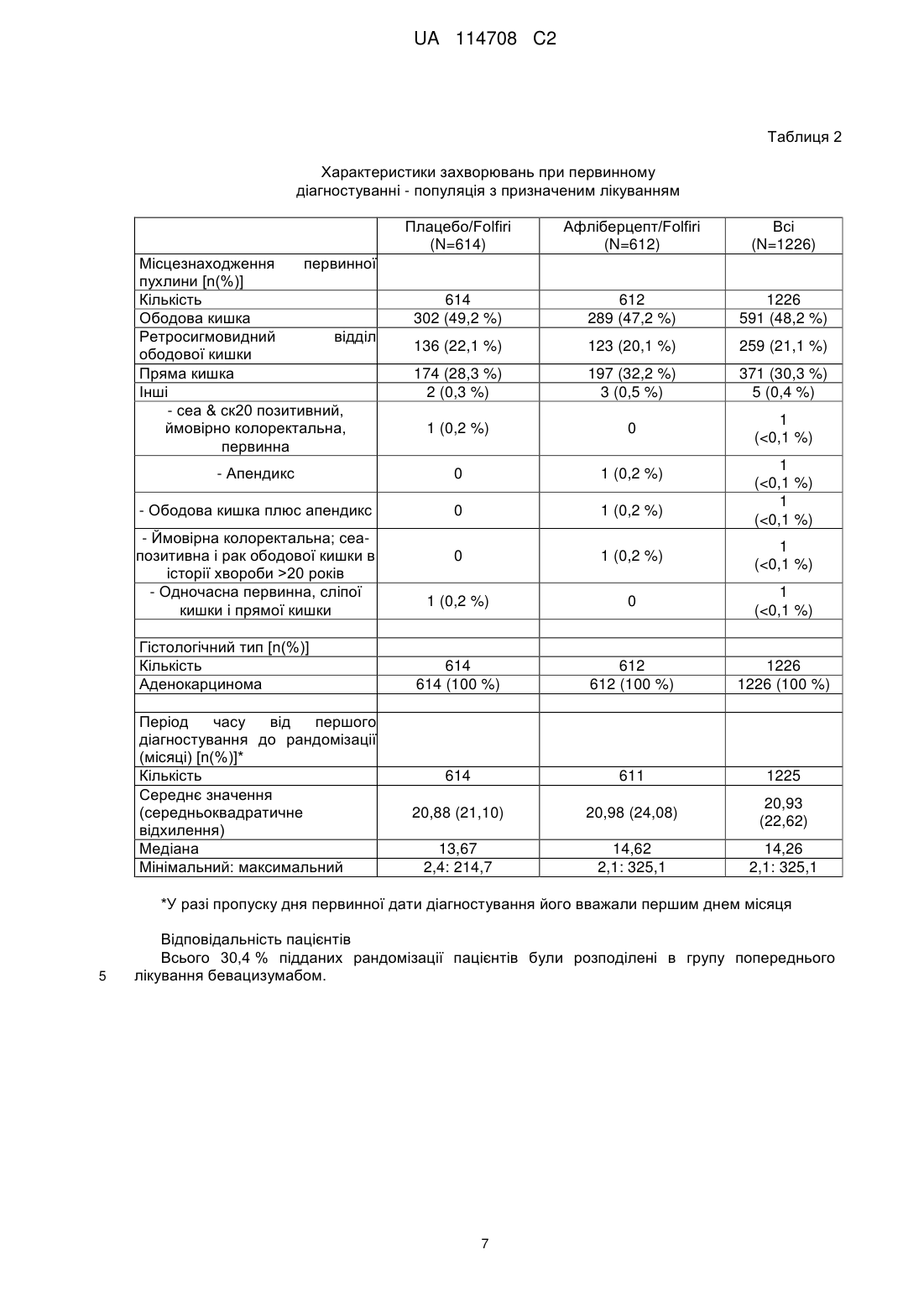
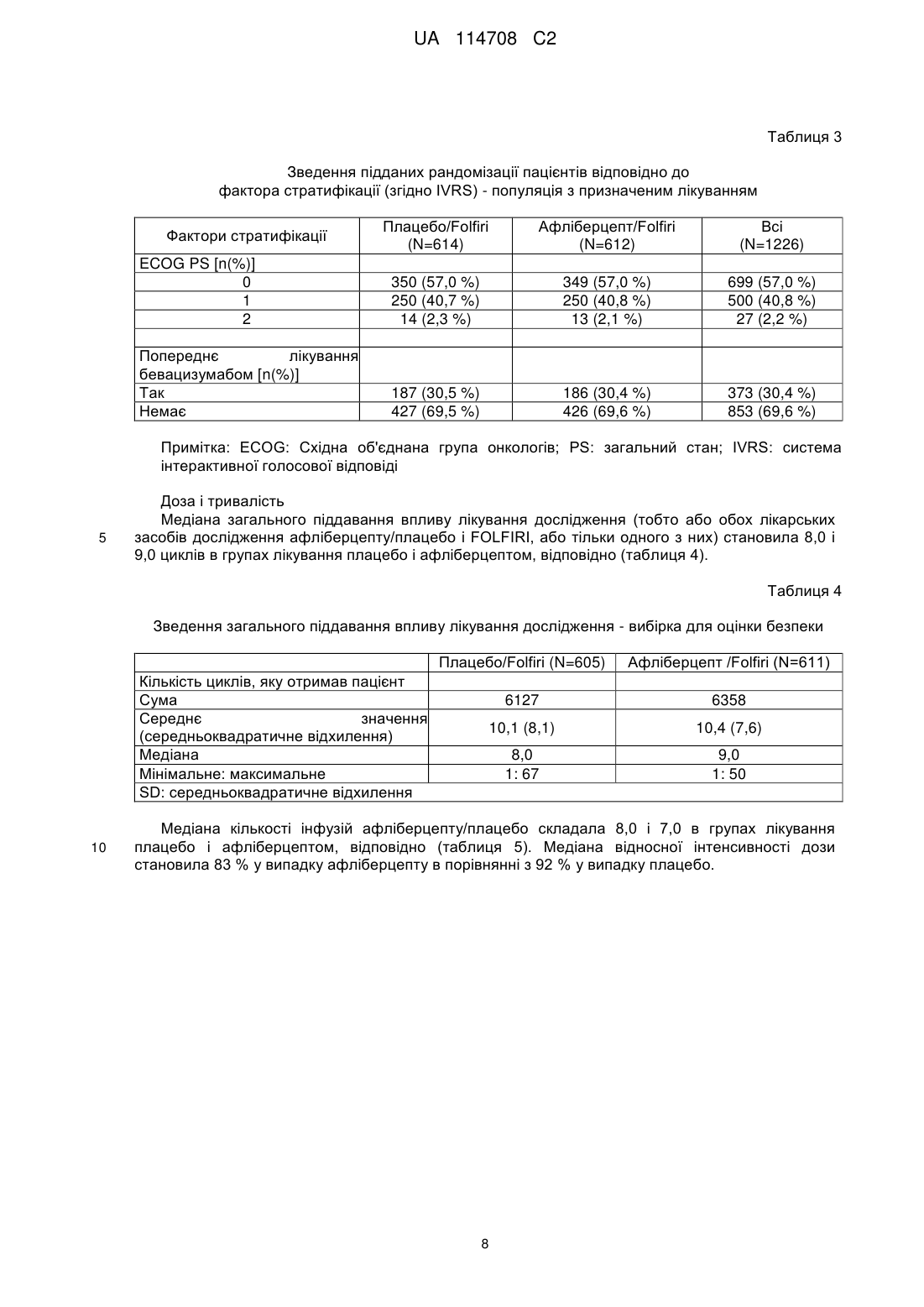
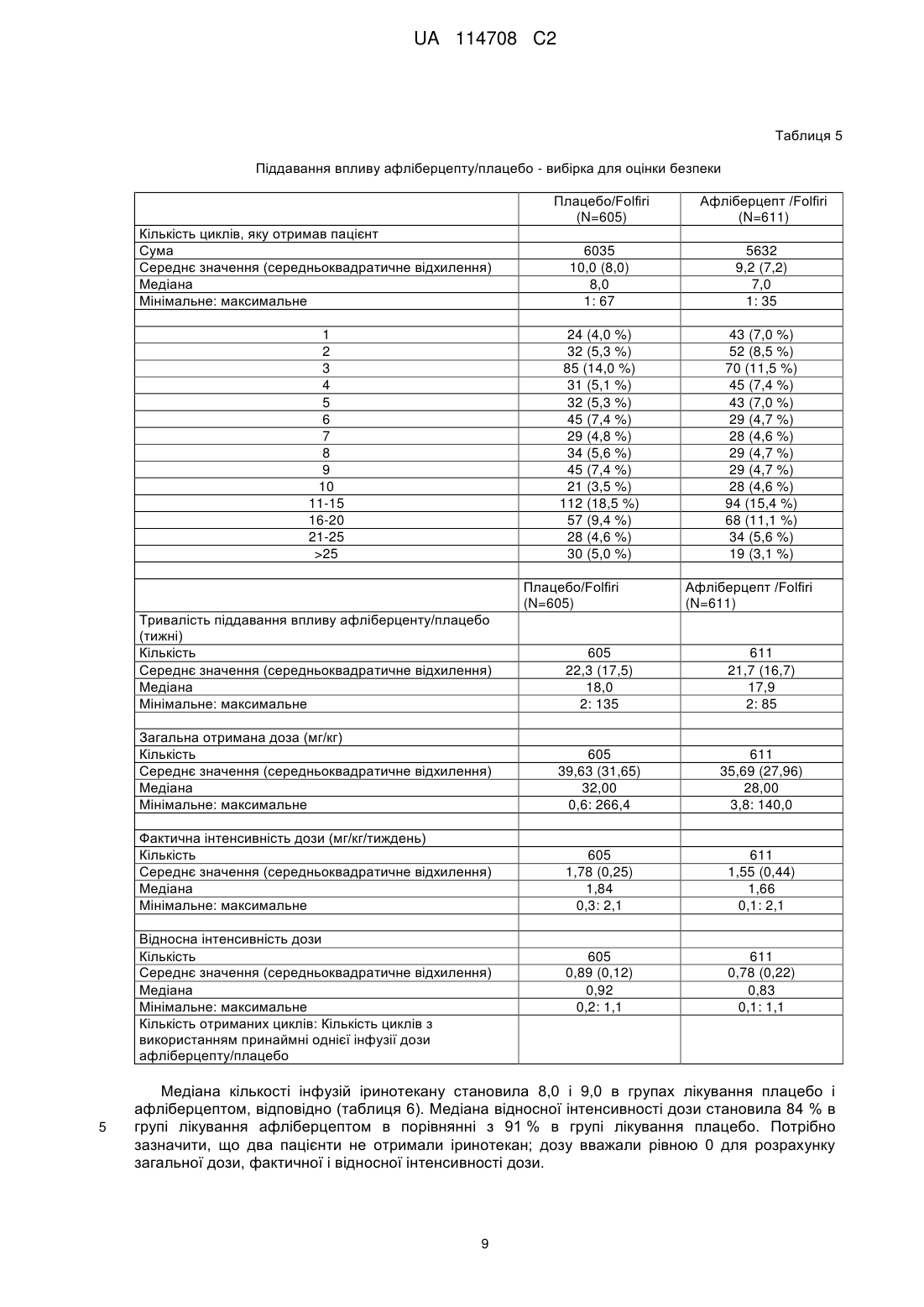
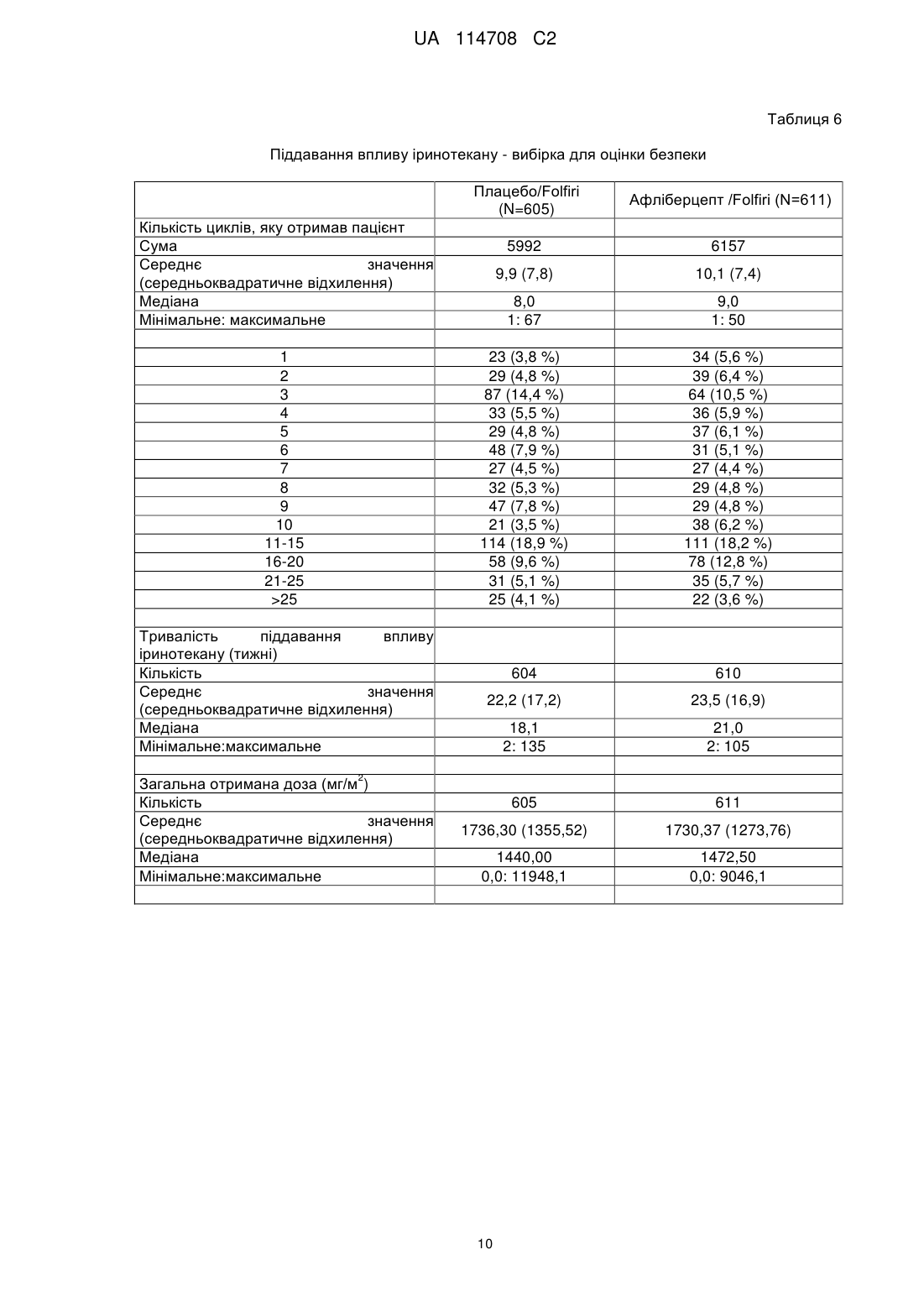
Реферат: Винахід стосується способу лікування колоректального раку або симптому колоректального раку у пацієнта, що цього потребує, де спосіб включає стадію на якій вводять вказаному пацієнту комбінацію, яка містить афліберцепт, фолінову кислоту, 5-фторурацилу (5-FU) і іриноцетан, причому афліберцепт вводять в дозі від приблизно 1 мг/кг до приблизно 10 мг/кг, і фолінову кислоту, 5-фторурацил (5-FU) й іриноцетан вводять у терапевтично ефективних кількостях. UA 114708 C2 (12) UA 114708 C2 UA 114708 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід стосується комбінацій афліберцепту, фолінової кислоти, 5-фторурацилу (5FU) і іриноцетану, які терапевтично застосовні при лікуванні колоректального раку (CRC) і, зокрема, метастатичного колоректального раку (CRC). Колоректальні раки входять в число типів пухлин, що найбільш часто зустрічаються в західних країнах, поступаючись першим місцем раку молочної залози у жінок і другим місцем раку легень і передміхурової залози у чоловіків. Кінцевий прогноз залежить від ступеня захворювання. Коефіцієнт виживаності протягом 5 років на ранній локалізованій стадії становить приблизно 90 %, зменшується до приблизно 60-65 % після поширення в сусідній орган(ів) або лімфатичних вузлів і складає менше 10 % після поширення у віддалені місця. При діагностуванні до ураження хворобою лімфатичних вузлів лікування звичайно обмежується хірургічним видаленням (або променевою терапією у разі пацієнтів з раком прямої кишки) і можливою участю в клінічних випробуваннях додаткових лікувальних заходів. Пацієнти з ураженням хворобою лімфатичних вузлів є кандидатами на додаткову хіміотерапію після первинного хірургічного втручання для того, щоб спробувати запобігти метастатичному рецидиву хвороби. Після поширення у віддалені місця лікування по суті складається з паліативної хіміотерапії. Приблизно 75-80 % від всіх пацієнтів з колоректальною карциномою будуть знаходитися на стадії, коли вся маса карциноми може бути хірургічно видалена. Однак майже половина цих пацієнтів, зрештою, помре від метастазів. Крім того, 20-25 % пацієнтів мають метастази при діагностуванні. Після появи метастазів медіана загальної виживаності при використанні комбінованої терапії, що є в розпорядженні, складає приблизно 20 місяців. Протягом останніх десятиріч 5-фторурацил (5-FU) залишався опорою хіміотерапії при колоректальному раку. Протягом років основним визначальним фактором при лікуванні пацієнтів з колоректальним раком було покращення схем введення 5-FU. Серед них схема введення два рази на місяць (LV5FU2) 5-FU, що призначається у вигляді болюсної ін'єкції/інфузії протягом 2 днів, як було встановлено, краще ніж схема введення у вигляді болюсної ін'єкції протягом 5 днів один раз на місяць (схеми Mayo) за показником частки, що відповіли (RR) (32,6 % проти 14,4 %), за показником виживання без прогресування (PFS) (27,6 проти 22,0 тижнів) і безпеки (de Gramont et al, Journal of Clinical Oncology 1997; 15(2): 808815). Однак статистично значуще покращення загальної виживаності (OS) не відмічалося до розробки, що почалася на початку дев'яностих, двох нових цитотоксичних агентів, оксаліплатину, DACH платини, і інгібітору топоізомерази I, іринотекану (іриноцетану). При використанні кожного з цих двох нових агентів медіана загальної виживаності в умовах первинних метастазів досягала 15-19 місяців в численних випробуваннях фази III. У дослідженні, опублікованому в 2004 Tournigand та інш. (Journal of Clinical Oncology 2004; 22(2): 229-237), в якому ці два лікарських засоби вводили послідовно в одному і тому ж протоколі, як лікування спочатку першої, а потім другої лінії пацієнтів з метастатичним колоректальним раком, був перетнутий поріг медіани загальної виживаності, що становить 20 місяців, яким би не був порядок послідовності лікування. Афліберцепт синтезований у вигляді злитого білка, що включає сигнальну послідовність VEGFR1, злиту з Ig-доменом D2 рецептора VEGFR1, який сам злитий з Ig-доменом D3 рецептора VEGFR2, який в свою чергу злитий з Fc-доменом IgG1. Афліберцепт також називають VEGFR1R2-Fc.DELTA.C1 або Flt1D2.Flk1D3.Fc.DELTA.C1. Амінокислотна послідовність (SEQ ID NO: 1) афліберцепту представлена на фіг. 1, а також представлена, зокрема, на фіг. 24 заявки на патент WO 00/75319. 5-фторурацил (5-FU або f5U) є лікарським засобом, який є аналогом піримідину, який використовують при лікуванні раку. Він є суїцидальним інгібітором і працює через необоротне інгібування тимідилатсинтази. Він належить до сімейства лікарських засобів, званих антиметаболітами. Фолінова кислота або лейковорин є додатковим до хіміотерапії раку засобом, що використовується в комбінації з 5-фторурацилом. Іринотекан є лікарським засобом, що використовується для лікування раку. Іринотекан є інгібітором топоізомерази 1, який перешкоджає розкрученню ДНК. FOLFIRI являє собою комбінацію фолінової кислоти, 5-фторурацилу (5-FU) і іриноцетану і буде використовуватися протягом всього цього документа. У дослідженні фази I (TCD6118) афліберцепт вводили внутрішньовенно в комбінації з 2 2 іринотеканом (180 мг/м в день 1), лейковорином (200 мг/м на день 1 і день 2) і 5-FU (у вигляді 2 болюсної ін'єкції/інфузії 400/600 мг/м в день 1 і день 2), кожних 2 тижні пацієнтам з солідними 1 UA 114708 C2 5 10 15 20 25 30 35 40 45 50 55 60 пухлинами на пізній стадії. Афліберцепт в дозі 4 мг/кг кожні 2 тижні вважався оптимальною дозою. У випробуванні фази II (NCI7498) афліберцепт вводили раніше підданим лікуванню пацієнтам з метастатичним колоректальним раком. Це випробування показало, що афліберцепт добре переноситься раніше підданими лікуванню пацієнтами з MCRC. Висновки полягають в тому, що на основі результатів дослідження потрібно дослідити афліберцепт як єдиний засіб або в комбінації (Tang et al, J. Clin Oncol 26: 2008 (May 20 suppl; abstr 4027). Але надані в цих двох дослідженнях результати не дали розуміння відносно ефективності. Крім того, випробування фази III афліберцепту для метастатичного раку підшлункової залози було припинене в 2009, а в 2011 дані випробування фази III, в якому афліберцепт оцінювався для лікування другої лінії недрібноклітинного раку легень (NSCLC), показали, що додавання афліберцепту до лікарського засобу, що використовується при хіміотерапії доцетакселу не задовольняло визначеним критеріям для основного кінцевого показника покращення загальної виживаності в порівнянні зі схемою введення доцетакселю плюс плацебо. У даний час встановлено, і це є об'єктом даного винаходу, що ефективність афліберцепту на загальну виживаність (OS) пацієнтів з колоректальним раком (CRC) можна значно покращити при його введенні в комбінації з FOLFIRI. Також було встановлено, і це є іншим об'єктом даного винаходу, що ефективність афліберцепту на виживання без прогресування (PFS) пацієнтів з колоректальним раком (CRC) можна значно покращити при його введенні в комбінації з FOLFIRI. Також було встановлено, і це є ще одним об'єктом даного винаходу, що ефективність афліберцепту на сумарну ефективність терапії (ORR) у пацієнтів з колоректальним раком (CRC) можна значно покращити при його введенні в комбінації з FOLFIRI. Даний винахід стосується способів, композицій і виробів, які тут описуються. В одному аспекті даним винаходом передбачається спосіб лікування колоректального раку (CRC) або симптому колоректального раку (CRC) у пацієнта, який цього потребує, при цьому вказаний спосіб включає введення вказаному пацієнту терапевтично ефективних кількостей афліберцепту і FOLFIRI. Цей спосіб є безпечним і ефективним. У другому аспекті даним винаходом передбачається спосіб збільшення загальної виживаності (OS) пацієнта, ураженого CRC, при цьому вказаний спосіб включає введення вказаному пацієнту терапевтично ефективних кількостей афліберцепту і FOLFIRI. У третьому аспекті даним винаходом забезпечується спосіб збільшення сумарної ефективності терапії (ORR) у пацієнта, ураженого CRC, при цьому вказаний спосіб включає введення вказаному пацієнту терапевтично ефективних кількостей афліберцепту і FOLFIRI. У четвертому аспекті даним винаходом забезпечується спосіб збільшення виживання без прогресування (PFS) пацієнта, ураженого CRC, при цьому вказаний спосіб включає введення вказаному пацієнту терапевтично ефективних кількостей афліберцепту і FOLFIRI. У рамках першої відмітної ознаки даним винаходом забезпечується спосіб відповідно до будь-якого з першого-четвертого аспекту, в якому вказаний пацієнт вже піддавався лікуванню у відношенні CRC або симптому CRC (терапія другої лінії). У конкретному варіанті здійснення CRC являє собою метастатичний колоректальний рак. У рамках другої відмітної ознаки даним винаходом передбачається спосіб відповідно до будь-якого з першого-четвертого аспекту або першої відмітної ознаки, в якій вказаний пацієнт раніше піддавався лікуванню з використанням хіміотерапії, променевої терапії або хірургічного втручання. В одному варіанті здійснення вказаний пацієнт дав незадовільний результат хіміотерапії, променевої терапії або хірургічного втручання. У рамках третьої відмітної ознаки даним винаходом забезпечується спосіб відповідно до будь-якого з першого-четвертого аспекту або першої відмітної ознаки, в якій вказаний пацієнт раніше піддавався лікуванню з використанням терапії на основі оксаліплатину або бевацизумабу. В одному варіанті здійснення вказаний пацієнт дав незадовільний результат терапії на основі оксаліплатину або бевацизумабу. У рамках четвертої відмітної ознаки даним винаходом забезпечується спосіб, в якому 2 пацієнту вводять фолінову кислоту в дозі, що находиться між приблизно 200 мг/м і приблизно 2 2 600 мг/м , 5-фторурацил (5-FU) в дозі, що знаходиться між приблизно 2 000 мг/м і приблизно 2 2 2 4000 мг/м , іриноцетан в дозі, що знаходиться між приблизно 100 мг/м і приблизно 300 мг/м , і афліберцепт в дозі, що знаходиться між приблизно 1 мг/кг і приблизно 10 мг/кг. У даній заявці під вказаною дозою фолінової кислоти повинна матися на увазі доза рацемічної суміші фолінової кислоти, тобто включаючи D- і L-форми. Якщо буде 2 UA 114708 C2 5 10 15 20 25 30 35 40 45 50 55 використовуватися тільки L-форма, доза повинна складати половину від дози, вказаної для рацемічної суміші. 2 Іншими словами, доза фолінової кислоти, що становить приблизно 200 мг/м , як указано в 2 2 даній заявці, відповідає приблизно 200 мг/м рацемічної суміші і приблизно 100 мг/м L-форми. У рамках п'ятої відмітної ознаки даним винаходом забезпечується спосіб, в якому пацієнту 2 вводять фолінову кислоту в дозі, що складає приблизно 400 мг/м , 5-фторурацил (5-FU) в дозі, 2 2 що складає приблизно 2800 мг/м , іриноцетану в дозі, що складає приблизно 180 мг/м , і афліберцепт в дозі, що складає приблизно 4 мг/кг. У рамках шостої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує внутрішньовенно фолінову кислоту в дозі, що складається з приблизно 400 2 2 мг/м , внутрішньовенно 5-фторурацил (5-FU) в дозі, що складає приблизно 2800 мг/м , 2 внутрішньовенно іриноцетан в дозі, що складається з приблизно 180 мг/м , і внутрішньовенно афліберцепт в дозі, що складає приблизно 4 мг/кг, кожні два тижні. У рамках сьомої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує внутрішньовенно фолінову кислоту, внутрішньовенно 5-фторурацил (5-FU), внутрішньовенно іриноцетан і внутрішньовенно афліберцепт кожні два тижні протягом періоду часу, що знаходиться між приблизно 9 і приблизно 18 тижнями. У рамках іншої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує внутрішньовенно фолінову кислоту відразу ж після введення афліберцепту. У рамках іншої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує внутрішньовенно іриноцетан відразу ж після введення афліберцепту. У рамках іншої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує внутрішньовенно іриноцетан відразу ж після введення афліберцепту протягом майже 90 хвилин. У рамках іншої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує внутрішньовенно 5-фторурацил (5-FU) відразу ж після введення афліберцепту. У рамках іншої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний пацієнт отримує першу частину 5-фторурацилу (5-FU), що вводиться внутрішньовенно відразу ж після введення афліберцепту, а другу частину - у вигляді безперервної інфузії. У рамках іншої відмітної ознаки даним винаходом забезпечується спосіб, в якому вказаний 2 пацієнт отримує приблизно 400 мг/м 5-фторурацилу (5-FU), що вводиться внутрішньовенно 2 протягом приблизно 2-4 хвилин після введення афліберцепту, і 2400 мг/м , що вводиться протягом приблизно 46 годин після введення афліберцепту у вигляді безперервної інфузії. У п'ятому аспекті відмітною ознакою даного винаходу є композиція, що включає терапевтично ефективні кількості афліберцепту в комбінації з фоліновою кислотою, 5фторурацилом (5-FU) і іриноцетаном, для лікування пацієнтів з CRC для одночасного введення. У шостому аспекті відмітною ознакою даного винаходу є композиція, що включає терапевтично ефективні кількості афліберцепту в комбінації з фоліновою кислотою, 5фторурацилом (5-FU) і іриноцетаном, для лікування пацієнтів з CRC для послідовного введення. У сьомому аспекті відмітною ознакою даного винаходу є композиція, що включає терапевтично ефективні кількості афліберцепту в комбінації з фоліновою кислотою, 5фторурацилом (5-FU) і іриноцетаном, для лікування пацієнтів з CRC для введення, яке розтягнуте протягом періоду часу для отримання максимальної ефективності комбінації. У восьмому аспекті відмітною ознакою даного винаходу є композиція, що включає терапевтично ефективні кількості афліберцепту в комбінації з фоліновою кислотою, 5фторурацилом (5-FU) і іриноцетаном і що включає фармацевтично прийнятний носій, для лікування пацієнтів з CRC. У рамках однієї відмітної ознаки цих аспектів пацієнт має метастази в печінці. У дев'ятому аспекті відмітною ознакою даного винаходу є готовий виріб, що включає: a) пакувальний матеріал b) афліберцепт і c) етикетку або листівку-вкладиш, що міститься у вказаному пакувальному матеріалі, що вказує на те, що афліберцепт в комбінації з фоліновою кислотою, 5-фторурацилом (5-FU) і іриноцетаном ефективний для лікування CRC. У рамках однієї відмітної ознаки дев'ятого аспекту етикетка або листівка-вкладиш, що міститься у вказаному пакувальному матеріалі, вказує на те, що афліберцепт в комбінації з FOLFIRI покращує загальну виживаність (OS). 3 UA 114708 C2 5 10 15 20 25 30 35 40 45 50 55 У рамках однієї відмітної ознаки дев'ятого аспекту етикетка або листівка-вкладиш, що міститься у вказаному пакувальному матеріалі, вказує на те, що афліберцепт в комбінації з FOLFIRI покращує виживаність без прогресування (PFS). У рамках однієї відмітної ознаки дев'ятого аспекту етикетка або листівка-вкладиш, що міститься у вказаному пакувальному матеріалі, вказує на те, що афліберцепт в комбінації з FOLFIRI поліпшує сумарну ефективність терапії (ORR). У десятому аспекті відмітною ознакою даного винаходу є набір для лікування пацієнтів з CRC, що включає: a) принаймні одну сполуку, що вибирається зі списку, який складається з афліберцепту, фолінової кислоти, 5-фторурацилу (5-FU) і іриноцетану; і b) етикетку або листівку-вкладиш, що міститься у вказаному наборі, що вказує на те, що афліберцепт повинен використовуватися в комбінації з фоліновою кислотою, 5-фторурацилом (5-FU) і іриноцетаном (FOLFIRI), або що фолінова кислота, 5-фторурацил (5-FU) і іриноцетан (FOLFIRI) повинні використовуватися в комбінації з Афліберцептом. В одинадцятому аспекті відмітною ознакою даного винаходу є набір, що включає в окремих контейнерах фармацевтичні композиції для спільного застосування при лікуванні CRC у пацієнта, який включає (1) фармацевтичну композицію, що включає афліберцепт, (2) фармацевтичну композицію, що включає фолінову кислоту, (3) фармацевтичну композицію, що включає 5-фторурацил (5-FU), і (4) фармацевтичну композицію, що включає іриноцетан. Афліберцепт може бути приготований у вигляді лікарського препарату, як описано в WO2006/104852. Кваліфікований в даній галузі техніки фахівець може звернутися зокрема, до WO2006/104852 або WO 00/75319 для виконання даного винаходу. Фігури Фіг. 1: Амінокислотна послідовність афліберцепту (SEQ ID NO: 1). Фіг 2: Загальна виживаність (місяці) - криві Каплана-Мейєра відповідно до групи лікування популяція з призначеним лікуванням. Фіг. 3: Загальна виживаність (місяці) - аналізи відповідно до підгруп (стовпчикова діаграма) – у відповідності з факторами стратифікації згідно IVRS - популяція з призначеним лікуванням. Фіг. 4: Загальна виживаність (місяці) - аналізи відповідно до підгруп (стовпчикова діаграма) – у відповідності з демографічними показниками пацієнтів - популяція з призначеним лікуванням. Фіг. 5: Загальна виживаність (місяці) - аналізи відповідно до підгруп (стовпчикова діаграма) – у відповідності з характеристиками на вихідному рівні - популяція з призначеним лікуванням. Фіг. 6: PFS на основі оцінки пухлин IRC (незалежним спостережливим комітетом) (місяці) аналіз відповідно до підгруп (стовпчикова діаграма) - відповідно до факторів стратифікації згідно IVRS - популяція з призначеним лікуванням. Наступний приклад ілюструє комбінацію відповідно до даного винаходу. EFC10262 (VELOUR)/(Багатонаціональне, рандомізоване, подвійне сліпе дослідження, в якому порівнюється ефективність афліберцепту, що призначається один раз на два тижні, з плацебо, на пацієнтах з метастатичним колоректальним раком (MCRC), підданих лікуванню комбінацією іринотекан/5-FU (FOLFIRI) після несприятливого виходу схеми на основі оксаліплатину EFC10262 було розроблене як рандомізоване, подвійне сліпе дослідження, що проводилося у безлічі центрів, в якій порівнюється афліберцепт в дозі = 4 мг/кг з плацебо, в поєднанні з комбінацією іринотекану і 5-фторурацилу (FOLFIRI), що призначається кожні 2 тижні як лікування другої лінії для пацієнтів з метастатичним колоректальним раком (MCRC) після несприятливого виходу схеми на основі оксаліплатину. Кожний підданий рандомізації пацієнт повинен був піддатися лікуванню до прогресування захворювання, смерті або недопустимої токсичності. Основною метою EFC102 62 була демонстрація покращення загальної виживаності (OS) у випадку афліберцепт+FOLFIRI в порівнянні з плацебо+FOLFIRI. Визначений рівень статистичної значущості для цього кінцевого аналізу дорівнював 0,0466 після коректування помилки типу I, затраченої на два проміжних аналізи, використовуючи витратну функцію О'Брайєна-Флемінга. Це дослідження включало один офіційний проміжний аналіз, запланований з метою ефективності, коли сталося 561 смертельних випадків (що становить 65 % частка від загального числа випадків, накопичених протягом всього дослідження). На вимогу незалежного комітету по моніторингу даних (DMC) був виконаний додатковий проміжний аналіз OS, щоб дати початкову оцінку відношення користь-ризик, коли сталося 315 смертельних випадків (що становить 36,5 % частка = число випадків/загальне очікуване число). 4 UA 114708 C2 5 10 15 20 25 30 35 40 Усього приблизно 863 смертей було потрібно для визначення зменшення рівня ризику, що становить 20 %, за показником OS зі 90 % статистичною потужністю дослідження, використовуючи двосторонній логарифмічний ранговий критерій, при загальному рівні значущості = 0,0499. Медіана часу доживання відповідно до прогнозу становила 11 місяців для контрольної групи. Загальний рівень значущості був розщеплений між загальною виживаністю (0,0499) і виживанням без прогресування як додатковий показник ефективності (0,0001). Планували піддати рандомізації приблизно 1200 пацієнтів (тобто 600 пацієнтів в кожній групі лікування). Стратифікацію призначення лікування здійснювали відповідно до попередньої терапії з використанням бевацизумабу (так чи ні) і загального стану (PS) по шкалі ECOG (Східної об'єднаної групи онкологів) (0 проти 1 проти 2). Зарахування було почате в листопаді 2007 і закінчене в березні 2010. Всього 1226 пацієнтів було піддано рандомізації. Аналіз ефективності був оснований на всіх підданих рандомізації пацієнтах (популяції з призначеним лікуванням: 614 в групі лікування плацебо і 612 пацієнтів в групі лікування афліберцептом). Аналіз безпеки був оснований на всіх підданих лікуванню пацієнтах (вибірці для оцінки безпеки: 605 і 611 пацієнтів в групах лікування плацебо і афліберцептом, відповідно). Групи лікування були однаково збалансовані за демографічними показниками, характеристиками захворювань і попереднім протираковим лікуванням, включаючи попереднє піддавання впливу бевацизумабу. Доза і схема введення Пацієнтам вводили або афліберцепт, або плацебо, в залежності від заданої групи. Відразу ж після цього пацієнти отримували іринотекан, 5-FU і лейковорин (схему FOLFIRI). Це лікування повторювали кожні 2 тижні. Афліберцепт/плацебо Група А, афліберцепт: 4 мг/кг вводили внутрішньовенно протягом 1 години в день 1, кожні 2 тижні, або Група В, плацебо: 4 мг/кг вводили внутрішньовенно протягом 1 години в день 1, кожні 2 тижні. Схема FOLFIRI Відразу ж після введення афліберцепту/плацебо всі пацієнти отримували: 2 - Іринотекан 180 мг/м у вигляді внутрішньовенної інфузії в 500 мл розчину 5 % декстрози у 2 воді (D5W) протягом 90 хвилин і форму з правим-лівим обертанням (dI) лейковорину 400 мг/м у вигляді внутрішньовенної інфузії протягом 2 годин, в той же самий час, в мішках, використовуючи вісь координат, а потім: 2 - 5-FU 400 мг/м у вигляді внутрішньовенної болюсної ін'єкції протягом 2-4 хвилин, а потім: 2 - 5-FU 2400 мг/м у вигляді безперервної внутрішньовенної інфузії в 500 мл D5W (що рекомендується) протягом 46 годин. Результати EFC10262 Демографічні показники і характеристики на вихідному рівні Демографічні показники пацієнтів і характеристики на вихідному рівні були подібними в 2 групах лікування (таблиця 1). 5 UA 114708 C2 Таблиця 1 Зведення демографічних показників пацієнтів і характеристик на вихідному рівні пацієнтів - популяція з призначеним лікуванням Плацебо/Folfiri (N=614) Стать [n(%)] Кількість Чоловіча Жіноча Вік (в роках) Кількість Медіана Середнє значення (середньоквадра-тичне відхилення) Мінімальний; максимальний Вікова група [n(%)] Кількість 65 але 75 Раса [n(%)] Кількість Європеоїдна/біла Чорна Монголоїдна/ азіатська Інші Район земної кулі Кількість Західна Європа Східна Європа Північна Америка Південна Америка Інші країни Афліберцепт/Folfiri (N=612) Всі (N=1226) 614 353 (57,5 %) 261 (42,5 %) 612 365 (59,6 %) 247 (40,4 %) 1226 718 (58,6 %) 508 (41,4 %) 614 61,0 612 61,0 1226 61,0 60,2 (10,8) 59,5 (10,5) 59,8 (10,7) 19: 86 21: 82 19: 86 614 376 (61,2 %) 199 (32,4 %) 39 (6,4 %) 612 407 (66,5 %) 172 (28,1 %) 33 (5,4 %) 1226 783 (63,9 %) 371 (30,3 %) 72 (5,9 %) 614 523 (85,2 %) 27 (4,4 %) 612 548 (89,5 %) 16 (2,6 %) 1226 1071 (87,4 %) 43 (3,5 %) 51 (8,3 %) 35 (5,7 %) 86 (7,0 %) 13 (2,1 %) 13 (2,1 %) 26 (2,1 %) 614 217 (35,3 %) 136 (22,1 %) 75 (12,2 %) 56 (9,1 %) 130 (21,2 %) 612 208 (34,0 %) 161 (26,3 %) 63 (10,3 %) 62 (10,1 %) 118 (19,3 %) 1226 425 (34,7 %) 297 (24,2 %) 138 (11,3 %) 118 (9,6 %) 248 (20,2 %) Примітка: інші країни = Австралія, Нова Зеландія, Південна Африка і Корея Характеристики захворювань при первинному діагностуванні і період діагностування до рандомізації були подібними в 2 групах лікування (таблиця 2). 5 6 часу від UA 114708 C2 Таблиця 2 Характеристики захворювань при первинному діагностуванні - популяція з призначеним лікуванням Плацебо/Folfiri (N=614) Афліберцепт/Folfiri (N=612) Всі (N=1226) 614 302 (49,2 %) 612 289 (47,2 %) 1226 591 (48,2 %) 136 (22,1 %) 123 (20,1 %) 259 (21,1 %) 174 (28,3 %) 2 (0,3 %) 197 (32,2 %) 3 (0,5 %) 371 (30,3 %) 5 (0,4 %) 1 (0,2 %) 0 1 (
ДивитисяДодаткова інформація
Назва патенту англійськоюComposition comprising aflibercept, folinic acid, 5-fluorouracil (5-fu) and irinocetan (folfiri)
Автори англійськоюCastan, Remi
Автори російськоюКастан Реми
МПК / Мітки
МПК: A61K 31/4745, A61K 31/519, A61K 31/505, A61K 38/17
Мітки: спосіб, колоректального, кислоту, лікування, містить, 5-фторурацил, яка, раку, іринотекан, фолінову, комбінацією, симптому, афліберцепт
Код посилання
<a href="https://ua.patents.su/32-114708-sposib-likuvannya-kolorektalnogo-raku-abo-simptomu-kolorektalnogo-raku-kombinaciehyu-yaka-mistit-aflibercept-folinovu-kislotu-5-ftoruracil-i-irinotekan.html" target="_blank" rel="follow" title="База патентів України">Спосіб лікування колоректального раку або симптому колоректального раку комбінацією, яка містить афліберцепт, фолінову кислоту, 5-фторурацил і іринотекан</a>
Попередній патент: Біспецифічна зв’язувальна молекула, яка зв’язується з vegf i ang2
Наступний патент: Кон’югат, що містить похідну оксинтомодуліну, fc-ділянку імуноглобуліну та непептидильний полімер, та його застосування
Випадковий патент: Рама універсальна