Похідні акрилової кислоти як фунгіциди, інсектициди або регулятори росту рослин
Номер патенту: 40565
Опубліковано: 15.08.2001
Автори: Б'ютімент Кевін, Годфрі Крістофер Річард Ейлс, Ентоні Вів'єн Маргарет, де Френ Поль, Бушелл Майкл Джон, КЛАФ Джон Мартін
Формула / Реферат
1. Производные акриловой кислоты общей формулы (I):
или их стереоизомеры, где
Х представляет собой водород, фтор, хлор, бром, (С1-С6) алкил, фенил(С1-С4) алкил, где фенильная группа необязательно может быть замещена фтором, хлором или метоксигруппой, трифторметил, бромметил, диметоксиметил, феноксиметил, необязательно замещенный хлором, пиридилэтил, фуранилэтил, тиенилэтил, этоксикарбонилэтил, этенил, необязательно замещенный фенилом, циано, (С1-Сз) алкоксикарбонилом, бензилоксикарбонилом, ацетилом, фурилом или бензтиазолилом, этинил, замещенный фенилом или трет-бутилом, фенил, (С1-С6) алкокси, аллилокси, необязательно замещенный фенилом, бензилокси, фенокси, необязательно замещенный фтором, хлором, бромом, гидрокси, метилом, трифторметилом, формилом, пропенилокси, пропаргилокси, ацетокси, метилсульфонилокси, фенилом, фенокси, нитро, амино, формиламино, ацетиламино или (С1-С6) алкокси, необязательно замещенным фтором, фенилтио, фенилсульфинил, нафтилокси, пиридилокси, необязательно замещенный трифторметилом, изобутирилокси, бензоилокси, необязательно замещенный трет-бутилом, формил, бензоил, необязательно замещенный метоксигруппой, (С1-С3) алкоксикарбонил, циклогексилоксикарбонил, аллилоксикарбонил, феноксикарбонил, замещенный метоксигруппой, нитро, бензоиламино, фуроиламино или N-тиенилкарбонил- N -метиламино;
Y представляет собой находящийся в орто- мета- или пара-положении относительно акрилатной группы заместитель, выбранный из водорода, фтора, хлора, брома, метила, фенилэтенила, нитро или фенокси;
Z представляет собой атом водорода или
Х и Y, когда они находятся в соседнем положении фенольного кольца, вместе друг с другом образуют конденсированное бензольное кольцо, необязательно замещенное фенилом, конденсированное нафталиновое кольцо, конденсированное бензофуранильное кольцо, конденсированное бензотиенильное кольцо или группу
Y и Z, когда они находятся в соседнем положении фенильного кольца вместе друг с другом образуют конденсированное бензольное кольцо,
за исключением того, что когда Х представляет водород, Y не является водородом или пара-хлором, в качестве фунгицидов, инсектицидов или регуляторов роста растений.
Разбивка приоритетов по признакам:
19.10.84.
Х представляет собой водород, фтор, хлор, бром, (С1-С6) алкил, фенил (С1-С4) алкил, где фенильная группа необязательно может быть замещена фтором, хлором или метоксигруппой, трифторметил, бромметил, диметоксиметил, феноксиметил, необязательно замещенный хлором, пиридилэтил, фуранилэтил, тиенилэтил, этоксикарбонилэтил, этенил, необязательно замещенный фенилом, циано, (С1- Сз) алкоксикарбонилом, бензилоксикарбонилом, ацетилом, фурилом или бензтиазолилом, этинил, замещенный фенилом или трет-бутилом, фенил, (С1-С6) алкокси, бензилокси, фенокси, необязательно замещенный фтором, хлором, бромом, гидрокси, метилом, трифторметилом, формилом, пропенилокси, пропаргилокси,
ацетокси, метилсульфонилокси, фенилом, фенокси, нитро, амино, формиламино, ацетиламино или (С1-С6)алкокси, необязательно замещенным фтором, формил, бензоил, необязательно замещенный метоксигруппой, (С1-Сз)алкоксикарбонил, циклогексилоксикарбонил, аллилоксикарбонил, феноксикарбонил, замещенный метоксигруппой, нитро, бензоиламино, фуроиламино;
Y представляет собой находящийся в орто- мета- или пара-положении относительно акрилатной группы заместитель, выбранный из водорода, фтора, хлора, брома, метила, фенилэтенила, нитро или фенокси.
23.05.85.
Х представляет собой аллилокси, необязательно замещенный фенилом, пиридилокси, необязательно замещенный трифторметилом, изобутирилокси, бензоилокси, необязательно замещенный трет - бутилом, N-тиенилкарбонил-N-метиламино;
Х и Y, когда они находятся в соседнем положении фенольного кольца, вместе друг с другом образуют конденсированное бензольное кольцо, необязательно замещенное фенилом, конденсированное нафталиновое кольцо, конденсированное бензофуранильное кольцо, конденсированное бензотиенильное кольцо или группу
Y и Z, когда они находятся в соседнем положении фенильного кольца вместе друг с другом образуют конденсированное бензольное кольцо.
Текст
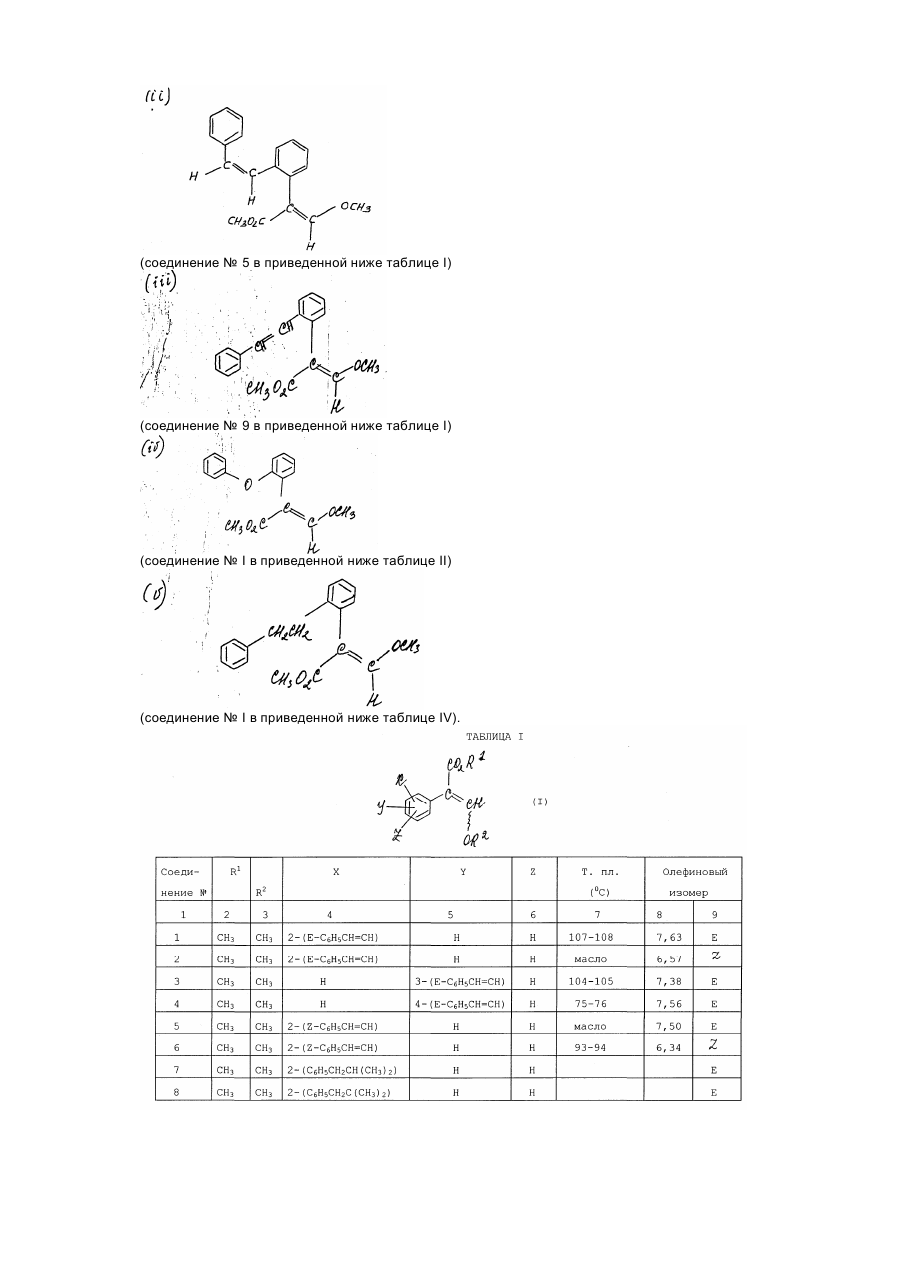
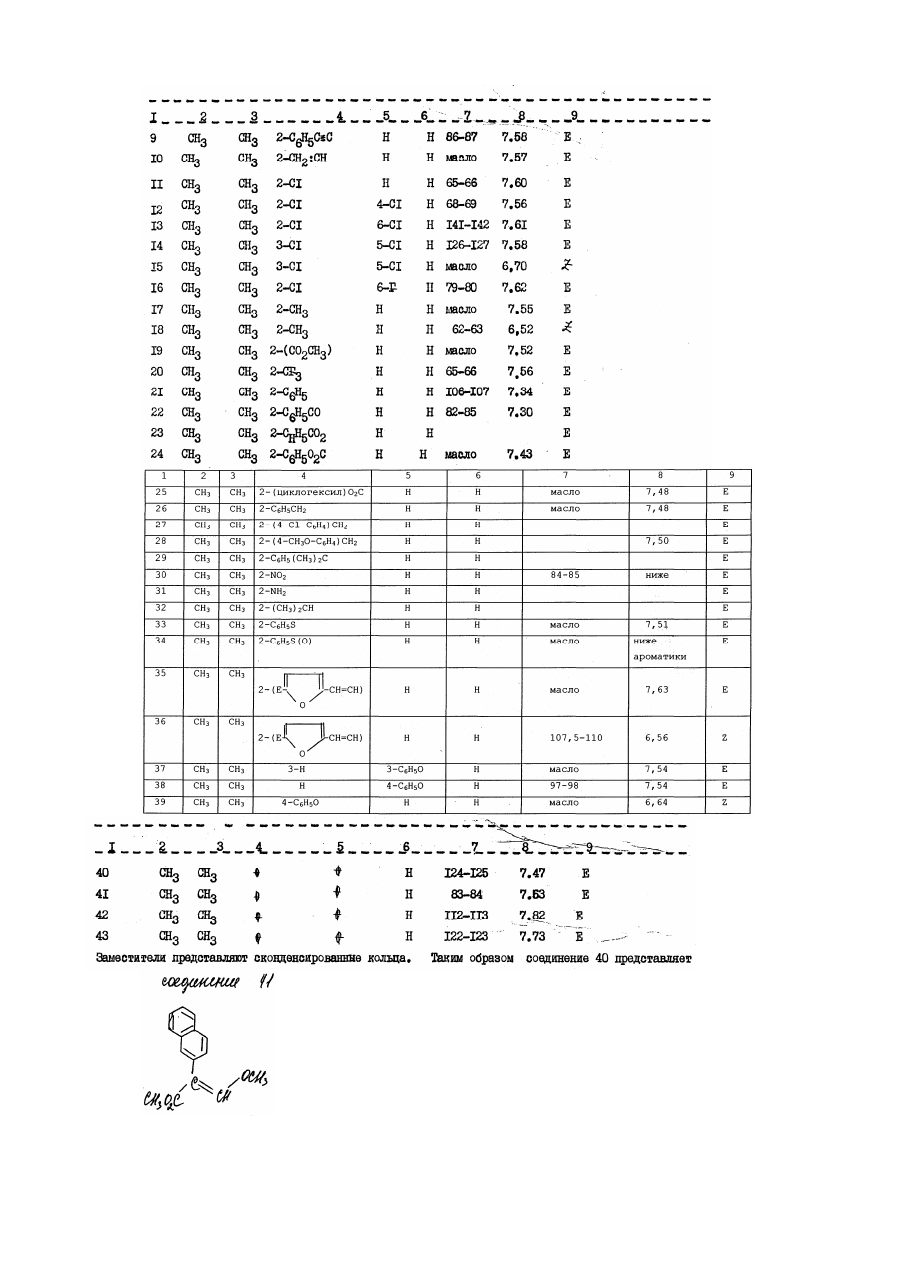
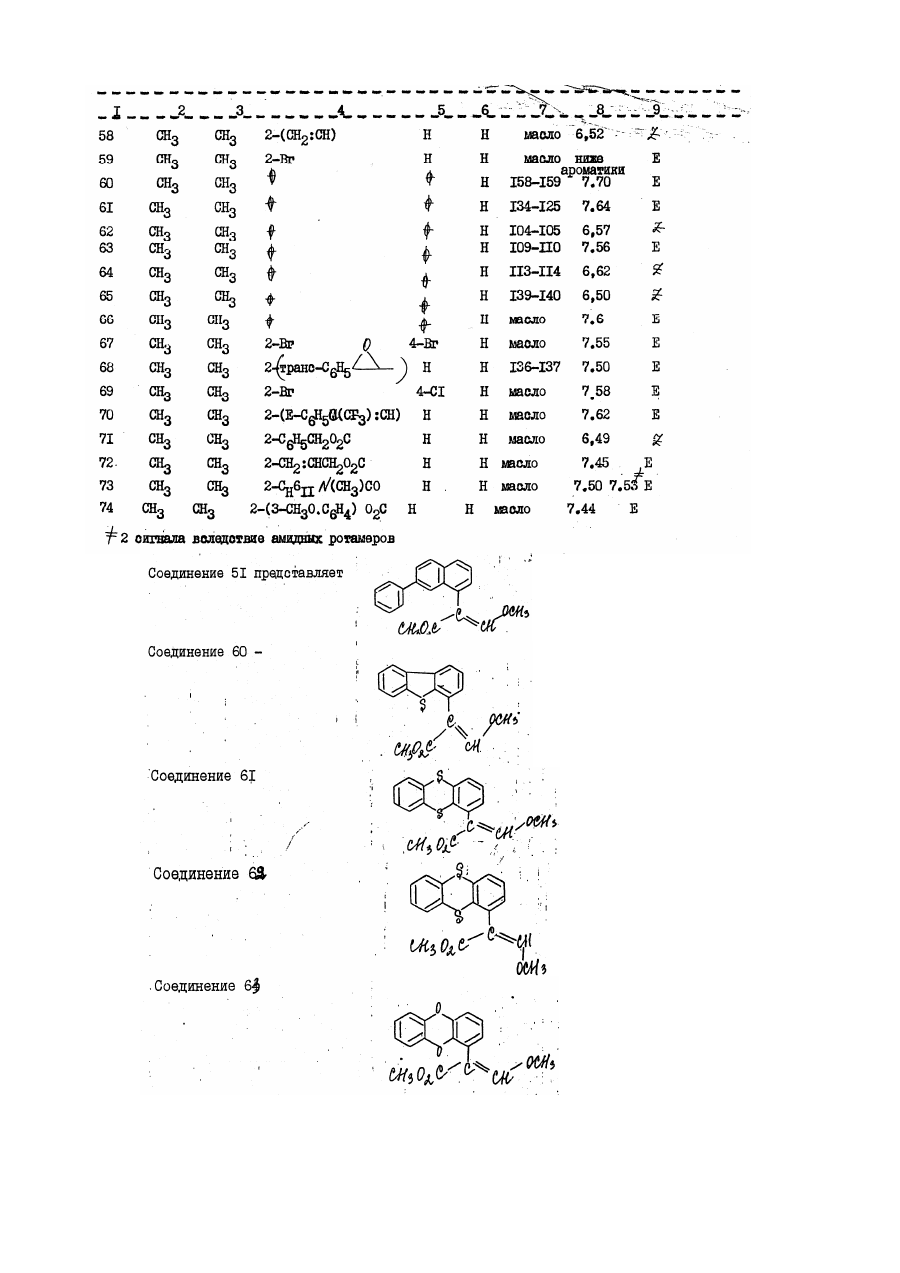
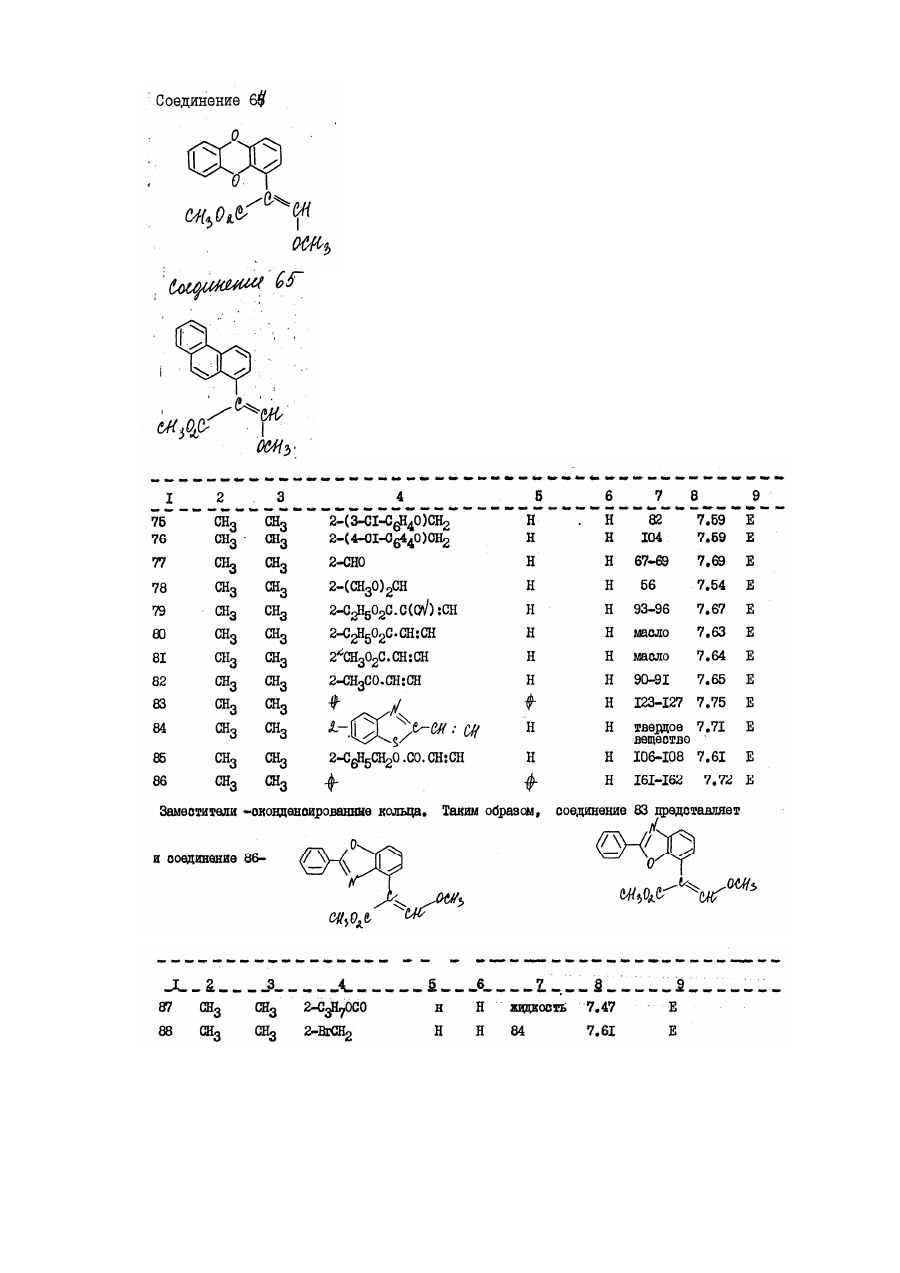
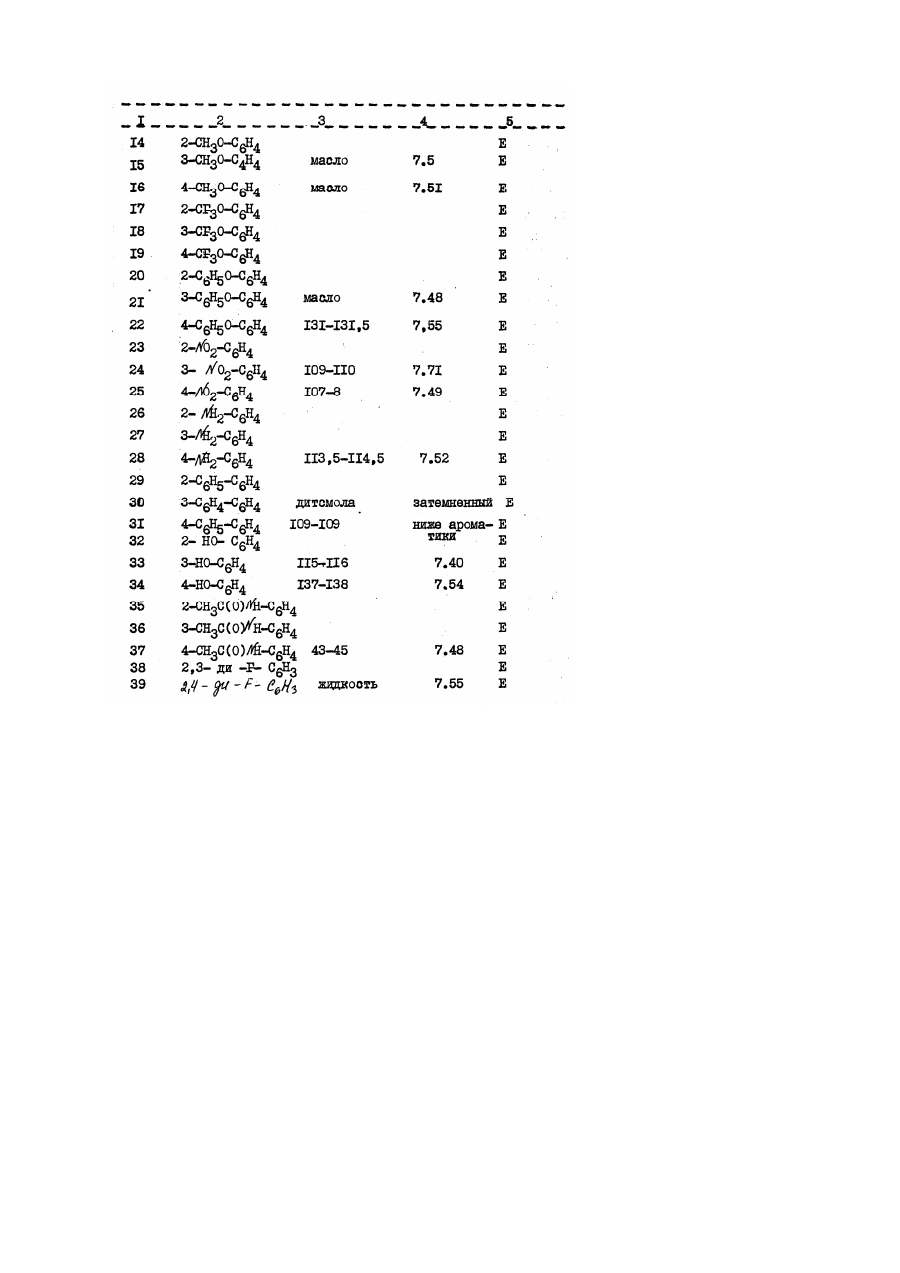
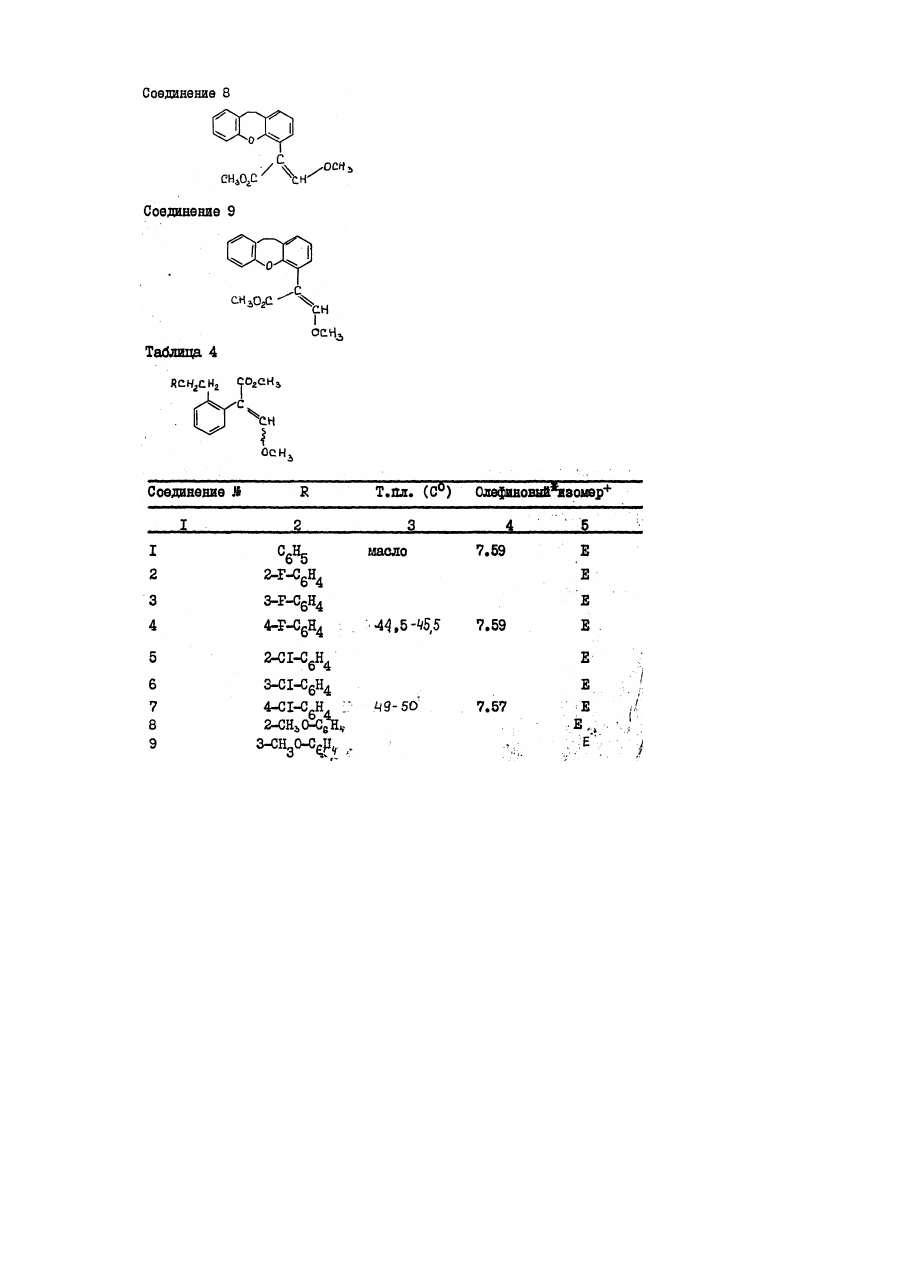
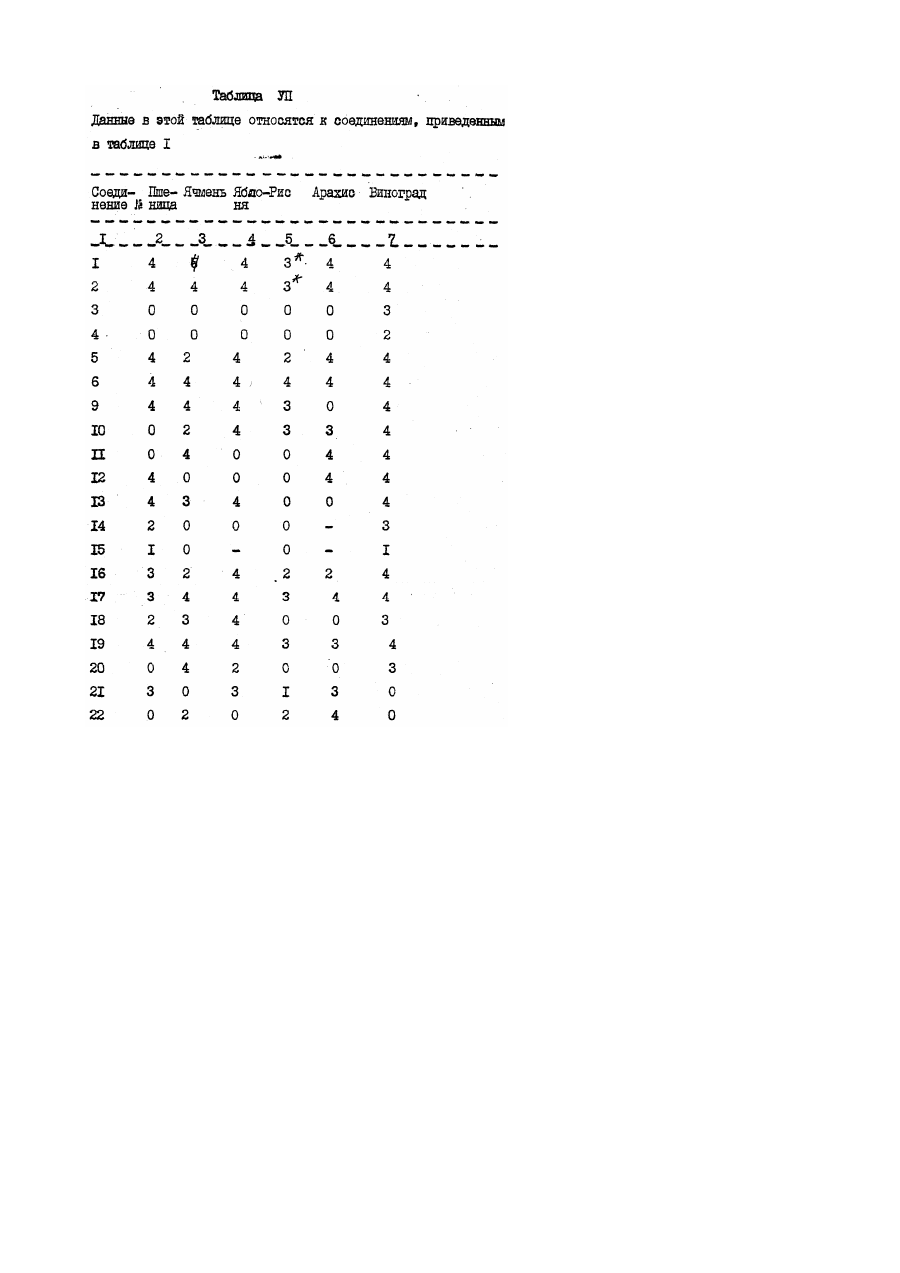
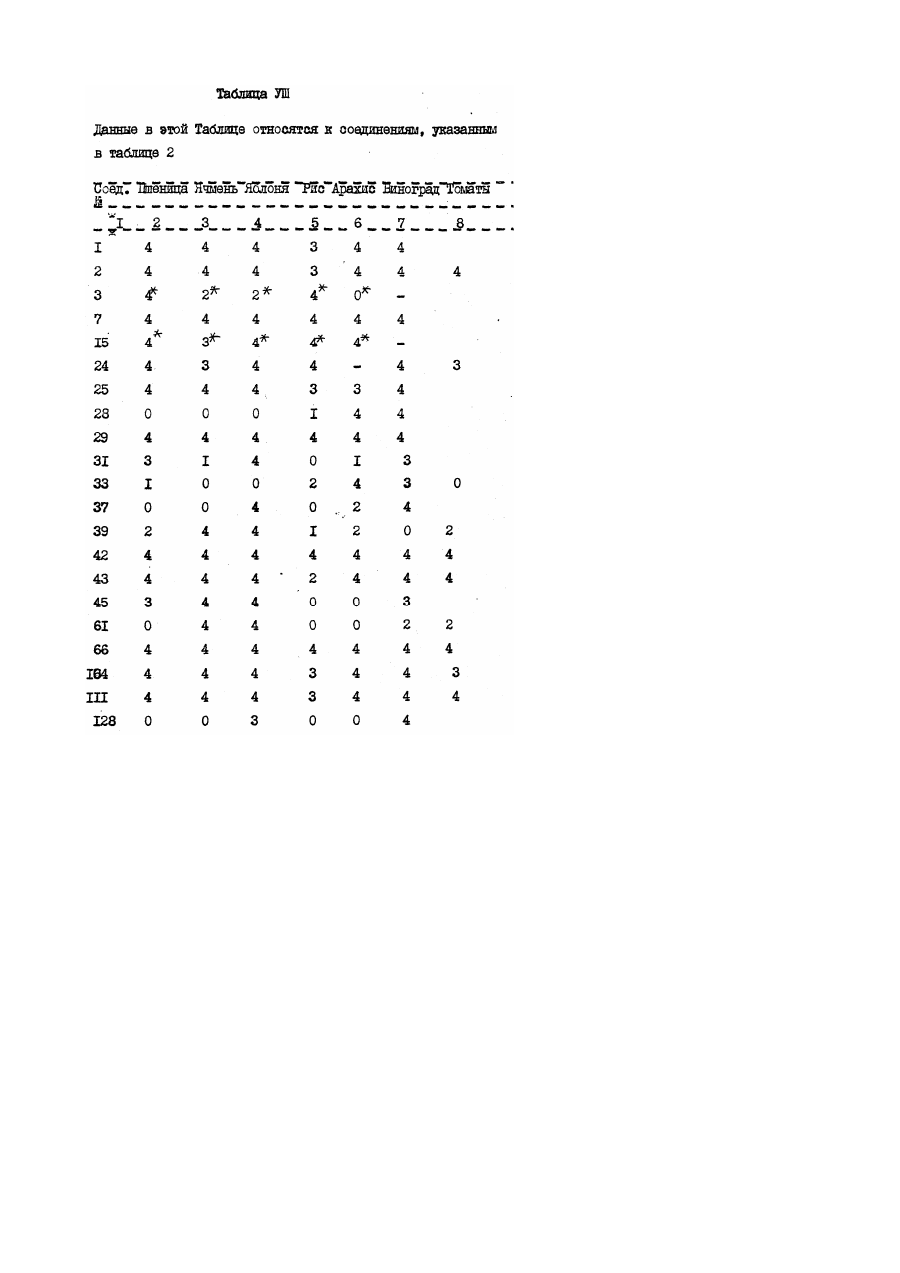
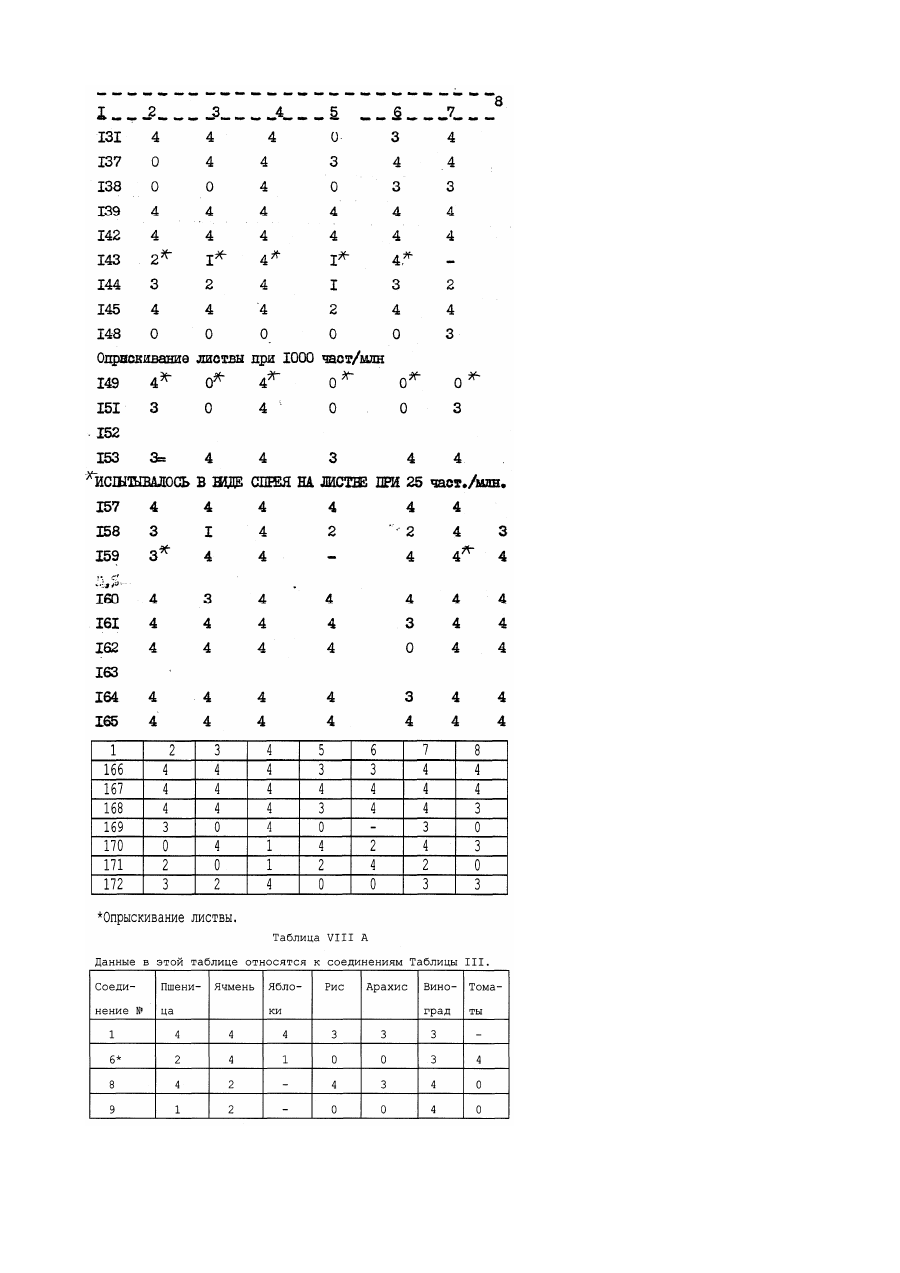
Настоящее изобретение относится к производным акрилевой кислоты, полезным в сельском хозяйстве и, в частности, пригодным для применения в качестве фунгицидов, инсектицидов или регуляторов роста растений. Согласно изобретению предлагается соединение общей Формулы (I) : и его стереоизомеры, где: Х, находящийся в орто-положении относительно акрилатной группы, представляет собой водород, фтор, хлор, бром, С1-С6 алкил, фенил С1-С4 алкил, в котором фенильная группа необязательно может быть замещена фтором, хлором или метоксигруппой; трифторметил; бромметил; диметоксиметил; феноксиметил, необязательно замещенный хлором; пиридилэтил; фуранилэтил; тиенилэтил; этоксикарбонилэтил; этенил, необязательно замещенный фенилом, циано С1-С3 алкоксикарбонилом, бензилоксикарбонилом, ацетилом, фурилом или бензтиазолилом, этинил, замещенный фенилом или третбутилом; фенил; С1-С6 алкокси; аллилокси, не обязательно замещенный фенилом; бензилокси, фенокси; необязательно замещенный фтором, хлором, бромом, гидрокси, метилом, трифторметилом, формилом, С1-С6 алкокси необязательно замещенным фтором, пропенилокси, пропаргилокси, ацетокси, метилсульфонилокси, фенилом, фенокси, нитро, амино, формиламино или ацетиламино; фенилтио, фенилсульфинил; нафтилокси, пиридилокси, необязательно замещенный трифторметилом, изобутирилокси, бензоилокси, необязательно замещенный третбутилом, формил, бензоил, необязательно замещенный метокси, С1-С3 алкоксикарбонил; циклогексилоксикарбонил; аллилоксикарбонил; феноксикарбонил, замещенный метокси, нитро, бензоиламино, фуроиламино или Nтиенилкарбонил - N- метиламино; У, находящийся в орто-, мета- или пара-положении относительно акрилатной группы, представляет собой водород, фтор, хлор, бром, метил, фенилэтенил, нитро или фенокси; Z представляет собой атом водорода, или Х и У, когда они находятся в соседних положениях фенильного кольца, вместе друг с другом образуют конденсированное бензольное кольцо, необязательно замещенное фенилом, конденсированное нафталиновое кольцо, конденсированное бензофуранильное кольцо, конденсированное бензотиенильное кольцо, или группу или группы У и Z, когда они находятся в соседних положениях фенильного кольца, вместе друг с другом образуют конденсированное бензольное кольцо, за исключением того, что, когда Х представляет водород, У не является водородом или пара-хлором. Соединение согласно изобретению содержит не менее одной двойной связи углерод-углерод, и иногда его получают в виде смесей геометрических изомеров. Однако, эти смеси могут быть разделены на индивидуальные изомеры, и настоящее изобретение охватывает подобнее изомеры. Алкильные группы могут быть представлены в виде прямоцепочечных или разветвленных радикалов, и примерами их являются метил, этил, пропил, (н – или изопропил) и бутил ( н - втор, изо- или трет-бутил). В качестве примеров согласно изобретению предлагаются соединения: (соединение № І в приведенной ниже таблице I) (соединение № 5 в приведенной ниже таблице I) (соединение № 9 в приведенной ниже таблице I) (соединение № І в приведенной ниже таблице IІ) (соединение № І в приведенной ниже таблице IV). Приведенная ниже таблица ІІІ охватывает соединения общей формулы: где группа включает все группы, приведенные в таблице II для каждой из нижеследующих схем замещения на приведенном выше фенильном кольце. Акрилатная группа МОЖЕТ иметь в каждом случае либо Е-геометрию, либо Z-геометрию. Конкретными примерами соединений, представленного в таблице III типа являются следующие: Сконденсированные кольцевые заместители Таблица V Таблица V охватывает соединения общей формулы где группа R, включает все группы R, приведенные в таблице ІV для каждой из нижеследующих характеров замещения на приведенном выше фенильном кольце_. В каждом случае акрилатная группа может иметь либо Е-геометрию, либо - Z-геометрию. Таблица VI: выбранные данные протонной ЯМР-спектроскопии. В таблице VІ приведены выбранные данные протонной ЯМР-спектроскопии для некоторых соединений, описанных в таблицах I, и охарактеризованных в них как масла. Химический сдвиг измерен в млн.дол. относительно тетраметилсилана, а в качестве растворителя использован дейтерохлороформ. Используются следующие сокращения: Соединения согласно изобретению, имеющие общую формулу (I), могут быть получены из замещенных бензолов общей формулы (IV) с помощью стадий, представленных на схеме I. В материалах схемы I радикалы R1 и R2 представляют метил, Х У и Z имеют приведенные выше определения, L-атом галогена (иод бром или хлор) или атом водорода, а М-атом металла (например, атом лития) или атом металла плюс ассоциированный атом галогена (например MgI, MgBr или MgCl). Так, соединения общей формулы (I), могут быть получены обработкой кетоэфиров общей формулы (II) фосфоранами общей формулы (V) в обычном растворителе, таком как диэтиловый эфир (см. например, W.Steglich, G.Schramm, T.Anke, K.Oberwinkler, Европейский патент № 0044448, 4,7.80). Кетоэфиры общей формулы (II) могут быть получены обработкой металлированных веществ (III) оксалатом (VI) в подходящем растворителе, таком как диэтиловый эфир или тетрагидрофуран. Предпочтительный способ зачастую включает медленное добавление раствора металлированных веществ (III) к перемешиваемому раствору избытка оксалата (VI) (см. например L.M.Weinstock, R.B.Curril, A.V.Lovell, Synthetic Communications, 1981, II, 943 и приведенные там ссылки). Металлированные вещества (III), в которых М - Mg I, MgBr или MgCl (реактивы Гриньяра), могут быть получены стандартными методами из соответствующих ароматических галогенидов (IV) где L=1, Br или Сl, соответственно. В случае некоторых заместителей Х, У и Z металлированные вещества (III), в которых М=Li, могут быть получены прямым литий-замещением соединений (ІV), в которых L=H с использованием сильного литиевого основания, такого как н-бутиллитий или литий-ди-изопропиламид Э (см. например, H.W.Grehwend, H.R.Rodriguez, Organic Reactions, 1879, 26, I). Соединения общей формулы (IV) могут быть получены стандартными методами, описанными в химической литературе. Схема I Альтернативные методы получения кетоэфиров общей формулы (II) описаны в химической литературе (см. например, D.C.Atkinson, K.F.Godfrey, B.Meek, Y.F.Savilh, M.R.Stillings, Y.Med.Chem 1983, 26, 1353, D.Horne, Y.Gandino, W.Y.Thompson Tetrahedson Lett 1984, 25, 3529 и G.P.Axiotis, Tetrahedson Lett 1981, 22, 1509). Альтернативные способы получения соединений согласно изобретению, имеющих общую формулу (I), проиллюстрированы схемой. В схеме II радикалы R, R2, X, Y и Z имеют приведенные выше определения. Схема II Соединения общей формулы (I) могут быть получение обработкой фенилацетатов обшей формулы (VII) основанием или эфиром муравьиной кислоты, таким как метилформиат или HCO2R1 іде R1 - определен выше в подходящем раствориете. Если реакцию гасят веществом общей формулы R2, где R2 - определен выше, а Q отщепляемая группа, такая как атом галогена, то могут быть получены соединения общей формулы (I). Соединения общей формулы (I), в которой R2=Н, могут быть преобразованы в соединения (I), в которых 2 R не является атомом водорода, последовательной обработкой основанием (например, карбонатом калия или гидридом натрия) и веществом общей формулы R2Q, где R2 и Q - определены выше, в подходящем растворителе. Далее, соединения общей формулы (I), могут быть получены из ацеталей общей формулы (VIII), в щелочных или кислотных условиях, в подходящем растворителе и при подходящих температурах. Примером подходящего основания является ди-изопропиламид лития, а кислый сульфат калия является примером подходящего кислого реагента (см. T.Yamada, H.Hagiwara, H.Uda, Y. of Chem Soc., Chem Commun, 1980, 838 и приведенные там ссылки.) Ацетали общей формулы (VIII), могут быть получены из сложных эфиров фенилуксусной кислоты, имеющих общую формулу (VII) обработкой алкилсилил-кетон-ацетальных производных веществ (VII) триалкилортоформиатами в присутствии кислоты Льюиса в подходящем растворителе и при подходящей температуре (см. например, R.Saigo, M.Osaki, T.Makaiyama, Chem Lett 1976, 769). Соединения общей формулы (VII) могут быть получены стандартными методами, описанными в химической литературе. Соединения и комплексы металлов согласно изобретению являются активными фунгицидами, особенно в отношении следующих заболеваний: Pyricularia oryzal на рисе, Puccinia recondita, Puccinia stiiformis и прочие ржавчины на пшенице, Puccinia hardci, Puccinia striiform и прочие ржавчины на ячмене, и ржавчины на других культурах, например, на кофе, грушах, яблонях, орехах, овощах и декоративных растениях, Eryziphe gronuinis (мучнистая роса) на ячмене и пшенице и прочие мучнистые росы на различных культурах, таких как Sphaerotheca macularis на хмеле, Sphaerotheca fuliginea на тыквенных (напр. огурцах), Podosphaera Leucotricha на яблонях, и Uncinula necator на винограде, Helminthosporium spp., Rhynohosporium spp., Septori spp., Pseudocercosporella herpotrichoides и Ganamannonyces grauinis на злаках, Cercospora arachidicola и Cercosporidium personota на орехах и прочие виды Cercospora на других культурах, например сахарной свекле, бананах сое-бобах и рисе, Botrytis cinerea (серая плесень) на томатах, землянике, овощах, винограде и прочих культурах, Alternaria spp., на овощах (например, огурцах) сурепице масличной, яблонях, томатах и прочих культурах, Venturia inaequnalis (парша на яблонях); Plasmopara viticola на винограде. Прочие ложные мучнистые росы, такие как Bremia lactucal на салате, Personospora spp, на сое-бобах, табаке, луке и других культурах и Pseudoperonospora buneu на хемеле и Pseudoperonospora cubensis на тыквенных, Phytophthora infestaus, на картофеле и томатах и прочие Phytophthora spp на овощах, землянике, авокадо, перце, декоративных растениях, табаке, какао и других культурах. Thanatephorus cucumeris на рисе и другие Phizoctonia spp на различных культурах, таких как пшеница и ячмень, овощи, хлопчатник и газонные травы. Некоторые из соединений проявляют также широкий спектр, активности по отношению к грибам in vitro. Они проявляют активность в отношении послеуборочных заболеваний плодов (напр. Penicillium digitatium и italium и Tricderma viride на апельсинах и Gloesporium musarum на бананах). Далее, некоторые из соединений могут применяться в качестве протравителей семян против Fusarium spp, Septori spp, Fillctia spp (твердая головня пшеницы), Rhizoctonia solouei на хлопчатнике и Pyricularia oryzae на рисе. Соединения могут перемещаться акропетально в тканях растений. Кроме того, соединения могут быть достаточно летучими, чтобы быть активными в паровой фазе в отношении грибов на растении. Соединения могут быть пригодными в качестве промышленных (в противоположность сельскохозяйственным) фунгицидам, например для защиты от действия грибов на древесину, шкуры, кожу и особенно, красочные пленки. Некоторые из соединений проявляют гербицидную активность а при повышенной норме внесения могут использоваться для борьбы с сорняками. Аналогично, некоторые соединения проявляют активность регулирования роста растений и могут употребляться с этой целью, также при подходящей норме внесения. Соединения могут применяться для фунгицидных целей как таковые, но более удобно их составление в виде композиций, содержащих соединение общей формулы (I), определенной выше, или его комплекс металла, и необязательно, носитель или разбавитель. Соединения согласно изобретению, могут применяться для борьбы с грибками, путем нанесения на растения, семена растений или на места произрастания растений или семян, соединения или его комплекса металла, как это определено выше. Соединения и комплексы металлов согласно изобретению могут наноситься разными способами. Например, они могут применяться в виде композиции или как таковые, непосредственно на листья растений, или к! они могут наноситься также на кусты или деревья, на семена или на другую среду, в которых растения, кусты иди деревья растут или предполагается их высаживание, или они могут разбрызгиваться, распаляться или наноситься в виде крема или пасты, в виде паров, или в виде гранул с замедленным выделениям активного вещества на любую часть растения, куста и/или дерева, например, на листья, стебли, ветви или корни, или на почву, окружающую корни, или на семена перед их посадкой, или же на почву вообще, вводиться в воду орошаемого поля или же в гидропонные системы культивирования. Соединения согласно изобретению могут использоваться также для инъекций в растения или деревья и разбрызгиваться на растительность с использованием методов электродинамического опрыскивания, или других малообъемных методов нанесения. Термин "растение", используемый здесь, включает проростки, саженцы, кусты и деревья. Фунгицидный способ, для которого могут применяться соединения, согласно изобретению, включает профилактическую, защитную, а также уничтожение. Соединения предпочтительно используют для сельскохозяйственных - полеводческих и садоводческих целей в виде композиции. Тип используемой в любом случае композиции определяется конкретным предполагаемым назначением. Композиции могут быть представлены в виде пылящих порошков или гранул, содержащих активный ингредиент, и твердый разбавитель, или носитель, например, такие наполнители, как каолин, бентонит, кизельгур, доломит, карбонат кальция, тальк, порошковую магнезию, фуллерову землю, гипс землю Хьюитта, диатомит и глинозем. Подобные гранулы могут быть в виде предварительно сформированных гранул, пригодных для нанесения на почву без дальнейшей обработки. Эти гранулы могут быть приготовлены либо пропитыванием окатышей наполнителя активным ингредиентом, либо гранулированием смеси активного ингредиента и порошкового наполнителя. Композиции для протравливания семян, например, могут содержать вещество (например, минеральное масло), способствующее адгезии композиции к семенам, в альтернативе активный ингредиент может преобразовываться в препаративную форму для целей протравливания семян с использованием органического растворителя (например, N-метил-пирролидона или диметилформамида). Композиции могут быть также в виде диспергируемых порошков, гранул или зерен, содержащих смачивающий агент для облегчения диспергирования в жидкостях порошка или зерен, которые могут также содержать наполнители и суспендируещие вещества. Водные дисперсии иди эмульсии могут быть приготовлены растворением активного ингредиента (ов) в органическом растворителе, необязательно содержащем смачивающие, диспергирующие или эмульгирующие вещества. Подходящими органическими растворителями являются этиленхлорид, изопропиловый спирт, пропиленгликоль, диацетоновый спирт, толуол, керосин, метилнафталин, ксилолы, трихлорэтилен, фурфуриловый спирт, тетрагидрофурфуриловый спирт и простые гликолевые эфиры (например, 2-этоксиэтанол и 2-бутоксиэтанол). Композиции, предназначенные для применения путем разбрызгивания, могут быть в виде аэрозолей, и в этом случае состав содержится в емкости под давлением в присутствии пропеллента, например, фтортрихлорметана или дихлордифторметана. Соединения могут быть смешаны в сухом состоянии с пиротехнической смесью с образованием композиции, пригодной для создания в замкнутых помещениях дыма, содержащего соединения. В альтернативе, соединения могут использоваться в микрокапсулированной форме. Они могут быть также составлены в виде биоразлагаемых полимерных составов, обеспечивающих медленное, регулируемое высвобождение активного вещества. Благодаря включению подходящих добавок, например, добавок для улучшения распределения, адгезионной силы и стойкости к дождю на обработанных поверхностях, самые разные композиции могут быть лучше приспособлены для различных целей. Соединения могут использоваться в смесях с удобрениями (например, азот-, калий или фосфор содержащими удобрениями). Предпочтительны композиции, содержащие лишь гранулы удобрения, включающие соединение, например, покрытые им. Подобные гранулы обычно содержат до 25 масс.% соединения. Поэтому, согласно изобретению предлагается удобрительная композиция, содержащая соединение общей формулы (I) или его комплексы металла. Композиции могут быть также представлены в виде жидких препаратов для применения а путем погружения или опрыскивания, которые обычно представляют собой водные дисперсии или эмульсии, содержащие активный ингредиент в присутствии одного или большего числа ПАВ, например, смачивающего, диспергирующего, эмульгирующего или суспендирующего вещества, или представляет собой разбрызгиваемые составы, пригодные для применения в электродинамических опрыскивателях. Указанные вещества могут быть катионными, анионными или неионными. Подходящими катионными веществами является четвертичными соединениями аммония, например, цетилтриметиламмонийбромид. Подходящими анионными веществами являются мыла, соли алифатических моноэфиров серной кислоты, (например, лаурилсульфат натрия) и соли сульфированных ароматических соединений (например, додецилбензолсульфонат натрия, лигносудьфоват натрия, кальция или аммония, бутилофталинсудьфонат, и смесь диизопропил- и три- изопропилнафталинсульфонатов натрия.). Подходящими неионными веществами являются продукты конденсации окиси этилена с жирными спиртами, такими как олеиловый или цетиловый спирт или с алкилфенолами, такими как октил- илин нонилфенол и октилкрезол. Другими неионными веществами являются частичные сложные эфиры на основе длинноцепочечных жирных кислот и гекситангидридов, продукты конденсации указанных частичных сложных эфиров с окисью этилена и лецитины. Подходящими суспендирующими веществами являются гидрофильные коллоиды (например, поливинилпирролидон и натрий-карбоксиметилцеллюлоза), и растительные камеди (например, аравийская камедь и трагакант). Композиции для применения в виде водных дисперсий или эмульсий обычно поставляются в виде концентрата, содержащего высокую долю активных ингредиентов и концентрат должен разбавляться водой перед употреблением. Эти концентраты зачастую должны выдерживать хранение в течение продолжительного времени и после такого хранения должны допускать разбавление водой для получения водных препаратов, которые остаются однородными в течение времени, достаточного для их нанесения традиционным и электродинамическо - распылительным оборудованием. Концентраты могут обычно содержать до 95%, более предпочтительно 10-85% например, 25-60% по массе активных ингредиентов. Эти концентраты обычно содержат органические кислоты (например, алкарил- или арил-сульфоновые кислоты, такие как ксилолсульфокислоты или додецилбензолсульфокислота), поскольку присутствие таких кислот может повышать растворимость активных ингредиентов в полярных растворителях, часто используемых в концентратах. Концентраты обычно содержат также и высокую долю ПАВ, чтобы получались достаточно стабильные эмульсии в воде. После разбавления с образованием водных препаратов, они могут содержать различные количества активных ингредиентов в зависимости от поставленной цели, но могут использоваться и водные препараты, содержащие от 0,0005% или 0,01% до 10% по массе активных ингредиентов. Композиции, могут содержать также и другие изобретения, имеющие биологическую активность, например, соединения, имеющие сходную или дополняющую фунгицидную активность, или соединения, проявляющие гербицидную или инсектицидную активность или активность регулирования роста растений. Другим фунгицидным соединением может быть, например, соединение, способное подавлять болезни колосьев злаков (например, пшеницы) вызываемые, например, Septoria, Gibberella и Helminthosporium spp., болезни, возникающие в семенах и почве, и ложную и истинную мучнистую росу на винограде, мучнистую росу и пару на яблонях и т.п. Эти смеси фунгицидов могут иметь более широкий спектр активности, чем соединение общей формулы (I) само по себе, кроме того, другой фунгицид может оказывать синергетический эффект на фунгицидную активность соединения общей формулы (I). Примерами других фунгицидных соединений являются карбендазим, беномил, тиофанат-метил, тиабендазод, фуберидазол, этридазол, дихлорфлуанид, цимоксанил, оксадиксил, офурас, металаксил, фуралаксил, беналаксил, фосетил-алюминий, фенаримол, ипродион, процимидион, винклозолин, пенконазол, миклобутанил, R 0151297, S 3308, пиразофос, этиримол, диталимфос, тридоморф, трифорин, нуаримл, триазбутил, гуазатин, пропикопазол, прохлораз, флутриафол, хлортриафол, т.е. химическое вещество I - (1,2,4-триазол-1-ил) -2- (2,4-дихлорфенил)-гексан -2- ол, DPХ Н6573 (I- ((бис-4фторфенилэ)метил силил) метил)-ІН-1,2,4-триазол-триадимефон, триадименол, дихлобутразол, фенпропиморф, фенпропидин, триадеморф, имизалил, фенфурам, карбоксин, оксикарбоксин, метфуроксам, додеморф, ВАS 454, бластицидин, касугамицин, эндифенфос, китазин Р, фталид, пробеназол, изопротиолан, трициклазол, пироквилан, хлорбензтиазон, неоасозин, полиоксин D валидамицин А, репронил, флутоланил, пенцисурон, дикломезин, феназиноксид, диметилдитиокарбамат никеля, теклофталам, битертанол, бупиримат, этаконазол, стрептолицин, ципофурам, билоксазол, квинометионат, диметиримол, фенапанил, толкфлос-метил, пироксифур, полирам, манеб, манкозеб, каптафол, хлороталонил, анилазин, тирам, каптан, фолпет, цинеб, пронинеб, сера, динокап, бинапакрил, нтро-тал-изопропил, додин, дитианон, фентин-гидроокись, фентин-ацетат, текназен, квинтозен, дихлоран, мель-содержащие соединения, такие как оксихлорид меди, сульфат меди и бордосская смесь, и ртуть-органические соединения, такие как 1-(2-циано-2-метоксииминоацетил)-3-этилмочевина. Соединения обшей формулы (I) могут быть смешаны с почвой, торфом или другой средой для размещения корневой системы, для защиты растений от грибных заболеваний, возбудители которых располагаются в семенах, почве иди на листве. Подходящими инсектицидами является пиримикарб, диметоат, деметон, -S-метил, формотион, карбарил, изопрокарб, ХМС, ВРМС, карбофуран, карбосульфан, диазинон, фентион, фенитротион, фентиоат, хлорпирифос, изоксатио, пропафос, монокротофас, булрофузин, этропроксифен и циклопротрин. Регулятором роста растений может быть соединение, которое регулирует рост сорняков или образование семенной шапки, или избирательно регулирует рост менее желательных растений (например, трав). Примерами подходящих регулирующих рост растений соединений для применения в сочетании с соединениями согласно изобретению являются гибереллины (например, GA3, GA4 или GA7), ауксины (например, индолуксусная кислота, индолбутировая, нафтоксиуксусная или нафтилуксусная кислоты), цитокинины (например, кинетин, дифенилмочевина, бензимидазол, бензиладенин или бензиламинопурин), феноксиуксусные кислоты (например, 2,4-D или МСРА), замещенные бензойные кислоты (например, трииодобензойная кислота), морфактины (например, хлорфторекол), малеиновый гидразин, глифосфат, глифосин, длинноцепочечные жирные кислоты и кислоты, декегулак, паклобутразол, флурпримидол, фторидамид, мефдуидид, замещенные четвертичные соединения аммония и фосфония (например, хлормекват, хлорфоний или мепикватхлорид) этефон, карбетамид, метил-3,6-дихлор-анизат, даминозид, асулам, абсцисиновая кислота, изопиримол, 1-(4хлорфенил)-4,6-диметил-2-оксо-1,2-дигидропиридин-3-карбоновая кислота, гидроксибензонитрилы (например, бромоксинил), дифензикват, бензоилпроп-этил-3,6-дихлорпиколиновая кислота, паклобутразол, фенпентезол, инабенфид, триапентонол и текназен. Нижеследующие примеры иллюстрируют изобретение. В примерах термин "эфир" относится к диэтиловому эфиру, сульфат магния используется для осушения растворов и реакции с участием чувствительных к воде промежуточных соединений осуществляют в атмосфере азота. Если нет иных указаний, хроматографию производят с использованием силикагеля в качестве неподвижной фазы. Там, где приведено данные ИК- и ЯМР- спектроскопии являются выборочными, не предпринимались попытки указать каждую линию поглощения. Использованы следующие сокращения: ТHF = тетрагидрoфуран (ТГФ) s = синглет (с) DMF = N,N-диметилформамид (ДМФА) d = дублет (д) GC = газовая хроматография t = триплет (т) МS = масс-спектр m = мультиплет (м) Пример 1 Этот пример иллюстрирует получение 2 Е,1n Z-метил-3-метокси-2-[2'- (2''-фенилэтенил) фенил] пропеноат (соединение № 5 в таблице 1). Трет-бутилат калия (5,30 г) добавляют в виде одной порции к энергично перемешиваемой суспензии бензилтрифенилфосфоний-хлорида (21,02 г) в сухом эфире (250 мл). Спустя 25 минут результирующую оранжевую смесь обрабатывают раствором 2-бром-бензальдегида (5,00 г) в сухом эфире (50 мл) и смесь светлеет по цвету. Спустя еще час смесь выливают в воду и экстрагируют эфиром. Экстракты промывают водой, осушают, концентрируют при пониженном давлении и хроматографируют с использованием дихлорметана в качестве элюента с получением 1-фенил-2-(2-бромфенил) этилена (5,95 г выход 85%), почти бесцветного масла в виде смеси 5:1 Z:Е-изомеров (по данным GC/MS). Раствор реактива Гриньяра, полученного из части смеси изомеров описанного выше 1-фенил-2-(2бромфенил) этилена (5,58 г) и магния в сухом ТГФ (20 мл) добавляют каплями в течение 30 минут к перемешиваемому раствору диметилоксалата (5,06 г) в сухом ТГФ (40 мл) охлаждением до -15°С. Результирующую смесь перемешивают при -15°С в течение 30 минут, затем при комнатной температуре в течение 1 часа, затем выливают в разбавленную хлористоводородную кислоту и экстрагируют эфиром. Экстракты промывают водой, осушают, концентрируют при пониженном давлении, затем дважды хроматографируют [(i) 30% эфиром в бензине : (ii) 20% гексаном в дихлорметане] с получением изомерного чистого Z-метил-2-(2'-фенилэтенил) фенилглиоксалата (1,76 г выход 31%) в виде желтого масла Н ЯМР (CDCl3) : δ 3,87 (3Н,с) 6,78 (центр 2 дублетов каждый по 1Н, j=12 Гц) млн-1. Трет-бутилат калия (2,00 г) добавляют в виде одной порции к перемешиваемой суспензии (метоксиметил) трифенил-фосфоний хлорида (6,78 г) в сухом эфире (80 мл). Спустя 25 минут результирующую красную суспензию обрабатывают раствором Z-метил2-(2'-фенилэтенил) фенилглиоксалата (1,76 г) в сухом эфире (20 мл), причем окраска светлеет. Спустя 1,5 часа, реакционную смесь выливают в воду и экстрагируют эфиром. Экстракты промывают водой, осушают, пропускают через короткую колонку с силикагелем с использованием дихлорметана, затем осторожно хроматографируют используя 30% эфир в бензине в качестве элюента, с получением целевого соединения (0,46 г, выход 24%) в виде масла, ИК-спектр (пленка) : 1715, 1635 см-1, 'Н ЯМР (СDС3) : δ 3,62 (3Н,с) 3,73 (3Н,с) 6,48 (2Н,с) 7,50 (1Н,c) млн-1. Пример 2 Этот пример иллюстрирует получение 2Е, І''Е - и 2Z І''Е-метил-3-метокси-2-[2-(2-фенилэтенил) фенил] пропеноата (соединения №№ 1 и 2 в таблице I). Раствор 2-бромбензальдегида (18,50 г) в сухом эфире (20 мл) добавляют каплями к перемешиваемому раствору бензилмагнийхлорида (получен из бензилхлорида (12,64 г) и магния (2,68 г) в сухом эфире (120 мл), причем в ходе добавления образуется густой осадок. Смесь перемешивают 1 час при комнатной температуре, затем выливают в воду, подкисляют 2М хлористоводородной кислотой, и экстрагируют эфиром. Смесь перемешивают 1 час при комнатной температуре, затем выливают в воду, подкисляют 2М хлористоводородной кислотой и экстрагируют эфиром. Смесь перемешивают 1 час при комнатной температуре, затем выливают в воду, подкисляют 2М хлористоводородной кислотой и экстрагируют эфиром. Экстракты промывают водой, осушают, концентрируют и хроматографируют с использованием дихлорметана-бензина (1:1) в качестве элюента, получая 1-(2-бром-фенил)-2-фенилэтан-1-ола (10,95 г 40%) в виде белого твердого вещества, температура плавления 84-85°С. Перемешиваемую смесь 1-(2-бром(фенил)-2-фенилэтан-1-ола (15,50 г) и ортофосфорной кислоты (150 мл) нагревают при 170°С в течение 1 часа, а затем выливают в воду со льдом и экстрагируют эфиром. Экстракты промывают водой, осушают и концентрируют с получением сырого продукта в виде оранжевого масла (14,29 г). Испарительная дистилляция (0,3 торр, температура в печи 140°С дает E-1-фенил-2-(2-бромфенил) этилен (12,53 г выход 86%) в виде бледно-желтого масла чистотой 97% по данным газовой хроматографии. Раствор реактива Гриньяра, полученного из Е-1-фенил-2-(2-бромфенил) этилена (8,56 г) магния (0,96 г) в сухом тетрагидрофуране (20 мл) добавляют каплями на протяжении 30 минут к перемешиваемому раствору диметилоксалата (7,76 г) в сухом тетрагидрофуране (70 мл), охлажденном до -15°С. Результирующую смесь перемешивают при -15°С в течение 30 минут, затем при комнатной температуре в течение 1 часа, после чего выливают в разбавленную хлористоводородную кислоту и экстрагируют эфиром. Экстракты промывают водой, осушают и концентрируют эфиром. Экстракты промывают водой, осушают и концентрируют с получением сырого продукта в виде желтого масла (17,22 г). Очистка хроматографией в колонке с использованием дихлорметана и бензина (1:1) в качестве элюента и последующая испарительная дистилляция (0,07 торр, температура в печи 170°С) дает Е-метил-2-(2-фенилэтенил) фенилглиоксалат (2,01 г, выход 23%) в виде желтого масла, чистого по данным газовой хроматографии, Н ЯМР (C DCl3) δ : 3,78 (3H,c) 6,88 (центр 2 дублетов, у каждый по 1Н, j = 1,6 Гц) млн-1. Третбутилат калия (2,19 г) добавляют в виде одной порции к перемешиваемой суспензии (метоксиметил) трифенилфосфоний хлорида (7,41 г) в сухом эфире (100 мл). Спустя 25 минут результирующую красную суспензию обрабатывают раствором Е-метил-2-(2-фенилэтенил) фенилгекглиоксалата (1,92 г) в сухом эфире (20 мл) причем цвет просветляется. Спустя 15 минут смесь выливают в воду и экстрагируют эфиром. Экстракты промывают водой, осушают и хроматографируют, используя 30% эфир в бензине в качестве элюента, с получением (i) 2Е І" Е – изомера целевого соединения, элюируемого первым, в виде бледно-желтого масла (1,06 г выход 50%), которое кристаллизуется при стоянии, давая белое твердое вещество, температура плавления 103-104°С. Аналитическая проба, перекристаллизованная из смеси эфир-бензин, имеет температуру плавления 107-108°С, ИК-спектр (взвесь в нуйоле):1700-1630 см-1 Н ЯМР (C DCl3) : δ 3,68 (3H,c) 3,80 (3H,c) 7,06 (2H,c) 7,63 (1H,c) млн-1, и (ii) 2Z, I" Е (изомера целевого соединения, элюируемого вторым, в виде вязкого масла (0,260 г выход 12% ИК-спектр (пленка) 1710, 1625 см-1 1Н ЯМР (C DCl3) δ : 3,65 (3H,c) 3,92 (3H,c) 6,57 (1H,c) 6,99 и 7,24 (каждый 1Н, д j = 16 Гц) млн-1. Пример 3 Этот пример иллюстрирует получением Е-метил 2-(2-)хлор-6-фторфенил)-3-метоксипропеноата (соединение №16 в таблице I). Смесь метил (2-хлор-6-фторфенил) ацетата (5,20 г) и метилформиата (31,4 мл в сухом) диметилформамиде (40 мл) каплями добавляют к перемешиваемой суспензии гидрада натрия (1,23 г) в сухом ДМФА (40 мл) при температуре от 0 до 5ºС. Наблюдается интенсивное выделение газа. Реакционную смесь перемешивают при комнатной температуре в течение 3,5 часов, затем выливают в смесь льда и водного карбоната натрия, и промывают эфиром. Результирующую водную смесь подкисляют концентрированной хлористоводородной кислотой и экстрагируют эфиром. Экстракты проливают водой, осушают и концентрируют с получением метил 2-(2-хлор-5-фторфенил)-3-гидроксипропеноата (3,44 г) в виде белого твёрдого вещества. Перемешиваемый раствор этого сырого продукта в сухом ДМФА (30 мл) последовательно обрабатывают карбонатом калия (4,11 г) и димэтилсульфатом (1,34 мл). Полученную смесь перемешивают 1 час при комнатной температуре и затем выливают в воду и экстрагируют эфиром. Экстракты промывают водой, осушают и концентрируют с получением целевого соединения (2,91 г) в виде белого твердого вещества, температура плавления 77-78ºС. Кристаллизация из бензина (60-80 ºС) дает бесцветные кристаллы (2,61 г выход 52% из метил (2-хлор-6-фторфенил)ацетата), температура плавления 79-80 ºС ЯМР (C DCl3) : δ 3,69 (3H,c) 3,84 (3H,c) 7,62 (1H,c) млн. Пример 4 Этот пример иллюстрирует получением Е-метил 2-(2-фенокси)-фенил-3-метоксиакрилаза (соединение № 1 в таблице II). Трет-бутилат калия (5,6 г) добавляют к перемешиваемому раствору дифенилового эфира (12,3 г) в сухом эфире (150 мл) при -70ºС. Результирующую смесь перемешивают при этой температуре 15 минут, затем добавляют Н-бутил-литий (30,5 мл 1,62 М раствора в гексане) с получением красно-коричневой суспензии, которую оставляют прогреваться до комнатной температуры. Эту смесь добавляют к перемешиваемой суспензии диметилоксалата (11,8 г) в эфире (250 мл) при -10 на протяжении 20 минут, после чего оставляют прогреваться до комнатной температуры. Спустя 30 минут смесь выливают в воду и экстрагируют эфиром. Скомбинированные экстракты промывают водой, осушают, затем концентрируют с получением красного масла (14,21 г). Хроматография с использованием 20% эфира в бензине в качестве элюента дает метил 2феноксибензоилформиат (2,23 г) в виде желтого масла. Трет-бутилат калия (2,64 г) добавляют к энергично перемешиваемой суспензии (метоксиметил) трифенил-фосфоний-хлорида (8,93 г) в сухом эфире (100 мл). Спустя 20 минут результирующую красную суспензию обрабатывают раствором метил-2-феноксибензоилформиата (2,23г) в сухом эфире (20 мл), причем цвет просветляется. Спустя 15 минут смесь выливают в воду и экстрагируют эфиром. Скомбинированные экстракты промывают водой, осушают и концентрируют с получением желтого масла (7,30 г). Хроматография с использованием дихлорметана в качестве элюента дает целевое соединение (0,61 г) в виде бесцветного масла. ИК-спектр (пленка) 1710, 1635 см-1, Н ЯМР (C DCl3) : δ 3,60 (3H,c) 3,75 (3H,c) 7,47 (1H,c) млн. Пример 5 Этот пример описывает альтернативный способ получения Е-метил-2-(2-фенокси) фенил-3метоксипропеноата (соединение №1 в таблице II). IM раствор боран-тетрагидрофуранового комплекса (30 мл) каплями добавляют к перемешиваемому раствору 2-фенокси-бензойной кислоты (5,35 г) в сухом ТГФ (50 мл), охлажденном до 0°С (бурное выделение газа). После добавления смесь перемешивают 15 минут при 0°С, затем 1,5 часа при комнатной температуре. Ее выливают в воду и экстрагируют эфиром. Экстракты последовательно промывают водой, водным бикарбонатом натрия, водным карбонатом натрия, затем осушают и концентрируют при пониженном давлении с получением 2феноксибензилового спирта (4,83 г 97%) в виде бесцветного масла. К раствору 2-феноксибензилового спирта (4,80 г) в сухом дихлорметане (50 мл). Полученную смесь перемешивают 2 часа при комнатной температуре, затем промывают водой (х2), водным бикарбонатом натрия (х2) и водным хлоридом натрия, осушают и концентрируют при пониженном давлении с получением 2феноксибензилхлорида (4,87 г 93%) в виде бесцветного масла. Двуокись углерода барботируют в раствор 2-фенокси-бензилмагнийхлорида (из 2феноксибензилхлорида (4,80г) м и магниевой стружки (0,64 г) в сухом эфире (15 мл) охлажденном до 0°С. Для улучшения растворимости добавляют сухой ТГФ. После прекращения экзотермической реакции через смесь двуокись, углерода больше не пропускают и смеси дают возможность прогреваться до комнатной температуры. Смесь выливают в воду, промывают эфиром, затем обрабатывают хлористоводородной кислотой и экстрагируют эфиром. Экстракты промывают водой, осушают и концентрируют при пониженном давления с получением 2феноксифенилуксусной кислоты (3,0 6 г 61%) в виде твердого вещества, температура правления 82-85°С. Аналитическая проба, перекристаллизованная из эфира/бензина, имеет температуру плавления 85-86 °С. Раствор 2-феноксифенилуксусной кислоты (2,75 г) в сухом метаноле (30 мл), содержащем концентрированную серную кислоту (0,3 мл) нагревают с обратным холодильником в течение 2 часов, а затем оставляют охлаждаться, выливают в воду и экстрагируют эфиром. Экстракты промывают водой, сушат и концентрируют при пониженном давлении с получением метил 2-феноксифенилацетата (2,65 г 91%) в виде бледно-желтого масла. Этот сложный эфир преобразуют в 2 стадии в ы целевое соединение по методике, описанной в примере 3, то есть по реакции гидрида натрия и метилформиата и обработкой получающегося энола карбонатом калия и диметилсульфатом (общий выход = 65%). Пример 6 Этот пример иллюстрирует получение Е-метил-2-(2-бензил-окси) фенил-3-метоксиакрилата (соединение №145 в таблице II). Смесь метилформиата (24,4 мл) и метил о-(бензилокси) фенил-ацетата (5,10 г) в сухом ДМФA. (30 мл) каплями добавляют к перемешиваемой суспензии гидрида натрия (0,95 г) в сухом ДМФА (30 мл) при температуре от 0 до 5°С. Наблюдается энергичное выделение газа. Реакционную смесь перемешивают 3,5 часа при комнатной температуре, затем выливают в смесь льда и водного карбоната натрия. Полученный водный раствор промывают эфиром (х3), затем подкисляют концентрированной хлористоводородной кислотой и экстрагируют эфиром, экстракты промывают водой, сушат и концентрируют с получением метил 2-(2-бензилокси) фенил-3гидроксиакрилата (4,38 г) в виде желтого масла. Карбонат калия (4,26 г) и диметилсульфат (1,38 г) последовательно добавляют к перемешиваемому раствору метил-2-(2-бензилокси) фенил-3-гидроксиакрилата (4,38 г) в сухом ДМФА (40 мл). Спустя час при комнатной температуре реакционную смесь выливают в воду и экстрагируют эфиром. Экстракты промывают водой, сушат, концентрируют и растирают с бензолом, получая целевое соединение (3,38 г выход 57% из метил о-(бензилокси)-фенилацетата) в виде белого твердого вещества, температура плавления 74-75°С. Кристаллизация всего образца из метанола дает бесцветные кристаллы (2,35 г) температура плавления 76-77°С Н ЯМР (CDCl3) : δ 3,63 (3H,c) 3,75 (3H,c) 5,05 (2H,c) 7,49 (1H,c) млн-1. Пример 7 Этот пример описывает получение Е-метил-2-2-(4-метил-фенокси) фенил-3/метоксипропеноата (соединение №13 в таблице II). 4-метилфенол (8,40 г) добавляют к перемешиваемому метанольному раствору метилата натрия (из натрия (1,78 г) и сухого метанола (50 мл). Спустя 0,5 часа метанол удаляют при пониженном давлении и смесь перемешивают с 4-метилфенолом (4,20 г) 2-хлор-ацетофенолом (6,00 г) и каталитическим количеством медной бронзы. Подученную смесь нагревают при 135°С в течение 1,5 часов, затем оставляют охлаждаться, разбавляют водой и экстрагируют эфиром. Экстракты последовательно промывают водной гидроокисью натрия и водным
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of acryl acid as fungicides, insecticides or plants growth regulators
Автори англійськоюAnthony Vivien Margaret, Beautyment Kevin, Bushell Michael John, KLAF John Martin, de Fren Paul, Godfrey Christopher Richard Ales
Назва патенту російськоюПроизводные акриловой кислоты в качестве фунгицидов, инсектицидов или регуляторов роста растений
Автори російськоюЭнтони Вивьен Маргарет, Бьютимент Кевин, Бушелл Майкл Джон, КЛАФ Джон Мартин, де Френ Поль, Годфри Кристофер Ричард Эйлс
МПК / Мітки
МПК: C07C 69/738, C07C 67/31, A01N 43/40, C07C 201/00, C07C 317/46, A01N 43/12, C07C 315/00, C07C 69/76, C07C 237/20, C07C 69/73, C07C 227/00, C07C 229/40, C07C 235/42, A01N 43/06, A01N 43/08, A01N 37/48, C07C 235/46, C07C 255/57, C07C 231/00, C07C 323/56, C07C 69/736, C07C 67/00, A01N 41/10, C07D 307/68, C07C 323/62, C07D 213/643, C07C 241/00, C07C 229/44, C07D 307/54, A01N 37/36, C07C 245/00, C07C 237/30, C07C 205/00, C07C 313/00, C07C 69/00, C07C 69/734, C07C 69/773, C07C 317/44, A01N 37/46, C07C 69/84, A01N 43/30, A01N 37/42, A01N 37/44, C07D 333/24
Мітки: рослин, росту, похідні, регулятори, кислоти, акрилової, інсектициди, фунгіциди
Код посилання
<a href="https://ua.patents.su/39-40565-pokhidni-akrilovo-kisloti-yak-fungicidi-insekticidi-abo-regulyatori-rostu-roslin.html" target="_blank" rel="follow" title="База патентів України">Похідні акрилової кислоти як фунгіциди, інсектициди або регулятори росту рослин</a>
Попередній патент: Система управління роликом для безступеневої передачі та безступенева передача
Наступний патент: Спосіб зварювання встик двох деталей
Випадковий патент: Автоматична інерційно-фрикційна муфта зчеплення двопотокова міф-1дп