Застосування n-(2-(морфолін-4-іл)пропіл)-2-нафталімідоацетаміду як інтерфероніндукуючого противірусного агента
Номер патенту: 87255
Опубліковано: 25.06.2009
Автори: Ляхов Сергій Анатолійович, Жолобак Надія Михайлівна, Олевінська Зоя Мечиславівна, Доровських Ірина Вікторівна, Карпенко Олександр Сергійович, Співак Микола Якович, Андронаті Сергій Андрійович
Формула / Реферат
Застосування N-(2-(морфолін-4-іл)пропіл)-2-нафталімідоацетаміду
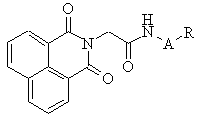 ,
,
де :
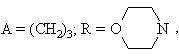
як інтерфероніндукуючого противірусного агента.
Текст
Застосування N-(2-(морфолін-4-іл)пропіл)-2нафталімідоацетаміду O H R N N A O O Винахід відноситься до вірусології, зокрема до стимулювання противірусного захисту, і може бути використаний для створення нових противірусних та імунокорегуючих засобів. Різноманітність інфекційних хвороб, порушень імунного статусу та онкологічних захворювань роблять пошук ефективних та безпечних імунокоректорів вкрай актуальним. До найбільш ефективних імунокоректорів відносяться індуктори інтерферону (ІФН) [Ершов Ф.И., Новохатский А.С. Индукторы интерферона. - М: Медицина, 1982, 180с.]. Незважаючи на наявність деяких клінічних індукторів (аміксин, циклоферон) цю проблему ще не можна вважати вирішеною. Найближчим аналогом винаходу, що заявляється, виходячи з біологічної активності та структури, є аміноалкілнафталіміди 1-9, які проявляють виражену інтерфероніндукуючу та противірусну активність [Карпенко О.С, Доровских І.В., Ляхов С.А., Андронаті С.А., Співак Н.Я., Жолобак Н.М., Олевінська З.М. Похідні аміноалкілнафталімідів як інтеркалюючі у ДНК індуктори інтерферону та противірусні агенти. Деклараційний патент України на корисну модель №17734, МПК C07D 213/00, С07С 209/00. Опубл. 16.10.2006. Бюл. №10], яка пов'я зана із здатністю цих сполук до інтеркаляції у ДНК, загальної формули: , де : N, A = (CH2)3; R = O (13) C2 як інтерфероніндукуючого противірусного агента. 87255 R2 O R1 N n (11) O де: N (1); H3C O N (2); N NH (3); N (4); HO H (19) n=1; R2= UA H3C R1=H; 3 87255 4 O H3C N R1=H; n=2; R2= (5); H N N H3C O O H N R O (6); N H3C A де : CH3 (7); N CH3 A=(CH2)3; R= O (8); H3C N R1=CH3; n=3; R2= N як інтерфероніндукуючий противірусний агент. Причинно-наслідковий взаємозв'язок між структурою об'єктів, що заявляються, і їхньою біологічною дією полягає, очевидно, у здатності наявного в їх структурі амідного зв'язку до гідролізу у фізіологічних умовах і, як наслідок, скорочення часу дії протонованого ліганду ДНК у клітині, при збереженні нафталімідного фрагменту, який забезпечує інтеркаляцію в ДНК, противірусну та інтерфероніндукуючу активності. Сполуку одержували конденсацією хлороангідриду нафталімідооцтової кислоти з морфолінопропіламіном, яку здійснювали змішуванням еквімольної кількості відповідного аміну із розчином хлорангідриду у безводному 1,4-діоксані з наступним виділенням та очисткою цільового продукту. Чистота цільової сполуки 10 підтверджена тонкошаровою хроматографією, будова - даними мас-спектрометрії та спектроскопії 1Н-ЯМР. (9). H3C Але ці сполуки характеризуються помітною цитотоксичністю. В основу винаходу поставлено задачу пошуку похідного нафталімідооцтової кислоти - N-(2(морфолін-4-іл)пропіл)-2-нафталімідоацетаміду як інтерфероніндукуючого противірусного агенту, в якого за рахунок модифікації структури бокового ланцюга забезпечується зниження цитотоксичності. Поставлена задача вирішена застосуванням N-(2-(морфолін-4-іл)пропіл)-2нафталімідоацетаміду наступної формули: R O Cl OH O O 11 O O N HN O O 12 Дослідження препарату проводили за схемою і за умов, що враховували адекватність тест-моделі можливому механізму інтерфероногенної активності, що передбачався на підставі аналізу структури хімічної сполуки, яка вивчалась [Вильнер Л.М. Актуальные вопросы скрининга и последующего изучения противовирусных препаратов типа интерфероногенов / В сб.: Методические вопросы научной разработки противовирусных средств. – Минск, 1977. – С. 134-136]. Цитотоксичність та інтерфероніндукуючу активність синтезованої сполуки вивчали як описано [Доклінічні дослідження лікарських засобів. Методичні рекомендації./ За ред. чл.-кор. АМН України О.В. Стефанова. - К: МОЗ, України. ДФЦ, 2001. - 392с.]. Отримання сполуки, що заявляється, підтверджено прикладами. Приклад 1. Отримання N-(2-(морфолін-4іл)пропіл)-2-нафталімідоацетаміду (10). Синтез проводили як описано у прикладі 3, виходячи із 2.73г (0.01 моль) хлороангідриду нафта O N 13 O H2N A 18-22 A O R O N O 10 лімідооцтової кислоти і 1.44г (0.01 моль) 3(морфолін-4-іл)пропіламіну. Вихід: 1.75г (46%). C21H23N3O4. M.W. 381.44. Мас-спектр (БША), m/z (%): 382 (100) [М+Н]+. Т пл. = 208-209°С. Приклад 2. Вивчення афінітету до ДНК. Приготування вихідних концентрованих розчинів Розчиняли 70мг ДНК у 100см3 води (одержали розчин "a"). 545мг NaCl розчиняли у 100см3 води (одержали розчин "b"). 36мг ЕДТА розчиняли у 100см3 води (одержали розчин "d"). 52.2мг етидію броміду розчиняли у 100см3 води; одержали розчин з концентрацією 1,324´10-3М (розчин "e"). Приготування концентрованого буферного розчину (розчин "c") Розчиняли у склянці на 50см3 164мг безводного ацетату натрію в 20см3 води і додавали по краплях розведену водою (1:3) оцтову кислоту до рН=5 (контролювали рН за допомогою повіреного й відкалибованого рН-метру). Вміст склянки кількі 5 сно перенесли у мірну колбу на 100см3 і додали воду до мітки. Приготування контрольного розчину для "гасіння" Внесли у мірну колбу на 50см3 4см3 розчину a, 3 5см розчину b, 5см3 розчину c, 5см розчину d і 0,151 (0,150-0,152)см3 розчину e. Додали воду до мітки (одержали розчин А). Приготування контрольного розчину для "витиснення" Внесли у мірну колбу на 50см3 0,1см3 розчину a, 5см3 розчину b, 5см3 розчину c, 5см3 розчину d і 0,096 (0,09-0,100)см3 розчину e. Додали воду до мітки (одержали розчин В). Приготування буфера розведення Внесли у мірну колбу на 50см3 10см3 розчину b, 10см3 розчину c, 10см3 розчину d. Додали воду до мітки (одержали розчин С). Приготування концентрованого розчину ліганду Розрахункову кількість ліганду розчиняли у 100см дистильованої води, прагнучи одержати розчин з концентрацією у 20-30 разів більшою, ніж очікуване значення С50 (одержали розчин D). Приготування вихідних розчину ліганду Додали у 8 мірних колб на 25см3 0,5, 0,9, 1,3, 2,5, 4,0, 7,5, 10,0, 15,0,см3 розчину D. Додали воду до мітки (одержали розчини Е1-Е8). Як розчин Е9 використовували розчин D. Приготування робочих розчинів ліганду У 9 пробірках змішували по 1см3 розчинів Е1Е9 з 1см3 розчину С (одержали розчини F1-F9). Приготування розчинів ліганду для вивчення гасіння У 9 пробірок, що містять по 2см3 розчинів F1F9 додавали по 2см розчину А (для вивчення гасіння), одержують розчини G1-G9 (одержали розчини G1-G9). Додатково готували розчин G10 змішуючи 2см3 розчину А, 1см3 води і 1см3 розчину С. Приготування розчинів ліганду для вивчення витиснення У 9 пробірок, що містять по 2см3 розчинів F1F9 додавали по 2см розчину В (для вивчення витиснення), одержують розчини Н1-Н9. Додатково готували розчин Н10 змішуючи 2см3 розчину В, 1см води і 1см розчину С. Проведення вимірів У кювету спектрофлуориметру додали 2,5см3 досліджуваного розчину, кювету установили у кюветоутримувач і записували спектр флуоресценції в інтервалі довжин хвиль 520-630нм. Виділяли пік, що відповідає етідію броміду (lmах=595±2нм) і з'єднували мінімуми прямою (базис). З вершини піка опускали перпендикуляр, відзначали точку його перетинання з базисом і вимірювали довжину отриманого відрізку. Процедуру повторювали для розчинів G1-G10 i H1-H10. Інтенсивність флуоресценції розчинів G1-G9 і Н1-Н9 виражали у відсотках щодо інтенсивності флуоресценції розчинів G10 і Н10 відповідно. Відсоток витиснення етидію броміду з комплексу визначали за формулою: D%=І%G-I%H На графіку відкладали величини D%, І%G i I%H як функції від концентрації. Проводили пряму 87255 6 D%=50% і з точки її перетину з графіком D%=F(З) опускали перпендикуляр. Отримане значення концентрації приймали за C50. Якщо величина I%н не перевищує 5-10%, то будували залежність І%G від lgCL. Отримані значення апроксимували сигмоїдою. Точку, що відповідає lgCL визначали як точку перегину, а її довірчий інтервал - як ширину коридору помилок при 50% витисненні. Логарифм константи асоціації ліганду з ДНК визначали за формулою: lgKa=lgCE-lgC50+7 Приклад 3. Визначення цитотоксичності препарату в умовах in vitro клітин за дією на моношар клітин та пригніченням їх життєздатності. Перещеплювану культуру клітин фібробластів свиней - перевивних тестикул поросяти (ПТП) вирощували у 96-лункових мікроплатах (в атмосфері, що містить 5% СО2). Через 24 год з лунок, де сформувався суцільний моношар клітин видаляли середовище росту і вносили підтримуюче середовище та розчинені препарати в діапазоні концентрацій від 5 до 500мкг/см3 (на одне розведення не менше 4 лунок). Контроль - лунки, в які було внесене тільки середовище для підтримання росту. Плати поміщали в термостат. Через 24 та 48 год після інкубації плат при 36°С в умовах 5% СО2 клітини проглядали за допомогою інвертованого мікроскопу при малому збільшенні з метою виявлення цитопатичної дії (ЦПД) препаратів, яку оцінювали за порушенням цілісності моношару, появою осередків дегенерованих клітин та визначали за чотириплюсовою системою. Визначали: ТЦД100 - тканинну цитотоксичну дозу (мкг/см3), що викликає повну деструкцію клітин, ТЦД50 - тканинну цитотоксичну дозу (мкг/см3), що викликає зміну 50% моношару клітин; МВК - максимально витримувану концентрацію - максимальну із досліджених доз речовини (мкг/см3), що не викликає незворотніх змін у морфології та життєздатності клітин у порівнянні з контролем (фактично вона відповідає ТЦД0). Розрахунок ТЦД50 проводили за методом Ріда і Менча за формулами: log2ТЦД50=log2A-(50-b)×log2d/(а-b) чи log2ТЦД30 =log2В+(а-50)×log2d/(а-b), де log2А і log2В - логарифми концентрацій за основою 2, що викликали ефекти відповідно більше чи менше 50%, але найближчі до 50%: а і b – ефект, викликаний концентраціями А і В, %: log2d логарифм за основою 2 співвідношення між досліджуваними концентраціями. Другим параметром, за яким оцінювали токсичність доз препарату було пригнічення їх життєздатності. [Методы испытания и оценки противовирусной активности химических соединений в отношении вируса гриппа. Методические указания. Сост. проф. В.И. Ильенко. - Л. - 1977. - 35с]. Підрахунок клітин та визначення їх життєздатності через 24 та 48 годин інкубації проводили після фарбування клітин водним розчином вітального фарбника трипанового синього. При відсутності токсичного ефекту клітини засвоювали вітальний барвник. Забарвлення контрольних культур приймали за 100%. Розведення препарату, що викли 7 87255 кало засвоєння фарбника на 50% вважали токсичним. Приклад 4. Вивчення інтерфероніндукуючих властивостей. Інтерфероніндукуючу активність синтезованої сполуки вивчали як описано [Доклінічні дослідження лікарських засобів. Методичні рекомендації. За редакцією член-кореспондента АМН України О.В. Стефанова. / Міністерство охорони здоров'я України. Державний фармакологічний центр., Київ, 2001. С. 392]. Інтерфероніндукуючу активність препарату в умовах in vitro вивчали в культурі клітин ПТП. Препарати в різних дозах (30-250мкг/см3) додавали до сформованого моношару клітин і культивували при 37°С на протязі 24 та 48 год, після чого надосадову рідину збирали і в ній визначали активність інтерферону за раніше опублікованою методикою. [Доклінічні дослідження лікарських засобів. Методичні рекомендації. За редакцією членкореспондента АМН України О.В. Стефанова. / Міністерство охорони здоров'я України. Державний фармакологічний центр., Київ, 2001. С. 392] (пригнічення цитопатогенної дії вірусу везикулярного стоматиту). 8 Визначення активності інтерферону здійснювали через 24-48год, коли доза внесеного вірусу везикулярного стоматиту (ВВС) 100 ТЦД50 викликає повну дегенерацію клітин у контролі вірусу (KB) за відсутністю дегенерації у неінфікованій культурі. За титр інтерферону в одиницях дії (ОД) приймали величину, зворотну розведенню препарату, при якому культура клітин в 50% лунок була повністю захищена від цитопатогенної дії індикаторного вірусу. Титр індукованого інтерферону (максимальне розведення супернатанту, при якому в 50% лунок цілком запобігалася дегенерація клітинного моношару) визначали в трьох паралельних експериментах. Виявлено, що в умовах in vitro досліджена речовина спричиняє утворення інтерферону (дані діапазон значень, що отримані у трьох паралельних експериментах - наведені в таблиці). Дані про цитотоксичність та інтерфероніндукуючу активність сполук 10-14 та сполук порівняння 1-9 наведені в таблиці. Таблиця Інтеркалююча здатність, цитотоксичність та інтерфероніндукуюча активність сполук, що заявляються Сполука lgKa токсичність, lgLC50 1 2 3 4 5 6 8 9 10 6,99 5,38 5,29 5,57 6,56 6,93 5,57 5,50 5,46 4,42 3,54 3,89 4,40 4,44 3,87 4,38 3,58 3,63 Противірусна активність, % живих клітин 30,5 72,2 44,4 16,6 16,6 30,5 2,8 100 100 Як видно з наведених даних, сполука, що заявляється, є інтеркалятором помірної сили та індуктором інтерферону, причому за своєю активністю Комп’ютерна верстка М. Ломалова Інтерфероніндукуюча активність (X Iog2) L929 ПТП (2.5 mМ) (11 mМ) (2.5 mМ) (11 mМ) 3 5 1 1 2,4 4,5 0,5 5 7 2 4 4,5 7 2 2 4 6 3 4 4,5 7 3,5 4 4 6,5 2 3 5 7 0 0 5 6 0 0 перевершує сполуки порівняння. Водночас, цитотоксична концентрація її дещо вища за ЦТК сполук порівняння. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of n-(2-(morpholine-4-yl)propyl)-2-naphthalimidoacetamide as interferone-inducing antiviral agent
Автори англійськоюKarpenko Oleksandr Serhiiovych, Dorovskykh Iryna Viktorivna, Liakhov Serhii Anatoliiovych, Andronati Serhii Andriiovych, Spivak Mykola Yakovych, Zholobak Nadia Mykhailivna, Olevinska Zoia Mechyslavivna
Назва патенту російськоюПрименение n-(2-(морфолин-4-ил)пропил)-2-нафталимидоацетамида в качестве интерферониндуцирующего противовирусного агента
Автори російськоюКарпенко Александр Сергеевич, Доровских Ирина Викторовна, Ляхов Сергей Анатольевич, Андронати Сергей Андреевич, Спивак Николай Яковлеич, Жолобак Надежда Михайловна, Олевинская Зоя Мечиславивна
МПК / Мітки
МПК: A61P 31/12, C07D 413/12
Мітки: застосування, інтерфероніндукуючого, агента, противірусного, n-(2-(морфолін-4-іл)пропіл)-2-нафталімідоацетаміду
Код посилання
<a href="https://ua.patents.su/4-87255-zastosuvannya-n-2-morfolin-4-ilpropil-2-naftalimidoacetamidu-yak-interferonindukuyuchogo-protivirusnogo-agenta.html" target="_blank" rel="follow" title="База патентів України">Застосування n-(2-(морфолін-4-іл)пропіл)-2-нафталімідоацетаміду як інтерфероніндукуючого противірусного агента</a>
Наступний патент: Спосіб знезараження води господарсько-питного призначення
Випадковий патент: Харчова композиція








