Інсектицидні феніл- або піридилпіперидини
Номер патенту: 101046
Опубліковано: 25.02.2013
Автори: Піттерна Томас, Корсі Камілла, Кассер Жером Ів, Майєнфіш Петер
Формула / Реферат
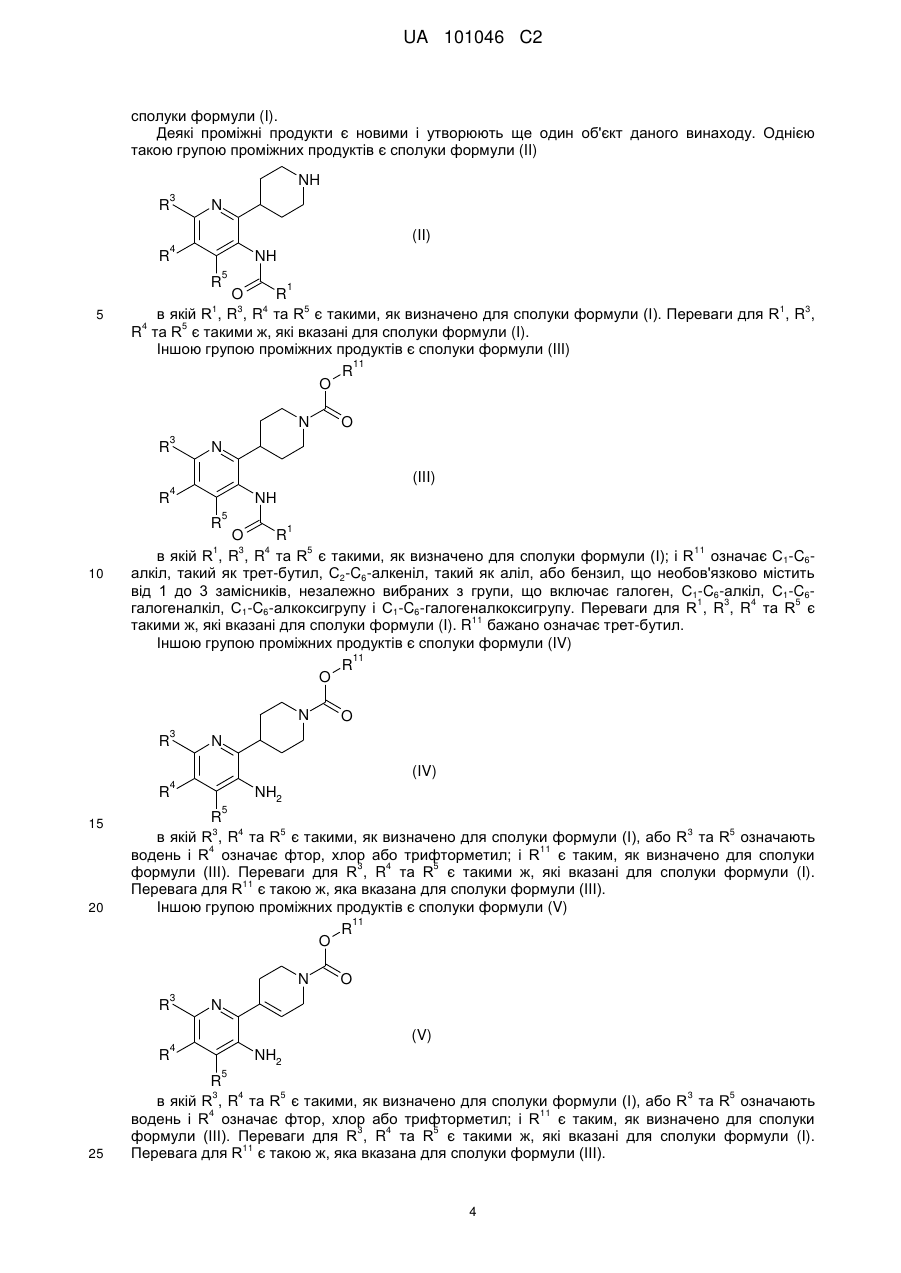
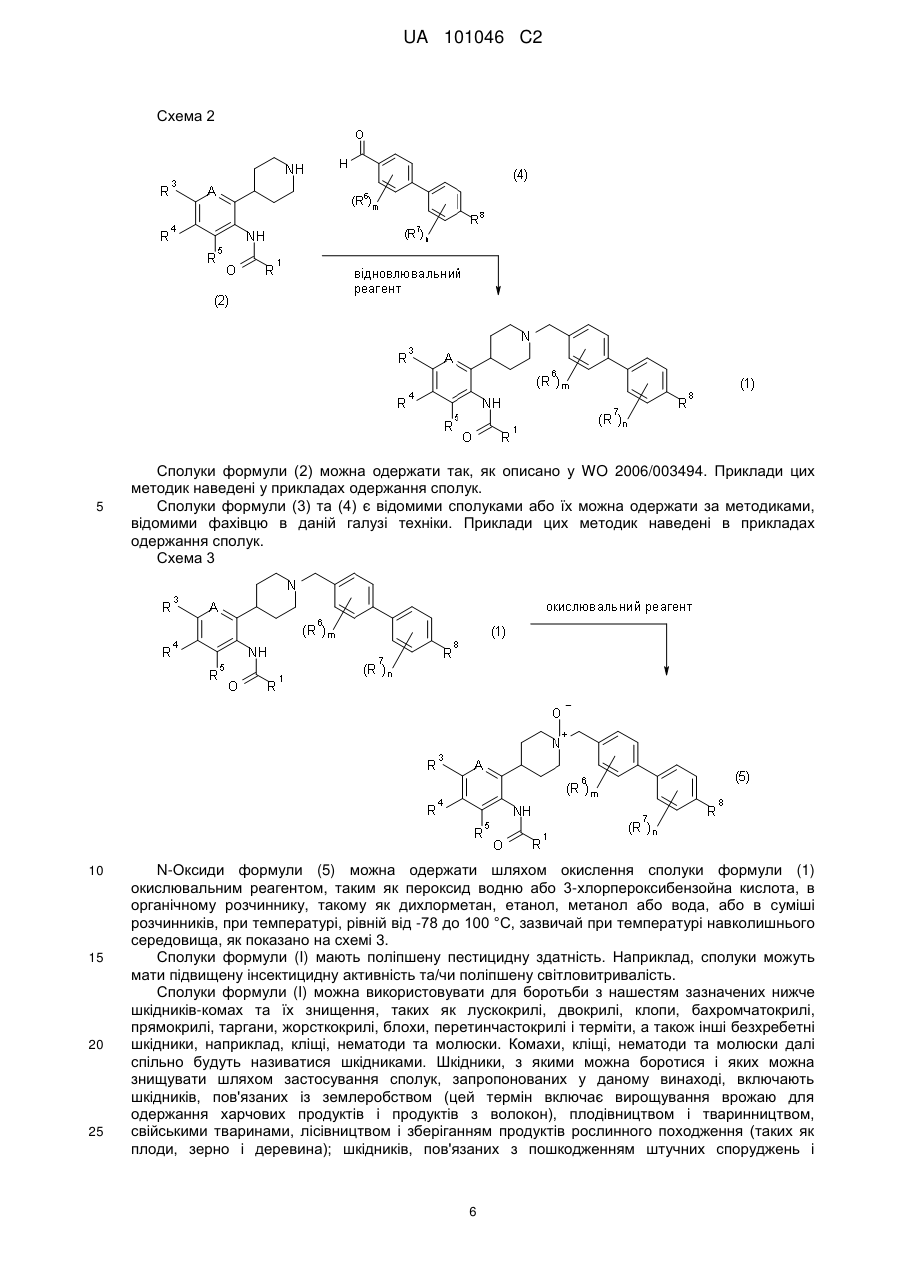
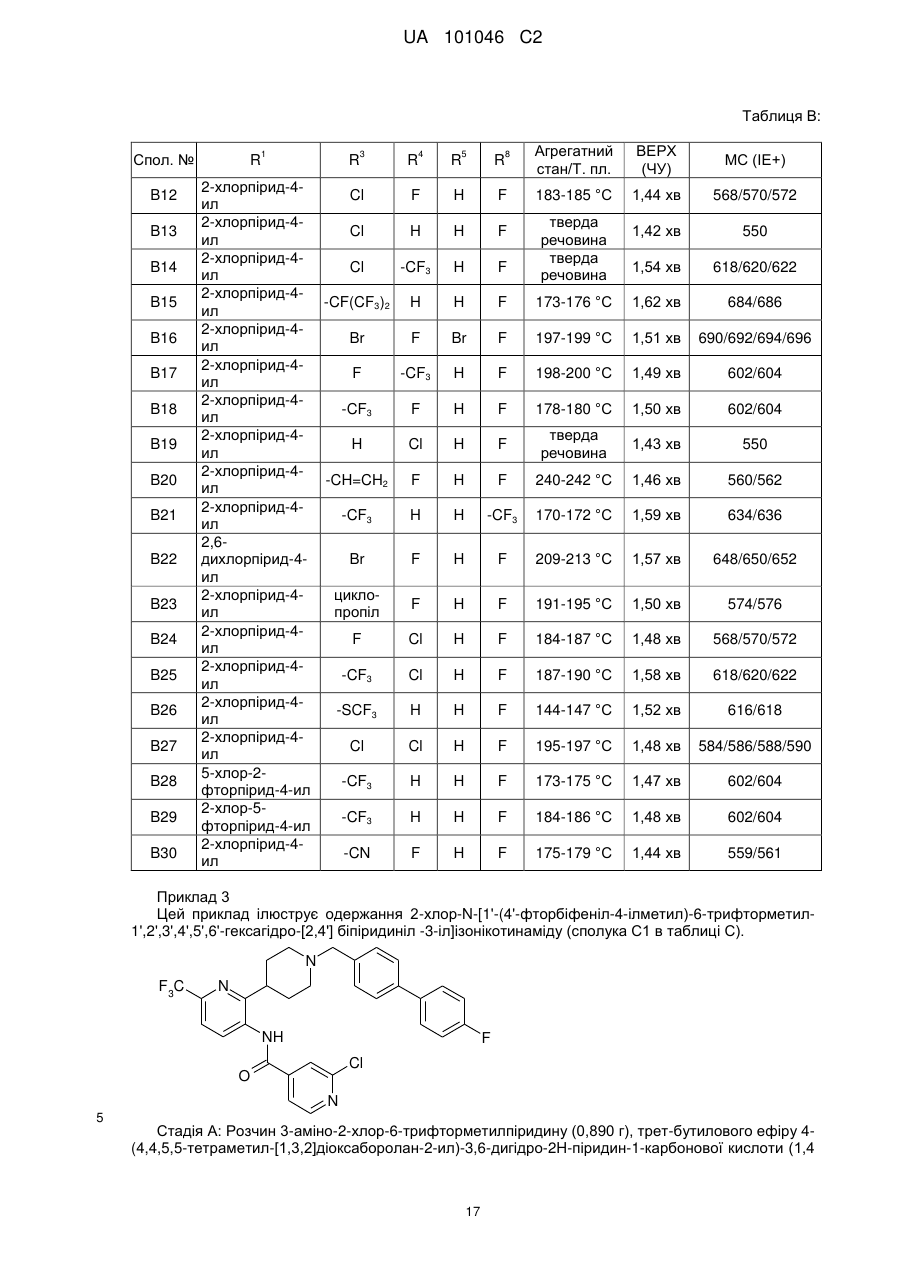
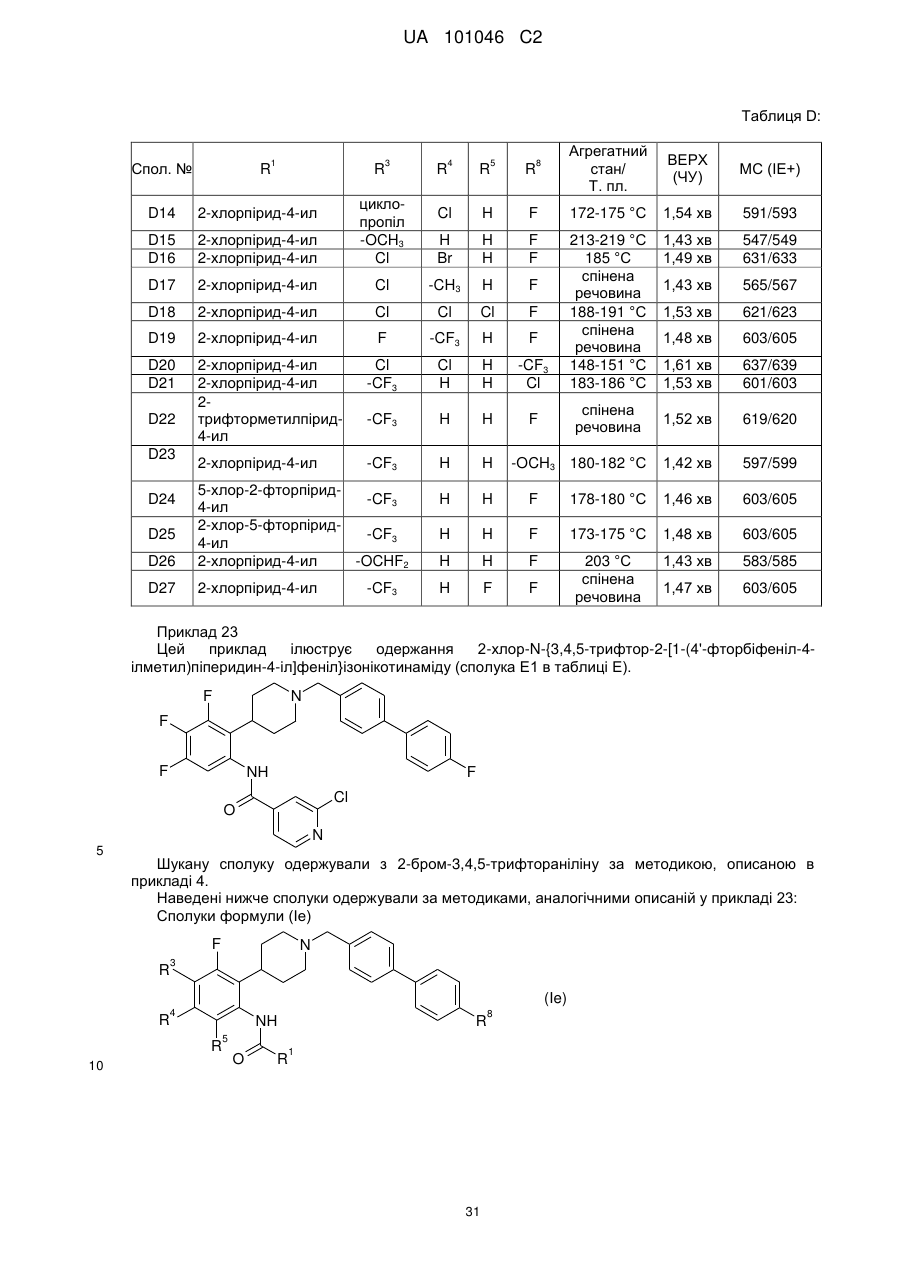
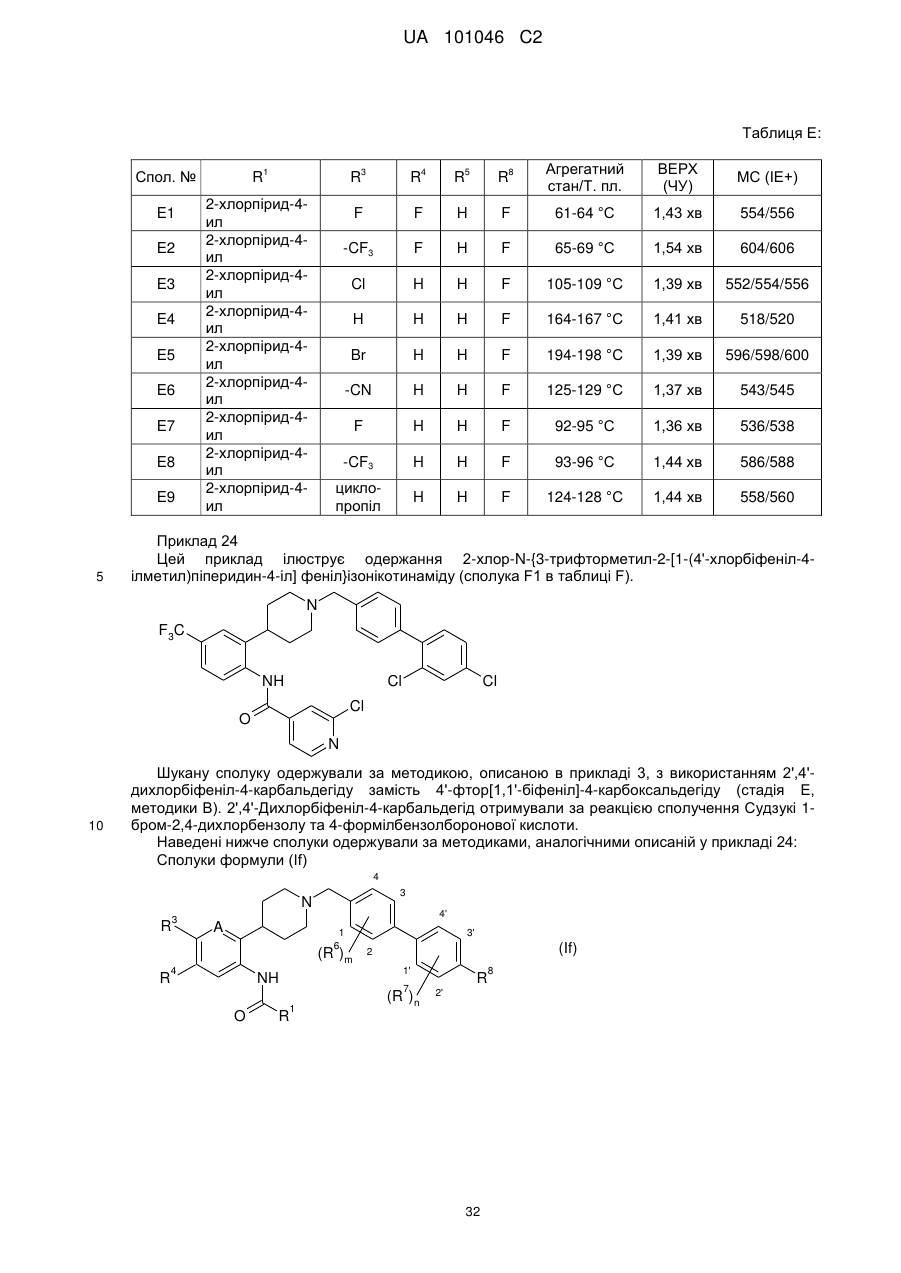
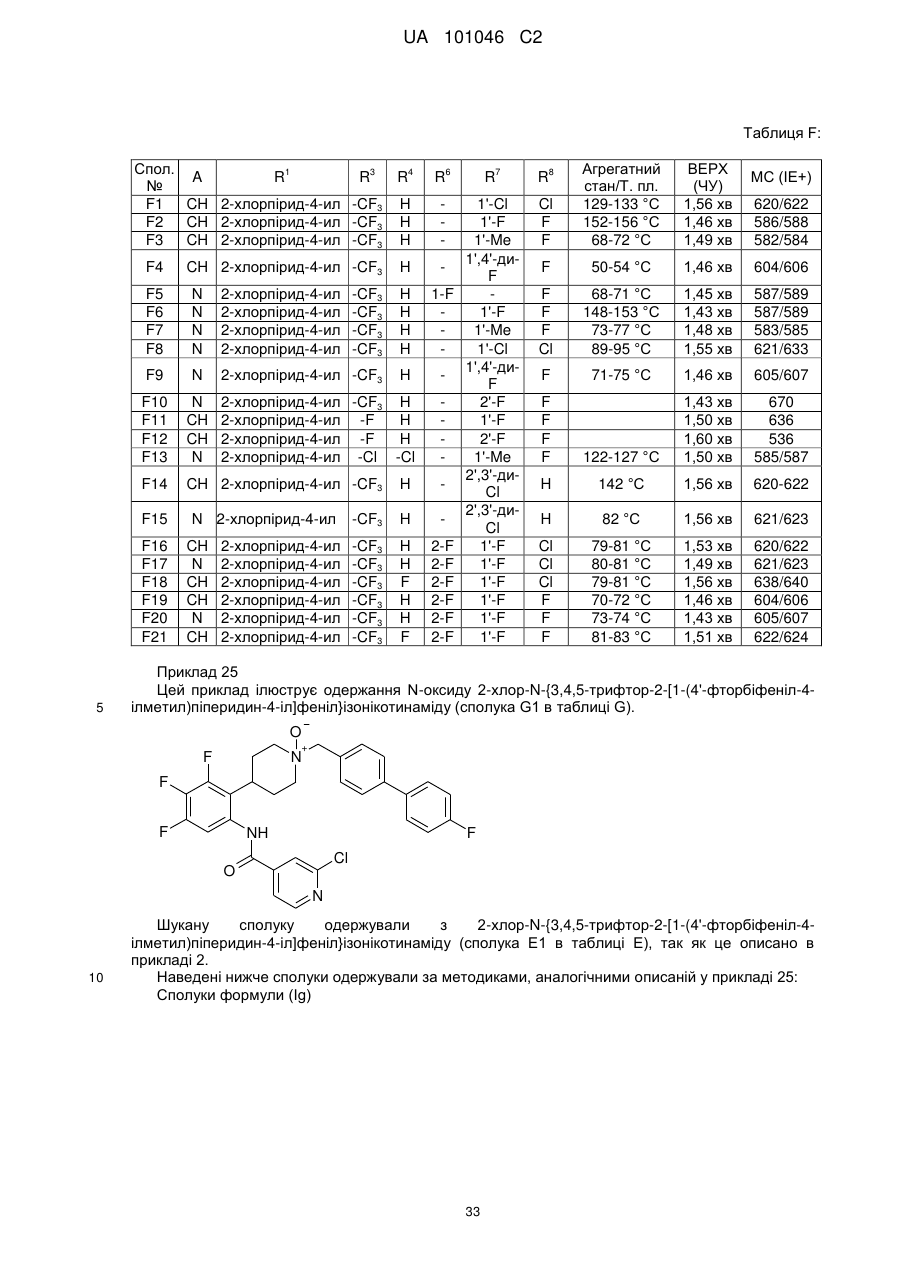
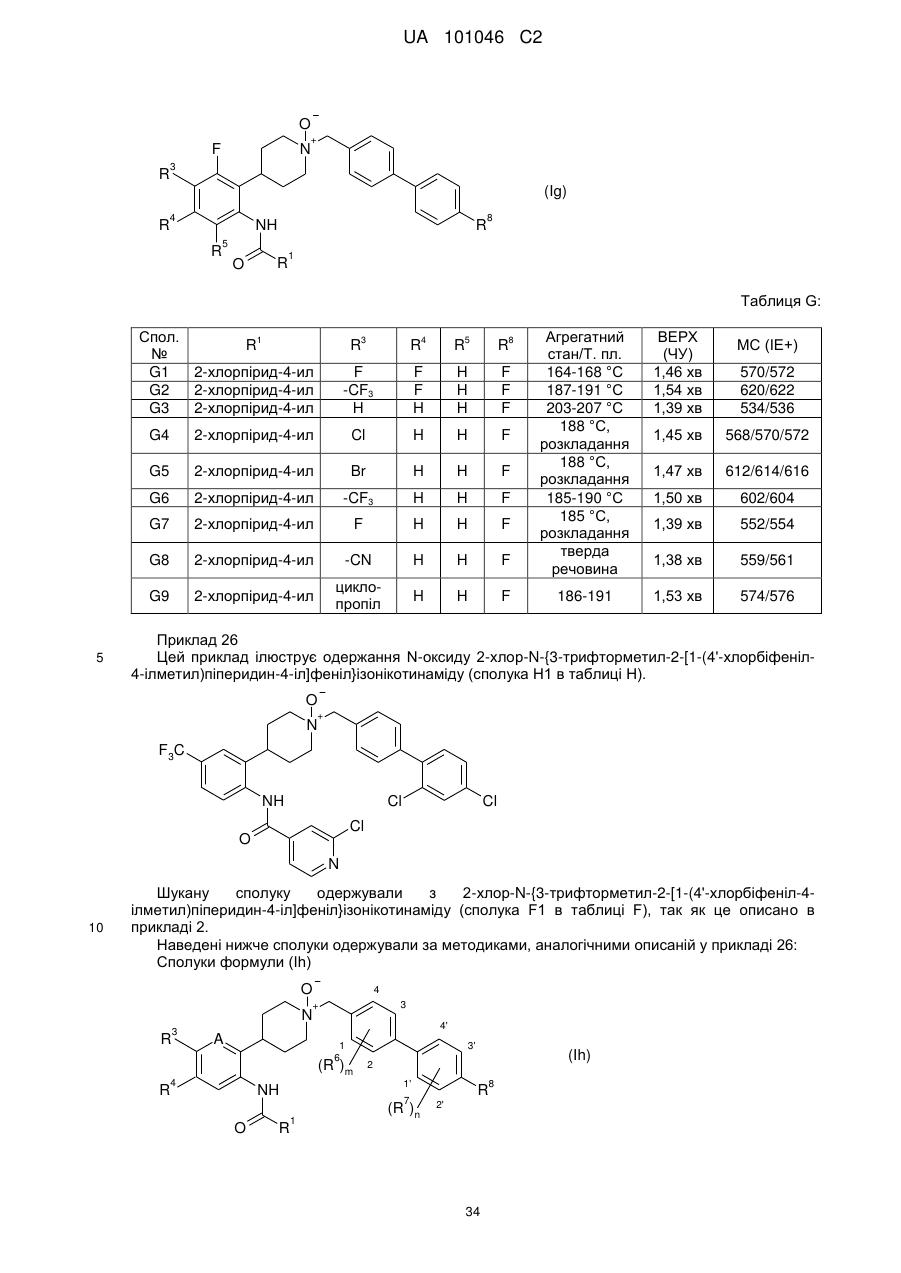
1. Сполука формули (І):
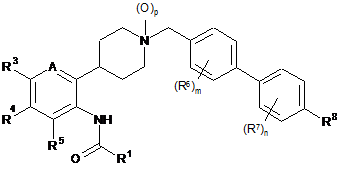 , (I)
, (I)
в якій
А означає CR2 або N;
р дорівнює 0 або 1;
R1 означає пірид-4-ил, що необов'язково містить 1 або 2 замісники, кожен з яких незалежно вибраний з галогену, С1-С3-алкілу або С1-С3-галогеналкілу;
R2 означає водень, галоген, С1-С3-галогеналкіл або С1-С3-галогеналкоксигрупу;
R3 та R4 незалежно означають водень, галоген, ціаногрупу, C1-C8-алкіл, C1-C8-галогеналкіл, C2-C8-алкеніл, C2-C8-галогеналкеніл, C3-C8-циклоалкіл, C3-C8-галогенциклоалкіл, C1-C8-алкоксигрупу, C1-C8-галогеналкоксигрупу, C1-C8-алкілтіогрупу або C1-C8-галогеналкілтіогрупу;
R5 означає водень або галоген;
кожен R6 та R7 незалежно означає галоген, C1-C8-алкіл, C1-C8-галогеналкіл, C1-C8-алкоксигрупу або C1-C8-галогеналкоксигрупу;
m дорівнює 0, 1 або 2;
n дорівнює 0, 1 або 2; і
R8 означає водень, галоген, ціаногрупу, C1-C8-алкіл, C1-C8-галогеналкіл, C3-C8-циклоалкіл, C2-C8-алкеніл, C2-C8-галогеналкеніл, C2-C8-aлкiнiл, C1-C8-алкоксигрупу або C1-C8-галогеналкоксигрупу; або її сіль.
2. Сполука за п. 1, в якій R1 означає пірид-4-ил, що необов'язково містить 1 або 2 замісники, кожен з яких незалежно вибраний з фтору, хлору, брому, метилу, дифторметилу, хлордифторметилу або трифторметилу.
3. Сполука за п. 1 або 2, в якій R3 означає водень, галоген, ціаногрупу, C1-С6-алкіл, C1-С6-галогеналкіл, C2-С6-алкеніл, C3-С6-циклоалкіл, C1-С6-алкоксигрупу, C1-С6-галогеналкоксигрупу, C1-С6-алкілтіогрупу або C1-С6-галогеналкілтіогрупу.
4. Сполука за будь-яким з попередніх пунктів, в якій R4 означає водень, галоген, ціаногрупу, C1-С6-алкіл, C1-С6-галогеналкіл, C2-С6-алкеніл, C3-С6-циклоалкіл, C1-С6-алкоксигрупу, C1-С6-галогеналкоксигрупу, C1-С6-алкілтіогрупу або C1-С6-галогеналкілтіогрупу.
5. Сполука за будь-яким з попередніх пунктів, в якій R5 означає водень, фтор, хлор або бром.
6. Сполука за будь-яким з попередніх пунктів, в якій кожен R6 незалежно означає галоген, C1-С6-алкіл або C1-С6-алкоксигрупу.
7. Сполука за будь-яким з попередніх пунктів, в якій m дорівнює 0 або 1.
8. Сполука за будь-яким з попередніх пунктів, в якій кожен R7 незалежно означає галоген, C1-С6-алкіл або C1-С6-алкоксигрупу.
9. Сполука за будь-яким з попередніх пунктів, в якій n дорівнює 0 або 1.
10. Сполука за будь-яким з попередніх пунктів, в якій R8 означає водень, галоген, ціаногрупу, C1-С6-алкіл, C1-С6-галогеналкіл, C3-С6-циклоалкіл, C2-С6-алкеніл, C2-С6-галогеналкеніл, C2-С6-алкініл, C1-С6-алкоксигрупу або C1-С6-галогеналкоксигрупу.
11. Спосіб боротьби з комахами, кліщами, молюсками або нематодами та їх знищення, який включає нанесення на шкідників, на осередок шкідників або на рослини, піддані нашестю шкідників, сполуки формули (І) за будь-яким з пп. 1-10 в інсектицидно, акарицидно, молюскоцидно або нематоцидно ефективній кількості.
12. Інсектицидна, акарицидна, молюскоцидна або нематоцидна композиція, що містить сполуку формули (І) за будь-яким з п. 1-10 в інсектицидно, акарицидно, молюскоцидно або нематоцидно ефективній кількості.
Текст
Реферат: 1 3 4 5 6 7 8 Сполука формули (І), в якій А, р, R , R , R , R , R , m, R , n та R є такими, як визначено в пункті 1 формули винаходу, композиція на її основі та спосіб боротьби з комахами, кліщами, молюсками і нематодами та їх знищення. (O)p N R 3 A (R6)m 4 R NH R (R7)n 5 O R R 8 1 (I) UA 101046 C2 (12) UA 101046 C2 UA 101046 C2 5 Даний винахід належить до деяких похідних піперидину, до проміжних продуктів, що застосовуються для їх одержання, до способів їх застосування для боротьби з комахами-, кліщами-, нематодами- і молюсками-шкідниками та їх знищення і до інсектицидних, акаріцидних, нематоцидних та молюскоцидних композицій, які їх містять. Похідні піперидину, що мають інсектицидну властивість, розкриті, наприклад у WO 2006/003494. Згідно винаходу неочікувано було встановлено, що деякі похідні піперидину мають покращені інсектицидні властивості. Тому даний винахід належить до сполуки формули (I): ( O )p N 3 R A (I) 6 (R )m 4 R 8 NH 7 5 R 10 15 20 25 30 35 40 45 50 O 1 R (R )n R в якій 2 A означає CR або N; p дорівнює 0 або 1; 1 R означає пірид-4-ил, що необов'язково містить 1 або 2 замісника, кожен з яких незалежно вибраний з галогену, C1-C3-алкілу або C1-C3-галогеналкілу; 2 R означає водень, галоген, C1-C3-галогеналкіл або C1-C3-галогеналкоксигрупу; 3 4 R та R незалежно означають водень, галоген, ціаногрупу, C 1-C8-алкіл, C1-C8-галогеналкіл, C2-C8-алкеніл, C2-C8-галогеналкеніл, C3-C8-циклоалкіл, C3-C8-галогенциклоалкіл, C1-C8алкоксигрупу, C1-C8-галогеналкоксигрупу, C1-C8-алкілтіогрупу або C1-C8-галогеналкілтіогрупу; 5 R означає водень або галоген; 6 7 кожен R та R незалежно означає галоген, C1-C8-алкіл, C1-C8-галогеналкіл, C1-C8алкоксигрупу або C1-C8-галогеналкоксигрупу; m дорівнює 0, 1 або 2; n дорівнює 0, 1 або 2; і 8 R означає водень, галоген, ціаногрупу, C1-C8-алкіл, C1-C8-галогеналкіл, C3-C8-циклоалкіл, C2-C8-алкеніл, C2-C8-галогеналкеніл, C2-C8-алкініл, C1-C8-алкоксигрупу або C1-C8галогеналкоксигрупу; або до її солі. Сполуки формули (I) можуть існувати в різних геометричних ізомерних або оптичних ізомерних або таутомерних формах. В обсяг даного винаходу входять усі такі ізомери і таутомери та їх суміші у всіх співвідношеннях, а також ізотопозаміщені форми, такі як дейтеровані сполуки. Кожен алкільний фрагмент, окремо або у вигляді частини більшої групи (такої як алкоксигрупа або алкілтіогрупа) має лінійний або розгалужений ланцюг і означає, наприклад метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил, ізобутил або трет-бутил. Алкільні групи бажано являють собою C1-C6-алкільні групи, більш бажано C1-C4-алкільні групи и найбільш бажано C1-C3-алкільні групи. Алкенільні та алкінільні фрагменти можуть перебувати у вигляді лінійних або розгалужених ланцюгів і алкенільні фрагменти, якщо це підходить, можуть перебувати в (E) або (Z)конфігурації. Прикладами є вініл, аліл і пропаргіл. Алкенільні та алкінільні групи бажано являють собою C2-C6-алкенільні або -алкінільні групи, більш бажано C2-C4- і найбільш бажано C2-C3алкенільні або -алкінільні групи. Галоген означає фтор, хлор, бром або йод. Галогеналкільні групи (окремо або у вигляді частини більш великої групи, такої як галогеналкоксигрупа або галогеналкілтіогрупа) являють собою алкільні групи, які заміщені одним або більшою кількістю однакових або різних атомів галогенів і являють собою, наприклад -CF3, -CF2Cl, -CH2CF3 або -CH2CHF2. Галогеналкільні групи являють собою алкільні групи, які заміщені одним або більшою кількістю однакових або різних атомів галогенів і являють собою, наприклад, CH=CF2 або CCl=CClF. Циклоалкільні групи можуть бути моно- або біциклічними і необов'язково можуть бути заміщені однією або більше метильними групами. Циклоалкільні групи бажано містять від 3 до 8 атомів вуглецю, більш бажано від 3 до 6 атомів вуглецю. Прикладами моноциклічних 1 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 циклоалкільних груп є циклопропіл, 1-метилциклопропіл, 2-метилциклопропіл, циклобутил, циклопентил і циклогексил. Галогенциклоалкільні групи являють собою циклоалкільні групи, які заміщені одним або більшою кількістю однакових або різних атомів галогенів і необов'язково можуть бути заміщені одним або більшою кількістю метильних груп. Прикладами моноциклічних галогенциклоалкільних груп є 2,2-дихлорциклопропіл-, 2,2-дихлор-1-метилциклопропіл і 2-хлор4-фторциклогексил. Солі складаються з зарядженої модифікації сполуки формули (I) і протилежно зарядженого протиіона. Сполуки формули (I) можуть бути позитивно заряджені, наприклад, по атому азоту піперидинового кільця, якщо атом азоту кватернізований шляхом протонування за допомогою органічної або неорганічної кислоти. Підходящі органічні кислоти включають бутилсульфонову кислоту, 2-хлорбензойну кислоту, етилсульфонову кислоту, 3-гідроксипропансульфонову кислоту, 4-метилбензолсульфонову кислоту, метансульфонову кислоту, 3-феноксипропіонову кислоту, тридеканову кислоту і трифтороцтову кислоту. Підходящі неорганічні кислоти включають хлористоводневу кислоту і фосфорну кислоту. N-Оксиди являють собою сполуки формули (I), в якій атом азоту окиснений. Зокрема, Nоксиди являютя собою сполуки формули (I), в якій окиснений атом азоту піперидинового кільця. Окиснювальні реагенти, за допомогою яких сполуку формули (I) можна перетворити в N-оксид формули (I), включають водний розчин пероксиду водню. 1 2 3 4 5 6 7 8 Бажані групи і значення для R , R , R , R , R , R , m, R , n і R в будь-якій їх комбінації є такими, як зазначено нижче. 1 Бажано, якщо R означає пірид-4-ил, що необов'язково містить 1 або 2 замісника, кожен з яких незалежно вибраний з групи, що включає фтор, хлор, бром, метил, дифторметил, 1 хлордифторметил і трифторметил; більш бажано, якщо R означає пірид-4-ил, що необов'язково містить 1 або 2 замісника, кожен з яких незалежно вибраний з групи, що включає 1 фтор, хлор і метил; найбільш бажано, якщо R означає пірид-4-ил, що необов'язково містить 1 або 2 замісника, кожен з яких незалежно вибраний з групи, що включає фтор і хлор. Бажано, щоб один замісник знаходився в положенні 2 пірид-4-илового кільця і другий замісник необов'язково знаходився в положенні 5 або положенні 6 пірид-4-илового кільця. Приклади 1 найбільш бажаних груп R включають 2-фторпірид-4-ил, 2-хлорпірид-4-ил, 2,5-дихлорпірид-4-ил і 2,6-дихлорпірид-4-ил. 2 Бажано, якщо R означає водень або галоген. 2 Більш бажано, якщо R означає водень, фтор або хлор. 2 Ще більш бажано, якщо R означає водень або фтор. 2 Найбільш бажано, якщо R означає водень. 3 Бажано, якщо R означає водень, галоген, ціаногрупу, C1-C6-алкіл, C1-C6-галогеналкіл, C2-C6алкеніл, C3-C6-циклоалкіл, C1-C6-алкоксигрупу, C1-C6-галогеналкоксигрупу, C1-C6-алкілтіогрупу або C1-C6-галогеналкілтіогрупу. 3 Більш бажано, якщо R означає водень, фтор, хлор, бром, ціаногрупу, метил, ізопропіл, фторметил, дифторметил, трифторметил, гептафторізопропіл, вініл, циклопропіл, метоксигрупу, етоксигрупу, дифторметоксигрупу, трифторметоксигрупу, 2,2,2-трифторетоксигрупу або трифторметилтіогрупу. 3 Ще більш бажано, якщо R означає водень, фтор, хлор, бром, дифторметил, трифторметил, гептафторізопропіл, вініл, циклопропіл, метоксигрупу, дифторметоксигрупу, трифторметоксигрупу або 2,2,2-трифторетоксигрупу. 3 Ще більш бажано, якщо R означає водень, фтор, хлор, бром, трифторметил, циклопропіл або трифторметоксигрупу. 3 Найбільш бажано, якщо R означає трифторметил. 4 Бажано, якщо R означає водень, галоген, ціаногрупу, C1-C6-алкіл, C1-C6-галогеналкіл, C2-C6алкеніл, C3-C6-циклоалкіл, C1-C6-алкоксигрупу, C1-C6-галогеналкоксигрупу, C1-C6-алкілтіогрупу або C1-C6-галогеналкілтіогрупу. 4 Більш бажано, якщо R означає водень, фтор, хлор, бром, метил, ізопропіл, фторметил, дифторметил, трифторметил, гептафторізопропіл, вініл, циклопропіл, метоксигрупу, етоксигрупу, дифторметоксигрупу, трифторметоксигрупу або 2,2,2-трифторетоксигрупу. 4 Ще більш бажано, якщо R означає водень, фтор, хлор, метил або трифторметил. 4 Найбільш бажано, якщо R означає водень. 5 Бажано, якщо R означає водень, фтор, хлор або бром. 5 Більш бажано, якщо R означає водень або фтор. 5 Найбільш бажано, якщо R означає водень. 6 Бажано, якщо кожен R незалежно означає галоген, C1-C6-алкіл або C1-C6-алкоксигрупу. 2 UA 101046 C2 6 5 10 15 20 25 30 35 40 45 50 55 60 Більш бажано, якщо кожен R незалежно означає фтор, хлор, метил або метоксигрупу. 6 Найбільш бажано, якщо кожен R незалежно означає фтор або хлор. Бажано, якщо m дорівнює 0 або 1. Найбільш бажано, якщо m дорівнює 0. 7 Бажано, якщо кожен R незалежно означає галоген, C1-C6-алкіл або C1-C6-алкоксигрупу. 7 Більш бажано, якщо кожен R незалежно означає фтор, хлор, метил або метоксигрупу. 7 Найбільш бажано, якщо кожен R незалежно означає фтор або хлор. Бажано, якщо n дорівнює 0 або 1. Найбільш бажано, якщо n дорівнює 0. 8 Бажано, якщо R означає водень, галоген, ціаногрупу, C1-C6-алкіл, C1-C6-галогеналкіл, C3-C6циклоалкіл, C2-C6-алкеніл, C2-C6-галогеналкеніл, C2-C6-алкініл, C1-C6-алкоксигрупу або C1-C6галогеналкоксигрупу. 8 Більш бажано, якщо R означає водень, фтор, хлор, бром, ціаногрупу, метил, трифторметил, циклопропіл, етиніл, метоксигрупу або трифторметоксигрупу. 8 Ще більш бажано, якщо R означає фтор, хлор, бром, трифторметил або трифторметоксигрупу. 8 Ще більш бажано, якщо R означає фтор, хлор або трифторметил. 8 Найбільш бажано, якщо R означає фтор. 1 3 4 5 8 Бажаним варіантом здійснення є сполуки формули (Ia), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), A означає C-H, і m, n та p дорівнюють 0. Переваги для 1 3 4 5 8 R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 4 5 8 Бажаним варіантом здійснення є сполуки формули (Ib), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), A означає C-H, m та n дорівнюють 0, і p дорівнює 1. 1 3 4 5 8 Переваги для R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 4 5 8 Бажаним варіантом здійснення є сполуки формули (Ic), в якій R , R , R , R та R є такими, як 1 3 визначено для сполуки формули (I), A означає N, і m, n та p дорівнюють 0. Переваги для R , R , 4 5 8 R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 4 5 8 Бажаним варіантом здійснення є сполуки формули (Id), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), A означає N, m та n дорівнюють 0, і p дорівнює 1. 1 3 4 5 8 Переваги для R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 4 5 8 Бажаним варіантом здійснення є сполуки формули (Ie), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), A означає C-F, і m, n та p дорівнюють 0. Переваги для 1 3 4 5 8 R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 6 7 8 Бажаним варіантом здійснення є сполуки формули (If), в якій A, R , R , R , m, R , n та R є 4 5 такими, як визначено для сполуки формули (I), R та R означають H, і p дорівнює 0, за умови, 1 3 6 7 8 що щонайменше один з m або n не дорівнює 0. Переваги для R , R , R , m, R , n та R є такими ж, які вказані для сполуки формули (I), за винятком того, що щонайменше один з m і n не дорівнює 0. 1 3 4 5 8 Бажаним варіантом здійснення є сполуки формули (Ig), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I) і A означає C-F, m та n дорівнюють 0, і p дорівнює 1. 1 3 4 5 8 Переваги для R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 6 7 8 Бажаним варіантом здійснення є сполуки формули (Ih), в якій A, R , R , R , m, R , n і R є 4 5 такими, як визначено для сполуки формули (I), R та R означають H, і p дорівнює 1, за умови, 1 3 6 7 8 що щонайменше один з m або n не дорівнює 0. Переваги для R , R , R , m, R , n та R є такими ж, які вказані для сполуки формули (I), за винятком того, що щонайменше один з m і n не дорівнює 0. 1 3 4 5 8 Бажаним варіантом здійснення є солі формули (Ij), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), A означає C-H, m та n дорівнюють 0, p дорівнює 1, і HX вибраний з групи, що включає 2-хлорбензойну кислоту, етансульфонову кислоту, хлористоводневу кислоту, 3-гідроксипропан-1-сульфонову кислоту, метансульфонову кислоту, (4-метилфеніл)сульфонову кислоту, 3-феноксипропіонову кислоту, фосфорну кислоту, 1 3 4 5 8 тридеканову кислоту, трифтороцтову кислоту. Переваги для R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 4 5 8 Бажаним варіантом здійснення є солі формули (Ik), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), HX є таким, як визначено для сполуки формули (Ij), A 1 3 4 5 8 означає N, m та n дорівнюють 0, і p дорівнює 1. Переваги для R , R , R , R та R є такими ж, які вказані для сполуки формули (I). 1 3 4 5 8 Бажаним варіантом здійснення є солі формули (Im), в якій R , R , R , R та R є такими, як визначено для сполуки формули (I), HX є таким, як визначено для сполуки формули (Ij), A 1 3 4 5 8 означає N, і m, n та p дорівнюють 0. Переваги для R , R , R , R та R є такими ж, які вказані для 3 UA 101046 C2 сполуки формули (I). Деякі проміжні продукти є новими і утворюють ще один об'єкт даного винаходу. Однією такою групою проміжних продуктів є сполуки формули (II) NH 3 R N (II) 4 R NH 5 R 5 1 O R 3 4 5 1 3 в якій R , R , R та R є такими, як визначено для сполуки формули (I). Переваги для R , R , 4 5 R та R є такими ж, які вказані для сполуки формули (I). Іншою групою проміжних продуктів є сполуки формули (III) 11 R O 1 N R 3 O N (III) R 4 NH R 10 5 1 O R 1 3 4 5 11 в якій R , R , R та R є такими, як визначено для сполуки формули (I); і R означає C1-C6алкіл, такий як трет-бутил, C2-C6-алкеніл, такий як аліл, або бензил, що необов'язково містить від 1 до 3 замісників, незалежно вибраних з групи, що включає галоген, C1-C6-алкіл, C1-C61 3 4 5 галогеналкіл, C1-C6-алкоксигрупу і C1-C6-галогеналкоксигрупу. Переваги для R , R , R та R є 11 такими ж, які вказані для сполуки формули (I). R бажано означає трет-бутил. Іншою групою проміжних продуктів є сполуки формули (IV) 11 R O N 3 R O N (IV) 4 R NH2 5 15 20 R 3 4 5 3 5 в якій R , R та R є такими, як визначено для сполуки формули (I), або R та R означають 4 11 водень і R означає фтор, хлор або трифторметил; і R є таким, як визначено для сполуки 3 4 5 формули (III). Переваги для R , R та R є такими ж, які вказані для сполуки формули (I). 11 Перевага для R є такою ж, яка вказана для сполуки формули (III). Іншою групою проміжних продуктів є сполуки формули (V) 11 R O N R 3 O N (V) R 4 NH2 5 25 R 3 4 5 3 5 в якій R , R та R є такими, як визначено для сполуки формули (I), або R та R означають 4 11 водень і R означає фтор, хлор або трифторметил; і R є таким, як визначено для сполуки 3 4 5 формули (III). Переваги для R , R та R є такими ж, які вказані для сполуки формули (I). 11 Перевага для R є такою ж, яка вказана для сполуки формули (III). 4 UA 101046 C2 Іншою групою проміжних продуктів є сполуки формули (VI) 11 R O N 3 R O N (VI) 4 R NO2 5 5 10 15 20 25 R 3 4 5 11 в якій R , R та R є такими, як визначено для сполуки формули (I); і R є таким, як 3 4 5 визначено для сполуки формули (III). Переваги для R , R та R є такими ж, які вказані для 11 сполуки формули (I). Перевага для R є такою ж, яка вказана для сполуки формули (III). Сполуки, запропоновані в даному винаході, можна одержати за різними методиками, як це описано у WO 2006/003494. Наприклад, сполуки формули (I) можна одержати у відповідності зі схемами 1, 2 та 3. 1 3 4 5 6 7 8 Таким чином, сполуку формули (1), в якій A, R , R , R , R , R , m, R , n та R є такими, як 1 3 4 визначено для сполуки формули (I), можна одержати зі сполуки формули (2), в якій A, R , R , R 5 та R є такими, як визначено для сполуки формули (I), за реакцією зі сполукою формули (3), в 6 7 8 якій R , m, R , n та R є такими, як визначено для сполуки формули (I) і X означає групу, що відщеплюється, таку як галогенід (наприклад, хлорид, бромід або йодид) або сульфонат (наприклад, мезилат або тозилат), у присутності основи, такої як третичний амін (наприклад, діізопропілетиламін або триетиламін), в органічному розчиннику, такому як дихлорметан, ацетонітрил або N, N-диметилформамід, при температурі, рівній від 0 до 100 °C, зазвичай при температурі навколишнього середовища, як показано на схемі 1. Схема 1 Альтернативно, сполуку формули (1), визначену вище, можна одержати зі сполуки формули 8 (2), визначеної вище, за реакцією з альдегідом формули (4), в якій R є таким, як визначено для сполуки формули (I), у присутності відновлювального реагенту, такого як (триацетокси)борогідрид натрію, ціаноборогідрид натрію або боран і т.п., в органічному розчиннику, такому як тетрагідрофуран, метанол або етанол, при температурі, рівній від 0 до 100 °C, зазвичай при температурі навколишнього середовища, як показано на схемі 2. 5 UA 101046 C2 Схема 2 5 10 15 20 25 Сполуки формули (2) можна одержати так, як описано у WO 2006/003494. Приклади цих методик наведені у прикладах одержання сполук. Сполуки формули (3) та (4) є відомими сполуками або їх можна одержати за методиками, відомими фахівцю в даній галузі техніки. Приклади цих методик наведені в прикладах одержання сполук. Схема 3 N-Оксиди формули (5) можна одержати шляхом окислення сполуки формули (1) окислювальним реагентом, таким як пероксид водню або 3-хлорпероксибензойна кислота, в органічному розчиннику, такому як дихлорметан, етанол, метанол або вода, або в суміші розчинників, при температурі, рівній від -78 до 100 °C, зазвичай при температурі навколишнього середовища, як показано на схемі 3. Сполуки формули (I) мають поліпшену пестицидну здатність. Наприклад, сполуки можуть мати підвищену інсектицидну активність та/чи поліпшену світловитривалість. Сполуки формули (I) можна використовувати для боротьби з нашестям зазначених нижче шкідників-комах та їх знищення, таких як лускокрилі, двокрилі, клопи, бахромчатокрилі, прямокрилі, таргани, жорсткокрилі, блохи, перетинчастокрилі і терміти, а також інші безхребетні шкідники, наприклад, кліщі, нематоди та молюски. Комахи, кліщі, нематоди та молюски далі спільно будуть називатися шкідниками. Шкідники, з якими можна боротися і яких можна знищувати шляхом застосування сполук, запропонованих у даному винаході, включають шкідників, пов'язаних із землеробством (цей термін включає вирощування врожаю для одержання харчових продуктів і продуктів з волокон), плодівництвом і тваринництвом, свійськими тваринами, лісівництвом і зберіганням продуктів рослинного походження (таких як плоди, зерно і деревина); шкідників, пов'язаних з пошкодженням штучних споруджень і 6 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 передачею хвороб людині та тваринам; а також дратівних шкідників (таких як мухи). Приклади видів шкідників, боротися з якими можна за допомогою сполук формули (I), включають: Myzus persicae (попелиця), Aphis gossypii (попелиця), Aphis fabae (попелиця), Lygus spp. (клопи), Dysdercus spp. (клопи), Nilaparvata lugens (дельфацид), Nephotettixc incticeps (цикадка), Nezara spp. (щитники), Euschistus spp. (щитники), Leptocorisa spp. (щитники), Frankliniella occidentalis (трипс), Thrips spp. (трипси), Leptinotarsa decemlineata (колорадський жук), Anthonomus grandis (довгоносик бавовняний), Aonidiella spp. (червці), Trialeurodes spp. (білокрилки), Bemisia tabaci (білокрилка), Ostrinia nubilalis (метелик кукурудзяний), Spodoptera littoralis (гусениця совки бавовняної), Heliothis virescens (гусениця тютюнової листовійкибрунькоїда), Helicoverpa armigera (коробковий хробак), Helicoverpa zea (коробковий хробак), Sylepta derogata (листовійка бавовняна), Pieris brassicae (капусниця), Plutella xylostella (моль капустяна), Agrotis spp. (совки), Chilo suppressalis (свердлильник рисовий стеблевий), Locusta migratoria (сарана), Chortiocetes terminifera (сарана), Diabrotica spp. (листоїди), Panonychus ulmi (кліщ червоний плодовий), Panonychus citri (кліщик червоний цитрусовий), Tetranychus urticae (кліщ двоплямовий павутинний), Tetranychus cinnabarinus (кліщ павутинний червоний), Phyllocoptruta oleivora (кліщ іржастий (іржавий) цитрусовий), Polyphagotarsonemus latus (широкий кліщ), Brevipalpus spp. (плоскі кліщі), Boophilus microplus (кліщ боофілюс), Dermacentor variabilis (іксодовий кліщ собачий), Ctenocephalides felis (блоха котяча), Liriomyza spp. (мінуючі мушки), Musca domestica (муха кімнатна), Aedes aegypti (комар), Anopheles spp. (кровопивні комарі), Culex spp. (кровопивні комарі), Lucillia spp. (м'ясні мухи), Blattella germanica (тарган), Periplaneta americana (тарган), Blatta orientalis (тарган), терміти сімейства Mastotermitidae (наприклад Mastotermes spp.), сімейства Kalotermitidae (наприклад Neotermes spp.), сімейства Rhinotermitidae (наприклад Coptotermes formosanus, Reticulitermes flavipes, R. speratu, R. virginicus, R. hesperus і R. santonensis) і сімейства Termitidae (наприклад Globitermes sulphureus), Solenopsis geminata (вогняна мураха), Monomorium pharaonis (фараонів мураха), Damalinia spp. і Linognathus spp. (пухоїди і воші), Meloidogyne spp. (кореневі нематоди), Globodera spp. і Heterodera spp. (гетеродериди), Pratylenchus spp. (нематоди, що ушкоджують рослини), Rhodopholus spp. (бананові норові або свердлувальні нематоди), Tylenchulus spp. (цитрусові нематоди), Haemonchus contortus (гемонхус), Caenorhabditis elegans (оцтова нематода), Trichostrongylus spp. (шлунково-кишкові нематоди) і Deroceras reticulatum (слимаки). Тому даний винахід належить до способу боротьби з комахами, кліщами, нематодами і молюсками або їх знищення, який включає нанесення сполуки формули (I) або композиції формули, що містить сполуку (I), в інсектицидно, акарицидно, нематоцидно або молюскоцидно ефективній кількості на шкідників, на осередок шкідників, бажано на рослину, або на рослину, що піддається нашестю шкідників. Сполуки формули (I) бажано використовувати проти комах, кліщів або нематод. При використанні в даному винаході термін "рослина" включає сіянці, чагарники і дерева. Культури слід розуміти і як такі, що включають культури, яким надана стійкість до гербіцидів або класів гербіцидів (наприклад, до інгібіторів ALS-, GS-, EPSPS-, PPO-, ACCase і HPPD) за допомогою звичайних методик селекції або генної інженерії. Прикладом культури, якій за допомогою звичайних методик надана стійкість, наприклад, до імідазолінонів, наприклад, до імазамоксу, є суріпиця Clearfield® (канола). Прикладами культур, яким за допомогою методик генної інженерії надана стійкість до гербіцидів, є сорти кукурудзи, стійкі, наприклад, до гліфосату або глуфосинату, які є у продажу під торгівельними назвами RoundupReady® та LibertyLink®. Під культурами також слід розуміти ті, у яких методами генної інженерії було вироблено стійкість до комах-шкідників, наприклад, Bt-кукурудзу (стійку до кукурудзяного метелика), Btбавовник (стійкий до бавовняного довогоносика), а також різноманітні сорти Bt-картоплі (стійкої ® до колорадського жука). Прикладами Bt-кукурудзи є гібриди кукурудзи Bt 176 сорту NK (Syngenta Seeds). Прикладами трансгенних рослин, які містять один чи більшу кількість генів, які кодують стійкість до інсектицидів та виробляють один або більшу кількість токсинів, є KnockOut® (кукурудза), Yield Gard® (кукурудза), NuCOTIN33B® (бавовна), Bollgard® (бавовна), NewLeaf® (картопля), NatureGard® та Protexcta®. Культурні рослини та їх насінний матеріал може бути стійким до гербіцидів і одночасно, також, до поїдання комахами (поєднані трансгенні характеристики). Насіння може, наприклад, мати здатність виробляти білок, що має інсектицидну активність Cry3 і одночасно бути стійкими стосовно гліфосату. Під культурами також слід розуміти ті, які одержані за звичайними методиками селекції або генної інженерії і зібраний врожай яких має додаткові характеристики (наприклад, покращену стабільність при зберіганні, більшу живильну цінність і покращений смак). 7 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 Для нанесення сполуки формули (I) у вигляді інсектициду, акарициду, нематоциду або молюскоциду на шкідників, на осередок шкідників або на рослини, що піддалися нашестю шкідників, сполуку формули (I), зазвичай, вносять в композицію, яка додатково до сполуки формули (I) включає підходящий інертний розріджувач або носій і необов'язково поверхневоактивну речовину (ПАР). ПАР є хімікатами, які здатні змінювати межі розділу (наприклад, межі розділу рідина\тверда речовина, рідина\повітря або рідина\рідина) шляхом зниження поверхневого натягу, що призводить до змін інших властивостей (наприклад, диспергування, емульгування і змочування). Бажано, щоб усі композиції (і тверді, і рідкі препарати) включали, в мас. %, від 0,0001 до 95 %, більш бажано від 1 до 85 %, наприклад, від 5 до 60 % сполуки формули(I). Композицію зазавичай застосовують для боротьби зі шкідниками таким чином, щоб сполука формули (I) наносилась в кількості, що становить від 0,1 г до 10 кг на гектар, бажано від 1 г до 6 кг на гектар, більш бажано від 1 г до 1 кг на гектар. При використанні для протравляння насіння сполука формули (I) застосовується в кількості, що становить від 0,0001 до 10 г (наприклад, 0,001 г або 0,05 г), бажано від 0,005 до 10 г, більш бажано від 0,005 до 4 г на 1 кг насіння. Іншим об'єктом даного винаходу є інсектицидна, акарицидна, нематоцидна або молюскоцидна композиція, що включає сполуку формули (I) в інсектицидно, акарицидно, нематоцидно або моллюскоцидно ефективній кількості і його підходящий носій або розріджувач. Композиція бажано є інсектицидною, акарицидною, нематоцидною або молюскоцидною композицією. Ще одним об'єктом даного винаходу є спосіб боротьби зі шкідниками в осередку, який включає обробку шкідників або осередку шкідників за допомогою композиції, що містить сполуку формули (I) в інсектицидно, акарицидно, нематоцидно або молюскоцидно ефективній кількості. Сполуки формули (I) бажано використовувати проти комах, кліщів або нематод. Композициї можна обирати з цілого ряду типів препаратів, включаючи порошки для обпилення (ПО), розчинні порошки (РП), розчинні у воді гранули (ВГ), диспергуючі у воді гранули (ДГ), порошки, що змочуються (ЗП), гранули (ГР) (з повільним або швидким вивільненням), розчинні концентрати (РК) рідини, що змішуються з маслом (МР), рідини зверхмалого об'єму (РЗ), концентрати, що емульгуються (ЕК), концентрати, що диспергуються (ДК), емульсії (і масло-в-воді (ЕМ), і вода-в-маслі (ЕВ)), мікроемульсії (МЕ), концентрати суспензій (СК), аерозолі, препарати для дрібнокрапельного обприскування/фумігації, капсульовані суспензії (КС) і препарати для обробки насіння. Обраний тип композиції в кожному разі буде залежати від конкретного призначення і фізичних, хімічних та біологічних характеристик сполуки формули (I). Порошки для обпилення (ПО) можна одержати шляхом змішування сполуки формули (I) з одним або більшою кількістю твердих розріджувачів (наприклад, природними глинами, каоліном, пірофілитом, бентонітом, оксидом алюмінію, монтморилонітом, кізельгуром, крейдою, діатомовою землею, фосфатами кальцію, карбонатами кальцію і магнію, сіркою, вапном, різними типами муки, тальком та іншими органічними і неорганічними твердими носіями) і механічного розмелу суміші в тонкоподрібнений порошок. Розчинні порошки (РП) можна одержати шляхом змішування сполуки формули (I) з одним або більшою кількістю розчинних у воді неорганічних солей (таких як бікарбонат натрію, карбонат натрію або сульфат магнію) чи з одним або більшою кількістю розчинних у воді органічних твердих речовин (таких як полісахарид) і, необов'язково, з одним або більшою кількістю змочувальних агентів, з одним або більшою кількістю диспергуючих агентів або сумішшю таких агентів для покращення диспергування/розчинності у воді. Потім суміш розмелюють у тонкоподрібнений порошок. Аналогічні композиції також можна гранулювати з одержанням розчинних у воді гранул (ВГ). Порошки, що змочуються (ЗП) можна одержати шляхом змішування сполуки формули (I) з одним або більшою кількістю твердих розріджувачів або носіїв, з одним або більшою кількістю змочувальних агентів та, бажано, з одним або більшою кількістю диспергуючих агентів та, необов'язково, з одним або більшою кількістю суспендуючих агентів для спрощення диспергування в рідинах. Потім суміш розмелюють в тонкоподрібнений порошок. Аналогічні композиції також можна гранулювати з одержанням диспергуючих у воді гранул (ДГ). Гранули (ГР) можна одержати або шляхом гранулювання суміші сполуки формули (I) з одним або більшою кількістю порошкоподібних твердих розріджувачів або носіїв, або із заздалегідь сформованих гранул, що не містять активного інгредієнта, шляхом абсорбції сполуки формули (I) (або його розчину в підходящому агенті) в пористому гранульованому матеріалі (такому як пемза, атапульгітова глина, фуллерова земля, кізельгур, діатомова земля або розмелені кукурудзяні качани) або шляхом адсорбції сполуки формули (I) (або його розчину 8 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 в підходящому агенті) в твердому наповнювачі (такому як пісок, силікати, неорганічні карбонати, сульфати або фосфати) з проведенням сушіння у випадку необхідності. Агенти, що зазвичай застосовуються для сприяння абсорбції або адсорбції, включають розчинники (такі як аліфатичні та ароматичні нафтові розчинники, спирти, прості ефіри, кетони і складні ефіри) та склеюючі агенти (такі як полівінілацетати, полівінілові спирти, декстрини, цукри і рослинні олії). У гранули також можна включити одну або більшу кількість інших добавок (наприклад, емульгуючий агент, агент, що змочує або диспергуючий агент). Диспергируючі концентрати (ДК) можна одержати шляхом розчинення сполуки формули (I) у воді або органічному розчиннику, такому як кетон, спирт або простий ефір гліколю. Ці розчини можуть містити поверхнево-активну речовину (наприклад, для покращення розведення водою або запобігання кристалізації в баку для обприскування). Емульгуючі концентрати (ЕК) або емульсії масло-в-воді (ЕМ) можна одержати шляхом розчинення сполуки формули (I) в органічному розчиннику (який необов'язково містить один або більшу кількість змочувальних агентів, один або більшу кількість емульгуючих агентів або суміш таких агентів). Органічні розчинники, що підходять для використання в ЕК включають ароматичні вуглеводні (такі як алкілбензоли або алкілнафталіни, прикладами яких є SOLVESSO 100, SOLVESSO 150 та SOLVESSO 200; SOLVESSO є зареєстрованим товарним знаком), кетони (такі як циклогексанон або метилциклогексанон) і спирти (такі як бензиловий спирт, фурфуриловий спирт або бутанол), N-алкілпіролідони (такі як N-метилпіролідон або Nоктилпіролідон), диметиламіди жирних кислот (такі як диметиламід жирної кислоти C8-C10) та хлоровані вуглеводні. Готовий ЕК може самовільно емульгуватися при додаванні до води з утворенням емульсії, що має достатню стабільність, щоб за допомогою підходящого обладнання було можливе проведення обприскування. Одержання ЕМ включає одержання сполуки формули (I) у вигляді рідини (якщо при кімнатній температурі воно не є рідиною, то його можна розплавити при підходящій температурі, зазвичай нижче 70 °C) або розчину (шляхом розчинення в підходящому розчиннику) з наступним емульгуванням одержаної рідини або розчину у воді, що містить одну або більшу кількість ПАР, при більшому рушійному зусиллі, з одержанням емульсії. Розчинники, що підходять для використання в ЕМ включають рослинні олії, хлоровані вуглеводні (такі як хлорбензоли), ароматичні розчинники (такі як алкілбензоли або алкілнафталіни) та інші підходящі органічні розчинники, що мають низьку розчинність у воді. Мікроемульсії (МЕ) можна одержати шляхом змішування води із сумішшю одного або більшої кількості розчинників з однією або більшою кількістю ПАР для забезпечення самовільного утворення термодинамічно стабільного ізотропного рідкого препарату. Сполука формули (I) знаходиться первісно або у воді, або у суміші розчинник/ПАР. Розчинники, що підходять для використання в МЕ включають зазначені вище для застосування в ЕК або ЕМ. МЕ може являти собою систему масло-у-воді або вода-у-маслі (визначити тип наявної системи можна шляхом виміру електропровідності) і вона може виявитися підходящою для змішування розчинюваних у воді і розчинюваних у маслі пестицидів в одному і тому ж препараті. МЕ придатна для розведення водою, в якій вона залишиться мікроемульсією або утворить звичайну емульсію масло-у-воді. Концентрати суспензій (СК) можуть включати водні або неводні суспензії тонкоподрібнених нерозчинних твердих часток сполуки формули (I). СК можна одержати шляхом розмелу на кульовому або бісерному млині твердої сполуки формули (I) у відповідному середовищі, необов'язково з одним або більшою кількістю диспергуючих агентів і одержати тонкоподрібнену суспензію сполуки. В композицію можна включити один або більшу кількість змочувальних агентів і можна включити агент, що суспендує для зниження швидкості осідання часток. Альтернативно, сполуку формули (I) можна піддати сухому розмелу і додати до води, що містить агенти, зазначені вище в даному винаході, та одержати шуканий готовий продукт. Аерозольні препарати включають сполуку формули (I) і підходящий пропілент (наприклад, нбутан). Сполуку формули (I) також можна розчинити або диспергувати у підходящому середовищі (наприклад, у воді або з рідиною, що змішується з водою, такою як н-пропанол) і одержати композиції для використання в ємностях для розпилення, що не перебувають під тиском і діють за допомогою ручних насосів. Сполуку формули (I) можна у сухому вигляді змішати з піротехнічною сумішшю і одержати композицію, придатну для утворення у закритому просторі диму, що містить сполуку. Капсульовані суспензії (КС) можна одержати способом, подібним до способу одержання препаратів ЕМ, але із включенням додаткової стадії полімеризації, так щоб утворилася водна дисперсія крапельок масла, у якій кожна крапелька масла капсульована за допомогою полімерної оболонки і містить сполуку формули (I) і, необов'язково, її носій або розріджувач. Полімерну оболонку можна одержати за допомогою міжфазової реакції поліконденсації або за 9 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 методикою коацервації. Композиції можуть використовуватися для врегульованого вивільнення сполуки формули (I) і їх можна використовувати для обробки насіння. Сполуку формули (I) також можна включити в полімерну матрицю, що біологічно розкладається, та забезпечити повільне, врегульоване вивільнення сполуки. Композиція може включати одну або більше добавок для поліпшення біологічних робочих характеристик композиції (наприклад, шляхом поліпшення змочування, утримання або розподілення на поверхнях; стійкості до впливу дощу на оброблені поверхні; або усмоктування або рухливості сполуки формули (I)). Такі добавки включають поверхнево-активні речовини, добавки для обприскування на основі масел, наприклад, деяких мінеральних масел або натуральних рослинних олій (таких як соєва олія і рапсова олія), та їх суміші з іншими посилюючими біологічний вплив допоміжними речовинами (інгредієнтами, які можуть сприяти впливу сполуки формули (I) або змінювати її вплив). Сполуку формули (I) також можна приготувати для застосування в якості засобу для обробки насіння, наприклад, у вигляді порошкоподібної композиції, включаючи порошок для сухої обробки насіння (ПС), розчинний у воді порошок (ВП) і диспергуючий у воді порошок для обробки суспензією (ДП), або у вигляді рідкої композиції, включаючи текучий концентрат (ТК), розчин (РЗ) і капсульовану суспензію (КС). Одержання композицій ПС, ВП, ДП, ТК і РЗ є дуже подібним до одержання зазначених вище композицій ПО, РП, ЗП, СК і ДК відповідно. Композиції для обробки насіння можуть включати агент, що сприяє адгезії композиції до насіння (наприклад, мінеральне масло або плівкоутворювальна захисна речовина). Змочувальні агенти, диспергуючі агенти та емульгуючі агенти можуть являти собою ПАР катіоногенного, аніоногенного, амфотерного або неіоногенного типу. Підходящі ПАР катіоногенного типу включають четвертинні амонієві сполуки (наприклад, цетилтриметиламонійбромід), імідазоліни та солі амінів. Підходящі аніоногені ПАР включають солі лужних металів жирних кислот, солі аліфатичних моноефірів сірчаної кислоти (наприклад, лаурилсульфат натрію), солі сульфованих ароматичних сполук (наприклад, додецилбензолсульфонат натрію, додецилбензолсульфонат кальцію, бутилнафталінсульфонат і суміші діізопропіл- і триізопропілнафталінсульфонатів натрію), сульфати простих ефірів, сульфати простих ефірів спиртів (наприклад, лаурет-3сульфат натрію), карбоксилати простих ефірів (наприклад, лаурет-3-карбоксилат натрію), фосфатні складні ефіри (продукти реакції одного або більшої кількості жирних спиртів з фосфорною кислотою (переважно складні моноефіри) або з пентаоксидом фосфору (переважно складні діефіри), наприклад, продукти реакції лаурилового спирту с тетрафосфорною кислотою; ці продукти також можуть бути етоксиловані), сульфосукцинамати, сульфонати парафінів або олефінів, таурати і лігносульфонати. Підходящі ПАР амфотерного типу включають бетаїни, пропіонати та гліцинати. Підходящі ПАР неіоногенного типу включають продукти конденсації алкіленоксидів, таких як етиленоксид, пропіленоксид, бутиленоксид, або їх сумішей з жирними спиртами (такими як олеіловий спирт або цетиловий спирт) або з алкілфенолами (такими як октилфенол, нонілфенол або октилкрезол); часткові складні ефіри, одержані з жирних кислот з довгими ланцюгами або ангідридів гекситу; продукти конденсації зазначених часткових складних ефірів з етиленоксидом; блок-полімери (що включають етиленоксид і пропіленоксид); алканоламіди; звичайні складні ефіри (наприклад, поліетиленгліколеві ефіри жирних кислот); оксиди амінів (наприклад, лаурилдиметиламіноксид); та лецитини. Підходящі суспендуючі агенти включають гідрофільні колоїди (такі як полісахариди, полівінілпіролідон або натрієва сіль карбоксиметилцелюлози) та глини, що набухають (такі як бентоніт або атапульгіт). Сполуку формули (I) можна вносити будь-якими відомими способами нанесення пестицидних сполук. Наприклад, її можна нанести, одну або в композиції, на шкідників або на осередок шкідників (такий як місце проживання шкідників або на рослину, що вирощується та піддана зараженню шкідниками) або на будь-яку частину рослини, включаючи листя, стебла, гілки або коріння, на насіння перед їх висіванням або на інші середовища, в яких виростає або повинна бути посіяна рослина (такі як ґрунт, що оточує коріння, ґрунт у цілому, вода для затоплення або гідропонні системи вирощування), безпосередньо або її можна вносити шляхом розбризкування, обпилення, наносити зануренням, вносити у вигляді препарату, що представляє собою крем або пасту, вносити у вигляді пару або вносити шляхом розподілу композиції (такий як гранульована композиція або композиція, упакована в розчинний у воді пакет) у ґрунті або у водному середовищі або включення в нього. Сполуку формули (I) також можна ввести в рослини шляхом ін'єкції або обприскування рослинного покриву з використанням електродинамічних методик обприскування або інших 10 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 малооб'ємних методик або внести на ділянку за допомогою наземних або авіаційних систем зрошування. Композиції для застосування в якості водних препаратів (водяних розчинів або дисперсій) зазвичай поставляються у вигляді концентрату, що містить значну частку активного інгредієнта, і перед застосуванням концентрат додають до води. Ці концентрати, які можуть являти собою ДК, СК, ЕК, ЕМ, МЕ, ВГ, РП, ЗП, ДГ і КС, часто повинні витримувати зберігання протягом тривалих періодів часу і після такого зберігання після додавання до води повинні бути здатні утворювати водні препарати, які залишаються однорідними протягом часу, достатнього для того, щоб їх можна було вносити за допомогою звичайного обладнання для розбризкування. Такі водні препарати можуть містити різні кількості сполуки формули (I) (наприклад, від 0,0001 до 10 мас. %) залежно від мети їх застосування. Сполуку формули (I) можна застосовувати в сумішах з добривами (наприклад, азото-, калієабо фосфоровмісними добривами). Підходящі типи препаратів включають гранули добрива. Бажано, щоб суміші містили до 25 мас. % сполуки формули (I). Тому даний винахід також відноситься до композиції добрива, що містить добриво і сполуку формули (I). Композиції, запропоновані в даному винаході, можуть містити інші сполуки, що мають біологічну активність, наприклад, мікродобрива або сполуки, що мають фунгіцидну активність або, що мають регулюючу ріст рослини, гербіцидну, інсектицидну, нематоцидну або акарицидну активність. Сполука формули (I) може бути єдиним активним інгредієнтом композиції або вона може бути змішана з одним або більшою кількістю додаткових активних інгредієнтів, таких як пестицид, фунгіцид, синергетик, гербіцид або регулятор росту рослин, якщо це доцільно. Додатковий активний інгредієнт може: давати композицію, що має більш широкий спектр активності або підвищену стійкість в осередку розповсюдження; підсилювати вплив або доповнювати вплив (наприклад, шляхом збільшення швидкості впливу або подолання несприйнятливості) сполуки формули (I); або сприяти подоланню чи попередженню розвитку резистентності стосовно окремих компонентів. Те, який конкретний додатковий активний інгредієнт буде використовуватися, залежить від призначення композиції. Приклади пестицидів, які підходять, наступні: a) Піретроїди, такі як перметрин, циперметрин, фенвалерат, есфенвалерат, дельтаметрин, цигалотрин (зокрема, лямбда-цигалотрин), біфентрин, фенпропатрин, цифлутрин, тефлутрін, безпечні для риб піретроїди (наприклад, етофенпрокс), натуральний піретрин, тетраметрин, Sбіоалетрин, фенфлутрин, пралетрин або 5-бензил-3-фурілметил-(E)-(1R, 3S) -2,2-диметил-3-(2оксотіолан-3-іліденметил) циклопропанкарбоксилат; b) Фосфорорганічні сполуки, такі як профенофос, сульпрофос, ацефат, метилпаратіон, азинфос-метил, деметон-s-метил, гептенофос, тіометон, фенаміфос, монокротофос, профенофос, тріазофос, метамідофос, диметоат, фосфамідон, малатіон, хлорпірифос, фозалон, тербуфос, фенсульфотіон, фонофос, форат, фоксим, піриміфос-метил, піриміфосетил, фенітротіон, фостіазат або діазинон; c) Карбамати (включаючи арилкарбамати), такі як піримікарб, тріазамат, клоетокарб, карбофуран, фуратіокарб, етіофенкарб, альдикарб, тіофурокс, карбосульфан, бендіокарб, фенобукарб, пропоксур, метоміл або оксаміл; d) Бензоїлсечовини, такі як дифлубензурон, трифлумурон, гексафлумурон, флуфеноксурон або хлорфлуазурон; e) Органічні сполуки олова, такі як цигексатин, фенбутатіноксид або азоциклотин; f) Піразоли, такі як тебуфенпірад або фенпіроксімат; g) Макроліди, такі як авермектини або мілбеміцини, наприклад, абамектин, емамектинбензоат, івермектин, мілбеміцин, спіносад, спінеторам або азадирахтин; h) Гормони і феромони; i) Хлорорганічні сполуки, такі як ендосульфан, бензолгексахлорид, ДДТ, хлордан або діелдрин; j) Амідини, такі як хлордимеформ або амітраз; k) Фуміганти, такі як хлорпікрин, дихлорпропан, метилбромід або метам; l) Неонікотиноїдні сполуки, такі як імідаклоприд, тіаклоприд, ацетаміприд, клотіанідин, нітенпірам, динотефуран або тіаметоксам; m) Діацилгідразини, такі як тебуфенозид, хромафенозид або метоксифенозид; n) Дифенілові ефіри, такі як диофенолан або пірипроксифен; o) Індоксакарб; p) Хлорфенапір; 11 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 60 q) Пиметрозин або пірифлуквіназон; r) Спіротетрамат, спіродиклофен або спіромезифен; s) Флубендиамід, хлорантраніліпрол або циантраніліпрол; t) Циенопірафен або цифлуметофен; або u) Сульфоксафлор. В доповнення до основних хімічних класів пестицидів, що перераховані вище, у композиціях можна використовувати інші пестициди, що впливають на певних шкідників, якщо це доцільно для призначення композиції. Наприклад, можна використовувати інсектициди, селективні для конкретних культур, наприклад, специфічні по відношенню до стеблових пильщиків інсектициди (такі як картап) або специфічні для амбарів інсектициди (такі як бупрофезин) для застосування для рису. Альтернативно, у композицію також можна включати інсектициди або акарициди, специфічні для конкретних видів/стадій розвитку комах (наприклад, акарицидні оволарвіциди, такі як клофентезин, флукбензимін, гекситиазокс або тетрадіфон; акарицидні мотиліциди, такі як дикофол або пропаргіт; акарициди, такі як бромпропілат або хлорбензилат; або регулятори росту, такі як гідраметилнон, циромазин, метопрен, хлорфлуазурон або дифлубензурон). Прикладами фунгіцидних сполук, які можна включати в композицію, запропоновану в даному винаході, є (E)-N-метил-2-[2-(2,5-диметилфеноксиметил)феніл]-2-метоксиіміноацетамід (SSF-129), 4бром-2-ціано-N, N-диметил-6-трифторметилбензимідазол-1-сульфонамід, -[N-(3-хлор-2,6ксиліл)-2-метоксиацетамідо]--бутиролактон, 4-хлор-2-ціано-N, N-диметил-5-п-толілімідазол-1сульфонамід (IKF-916, ціамідузосульфамід), 3-5-дихлор-N-(3-хлор-1-етил-1-метил-2оксопропіл)-4-метилбензамід (RH-7281, зоксамід), N-аліл-4,5,-диметил-2-триметилсилілтіофен3-карбоксамід (MON65500), N-(1-ціано-1,2-диметилпропіл)-2-(2,4-дихлорфенокси)пропіонамід (AC382042), N-(2-метокси-5-піридил)циклопропанкарбоксамід, ацибензолар (CGA245704), аланікарб, альдіморф, анілазин, азаконазол, азоксистробін, беналаксил, беноміл, білоксазол, бітертанол, бластицидин S, бромуконазол, бупіримат, каптафол, каптан, карбендазим, карбендазимхлоргідрат, карбоксин, карпропамід, карвон, CGA41396, CGA41397, хінометіонат, хлороталоніл, хлорозолінат, клозилакон, сполуки що містять мідь, такі як оксихлорид міді (II), оксихінолат міді (II), сульфат міді (II), таллат міді (II) і бордоська рідина, цимоксаніл, ципроконазол, ципродиніл, дебакарб, ди-2-піридилдисульфід 1,1'-діоксид, дихлофлуанід, дикломезин, диклоран, діетофенкарб, дифеноконазол, дифензокват, дифлуметорим, O, Oдіізопропіл-S-бензилтіофосфат, димефлуазол, диметконазол, диметоморф, диметиримол, диніконазол, динокап, дитианон, додецилдиметиламонійхлорид, додеморф, додин, догуадин, едифенфос, епоксиконазол, етіримол, етил-(Z)-N-бензилN([метил(метилтиоетилиденамінооксикарбоніл)аміно]тио)--аланінат, етридіазол, фамоксадон, фенамідон (RPA407213), фенаримол, фенбуконазол, фенфурам, фенгексамід (KBR2738), фенпіклоніл, фенпропідин, фенпропіморф, фентинацетат, фентингідроксид, фербам, феримзон, флуазинам, флудіоксоніл, флуметовер, фторимід, флухінконазол, флусилазол, флутоланіл, флутриафол, фолпет, фуберидазол, фуралаксил, фураметпир, гуазатин, гексаконазол, гідроксиізоксазол, гімексазол, імазаліл, імібенконазол, іміноктадин, іміноктадин триацетат, іпконазол, іпробенфос, іпродіон, іпровалікарб (SZX0722), ізопропанілбутилкарбамат, ізопротіолан, касугаміцин, крезоксим-метил, LY186054, LY211795, LY248908, манкозеб, манеб, мефеноксам, мепаніпірим, мепронил, металаксил, метконазол, метирам, метирам-цинк, метоминостробін, міклобутанил, неоасозин, диметилдитіокарбамат нікелю, нітротал-ізопропіл, нуарімол, офурац, ртутьорганічні сполуки, оксадиксил, оксасульфурон, оксолінова кислота, окспоконазол, оксикарбоксин, перфуразоат, пенконазол, пенцикурон, феназиноксид, фосетилAl, фосфоровмісні кислоти, фталід, пікоксистробін (ZA1963), поліоксин D, полірам, пробеназол, прохлораз, процимідон, пропамокарб, пропіконазол, пропінеб, пропіонова кислота, піразофос, пірифенокс, піриметаніл, пірохілон, піроксифур, піролнітрин, четвертинні амоніеві сполуки, хінометіонат, хіноксифен, квінтоцен, сіпконазол (F-155), пентахлорфенат натрію, спіроксамин, стрептоміцин, сірка, тебуконазол, теклофталам, текназен, тетраконазол, тиабендазол, тифлузамід, 2-(тіоціанометилтіо)бензотіазол, тіофанат-метил, тирам, тимибенконазол, толклофос-метил, толілфлуанід, тріадимефон, тріадименол, тріазбутил, тріазоксид, трициклазол, тридеморф, трифлоксистробин (CGA279202), трифорин, трифлумизол, тритиконазол, валідаміцин A, вапам, вінклозолін, зінеб та зірам. Сполуки формули (I) можна змішувати із ґрунтом, торфом або іншими середовищами для вкорінення з метою захисту рослин від розповсюджуваних насіннями, переданих через ґрунт або листових грибкових хвороб. Приклади синергістів, що підходять для застосування в композиціях, включають піперонілбутоксид, сезамекс, сафроксан та додецилімідазол. 12 UA 101046 C2 5 10 15 20 25 30 Те, які гербіциди та регулятори росту рослин виявляться підходящими для включення в композиції, буде залежати від об'єкта впливу та необхідного ефекту. Прикладом селективного гербіциду для рису, що можна включити, є пропаніл. Прикладом регулятора росту рослин, призначеного для бавовни, є PIX. Деякі суміші можуть включати активні інгредієнти, які мають суттєво інші фізичні, хімічні, або біологічні характеристики, так що самі по собі вони нелегко включаються в такий же звичайний тип препарату. У таких випадках можна одержати інші типи препаратів. Наприклад, якщо один активний інгредієнт являє собою нерозчинну у воді тверду речовину, а інший - нерозчинну у воді рідину, все ж таки можна диспергувати кожен активний інгредієнт в одній і тій самій безперервній водній фазі шляхом диспергування твердого активного інгредієнта у вигляді суспензії (із застосуванням методики, аналогічній тій, що використовується для одержання СК), але диспергування рідкого активного інгредієнта у вигляді емульсії (із застосуванням методики, аналогічній тій, що використовується для одержання ЕМ). Одержана композиція являє собою препарат суспензія-емульсія (СЕ). Даний винахід ілюструється наведеними нижче прикладами: РХМС (рідинна хроматографія-мас-спектроскопія). Спектри знімали на мас-спектрометрі ZMD (Micromass, Manchester UK) або на спектрометрі ZQ (Waters Corp. Milford, MA, USA), який оснащений джерелом електророзпилення (ДЕР; температура джерела від 80 до100 °C; температура десольватації від 200 до 250 °C; напруга на конусі 30 В; швидкість газу на конусі 50 л/г, швидкість газу при десольватації від 400 до 600 л/г, діапазон мас: від 150 до 1000 Да), і за допомогою приладу Agilent 1100 HPLC (колонка: Gemini C18, розмір часток 3 мкм, 110 Å, 303 мм (Phenomenex, Torrance, CA, USA); температура колонки: 60 °C; швидкість потоку 1,7 мл/хв; елюент A: H2O/HCOOH 100:0,05; елюент B: MeCN/MeOH/HCOOH 80:20:0,04; градієнтний режим: 0 хв 5 % B; 2-2,8 хв 100 % B; 2,9-3 хв 5 % B; УФ-детектування: 200-500 нм, роздільна здатність 2 нм. Перед аналізом за допомогою МС потік розділяли після його проходження через колонку. ЧУ означає час утримування. Альтернативно, для сполук A25, A26, A27, A28, A27, C27 та C29 використовували методику РХМС (Waters Alliance 2795 LC) і наведені нижче умови градієнтного режиму для ВЕРХ (розчинник A: 0,1 % мурашиної кислоти у воді і розчинник B: 0,1 % мурашиної кислоти в ацетонітрилі). Час (хв) 0 2,5 2,8 2,9 35 A (%) 80 0 0 80 B (%) 20 100 100 20 Швидкість потоку (мл/хв) 1,7 1,7 1,7 1,7 Тип колонки: Waters atlantis dc18; довжина колонки: 20 мм; внутрішній діаметр колонки: 3 мм; розмір часток: 3 мкм; температура: 40 °C. Приклад 1 Цей приклад ілюструє одержання 2-хлор-N-{4,5-дифтор-2-[1-(4'-фторбіфеніл-4ілметил)піперидин-4-іл]феніл}ізонікотинаміду (сполука A3 в таблиці A). N F F NH F Cl O N 40 45 Суміш 2-хлор-N-(4,5-дифтор-2-піперидин-4-ілфеніл)ізонікотинаміду (100 мг) (одержували за методиками, аналогічними описаним у WO 2006/003494), 4-хлорметил-4'-фторбіфенілу (52,1 мг) (одержували так, як це описано у WO 2003/084916) і карбонату калію (104 мг) в ацетонітрилі (10 мл) перемішували при 60 °C протягом 48 год. Розчинник випарювали і залишок очищали за допомогою хроматографії на силікагелі (елюент: етилацетат + 1 % метанолу) і одержували шукану сполуку (100 мг) у вигляді білої аморфної твердої речовини. МС (ІЕ+) (мас1 спектрометрія з іонізацією електророзпиленням) 536/538 (MH+); H ЯМР (400 МГц, CDCl3) 1,77 (m, 4H), 2,08 (m, 2H), 2,55 (m, 1H), 3,06 (m, 2H), 3,56 (s, 2H), 7,07-7,73 (m, 13H), 8,60 (d, 1H). 13 UA 101046 C2 Наведені нижче сполуки одержували за методиками, аналогічними описаній у прикладі 1: Сполуки формули (Ia) N 3 R (Ia) 4 R 8 NH R 5 R 1 R O Таблиця A: Спол. № R 1 R 3 R 4 R 5 R 8 A1 2-хлорпірид-4-ил H -CH3 H F A2 2-хлорпірид-4-ил F F F F A3 2-хлорпірид-4-ил F F H F A4 2-хлорпірид-4-ил H -CF3 H F A5 2-хлорпірид-4-ил F H H F A6 2-хлорпірид-4-ил -OCF3 H H F A7 2-хлорпірид-4-ил -CF3 H H F A8 2-хлорпірид-4-ил -OCHF2 H H F A9 2-фторпірид-4-ил -OCHF2 H H F A10 2,6-дихлорпірид-4ил -OCHF2 H H F A11 2-хлорпірид-4-ил -CF(CF3)2 H H F A12 2-хлорпірид-4-ил Br -CF3 H F A13 2-хлорпірид-4-ил Cl H H F A14 2-хлорпірид-4-ил Br F H F A15 2-хлорпірид-4-ил Cl F H F A16 2-хлорпірид-4-ил H Cl H F A17 2-хлорпірид-4-ил Cl -CF3 H F A18 2-хлорпірид-4-ил Br F Br F A19 2-хлорпірид-4-ил F -CF3 H F A20 2-хлорпірид-4-ил -CF3 F H F A21 2-фторпірид-4-ил F H H F A22 2-бромпірид-4-ил F H H F 14 Агрегатний ВЕРХ стан/ МС (ІЕ+) (ЧУ) Т. пл.* тверда 1,39 хв 514 речовина тверда 1,42 хв 554 речовина тверда 1,45 хв 536 речовина тверда 1,48 хв 568 речовина тверда 1,37 хв 518 речовина тверда 1,48 хв 584 речовина тверда 1,42 хв 568 речовина тверда 1,48 хв 566/568 речовина тверда 1,31 хв 550 речовина тверда 1,47 хв 600/602/604 речовина тверда 1,65 хв 668/670 речовина тверда 1,65 хв 646/648/650 речовина тверда 1,39 хв 534 речовина смолоподібна 1,41 хв 596/598/600 речовина 90-92 °C 1,41 хв 552/554/556 тверда 1,38 хв 534 речовина тверда 1,50 хв 602/604/606 речовина тверда 1,47 хв 674/676/678/680 речовина тверда 1,45 хв 586/588 речовина тверда 1,47 хв 586/588 речовина тверда 1,29 хв 502 речовина тверда 1,34 хв 562 речовина UA 101046 C2 Таблиця A: 4 R 5 R F H H F 2-хлорпірид-4-ил -CH=CH2 F H F A25 A26 A27 A28 A29 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил H H H H H H H H H H -CF3 H Cl -CH3 Br A30 2-хлорпірид-4-ил F H F A31 A32 H H H H Cl -CF3 Br F H F 87-89 °C 1,53 хв 630/632/634/636 -OCF3 F -CF3 -CF3 -SCF3 Cl -CN Cl Cl H Cl H Cl F H H H H H H H F F -OCH3 F F F F -CF3 H H F -CF3 H H F -CF3 -CF3 -CF3 H -CF3 H H H -OCF3 H H H H H H A48 2-хлорпірид-4-ил -CF3 H H -CN -OCF3 Br F -C≡CH циклопропіл 64-68 °C 49-53 °C 150-152 °C 165-167 °C 59-63 °C 71-73 °C 162-165 °C спінена речовина спінена речовина 97-98 °C 80-81 °C 80-81 °C 104-105 °C 80-81 °C 1,54 хв 618/620/622 1,43 хв 552/554 1,44 хв 580/582 1,52 хв 602/604 1,52 хв 600/602 1,43 хв 568/570/572/574 1,36 хв 543/545 A43 A44 A45 A46 A47 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2,6-дихлорпірид-4ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 5-хлор-2-фторпірид4-ил 2-хлор-5-фторпірид4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил F F F F F циклопропіл -CF3 -CF3 Агрегатний стан/ Т. пл.* тверда речовина тверда речовина тверда речовина >250 °C 167-171 °C -CF3 H H -CF3 H -CF3 Спол. № R A23 2,6-дихлорпірид-4ил A24 A33 A34 A35 A36 A37 A38 A39 A40 A41 A42 A49 A50 A51 A52 A53 1 2-хлор-6пропілпірид-4-ил 2-хлор-6-етилпірид4-ил 3трифторметилпірид4-ил пірид-4-ил 2,5-дифторпірид-4ил R 3 R 8 ВЕРХ (ЧУ) МС (ІЕ+) 1,42 хв 552 1,42 хв 544/546 1,28 хв 1,15 хв 1,21 хв 1,17 хв 1,25 хв 568,2 500,2 534,2 514,2 578,1 1,46 хв 558/560 1,50 хв 1,54 хв 584/586 618/620 1,43 хв 586/588 1,43 хв 586/588 1,39 хв 1,49 хв 1,52 хв 1,46 хв 1,48 хв 575/577 634/635/636 628/630 584/586 574/576 1,55 хв 590/592 F 1,44 хв 610 H F 1,37 хв 596 H H F 1,18 хв 602 -CF3 H H F 1,04 хв 534 -CF3 H H F 1,39 хв 581 82-83 °C 212 °C *Т. пл. = температура плавлення Приклад 2 Цей приклад ілюструє одержання 2-хлор-N-{4,5-дифтор-2-[1-(4'-фторбіфеніл-4-ілметил)-1оксипіперидин-4-іл]феніл}ізонікотинаміду (сполука B1 в таблиці B). 15 UA 101046 C2 O + N F F NH F Cl O N 5 10 Розчин 3-хлорпероксибензойної кислоти (21,6 мг) в дихлорметані (1 мл) при -40 °C по краплям додавали до розчину 2-хлор-N-{4,5-дифтор-2-[1-(4'-фторбіфеніл-4-ілметил)-піперидин4-іл]феніл}ізонікотинаміду (приклад 1) (47 мг) в дихлорметані (5 мл). Розчин перемішували при 40 °C протягом 1 год., потім нагрівали до 0 °C і реакцію зупиняли шляхом додавання водного розчину карбонату калію (10 мас. %) (3 мл). Суміш 3 рази екстрагували дихлорметаном. Об'єднані органічні екстракти сушили над сульфатом натрію та концентрували у вакуумі і 1 одержували шукану сполуку у вигляді аморфної твердої речовини. МС (ІЕ+) 552/554 (MH+); H ЯМР (400 МГц, MeOD) 1,80 (m, 2H), 2,40 (m, 2H), 2,93 (m, 1H), 3,23 (m, 2H), 3,48 (m, 2H), 4,44 (s, 2H), 7,18 (t, 2H), 7,28 (dd, 1H), 7,43 (dd, 1H), 7,64 (m, 6H), 7,83 (d, 1H), 7,95 (s, 1H), 8,56 (d, 1H). Наведені нижче сполуки одержували за методиками, аналогічними описаній у прикладі 2: Сполуки формули (Ib) O + N 3 R (Ib) 4 R 8 NH R 5 R 1 R O Таблиця B: Спол. № B1 B2 B3 B4 B5 B6 B7 B8 B9 B10 B11 R 1 2-хлорпірид-4ил 2-хлорпірид-4ил 2-хлорпірид-4ил 2-хлорпірид-4ил 2-хлорпірид-4ил 2-хлорпірид-4ил 2-хлорпірид-4ил 2-фторпірид-4ил 2,6дихлорпірид-4ил 2-хлорпірид-4ил 2-хлорпірид-4ил R 3 R 4 R 5 R 8 Агрегатний стан/Т. пл. тверда речовина тверда речовина тверда речовина тверда речовина тверда речовина тверда речовина тверда речовина тверда речовина ВЕРХ (ЧУ) МС (ІЕ+) 1,40 хв 552 1,52 хв 584 1,48 хв 570 1,41 хв 534 1,47 хв 600 1,48 хв 584 1,41 хв 582/584 1,38 хв 566 F F H F H -CF3 H F F F F F F H H F -OCF3 H H F -CF3 H H F -OCHF2 H H F -OCHF2 H H F -OCHF2 H H F тверда речовина 1,60 хв 616/618/620 Br -CF3 H F 192-194 °C 1,54 хв 662/664/666 Br F H F 194-196 °C 1,48 хв 612/614/616 16 UA 101046 C2 Таблиця B: Спол. № B12 B13 B14 B15 B16 B17 B18 B19 B20 B21 B22 B23 B24 B25 B26 B27 B28 B29 B30 R 1 R 3 R 4 2-хлорпірид-4Cl F ил 2-хлорпірид-4Cl H ил 2-хлорпірид-4Cl -CF3 ил 2-хлорпірид-4-CF(CF3)2 H ил 2-хлорпірид-4Br F ил 2-хлорпірид-4F -CF3 ил 2-хлорпірид-4-CF3 F ил 2-хлорпірид-4H Cl ил 2-хлорпірид-4-CH=CH2 F ил 2-хлорпірид-4-CF3 H ил 2,6дихлорпірид-4Br F ил 2-хлорпірид-4циклоF ил пропіл 2-хлорпірид-4F Cl ил 2-хлорпірид-4-CF3 Cl ил 2-хлорпірид-4-SCF3 H ил 2-хлорпірид-4Cl Cl ил 5-хлор-2-CF3 H фторпірид-4-ил 2-хлор-5-CF3 H фторпірид-4-ил 2-хлорпірид-4-CN F ил Агрегатний стан/Т. пл. ВЕРХ (ЧУ) МС (ІЕ+) 183-185 °C 1,44 хв 568/570/572 1,42 хв 550 1,54 хв 618/620/622 173-176 °C 1,62 хв 684/686 F 197-199 °C 1,51 хв 690/692/694/696 H F 198-200 °C 1,49 хв 602/604 H F 178-180 °C 1,50 хв 602/604 H F тверда речовина 1,43 хв 550 H F 240-242 °C 1,46 хв 560/562 H -CF3 170-172 °C 1,59 хв 634/636 H F 209-213 °C 1,57 хв 648/650/652 H F 191-195 °C 1,50 хв 574/576 H F 184-187 °C 1,48 хв 568/570/572 H F 187-190 °C 1,58 хв 618/620/622 H F 144-147 °C 1,52 хв 616/618 H F 195-197 °C 1,48 хв 584/586/588/590 H F 173-175 °C 1,47 хв 602/604 H F 184-186 °C 1,48 хв 602/604 H F 175-179 °C 1,44 хв 559/561 5 R H F H F H F H F Br R 8 тверда речовина тверда речовина Приклад 3 Цей приклад ілюструє одержання 2-хлор-N-[1'-(4'-фторбіфеніл-4-ілметил)-6-трифторметил1',2',3',4',5',6'-гексагідро-[2,4'] біпіридиніл -3-іл]ізонікотинаміду (сполука C1 в таблиці C). N F3C N NH F Cl O N 5 Стадія A: Розчин 3-аміно-2-хлор-6-трифторметилпіридину (0,890 г), трет-бутилового ефіру 4(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-ил)-3,6-дигідро-2H-піридин-1-карбонової кислоти (1,4 17 UA 101046 C2 5 10 15 20 25 30 35 40 45 50 55 г) (одержували так, як це описано у WO 2006/003494) и тетракіс(трифенілфосфін)паладію (0,200 г) в 1,2-диметоксиетані (45 мл) обробляли водним розчином фосфату калію (1,1 M) (1,92 г). Реакційну суміш перемішували при 80 °C протягом 3 год. Обробка водного розчину етилацетатом давала залишок, який очищали за допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 1:1) і одержували трет-бутиловий ефір 3-аміно-6-трифторметил3',6'-дигідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (1,5 г) у вигляді білої твердої речовини. 1 МС (ІЕ+) 288 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,50 (s, 9H), 2,61 (m, 2H), 3,67 (t, 2H), 4,10 (m, 2H), 4,21 (s, 2H), 6,11 (s, 1H), 7,03 (d, 1H), 7,33 (d, 1H). Стадія B: Сполуку, одержану на стадії A (1 г), розчиняли в етанолі (40 мл) і після дегазації додавали паладій на деревному вугіллі (10 мас. %) (100 мг). Реакційну суміш перемішували в атмосфері водню при температурі навколишнього середовища протягом 2 днів. Фільтрування через целіт® давало трет-бутиловий ефір 3-аміно-6-трифторметил-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (1 г) у вигляді білої твердої речовини. МС (ІЕ+) 290/292 1 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,85 (m, 4H), 2,77 (m, 1H), 2,88 (m, 2H), 3,97 (s, 2H), 4,24 (m, 2H), 6,97 (d, 1H), 7,32 (d, 1H). Стадія C: Розчин сполуки, одержаної на стадії C (1 г), в толуолі (40 мл) обробляли N, Nдіізопропілетиламіном (1,05 мл) і потім 2-хлорізонікотиноїлхлоридом. 2Хлорізонікотиноїлхлорид одержували з 2-хлорізонікотинової кислоти (0,496 г) та оксалілхлориду (0,346 мл) в дихлорметані (40 мл). Реакційну суміш перемішували при температурі навколишнього середовища протягом 2 год., виливали в насичений водний розчин гідрокарбонату натрію, екстрагували етилацетатом, промивали водою, сушили над сульфатом натрію і потім концентрували у вакуумі. Залишок очищали за допомогою хроматографії на силікагелі (елюент: гексан/етилацетат 1:1) і одержували трет-бутиловий ефір 3-[(2-хлорпіридин4-карбоніл)аміно]-6-трифторметил-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової 1 кислоти (1,1 г). МС (ІЕ+) 485/487 (MH+), 429/431 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,47 (s, 9H), 1,79 (m, 2H), 1,96 (m, 2H), 2,88 (m, 2H), 2,95 (m, 1H), 4,25 (m, 2H), 7,61 (d, 1H), 7,66 (m, 1H), 7,79 (s, 1H), 8,05 (s, 1H), 8,32 (d, 1H), 8,64 (d, 1H). Стадія D: Розчин сполуки, одержаної на стадії C (300 мг), в дихлорметані (15 мл) обробляли трифтороцтовою кислотою (1,2 мл) при температурі навколишнього середовища протягом 1 год. Випарювання розчинника і сушка твердої речовини у високому вакуумі давали 2-хлор-N-(6трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл)ізонікотинамідтрифторацетат. Вільне основу одержували за допомогою лужної екстракції (етилацетат, насичений водний розчин гідрокарбонату). Стадія E: Методика A: Суміш 2-хлор-N-(6-трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3іл)ізонікотинаміду (150 мг), 4-хлорметил-4'-фторбіфенілу (одержували так, як це описано у WO 2003/084916) (68 мг) і N, N-діізопропілетиламіну (0,21 мл) в ацетонітрилі (10 мл) перемішували при температурі навколишнього середовища протягом 16 год. Розчинник випарювали і залишок очищали за допомогою хроматографії на силікагелі (елюент: етилацетат) і одержували шукану сполуку (79 мг). Методика B: До суміші 2-хлор-N-(6-трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3іл)-ізонікотинаміду (3 г) (одержували так, як це описано у WO 2006/003494) і 4'-фтор[1,1'біфеніл]-4-карбоксальдегіду (1,24 г) в тетрагідрофурані (120 мл) при температурі навколишнього середовища додавали (триацетокси)борогідрид натрію (2 г). Реакційну суміш перемішували при температурі навколишнього середовища протягом 16 год. Реакцію зупиняли шляхом додавання насиченого водного розчину гідрокарбонату натрію. Суміш екстрагували етилацетатом. Органічний екстракт сушили над сульфатом натрію і концентрували у вакуумі. Залишок очищали за допомогою хроматографії на силікагелі (елюент: етилацетат) і одержували шукану сполуку у вигляді твердої речовини (2,4 г). 2-Хлор-N-[1'-(4'-фторбіфеніл-4-ілметил)-6-трифторметил-1',2',3',4',5',6'-гексагідро1 [2,4']біпіридиніл-3-іл]-ізонікотинамід: Т. пл. 63-66 °C; МС (ІЕ+) 569/571 (MH+); H ЯМР (400 МГц, CDCl3) 1,80 (m, 2H), 2,18 (m, 4H), 2,79 (m, 1H), 3,10 (m, 2H), 3,59 (s, 2H), 7,11 (m, 2H), 7,39-7,61 (m, 8H), 7,76 (s, 1H), 7,87 (bs, 1H), 8,45 (d, 1H), 8,64 (d, 1H). Приклад 4 Цей приклад ілюструє одержання 2-хлор-N-[6-хлор-5-фтор-1'-(4'-фторбіфеніл-4-ілметил)1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C17 в таблиці C). 18 UA 101046 C2 N Cl N F NH F Cl O N 5 10 15 20 25 30 35 40 45 50 Шукану сполуку одержували з 2-хлор-N-(6-хлор-5-фтор-1',2',3',4',5',6'-гексагідро[2,4']біпіридиніл-3-іл)ізонікотинаміду, так як це описано на стадії E прикладу 3. 2-Хлор-N-(6-хлор5-фтор-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл)ізонікотинамід одержували наступним чином: Стадія A: Дегазований розчин 2-хлор-5-фтор-3-амінопіридину (3,5 г), трет-бутилового ефіру 4-(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)-3,6-дигідро-2H-піридин-1-карбонової кислоти (8,89 г) (одержували так, як це описано у WO 2006/003494) та біс(трифенілфосфін)паладій(II)хлориду (0,84 г) в діоксані (157 мл) обробляли дегазованим розчином карбонату натрію (7,6 г) у воді (72 мл). Реакційну суміш перемішували при кип'ятінні зі зворотним холодильником протягом 1 год., охолоджували до температури навколишнього середовища і розчинник випарювали у вакуумі. Залишок розбавляли етилацетатом, промивали водою та розсолом, сушили над сульфатом натрію і концентрували у вакуумі. Хроматографія на силікагелі (елюент: циклогексан/етилацетат 8:2) давала трет-бутиловий ефір 3-аміно-5-фтор3',6'-дигідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (4,6 г) у вигляді твердої речовини. МС 1 (ІЕ+) 294 (MH+), 238 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 2,53 (m, 2H), 3,64 (t, 2H), 3,99 (m, 2H), 4,08 (m, 2H), 5,99 (m, 1H), 6,70 (dd, 1H), 7,85 (d, 1H). Стадія B: Сполуку, одержану на стадії A (4,4 г), розчиняли в етанолі (170 мл). Додавали форміат амонію (9,4 г) і потім паладій на деревному вугіллі (10 мас. %) (1 г). Реакційну суміш перемішували при температурі навколишнього середовища протягом 90 хв, фільтрували через целіт® і розчинник видаляли у вакуумі та одержували трет-бутиловий ефір 3-аміно-5-фтор3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (4,3 г) у вигляді твердої речовини. 1 МС (ІЕ+) 296 (MH+), 240 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,45 (s, 9H), 1,77 (m, 4H), 2,69 (m, 1H), 2,81 (m, 2H), 4,23 (m, 4H), 6,67 (dd, 1H), 7,85 (d, 1H). Стадія C: Розчин сполуки, одержаної на стадії B (3,4 г), і N-хлорсукциніміду (1,72 г) в Nметилпіролідиноні (35 мл) перемішували при 110 °C протягом 1 год. Реакційну суміш охолоджували до температури навколишнього середовища, виливали у воду і кілька разів екстрагували діетиловим ефіром. Об'єднані органічні шари промивали розведеним водним розчином хлористоводневої кислоти і водою, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: циклогексан/етилацетат 8:2) давала трет-бутиловий ефір 3-аміно-5-фтор-6-хлор-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'карбонової кислоти (2,9 г) у вигляді твердої речовини. МС (ІЕ+) 330 (MH+), 274/276 (M-ізопрен); 1 H ЯМР (400 МГц, CDCl3) 1,47 (s, 9H), 1,77 (m, 4H), 2,64 (m, 1H), 2,81 (m, 2H), 3,78 (m, 2H), 4,25 (m, 2H), 6,76 (d, 1H). Стадія D: Розчин сполуки, одержаної на стадії C (2 г), в дихлорметані (100 мл) обробляли гідрокарбонатом натрію (5 г) і потім 2-хлорізонікотиноїлхлоридом. 2-Хлорізонікотиноїлхлорид одержували з 2-хлорізонікотинової кислоти (1,24 г) і оксалілхлориду (0,72 мл) в дихлорметані (100 мл). Реакційну суміш перемішували при температурі навколишнього середовища протягом 18 год., виливали в насичений водний розчин гідрокарбонату натрію, екстрагували дихлорметаном, промивали водою, сушили над сульфатом натрію і потім концентрували у вакуумі та одержували трет-бутиловий ефір 6-хлор-3-[(2-хлорпіридин-4-карбоніл)аміно]-5-фтор3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (2,2 г). МС (ІЕ+) 369/371 (MH+BOC). Стадія E: Розчин сполуки, одержаної на стадії D (366 мг), в дихлорметані (10 мл) обробляли трифтороцтовою кислотою (0,6 мл) при температурі навколишнього середовища протягом 1 год. 30 хв. Випарювання розчинника і осадження із диетилового ефіру давали 2-хлор-N-(6-хлор5-фтор-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл)ізонікотинамідтрифторацетат. Приклад 5 Цей приклад ілюструє одержання 2-хлор-N-[5,6-дихлор-1'-(4'-фторбіфеніл-4-ілметил)1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C2 в таблиці C). 19 UA 101046 C2 N Cl N Cl NH F Cl O N 5 10 15 Шукану сполуку одержували з 2-хлор-N-(5,6-дихлор-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл3-іл)ізонікотинаміду за методиками, аналогічними описаним в прикладі 4, використовуючи в якості вихідної речовини 2,5-дихлор-3-амінопіридин замість 2-хлор-5-фтор-3-амінопіридину. Замість стадії B використовували наведену нижче методику: Стадія B': Проміжний тетрагідропіридин, одержаний на стадії A (3 г), гідрували в метанолі (350 мл) в присутності 1,1'-біс(діізопропілфосфіно)фероцен(1,5циклооктадієн)родій(I)тетрафторборату (46 мг) при 80 °C і тиску водню, що дорівнює 100 бар, протягом 21 год. і одержували трет-бутиловий ефір 3-аміно-5-фтор-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти. Альтернативно, останній проміжний продукт можна одержати так, як це описано в WO 2006/003494, за реакцією сполучення Негіші 2,5-дихлор-3-амінопіридину і трет-бутилового ефіру 4-йодпіперидин-1-карбонової кислоти. Приклад 6 Цей приклад ілюструє одержання N-[6-бром-5-фтор-1'-(4'-фторбіфеніл-4-ілметил)1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]-2-хлорізонікотинаміду (сполука C5 в таблиці C). N Br N F NH F Cl O N 20 Шукану сполуку одержували за методиками, аналогічними описаним у прикладі 4, шляхом заміни на стадії C N-хлорсукциніміду на N-бромсукцинімід. Приклад 7 Цей приклад ілюструє одержання 2-хлор-N-[6-хлор-1'-(4'-фторбіфеніл-4-ілметил)-5-метил1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C16 в таблиці C). N Cl N N F3C F Cl O N 25 30 Шукану сполуку одержували за методиками, аналогічними описаним у прикладі 4, використовуючи в якості вихідної речовини 3-аміно-2-хлор-5-трифторметилпіридин (одержували так, як це описано у EP 178260, EP 272824) замість 2-хлор-5-фтор-3-амінопіридину. Альтернативно, останній проміжний продукт можна одержати безпосередньо за реакцією сполучення Судзукі 3-аміно-2,6-дихлор-5-трифторметилпіридину і трет-бутилового ефіру 4(4,4,5,5-тетраметил-[1,3,2]діоксаборолан-2-іл)-3,6-дигідро-2H-піридин-1-карбонової кислоти (одержували так, як це описано у WO 2006/003494) з використанням умов, описаних в прикладі 3, з подальшим гомогенним каталітичним гідруванням так, як це описано в прикладі 5 (стадія B'). 20 UA 101046 C2 5 10 Одержування 3-аміно-2,6-дихлор-5-трифторметилпіридину з 3-аміно-2-хлор-5трифторметилпіридину проводили наступним чином. Розчин 3-аміно-2-хлор-5трифторметилпіридину (5 г) (одержували так, як це описано у EP 178260, EP 272824) та Nхлорсукциніміду (3,7 г) в ацетонітрилі (125 мл) перемішували при температурі навколишнього середовища протягом 16 год. Реакційну суміш виливали у воду, екстрагували етилацетатом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 3:1) давала 3-аміно-2,6-дихлор-5-трифторметилпіридин (3,5 г): МС 1 (ІЕ+) 231/233/235 (MH+); H ЯМР (400 МГц, CDCl3) 4,34 (s, 2H), 7,35 (s, 1H). Приклад 8 Цей приклад ілюструє одержання 2-хлор-N-[6-бром-1'-(4'-фторбіфеніл-4-ілметил)-5-метил1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C15 в таблиці C). N Br N N F3C F Cl O N 15 Шукану сполуку одержували за методиками, аналогічними описаним у прикладі 7, шляхом заміни N-хлорсукциніміду на N-бромсукцинімід. Приклад 9 Цей приклад ілюструє одержання 2-хлор-N-{4,5,6-трихлор-1'-(4'-фторбіфеніл-4-ілметил)1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}ізонікотинаміду (сполука C30 в таблиці C). N Cl N N Cl Cl F Cl O N 20 Шукану сполуку одержували за методиками, аналогічними описаним у прикладі 5, з використанням 2 екв. N-хлорсукциніміду на стадії хлорування (стадія C). Приклад 10 Цей приклад ілюструє одержання 2-хлор-N-{1'-(4'-фторбіфеніл-4-ілметил)-4-фтор-6трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}ізонікотинаміду (сполука C41 в таблиці C). N F3C N F N F Cl O N 25 30 Стадія A: Розчин сполуки, одержаної на стадії B прикладу 3 (10,35 г), і N-хлорсукциніміду (4,4 г) в N-метилпіролідиноні (150 мл) перемішували при температурі навколишнього середовища протягом 2,5 год. Реакційну суміш виливали у воду і кілька разів екстрагували етилацетатом. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 1:1) давала трет-бутиловий ефір 3-аміно-4-хлор-6-трифторметил-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (9,6 г) у вигляді спіненої речовини. МС (ІЕ+) 380/382 21 UA 101046 C2 1 5 10 15 20 25 30 35 (MH+), 324/326 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,85 (m, 4H), 2,82 (m, 3H), 4,24 (m, 2H), 4,41 (br s, 2H), 7,46 (s, 1H). Стадія B: Розчин сполуки, одержаної на стадії A (7,6 г), і трифтороцтової кислоти (61,7 мл) в дихлорметані (380 мл) нагрівали до 55 °C. При цій самій температурі протягом 30 хв повільно додавали водний розчин пероксиду водню (30 мас. %) (23 мл). Реакційну суміш витримували при цій самій температурі протягом ще 2 год. Реакційну суміш виливали у воду і кілька разів екстрагували дихлорметаном. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Залишок повторно розчиняли в дихлорметані (200 мл). Потім додавали ди-трет-бутилдикарбонат (5,4 г) та N,Nдіізопропілетиламін (14,2 мл) і реакційну суміш перемішували протягом 16 год. Реакцію зупиняли водою і суміш екстрагували дихлорметаном. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 5:1) давала трет-бутиловий ефір 4-хлор-3-нітро-6трифторметил-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (4,9 г) у вигляді 1 спіненої речовини. МС (ІЕ+) 410/412 (MH+), 354/356 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,77 (m, 2H), 1,95 (m, 2H), 2,85 (m, 3H), 4,26 (m, 2H), 7,74 (s, 1H). Стадія C: Розчин сполуки, одержаної на стадії B (1,2 г), і висушеної розпиленням фториду калію (339 мг) в диметилсульфоксиді (57 мл) перемішували при 80 °C протягом 1 год. Реакційну суміш виливали у воду і кілька разів екстрагували етилацетатом. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 5:1) давала трет-бутиловий ефір 4фтор-3-нітро-6-трифторметил-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти 1 (0,7 г) у вигляді спіненої речовини. МС (ІЕ+) 338/339 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,79 (m, 2H), 1,94 (m, 2H), 2,79 (m, 2H), 2,99 (m, 1H), 4,26 (m, 2H), 7,51 (d, 1H). Стадія D: Сполуку, одержану на стадії C (1,8 г), розчиняли в етанолі (48 мл) і після дегазації додавали паладій на деревному вугіллі (10 мас. %) (500 мг). Реакційну суміш перемішували в атмосфері водню при температурі навколишнього середовища протягом 1 дня. Фільтрування через целіт® давало трет-бутиловий ефір 3-аміно-4-фтор-6-трифторметил-3',4',5',6'-тетрагідро2'H-[2,4']біпіридиніл-1'-карбонової кислоти (1,6 г) у вигляді білої твердої речовини. МС (ІЕ+) 1 364/365 (MH+), 308/309 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,85 (m, 4H), 2,86 (m, 3H), 3,90 (br s, 2H), 4,25 (m, 2H), 7,22 (d, 1H). Потім сполуку, одержану на стадії D, обробляли за методиками, описаними у прикладі 3 (стадія C та стадія D), і одержували шукану сполуку. Приклад 11 Цей приклад ілюструє одержання 2-хлор-N-{1'-(4'-фторбіфеніл-4-ілметил)-6-фтор-5трифторметил-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}ізонікотинаміду (сполука C31 в таблиці C). N F N NH F3C F Cl O N 40 45 50 Стадія A: До розчину проміжного трет-бутилового ефіру 3-аміно-6-хлор-5-трифторметил3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (4 г), одержаного так, як це описано у прикладі 8, за рекцією сполучення Судзукі з подальшим каталітичним гідруванням, в дихлорметані (200 мл), додавали трифтороцтову кислоту (32 мл). Розчин нагрівали до 55 °C і при цій самій температурі протягом 30 хв повільно додавали водний розчин пероксиду водню (30 мас. %) (10,5 мл). Реакційну суміш витримували при цій самій температурі протягом ще 90 хв, потім виливали у воду і кілька разів екстрагували дихлорметаном. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Залишок повторно розчиняли в дихлорметані (110 мл). Потім додавали ди-трет-бутилдикарбонат (3,5 г) та N,N-діізопропілетиламін (7,6 мл) і реакційну суміш перемішували при температурі навколишнього середовища протягом 16 год. Реакцію зупиняли водою та суміш екстрагували дихлорметаном. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 10:1) 22 UA 101046 C2 5 10 15 давала трет-бутиловий ефір 6-хлор-3-нітро-5-трифторметил-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (3 г) у вигляді спіненої речовини. МС (ІЕ+) 410/412 (MH+), 1 354/356 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,49 (s, 9H), 1,89 (m, 4H), 2,84 (m, 2H), 3,50 (m, 1H), 4,29 (m, 2H), 8,48 (s, 1H). Стадія B: Розчин сполуки, одержаної на стадії A (2,5 г), і висушеної розпиленням фториду калію (710 мг) в диметилсульфоксиді (120 мл) перемішували при 80 °C протягом 40 хв. Реакційну суміш виливали в суміш води з льодом і кілька разів екстрагували етилацетатом. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 5:1) давала трет-бутиловий ефір 6-фтор-3-нітро-5-трифторметил-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'1 карбонової кислоти (1,13 г) у вигляді спіненої речовини. МС (ІЕ+) 338/339 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,48 (s, 9H), 1,90 (m, 4H), 2,84 (m, 2H), 3,53 (m, 1H), 4,29 (m, 2H), 8,57(d, 1H). Потім сполуку, одержану на стадії B, обробляли за методиками, описаними у прикладі 3 (стадія B, стадія C та стадія D), і одержували шукану сполуку. Приклад 12 Цей приклад ілюструє одержання 2-хлор-N-{1'-(4'-фторбіфеніл-4-ілметил)-5,6-дифтор1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}ізонікотинаміду (сполука C25 в таблиці C). N F N F NH F Cl O N 20 25 30 35 40 45 Стадія A: До розчину сполуки, отриманої на стадії C прикладу 4 (5 г), і трифтороцтової кислоти (46,5 мл) у хлороформі (324 мл) при 50 °C по краплям додавали водний розчин пероксиду водню (30 мас. %) (15,7 мл). Реакційну суміш перемішували при 55 °C протягом 1 год., охолоджували до температури навколишнього середовища і розбавляли дихлорметаном. Розчин промивали водою і розсолом, сушили над сульфатом натрію і концентрували у вакуумі та одержували проміжний продукт, 6-хлор-5-фтор-3-нітро-1',2',3',4',5',6'-гексагідро[2,4']біпіридиніл (4 г), у вигляді масла. МС (ІЕ+) 260 (MH+). Проміжний продукт обробляли дитрет-бутилдикарбонатом (4 г) і триетиламіном (6,3 мл) в дихлорметані (250 мл) протягом 12 год. і після обробки водою одержували трет-бутиловий ефір 6-хлор-5-фтор-3-нітро-3',4',5',6'тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (4,3 г) у вигляді червоного масла. МС (ІЕ+) 360 (MH+), 345 (M-ізопрен + CH3CN), 305 (M-ізопрен), 260 (MH+-BOC). Стадія B: Продукт, одержаний на стадії A (3,3 г), висушений розпиленням фториду калію (1,06 г) і тетрафенілфосфонійброміду (7,6 г) розчиняли в ацетонітрилі (23 мл) і реакційну суміш кип'ятили зі зворотним холодильником протягом 8 год. Реакційну суміш охолоджували до температури навколишнього середовища, білу тверду речовину видаляли фільтруванням і фільтрат концентрували у вакуумі. Хроматографія на силікагелі (елюент: циклогексан/етилацетат 9:1) давала трет-бутиловий ефір 5,6-дифтор-3-нітро-3',4',5',6'тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (0,85 г): МС (ІЕ+) 329 (M-ізопрен+CH3CN), 1 288 (M-ізопрен), 244 (MH+-BOC); H ЯМР (400 МГц, CDCl3) 1,45 (s, 9H), 1,80 (m, 4H), 2,79 (m, 1H), 3,43 (m, 2H), 4,22 (m, 2H), 8,13 (t, 1H). Стадія C: Продукт, одержаний на стадії B (694 мг), гідрували в метанолі при температурі навколишнього середовища і одержували трет-бутиловий ефір 3-аміно-5,6-дифтор-3',4',5',6'тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (390 мг) у вигляді жовтого масла: МС (ІЕ+) 1 314 (MH+), 258 (M-ізопрен); H ЯМР (400 МГц, CDCl3) 1,45 (s, 9H), 1,75 (m, 4H), 2,70 (m, 1H), 2,80 (m, 2H), 3,90 (m, 2H), 4,23 (m, 2H), 6,90 (t, 1H). Продукт, одержаний на стадії C (313 мг) перетворювали на шуканий продукт за методиками, аналогічними описаним у прикладі 4 (стадія D та стадія E). 23 UA 101046 C2 Приклад 13 Цей приклад ілюструє одержання 2-хлор-N-{1'-(4'-фторбіфеніл-4-ілметил)-6-дифторметил1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}ізонікотинаміду (сполука C6 в таблиці C). N F F N F NH Cl O N 5 10 15 20 25 30 35 40 Стадія A: 6-(Хлордифторметил)-нікотинонітрил (35,4 г, одержували так, як це описано у публікації Tetrahedron Letters, 39 (43), 1998, 7965) суспендували у концентрованій хлористоводневій кислот (245 мл) і перемішували при 110 °C протягом 16 год. Реакційну суміш охолоджували до температури навколишнього середовища і додавали суміш води з льодом. Білу тверду речовину відокремлювали фільтруванням і сушили у високому вакуумі та 1 одержували 6-(хлордифторметил)нікотинову кислоту (36 г). H ЯМР (400 МГц, ДМСО-d6) 3,30 (br s, 1H), 8,00 (dd, 1H), 8,51 (dd, 1H), 9,17 (d, 1H). Стадія B: В атмосфері азоту готували розчин трет-бутанолу (100 мл), порошкоподібних молекулярних сит (4 Å) (23 г) і триетиламіну (9,36 мл). Після перемішування при температурі навколишнього середовища протягом 5 хв додавали сполуку, отриману на стадії A (10 г), потім дифенілфосфорилазид (16,3 г). Реакційну суміш кип'ятили зі зворотнім холодильником протягом 3 год. і потім фільтрували через целіт®. Реакційну суміш виливали у воду і кілька разів екстрагували діетиловим ефіром. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 5:1) давала трет-бутиловий ефір [6-(хлордифторметил)-піридин-3-іл]1 карбамінової кислоти (10,6 г). МС (ІЕ+) 279/281 (MH+); H ЯМР (400 МГц, CDCl3) 1,55 (s, 9H), 7,52 (d, 1H), 8,19 (m, 1H), 8,47 (d, 1H). Стадія C: Сполуку, отриману на стадії B (5,57 г), розчиняли в етанолі (110 мл) і після дегазації додавали паладій на деревному вугіллі (10 мас. %) (1 г). Реакційну суміш перемішували в атмосфері водню при температурі навколишнього середовища протягом 5 год. Фільтрування через целіт® давало трет-бутиловий ефір (6-дифторметилпіридин-31 іл)карбамінової кислоти (4,8 г) у вигляді спіненої речовини. МС (ІЕ+) 245/246 (MH+); H ЯМР (400 МГц, CDCl3) 1,54 (s, 9H), 7,15 (t, 1H), 7,91 (m, 1H), 9,03 (m, 1H), 9,33 (m, 2H). Стадія D: Розчин сполуки, одержаної на стадії C (5,9 г), в дихлорметані (80 мл) обробляли трифтороцтовою кислотою (3,7 мл) при температурі навколишнього середовища протягом 12 год. Реакційну суміш виливали в насичений водний розчин гідрокарбонату натрію і кілька разів промивали дихлорметаном. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: 1 гексан/етилацетат 1:1) давала 6-дифторметилпіридин-3-іламін (2,1 г): H ЯМР (400 МГц, CDCl3) 3,98 (br s, 2H), 6,56 (t, 1H), 7,03 (dd, 1H), 7,40 (d, 1H), 8,06 (d, 1H). Стадія E: Розчин сполуки, одержаної на стадії D (2,1 г), і N-бромсукциніміду (2,56 г) в ацетонітрилі (50 мл) перемішували при 0 °C протягом 10 хв. Реакційну суміш виливали у воду і кілька разів екстрагували етилацетатом. Об'єднані органічні шари промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 1:1) давала 2-бром-6-дифторметилпіридин-3-іламін (2,5 г) у вигляді твердої 1 речовини. МС (ІЕ+) 223/225 (MH+); H ЯМР (400 МГц, CDCl3) 4,38 (br s, 2H), 6,52 (t, 1H), 7,08 (d, 1H), 7,41 (d, 1H). Потім сполуку, отриману на стадії E, обробляли за методиками, описаними у прикладі 4 (стадія A, стадія В, стадія C та стадія D), і одержували шукану сполуку. 24 UA 101046 C2 Приклад 14 Цей приклад ілюструє одержання 2-хлор-N-{1'-(4'-фторбіфеніл-4-ілметил)-6-дифторметокси1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл}ізонікотинаміду (сполука C40 в таблиці C). F F N N O NH F Cl O N 5 10 15 20 25 30 Шукану сполуку одержували з 2-бром-6-дифторметоксипіридин-3-іламіну за методиками, описаними в прикладі 4. 2-Бром-6-дифторметоксипіридин-3-іламін одержували наступним чином: Стадія A: 2-Гідрокси-5-нітропіридин (5 г) обробляли хлордифторацетатом натрію (11,5 г) в киплячому ацетонітрилі (186 мл) протягом 2 днів. Розчинник випарювали, залишок виливали в етилацетат, промивали розсолом, сушили над сульфатом натрію і потім концентрували у вакуумі. Хроматографія на силікагелі (елюент: гексан/етилацетат 1:1) давала 2-дифторметокси5-нітропіридин (1 г, 15 %) і 1-дифторметил-5-нітро-1H-піридин-2-он (90 мг, 1,5 %). 21 Дифторметокси-5-нітропіридин: МС (ІЕ+) 191 (MH+); H ЯМР (400 МГц, CDCl3) 7,05 (d, 1H), 7,51 (t, 1H), 8,53 (dd, 1H), 9,09 (d, 1H). 1-Дифторметил-5-нітро-1H-піридин-2-он: МС (ІЕ+) 191 (MH+); 6,65 (d, 1H), 7,63 (t, 1H), 8,14 (dd, 1H), 8,73 (d, 1H). Стадія B: 2-Дифторметокси-5-нітропіридин, одержаний на стадії A (1,6 г), обробляли залізом (5 г) та концентрованою хлористоводновою кислотою (0,23 мл) в етанолі (15 мл) і воді (2,5 мл) при 80 °C протягом 20 хв. Фільтрування через целіт® і випарювання розчинника давало 61 дифторметоксипіридин-3-іламін (1,4 г) у вигляді помаранчевої твердої речовини. H ЯМР (400 МГц, CDCl3) 3,51 (br s, 2H), 6,89 (d, 1H), 7,23 (d, 1H), 7,44 (dd, 1H), 7,80 (d, 1H). Стадія C: 6-Дифторметоксипіридин-3-іламін, одержаний на стадії B (1,36 г), обробляли Nбромсукцинімідом (1,51 г) в ацетонітрилі протягом 10 хв. Розчин виливали у воду, екстрагували етилацетатом, органічний шар сушили над сульфатом натрію і концентрували у вакуумі. Хроматографія на силікагелі (елюент: циклогексан/етилацетат 7:3) давала 2-бром-61 дифторметоксипіридин-3-іламін у вигляді червоного масла. H ЯМР (400 МГц, CDCl3) 3,95 (br s, 2H), 6,72 (d, 1H), 7,07 (d, 1H), 7,24 (dd, 1H). Приклад 15 Цей приклад ілюструє одержання 2-хлор-N-[5-хлор-1'-(4'-фторбіфеніл-4-ілметил)-6-(2,2,2трифторетокси)-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C9 в таблиці C). F3C N O N NH Cl F Cl O N 35 40 Шукану сполуку одержували з 2-бром-5-хлор-6-трифторетоксипіридин-3-іламіну за методиками, описаними в прикладі 5 (без проведення стадії C). 2-Бром-5-хлор-6трифторетоксипіридин-3-іламін одержували наступним чином: Стадія A: Розчин 2,3-дихлор-5-нітропіридину (5 г, Synthesis, 1990 (6), 499-501), 2,2,2трифторетанолу (2,6 г) і карбонату калію (5,4 г) в N, N-диметилформаміді (50 мл) перемішували при 80 °C протягом 1 год. Реакційну суміш виливали у воду із льодом. Осад відокремлювали фільтруванням та сушили у високому вакуумі і одержували 3-хлор-5-нітро-2-(2,2,2трифторетокси)-піридин (5,65 г). Стадія B: 3-Хлор-5-нітро-2-(2,2,2-трифторетокси)піридин (5,39 г), одержаний на стадії A, відновлювали з використанням заліза (13,6 г) та концентрованої хлористоводневої кислоти (0,73 мл) в етанолі (6,5 мл) і воді (1 мл) при 80 °C протягом 1 год. Фільтрування через целіт® і 25 UA 101046 C2 5 10 випарювання розчинника з подальшою хроматографією на силікагелі (елюент: циклогексан/етилацетат 9:1) давали 3-хлор-5-аміно-2-(2,2,2-трифторетокси)піридин (3,1 г). Стадія C: 3-Хлор-5-аміно-2-(2,2,2-трифторетокси)піридин (3,05 г), одержаний на стадії B, бромували N-бромсукцинімідом (2,4 г) в ацетонітрилі (68 мл), так як це описано в прикладі 14, стадія C, і одержували 2-бром-5-хлор-6-трифторетоксипіридин-3-іламін (4,12 г) у вигляді + + 1 червоного масла. МС (ІЕ+) 305/307/309 (MH ); 346/348/350 (MH + CH3CN); H ЯМР (400 МГц, CDCl3) 3,80 (br s, 2H), 4,65 (q, 2H), 7,10 (s, 1H). Приклад 16 Цей приклад ілюструє одержання 2-хлор-N-[1'-(4'-фторбіфеніл-4-ілметил)-6-метокси1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C10 в таблиці C). N O N NH F Cl O N 15 Шукану сполуку одержували з 2-хлор-6-метоксипіридин-3-іламіну за методиками, описаними в прикладі 3. Приклад 17 Цей приклад ілюструє одержання 2-хлор-N-[1'-(4'-фторбіфеніл-4-ілметил)-6-вініл1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C11 в таблиці C). N N N F Cl O N 20 25 30 Шукану сполуку одержували з трет-бутилового ефіру 3-аміно-6-вініл-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти за методиками, описаними в прикладі 3, стадії C-E. Третбутиловий ефір 3-аміно-6-вініл-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти одержували наступним чином: Розчин трет-бутилового ефіру 3-аміно-6-бром-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'карбонової кислоти (0,49 г, одержували з 3-аміно-2-бромпіридину за методиками, описаними в прикладі 6, стадії A-C), трибутилвінілолова (0,36 г) і тетракіс(трифенілфосфін)паладію (0,035г) в толуолі (20 мл) кип'ятили зі зворотнім холодильником протягом 3 год. Реакційну суміш охолоджували до температури навколишнього середовища і розчинник видаляли у вакуумі. Залишок очищали за допомогою хроматографії на силікагелі (елюент: циклогексан/етилацетат 1:1) і одержували трет-бутиловий ефір 3-аміно-6-вініл-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл+ 1 1'-карбонової кислоти (0,32 г) у вигляді жовтої твердої речовини. МС (ІЕ+) 443/445 (MH ); H ЯМР (400 МГц, CDCl3) 1,40 (s, 9H), 1,70 (m, 2H), 1,90 (m, 2H), 2,75 (m, 2H), 2,80 (m, 1H), 4,15 (m, 2H), 5,4 (d, 1H), 6,2 (d, 1H), 6,7 (dd, 1H), 7,15 (d, 1H), 7,6 (d, 1H), 7,7 (s, 1H), 7,8 (m, 1H), 7,9 (s, 1H), 8,5 (d, 1H). 26 UA 101046 C2 Приклад 18 Цей приклад ілюструє одержання 2-хлор-N-[5-хлор-6-циклопропіл-1'-(4'-фторбіфеніл-4ілметил)-1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C13 в таблиці C). N N N Cl F Cl O N 5 10 15 20 25 Шукану сполуку одержували з трет-бутилового ефіру 3-аміно-5-хлор-6-циклопропіл-3',4',5',6'тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти за методиками, описаними в прикладі 3, стадії C-E. Трет-бутиловий ефір 3-аміно-5-хлор-6-циклопропіл-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти одержували наступним чином: Розчин трет-бутилового ефіру 3-аміно-5-хлор-6-бром-3',4',5',6'-тетрагідро-2'H[2,4']біпіридиніл-1'-карбонової кислоти (0,59 г, одержували за методиками, описаними в прикладі 5, з використанням N-бромсукциніміду замість N-хлорсукциніміду на стадії C), циклопропілборонової кислоти (0,086 г), тетракіс(трифенілфосфін)паладію (0,094 г) і карбонату калію (0,14 г) в 1,2-диметоксиетані (5 мл) і воді (0,2 мл) опромінювали в мікрохвильовій печі при 150 °C протягом 20 хв. Реакційну суміш охолоджували до температури навколишнього середовища, розбавляли етилацетатом, промивали насиченим водним розчином гідрокарбонату натрію, водою і потім розсолом. Органічний шар сушили над сульфатом натрію і розчинник видаляли у вакуумі. Залишок очищали за допомогою хроматографії на силікагелі (елюент: дихлорметан/етилацетат 9:1) і одержували трет-бутиловий ефір 3-аміно-5-хлор-6циклопропіл-3',4',5',6'-тетрагідро-2'H-[2,4']біпіридиніл-1'-карбонової кислоти (0,30 г) у вигляді + 1 жовтої твердої речовини. МС (ІЕ+) 491/493 (MH ); H ЯМР (400 МГц, CDCl3) 1,0-1,1 (m, 4H), 1,45 (s, 9H), 1,60 (m, 1H), 1,70 (m, 2H), 1,85 (m, 2H), 2,50 (m, 1H), 2,80 (m, 2H), 4,20 (m, 2H), 7,65 (d, 1H), 7,75 (s, 1H), 7,80 (s, 1H), 7,9 (m, 1H), 8,60 (d, 1H). Приклад 19 Цей приклад ілюструє одержання N-[5-бром-1'-(4'-фторбіфеніл-4-ілметил)-1',2',3',4',5',6'гексагідро-[2,4']біпіридиніл-3-іл]-2-хлорізонікотинаміду (сполука C23 в таблиці C). N N N Br F Cl O N 30 Шукану сполуку одержували з 2,5-дибром-3-амінопіридину за методиками, описаними в прикладі 5, не проводячи стадію C. Приклад 20 Цей приклад ілюструє одержання N-[5-бром-6-хлор-1'-(4'-фторбіфеніл-4-ілметил)1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]-2-хлорізонікотинаміду (сполука C24 в таблиці C). N Cl N N Br F Cl O N 27 UA 101046 C2 5 Шукану сполуку одержували з 2,5-дибром-3-амінопіридину за методиками, описаними в прикладі 5. Приклад 21 Цей приклад ілюструє одержання 2-хлор-N-[6-хлор-1'-(4'-фторбіфеніл-4-ілметил)-5-метил1',2',3',4',5',6'-гексагідро-[2,4']біпіридиніл-3-іл]ізонікотинаміду (сполука C26 в таблиці C). N Cl N N F Cl O N 10 Шукану сполуку одержували з 2-бром-5-метил-3-амінопіридину за методиками, описаними в прикладі 4. Наведені нижче сполуки одержували за методиками, аналогічними описаним в прикладах 321: Сполуки формули (Ic) N 3 R N (Ic) 4 R 8 NH R 5 R 1 O R Таблиця C: Спол. № R 1 R 3 R 4 R 5 R 8 Агрегатний стан/ Т. пл. 63-66 °C 84-86 °C тверда речовина тверда речовина 88-93 °C тверда речовина C1 C2 2-хлорпірид-4-ил 2-хлорпірид-4-ил -CF3 Cl H Cl H H F F C3 2-фторпірид-4-ил -CF3 H H F C4 2,6-дихлорпірид-4-ил -CF3 H H F C5 2-хлорпірид-4-ил Br F H F C6 2-хлорпірид-4-ил -CHF2 H H F C7 2(хлордифторметил)пірид-4-ил -CF3 H H F C8 2,6-дихлорпірид-4-ил -CHF2 H H F C9 C10 C11 C12 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил 2-хлорпірид-4-ил Cl H H Cl H H H H F F F F C13 2-хлорпірид-4-ил Cl H F 78-80 °C C14 2-хлорпірид-4-ил -OCH2CF3 -OCH3 -CH=CH2 -CH=CH2 циклопропіл циклопропіл тверда речовина 82-86 °C 87-90 °C 79-80 °C 88-90 °C H H F C15 2-хлорпірид-4-ил Br -CF3 H F 28 ВЕРХ (ЧУ) МС (ІЕ+) 1,42 хв 1,46 хв 569/571 569/571 1,40 хв 553 1,51 хв 603/605/607 1,41 хв 597/599 1,36 хв 551/553 тверда 1,48 хв 619/621/623 речовина 1,45 хв 585/587/589 1,52 хв 1,35 хв 1,36 хв 1,60 хв 633/635 531 527 561/563 1,63 хв 575/577 тверда 1,52 хв 541/543 речовина тверда 1,63 хв 649/651/653 речовина
ДивитисяДодаткова інформація
Назва патенту англійськоюInsecticidal phenyl- or pyridyl-piperidine compounds
Автори англійськоюPitterna, Thomas, Cassayre, Jerome Yves, Corsi, Camilla, Maienfisch, Peter
Назва патенту російськоюИнсектицидные фенил- или пиридилпиперидины
Автори російськоюПиттерна Томас, Кассер Жером Ив, Корси Камилла, Майенфиш Петер
МПК / Мітки
МПК: C07D 401/14, A01N 43/40, C07D 401/12, A01P 7/04
Мітки: піридилпіперидини, феніл, інсектицидні
Код посилання
<a href="https://ua.patents.su/41-101046-insekticidni-fenil-abo-piridilpiperidini.html" target="_blank" rel="follow" title="База патентів України">Інсектицидні феніл- або піридилпіперидини</a>
Попередній патент: Спосіб сепарації продукту помелу в текучому середовищі та млиновий сепаратор
Наступний патент: Гідроакустичний пристрій моніторингу морських трубопроводів
Випадковий патент: Спосіб неінвазивної оцінки ступеня фіброзу печінки у дітей з хронічними вірусними гепатитами