Імідазоло-5-іл-2-анілінопіримідини як агенти для інгібування проліферації клітин
Номер патенту: 74206
Опубліковано: 15.11.2005
Автори: Томас Ендрю Пітер, Бро Глорія Анн, Н'юком Ніколас Джон
Формула / Реферат
1. Сполука формули (І):
 ,
,
де:
R1 являє собою галоген, нітро, ціано, гідрокси, аміно, карбокси, карбамоїл, меркапто, С1-6алкіл, С1-6алкокси, С2-6алкеніл або С2-6алкініл;
р дорівнює 0-4; де значення R1 можуть бути однаковими або різними;
R2 являє собою сульфамоїл або групу Ra-Rb-;
q дорівнює 0-2; де значення R2 можуть бути однаковими або різними; і де р+q=0-5;
R3 являє собою галоген, нітро, ціано, гідрокси, трифторметил, трифторметокси, аміно, карбокси, карбамоїл, меркапто, сульфамоїл, С1-3алкіл, С2-3алкеніл, С2-3алкініл, С1-3алкокси, С1-3алканоїл, N-(С1-3алкіл)аміно, N,N-(С1-3алкіл)2аміно, С1-3алканоїламіно, N-(С1-3алкіл)карбамоїл, N,N-(С1-3алкіл)2карбамоїл, С1-3алкілS(O)а, де а дорівнює 0-2, N-(С1-3алкіл)сульфамоїл або N,N-(С1-3алкіл)2сульфамоїл; де R3 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rc;
n дорівнює 0-2, де значення R3 можуть бути однаковими або різними;
R4 являє собою водень, С1-6алкіл, С2-6алкеніл, С2-6алкініл, С3-8циклоалкіл, фенілабо гетероциклічну групу, зв'язану з вуглецем; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rn;
R5 і R6 є незалежно вибраними з водню, галогену, нітро, ціано, гідрокси, трифторметокси, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, С1-6алкілу, С2-6алкенілу, С2-6алкінілу, С1-6алкокси, С1-6алканоїлу, С1-6алканоїлокси, N-(С1-6алкіл)аміно, N,N-(С1-6алкіл)2аміно, С1-6алканоїламіно, N-(С1-6алкіл)карбамоїлу, N,N-(С1-6алкіл)2карбамоїлу, С1-6алкілS(O)а, де а дорівнює 0-2, С1-6алкоксикарбонілу, N-(С1-6алкіл)сульфамоїлу, N,N-(С1-6алкіл)2сульфамоїлу, С1-6алкілсульфоніламіно, С3-8циклоалкілу або 4-7-членної насиченої гетероциклічної групи; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Re; і де, якщо вказана 4-7-членна насичена гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rf;
Ra є вибраним з С1-6алкілу, С2-6алкенілу, С2-6алкінілу, С3-8циклоалкілу, С3-8циклоалкілС1-6алкілу, фенілу, гетероциклічної групи, фенілС1-6алкілу або (гетероциклічна група)С1-6алкілу; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rh;
Rb являє собою -С(O)-, -N(Rm)С(О)-, -C(O)N(Rm)-, -S(O)r-, -ОС(O)N(Rm)SO2-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або С1-6алкіл, необов'язково заміщений одним або декількома Ri, і r дорівнює 1-2;
Rd, Rg і Ri є незалежно вибраними з галогену, нітро, ціано, гідрокси, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, С1-6алкілу, С2-6алкенілу, С2-6алкінілу, С1-6алкокси, С1-6алкоксіС1-6алкокси, С1-6алкоксіС1-6алкоксіС1-6алкокси, С1-6алканоїлу, С1-6алканоїлокси, N-(С1-6алкіл)аміно, N,N-(С1-6алкіл)2аміно, С1-6алканоїламіно, N-(С1-6алкіл)карбамоїлу, N,N-(С1-6алкіл)2карбамоїлу, С1-6алкілS(O)а, де а дорівнює 0-2, С1-6алкоксикарбонілу, N-(С1-6алкіл)сульфамоїлу, N,N-(С1-6aлкiл)2cyльфaмoїлy, С1-6алкілсульфоніламіно, С3-8циклоалкілу, фенілу, гетероциклічної групи, фенілС1-6алкіл-Ro-, (гетероциклічна група)С1-6алкіл-Ro-, феніл-Ro- або (гетероциклічна група)-R°-; де Rd, Rg і Ri незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Rj; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rk;
Ro являє собою -О-, -N(Rp)-, -C(O)-, -N(Rp)C(O)-, -C(O)N(Rp)-, -S(O)s-, -SO2N(Rp)- або -N(Rp)SO2-; де Rp являє собою водень або С1-6алкіл, і s дорівнює 0-2;
Rf, Rh, Rk і Rn є незалежно вибраними з С1-4алкілу, С1-4алканоїлу, С1-4алкілсульфонілу, С1-4алкоксикарбонілу, карбамоїлу, N-(С1-4алкіл)карбамоїлу, N,N-(С1-4алкіл)карбамоїлу, бензилу, бензилоксикарбонілу, бензоїлу і фенілсульфонілу; де Rf, Rh, Rk і Rn, незалежно один від одного, можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Rl; і
Rc, Re, Rl і Rj є незалежно вибраними з галогену, нітро, ціано, гідрокси, трифторметокси, трифторметилу, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, метилу, етилу, метокси, етокси, ацетилу, ацетокси, метиламіну, етиламіно, диметиламіно, діетиламіно, N-метил-N-етиламіно, ацетиламіно, N-метилкарбамоїлу, N-етилкарбамоїлу, N,N-диметилкарбамоїлу, N,N-діетилкарбамоїлу, N-метил-N-етилкарбамоїлу, метилтіо, етилтіо, метилсульфінілу, етилсульфінілу, мезилу, етилсульфонілу, метоксикарбонілу, етоксикарбонілу, N-метилсульфамоїлу, N-етилсульфамоїлу, N,N-диметилсульфамоїлу, N,N-діетилсульфамоїлу або N-метил-N-етилсульфамоїлу;
або її фармацевтично прийнятна сіль або її складний ефір, що гідролізується in vivo.
2. Сполука формули (І) за п. 1, де R1 являє собою галоген, аміно, С1-6алкіл або С1-6алкокси, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
3. Сполука формули (І) або за п. 1, або за п. 2, де р дорівнює 0-2; де значення R1 можуть бути однаковими або різними, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
4. Сполука формули (І) за будь-яким з пп. 1-3, де R2 являє собою сульфамоїл або групу Ra-Rb-; де
Ra є вибраним з С1-6алкілу, С2-6алкенілу, С2-6алкінілу, С3-8циклоалкілу, фенілу або гетероциклічної групи; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg;
Rb являє собою -N(Rm)C(O)-, -C(O)N(Rm)-, -S(O)r, -OC(O)N(Rm)SO2-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або С1-6алкіл, і r дорівнює 2;
Rg є вибраним з галогену, гідрокси, аміно, ціано, карбамоїлу, С1-6алкілу, С1-6алкокси, С1-6алкоксіС1-6алкокси, С1-6алкоксіС1-6алкоксіС1-6алкокси, N,N-(С1-6алкіл)2аміно, С1-6алкілS(O)а, де а дорівнює 2, С3-8циклоалкілу, фенілу, гетероциклічної групи, фенілС1-6алкіл-Ro- або (гетероциклічна група)-R°-; де Rg може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rj;
R° являє собою -О-; і
Rj є вибраним з галогену, гідрокси, метилу або метокси;
або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
5. Сполука формули (І) за будь-яким з пп. 1-4, де q дорівнює 0 або 1, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
6. Сполука формули (І) за будь-яким з пп. 1-5, де q дорівнює 1, і R2 знаходиться в параположенні по відношенню до -NH-групи аніліну формули (І), або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
7. Сполука формули (І) за будь-яким з пп. 1-6, де R3 являє собою галоген, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
8. Сполука формули (І) за будь-яким з пп. 1-7, де n дорівнює 0 або 1, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
9. Сполука формули (І) за будь-яким з пп. 1-8, де R4 являє собою водень, С1-6алкіл або С2-6алкеніл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; де
Rd є вибраним з галогену, аміно, С1-6алкокси, С1-6алканоїламіно, С1-6алкілсульфоніламіно, фенілу або гетероциклічної групи;
або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
10. Сполука формули (І) за будь-яким з пп. 1-9, де R5 і R6 є незалежно вибраними з водню або С1-6алкілу; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Re; де
Re є вибраним з галогену або метокси;
або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
11. Сполука формули (І) за п. 1, де:
R1 являє собою хлор, аміно, метил або метокси;
р дорівнює 0-2; де значення R1 можуть бути однаковими або різними;
R2 являє собою сульфамоїл, N-(тетрагідрофур-2-илметил)сульфамоїл, N-(циклопропілметил)сульфамоїл, N-(фур-2-илметил)сульфамоїл, N-(2,2-диметил-1,3-діоксолан-4-ілметил)сульфамоїл, N-(ціанометил)сульфамоїл, N-(карбамоїлметил)сульфамоїл, N-метилсульфамоїл, N-(4-фторбензил)сульфамоїл, N-(піридин-2-ілметил)сульфамоїл, N-(піридин-3-ілметил)сульфамоїл, N-(4-метилтіазол-2-іл)сульфамоїл, N-(3-метилоксазол-5-ілметил)сульфамоїл, N-(тетрагідропіран-2-ілметил)сульфамоїл, N-(2-метилпіразин-5-іл)сульфамоїл, N-[2-(2-гідроксіетоксі)етил]сульфамоїл, N-(2-гiдpoкcieтил)cyльфaмoїл, N-(2,2,2-трифторетил)сульфамоїл, N-(2-метоксіетил)сульфамоїл, N-(2-мезилетил)сульфамоїл, N-(2-бензилоксіетил)сульфамоїл, N-(2,2-диметоксіетил)сульфамоїл, N-[2-(N,N-димeтилaмiнo)eтил]cyльфaмoїл, N-(2-піперидин-1-ілетил)сульфамоїл, N-[2-(метоксиметоксі)етил]сульфамоїл, N-етилсульфамоїл, N-[2-(2-метоксіетоксі)етил]сульфамоїл, N-{2-[2-(2-метоксіетокси)етокси]етил}сульфамоїл, N-(2-{2-[2-(2-метоксіетоксі)етокси]етокси}етил)сульфамоїл, N-(2-піридин-2-ілетил)сульфамоїл, N-(2-піридин-4-ілетил)сульфамоїл, N-(2-ізоксазол-3-ілоксіетил)сульфамоїл, N-(2-ізотіазол-3-ілоксиетил)сульфамоїл, N-(2-1,2,5-тіадіазол-3-ілоксіетил)сульфамоїл, N-метил-N-(2-метоксіетил)сульфамоїл, N-[3-(2-оксопіролідин-1-іл)пропіл]сульфамоїл, N-(3-метоксипропіл)сульфамоїл, N-пропілсульфамоїл, N-(2,3-дигідроксипропіл)сульфамоїл, N-(3-морфолінопропіл)сульфамоїл, N-[3-(N,N-диметиламіно)пропіл]сульфамоїл, N-(3,3,3-трифторпропіл)сульфамоїл, N-(2,2-диметил-3-гідроксипропіл)сульфамоїл, N-(3-гідроксипропіл)сульфамоїл, N-(3-етоксипропіл)сульфамоїл, N-(2-гідроксипропіл)сульфамоїл, N-(3-ізопропоксипропіл)сульфамоїл, N-(3-ізопропокси-2-гідроксипропіл)сульфамоїл, N-(3-ізоксазол-3-ілоксипропіл)сульфамоїл, N-(3-ізотіазол-3-ілоксипропіл)сульфамоїл, N-(3-1,2,5-тіадіазол-3-ілоксипропіл)сульфамоїл, N-(1,1-диметилпропіл)сульфамоїл, N-метил-N-(3-морфолінопропіл)сульфамоїл, N-бутилсульфамоїл, N-трет-бутилсульфамоїл, N-(2-гідроксибутил)сульфамоїл, N-метил-N-трет-бутилсульфамоїл, N-пентилсульфамоїл, N-(5-гідроксипентил)сульфамоїл, N-(4,5-диметилоксазол-2-іл)сульфамоїл, N-(циклопропіл)сульфамоїл, N-(циклобутил)сульфамоїл, N-(3-тpифтopмeтилфeнiл)cyльфaмoїл, N-алілсульфамоїл, N-(2-пропініл)сульфамоїл, N-метилкарбамоїл, ацетамідо, мезиламіно або мезил;
q дорівнює 0 або 1;
R3 являє собою бром або хлор;
n дорівнює 0 або 1;
R4 являє собою водень, метил, етил, ізопропіл, 3-бутеніл, бензил, 2-фталімідоетил, 2-аміноетил, 2-метоксіетил, 2-ацетамідоетил, 2-мезиламіноетил або 2,2,2-трифторетил;
R5 і R6 є незалежно вибраними з водню, метилу, етилу, ізопропілу, трифторметилу або метоксиметилу;
або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
12. Сполука формули (І) за п. 1, вибрана з:
2-{4-[N-(циклопропілметил)сульфамоїл]аніліно}-4-(1,2-диметилімідазол-5-іл)піримідину;
4-(1-етил-2-метилімідазол-5-іл)-2-{4-[N-(2-метоксіетил)сульфамоїл]аніліно}піримідину;
4-(1-етил-2-метилімідазол-5-іл)-2-{4-[N-(3-метоксипропіл)сульфамоїл]аніліно}піримідину;
4-(1-етил-2-метилімідазол-5-іл)-2-{4-[N-(циклопропілметил)сульфамоїл]аніліно)піримідину;
4-(1-етил-2-метилімідазол-5-іл)-2-[4-(N-циклопропілсульфамоїл)аніліно]піримідину;
4-(1-метил-2-ізопропілімідазол-5-іл)-2-{4-[N-(циклопропілметил)сульфамоїл]аніліно}піримідину;
4-(1,2-диметилімідазол-5-іл)-2-[4-(N-циклопропілсульфамоїл)аніліно]піримідину;
4-(1,2-диметилімідазол-5-іл)-2-[4-(N-циклобутилсульфамоїл)аніліно]піримідину;
4-(1,2-диметилімідазол-5-іл)-2-{4-[N-(2,2,2-трифторетил)сульфамоїл]аніліно}піримідину і
4-(1-ізопропіл-2-метилімідазол-5-іл)-2-[4-(N-циклобутилсульфамоїл)аніліно]піримідину;
або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo.
13. Сполука формули (І) або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo, за будь-яким з пп. 1-12, придатна як лікарський засіб.
14. Фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, за будь-яким з пп. 1-12, в поєднанні з фармацевтично прийнятним розріджувачем або носієм.
15. Фармацевтична композиція за п. 14, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, за будь-яким з пп. 1-12, в поєднанні з фармацевтично прийнятним розріджувачем або носієм, придатна для продукування інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровної тварини, такої як людина.
16. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних при наданні інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровних тварин, таких як людина.
17. Спосіб продукування інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровної тварини, такої як людина, потребуючої такого лікування, при якому вводять вказаній тварині ефективну кількість сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12.
18. Спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі або ефіру, що гідролізується in vivo, за п. 1, при якому проводять взаємодію піримідину формули (II)
 , (II)
, (II)
де R3, R4, R5, R6, n мають значення вказані вище, а L є групою, що заміщується,
з аніліном формули (III)
 , (III)
, (III)
де R1, R2, p, q мають значення, вказані вище, і,
якщо необхідно, наступне перетворення сполуки формули (І) в іншу сполуку формули (І);
видалення будь-якої захисної групи;
утворення фармацевтично прийнятної солі або солі, що гідролізується in vivo.
19. Спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі або ефіру, що гідролізується in vivo, за п. 1, при якому проводять взаємодію сполуки формули (IV)
 , (IV)
, (IV)
де R1, R2, p, q мають значення вказані вище;
із сполукою формули (V)
 , (V)
, (V)
де R3, R4, R5, R6, n мають значення, вказані вище, Т є О або S; Rx може бути однаковим або різним і вибраний з С1-6алкілу, і,
якщо необхідно, наступне перетворення сполуки формули (І) в іншу сполуку формули (І);
видалення будь-якої захисної групи;
утворення фармацевтично прийнятної солі або солі, що гідролізується in vivo.
20. Спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі або ефіру, що гідролізується in vivo, за п. 1, де R2 є сульфамоїльною групою або групою Ra-Rb-, і Rb являє собою групу NHSO2 -, при якому здійснюють взаємодію піримідину формули (VI)
 , (VI)
, (VI)
де R3, R4, R5, R6, n мають значення, вказані вище, а Х є групою, що заміщується,
з аміном формули (VII)
Ra-NH2 , (VII)
де Ra має значення, вказане вище, і,
якщо необхідно, наступне перетворення сполуки формули (І) в іншу сполуку формули (І);
видалення будь-якої захисної групи;
утворення фармацевтично прийнятної солі або солі, що гідролізується in vivo.
21. Спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі або ефіру, що гідролізується in vivo, за п. 1, при якому проводять взаємодію піримідину формули (VIII)
 , (VIII)
, (VIII)
де R3, R4, R5, R6, n мають значення, вказані вище,
із сполукою формули (IX)
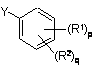 , (IX)
, (IX)
де R1, R2, p, q мають значення, вказані вище, а Y є групою, що заміщується; і,
якщо необхідно, наступне перетворення сполуки формули (І) в іншу сполуку формули (І);
видалення будь-якої захисної групи;
утворення фармацевтично прийнятної солі або солі, що гідролізується in vivo.
22. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних для лікування раку.
23. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних для лікування лейкемії і раку грудей, легень, товстої кишки, прямої кишки, шлунка, простати, сечового міхура, підшлункової залози і яєчників.
24. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних для лікування лейкемій, лімфоїдних злоякісних і солідних пухлин, таких як карцинома і саркома тканин, таких як печінка, нирки, простата і підшлункова залоза.
25. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних для уповільнення росту первинних і рецидивуючих солідних пухлин, наприклад, товстої кишки, грудей, простати, легень і шкіри.
26. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних для інгібування росту первинних і рецидивуючих солідних пухлин, наприклад, деяких пухлин товстої кишки, грудей, простати, легень, вульви і шкіри.
27. Застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, за будь-яким з пп. 1-12, у виробництві лікарських засобів, придатних для лікування раку (солідних пухлин і лейкемій), фібропроліферативних і диференціюючих порушень, псоріазу, ревматоїдного артриту, саркоми Капоші, ангіоматозу, гострих і хронічних нефропатій, атероми, атеросклерозу, артеріального рестенозу, аутоімунних захворювань, гострого і хронічного запалення, захворювань кісток і захворювань очей з поліферацією сітчастих судин.
Текст
Даний винахід відноситься до піримідинових похідних або до їх фармацевтично прийнятних солей, або до їх складних ефірів, що гідролізуються in vivo, які володіють інгібіторною активністю по відношенню до клітинного циклу, і, відповідно, є придатними для використання, завдяки їх активності проти проліферації клітин (наприклад, проти раку), і з цієї причини є придатними для використання в способах лікування організму людини або тварини. Даний винахід також відноситься до способів одержання вказаних піримідинових похідних, до фармацевтичних композицій, що містять їх, і до їх використання при виробництві лікарських засобів, що використовуються для продукування впливу проти проліферації клітин у теплокровної тварини, такої як людина. Сімейство внутрішньоклітинних білків, які називаються циклінами, грає центральну роль в клітинному циклі. Синтез і деградація циклінів щільно контролюється, так що їх рівень експресування коливається протягом клітинного циклу. Цикліни зв'язуються з циклін-залежними серин/фреонін кіназами (CDK), і це зв'язування є самим важливим для активності CDK (таких як CDK1, CDK2, CDK4 і/або CDK6) в клітині. Хоча конкретні деталі відносно того, як кожний з цих факторів об'єднується для регуляції активності CDK, є малозрозумілим, рівновага між ними двома диктує, чи буде клітина розвиватися в межах клітинного циклу чи ні. Останні дослідження конвергенції онкогена і гена супресора пухлини ідентифікують входження в клітинний цикл як ключову точку для контролю мітогенезу пухлин. Більш того CDK, видимо, знаходяться в циклі після деякої кількості сигнальних шляхів онкогена. Розрегуляція активності CDK шляхом позитивної регуляції циклінів і/або стирання ендогенних інгібіторів, видимо, є важливою віссю між мітогенними сигнальними шляхами і проліферацією клітин пухлини. Відповідно, було виявлено, що інгібітор клітинних циклокіназ, особливо, інгібітори CDK2, CDK4 і/або CDK6 (які працюють в S-фазі, G1-S і G1-S фазі, відповідно), повинен являти собою цінність як інгібітор проліферації клітини, такої як зростання ракових клітин у ссавців. Даний винахід базується на виявленні того факту, що певні піримідинові сполуки несподівано інгібують вплив клітинних циклокіназ, демонструючи селективність по відношенню до CDK2, CDK4 і CDK6, і, таким чином, володіють властивостями, направленими проти проліферації клітин. Такі властивості, як очікується, представляють цінність при лікуванці хворобливих станів, що зв'язуються з відхиленнями в клітинних циклах і в проліферації клітин, таких як ракові захворювання (солідні пухлини і різні види лейкемії), фібропроліферативні і диференціаційні розлади, псоріаз, ревматоїдний артрит, саркома Капоши, хемангіома, гострі і хронічні невропатії, атерома, атеросклероз, артеріальний рестеноз, аутоімунні захворювання, гостре і хронічне запалення, захворювання кісток і захворювання очей з проліферацією ретинальних судин. Відповідно, даний винахід передбачає сполуку фррмули (І): де: R1 являє собою галоген, нітро, ціано, гідрокси, аміно, карбокси, карбамоїл, меркапто, С1-6алкіл, С16алкокси, С 2-6алкеніл або С 2-6алкініл; р дорівнює 0-4; де значення R1 можуть бути однаковими або різними; R2 являє собою сульфамоїл або групу Ra-Rb-; q дорівнює 0-2; де значення R2 можуть бути однаковими або різними; і де р+q=0-5; R3 являє собою галоген, нітро, ціано, гідрокси, трифторметил, трифторметокси, аміно, карбокси, карбамоїл, меркапто, сульфамоїл, С1-3алкіл, С2-3алкеніл, С2-3алкініл, С1-3алкокси, С1-3алканоїл, N-(С13алкіл)аміно, Ν,Ν-(С 1-3алкіл)2аміно, С 1-3алканошаміно, N-(С 1-3алкіл)карбамоїл, N,N-(С 1-3алкіл)2карбамоїл, С 13 3алкіл S(O)a, де а дорівнює 0-2, N-(С 1-3алкіл)сульфамоїл або Ν,Ν-(С 1-3алкіл)2сульфамоїл; де R може бути с необов'язково заміщенім на атомі вуглецю одним або декількома R ; n дорівнює 0-2, де значення R3 можуть бути однаковими або різними; R4 являє собою водень, С1-6алкіл, С2-6алкеніл, С2-6алкініл, С3-8циклоалкіл, феніл або гетероциклічну груп у, пов'язану з вуглецем; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rn; R5 і R6 є незалежно вибраними з водню, галогену, нітро, ціано, гідрокси, трифторметокси, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, С1-6алкілу, С2-6алкенілу, С2-6алкінілу, С1-6алкокси, С1С1-6алканоїлокси, N-(С1-6алкіл)аміно, N,N-(С1-6алкіл)2аміно, С1-6алканоїламіно, N-(С16алканоїлу, 6алкіл)карбамоїлу, N,N-(С 1-6алкіл)2карбамоїлу, С 1-6алкілS(О)а, де а дорівнює 0-2, С 1-6алкоксикарбонілу, N(С1-6алкіл)сульфамоїлу, Ν,Ν-(С1-6алкіл)2сульфамоїлу, С1-6алкілсульфоніламіно, С3-8циклоалкілу або 4-7 членної насиченої гетероциклічної групи; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Re; і де, якщо вказана 4-7 членна насичена гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rf; Ra є вибраним з С1-6алкілу, С2-б алкенілу, С2-б алкінілу, С3-8циклоалкілу, С3-8циклоалкілС 1-6алкілу, фенілу, гетероциклічної групи, фенілС1-6алкілу або (гетероциклічна група)С1-6алкілу; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg ; і де, якщо виказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rh; Rb являє собою -С(О)-, -N(Rm)С(О)-, -C(O)N(Rm)-, -S(O)r-, -OC(O)N(Rm)SO2-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або С 1-6алкіл, необов'язково заміщений одним або декількома R1, і r дорівнює 12; Rd, Rg і Ri є незалежно вибраними з галогену, нітро, ціано, гідрокси, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, С1-6алкілу, С 2-б алкенілу, С2-6алкінілу, С1-6алкокси, С1-6алкоксиС 1-6алкокси, С16алкоксиС 1-6алкоксиС 1-6алкокси, С 1-6алканоїлу, С 1-6алканоїлокси, N-(С 1-6алкіл)аміно, N,N-(С 1-6алкіл)2аміно, С1-6алканоїламіно, N-(С1-6алкіл)карбамоїлу, N,N-(С1-6алкіл)2карбамоїлу, С1-6алкілS(О)а, де а дорівнює 0-2, С1-6алкоксикарбоні|лу, N-(С1-6алкіл)сульфамоїлу, N,N-(С1-6алкіл)2сульфамоїлу, С1-6алкілсульфоніламіно, С3o o 8циклоалкілу, фенілу, ге тероциклічної групи, фенілС 1-6алкіл-R -, (гетероциклічна група)С1-6алкіл-R -, фенілo o d g i R - або (гетероциклічна група)-R -; де R , R і R незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Rj; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rk; Ro являє собою -О-, -N(Rp)-, -C(O)-, -N(Rp)C(O)-, -C(O)N(Rp)-, -C(O)s-, -SO2N(Rp)- або -N(Rp)SO2-; де Rp являє собою водень або С1-6алкіл, і s дорівнює 0-2; Rf, Rh, R k і R n є незалежно вибраними з С1-4алкілу, С1-4алканоїлу, С1-4алкілсульфонілу, С1алкоксикарбонілу, карбамоїлу, N-(С1-4алкіл)карбамоїлу, N,N-(С1-4алкіл) карбамоїлу, бензилу, 4 бензилокрикарбонілу, бензоїлу і фенілсуль фонілу; де Rf, R h, R k і Rn, незалежно один від одного, можуть бути необов'язково заміщеними на атомі вуглецю одним абр декількома R І; і Rc, Re, RІ і Rj є незалежно вибраними з галогену, нітро, ціано, гідрокси, трифторметокси, трифторметилу, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, метилу, етилу, метокси, етокси, ацетилу, ацетокси, метиламіну, етиламіно, диметиламіно, діетиламіно, N-метил-N-етиламіно, ацетиламіно, N-метилкарбамоїлу, N-етилкарбамоїлу, N,N-диметилкарбамоїлу, Ν,Ν-діетилкарбамоїлу, N-метил-Nетилкарбамоїлу, метилтіо, етилтіо, метилсульфінілу, етилсульфінілу, мезилу, етилсульфонілу, метоксикарбонілу, етоксикарбонілу, Ν-метилсульфамоїлу, N-етилсульфамоїлу, Ν,Ν-диметилсульфамоїлу, Ν,Ν-діетилсульфамоїлу або N-мeтил-N-eтилcyльфaмoїл; або їх фармацевтично прийнятну сіль або їх складний ефір, що гідролізується in vivo. В іншому аспекті даного винаходу передбачаєтьс^ сполука формули (І): де: R1 являє собою галоген, нітро, ціано, гідрокси, аміно, карбокси, карбамоїл, меркапто, С1-6алкіл, С16алкокси, С 2-6алкеніл або С 2-6алкініл; р дорівнює 0-4; де значення RІ можуть бути однаковими або різними; R2 являє собою сульфамоїл або групу Ra-Rb-; q дорівнює 0-2; де значення R2 можуть бути однаковими або різними; і де р+q=0-5; R3 являє собою галоген, нітро, ціано, гідрокси, трифторметил, трифторметокси, аміно, карбокси, карбамоїл, меркапто, сульфамоїл, С1-3алкіл, С2-3алкеніл, С2-3алкініл, С1-3алкокси, С1-3алканоїл, N-(С13алкіл)аміно, N,N-(С 1-3алкіл)2аміно, С 1-3алканоїламіно, N-(С 1-3алкіл)карбамоїл, N,N-(С 1-3алкіл)2карбамоїл, С 13 3алкілS(О)а, де а дорівнює 0-2, N-(С 1-3алкіл)сульфамоїл або N,N-(С 1-3алкіл)2сульфамоїл; де R може бути c необов'язково заміщеним на атомі вуглецю одним або декількома R ; n дорівнює 0-2, де значення R можуть бути однаковими або різними; R4 являє собою водень, С1-6алкіл, С2-6алкеніл, С2-6алкініл, С3-8циклоалкіл, феніл або гетероциклічну груп у, пов'язану з вуглецем; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rn; R5 і R6 є незалежно вибраними з водню, галогену, нітро, ціано, гідрокси, трифторметокси, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, С1-6алкілу, С2-6алкенілу, С2-6алкінілу, С1-6алкокси, С16алканоїлу, С 1- 6алканоїлокси, N-(С 1-6алкіл)аміно, N,N-(С 1-6алкіл)2аміно, С 1-6алканоїламіно, N-(С 1-6алкіл) карбамоїлу, N,N-(С1-6алкіл)2карбамоїлу, С1-6алкілS(О)2, де а дорівнфє 0-2, С1-6алкоксикарбонілу, N-(С14-76алкіл)сульфамоїлу, N,N-(С 1-6алкіл)2сульфамоїл|у, С 1-6алкілсульфоніламіно, С 3-8циклоалкілу або членної насиченої гетероциклічної групи; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Re; і де, якщо вказана 4-7-членна насичена гетероциклічна група містить залишок -NH-, його азoт може бути необов'язково заміщеним групою, вибраною з Rf; Ra є вибраним з С1-6алкілу, С2-6алкенілу, С2-6алКінілу, С3-8циклоалкілу, С3-8циклоалкілС 1-6алкілу, фенілу, гетероциклічної групи, фенілС1-6алкілу або (гетероциклічна група)С1-6алкілу; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg ; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rh; Rb являє собою -С(О)-, -N(Rm)C(O)-, -C(O)N(Rm)-, -S(O)r-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або С 1-6алкіл, необов'язково заміщений одним або декількома Ri, і r дорівнює 1-2; Rd, Rg і Ri є незалежно вибраними з галогену, нітро, ціано, гідрокси, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, С 1-6алкілу, С2-6алкенілу, С2-6алкінілу, С1-6алкокси, С1-6алканоїлу, С1-6алканоїлокси, N-(С1-6алкіл) аміно, N,N-(С1-6алкіл)2аміно, С1-6алканоїламіно, N-(С1-6алкіл)карбамоїлу, N,N-(С16алкіл)2карбамоїлу, С 1-6алкілS(О)а де а дорівнює 0-2, С 1-6алкоксикарбонілу, N-(С 1-6алкіл)сульфамоїлу, N,N(С1-6алкіл)2сульфамоїлу, С1-6алкілсульфоніламіно, С3-8циклоалкілу, фенілу, гетероциклічної групи, феніл-Roабо (гетероциклічна група)-Ro-; де Rd, Rg і Ri незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Rj; і де, якщо вказана гетероциклічна група містить залишок -NH-, його азот може бути необов'язково заміщеним групою, вибраною з Rk; Ro являє собою -О-, -N(Rp)-, -С(О), -N(Rp)C(O)-, -C(O)N(Rp)-, -S(O)s-, -SO2N(Rp)- або -N(Rp)SO2-; де Rp являє собою водень абo С1-6алкіл, і s дорівнює 0-2; Rf, Rh, R k і R n є незалежно вибраними з С1-4алкілу, С1-4алканоїлу, С1-4алкілсульфонілу, С1алкоксикарбонілу, карбамоїлу, N-(С1-4алкіл)карбамоїлу, Ν,Ν-(С1-4алкіл)карбамоїлу, бензилу, 4 бензилоксикарбонілу, бензоїлу і фенілсуль фонілу; де Rf, Rh і R k незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Rl; і Rc, Re, Rl і Rj є незалежно вибраними з галогену, нітро, ціано, гідрокси, трифторметокси, трифторметилу, аміно, карбокси, карбамоїлу, меркапто, сульфамоїлу, метилу, етилу, метокси, етокси, ацетилу, ацетокси, метиламіно, етиламіно, диметиламіно, діетиламіно, N-метил-N-етиламіно, ацетиламіно, N-метилкарбамоїлу, N-етилкарбамоїлу, Ν,Ν-диметилкарбамоїлу, Ν,Ν-діетилкарбамоїлу, N-метил-Nетилкарбамоїлу, метилтіо, етилтіо, метилсульфінілу, етилсульфінілу, мезилу, етилсульфонілу, метоксикарбонілу, етоксикарбонілу, N-метилсульфамоїлу, N-етилсульфамоїлу, Ν,Ν-диметилсульфамоїлу, Ν,Ν-діетилсульфамоїлу або N-метил-N-етилсульфамоїлу; або їх фармацевтично прийнятну сіль, або їх складний ефір, що гідролізується in vivo. У даному описі термін "алкіл" включає в себе ал|кільні групи, як з прямим, так і з розгалуженим ланцюгом, але посилання на індивідуальні алкільні групи, такі як "пропіл", вказують тільки на варіант з прямим ланцюгом. Наприклад, "С1-6алкіл" включає в себе С 1-4алкіл, С1-3алкіл, пропіл, ізофопіл і трет-бутил. Однак, посилання на індивідуальні алкільні групи, такі як "пропіл", вказують тільки на варіант з прямим ланцюгом, а посилання на індивідуальні алкільні групи з розгалуженим ланцюгом, такі як "ізопропіл" вказують тільки на варіант з розгалуженим ланцюгом. Подібна ж умова застосовується до інших радикалів, наприклад "фенілС1-6алкіл" включає в себе фенілС 1-4арікіл, бензил, 1-фенілетил і 2-фенілетил. Термін "галоген" відноситься до фтору, хлор у, брому і йоду. Там, де необов'язкові замісники вибираються з "однієї або декількох" гр уп, необхідно зрозуміти, що це визначення включає в себе всі замісники, які вибирають тільки з однієї з вказаних груп або замісники, які вибирають з двох або з декількох вказаних груп. "Гетероциклічна група" являє собою насичене, часткове насичене або ненасичене, моно або біциклічне кільце, що містить 4-12 атомів, з яких, щонайменше, один атом вибирається з азоту, сірки або кисню, який, якщо не вказано іншого, може бути пов'язаний з атомами вуглецю або азоту, де гр упа -СН2- може необов'язково бути замінена -С(О)-, кільцевий атом азоту може необов'язково нести на собі С 1-6алкільну груп у і утворювати четвертинну сполуку, або кільцевий атом азоту і/або сірки може необов'язково бути окислений, з утворенням N-оксидів і/або S-оксидів. Приклади і відповідні значення терміну "гетероциклічна група" являють собою морфоліно, піперидил, піридил, піраніл, піроліл, ізотіазоліл, індоліл, хіноліл, тієніл, 1,3-бензодіоксоліл, тіадіазоліл, піперазиніл, тіазолідиніл, піролідиніл, тіоморфоліно, піролініл, гомопіперазиніл, 3,5-діоксапіперидиніл, тетрагідропіраніл, імідазоліл, піримідил, піразиніл, піридазиніл, ізоксазоліл, N-метилпіроліл, 4-піридон, 1-ізохінолон, 2-піролідон, 4-тіазолідон, піридин-N-оксид і хінолін-Nоксид. Переважно, "гетероциклічна група" являє собою насичене, часткове насичене або ненасичене, моно або біциклічне кільце, що містить 5 або 6 атомів, з яких, щонайменше, один атом вибирається з азоту, сірки або кисню, він може, якщо не вказано іншого, бути пов'язаним з атомами вуглецю або азоту, група -СН2може необов'язково бути замінена -С(О)-, і кільцевий атом сірки може бути необов'язково окислений з утворенням S-оксидів. Більш переважно "гетероциклічна група" являє собою тетрагідрофурил, піридил, піролидиноніл, морфоліно, імідазоліл, піперидиніл або піролідиніл. Особливо, "гетероциклічна група" являє собою тетрагідрофурил або морфоліно. В іншому аспекті даного винаходу, особливо, "гетероциклічна група" являє собою тетрагідрофуран-2-іл, 2-оксопіролидин-1-іл, фуран-2-іл, оксазоліл, морфоліно, піперидиніл, тіазоліл, піразиніл, ізоксазоліл, тетрагідропіран, піридил, ізоксазоліл, ізотіазоліл, 1,2,5тіадіазоліл, фталімідо. "4-7-Членна насичена гетероциклічна група" являє собою насичене моноциклічне кільце, що містить 4-7 атомів, з яких, щонайменше, один атом вибирається з азоту, сірки або кисню, який може, якщо не вказано іншого, бути пов'язаний з атомами вуглецю або азоту, де група -СН2- може необов'язково бути замінена С(О)-, і атом сірки може бути необов'язково окислений з утворенням S-оксидів. Приклади і відповідні значення терміну "гетероциклічна група" являють собою морфоліно, піперидил, 1,4-діоксаніл, 1,3діоксоланіл, 1,2-оксатіоланіл, імідазолідиніл, піразолідиніл, піперазиніл, тіазолідиніл, піролідиніл, тіоморфоліно, гомопіперазиніл і тетрагідропіраніл. Приклад "С1-6алканоїлокси" являє собою ацетокси. Приклади "С1-6алкоксикарбонілу" включають в себе С1-4алкоксикарбоніл, метоксикарбоніл, етоксикарбоніл, н- і трет-бутоксикарбоніл. Приклади "С1-6алкокси" включають в себе С 1-4алкокси, С1-3алкокси, метокси, етокси і пропокси. Приклади "С1-6алканоїламіно" включають в себе формамідо, ацетамідо і пропіоніламіно. Приклади "С1-6алкілS(О)а де а дорівнює 0-2" включають в себе С 1-6алкілсульфоніл, метилтіо, етилтіо, метилсульфініл, етилсульфініл, мезил і етилсульфоніл. Приклади "С1-6алкілС(О)r, де r дорівнює 1-2" включають в себе метилсульфініл, етилсульфініл, мезил і етилсульфонил. Приклади "С1-6алканоїлу" включають в себе С1-6алканоїл, пропіоніл і ацетил. Приклади "N-С1-6алкіламіно" включають в себе метиламіно і етиламіно. Приклади "N,N-(С16алкіл)2аміно" включають ди-N-метиламіно, ді-(N-етил)аміно і N-етил-N-метиламіно. Приклади "С 2-6алкенілу" являють собою вініл, аліл і 1-пропеніл. Приклади "С2-балкінілу" являють собою етиніл, 1-пропініл і 2пропініл. Приклади "N-(С1-6алкіл)сульфамоїлу" являють собою N-(метил)сульфамоїл і N-(етил)сульфамоїл. Приклади "N-(С1-6алкіл)2сульфамоїлу" являють собою N,N-(диметил)сульфамоїл і N-(метил)-N(етил)сульфамоїл. Приклади "N-(С1-6алкіл)карбамоїлу" являють собою N-(С1-4алкіл)карбамоїл, метиламінокарбоніл і етиламінокарбоніл. Приклади "N,N-(С1-6алкіл)2карбамоїлу" являють собою N,N(С14алкіл)2карбамоїл, диметиламінокарбоніл і метилетиламінокарбоніл. Приклади "С 3-8циклоалкілу" являють собою циклопропіл, циклобутил, циклопропіл і циклогексил. Приклади "(гетероциклічна група)С1-6алкілу" включають в себе піридилметил, 3-морфолінопропіл і 2-піримід-2-ілетил. Приклади "С3-8циклоалкілС16алкілу" являють собою циклопропілетил, циклобутилметил, 2-циклопропілпропіл і циклогексилетил. Придатна для використання фармацевтично прийнятна сіль сполуки згідно з даним винаходом являє собою, наприклад, кислотно-адитивну сіль сполуки згідно з даним винаходом, яка є досить основною, наприклад, кислотно-адитивна сіль, наприклад, неорганічної або органічної кислоти, наприклад, хлористоводневої, бромисто-водневої, сірчаної, фосфорної, трифтороцтової, лимонної або малеїнової кислоти. Крім того, придатна для використання фармацевтично прийнятна сіль сполуки згідно з даним винаходом, яка є досить кислотною, являє собою сіль лужного металу, наприклад, сіль натрію або калію, сіль лужноземельного металу, наприклад, сіль кальцію або магнію, сіль амонію або сіль органічної основи, яка дає фізіологічно прийнятний катіон, наприклад, сіль метиламіну, диметиламіну, триметиламіну, піперидину, морфоліну або трис-(2-гідроксіетил)аміну. Складний ефір, що гідролізується in vivo, сполуки формули (І), що містить карбокси або гідроксигрупу, являє собою, наприклад, фармацевтично прийнятний складний ефір, який гідролізується в організмі людини або тварини, з одержанням початкової кислоти або спирту. Придатні для використання фармацевтично прийнятні складні ефіри для карбокси включають в себе С 1-6алкоксиметилові складні ефіри, наприклад, метоксиметиловий, С1-6алканоїлоксиметилові складні ефіри, наприклад, півалоїлоксиметиловий, фталідилові складні ефіри, С3-8циклоалкоксикарбонілоксіСі.балкілові складні ефіри, наприклад, 1-циклогексилкарбонілоксіетиловий; 1,3-діоксолен-2-онілметилові складні ефіри, наприклад, 5метил-1,3-діоксолен-2-онілметиловий; і С 1-6алкоксикарбонілоксіетилові складні ефіри, наприклад, 1метоксикарбонілоксіетиловий, і можуть бути утворені на будь-якій карбоксигрупі в сполуках згідно з даним винаходом. Складний ефір, що гідролізується in vi vo, сполуки формули (І), що містить гідроксигрупу, включає в себе неорганічний складні ефіри, такі як фосфатні складні ефіри, і a-ацилоксіалкілові прості ефіри, і родинні сполуки, які внаслідок гідролізу складного ефіру in vivo розпадаються, з одержанням початкової гідроксигрупи. Приклади a-ацилоксіалкілових простих ефірів включають в себе ацетоксиметокси і 2,2диметилпропіонілоксиметоксй. Вибір груп, утворюючих складні ефіри, що гідролізуються in vivo, для гідрокси, включає в себе алканоїл, бензоїл, фенілацетил, і заміщений бензоїл і фенілацетил, алкоксикарбоніл (з одержанням алкілкарбонатних складних ефірів), діалкілкарбамоїл і N-(діалкіламіноетил)N-алкілкарбамоїл (з одержанням карбаматів), діалкіламіноацетил і карбоксіацетил. Приклади замісників на бензоїлі включають в себе морфоліно і піперазино, пов'язані з кільцевим атомом азоту через метиленову груп у в 3- або 4-положенні бензоїльного кільця. Деякі сполуки формули (І) можуть мати хіральні центри і/або геометричні ізомерні центри (Е-і Zізомери), і необхідно зрозуміти, що даний винахід охоплює всі такі оптичні ізомери, діастереоізомери і геометричні ізомери, які володіють інгібіторною активністю по відношенню до CDK. Даний винахід відноситься до будь-якої таутомерної форми сполук формули (І), які володіють інгібіторною активністю по відношенню до CDK, і до всіх них разом. Зокрема, фахівець в даній області помітить, що там, де R4 являє собою водень, імідазольне кільце, зображене на формулі (І), може таутомеризуватися. Необхідно також зрозуміти, що певні сполуки формули (І), можуть існувати як в сольватованій, так і в несольватованій формах, наприклад, в таких формах, як гідратовані форми. Необхідно зрозуміти, що даний винахід охоплює всі сольватовані форми, які володіють інгібіторною активністю по відношенню до CDK. Переважні значення R1, R2, R3, R 4, R5 , R6, n, p і q є наступними. Такі значення можуть використовува тися там, де це необхідно, разом з будь-яким з визначень, пунктів формули винаходу або втілень, визначених вище або нижче. Переважно, R1 являє собою галоген, аміно, С1-6алкіл або С1-6алкокси. Більш переважно, R1 являє собою галоген, С1-4алкіл або С1-4алкокси. Конкретно, R1 являє собою хлор, С1-3алкіл або С1-3алкокси. Більш конкретно, R1 являє собою хлор. В іншому аспекті даного винаходу, R1 , переважно, являє собою галоген, аміно, С1-6алкіл або С16алкокси. В іншому аспекті даного винаходу, R1 , більш переважно, являє собою хлор, аміно, метил або метокси. Переважно, р дорівнює 0-2; де значення R1 можуть бути однаковими або різними. Більш переважно, р дорівнює 0 або 1. В одному з аспектів даного винаходу, переважно, р дорівнює 0. В іншому аспекті даного винаходу, переважно, р дорівнює 1. Переважно, коли р дорівнює 1, R1 являє собою групу, що знаходиться в мета- або параположенні по відношенню до -NH-групи аніліну формули (І). Більш переважно, коли р дорівнює 1, R1 знаходиться в метаположенні по відношенню до -NH-групи аніліну формули (І). Переважно, R2 являє собою сульфамоїл або групу R a-Rb-; де Ra є вибраним з С1-6алкілу, С3-8циклоалкілу, С3-8циклоалкілС 1-6алкілу, фенілу, гетероциклічної групи, фенілС 1-6алкілу або (гетероциклічна група)С1-6алкілу; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg ; Rb являє собою -N(Rm)C(O), -C(O)N(Rm)-, -SO2N(Rm)- aбo -N(Rm)SO 2-; де R m являє собою водень; Rg є вибраним з галогену, гідрокси, аміно, карбамоїлу, С1-6алкілу або С1-6алкокси; і Rj є вибраним з галогену або гідрокси. Більш переважно, R2 являє собою сульфамоїл або групу Ra-Rb-; де Ra є вибраним з С1-6алкілу, С3-8циклоалкілС 1-6алкілу, фенілС 1-6алкілу або (гетероциклічна група)С1a g 6aлкілу; де R може бути необов'язково заміщеним на атомі вуглецю одним або декількома R ; Rb являє собою -N(Rm)SO2-; де R m являє собою водень; Rg є вибраним з галогену, гідрокси, карбамоїлу або С1-6алкокси; і Rj є вибраним з гідрокси. Конкретно, R2 являє собою сульфамоїл, N-(тетрагідрофуран-2-ілметил)сульфамоїл, N-[3-(2оксопіролідин-1-іл)пропіл]сульфамоїл, N-(3-метоксипропіл)сульфамоїл, N-(4-фторбензил)сульфамоїл, N(циклопропілметил)сульфамоїл, N-пропілсульфамоїл, N-(2,3-дигідроксипропіл)сульфамоїл, N-[2-(2гідроксіетокси)етил]сульфамоїл, N-(фуран-2-ілметил)сульфамоїл, N-(2-гідроксіетил)сульфамоїл або N(карбамоїлметил)сульфамоїл. В іншому аспекті даного винаходу, R2 , переважно, являє собою сульфамоїл або групу Ra-Rb-; де Ra є вибраним з С 1-6алкілу, С2-6алкенілу, С2-6алкінілу, С3-8циклоалкілу, фенілу або гетероциклічної групи; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg ; Rb являє собою -N(Rm)C(O)-, -C(O)N(Rm)-, -S(O)r, -OC(O)N(Rm)SO 2-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або С1-6алкіл, і r дорівнює 2; Rg є вибраним з галогену, гідрокси, аміно, ціано, карбамоїлу, С1-6алкілу, С 1-6алкокси, С1-6алкоксиС 16алкокси, С 1-6алкоксиС 1-6алкоксиС 1-6алкокси, N,N-(С 1-6алкіл)2аміно, С 1-6алкілS(О)а де а дорівнює 2, С 3o o G 8циклоалкілу, фенілу, гетероциклічної групи, фенілС 1-6алкіл-R - або (гетероциклічна група)-R -; де R може бути необов'язково заміщеним на атомі вуглецю одним або декількома R j; Ro являє собою -О-; і Rj є вибраним з галогену, гідрокси, метилу або метокси. В іншому аспекті даного винаходу, R2 , більш переважно, являє собою сульфамоїл або групу Ra-Rb-; де Ra є вибраним з метилу, етилу, пропілу, трет-бутилу, пентилу, 1,1-диметилпропілу, 2,2-диметилпропілу, алілу, 2-пропінілу, циклопропілу, циклобутилу, фенілу або оксазолілу; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rg ; Rb являє собою -N(Rm)C(O)-, -C(O)N(Rm)-, -S(O) 2-, -OC(O)N(Rm)SO 2-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або метил; Rg є вибраним з фтору, гідрокси, аміно, ціано, карбамоїлу, метилу, метокси, етокси, ізопропокси, етоксіетокси, етоксіетоксіетокси, Ν,Ν-диметиламіно, мезилу, циклопропілу, фенілу, те трагідрофуранілу, 2оксопіролідинілу, 1,3-діоксоланілу, морфоліно, піперидинілу, фурану, тіазолілу, піразинілу, ізоксазолілу, тетрагідропірану, піридилу, бензилокси, ізоксазолілокси, ізотіазолілокси, 1,2,5-тіадіазолілокси, де Rg може бути необов'язково заміщеним на атомі вуглецю одним або декількома R j; і Rj є вибраним з фтору, гідрокси, метилу або метокси. В іншому аспекті даного винаходу, конкретно, R2 являє собою сульфамоїл, N-(третбутоксикарбоніл)сульфамоїл, N-(тетрагідрофур-2-ілметил)сульфамоїл, N-(циклопропілметил)сульфамоїл, N-(фур-2-ілметил)сульфамоїл, N-(ціанометил)сульфамоїл, N-(2,2-диметил-1,3-діоксолан-4ілметил)сульфамоїл, N-(карбамоїлметил)сульфамоїл, N-метилсульфамоїл, N-(4-фторбензил)сульфамоїл, N-(піридин-2-ілметил)сульфамоїл, N-(піридин-3-ілметил)сульфамоїл, N-(4-метилтіазол-2-іл)сульфамоїл, N(3-метилізоксазол-5-ілметил)сульфамоїл, N-(тетрагідропіран-2-ілметил)сульфамоїл, N-(2-метилпіразин-5іл)сульфамоїл, N-[2-(2-гідроксіетокси)етил]сульфамоїл, N-(2-гідроксіетил)сульфамоїл, N-(2,2,2трифторетил)сульфамоїл, N-(2-метоксіетил)сульфамоїл, N-(2-мезилетил)сульфамоїл, N-(2бензилоксіетил)сульфамоїл, N-(2,2-диметоксіетил)сульфамоїл, N-[2-(N,N-димeтилaмiнo)eтил]cyльфaмoїл, N-(2-піперидин-1-ілетил)сульфамоїл, N-[2-(метоксиметокси)етил]сульфамоїл, N-етилсульфамоїл, N-[2-(2метоксіетокси)етил]сульфамоїл, N-{2-[2-(2-метоксіетокси)етокси]етил)сульфамоїл, N-(2-{2-[2-(2метоксіетокси)етокси]етокси}етил)сульфамоїл, N-(2-піридин-2-ілетил)сульфамоїл, N-(2-піридин-4ілетил)сульфамоїл, N-(2-ізоксазол-3-ілоксіетил)сульфамоїл, N-(2-ізотіазол-3-ілоксіетил)сульфамоїл, N-(21,2,5-тіадіазол-3-ілоксіетил)сульфамоїл, N-метил-N-(2-метоксіетил)сульфамоїл, N-[3-(2-оксопіролідин-1ил)пропіл]сульфамоїл, N-(3-метоксипропіл)сульфамоїл, N-пропілсульфамоїл, N-(2,3дигідроксипропіл)сульфамоїл, N-(3-морфолінопропіл)сульфамоїл, N-[3-(N,Nдиметиламіно)пропіл]сульфамоїл, N-(3,3,3-трифторпропіл)сульфамоїл, N-(2,2-диметил-3гідроксипропіл)сульфамоїл, N-(3-гідроксипропіл)сульфамоїл, N-(3-етоксипропіл)сульфамоїл, N-(2гідроксипропіл)сульфамоїл, N-(3-ізопропоксипропіл)сульфамоїл, N-(3-ізопропокси-2гідроксипропіл)сульфамоїл, N-(3-ізоксазол-3-ілоксипропіл)сульфамоїл, N-(3-ізотіазол-3ілоксипропіл)сульфамоїл, N-(3-1,2,5-тіадіазол-3-ілоксипропіл)сульфамоїл, N-(1,1диметилпропіл)сульфамоїл, N-метил-N-(3-морфолінопропіл)сульфамоїл, N-бутилсульфамоїл, N-третбутилсульфамоїл, N-(2-гідроксибутил)сульфамоїл, N-метил-N-трет-бутилсульфамоїл, N-пентилсульфамоїл, N-(5-гідроксипентил)сульфамоїл, N-(4,5-диметилоксазол-2-іл)сульфамоїл, N-(циклопропіл)сульфамоїл, N(циклобутил)сульфамоїл, N-(3-трифторметилфеніл)сульфамоїл, N-алілсульфамоїл, N-(2пропініл)сульфамоїл, N-метилкарбамоїл, ацетамідо, мезиламіно або мезил. В іншому аспекті даного винаходу, більш конкретно, R2 являє собою N-(циклопропілметил)сульфамоїл, N-(2,2,2-трифторетил)сульфамоїл, N-(2-метоксіетил)сульфамоїл, N-(3-метоксипропіл)сульфамоїл, N(циклопропіл) сульфамоїл або N-(циклобутил)сульфамоїл. Переважно, q дорівнює 0 або 1. В одному з аспектів даного винаходу, переважно, q дорівнює 0. В іншому аспекті даного винаходу, переважно, q дорівнює 1. Переважно, коли q дорівнює 1, R2 знаходиться в мета- або параположенні по відношенню до -NH-групи аніліну формули (І). Більш переважно, коли q дорівнює 1, R2 знаходиться в параположенні по відношенню до -NH-групи аніліну формули (І). Переважно, р+q=0-3. Більш переважно, р+q дорівнює 0-2. Конкретно, р+q дорівнює 0 або 1. В одному з аспектів даного винаходу, переважно, р+q дорівнює 0. В іншому аспекті даного винаходу, переважно, р+q дорівнює 1. Переважно, R3 являє собою галоген. Більш переважно, R3 являє собою бром. В іншому аспекті даного винаходу, переважно, R3 являє собою бром або хлор. Переважно, n дорівнює 0 або 1. В одному з аспектів даного винаходу, більш переважно, n дорівнює 0. В іншому аспекті даного винаходу, більш переважно, n дорівнює 1. Переважно, коли n дорівнює 1, R3 знаходиться в 5-положенні піримідинового кільця. Переважно R4 являє собою водень, С1-6алкіл, С2-6алкеніл, С2-6алкініл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; де Rd є таким, як визначено тут нижче. Більш переважно, R4 являє собою водень або С 1-6алкіл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; Rd є вибраним з аміно, С1-6алкокси, С1-6алканоїламіно, С1-6алкілсульфоніламіно, фенілу, гетероциклічної групи, або (гетероциклічна група)-Ro-; де Rd може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rj; Ro являє собою -C(O)N(Rp)-; де Rp являє собою водень; і Rj являє собою галоген. Конкретно, R4 являє собою водень або С 1-6алкіл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; Rd є вибраним з аміно, С1-6алкокси, фенілу або гетероциклічної групи. Більш конкретно, R4 являє собою водень, метил, етил, бензил, 2-фталімідоетил, 2-аміноетил або 2метоксіетил. Конкретно, переважний R4 являє собою метил або етил. В іншому аспекті даного винаходу, переважно, R4 являє собою водень, С1-6алкіл або С2-6алкеніл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома R d; де Rd є вибраним з галогену, аміно, С1-6алкокси, С1-6алканоїламіно, С1-6алкілсульфоніламіно, фенілу або гетероциклічної групи. В іншому аспекті даного винаходу, більш переважно, R4 являє собою водень, метил, етил, ізопропіл або 3-бутеніл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; де Rd є вибраним з фтору, аміно, метокси, ацетамідо, мезиламіно, фенілу або фталімідо. В іншому аспекті даного винаходу, конкретно, R4 являє собою водень, метил, етил, ізопропіл, 3-бутеніл, бензил, 2-фталімідоетил, 2-аміноетил, 2-метоксіетил, 2-ацетамідоетил, 2-мезиламіноетил або 2,2,2трифторетил. В іншому аспекті даного винаходу, більш конкретно, R4 являє собою метил, етил або ізопропіл. Переважно, R5 і R6 є незалежно вибраними з водню або С1-6алкілу. Більш переважно R5 і R6 є незалежно вибраними з водню або метилу. Конкретно, R5 є вибраним з водню або метилу, і R 6 являє собою водень. В іншому аспекті даного винаходу, переважно, R5 і R6 є незалежно вибраними з водню або С1-6алкілу; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Re; де Re є вибраним з галогену або метокси. В іншому аспекті даного винаходу, більш переважно, R5 і R6 є незалежно вибраними з водню, метилу, етилу або ізопропілу; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома Re; де Re є вибраним з фтору або метокси. В іншому аспекті даного винаходу, більш переважно, R5 і R6 є незалежно вибраними з водню, метилу, етилу, ізопропілу, трифторметилу або метоксиметилу. В іншому аспекті даного винаходу, більш переважно, R5 являє собою метил або ізопропіл, і R6 являє собою водень. З цієї причини, в іншому аспекті даного винаходу, передбачається сполука формули (І) (як показано вище) де: R1 являє собою хлор; p дорівнює 0 або 1; R2 являє собою сульфамоїл або групу Ra-Rb-; Ra є вибраним з С1-6алкілу, С3-8циклоалкілС 1-6алкілу, фенілС 1-6алкілу або (гетероциклічна група)С1a g 6алкілу; де R може бути необов'язково заміщеним на атомі вуглецю одним або декількома R ; b m m R являє собою -N(R )SO2; де R являє собою водень; Rg є вибраним з галогену, гідрокси, карбамоїлу або С1-6алкокси; Rj є вибраним з гідрокси; q дорівнює 0 або 1;p+q дорівнює 0 або 1; n дорівнює 0; R4 являє собою водень або С 1-6алкіл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; Rd є вибраним з аміно, С1-6алкокси, фенілу або гетероциклічної групи; і R5 і R6 є незалежно вибраними з водню або С 1-6алкілу; або їх фармацевтично прийнятна сіль або їх складний ефір, що гідролізується in vivo. З цієї причини, в подальшому аспекті даного винаходу, передбачається сполука формули (І) (як зображено вище), де: R1 являє собою хлор; p дорівнює 0 або 1; і, коли ρ дорівнює 1, R1 знаходиться в метаположенні по відношенню до -NH-групи аніліну формули (І); R2 являє собою сульфамоїл, N-(тетрагідрофуран-2-ілметил)сульфамоїл, N-[3-(2-оксопіролідин-1іл)пропіл]сульфамоїл, N-(3-метоксипропіл)сульфамоїл, N-(4-фторбензил)сульфамоїл, N(циклопропілметил)сульфамоїл, Ν-пропілсульфамоїл, N-(2,3-дигідроксипропіл)сульфамоїл, N-[2-(2 гідроксіетокси)етил]сульфамоїл, Ν-(фуран-2-ілметил)сульфамоїл, N-(2-гідроксіетил)сульфамоїл або Ν(карбамоїлметил)сульфамоїл; q дорівнює 0 або 1; і, коли q дорівнює 1, R2 знаходиться в параположенні по відношенню до -NH-групи аніліну формули (І); p+q дорівнює 1; n дорівнює 0; R4 являє собою метил або етил; і R5 є вибраним з водню або метилу, і R6 являє собою водень; або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo. З цієї причини, в подальшому додатковому аспекті даного винаходу, передбачається сполука формули (І) (як зображено вище), де: R1 являє собою галоген, аміно, С1-6алкіл або С1-6алкокси; р дорівнює 0-2; де значення R1 можуть бути однаковими або різними; R2 являє собою сульфамоїл або групу Ra-Rb-; де Ra є вибраним з С 1-6алкілу, С2-6алкенілу, С2-6алкінілу, С3-8циклоалкілу, фенілу або гетероциклічної групи; де Ra може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rs; Rb являє собою -N(Rm)C(O)-, -C(O)N(Rm)-, -S(O)r-, -OC(O)N(Rm)SO2-, -SO2N(Rm)- або -N(Rm)SO2-; де Rm являє собою водень або С1-6алкіл, і r дорівнює 2; Rg є вибраним з галогену, гідрокси, аміно, ціано, карбамоїлу, С1-6алкілу, С 1-6алкокси, С1-6алкоксиС 16алкокси, С 1-6алкоксиС 1-б алкоксиС 1-6алкокси, N,N-(С 1-6алкіл)2аміно, С 1-6алкілS(O)а де а дорівнює 2, С 3o o g 8циклоалкілу, фенілу, ге тероциклічної групи, фенілС 1-6алкіл-R - або (гетероциклічна rpyna)-R -; де R може бути необов'язково заміщеним на атомі вуглецю одним або декількома R j; Ro являє собою -O-; Rj є вибраним з галогену, гідрокси, метилу або метокси; q дорівнює 0 або 1; R3 являє собою галоген; n дорівнює 0 або 1; R4 являє собою водень, С1-6алкіл або С 2-б алкеніл; де R4 може бути необов'язково заміщеним на атомі вуглецю одним або декількома Rd; де Rd є вибраним з галогену, аміно, С1-6алкокси, С1-6алканоїламіно, С1-6алкілсульфоніламіно, фенілу або гетероциклічної групи; і R5 і R6 є незалежно вибраними з водню або С 1-6алкілу; де R5 і R6 незалежно один від одного можуть бути необов'язково заміщеними на атомі вуглецю одним або декількома R e; де Re є вибраним з галогену або метокси, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo. З цієї причини, в іншому подальшому додатковому аспекті даного винаходу, передбачається сполука формули (І) (як зображено вище), де: R1 являє собою хлор, аміно, метил або метокси, p дорівнює 0-2; де значення R 1 можуть бути однаковими або різними; R2 являє собою сульфамоїл, N-(тетрагідрофур-2-ілметил)сульфамоїл, Ν(циклопропілметил)сульфамоїл, N-(фур-2-ілметил)сульфамоїл, N-(2,2-диметил-1,3-діоксолан-4ілметил)сульфамоїл, N-(ціанометил)сульфамоїл, N-(карбамоїлметил)сульфамоїл, N-метилсульфамоїл, N(4-фторбензил)сульфамоїл, N-(піридин-2-ілметил)сульфамоїл, N-(піридин-3-ілметил)сульфамоїл, N-(4метилтіазол-2-іл)сульфамоїл, N-(3-метилізоксазол-5-ілметил)сульфамоїл, N-тетрагідропіран-2ілметил)сульфамоїл, N-(2-метилпіразин-5-іл)сульфамоїл, N-[2-(2-гідроксіетокси)етил]сульфамоїл, N-(2гідроксіетил)сульфамоїл, N-(2,2,2-трифторетил)сульфамоїл, N-(2-мeтoкcieтил)cyльфaмoїл, N-(2-мeзилeтил) сульфамоїл, N-(2-бензилоксіетил)сульфамоїл, N-(2,2-диметоксіетил)сульфамоїл, N-[2-(N,Nдимeтилaмiнo)eтил]cyльфaмoїл, N-(2-піперидин-1-ілетил)сульфамоїл, N-[2(метоксиметокси)етил]сульфамоїл, N-етилсульфамоїл, N-[2-(2-метоксіетокси)етил]сульфамоїл, N-{2-[2-(2метоксіетокси)етокси]етил}сульфамоїл, N-(2-{2-[2-(2-метоксіетокси)етокси]етокси}етил)сульфамоїл, N-(2піридин-2-ілетил)сульфамоїл, N-(2-піридин-4-ілетил)сульфамоїл, N-(2-iзoкcaзoл-3-iлoкcieтил)cyльфaмoїл, N-(2-ізотіазол-3-ілоксіетил)сульфамоїл, N-(2-1,2-5-тіадіазол-3-ілоксіетил)сульфамоїл, N-мeтил-N-(2мeтoкcieтил)cyльфaмoїл, N-[3-(2-oкcoпipoлiдин-l-iл)пpoпiл]сульфамоїл, N-(3-метоксипропіл)сульфамоїл, Nпропілсульфамоїл, N-(2,3-дигідроксипропіл)сульфамоїл, N-(3-морфолінопропіл)сульфамоїл, N-[3-(N,Nдиметиламіно)пропіл]сульфамоїл, N-(3,3,3-трифторпропіл)сульфамоїл, N-(2,2-диметил-3гідроксипропіл)сульфамоїл, N-(3-гiдpoкcипpoпiл)cyльфaмoїл, N-(3-етоксипропіл)сульфамоїл, N-(2гідроксипропіл)сульфамоїл, N-(3-ізопропоксипропіл)сульфамоїл, N-(3-ізопропокси-2-гідроксипропіл) сульфамоїл, N-(3-ізоксазол-3-ілоксипропіл)сульфамоїл, N-(3-ізотіазол-3-ілоксипропіл)сульфамоїл, N-(3-1,25-тіадіазол-3-ілоксипропіл)сульфамоїл, N-(1,1-диметилпропіл)сульфамоїл, N-метил-N-(3морфолінопропіл)сульфамоїл, N-бутилсульфамоїл, N-трет-бутилсульфамоїл, N-(2гідроксибутил)суль фамоїл, N-метил-трет-бутилсульфамоїл, N-пентилсульфамоїл, N-(5гідроксипентил)сульфамоїл, N-(4,5-диметилоксазол-2-іл)сульфамоїл, N-(циклопропіл)сульфамоїл, N(циклобутил)сульфамоїл, N-(3-трифторметилфеніл)сульфамоїл, N-алілсульфамоїл, N-(2пропініл)сульфамоїл, N-метилкарбамоїл, ацетамідо, мезиламіно або мезил; q дорівнює 0 або 1; R3 являє собою бром або хлор; n дорівнює 0 або 1; R4 являє собою водень, метил, етил, ізопропіл, 3-бутенін, бензил, 2-фталімідоетил, 2-аміноетил, 2метоксіетил, 2-ацетамідоетил, 2-мезиламіноетил або 2,2,2-трифторетил; R5 і R6 є незалежно вибраними з водню, метилу, етилу, ізопропілу, трифторметилу або метоксиметилу; або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo. В іншому аспекті даного винаходу, переважні сполуки згідно з даним винаходом являють собою будьяку сполуку з представлених прикладів або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo. Ще в одному аспекті даного винаходу, переважні сполуки даного винаходу являють собою сполуки, одержані в прикладах 25, 37, 42, 43, 53, 61, 121, 122, 123 і 136. Переважні аспекти даного винаходу являють собою такі аспекти, які відносяться до сполуки формули (І) або до її фармацевтично прийнятної солі. Інший аспект даного винаходу передбачає спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі або її складного ефіру, що гідролізується in vivo, цей спосіб (де R1, R2, R3, R4, R 5, R 6, n, p і q, якщо не вказано іншого, є такими, як визначено в формулі (І)), складається з: Способу а) взаємодії піримідину формули (II): де L являє собою групу, що замінюється; з аніліном формули (III): або Способу b) взаємодії сполуки формули (IV): із сполукою формули (V): де Τ являє собою О або S; R x можуть бути однаковими або різними, і є вибраними з С 1-6алкілу; Способу с) для сполук формули (І), де R2 являє собою сульфамоїл або групу R a-Rb-, і Rb являє собою NHSO2-; взаємодії піримідину формули (VI): де X являє собою гр упу, що замінюється; з аміном формули (VII): Способу d) для сполук формули (І); взаємодії піримідину формули (VIII) із сполукою формули (IX): де Υ являє собою гр упу, що замінюється; і після цього, якщо необхідно: і) перетворення сполуки формули (І) в іншу сполук у формули (І); іі) видалення будь-яких захисних гр уп; ііі) утворення фармацевтично прийнятної солі або складного ефіру, що гідролізується in vi vo. L являє собою групу, що замінюється, придатні для використання значення для L являють собою, наприклад, галогенову або сульфонілоксигрупу, наприклад хлор, бром, метансульфонілокси або толуол-4сульфонілоксигрупу. X являє собою групу, що замінюється, придатні для використання значення для X являють собою, наприклад, групу фтору або хлор у. Переважно, X являє собою фтор. Υ являє собою групу, що замінюється, придатні для використання значення для Υ являють собою, наприклад, галогенову або сульфонілокси групу, наприклад, бром, йод або трифторметансульфонілоксигрупу. Переважно, Υ являє собою йод. Конкретні умови реакції для вказаних вище реакцій є наступними. Спосіб а) Піримідини формули (II) і аніліни формули (III) можуть взаємодіяти разом: і) в присутності відповідного розчинника, наприклад, кетону, такого як ацетон, або спирту, такого як етанол або бутанол, або ароматичного вуглеводню, такого як толуол або N-метилпіролідин, необов'язково, в присутності відповідної кислоти, наприклад, неорганічної кислоти, такої як хлористоводнева кислота або сірчана кислота, або органічної кислоти, такої як оцтова кислота або мурашина кислота (або відповідної кислоти Л'юїса) і при температурі в межах від 0°С до температури кипіння, переважно, при температурі кипіння; або іі) при стандартних умовах Бухвальда [наприклад, дивись J. Am. Chem. Soc, 118, 7215; J. Am. Chem. Soc, 119, 8451; J. Org. Chem., 62, 1568 and 6066], наприклад, в присутності ацетату паладію, у відповідному розчиннику, наприклад, в ароматичному розчиннику, такому як толуол, бензол або ксилол, з відповідною основою, наприклад, з неорганічною основою, такою як карбонат цезію, або з органічною основою, такою як трет-бутоксидкалій, в присутності відповідного ліганду, такого як 2,2'-біс(дифенілфосфіно)-1,1'-бінафтил, і при температурі в інтервалі від 25 до 80°С. Піримідини формули (II), де L являє собою хлор, можуть бути приготовлені відповідно до схеми 1: Аніліни формули (III) є комерційно доступними сполуками, або вони відомі з літератури, або вони приготовляються за допомогою стандартних способів, відомих в даній області. Спосіб b) Сполуки формули (IV) і сполуки формули (V) взаємодіють разом у відповідному розчиннику, такому як N-метилпіролідинон або бутанол, при температурі в інтервалі 100-200°С, переважно, в інтервалі 150-170°С. Взаємодія переважно проводиться в присутності відповідної основи, такої, наприклад, як гідрид натрію, метоксид натрію або карбонат калію. Сполуки формули (V) можуть бути приготовлені відповідно до схеми 2: Сполуки формули (IV) і (Va) є комерційно доступними сполуками, або вони відомі з літератури, або вони приготовляються за допомогою стандартних способів, відомих в даній області. Спосіб с) Сполуки формули (VI) і аміни формули (VII) можуть взаємодіяти разом в присутності інертного розчинника, такого як N-метилпіролідинон або піридин, в присутності основи, наприклад, неорганічної основи, такої як карбонат цезію, або в присутності органічної основи, такої як надлишок (VII), і при температурі в інтервалі від 25 до 80°С. Сполуки формули (VI) (де X являє собою хлор) можуть бути приготовлені відповідно до схеми 3: Сполуки формули (VIa) можуть бути приготовлені відповідно до способу а, способу b або способом d, де q дорівнює 0. Спосіб d) Сполуки формули (VIII) і аміни формули (IX) можуть взаємодіяти разом при стандартних умовах Бухвальда, як описано в способі а. Синтез сполук формули (VIII) описаний в схемі 1. Сполуки формули (IX) є комерційно доступними сполуками, або вони відомі з літератури, або вони приготовляються за допомогою стандартних способів, відомих в даній області. Аміни формули (VI) є комерційно доступними сполуками, або вони відомі з літератури, або вони приготовляються за допомогою стандартних способів, відомих в даній області. Деякі з різних кільцевих замісників в сполуках згідно з даним винаходом можуть бути введені за допомогою стандартних реакцій ароматичного заміщення або генеруватися за допомогою звичайних модифікацій функціональних груп, або до, або безпосередньо після процесів, розглянутих вище, і, як такі, включаються в аспект способу даного винаходу. Такі взаємодії і модифікації включають в себе, наприклад, введення замісника за допомогою реакції ароматичного заміщення, відновлення замісників, алкілування замісників і окислення замісників. Реагенти і реакційні умови для таких процедур є добре відомими в області хімії. Конкретні приклади реакцій ароматичного заміщення включають в себе введення нітрогрупи з використанням концентрованої азотної кислоти, введення ацильної групи з використанням, наприклад, ацилгалогеніду і кислоти Л'юїса (такої як трихлорид алюмінію) в умовах Фриделя-Крафтса; введення алкільної групи з використанням алкілгалогеніду і кислоти Л'юїса (такої як трихлорид алюмінію) в умовах Фриделя-Крафтса; і введення групи галогену. Конкретні приклади модифікацій включають в себе відновлення нітрогрупи до аміногрупи, наприклад, шляхом каталітичного гідрування за допомогою нікелевого каталізатора, або обробку за допомогою заліза в присутності хлористоводневої кислоти при нагріванні; окислення алкілтіо до алкілсульфінілу або алкілсульфонілу. Можна також помітити, що в деяких з реакцій, розглянутих тут, може бути необхідним/бажаним захищати які-небудь чутливі групи в сполуках. Випадки, де захист є необхідним або бажаним, і відповідні способи для захисту відомі фахівцям в даній області. Можуть бути використані звичайні захисні групи відповідно до стандартної практики [ілюстрації дивись в T.W. GReen, Protective Groups in Organic Synthesis, John Wiley and Sons, 1991]. Таким чином, якщо реагенти включають в себе такі групи як аміно, карбокси або гідрокси, може виявитися бажаним захищати гр упу в деяких з реакцій, що розглядаються тут. Придатна для використання захисна група для аміно або алкіламіногрупи являє собою, наприклад, ацильну груп у, наприклад, алканоїльну груп у, таку як ацетильна, алкоксикарбонільна група, наприклад, метоксикарбонільна, етоксикарбонільна або трет-бутоксикарбонільна група, арилметоксикарбонільна група, наприклад, бензилоксикарбонільна або ароїльна група, наприклад, бензоїльна. Умови зняття захисту вказаних вище захисних груп за необхідністю розрізнюються в залежності від вибору захисної групи. Так, наприклад, ацильна група, така як алканоїльна або алкоксикарбонільна група, або ароїльна група, може бути видалена, наприклад, шляхом гідролізу за допомогою відповідної основи, такої як гідроксид лужного металу, наприклад, гідроксид літію або натрію. Альтернативно, ацильна група, така як третбутоксикарбонільна група, може бути видалена, наприклад, шляхом обробки за допомогою відповідної кислоти, такою як хлористоводнева, сірчана або фосфорна кислота, або трифтороцтова кислота, і арилметоксикарбонільна група, така як бензилоксикарбонільна група, може бути видалена, наприклад, шляхом гідрування над каталізатором, таким як паладій-на-вугіллі, або шляхом обробки за допомогою кислоти Л'юїса, наприклад, бортрис(трифторацетату). Відповідна альтернативна захисна група для первинної аміногрупи являє собою, наприклад, фталоїльну групу, яка може бути видалена шляхом обробки за допомогою алкіламіну, наприклад, диметиламінопропіламіну, або за допомогою гідразину. Відповідна захисна група для гідроксигрупи являє собою, наприклад, ацильну груп у, наприклад, алканоїльну груп у, таку як ацетильна, ароїльна група, наприклад, бензоїльна, або арилметильна група, наприклад, бензильна. Умови для зняття захисту з вказаних вище захисних гр уп будуть змінюватися в залежності від вибору захисної гр упи. Так, наприклад, ацильна група, така як алканоїльна або ароїльна група, може бути видалена, наприклад, шляхом гідролізу за допомогою відповідної основи, такої як гідроксид лужного металу, наприклад, гідроксид літію або натрію. Альтернативно, арилметильна група, така як бензильна група, може бути видалена, наприклад, шляхом гідрування над каталізатором, таким як паладій-на-вугіллі. Відповідна захисна група для карбоксигрупи являє собою, наприклад, етерифікуючу гр упу, наприклад, метильну або етильну груп у, яка може бути видалена, наприклад, шляхом гідролізу за допомогою основи, такої як гідроксид натрію, або, наприклад, трет-бутильну гр упу, яка може бути видалена, наприклад, шляхом обробки за допомогою кислоти, наприклад, органічної кислоти, такої як трифтороцтова кислота, або, наприклад, бензильну гр упу, яка може бути видалена, наприклад, шляхом гідрування над каталізатором, таким як паладій-на-вугіллі. Захисні групи можуть бути видалені на будь-якій зручній стадії синтезу, з використанням звичайних методик, добре відомих в даній області. Як затверджувалося вище, сполуки, що визначаються в даному винаході, володіють активністю проти проліферації клітин, такою як протиракова активність, яка, як передбачається, виникає в зв'язку з інгібіторною активністю сполуки по відношенню до CDK. Ці властивості можуть бути оцінені, наприклад, з використанням процедури, приведеної нижче: Аналізи Використовуються наступні скорочення: HEPES являє собою N-[2-гідроксіетил]піперазин-N'-[2-етансульфонову кислоту] DTT являє собою дитіофреітол PMSF являє собою фенілметилсульфонілфторид Сполуки досліджуються за допомогою аналізу кінази in vitro в 96-ямковому форматі з використанням Scintillation Proximity Assay (SPA - одержано від Amersham) для вимірювання включення [g-33-Р]аденозинтрифосфату в субстрат, що досліджується (білок ретинобластоми - GST; GST-Rb). У кожну ямку вміщується сполука, що підлягає дослідженню (розбавлена в ДМСО і у воді, для коректування концентрацій), а в контрольні ямки або росковітин як інгібіторний контроль, або ДМСО як позитивний контроль. У кожну ямку додають приблизно 0,2мкл частково очищених ферменту СБK2/циклін Ε (кількість залежить від активності ферменту), розбавленого в 25мкл інкубаційного буферу, а потім 20мкл суміші GSTRb/ATP/АТР33 (містить 0,5мкг GST-Rb і 0,2мкМ АТР, і 0,14мккюрі [g-33-Р]-аденозинтрифосфату в інкубаційному буфері), і одержану в результаті суміш обережно струшують, а потім інкубують при кімнатній температурі протягом 60 хвилин. Потім в кожну ямку додають по 150мкл стоп-розчину, що містить (0,8мг/ямка кульок Protein A-PVT SPA (Amersham)), 20пМ/ямка антиглютатіон трансферази, IgG кролика (одержаний від Molecular Probes), 61мМ EDTA і 50мМ HEPES, рН 7,5, що містить 0,05% азиду натрію. Планшети герметизують за допомогою ущільнень для планшетів Topseal-S, залишають на дві години, а потім центрифугують при 2500об/хв, 1124 x g, протягом 5 хвилин. Здійснюють відліки планшетів на Topcount, по 30 секунд на кожну ямку. Інкубаційний буфер, що використовується для розбавлення сумішей ферменту і субстрату, містить 50мМ HEPES, рН 7,5, 10мМ МnСl2, 1мМ DTT, 100мкМ ванадату натрію, 100мкМ NaF, 10мМ гліцерофосфату натрію, BSA (кінцева концентрація 1мг/мл). Субстрат, що досліджується У цьому аналізі використовується тільки частина білка ретинобластоми [Science 1987 Маr 13;235(4794):1394-1399; Lee W.H., Bookstein R., Hong F., Young L.J., Shew J.Y., Lee E.Y.], злитого з міткою GST. Здійснюють PCR гена ретинобластоми, що кодує амінокислоти 379-928, (одержані від плазміда ретинобластоми АТСС pLRbRNL), і послідовність клонується у вектор злиття pGEx 2T [Smith D.B. and Johnson, K.S. Gene 67, 31 (1988)]: який містить промотор tac для експресії, що індукується, внутрішній ген lac Iq для використання в якій-небудь клітині-хазяїні Е.Соlі, і кодуючий регіон для розщеплення тромбіну (одержаний від Pharmacia Biotech), який використовується для ампліфікації амінокислот 792-928. Ця послідовність знову клонується в pGEx 2T. Послідовність 792-928 ретинобластоми, одержана таким чином, експресується в Е.Соlі (клітини BL21 (DE3) pLysS), використовуючи методики експресії, що індукується, і очищають таким чином. Пасту Е.соlі повторно суспендують в 10мл/г буфері NETN (50мМ Tris, рН 7,5, 120мМ NaCl, 1мМ EDTA, 0,5%об./об. NP-40, 1мМ PMSF, 1мкг/мл лейпептину, 1мкг/мл апротиніну і 1мкг/мл пепстатину) і обробляють ультразвуком протягом 2´45 секунд на 100мл гомогенату. Після центрифугування супернатант завантажують в 10мл глютатіону в колонку Sepharose (Pharmacia Biotech, Herts, UK) і промивають буфером NETN. Після промивання кіназним буфером (50мМ HEPES, рН 7,5, 10мМ MgCl2, 1мМ DTT, 1мМ PMSF, 1мкг/мл лейпептину, 1мкг/мл апротиніну і 1мкг/мл пепстатину), білок елююють за допомогою 50мМ відновленого глютатіону в кіназному буфері. Фракції, що містять GST-Rb (792-927), збирають і піддають діалізу протягом ночі з кіназним буфером зовні. Кінцевий продукт аналізують за допомогою гельелектрофорезу (поліакриламідний гель), з використанням додецилсульфату натрію (SDS), використовуючи гелі на основі 8-16% Трис-гліцину (Novex, San Diego, USA). CDK2 і циклін Е Відкриті рамки зчитування CDK2 і цикліну Ε виділяють за допомогою PCR із зворотною траскриптазою, використовуючи мРНК клітин HeLa і активованих Τ лімфоцитів як шаблони, і клонують у вектор експресії комах pVL1393 (одержують від In vitrogen 1995, номер за каталогом: V1392-20). Потім CDK2 і циклін Ε дуально експресують [використовуючи стандартну те хніку спільного інфікування вірусом Baculogold] в клітинну систему комах SF21 (клітини Spodoptera Frugiperda, одержані з тканини яєчників Fall Army Worm комерційно доступні). Приклад продукування цикліну E/CDK2 Наступний далі приклад приводить деталі продукування цикліну E/CDK2 в клітинах SF21 (в ТС 100 + 10% FBS (TCS) + 0,2% Pluronic), що одержали дуальне інфікування МОl 3 кожним вірусом, цикліном Ε і CDK2. Клітини SF21, вирощені в культурі у флаконі, що обертається, до кількості 2,33´10бклітин/мл, використовуються для інокуляції 10´500мл колб, що обертаються, при 0,2´106клітин/мл. Флакони, що обертаються, інкубують на стійці, що обертається, при 28°С. Через 3 дні (72 години), роблять підрахунок клітин, і середнє значення для 2 флаконів, як виявлено, становить 1,86´10б клітин/мл (99% життєздатних). Потім культури інфікуються дуальними вірусами при МОl 3 для кожного вірусу. Віруси змішуються разом перед доданням до культур, і культури повертають на стійку, що обертається, при 28°С. Через 2 дні (48 годин) після інфікування, збирають 5 літрів культури. Загальна кількість клітин при зборі становить 1,58´106клітин/мл (99% життєздатність). Клітини центрифугують при 2500об/хв, 30хв., 4°С, в Heraeus Omnifuge 2,0 RS, порціями по 250мл. Супернатант зливають. Часткове спільне очищення CDK2 і цикліну Ε Клітини SF21 повторно суспендують в лізисному буфері (50мМ Tris, pH 8,2, 10мМ MgCl2, 1мМ DTT, 10мМ гліцерофосфату, 0,1мМ ортованадату натрію, 0,1мМ NaF, 1мМ PMSF, 1мкг/мл лейпептину і 1мкг/мл апротиніну) і гомогенізують протягом 2 хвилин в 10мл гомогенізаторі Dounce. Після центрифугування, супернатант завантажують в аніонообмінну колонку Poros HQ/M 1,4/100 (ΡΕ Biosystems, Hertford, UK). CDK2 і циклін Е спільно елююються на початку проходження 0-1Μ градієнта NaCl (здійснюють в лізисному буфері мінус інгібітори протеази), в 20 об'ємах колонки. Спільне елюювання відстежується за допомогою вестернблотингу з використанням антитіл як проти CDK2, так і проти цикліну Ε (Santa Cruz Biotechnology, California, US). Аналогічно, можуть бути побудовані аналізи, сконструйовані для оцінки інгібування CDK4 і CDK6. CDK2 (№ доступу EMBL X62071) може бути використаний разом з цикліном А або цикліном Ε (дивись EMBL, номер доступу М73812), і подальші деталі таких аналізів містяться в Міжнародній публікації РСТ №W099/21845, відповідні розділи Біохімічна і Біологічна Оцінка з якої включаються сюди як посилання. Хоча фармакологічні властивості сполук формули (І) змінюються разом з структурними змінами, загалом, активність, якою володіють сполуки формули (І), може бути продемонстрована при концентраціях або дозах ІС50 в межах від 250мкМ до 1нМ. При дослідженні у вказаному ви ще аналізі in vitro, інгібіторна активність CDK2 з прикладу 14 виміряна як ІС 50=0,146мкМ. Активність in vi vo сполук згідно з даним винаходом може бути оцінена за допомогою стандартних методик, наприклад, шляхом вимірювання інгібування зростання клітин і оцінки цитотоксичності. Інгібування зростання клітин може бути виміряно шляхом фарбування клітин за допомогою сульфородаміну В (SRB), флуоресцентного барвника, який забарвлює білки, і, як наслідок, дає оцінку кількості білка (тобто клітин) в ямці [дивись Boyd, M.R. (1989) Status of the NCI preclinical antitumour drug discovery screen. Prin. Prac Oncol 10:1-12]. Таким чином, при вимірюванні інгібування зростання клітин передбачаються наступні деталі: Клітини у відповідному середовищі, в об'ємі 100мкл, вміщуються в 96 ямкові планшети; середовища являють собою модифіковані Дюльбекко середовища Ігла для MCF-7, SK-UT-1B і SK-UT-1. Клітинам дають можливість прикріпитися протягом ночі, потім додають інгібіторні сполуки при різних концентраціях, при максимальній концентрації 1% ДМСО (об'єм/об'єм). Контрольний планшет аналізується для одержання значення для кількості клітин перед дозуванням. Клітини інкубуються при 37°С, (5% СО2) протягом трьох днів. Після проходженні трьох днів, в планшети додають ТСА до кінцевої концентрації 16% (об'єм/об'єм). Потім планшети інкубують при 4°С протягом 1 години, супернатант видаляють, і планшети промивають у водопровідній воді. Після сушіння додають 100мкл барвника SRB (0,4% SRB в 1% оцтовій кислоті), протягом 30 хвилин, при 37°С. Надлишок SRB видаляють і планшети промивають в 1% оцтовій кислоті. SRB, пов'язаний з білком, солюбілізують в 10мМ Tris, pH 7,5, і струшують протягом 30 хвилин при кімнатній температурі. Значення OD реєструють при 540нм, і концентрація інгібітору, що викликає 50% інгібування росту, визначається за напівлогарифмічним графіком концентрації інгібітору як функції коефіцієнта поглинання. Концентрація сполуки, яка знижує оптичну щільність до значення, більш низького, ніж те, яке виходить, коли клітини вміщуються в планшет на початку експерименту, дає значення для токсичності. Типові значення lС50 для сполук згідно з даним винаходом, коли вони досліджуються в аналізі з використанням SRB, знаходяться в межах від 1мМ до 1н М. Відповідно до подальшого аспекту даного винаходу, передбачається фармацевтична композиція, яка містить піримідинове похідне формули (І), або його фармацевтично прийнятну сіль, або його складний ефір, що гідролізується in vivo, як визначено вище, в поєднанні з фармацевтично прийнятним розріджувачем або носієм. Композиція може знаходитися в формі, придатній для використання при пероральному введенні, наприклад, у вигляді таблетки або капсули, для парентеральної ін'єкції (включаючи внутрішньовенну, підшкірну, внутрішньом'язову, вн утрішньосудинну ін'єкцію або вливання), у вигляді стерильного розчину, суспензії або емульсії, для місцевого введення, у вигляді мазі або крему, або для ректального введення, у вигляді супозиторію. Як правило, вказані вище композиції можуть бути приготовлені звичайним способом, з використанням звичайних розріджувачів. Сполука формули (І), як правило, може бути введена теплокровній тварині, при одиничній дозі, що знаходиться в межах 5-5000мг на квадратний метр поверхні тіла тварини, тобто, приблизно 0,1-100мг/кг, і це, як правило, забезпечує терапевтично-ефективну дозу. Одинична дозована форма, така як таблетка або капсула, повинна, як правило, містити, наприклад, 1-250мг активного інгредієнта. Переважно, використовується денна доза в межах 1-50мг/кг. Однак щоденна доза за необхідністю буде мінятися, в залежності від суб'єкта, що піддається лікуванню, конкретного способу введення і тяжкості захворювання, яке зазнає лікування. Відповідно до цього, оптимальна доза може бути визначена лікуючим лікарем, який лікує конкретного пацієнта. Відповідно до подальшого аспекту даного винаходу, створюється сполука формули (І) або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo, як визначено вище, для використання в способі лікування організму людини або тварини за допомогою терапії. Автори виявили, що сполуки, що визначаються в даному винаході, або їх фармацевтично прийнятна сіль або їх складний ефір, що гідролізується in vivo, є ефективними інгібіторами клітинного циклу (агентами проти проліферації клітин), як передбачається, ця властивість виникає через їх властивості відносно інгібування CDK. Відповідно, сполуки згідно з даним винаходом, як очікується, є придатними для використання при лікуванні захворювань або медичних станів, що опосередковуються повністю або частково, ферментами CDK, тобто сполуки можуть використовуватися для надання інгібіторного впливу на CDK у теплокровної тварини, потребуючої такого лікування. Таким чином, сполуки згідно з даним винаходом передбачають спосіб лікування проліферації злоякісних клітин, інгібуванням ферментів, що характеризується CDK, тобто ці сполуки можуть бути використані для надання протипроліферативного впливу, що опосередковується повністю або частково інгібуванням CDK. Така сполука згідно з даним винаходом, як очікується, володіє широким набором протиракових властивостей, оскільки CDK беруть участь в розвитку багатьох поширених ракових захворюваннях у людей, таких як лейкемія і рак грудей, легенів, товстої кишки, прямої кишки, шлунка, простати, сечового міхура, підшлункової залози і яєчників. Таким чином, очікується, що сполука згідно з даним винаходом буде володіти протираковою активністю по відношенню до цих ракових захворювань. У доповнення до цього, очікується, що сполука згідно з даним винаходом буде володіти активністю проти ряду лейкемій, злоякісних захворювань лімфатичної системи і солідних пухлин, такий як карциноми і саркоми, в таких тканинах, як печінка, нирки, простата і підшлункова залоза. Конкретно, такі сполуки згідно з даним винаходом, як очікується, переважно сповільнюють зростання первинних і вторинних солідних пухлин, наприклад, товстої кишки, грудей, простати, легенів і шкіри. Більш конкретно, такі сполуки згідно з даним винаходом або їх фармацевтично прийнятна сіль, або їх складний ефір, що гідролізується in vivo, як очікується, інігбують зростання тих первинних і вторинних солідних пухлин, які асоціюються з CDK, особливо тих п ухлин, які істотно залежать від CDK при їх зростанні і поширенні, включаючи, наприклад, певні пухлини товстої кишки, грудей, простати, легенів, жіночих зовнішніх статеви х органів і шкіри. У доповнення до цього, очікується, що сполука згідно з даним винаходом буде володіти активністю проти інших захворювань, пов'язаних з проліферацією клітин, в широкому діапазоні інших хворобливих станів, включаючи різні види лейкемії, фібропроліферативні і диференціаційні розлади, псоріаз, ревматоїдний артрит, саркому Капоши, хемангіому, гострі і хронічні невропатії, атерому, атеросклероз, артеріальний рестеноз, аутоімунні захворювання, гострі і хронічні запалення, захворювання кісток і захворювання очей з проліферацією ретинальних судин. Таким чином, відповідно до цього даний винахід відноситься до сполуки формули (І) або її фармацевтично прийнятної солі або її складного ефіру, що гідролізується in vivo, як визначено вище, для використання як лікарського засобу; і використанню сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, як визначено вище, для одержання лікарського засобу для продукування інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровної тварини, такої як людина. Зокрема, інгібіторний вплив проводиться шляхом запобігання входу або розвитку в S фазі шляхом інгібування CDK2, CDK4 і/або CDK6, особливо, CDK2. Відповідно до подальшої особливості даний винахід відноситься до сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, як визначено тут вище, для одержання лікарського засобу, призначеного для лікування ракових захворювань (солідних пухлин і різних видів лейкемії), фібропроліферативних і диференціаційних розладів, псоріазу, ревматоїдного артриту, саркоми Капоши, хемангіоми, гострих і хронічних невропатій, атероми, атеросклерозу, артеріального рестенозу, аутоімунних захворювань, гострих і хронічних запалень, захворювання кісток і захворювання очей з проліферацією ретинальних судин, зокрема, при лікуванні ракових захворювань. Крім того, даний винахід відноситься до способу продукування інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровної тварини, такої як людина, потребуючої такого лікування, який включає в себе введення вказаній тварині ефективної кількості сполуки, як визначено безпосередньо вище. Зокрема, інгібіторний вплив здійснюється шляхом запобігання входу або розвитку в S фазі шляхом інгібування CDK2, CDK4 і/або CDK6, особливо, CDK2. Даний винахід також відноситься до способу продукування інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровної тварини, такої як людина, потребуючої такого лікування, який включає в себе введення вказаній тварині ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vi vo, як визначено тут ви ще. Зокрема, інгібіторний вплив здійснюється шляхом запобігання входу або розвитку в S фазі шляхом інгібування CDK2, CDK4 і/або CDK6, особливо, CDK2. Більш того даний винахід відноситься до способу лікування ракових захворювань (солідних пухлин і різних видів лейкемії), фібропроліферативних і диференціаційних розладів, псоріазу, ревматоїдного артриту, саркоми Капоши, хемангіоми, гострих і хронічних невропатій, атероми, атеросклерозу, артеріального рестенозу, аутоімуних захворювань, гострого і хронічного запалення, захворювання кісток і захворювання очей з проліферацією ретинальних судин, у теплокровних тварин, таких як людина, потребуючих такого лікування, який включає в себе введення вказаній тварині ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vi vo, як визначено тут ви ще. Зокрема, передбачається спосіб лікування ракового захворювання у теплокровної тварини, такої як людина, потребуючої такого лікування, який включає в себе введення вказаній тварині ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vi vo, як визначено тут ви ще. У подальшому аспекті даного винаходу передбачається фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, як визначено тут вище, в поєднанні з фармацевтично прийнятним розріджувачем або носієм, придатна для продукування інгібіторного впливу на клітинний цикл (проти проліферації клітин) у теплокровної тварини, такої як людина. У подальшому аспекті даного винаходу передбачається фармацевтична композиція, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, як визначено тут вище, в поєднанні з фармацевтично прийнятним розріджувачем або носієм, придатна при лікуванні ракових захворювань (солідних пухлин і різних видів лейкемії), фібропроліферативних і диференціаційних розладів, псоріазу, ревматоїдного артриту, саркоми Капоши, хемангіоми, гострих і хронічних невропатій, атероми, атеросклерозу, артеріального рестенозу, аутоімунних захворювань, гострих і хронічних запалень, захворювання кісток і захворювання очей з проліферацією ретинальних судин, у теплокровної тварини, такої як людина. Далі даний винахід відноситься до фармацевтичної композиції, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, як визначено тут ви ще, в поєднанні з фармацевтично прийнятним розріджувачем або носієм, придатної при лікуванні ракового захворювання у теплокровної тварини, такої як людина. Запобігання синтезу ДНК клітинами шляхом інгібування основної ініціюючої активності при входженні в S фазу, такої як ініціація CDK2, може бути корисним також при захисті нормальних клітин організму від токсичності циклоспецифічних фармацевтичних агентів. Інгібування CDK2 або 4 буде запобігати розвитку клітинного циклу у нормальних клітин, що могло б обмежувати токсичність циклоспецифічних фармацевтичних агентів, які діють в S фазі, в G2 фазі або при мітозі. Такий захист може приводити до запобігання втраті волосся, звичайно пов'язаній із застосуванням цих агентів. З цієї причини, в подальшому аспекті даного винаходу передбачається сполука формули (І), як визначено вище, або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo, для використання як агента для захисту клітин. З цієї причини, в подальшому аспекті даного винаходу передбачається сполука формули (І), як визначено тут ви ще або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo, для використання при запобіганні втраті волосся, що відбувається при лікуванні злоякісних станів за допомогою фармацевтичних агентів. Приклади фармацевтичних агентів для лікування злоякісних станів, які, як відомо, викликають втрату волосся, включають в себе алкілуючі агенти, такі як іфосфамід і циклофосфамід; антиметаболіти, такі як метотрексат, 5-фтороурацил, гемцитабін і цитарабін; vinca алкалоліди і аналоги, такі як вінкристин, вінбалстин, віндезин, вінорелбін; таксани, такі як паклітаксель і доцетаксель; інгібітори топоізомерази І, такі як іринтотекан і топотекан; цитоксичні антибіотики, такі як доксорубіцин, даунорубіцин, мітоксантрон, актиноміцин-D і мітоміцин; і інші, такі як етопозид і третиноїн. В іншому аспекті даного винаходу, сполука формули (І) або її фармацевтично прийнятна сіль, або її складний ефір, що гідролізується in vivo, можуть вводитися в поєднанні з одним або декількома з вказаних вище фармацевтичних агентів. У цьому випадку, сполука формули (І) може вводитися за допомогою системних або несистемних засобів. Зокрема, сполука формули (І) може вводитися за допомогою несистемних засобів, наприклад, місцевого введення. Тому даний винахід стосується способу запобігання втраті волосся під час лікування одного або більше злоякісних станів у теплокровної тварини, такої як людина, за допомогою фармацевтичних агентів, що включає введення вказаній тварині ефективної кількості сполуки формули (І), або її фармацевтично прийнятної солі або ефіру, що гідролізується in vi vo. Крім того, винахід стосується способу запобігання втраті волосся під час лікування одного або більше злоякісних станів у теплокровної тварини, такої як людина, фармацевтичними агентами шляхом введення вказаній тварині ефективної кількості сполуки формули (І), або її фармацевтично прийнятної солі або її складного ефіру, що гідролізується in vivo, з ефективною кількістю вказаного фармацевтичного агента, при одночасному, послідовному або роздільному введенні. Відповідно до подальшого аспекту даного винаходу передбачається фармацевтична композиція, придатна для запобіганні втраті волосся, виникаючій в зв'язку з лікуванням злоякісних станів за допомогою фармацевтичних агентів, яка містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, і вказаний фармацевтичний агент, в поєднанні з фармацевтично прийнятним розріджувачем або носієм. Відповідно до подальшого аспекту даного винаходу передбачається набір, що містить сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vivo, і фармацевтичний агент для лікування злоякісних станів, про який відомо, що він викликає втрату волосся. Відповідно до подальшого аспекту даного винаходу передбачається набір, що містить: a) сполуку формули (І) або її фармацевтично прийнятну сіль, або її складний ефір, що гідролізується in vi vo, в першій стандартній дозованій формі; b) фармацевтичний агент для лікування злоякісних станів, про який відомо, що він викликає втрату волосся; у др угій стандартній дозованій формі; і c) контейнер для розміщення вказаних першої і другої дозованих форм. Відповідно до іншої особливості даного винаходу, передбачається застосування сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, при виробництві лікарського засобу для запобігання втраті волосся під час лікування злоякісних станів за допомогою фармацевтичних агентів. Відповідно до подальшого аспекту даного винаходу, передбачається комбіноване лікування для запобігання втраті волосся, яке включає в себе введення ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі, або її складного ефіру, що гідролізується in vivo, необов'язково, разом з фармацевтично прийнятним розріджувачем або носієм, з одночасним, послідовним або роздільним введенням ефективної кількості фармацевтичного агента для лікування злоякісних станів теплокровній тварині, такій як людина. Як указано вище, розмір дози, необхідної для терапевтичного або профілактичного лікування конкретного захворювання, пов'язаного з проліферацією клітин, за необхідністю буде змінюватися, в залежності від об'єкта лікування, способу введення і тяжкості захворювання, що зазнає лікування. Передбачається стандартна доза, що знаходиться в діапазоні, наприклад, 1-100мг/кг, переважно 1-50мг/кг. Інгібіторна активність по відношенню до CDK, визначена вище, може застосовуватися як єдиний вид терапії або може включати в себе, в доповнення до сполуки згідно з даним винаходом, одну або декілька інших речовин і/або видів лікування. Таке комбіноване лікування може бути досягнуте шляхом одночасного, послідовного або роздільного введення індивідуальних компонентів лікування. В області медичної онкології нормальною практикою є використання поєднання різних форм лікування для лікування кожного пацієнта з раковим захворюванням. У медичній онкології, іншим компонентом (компонентами) такого комбінованого лікування, в доповнення до лікування з інгібуванням клітинного циклу, визначеного вище, може бути хірургія, радіаційна терапія або хіміотерапія. Така хіміотерапія може включати три головних категорії терапевтичного агента: (і) інші агенти, що інгібують клітинний цикл, які працюють за тими ж самими механізмами, що і описані вище, або за іншими; (іі) цитостатичні агенти, такі як антиестрогени (наприклад, тамоксифен, тореміфен, ралоксифен, дролоксифен, йодоксифен), прогестогени (наприклад, мегестрол ацетат), інгібітори ароматази (наприклад, анастрозол, летразол, воразол ексеместан), антипрогестогени, антиандрогени (наприклад, флутамід, нілутамід, бікалютамід, ципротерон ацетат), агоністи і антагоністи LHRH (наприклад, гозерелін ацетат, люпролід), інгібітори тестостерон 5a-дигідроредуктази (наприклад, фінастерид), антиінвазивні агенти (наприклад, інгібітори металопротеїнази, подібні маримастату, і інгібітори активатора функції рецептора плазміногену урокінази) і інгібітори функції фактора росту (такі фактори росту включають в себе, наприклад, фактор росту, одержаний з тромбоцитів, і фактор росту гепатоцитів, такі інгібітори включають в себе антитіла факторів росту, антитіла рецепторів фактора росту, інгібітори тирозинкінази і інгібітори серин/фреонін кінази); і (ііі) лікарські засоби проти проліферації/новоутворень і їх поєднання, які використовуються в медичній онкології, такі як антиметаболіти (наприклад, антифоліати, подібні метотрексату, фторпіримідини, подібні 5фтор урацилу, аналоги пурину і аденозину, цитозин арабінозид); протипухлинні антибіотики (наприклад, антрацикліни, подібні доксорубіцину, да уноміцину, епірубіцину і ідарубіцину, мітоміцин-С, дактиноміцин, мітраміцин); сполуки платини (наприклад, цисплатин, карбоплатин); алкілуючі агенти (наприклад, азотистий іприт, мельфалан, хлорамбуцил, бусульфан, циклофосфамід, іфосфамід, нітрозосечовини, тіотепа); антимітотичні агенти (наприклад, вінка алкалоїди, подібні вінкристину, і таксоїди, подібні таксолу, таксотере); інгібітори топоізомерази (наприклад, епіподофілотоксини, подібні етопозиду і теніпозиду, амсакрин, топотекан). Відповідно до цього аспекту даного винаходу, передбачається фармацевтичний продукт, що містить сполуку формули (І), як визначено вище, і додаткову протипухлинну речовину, як визначено вище, для комбінованого лікування ракового захворювання. У доповнення до їх використання в терапевтичній медицині, сполуки формули (І) і їх фармацевтично прийнятні солі є також корисними як фармакологічні інструменти при розробці і стандартизації систем дослідження in vitro і in vivo для оцінки впливу інгібіторів, на їх активність відносно клітинного циклу, на лабораторних тваринах, таких як коти, собаки, кролики, мавпи, щури і миші, як частина дослідження нових терапевтичних агентів. Для вказаної вище іншої фармацевтичної композиції, способу, процесу, використання і особливостей виробництва лікарських засобів, також заявляються альтернативні і переважні втілення сполук згідно з даним винаходом, описаних тут. Приклади Тепер винахід буде ілюструватися за допомогою наступних далі необмежувальних прикладів, в яких, якщо не затверджується іншого: (і) температури приведені в градусах Цельсію (°С); операції здійснюють при кімнатній температурі або температурі навколишнього середовища, тобто, при температурі в межах 18-25°С; (іі) органічні розчини сушать над безводним сульфатом магнію; випаровування розчинника здійснюють з використанням роторного випарника при зниженому тиску (600-4000 Паскалів; 4,5-30мм.рт.ст.), при температурі бані аж до 60°С; (ііі) хроматографія означає флеш-хроматографію на силікагелі; тонкошарову хроматографію (ТШХ) здійснюють на пластинах, покритих силікагелем; (iv) як правило, після здійснення реакцій, проводять ТШХ, і часи реакцій приведені тільки для ілюстрації; (ν) кінцеві продукти мають задовільні спектри протонного ядерного магнітного резонансу (ЯМР) і/або мас-спектри; (vi) ви ходи приведені тільки для ілюстрації, і вони не обов'язково є тими, які можуть бути одержані при ретельній розробці способу; якщо потрібно більше матеріалу, приготування повторюють; (vii) коли вони приведені, дані ЯМР приводяться в формі значень дельта для головних діагностичних протонів, вони приводяться в мільйонних частках (м.д.) по відношенню до тетраметилсилану (TMS), як внутрішній стандарт, визначаються при 300МГц, з використанням пердейтерій диметил сульфоксиду (ДМСО-dб ) як розчинника, якщо не указано іншого; (viii) хімічні символи мають їх звичайні значення; використовуються одиниці і символи СІ; (іх) відношення розчинників приведені в об'єм/об'єми (об./об.); і (х) мас-спектри одержують при енергії електронів 70 електронвольт, в режимі хімічної іонізації (СІ), використовуючи пряму експозицію зразка; там, де указано, іонізація здійснюється за допомогою електронного удару (ЕІ), бомбардуванням швидкими атомами (FAB) або електророзпиленням (ESP); приводяться значення для m/z; як правило, повідомляється тільки про іони, які показують початкову масу; і якщо не стверджується іншого, іон порівняння являє собою (МН)+; (хі) якщо не стверджується іншого, сполука, що містить асиметрично заміщений атом вуглецю і/або сірки, не дозволяються; (хіі) там, де синтез описується, як аналогічний тому, який описаний в попередньому прикладі, кількості, що використовуються є еквівалентами мілімолярних відношень по відношенню до тих, які використовуються в попередньому прикладі; (xvi) використовуються наступні скорочення: ТГФ тетрагідрофуран; ДМФ Ν,Ν-диметилформамід; DMFD MA диметилформамід диметилацеталь; EtOAc етилацетат; МеОН метанол; ЕtOН етанол; DCM дихлорметан; і ДМСО диметилсульфоксид. xvii) там, де згадується колонка Isolute SCX-2, це означає "іонообмінний" екстракційний картридж для адсорбції основних сполук, тобто поліпропіленову тр убку, що містить сильний катіонообмінний сорбент на основі бензолсульфонової кислоти, що використовується відповідно до інструкцій виробника, одержаний від International Sorbent Technologies Limited, Dyffryn Business Park, Hengeod, Mid Glamorgan, UK, CF82 7RJ; xviii) там, де згадується амінова колонка Isolute, це означає "іонообмінний" екстракційний картридж для адсорбції кислотних сполук, тобто поліпропіленову тр убку, що містить амiносилан, ковалентно пов'язаний з частками з окислу кремнію, що використовується відповідно до інструкцій виробника, одержаний від International Sorbent Technologies Limited, Dyffryn Business Park, Hengeod, Mid Glamorgan, UK, CF82 7RJ; хі х) там, де згадується колонка Chemelut, це означає екстракційний картридж для видалення води, тобто поліпропіленову трубку, що містить діатомову землю, що використовується відповідно до інструкцій виробника, одержаний від Varian, Harbor City, California, USA. Приклад 1 2-(3-Хлораніліно)-4-(2-метилімідазол-5-іл)піримідин Гідрид натрію (45мг 60% суспензії в мінеральному маслі, 1,12ммоль) додають до суспензії, що перемішується, 5-(3-диметиламінопроп-2-ен-1-оїл)-2-метилімідазолу (100мг, 0,56ммоль) і 3хлорфенілгуанідину (95мг, 0,56ммоль) в сухому 1-бутанолі (4,0мл) в атмосфері азоту. Суміш перемішують при температурі навколишнього середовища протягом 15 хвилин, потім нагрівають при 126°С протягом 26 годин. Реакційній суміші дають можливість охолодитися, і леткі продукти видаляють шляхом випаровування. Залишок суспендують у воді (20мл), і додають оцтову кислоту (67мкл), і розчин екстрагують DCM (3´20мл). Екстракти об'єднують, сушать (Na2SO4), і розчинник видаляють шляхом випаровування. Залишок очищають за допомогою колонкової хроматографії, елююючи DCM/MeOH (100:0, із збільшенням полярності до 92:8), з одержанням вказаної в заголовку сполуки, 33мг (21%), у вигляді твердого продукту. ЯМР: 2,35 (с, 3Н), 6,95 (д, 1Н), 7,23 (д, 1Н), 7,30 (т, 1Н), 7,67 (с, 1Н), 7,72 (с, 1Н), 8,05 (с, 1Н), 8,43 (д, 1Н), 9,62 (с, 1Н), 12,15 (с, 1Н); m/z: 286. Приклад 2 2-(3-(Хлораніліно)-4-(1,2-диметилімідазол-5-іл)піримідин 5-(3-Диметиламінопроп-2-ен-1-оїл)-1,2-диметилімідазол (спосіб 1; 111мг, 0,58ммоль) і 3хлорфенілгуанідин (97мг, 0,58ммоль) обробляють, як описано в прикладі 1, з одержанням вказаної в заголовку сполуки, 51мг (29%), у вигляді твердого продукту. ЯМР: 2,40 (с, 3Н), 3,97 (с, 3Н), 6,98 (д, 1Н), 7,15 (д, 1Н), 7,30 (т, 1Н), 7,58 (д, 1Н), 7,67 (с, 1Н), 7,97 (с, 1Н), 8,40 (д, 1Н), 9,68 (с, 1Н); m/z: 300. Приклад 3 2-Аніліно-(2-метилімідазол-5-іл)піримідин Гідрид натрію (167мг 60% суспензії в мінеральному маслі, 4,18ммоль) додають до суспензії, що перемішується, 5-(3-диметиламінопроп-2-ен-1-оїл)-2-метилімідазолу (250мг, 1,39ммоль) і фенілгуанідин бікарбонату (275мг, 1,39ммоль), суспендують в сухому 1-бутанолі (10мл), в атмосфері азоту, і суміш перемішують і нагрівають в атмосфері азоту, при 126°С, протягом 18 годин. Реакційній суміші дають можливість охолодитися, а потім додають фенілгуанідин бікарбонат (275мг, 1,39ммоль) і гідрид натрію (111мг 60% суспензія в мінеральному маслі, 2,78ммоль), і суміш перемішують і нагрівають при 126°С протягом додаткових 20 годин. Потім реакційну суміш витягують, як описано в прикладі 1, з одержанням вказаної в заголовку сполуки 159мг, (46%) у вигляді твердого продукту. ЯМР: 2,33 (с, 3Н), 6,92 (т, 1Н), 7,18 (д, 1Н), 7,27 (т, 2Н), 7,67 (с, 1Н), 7,80 (д, 2Н), 8,36 (д, 1Н), 9,37 (с, 1Н), 12,12 (с, 1Н); m/z: 252. Приклад 4 4-(2-Метилімідазол-5-іл)-2-(4-сульфамоїланіліно)піримідин Тіонілхлорид (2,0мл) додають до 2-аніліно-4-(2-метилімідазол-5-іл)піримідину (приклад 3; 98мг, 0,39ммоль), охолодженому при 0°С, в атмосфері азоту. Додають хлорсульфонову кислоту (104мкл, 1,56ммоль), і суміш перемішують при 0°С протягом 30 хвилин. Надлишок тіонілхлориду видаляють шляхом випаровування, і залишок обробляють сумішшю ТГФ (4,0мл) і концентрованого водного розчину амонію (1,0мл). Суміш перемішують протягом 15 хвилин, і леткі продукти видаляють шляхом випаровування. Залишок розтирають з водою, і осаджений твердий продукт збирають шляхом фільтрування, промивають дистильованою водою і сушать у вакуумі з одержанням вказаної в заголовку сполуки, 62мг, (48%). ЯМР: 2,33 (с, 3Н), 7,10 (с, 2Н), 7,24 (д, 1Н), 7,72 (т, 3Н), 7,95 (д, 2Н), 8,43 (д, 1Н), 9,83 (с, 1Н); m/z: 331. Приклад 5 2-Аніліно-4-(1,2-диметилімідазол-5-іл)піримідин 5-(3-Диметиламінопроп-2-еноїл)-1,2-диметилімідазол (спосіб 1; 314мг, 1,62ммоль) і фенілгуанідин бікарбонат (321мг, 1,62ммоль) обробляють, як описано в прикладі 1, з одержанням вказаної в заголовку сполуки, 113мг, (26%), у вигляді твердого продукту. Я МР: 2,37 (с, 3Н), 3,93 (с, 3Н), 6,95 (т, 1Н), 7,08 (д, 1Н), 7,28 (т, 2Н), 7,59 (с, 1Н), 7,69 (д, 2Н), 8,35 (д, 1Н), 9,43 (с, 1Н); m/z: 266. Приклад 6 4-(1,2-Диметилімідазол-5-іл)-2-(4-сульфамоїланіліно)піримідин Тіонілхлорид (2,0мл) додають до 2-аніліно-4-(1,2-диметилімідазол-5-іл)піримідину (приклад 5; 94мг, 0,36ммоль), охолодженому при 0°С, в атмосфері азоту. Додають хлорсульфонову кислоту (94мкл, 1,56ммоль), і суміш перемішують при 0°С протягом 30 хвилин, потім дають можливість нагрітися і перемішують протягом двох годин при температурі навколишнього середовища, а потім нагрівають при 90°С протягом однієї години. Надлишок тіонілхлориду видаляють шляхом випаровування, і залишок азеотропно відганяють разом з толуолом. Одержаний сирий сульфонілхлорид обробляють сумішшю ТГФ (4,0мл), води (2,0мл) і концентрованого водного розчину амонію (1,0мл). Суміш перемішують протягом 15 хвилин, і ле ткі продукти видаляють шляхом випаровування. Залишок розтирають з водою (5мл), і осаджений твердий продукт збирають шляхом фільтрування, промивають дистильованою водою і сушать у вакуумі. Сирий продукт потім суспендують і перемішують в DC M (10мл), що містить декілька крапель МеОН. Твердий продукт збирають шляхом фільтрування, промивають DCM і сушать у вакуумі з одержанням вказаної в заголовку сполуки, 67мг (54%). ЯМР: 2,38 (с, 3Н), 3,96 (с, 3Н), 7,13 (с, 2Н), 7,20 (д, 1Н), 7,63 (с, 1Н), 7,73 (д, 2Н), 7,88 (д, 2Н), 8,43 (д, 1Н), 9,88 (с, 1Н); m/z: 345. Приклад 7 4-(1-Бензил-2-метилімідазол-5-іл)-2-(3-хлораніліно)піримідин Метоксид натрію (36,8мг, 0,68ммоль) додають до суспензії, що перемішується, 1-бензил-5-(3диметиламінопроп-2-ен-1-оїл)-2-метилімідазолу (спосіб 5; 153мг, 0,57ммоль) і 3-хлорфенілгуанідину (106мг, 0,62ммоль) в сухому 1-бутанолі (1,0мл) в атмосфері азоту. Реакційну суміш нагрівають із зворотним холодильником протягом 4 годин, потім дають їй можливість охолодитися. Леткі продукти видаляють шляхом випаровування, і залишок розподіляють між EtOAc і насиченим водним розчином бікарбонату натрію. Органічну фазу відділяють, сушать, і розчинник видаляють шляхом випаровування. Залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (97:3), з одержанням вказаної в заголовку сполуки, 73мг (34%). ЯМР: 2,35 (с, 3Н), 5,78 (с, 2Н), 6,84-7,00 (м, 5Н), 7,07 (т, 1Н), 7,15-7,30 (м, 4Н), 7,56-7,65 (м, 2Н), 8,29 (д, 1Н); m/z 374. Приклад 8 2-(3-Хлораніліно)-4-[1-(2-метоксіетил)імідазол-5-іл]піримідин гідрохлорид Трифторметилсульфоновий ангідрид (0,16мл, 0,93ммоль) додають до розчину 2-метоксіетанолу (73,7мл, 0,88ммоль) і діізопропілетиламіну (0,20мл, 1,17ммоль) в DCM (1мл), при -20°С, і розчин перемішують протягом 30 хвилин. Потім цю суміш додають до розчину 2-(3-хлораніліно)-4-(1трифенілметилімідазол-4-іл)піримідину (спосіб 2; 300мг, 0,58ммоль) в DCM (5мл) при -20°С, і реакційній суміші дають можливість нагрітися, і перемішують протягом 2 годин при температурі навколишнього середовища. Суміш розподіляють між EtOAc і насиченим водним розчином бікарбонату натрію. Органічну фазу відділяють, сушать, і леткі продукти видаляють шляхом випаровування. Залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (99,5:0,5, із збільшенням полярності до 96:4). Очищений продукт розчиняють в простому ефірі, і обробляють ефірним розчином хлористого водню. Преципітат збирають шляхом фільтрування, промивають простим ефіром і сушать з одержанням вказаної в заголовку сполуки, 132мг (69%). ЯМР: 3,17 (с, 3Н), 3,63 (т, 2Н), 4,96 (т, 2Н), 5,86 (ушир.с, 1Н), 7,04 (д, 1Н), 7,28-7,44 (м, 2Н), 7,60 (д, 1Н), 7,88 (с, 1Н), 8,56 (с, 1Н), 8,64 (д, 1Н), 9,28 (с, 1Н), 10,0 (с, 1Н); m/z: 330. Приклад 9 2-(3-Хлораніліно)-4-(імідазол-5-іл)піримідин Суміш 2-(3-хлораніліно)-4-(1-трифенілметилімідазол-4-іл)піримідину (спосіб 2; 256мг, 0,5ммоль) в МеОН (3мл) і 2М хлористоводневої кислоти (1мл) перемішують протягом 15 хвилин. Леткі продукти видаляють шляхом випаровування, і залишок розподіляють між EtOAc і насиченим водним розчином бікарбонату натрію. Органічний шар відділяють, сушать, і розчинник видаляють шляхом випаровування. Залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (99,5:0,5, із збільшенням полярності до 93:7), з одержанням вказаної в заголовку сполуки, 102мг (75%), у вигляді твердого продукту. ЯМР: 6,95 (дд, 1Н), 7,25-7,33 (м, 2Н), 7,73 (дд, 1Н), 7,81 (д, 2Н), 8,06 (с, 1Н), 8,46 (д, 1Н), 9,68 (с, 1Н), 12,48 (ушир.с, 1Н); m/z: 270. Приклад 10 2-(3-Хлораніліно)-4-[1-(2-фталімідоетил)імідазол-5-іл]піримідин 2-Фталімідоетилтрифлат (660мг, 2,04ммоль) додають до розчину 2-(3-хлораніліно)-4-(1трифенілметилімідазол-4-іл) піримідину (спосіб 2; 1,00г, 1,95ммоль) в DCM (5мл), і реакційну суміш перемішують протягом 4 годин. Розчинник видаляють шляхом випаровування, і до залишку додають МеОН (6мл) і 2М хлористоводневу кислоту (1,5мл). Суміш перемішують протягом 5 хвилин, леткі продукти видаляють шляхом випаровування, і залишок розподіляють між EtOAc і насиченим водним розчином бікарбонату натрію. Одержаний преципітат збирають шляхом фільтрування, промивають водою і EtOAc і сушать, з одержанням вказаної в заголовку сполуки, 350мг (40%), у вигляді твердого продукту. Я МР: 3,813,96 (м, 2Н), 4,77-4,92 (м, 2Н), 6,98 (д, 1Н), 7,06 (д, 1Н), 7,31 (т, 1Н), 7,37 (д, 1Н), 7,63-7,80 (м, 6Н), 7,92 (с, 1Н), 8,27 (д, 1Н), 9,50 (с, 1Н); m/z: 443. Приклад 11-12 Наступні далі сполуки приготовляють за допомогою способу, аналогічного тому, що описується в прикладі 10, з використанням відповідних початкових матеріалів1, але при витягуванні органічний шар відділяють, сушать, розчинник видаляють шляхом випаровування, і залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (99,5:0,5, із збільшенням полярності до 93:7). Пр. 11 12 Сполука 2-(3-Хлораніліно)-4-(1етилімідазол-5-іл)піримідин 2-(3-Хлораніліно)-4-(1метилімідазол-5-іл)піримідин ЯМР 1,26 (т, 3Н), 4,56 (кв, 2Н), 7,00 (д, 1Н), 7,21 (д, 1Н), 7,30 (т,1Н), 7,57 (д, 1Н), 7,87-7,91 (м, 1Н), 8,44 (д, 1Н), 9,62 (с, 1Н) 4,03 (с, 3Н), 6,95-7,10 (м, 2Н), 7,15-7,38 (м, 3Н), 7,45-7,60 (м, 2Н), 7,65 (с, 1Н), 7,87 (с, 1Н), 8,38 (д, 1Н) m/z 300 286 1 У випадку прикладу 12, три флатний початковий матеріал, що використовується, являє собою триметилсилілметил трифлат Приклад 13 4-[1-(2-Аміноетіл)імідазол-5-іл1-2-(3-хлораніліно)піримідин Гідразин гідрат (54мл, 1,73ммоль) додають до суспензії 2-(3-хлораніліно)-4-[1-(2фталімідоетил)імідазол-5-іл]піримідину (приклад 10; 163мг, 0,37ммоль) в EtOH (5мл), і суміш нагрівають із зворотним холодильником протягом 2 годин. Суміші дають можливість охолодитися, леткі продукти видаляють шляхом випаровування, і залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (90:10), з одержанням вказаної в заголовку сполуки, 69мг (59%), у вигляді твердого продукту. Я МР: 1,41 (ушир.с, 2Н), 2,99 (т, 2Н), 4,55 (т, 2Н), 7,00-7,09 (м, 2Н), 7,22-7,35 (м, 3Н), 7,65-7,70 (м, 2Н), 7,73-7,78 (м, 1Н), 8,39 (д, 1Н); m/z: 315. Приклад 14 2-Аніліно-4-(1-метилімідазол-5-іл)піримідин Метоксид натрію (2,63г, 48,7ммоль) додають до розчину 5-(3-диметиламінопроп-2-ен-1-оїл)-1метилімідазолу (спосіб 4; 2,91г, 16,2ммоль) і фенілгуанідин бікарбонату (3,52г, 17,9ммоль) в 2-пропанолі (14мл), і реакційну суміш нагрівають із зворотним холодильником протягом 3 годин. Реакційній суміші дають можливість охолодитися, і розподіляють між EtOAc і насиченим водним розчином бікарбонату натрію. Органічну фаз у відділяють, сушать, і розчинник видаляють шляхом випаровування. Залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (97:3), з одержанням вказаної в заголовку сполуки, 2,57г (64%), у ви гляді твердого продукту; m/z: 252. Приклад 15 4-(1-Метилімідазол-5-іл)-2-(4-сульфамоїланіліно)піримідин Хлорсуль фонову кислоту (0,48мл, 7,16ммоль) додають до суспензії 2-аніліно-4-(1-метилімідазол-5іл)піримідину (приклад 14; 449мг, 1,79ммоль) в тіонілхлориді (9мл), охолодженої при 0°С. Суміші дають можливість нагрітися до температури навколишнього середовища, потім нагрівають із зворотним холодильником протягом 30 хвилин. Леткі продукти видаляють шляхом випаровування, і залишок сушать у високому вакуумі. До залишку додають 7М метанольний розчин амонію (30мл), і суміш перемішують протягом 10 хвилин. Леткі продукти видаляють шляхом випаровування, з одержанням вказаної в заголовку сполуки, 360мг (61%), у вигляді твердого продукту. ЯМР: 4,04 (с, 3Н), 7,15 (с, 2Н), 7,27 (д, 1Н), 7,73 (д, 2Н), 7,84-7,91 (м, 3Н), 8,06 (с, 1Н), 8,50 (д, 1Н), 9,92 (с, 1Н); m/z: 331. Приклад 16 2-(4-[N-(3-Метоксипропіл)сульфамоїл1аніліно}-4-(1-метилімідазол-5-іл)піримідин Хлорсуль фонову кислоту (0,22мл, 3,18ммоль) додають до суспензії 2-аніліно-4-(1-метилімідазол-5іл)піримідину (приклад 14; 200мг, 0,80ммоль) в тіонілхлориді (4мл), охолодженої при 0°С. Суміші дають можливість нагрітися до температури навколишнього середовища, перемішують протягом 15 хвилин, потім нагрівають із зворотним холодильником протягом 20 хвилин. Леткі продукти видаляють шляхом випаровування, і твердий залишок сушать у високому вакуумі. Залишок суспендують в піридині (3мл), охолоджують до -20°С, і додають діізопропілетиламін (0,56мл, 3,98ммоль), а потім 3-метоксипропіламін (0,16мл, 1,60ммоль). Реакційній суміші дають можливість нагрітися до температури навколишнього середовища, і перемішують протягом 30 хвилин. Додають EtOAc (15мл), і суміш промивають насиченим водним розчином бікарбонату натрію (15мл), а потім насиченим розчином солі (15мл). Розчинник видаляють шляхом випаровування, і залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 2М метанольним розчином амонію (100:0, із збільшенням полярності до 85:15), з одержанням вказаної в заголовку сполуки, 89мг (28%), у вигляді твердого продукту. ЯМР: 1,75 (м, 2Н), 2,76 (кв, 2Н), 3,14 (с, 3Н), 3,22-3,30 (м, 2Н), 4,01 (с, 3Н), 7,25 (д, 1Н), 7,34 (т, 1Н), 7,70 (д, 2Н), 7,77 (с, 1Н), 7,83 (с, 1Н), 7,91 (д, 2Н), 8,47 (д, 1Н), 9,92 (с, 1Н); m/z: 403. Приклади 17-25 Наступні далі сполуки приготовляють способом, аналогічним тому, що описується в прикладі 15, з використанням відповідних проміжних сполук. Пр. Сполука 17 4-(1-Метилімідазол-5-іл)-2-[4-(Nпропілсульфамоїл)анілін]піримідин 18 2-{4-(N-(2,3 ЯМР m/z 0,77 (т, 3Н), 1,35 (м, 2Н), 2,67 (кв, 2Н), 4,01 (с, 3Н), 7,25 (д, 1Н), 7,34 (т, 1Н), 7,69 (д, 2Н), 7,77 (с, 1Н), 373 7,83 (с, 1Н), 7,90 (д, 2Н), 8,47 (д, 1Н), 9,92 (с, 1Н) 2,53-2,64 (м, 1Н), 2,79-2,90 (м, 1Н), 3,25 (т, 2Н), 405 19 20 21 22 23 24 25 дигідроксипропіл)сульфамоїл]аніліно}-4-(1- 3,39-3,50 (м, 1Н), 4,02 (с, 3Н), 4,49 (т, 1Н), 4,71 (д, метилімідазол-5-іл)піримідин 1Н), 7,22-7,29 (м, 2Н), 7,70 (д, 2Н), 7,77 (с, 1Н), 7,83 (с, 1Н), 7,91 (д, 2Н), 8,47 (д, 1Н), 9,93 (с, 1Н) 2,88 (кв, 2Н), 3,24-3,48 (м, 6Н), 4,02 (с, 3Н), 4,51 (т, 2-(4-{N-[2-(21Н), 7,25 (д, 1Н), 7,42 (т, 1Н), 7,70 (д,2Н), 7,77 гідроксіетокси)етил]сульфамоїл}аніліно)-4(с,1Н), 7,83 (с, 1Н), 7,90 (д, 2Н), 8,47 (д, 1Н), 9,92 (1-метилімідазол-5-іл)піримідин (с, 1Н) 3,97 (д,2Н), 4,02 (с,3Н), 6,16 (дд, 1Н), 6,30 (дд, 2-{4-[N-(21Н), 7,25 (д, 1Н), 7,47-7,50 (м, 1Н), 7,68 (д, 2Н), Фуранілметил)сульфамоїл]анілін}-4-(17,77 (с, 1Н), 7,83 (с, 1Н), 7,85-7,94 (м, 3Н), 8,48 (д, метилімідазол-5-іл)піримідин 1Н),9,91(с, 1Н) 2,77 (кв, 2Н), 3,55 (кв, 2Н), 4,02 (с, 3Н), 4,61 (т, 2-{4-[N-2-Гідроксіетил)сульфамоїл]аніліно}- 1Н), 7,25 (д, 1Н), 7,33 (т, 1Н), 7,70 (д, 2Н), 7,77 (с, 4-(1-метилімідазол-5-іл)піримідин 1Н), 7,83 (с, 1Н), 7,90 (д, 2Н), 8,47 (д, 1Н), 9,91 (с, 1Н) 3,29-3,37 (м, 2Н), 4,02 (с, 3Н), 7,06 (ушир.с, 1Н), 2-{4-[N7,20 (ушир.с, 1Н), 7,25 (д, 1Н), 7,58 (т, 1Н), 7,71 (д, Карбамоїлметил)сульфамоїл]аніліно}-4-(12Н), 7,77 (с, 1Н), 7,83 (с, 1Н), 7,90 (д, 2Н), 8,47 (д, метилімідазол-5-іл)піримідин 1Н), 9,93 (с, 1Н) 1,75 (м, 2Н), 2,37 (с, 3Н), 2,76 (т, 2Н), 3,14 (с, 3Н), 4-(1,2-Диметилімідазол-5-іл)-2-{4-N-(33,26 (т, 2Η), 3,96 (с, 3Н), 7,19 (д, 1Н), 7,33 (ушир.с, метоксипропіл)сульфамоїл]аніліно}піриміди 1Н), 7,63 (с, 1Н), 7,68 (д, 2Н), 7,92 (д, 2Н), 8,43 (д, н 1Н), 9,91(с, 1Н) 2,37 (с, 3Н), 3,94 (с, 2Н), 3,95 (с, 3Н), 7,04-7,12 (м, 4-(1,2-Диметилімідазол-5-іл)-2-{4-(N-(42Н), 7,20 (д, 1Н), 7,24-7,29 (м, 2Н), 7,63 (с, 1Н), фторбензил)сульфамоїл]аніліно}піримідин 7,70 (д, 2Н), 7,88-7,95 (м, 3Н), 8,43 (д, 1Н), 9,91 (с, 1Н) 0,00-0,05 (м, 2Н), 0,27-0,33 (м, 2Н), 0,7-0,8 (м, 1Н), 2-{4-[N2,34 (с, 3Н), 2,59 (т, 2Н), 3,91 (с, 3Н), 7,15 (д, 1Н), (Циклопропілметил)сульфамоїл]аніліно}-47,44 (т, 1Н), 7,60 (с, 1Н), 7,66 (д, 2Н), 7,87 (д, 2Н), (1,2-диметилімідазол-5-іл)піримідин 8,39 (д, 1Н), 9,86 (с, 1Н) 419 411 375 388 417 453 399 Приклад 26 4-(1,2-Диметилімідазол-5-іл)-2-(4-{N-[3-(піролидин-2-он-1-іл)пропіл]сульфамоїл}аніліно)піримідин Ефірний розчин хлористого водню (1 мл 1М розчину, 1,0ммоль) додають до розчину 4-{N-[3-(піролідин2-он-1-іл)пропіл]сульфамоїл}аніліну (спосіб 13, 300мг, 1,0ммоль) в МеОН (мінімальний об'єм). Леткі продукти видаляють шляхом випаровування, і до залишку додають ціанамід (50мг, 1,2ммоль), а потім диметилацетамід (0,5мл). Суміш нагрівають до 100°С протягом 30 хвилин. Додають 5-(3диметиламінопроп-2-еноїл)-1,2-диметилімідазол (спосіб 1; 180мг, 0,93ммоль) і метоксид натрію (110мг, 2,0ммоль), і суміш нагрівають із зворотним холодильником протягом однієї години. Суміші дають можливість охолодитися, і розподіляють між EtOAc і водним розчином бікарбонату натрію. Органічний шар відділяють, промивають насиченим розчином солі, сушать (Nа2SО4) і леткі продукти видаляють шляхом випаровування. Залишок очищають за допомогою колонкової хроматографії, елююючи DCM і 7М метанольним розчином амонію (96:4), з одержанням вказаної в заголовку сполуки, 220мг (50%). ЯМР: 1,481,58 (м, 2Н), 1,79-1,89 (м, 2Н), 2,14 (т, 2Н), 2,37 (с, 3Н), 2,68 (кв, 2Н), 3,10 (т, 2Н), 3,21 (т, 2Н), 3,95 (с, 3Н), 7,19 (д, 1Н), 7,34 (т, 1Н), 7,63 (с, 1Н) 7,69 (д, 2Н), 7,92 (д, 2Н) 8,43 (д, 1Н), 9,92 (с, 1Н); m/z: 470. Приклад 27 Наступну далі сполуку приготовляють способом, аналогічним тому, що описується в прикладі 26, з використанням відповідних проміжних сполук. Пр. 27 Сполука ЯМР, ДМСО-d 6, 300МГц @ 303,1 k m/z 1,45-1,56 (м, 1Н), 1,68-1,88 (м, 3Н), 2,37 (с, 3Н), 2,75 (т, 2Η), 3,51-3,58 (м, 1Н), 3,634-(1,2-Диметилімідазол-5-m)-2-{4-[N-(23,70 (м, 1Н), 3,73-3,82 (м, 1Н), 3,95 (с, 3Н), 429 тетрагідрофуранілметил)сульфамоїл]анілін}піриміди 7,19 (д, 1Н), 7,46 (т, 1Н), 7,63 (с, 1Н), 7,70 н (д, 2Н), 7,91 (д, 2Н), 8,43 (д, 1Н), 9,90 (с, 1Н) Приклад 28 2-Аніліно-4-(1-етил-2-метилімідазол-5-іл)піримідин 5-(3-Диметиламінопроп-2-ен-1-оїл)-1-етил-2-метилімідазол (спосіб 16; 2,10г, 10,1ммоль), фенілгуанідин бікарбонат (2,2г, 11,1ммоль) і метоксид натрію (1,2г, 22,2ммоль) суспендують в безводному DMA (15мл), і суміш нагрівають при 110°С протягом 18 годин. Реакційній суміші дають можливість охолодитися до температури навколишнього середовища, і виливають у воду (50мл). Розчин екстрагують EtOAc (2´50мл). Об'єднані екстракти промивають водою (2´50мл), а потім насиченим розчином солі (2´50мл), сушать, і леткі продукти видаляють шляхом випаровування. Залишок розтирають з простим ефіром, збирають шляхом фільтрування, і сушать на повітрі, з одержанням вказаної в заголовку сполуки (1,48г, 53%) у вигляді червонувато-коричневого твердого продукту. ЯМР 1,17 (т, 3Н), 2,38 (с, 3Н), 4,52 (кв, 2Н), 6,93 (т, 1Н), 7,08 (д, 1Н), 7,27 (т, 2Н), 7,60 (с, 1Н), 7,62 (д, 2Н), 8,35 (д, 1Н), 9,35 (с, 1Н); m/z 280. Приклади 29-33 Наступні далі сполуки синтезують аналогічно способу прикладу 28. Пр. Сполука ЯМР 1,23 (т, 3Н), 2,90 (кв, 2Н), 3,92 (с, 3Н), 6,92 (т, 1Н), 2-Аніліно-4-(1-метил-27,08 (д, 1Н), 7,25 (т, 2Н), 7,59 (с, 1Н), 7,70 (д, 1Н), етилімідазол-5-іл)піримідин 8,38 (д, 1Н), 9,42 (с, 1Н) 2-Аніліно-4-[1-(2,2,22,41 (с, 3Н), 5,76 (кв, 2Н), 6,98 (т, 1Н), 7,13 (д,1Н), трифторетил)-2-метилімідазол-5- 7,29 (т, 3Н), 7,60 (д, 2Н), 7,71 (с, 1Н), 8,38 (д, 1Н), іл]піримідин 8,56 (с, 1Н) 2,26 (с, 3Н), 2,32 (с, 3Н), 3,72 (с, 3Н), 6,85 (д, 1Н), 2-Аніліно-4-(1,2,4триметилімідазол-5-іл)піримідин 6,94 (дд, 1Н), 7,24 (дд, 1Н), 7,73 (д, 2Н), 8,42 (д, 1Н), 9,45 (с, 1Н) 1,44 (д,6Н), 2,51(с,3Н), 5,72 (септаплет, 1Н), 6,99 (т, 2-Аніліно-4-(1-ізопропіл-21Н), 7,04 (д, 1Н), 7,30 (т, 2Η), 7,42 (с, 1Н), 7,67 (д, метилімідазол-5-іл)піримідин 2Н), 8,39 (д, 1Н), 9,42 (с, 1Н) 2-Аніліно-4-(1-метил-23,30 (с, 3Н) 3,99 (с, 3Н), 4,50 (с, 2Н), 6,94 (т, 1Н), метоксиметилімідазол-57,13 (д, 1Н), 7,28 (т, 2Н), 7,65 (с, 1Н), 7,69 (д, 2Н), іл)піримідин 8,41 (д, 1Н), 9,48 (с, 1Н) 29 30 311 322 333 m/z SM 280 Спос.20 334 Спос.21 279 Спос.24 294 Спос.19 296 Спос.25 1 Реакційну суміш нагрівають при 150°С протягом 18 годин. Додають воду, осаджений твердий продукт збирають шляхом фільтрування, і очищають за допомогою флеш-хроматографії на силікагелі, елююючи DCM/MeOH (100:0, із збільшенням полярності до 95:5). 2 Твердий продукт кристалізується з EtOAc. 3 Очи щають за допомогою флеш-хроматографії на силікагелі, елююючи DCM/MeOH (100:0, із збільшенням полярності до 97:3). Приклад 34 4-(1,2-Диметилімідазол-5-іл)-2-(4-мезиламіноаніліно)піримідин Метансуль фонілхлорид (0,055мл, 0,71ммоль) додають до розчину 4-(1,2-диметилімідазол-5-іл)-2-(4аміноаніліно)піримідину (приклад 165; 0,18г, 0,64ммоль) і піридину (0,052мл, 0,64ммоль) в DCM (2,0мл), охолодженому при 4°С. Суміші дають можливість нагрітися до температури навколишнього середовища. Суміш розподіляють між насиченим водним розчином бікарбонату натрію і EtOAc. Органічний шар відділяють, леткі продукти випаровують, і залишок очищають за допомогою колонкової хроматографії на силікагелі, елююючи DCM/7M метанольним розчином амонію (96:4), з одержанням вказаної в заголовку сполуки (0,15г, 65%) у вигляді твердого продукту. ЯМР: 2,36 (с, 3Н), 2,90 (с, 3Н), 3,91 (с, 3Н), 7,06 (д, 1Н), 7,14 (д, 2Н), 7,57 (с, 1Н), 7,64 (д, 2Н), 8,33 (д, 1Н), 9,37 (ушир.с, 1Н), 9,42 (с, 1Н); m/z 359. Приклад 35 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(2-метоксіетил)сульфамоїл]аніліно}піримідин Натрій трет-бутоксид (1,04г, 10,8ммоль) додають до дегазованого розчину 2-аміно-4-(1,2диметилімідазол-5-іл)піримідину (спосіб 26; 567мг, 3ммоль), N-(2-метоксіетил)-4-йодбензолсульфонаміду (спосіб 40; 1,54г, 4,5ммоль), трис(дибензилиденацетон)дипаладію(0) (72мг, 0,15ммоль) і 2,2'біс(дифенілфосфіно)-1,1'-бінафтилу (102мг, 0,15ммоль) в діоксані (36мл), і суміш нагрівають при 80°С протягом ночі. Реакційну суміш охолоджують до кімнатної температури, і додають МеОН (5мл), і суміш виливають в колонку Isolute SCX-2, елююючи спочатку МеОН (10´30мл), а потім продукт елююють 2% метанольним розчином амонію (10´30мл). Розчинник видаляють шляхом випаровування, і залишок розчиняють в EtOAc (100мл), промивають водою (3´100мл), а потім насиченим розчином солі (100мл), сушать, і розчинник видаляють шляхом випаровування, з одержанням вказаної в заголовку сполуки (1,01г, 84%) у вигляді піни. ЯМР 2,40 (с, 3Н), 3,07 (кв, 2Н), 3,20 (с, 3Н), 3,38 (т, 2Η), 3,86 (с, 3Н), 5,00 (т, 1Н), 6,95 (д, 1Н), 7,47 (с, 2Н), 7,71 (м, 4Н), 8,36 (д, 1Н); m/z 403. Приклади 36-72 Наступні далі сполуки синтезують аналогічно способу прикладу 35. Пр. Сполука 36 4-(1,2-Диметилімідазол-5-іл)-2-[4-[N-третбутоксикарбонілсульфамоїл)аніліно]піримідин 37 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-[N-(2метоксіетил)сульфамоїл]аніліно}піримідин 38 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-2,2-диметил1,3-діоксалон-4ілметил)сульфамоїл]аніліно}піримідин 39 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(2бензилоксіетил)сульфамоїл]аніліно}піримідин ЯМР 1,40 (с,9Н), 2,49 (с, 3Н), 3,96 (с, 3Н), 7,03 (д, 1Н), 7,38 (с, 1Н), 7,82 (д, 2Н), 7,96 (д, 2Н), 8,08 (с, 1Н), 8,43 (д, 1Н) 1,25 (т, 3Н), 2,40 (с, 3Н), 3,05 (кв, 2Н), 3,20 (с, 3Н), 3,36 (т, 2Н), 4,43 (кв, 2Н), 4,92 (т, 1Н), 6,95 (д, 1Н), 7,32 (с, 1Н), 7,50 (с, 1Н), 7,72 (м, 4Н), 8,35 (д, 1Н) 1,20 (с, 3Н), 1,25 (с, 3Н), 2,40 (с, 3Н), 2,91 (м, 1Н), 3,12 (м, 1Н), 3,60 (м, 1Н), 3,86 (с, 3Н), 3,92 (м, 1Н), 4,13 (м, 1Н), 4,83 (т, 1Н), 6,95 (д, 1Н), 7,38 (с, 1Н), 7,49 (с, 1Н), 7,72 (м, 4Н), 8,35 (д, 1Н) 2,40 (с, 3Н), 3,12 (кв, 2Н), 3,46 (т, 2Н), 3,90 (с, 3Н), 4,37 (с, 2Н), 4,95 (т,1Н), 6,95 (д,1Н), 7,20 (м, 5Н), 7,40 (с, 1Н), 7,46 (с, 1Н), 7,73 (м,4Н), 8,33 (д, 1Н) m/z SM 445 Спос.54, Спос.26 417 Спос.40, Спос.27 459 Спос.42, Спос.26 479 Спос.43, Спос.26 40 41 421 431 44 451 461 47 481 49 501 511 521 531 2,40 (с, 3Н), 3,00 (т, 2Η), 3,28 (с, 6Н), 3,89 (с, 3Н), 4,28 (т, 1Н), 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(2,24,75 (т, 1Н), 6,95 (д, 1Н), 7,40 (с, 433 диметоксіетил)сульфамоїл]аніліно}піримідин 1Н), 7,48 (с, 1Н), 7,76 (м, 4Н), 8,32 (д, 1Н) 1,24 (т, 3Н), 1,50 (м, 1Н), 1,80 (м, 3Н), 2,43 (с, 3Н), 2,80 (т, 1Н), 3,62 (кв, 1Н), 3,74 (м, 1Н), 3,84, 4-(1-Етил-2-метилімідазол-5-іл)-2-(4-{N-[2-(2тетрагідрофур-2(м, 1Н), 4,73 (кв, 2Н), 7,32 (д, 441 іл)метил]сульфамоїл}аніліно)піримідин 1Н), 7,56 (т, 1Η), 7,78 (д, 2Н), 7,94 (д, 2Н), 8,50 (д, 1Н), 9,90 (с, 1Н) 1,18 (т, 3Н), 1,58 (м,2Н), 2,40 (с, 3Н), 2,78 (кв, 2Н), 3,16 (с, 3Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-[N-(33,30 (м, 2Н), 4,58 (кв, 2Н), 7,20 431 метоксипропіл)сульфамоїл]аніліно}піримідин (д, 1Н), 7,36 (т, 1Η), 7,70 (м,3Н), 7,90 (д, 2Н), 8,41 (Д, 1Н), 9,80 (с, 1Н) 0,01 (кв, 2Н), 0,40 (кв, 2Н), 0,81 (м, 1Н), 1,24 (т, 3Н), 2,40 (с, 3Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-[N2,78 (т, 2Η), 4,42 (кв, 2Н), 4,56 413 (циклопропілметил)сульфамоїл]аніліно}піримідин (т, 1Н), 6,96 (д, 1Н), 7,30 (с, 1Н), 7,50 (с, 1Н), 7,68 (д, 2Н), 7,76 (д, 2Н), 8,36 (Д, 1Н) 2,40 (с, 3Н), 2,78 (с, 3Н), 3,16 (т, 2Н), 3,22 (с, 3Н), 3,45 (т, 3Н), 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(23,89 (с, 3Н), 6,95 (д, 1Н), 7,37 (с, 417 метоксіетил)-N-метилсульфамоїл]аніліно}піримідин 1Н), 7,46 (с, 1Н), 7,70 (м,4Н), 8,38 (д, 1Н) 1,24 (т, 3Н), 2,40 (с, 3Н), 2,78 (с, 3Н), 3,16 (т, 2Н), 3,23 (с, 3Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-[N-(23,45 (т, 3Н), 4,43 (кв, 2Н), 6,95 431 метоксіетил-N-метилсульфамоїл]аніліно}піримідин (д, 1Н), 7,26 (с, 1Н), 7,46 (с, 1Н), 7,70 (м, 4H), 8,38 (д, 1Н) 2,40 (с, 3Н), 2,98 (с, 3Н), 3,86 (с, 4-(1,2-Диметилімідазол-5-іл)-2-(43Н), 6,96 (д, 1Н), 7,40 (с, 1Н), 344 мезиланіліно)піримідин 7,51 (с,1Н), 7,80 (м,4Н), 8,38 (д, 1Н) 1,76 (м, 2Н), 2,40 (м, 6Н), 2,46 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(3(с, 3Н), 2,73 (с, 3Н), 3,10 (т, 3Н), морфолінопропіл)-N7,71 (м, 4Н), 3,97 (с, 3Н), 7,03 (д, 486 1Н), 7,37 (с, 1Н), 7,53 (с, 1Н), метилсульфамоїл]аніліно}піримідин 7,77 (м, 4Н), 8,40 (д, 1Н) 1,87 (м, 2Н), 2,16 (с, 6Н), 2,33 (т, 2Н), 2,50 (с, 3Н), 3,16 (м, 2Н), 4-(1,2-Диметилімідазол-5-іл)-2-{4-[3-[N,N3,96 (с, 3Н), 7,02 (д, 1Н), 7,45 (с, 415 диметиламіно)пропілсульфоніл]аніліно}піримідин 1Н), 7,57 (с, 1Н), 7,83 (м, 4Н), 8,41 (д, 1Н) 2,48 (с, 3Н), 2,57 (м, 2Н), 3,31 4-(1,2-Диметилімідазол-5-іл)-2-[4-(3,3,3(м, 2Н), 3,96 (с, 3Н), 7,03 (д, 1Н), 426 трифторпропілсульфоніл)аніліно]піримідин 7,56 (с, 2Н), 7,84 (м, 4Н), 8,40 (д, 1Н) 0,80 (т, 3Н), 1,31 (м,2Н), 1,51 (м,2Н), 2,38 (с, 3Н), 3,19 (м, 2Н), 4-(1,2-Диметилімідазол-5-іл)-2-(43,96 (с, 3Н), 7,20 (д, 1Н), 7,61 (с, 386 бутилсульфоніланіліно)піримідин 1Н), 7,76 (д, 2Н), 7,98 (д, 2Н), 8,43 (д, 1Н), 10,05 (с, 1Н) 2,02 (м, 2Н), 2,48 (с, 3Н), 3,20 4-(1,2-Диметилімідазол-5-іл)-2-[4-(3(м, 2Н), 3,27 (с, 3Н), 3,45 (т, 2Н), 402 метоксипропілсульфоніл)аніліно]піримідин 3,95 (с, 3Н), 7,03 (д, 1Н), 7,56 (с, 2Н), 7,83 (с,. 4Н), 8,40 (д, 1Н) 1,34 (т, 3Н), 2,50 (с, 3Н), 3,17 4-(1-Етил-2-метилімідазол-5-іл)-2-(4-{N-[2(кв, 2Н), 3,31 (с, 3Н), 3,59 (т, 447 (метоксиметокси)етил]сульфамоїл}аніліно)піриміди 2Н), 4,53 (м, 4Н), 5,09 (т, 1Н), н 7,03 (д, 1Н), 4,39 (с, 1Н), 7,56 (с, 1Н), 7,80 (м, 4Н), 8,39 (д, 1Н) 0,33 (м, 2Н), 0,45 (м, 2Н), 1,12 (т, 3Н), 2,08 (м, 1Н), 2,40 (с, 3Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-[4-(N4,59 (кв, 2Н), 7,16 (д, 1Н), 7,68 399 циклопропілсульфамоїл)аніліно]піримідин (м, 3Н), 7,86 (д, 2Н), 8,41 (д, 1Н), 9,80 (с, 1Н) Спос.44, Спос.26 Спос.45, Спос.27 Спос.46, Спос.27 Спос.41, Спос.27 Спос.62, Спос.26 Спос. 62, Спос.27 Спос. 65, Спос.26 Спос.63 Спос.70, Спос.26 Спос.71, Спос.26 Спос.72, Спос. 26 Спос.74, Спос.26 Спос.39, Спос.27 Спос.47, Спос.27 542 552 562 57 58 59 60 613 624 635 646 656 667 677 1,24 (т, 3Н), 2,23 (с, 3Н), 2,70 (с, 3Н), 4,10 (д, 2Н), 4,70 (кв, 2Н), 7,12 (с, 1Н), 7,38 (д, 1Н), 7,73 (д, 470 2Н), 7,86 (д, 2Н), 8,40 (м, 2Н), 8,65 (д, 1Н), 10,11 (с, 1Н) 1,24 (т, 3Н), 2,10 (с, 3Н), 2,68 (с, 3Н), 4,10 (д, 2Н), 4,70 (кв, 2Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-(N-(36,03 (с, 1Н), 7,37 (д, 1Н), 7,69 (д, метилізоксазол-5454 2Н), 7,84 (д, 2Н), 8,20 (т, 1Н), ілметил)сульфамоїл]аніліно}піримідин 8,36 (с, 1Н), 8,63 (д, 1Н), 10,09 (с, 1Н) 1,23 (т, 3Н), 2,70 (с, 3Н), 2,74 (т, 2Н), 3,10 (м, 1Н), 3,70 (м, 6Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-[N-(1,4-діоксан- 4,70 (кв, 2Н), 7,35 (д, 1Н), 7,59 459 2-ілметил)сульфамоїл]аніліно}піримідин (т, 1Н), 7,72 (д, 2Н), 7,86 (д, 2Н), 8,40 (с, 1Н), 8,63 (д, 1Н), 10,09 (ушир.с, 1Н) 0,78 (т, 3Н), 1,35 (м, 2Н), 2,4 (с, 3Н), 2,67 (м, 2Н), 3,8 (с, 3Н), 5-Хлор-4-(1,2-диметилімідазол-5-іл)-2-[4-(N419 7,33 (т, 1Н), 7,65 (с, 1Н), 7,72 (д, М-Нпропілсульфамоїл)аніліно]піримідин 2Н), 7,87 (д, 2Н), 8,63 (с, 1Н), 10,14 (с,1Н) 0,0 (м, 2Н), 0,27 (м, 2Н), 0,72 (м, 1Н), 2,35 (с, 3Н), 2,57 (т, 2Н), 5-Хлор-4-(1,2-диметилімідазол-5-іл)-2-{4-[N431 (циклопропілметил)сульфамоїл]аніліно}піримідин 3,73 (с, 3Н), 7,43 (т, 1Н), 7,6 (с, М-Н1Н), 7,66 (д, 2Н), 7,8 (д, 2Н), 8,55 (с, 1Н), 10,08 (с, 1Н). 1,57 (м, 2Н), 2,42 (с, 3Н), 2,75 (м, 2Н), 3,13 (с, 3Н), 3,25 (м, 2Н), 449 5-Хлор-4-(1,2-диметилімідазол-5-іл)-2-(4-[N-(33,78 (с, 3Н), 7,35 (т, 1Н), 7,63 (с, М-Нметоксипропіл)сульфамоїл]аніліно}піримідин 1Н), 7,7 (д, 2Н), 7,87 (д, 2Н), 8,6 (с, 1Н), 10,15 (с, 1Н) 1,07 (с, 9Н), 2,4 (с, 3Н), 3,78 (с, 5-Хлор-4-(1,2-диметилімідазол-5-іл)-2-{4-(N-(трет- 3Н), 7,27 (с, 1Н), 7,65 (с, 1Н), 433 бутил)сульфамоїл]аніліно}піримідин 7,73 (д, 2Н), 7,83 (д, 2Н), 8,6 (с, М-Н1Н), 10,12 (с, 1Н) 2,40 (с, 3Н), 2,89 (с, 3Н), 3,12 (с,3Н), 3,18 (с, 3Н), 3,31 (т, 2Н), 4-[1-(2-Метоксіетіл)-2-метилімідазол-5-іл]-2-{4-(N3,52 (т, 2Н), 4,77 (т, 2Н), 7,24 (д, 447 (2-метоксіетил)сульфамоїл]аніліно}піримідин 1Н), 7,50 (ушир, с, 1Н), 7,71 (д, 3Н), 7,88 (д, 2Н), 8,42 (д, 1Н), 9,81 (с, 1Н) 2,29 (кв, 2Н), 2,39 (с, 3Н), 2,88 (ушир. кв, 2Н), 3,18 (с, 3Н), 3,30 4-[1-(1-Бутен-4-іл)-2-метилімідазол-5-іл]-2-{4-[N-(2- (т, 2Н), 4,63 (т, 2Н), 4,84 (д, 1Н), 4,88 (с, 1Н), 5,62 (м, 1Н), 7,22 (д, 443 метоксіетил)сульфамоїл]аніліно}піримідин 1Н), 7,48 (ушир.т, 1Н), 7,67 (с, 1Н), 7,71 (д, 2Н), 7,87 (д, 2Н), 8,44 (д, 1Н), 9,82 (с, 1Н) 2,39 (с, 3Н), 3,70 (с, 3Н), 6,99 2-Аніліно-5-бром-4-(1,2-диметилімідазол-5(дд, 1Н), 7,30 (дд, 1Н), 7,60 (с, 343 іл)піримідин 1Н), 7,64 (д, 2Н), 8,60 (с, 1Н), 9,70 (с, 1Н) 1,41 (т, 3Н), 1,96 (м,4Н), 2,77 (кв, 2Н), 2,93 (м, 1Н), 3,16 (м, 1Н), 4-(1-Метил-2-етилімідазол-5-іл)-2-{4-[N3,73 (м, 2Н), 3,96 (с, 3Н), 4,82 443 (тетрагідрофур-2(м,1Н), 7,01 (д,1Н), 7,38 (с, 1Н), ілметил)сульфамоїл]аніліно}піримідин 7,53 (с, 1Н), 7,80 (м, 4Н), 8,39 (д, 1Н) 1,39 (т, 3Н), 2,78 (кв, 2Н), 3, 13 (кв, 2Н), 3,28 (с, 3Н), 3,45 (т, 4-(1-Метил-2-етилімідазол-5-іл)-2-{4-[N-(22Н), 3,95 (с, 3Н), 4,92 (т, 1Н), 417 метоксіетил)сульфамоїл]аніліно}піримідин 7,03 (д, 1Н), 7,40 (с, 1Н), 7,58 (с, 1Н), 7,80 (м, 4Н), 8,39 (д, 1Н) 1,40 (т, 3Н), 3,15 (кв, 2Н), 3,30 (с, 3Н), 3,42 (т, 2Н), 3,96 (с, 3Н), 4-(1-Метил-2-ізопропілімідазол-5-іл)-2-{4-[N-(24,98 (т, 1Н), 7,03 (д, 1Н), 7,49 (с, 431 метоксіетил)сульфамоїл]аніліно}піримідин 1Н), 7,58 (с, 1Н), 7,80 (м, 4Н), 8,40 (д, 1Н) 0,08 (м, 2Н), 0,39 (м, 2Н), 0, 84 4-(1-Метил-2-ізопропілімідазол-5-іл)-2-{4-(N427 (циклопропілметил)сульфамоїл]аніліно}піримідин (м, 1Н), 1,30 (д, 6Н), 2,67 (м, 2Н), 3,20 (м, 1Н), 3,96 (с, 3Н), 4-(1-Етил-2-метилімідазол-5-іл)-2-{4-[N-(4метилтіазол-2ілметил)сульфамоїл]аніліно}піримідин Спос.48, Спос.27 Спос.49, Спос.27 Спос.50, Спос.27 Спос.111, Спос.51 Спос.111, Спос.41 Спос.111, Спос.46 Спос.111, Спос.52 Спос.28, Спос.40 Спос.29, Спос.40 Спос.61 Спос.30, Спос.45 Спос.30, Спос.40 Спос.31, Спос.40 Спос.31, Спос.41 4-(1-Метил-2-ізопропілімідазол-5-іл)-2-{4-[N687 (тетрагідрофур-2ілметил)сульфамоїл]аніліно}піримідин 696 4-(1-Метил-2-етилімідазол-5-іл)-2-{4-[N(циклопропілметил)сульфамоїл]аніліно}піримідин 4-(1-Метил-2-трифторметилімідазол-5-іл)-2-{4-[N707 (тетрагідрофур-2ілметил)сульфамоїл]анілін}піримідин 71 5-Хлор-4-(1,2-диметилімідазол-5-іл)-2-[4-(Ν-третбутил-Ν-метилсульфамоїл)аніліно]піримідин 72 4-(1-Етил-2-метилімідазол-5-іл)-2-[4-(Nалілсульфамоїл)аніліно]піримідин 7,27 (д, 1Н), 7,50 (т, 1Н), 7,69 (с, 1Н), 7,75 (д, 2Н), 7,97 (д, 2Н), 8,43 (д, 1Н), 9,93 (с, 1Н) 1,41 (д, 6Н), 1,90 (м, 3Н), 2,94 (м, 1Н), 3,15 (м, 2Н), 3,72 (кв, 1Н), 3,80 (кв, 1Н), 3,95 (м, 1Н), 457 4,04 (с, 3Н), 4,82 (т, 1Н), 7,08 (д, 1Н), 7,36 (с, 1Н), 7,60 (с, 1Н), 7,82 (м,4Н), 8,41 (д,2Н) 0,10 (м, 2Н), 0,45 (м, 2Н), 0, 91 (м, 1Н), 1,30 (т, 3Н), 2,82 (м, 4Н), 3,96 (с, 3Н), 4,76 (м, 1Н), 7,03 (д, 413 1Н), 7,46 (с, 1Н), 7,58 (с, 1Н), 7,82 (м, 4Н), 8,40 (д, 1Н) 1,51 (м, 1Н), 1,78 (м, 3Н), 2,74 (т, 2Н), 3,56 (м, 1Н), 3,65 (кв, 1Н), 3,76 (м, 1Н), 4,16 (с, 3Н), 7,36 (д, 483 1Н), 7,49 (т, 1Η), 7,73 (д, 2Н), 7,90 (м, 3Н), 8,60 (д, 1Н), 10,10 (с, 1Н) 1,23 (с, 9Н), 2,42 (с, 3Н), 2,85 (с, 3Н), 3,77 (с, 3Н), 7,65 (с, 1Н), 7,7 447 (д, 2Н), 7,87 (д, 2Н), 8,62 (с, 1Н), М-Н10,17 (с, 1Н) 1,20 (т, 3Н), 2,39 (с, 3Н), 3,40 (м, 2Н), 4,57 (кв, 2Н), 5,00 (д, 1Н), 5,14 (д,1Н), 5,67 (м,1Н), 7,21 (д, 399 1Н), 7,59 (т, 1Н), 7,68 (с, 1Н), 7,70 (д, 2Н), 7,89 (д, 2Н), 8,43 (д, 1Н), 9,82 (с, 1Н) Спос.31, Спос.45 Спос.30, Спос.41 Спос.32, Спос.45 Спос.111, Спос.64 Спос.27, Спос.53 1 Очи щають за допомогою флеш-хроматографії на силікагелі, елююючи DCM/2% метанольним розчином амонію (100:0, із збільшенням полярності до 95:5). 2 Очи щають за допомогою препаративної ВЕРХ (градієнт H2O:CH3CN (5:95, із збільшенням полярності до 95:5), що містить 0,2% ТФО протягом 8хв. на 21´100мм деактивованої RPB основній колонці з набиванням із С18). 3 Реакційну суміш випаровують перед витяганням у водній фазі з екстрагуванням EtOAc. Сирий продукт очищають за допомогою флеш-хроматографії на силікагелі, елююючи DCM/2% метанольним розчином амонію (100:0, із збільшенням полярності до 92:8). 4 Реакційну суміш випаровують перед витяганням у водній фазі з екстрагуванням EtOAc. Сирий продукт очищають за допомогою флеш-хроматографії на силікагелі, елююючи DCM/MeOH (98:2, із збільшенням полярності до 92:8). 5 Очи щають за допомогою флеш-хроматографії, елююючи DCM/MeOH (100:0, із збільшенням полярності до 95:5). 6 Очи щають за допомогою флеш-хроматографії, елююючи EtOAc/MeOH (100:0, із збільшенням полярності до 80:20). 7 Очи щають за допомогою флеш-хроматографії, елююючи EtOAc/MeOH (100:0, із збільшенням полярності до 90:10). Приклад 73 4-(1,2-Диметилімідазол-5-іл)-2-(4-{N-[2-(2-метоксіетокси)етил]сульфамоїл}аніліно)піримідину гідрохлорид 1М Ефірний розчин хлористого водню (4мл) додають до розчину 4-(1,2-диметилімідазол-5-іл)-2-(4-(Nтрет-бутоксикарбоніл)-N-[2-(2-метоксіетокси)етил]сульфамоїл)аніліно)піримідину (спосіб 55; 77мг, 0,14ммоль) в безводному діоксані (2мл), і суміш перемішують при температурі навколишнього середовища протягом 5 днів. Леткі продукти видаляють шляхом випаровування, і залишок розтирають з простим ефіром, збирають шляхом фільтрування, промивають простим ефіром (2´10мл) і сушать, з одержанням вказаної в заголовку сполуки (65мг (96%)) у вигляді жовтого твердого продукту. ЯМР 2,70 (с, 3Н), 2,86 (м, 2Н), 3,18 (с, 3Н), 3,36 (м, 4Н), 3,42 (м, 2Н), 4,08 (с, 3Н), 7,38 (д, 1Н), 7,58 (с, 1Н), 7,74 (д, 2Н), 7,93 (д, 2Н), 8,40 (с, 1Н), 8,69 (д, 1Н), 10,25 (с, 1Н); m/z 447. Приклади 74-75 Наступні далі сполуки синтезують аналогічно способу прикладу 73. Пр. Сполука 4-(1,2-Диметилімідазол-5-іл)-2-[4-(N-{2-[2-(274 метоксіетокси)етокси]етил}сульфамоїл)аніліно]піримідин гідрохлорид 75 4-(1,2-Диметилімідазол-5-іл)-2-{4-(N-(2-{2-[2-(2 ЯМР m/z SM 2,63 (с, 3Н), 2,84 (м, 2Н), 3,20 (с, 3Н), 3,40 (м, 10Н), 4,08 (с, 3Н), 7,38 (д, 1Н), 7,48 (м, 1Н), 7,73 491 Спос.56 (д, 2Н), 7,90 (д, 2Н), 8,38 (с, 1Н), 8,66 (д, 1Н), 10,22 (с, 1Н) 2,68 (с, 3Н), 2,85 (м, 2Н), 535 Спос.57 метоксіетокси)етокси]етокси}етил)сульфамоїл]аніліно}піриміди 3,20 (с, 3Н), 3,40 (м, н гідрохлорид 14Н), 4,08 (с, 3Н), 7,32 (д, 1Н), 7,46 (м, 1Н), 7,73 (д, 2Н), 7,89 (д, 2Н), 8,40 (с, 1Н), 8,62 (д, 1Н), 10,22 (с, 1Н) Приклад 76 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(2-мезилетил)сульфамоїл]аніліно}піримідин 4-Диметиламінопіридин (3мг, 0,025ммоль) і 3-метоксипропіламін (200мкл, 2ммоль) додають до розчину 4-(1,2-диметилімідазол-5-іл)-2-(4-(фторсульфоніл)аніліно)піримідину (спосіб 59; 87мг, 0,25ммоль) в NMP (1мл), і суміш нагрівають при 100°С протягом 18 годин. Суміші дають можливість охолодитися до температури навколишнього середовища, і розчинник видаляють шляхом випаровування. Залишок очищають за допомогою препаративної РХ-МС (постійний потік 5%об./об. (35% NH3 в МеОН) з градієнтом H2O:CH3CN) (5:95, із збільшенням полярності до 95:5) протягом 7,5хв.), з одержанням вказаної в заголовку сполуки (91мг, 81%) у вигляді твердого продукту. Я МР 2,38 (с, 3Н), 2,97 (с, 3Н), 3,11 (м, 2Н), 3,21 (м, 2Н), 3,95 (с, 3Н), 7,20 (д, 1Н), 7,61 (с, 1Н), 7,75 (м, 3Н), 7,95 (д, 2Н), 8,43 (д, 1Н), 9,95 (с, 1Н); m/z 451. Приклади 77-79 Наступні далі сполуки синтезують аналогічно способу прикладу 76. Пр. Сполука ЯМР 1,58 (м, 2Н), 2,33 (м, 9Н), 3,02 (т, 2Н), 3,64 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(3морфолінопропіл)сульфамоїл]аніліно}піримідин (м, 5Н), 3,90 (с, 3H), 6,95 (д, 1Н), 7,45 (м, 2Н), 7,72 (м, 4Н), 8,35 (д, 1Н) 2,01 (с, 6Н), 2,24 (т, 2Н), 2,40 (с, 3Н), 2,91 4-(1,2-Диметилімідазол-5-іл)-2-(4-{N-[2-(N,Nдиметиламіно)етил]сульфамоїл}аніліно)піримідин (т, 2Н), 3,93 (с, 3Н), 6,95 (д, 1Н), 7,42 (м, 2Н), 7,72 (м, 4Н), 8,34 (д, 1Н) 4-(1,2-Диметилімідазол-5-іл)-2-{4-[N-(2-піперидин- 1,40 (м, 6Н), 2,13 (м, 3Н), 2,30 (м, 6Н), 2,89 (т, 2Н), 3,90 (с, 3Н), 6,95 (д, 1Н), 7,45 (м, 1-ілетил)сульфамоїл]аніліно}піримідин 2Н), 7,72 (м, 4Н), 8,35 (д, 1Н) 77 78 79 m/z 472 416 456 Приклад 80 4[1-(2-Метоксіетил)-2-метилімідазол-5-іл]-(4-[N-(тетрагідрофур-2-ілметил)сульфамоїл]аніліно}піримідин Суміш 4-[1-(2-метоксіетил)-2-метилімідазол-5-іл]-2-N-(4-фторсульфоніланіліно)піримідину (спосіб 60; 200мг, 0,51ммоль) і диметиламінопіридину, нанесеного на полістирол (800мг: 1,6ммоль/г смоли) в 1-метил2-піролідоні (4мл) перемішують протягом 10 хвилин при температурі навколишнього середовища. Додають тетрагідрофур фуриламін (258мг, 2,55ммоль), і реакційну суміш нагрівають при 90°С протягом 40 годин, потім, при 100°С протягом 48 годин. Леткі продукти видаляють шляхом випаровування, і залишок очищають за допомогою колонкової хроматографії на силікагелі, елююючи DCM/MeOH (99:1, із збільшенням полярності до 96:4), для одержання очищеного продукту (120мг), розтирають з простим ефіром, збирають шляхом фільтрування і сушать при 80°С у вакуумі, з одержанням вказаної в заголовку сполуки (55мг, 23%). ЯМР 1,52 (м, 1Н), 1,70-1,88 (м, 3Н), 2,39 (с, 3Н), 2,75 (м, 2Н), 3,10 (с, 3Н), 3,49 (т, 2Н), 3,55 (м, 1Н), 3,67 (м, 1Н), 3,78 (м, 1Н), 4,74 (т, 2Н), 7,23 (д, 1Н), 7,49 (т, 1Н), 7,70 (д, 3Н), 7,85 (д, 2Н), 8,42 (д, 1Н), 9,79 (с, 1Н); m/z 473. Приклади 81-82 Наступні далі сполуки синтезують аналогічно прикладу 80. Пр. Сполука ЯМР m/z 0,06 (м, 2Н), 0,34 (м, 2Н), 0,79 (м, 1Н), 2,40 (с, 4-[1-(2-Метоксіетил)-2-метилімідазол-5-іл]-2-{43Н), 2,62 (т, 2Н), 3,11 (с, 3Н), 3,50 (т, 2Н), 4,76 [N443 (т, 2Н), 7,24 (д, 1Н), 7,50 (т, 1Н), 7,69 (с, 1Н), (циклопропілметил)сульфамоїл]аніліно}піриміди 7,70 (д, 2Н), 7,87 (д, 2Н), 8,42 (д, 1Н), 9,79 (с, н 1Н) 1,60 (м, 2Н), 2,40 (с, 3Н), 2,77 (ушир.т, 2Н), 4-[1-(2-Метоксіетил)-2-метилімідазол-5-іл]-2-{4- 3,12 (с, 3Н), 3,15 (с, 3Н), 3,28 (м, 2Н), 3,52 (т, [N-(32Н), 4,74 (т, 2Н), 7,24 (д, 1Н), 7,36 (ушир.с, 1Н), 461 7,70 (д, 3Н), 7,88 (д, 2Н), 8,40 (д, 1Н), 9,80 (с, метоксипропіл)сульфамоїл]аніліно}піримідин 1Н) 811 822 1 Очи щають за допомогою колонкової хроматографії, елююючи DCM/MeOH (98:2, із збільшенням полярності до 90:10). 2 Очи щають за допомогою колонкової хроматографії, елююючи DCM/MeOH (98:2, із збільшенням полярності до 95:5). Приклад 83 4-(1-Етил-2-метилімідазол-5-іл)-2-(4-(N-(гідроксіетил)сульфамоїл)аніліно)піримідин Хлорсуль фонову кислоту (150мкл, 2,16ммоль) додають по краплях до розчину 2-аніліно-4-(1-етил-2метилімідазол-5-іл)піримідину (приклад 28; 150мг, 0,54ммоль) в тіонілхлориді (3мл), охолодженому при 0°С, і суміш перемішують при 0°С протягом 10 хвилин, потім нагрівають при 90°С протягом 90 хвилин. Леткі продукти видаляють шляхом випаровування, і залишок сушать у високому вакуумі (
ДивитисяДодаткова інформація
Назва патенту англійськоюImidazolo-5-yl-2-anilinepyrimidines as agents for inhibiting cells proliferation
Назва патенту російськоюИмидазоло-5-ил-2-анилинопиримидины как агенты для ингибирования пролиферации клеток
Автори російськоюThomas, Andrew, Peter
МПК / Мітки
МПК: C07D 403/04, A61P 37/02, A61P 9/10, A61P 27/02, C07D 403/14, C07D 417/14, A61P 43/00, A61P 19/02, A61K 31/506, C07D 413/14, A61P 19/08, A61K 31/5377, C07D 405/14, A61P 17/06, A61P 35/02, A61P 29/00, C07D 401/14, A61P 35/00
Мітки: імідазоло-5-іл-2-анілінопіримідини, агенти, клітин, проліферації, інгібування
Код посилання
<a href="https://ua.patents.su/41-74206-imidazolo-5-il-2-anilinopirimidini-yak-agenti-dlya-ingibuvannya-proliferaci-klitin.html" target="_blank" rel="follow" title="База патентів України">Імідазоло-5-іл-2-анілінопіримідини як агенти для інгібування проліферації клітин</a>
Попередній патент: Відеопроекційна система для зовнішньої та внутрішньої реклами
Наступний патент: Головний аеродинамічний обтічник космічної ракети
Випадковий патент: Пристрій для компресійного остеосинтезу при оперативному лікуванні ушкоджень проксимального відділу стегна












