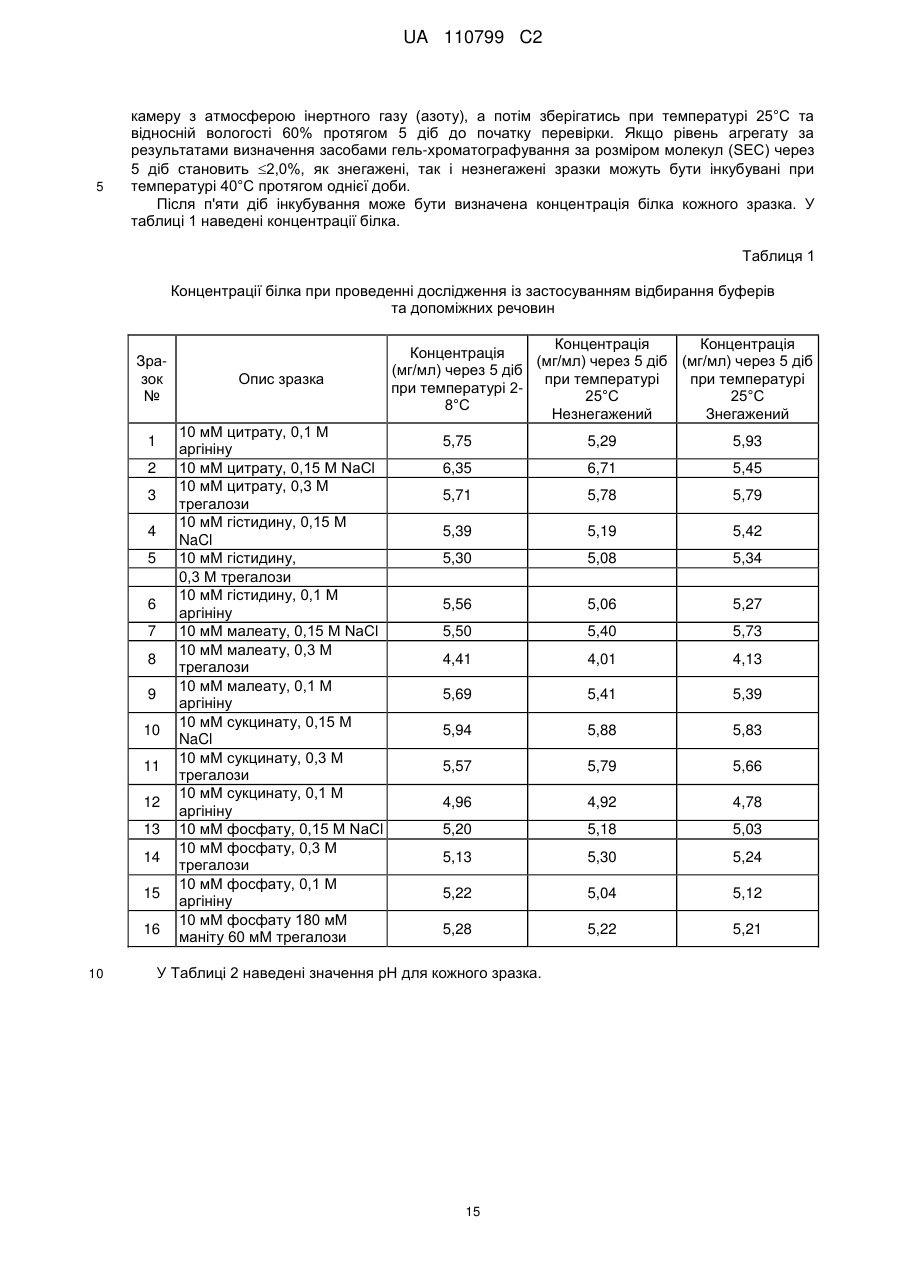
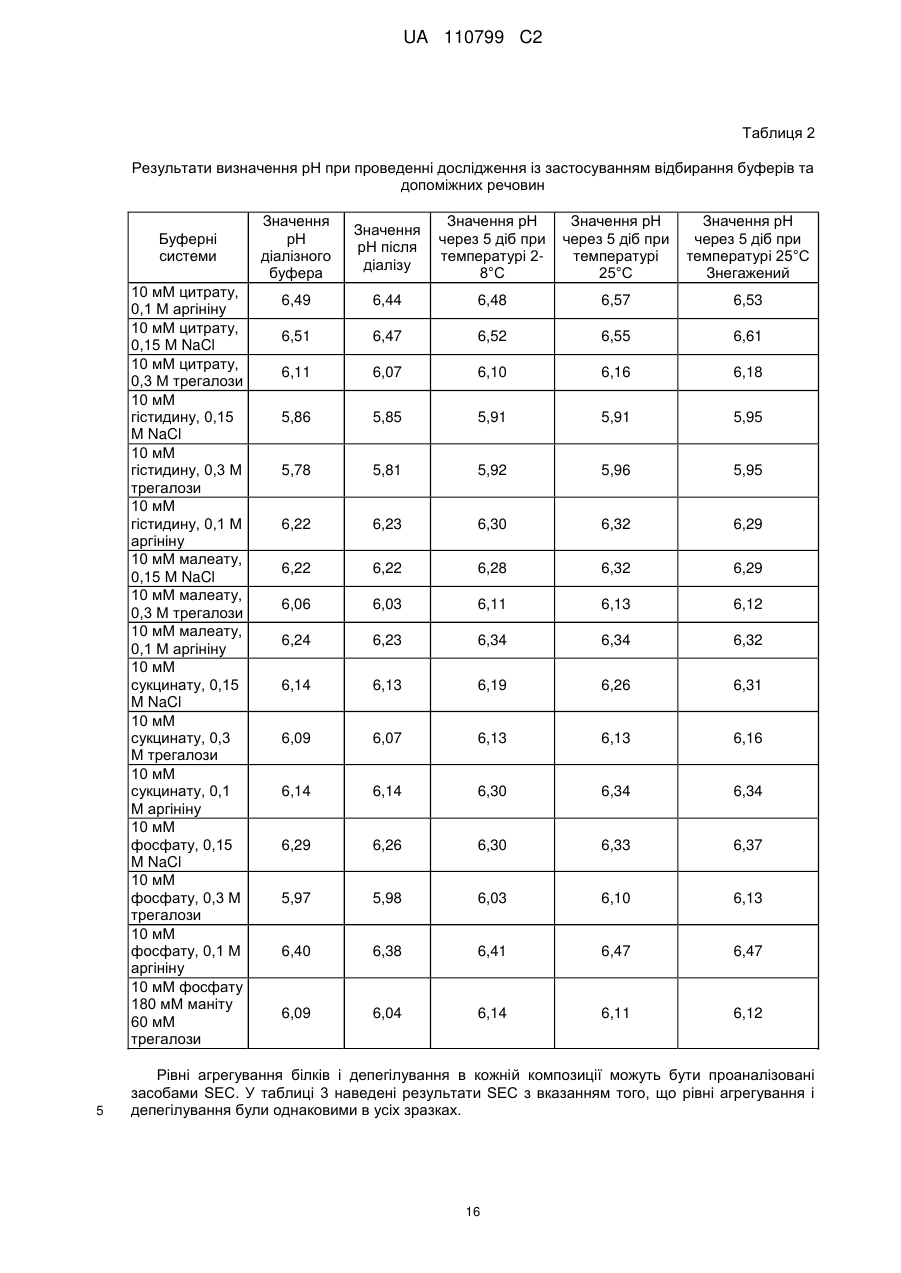
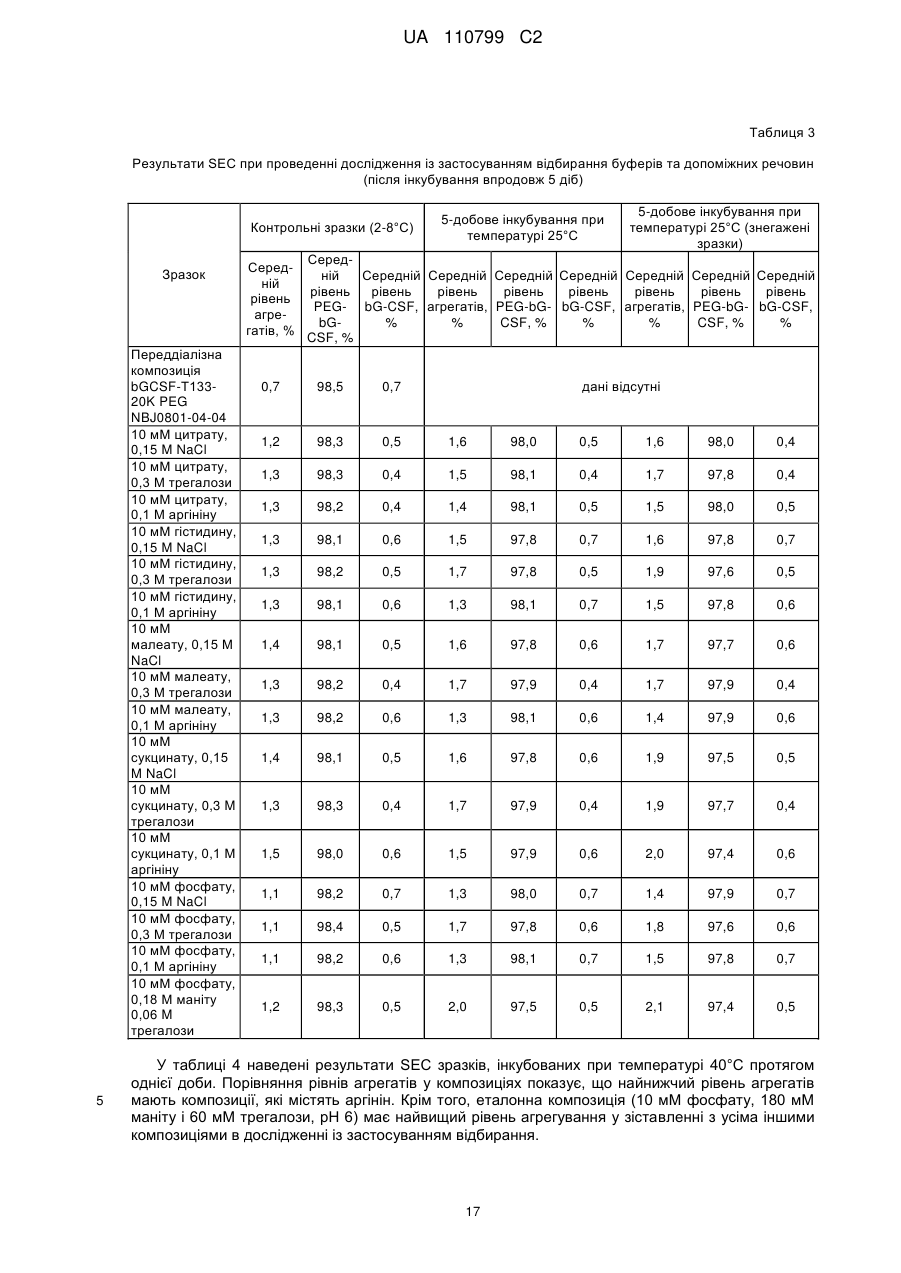
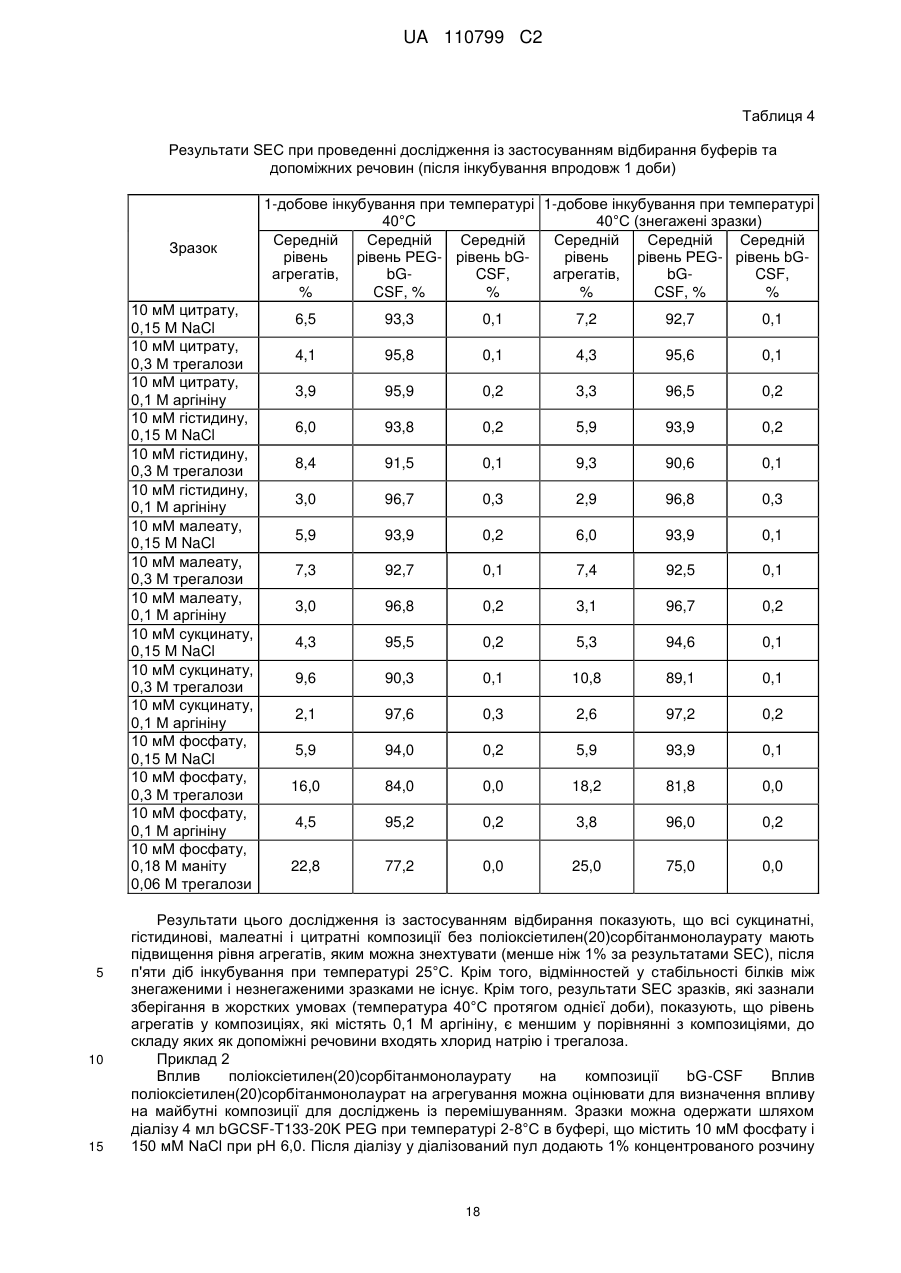
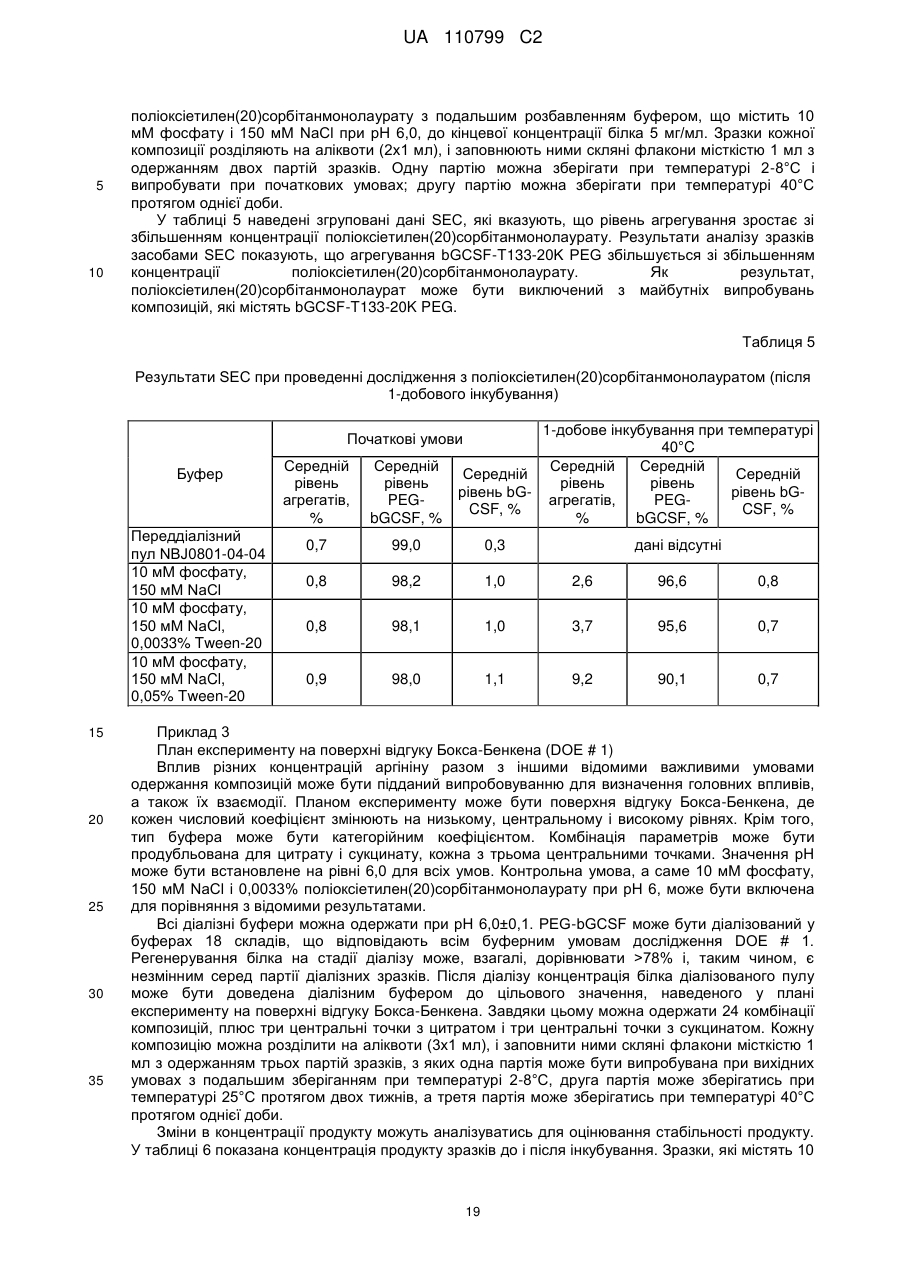
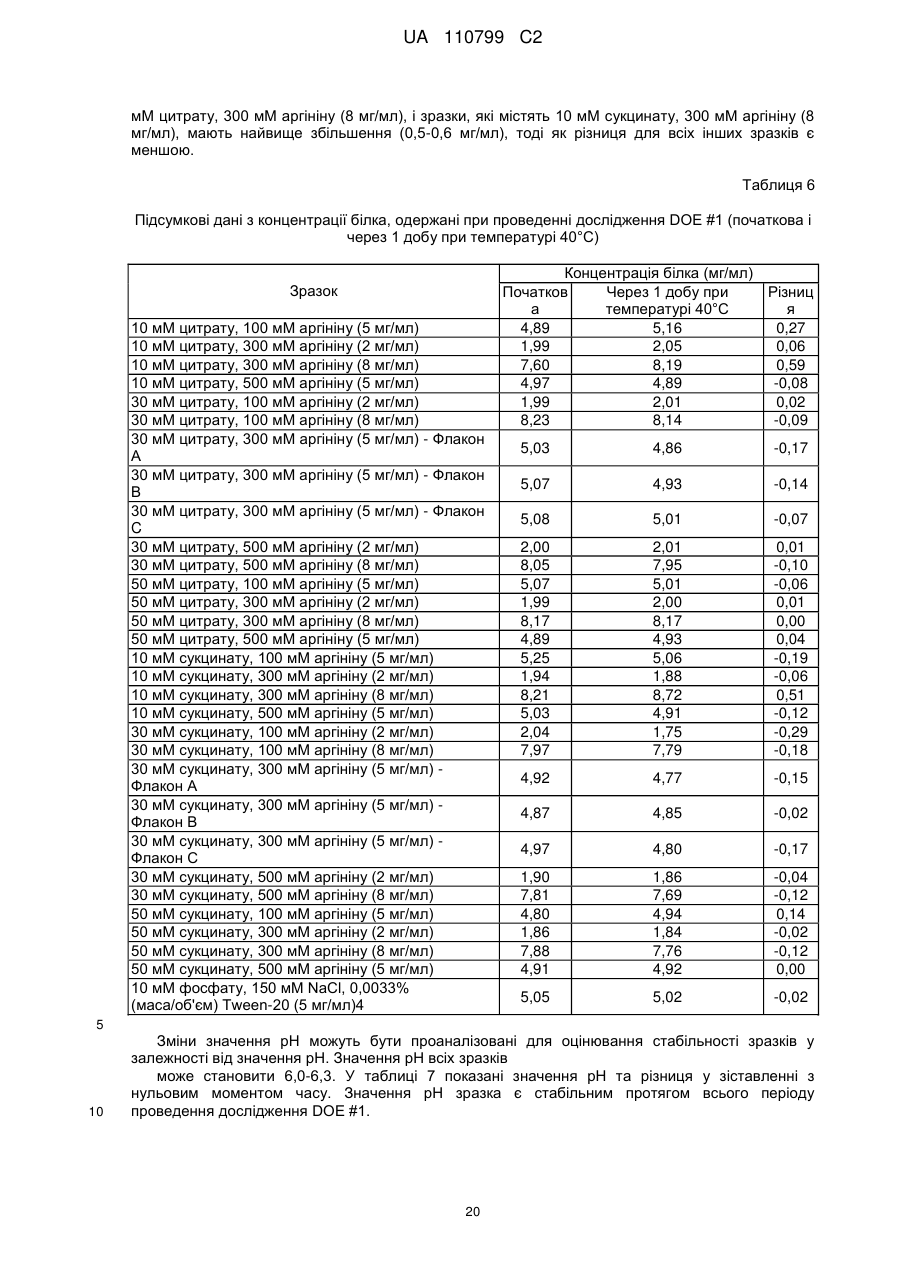
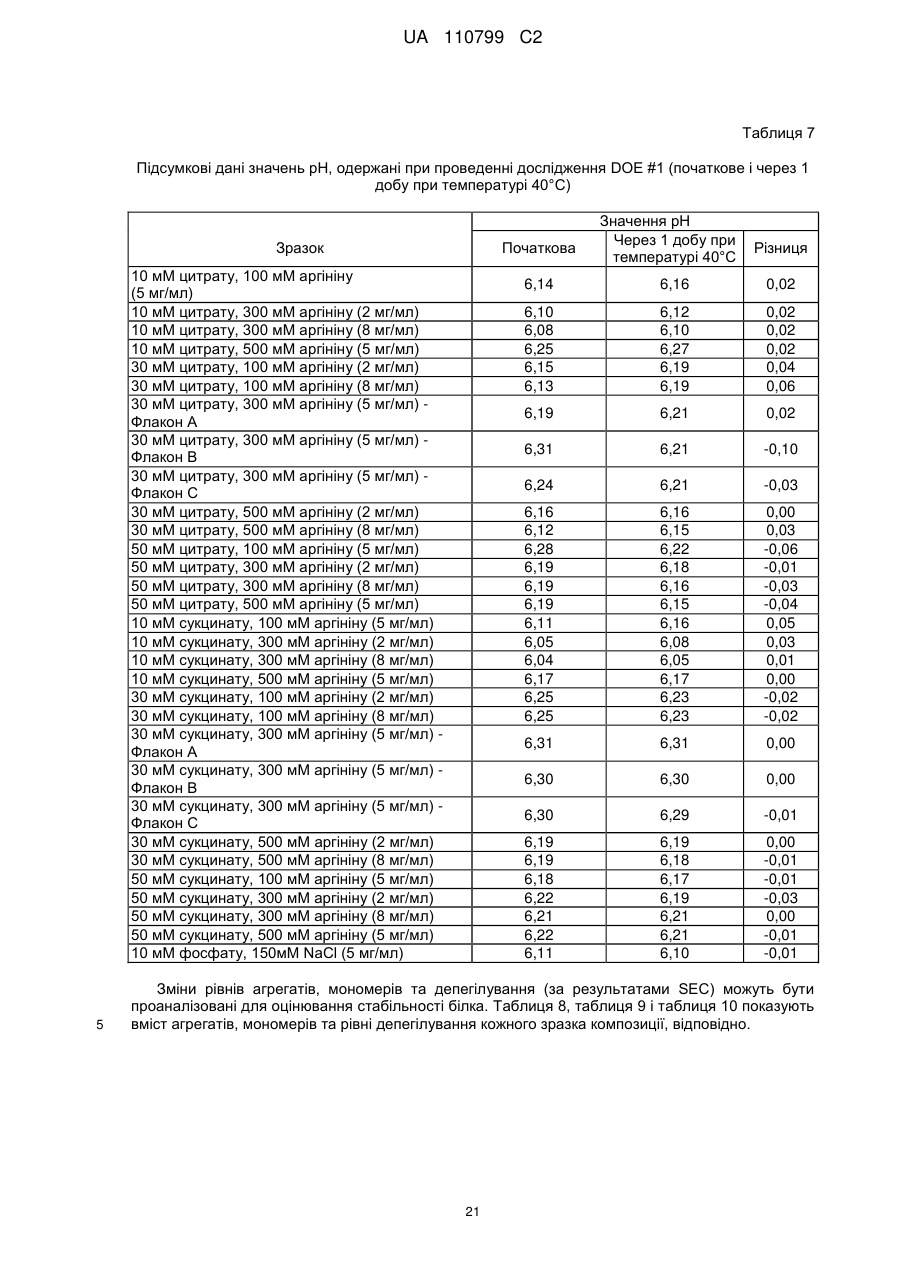
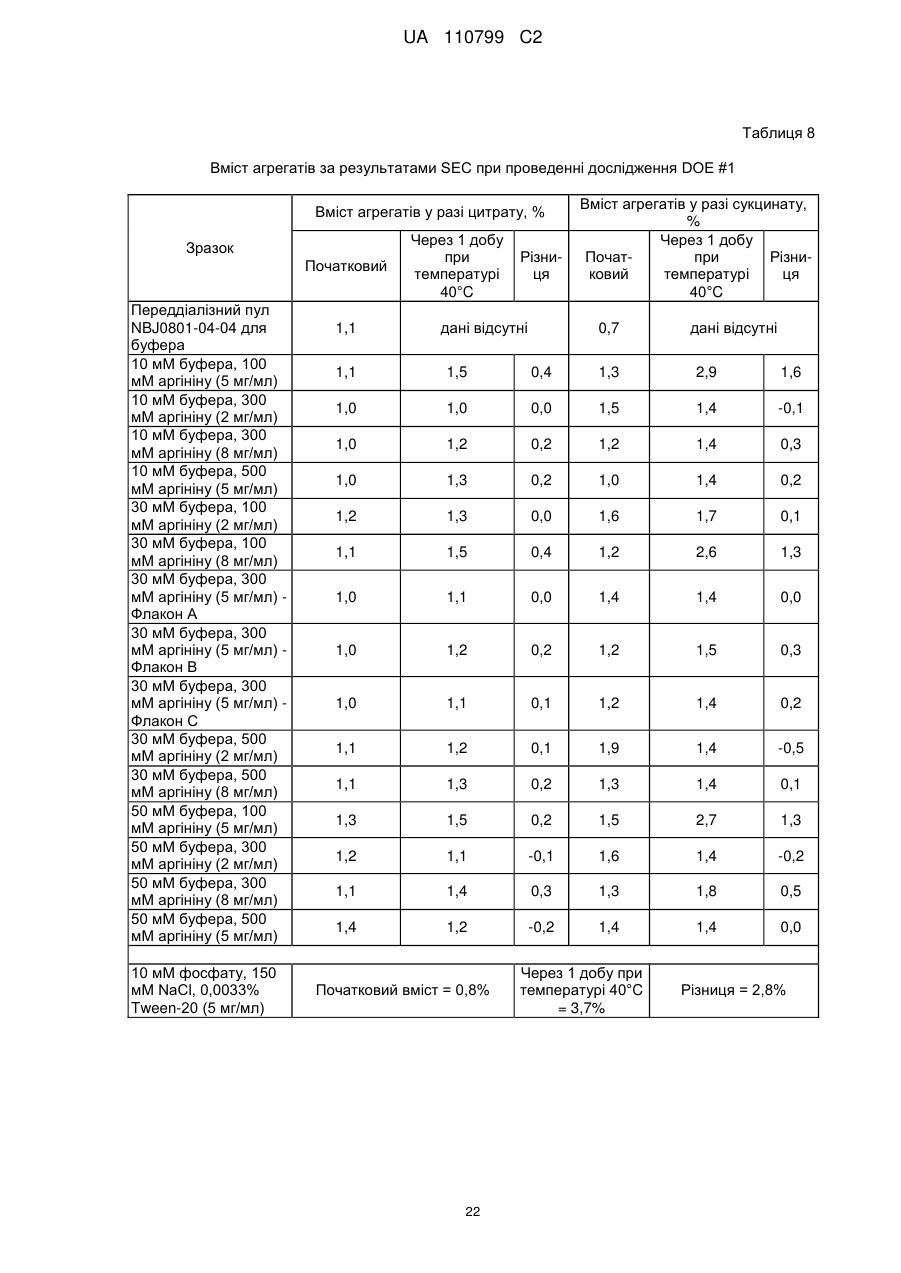
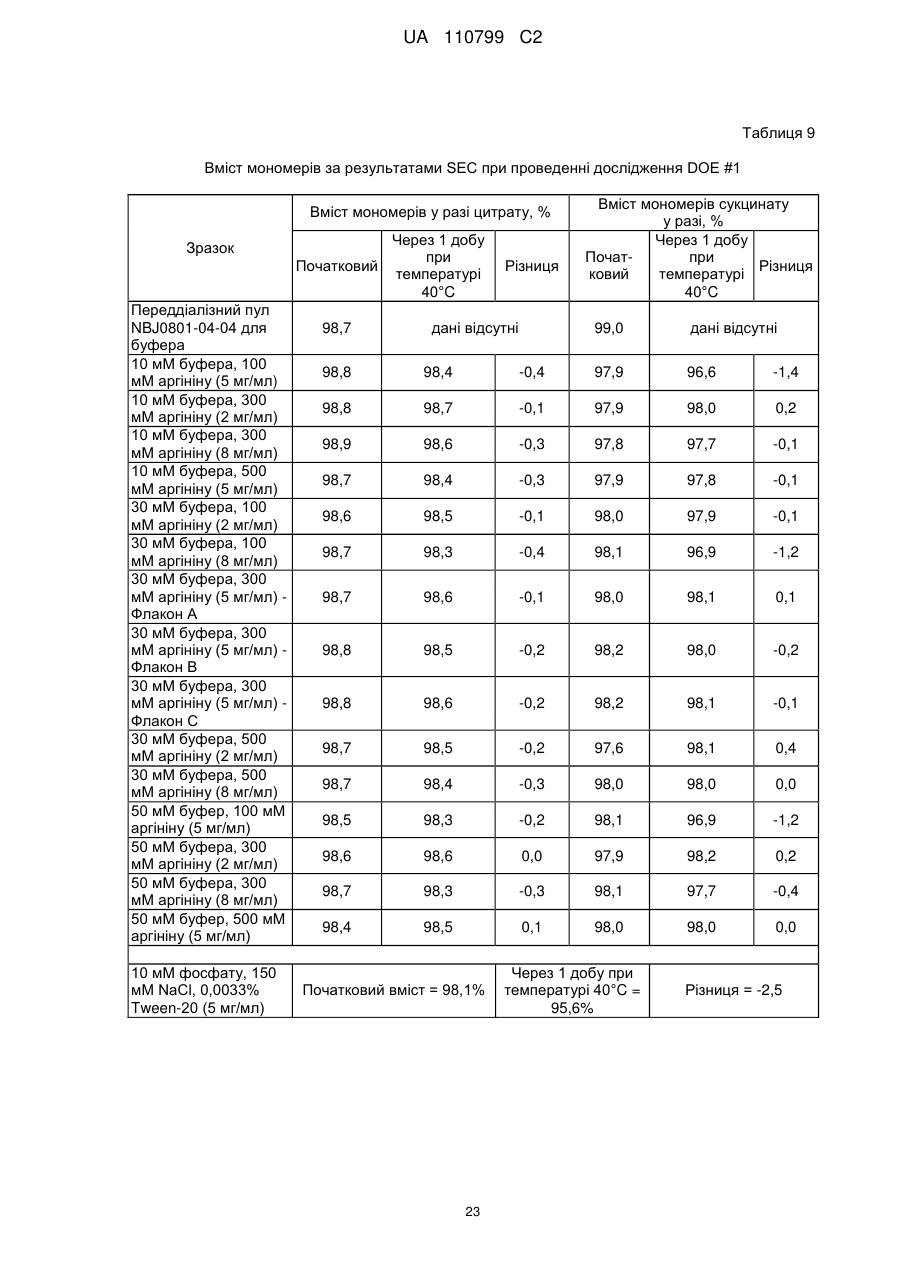
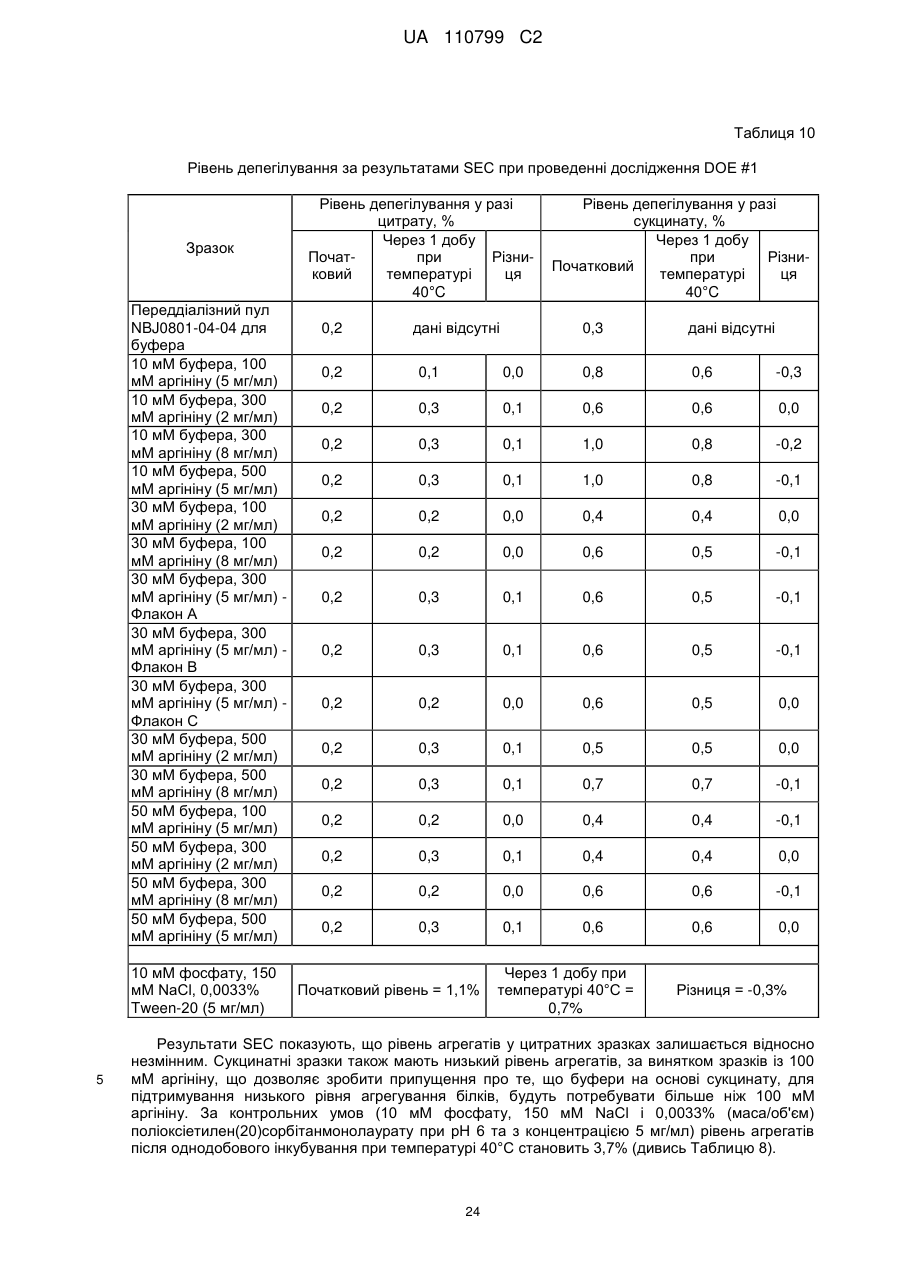
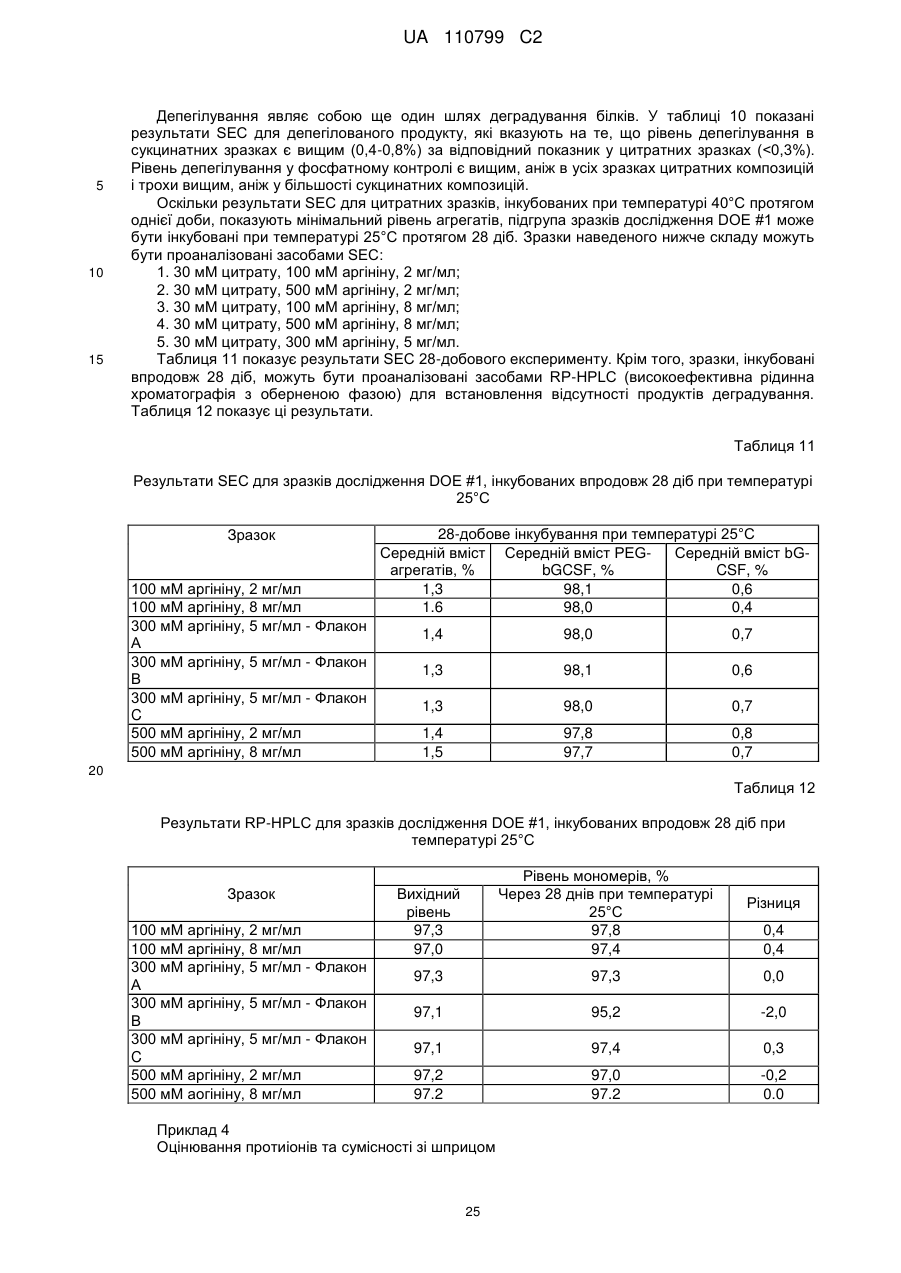
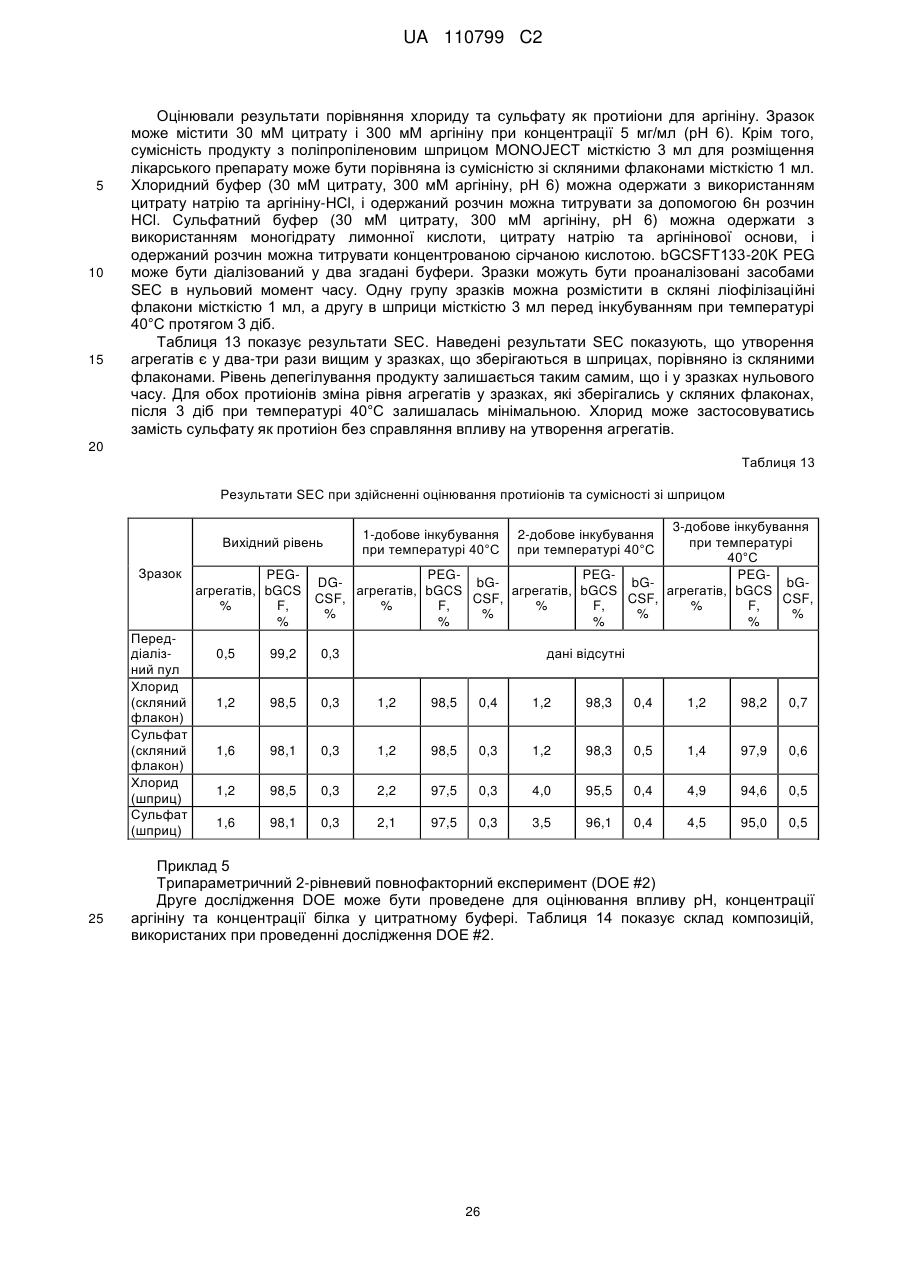
Стабільна водна композиція, яка містить бичачий гранулоцитарний колонієстимулювальний фактор
Номер патенту: 110799
Опубліковано: 25.02.2016
Автори: Кха Кетрін Нгань, Клотц Алан Воскемп, Даваньїно Джуан
Формула / Реферат
1. Стабільна водна композиція, яка містить bG-CSF-T133pAF-20K PEG, цитратний або сукцинатний буфер, аргінін і факультативно - протиіон для аргініну, причому ця композиція містить менше ніж 0,001 % поверхнево-активної речовини.
2. Композиція за п. 1, яка відрізняється тим, що протиіон для аргініну являє собою хлорид або сульфат.
3. Композиція за п. 1 або п. 2, яка відрізняється тим, що поверхнево-активна речовина являє собою поверхнево-активну речовину типу полісорбату.
4. Композиція за будь-яким із пп. 1-3, яка відрізняється тим, що bG-CSF-T133pAF-20K PEG присутній у кількості від приблизно 0,5 г/л до приблизно 12 г/л, згаданий буфер є цитратним буфером, який має молярність приблизно 30 мМ, аргінін має молярність приблизно 250 мМ, причому значення рН композиції становить від приблизно 5,7 до приблизно 6,6.
5. Композиція за будь-яким із пп. 1-4, яка факультативно містить один або декілька інших терапевтичних інгредієнтів.
6. Спосіб лікування тварини, яка має розлад, модульований bG-CSF, який включає введення згаданій тварині терапевтично ефективної кількості композиції за будь-яким із пп. 1-5.
7. Спосіб за п. 6, який відрізняється тим, що згаданим розладом є мастит і згаданою твариною є корова у перед- та післяпологовий період.
Текст
Реферат: Винахід стосується стабільної водної композиції, яка містить bG-CSF-T133pAF-20K PEG, цитратний або сукцинатний буфер, аргінін і факультативно - протиіон для аргініну, причому ця композиція містить менше ніж 0,001 % поверхнево-активної речовини, та її застосування для лікування тварин. UA 110799 C2 (12) UA 110799 C2 UA 110799 C2 5 10 15 20 25 30 35 40 45 50 55 60 Гранулоцитарний колонієстимулювальний фактор (G-CSF) є членом мультигенної родини, що включає гени гормону росту. G-CSF стимулює проліферацію специфічних клітинпопередників кісткового мозку і їх диференціацію в гранулоцити. Крім того, G-CSF є потужним стимулом для проліферації і визрівання нейтрофілів in vivo (Cohen et al., Proc. Natl. Acad. Sci. 1987; 84: 2484-2488; дивись також Heidari et al., Vet. Immol. Imunopathol. 2001; 81:45-57). G-CSF також здатен індукувати функціональну активацію або "праймування" зрілих нейтрофілів in vitro (Weisbart R.H. et al., Annals of Internal Medicine 1989; 110:297-303). Було показано, що G-CSF праймує людські гранулоцити і посилює вивільнення супероксиду, стимульоване хемотактичним пептидом, N-формілметіоніллейцилфенілаланіном (S. Kitagawa, et al., Biochem. Biophys. Res. Commun. 1987; 144:1143-1146, та CF. Nathan, Blood 1989; 74:301-306), та активує IgAопосередкований фагоцитоз людськими нейтрофілами (Weisbart R.H., et al., Nature 1988; 332: 647-649). Було встановлено, що G-CSF є придатним для лікування симптомів, для яких збільшення кількості нейтрофілів буде забезпечувати сприятливий вплив. G-CSF є також корисним окремо або в комбінації з іншими сполуками (такими як інші цитокіни) для росту або розмноження клітин в культурі, наприклад, для трансплантатів кісткового мозку. Були описані клонування кДНК і експресія рекомбінантного людського G-CSF (hG-CSF), і рекомбінантний hG-CSF демонструє більшість (якщо не всі) біологічних властивостей природної молекули (Souza L. et al., Science 232, 61-65 (1986)). Аналіз послідовності кДНК і геномних клонів ДНК дозволив встановити амінокислотну послідовність і показав, що довжина білка становить 204 амінокислоти із сигнальною послідовністю з 30 амінокислот. Довжина зрілого білка становить 174 амінокислоти, і він не має потенційних N-сполучених центрів глікозилування, а лише декілька можливих центрів для О-сполученого глікозилування. Фармацевтичні препарати, які містять hG-CSF, є відомими в цій галузі і охоплюють численні композиції. Наприклад, різні композиції hG-CSF описані у Piedmonte et al., Advanced Drug Delivery Reviews, 60: 50-58 (2008), Herman et al., Formulation, Characterization, and Stability of Protein Drugs, Rodney Pearlman and Y. John Wang, eds., Plenum Press, New York (1996), патенті США № 5,919,757 на ім'я Michaelis et al., та патенті США № 6,908,610 на ім'я Sato et al. Поверхнево-активні речовини традиційно включають до складу композицій, які містять hG-CSF, і вони можуть запобігати взаємодії hG-CSF, розташованого на потенційно дестабілізувальних поверхнях розділу, з поверхнями, з якими зустрічаються під час обробки, а також запобігати зміні його конформаційної стабільності. Були описані також клонування кДНК і експресія рекомбінантного бичачого G-CSF (bG-CSF). Наприклад, полінуклеотидна і поліпептидна послідовність зрілого bG-CSF описана у патенті США № 5,849,883, в якому також описані способи клонування, виділення і очищення поліпептиду і його аналогів. Зрілий bG-CSF має 174 амінокислоти в довжину і 82% гомологію з hG-CSF. Heidari et al., supra, описує експресію, очищення і біологічні активності bG-CSF. Введення b-CSF великій рогатій худобі може забезпечити сприятливу терапевтичну дію. Відповідно, бажано використовувати терапевтичний потенціал фармацевтичної композиції, яка містить bG-CSF. Однак результатом розробки фармацевтичних композицій, які містять b-CSF, за традиційними способами, відомими в цій галузі, є одержання небажаних властивостей продукту, таких як агрегування і дестабілізування поліпептиду bG-CSF та/або такої композиції. Отже, існує потреба в стабільній фармацевтичній композиції, яка містить bG-CSF, з бажаними властивостями, такими як мінімальний рівень агрегування і дестабілізування продукту. Відповідно, цей винахід пропонує стабільні водні фармацевтичні композиції з поліпептидом bG-CSF або його варіантом, які демонструють бажані властивості, а також забезпечують відповідні переваги. Цей винахід пропонує стабільні водні композиції, які містять поліпептид bG-CSF або його варіант, буферну речовину та допоміжну речовину, при цьому згадана композиція по суті не містить поліоксіетилен(20)сорбітанмонолаурату. Цей винахід також пропонує способи застосування ліофілізованої або порошкоподібної форми і способи одержання композиції. Стабільні водні композиції бичачого гранулоцитарного колонієстимулювального фактора ("bG-CSF") за цим винаходом містять поліпептид bG-CSF або його варіант. У значенні, вжитому у цьому описі, термін "бичачий поліпептид G-CSF" (який альтернативно позначається як "поліпептид bG-CSF", "бичачий G-CSF" або "bG-CSF") та його варіанти, буде охоплювати ті поліпептиди і білки та їх варіанти, які мають щонайменше одну біологічну активність CSF, аналоги bG-CSF, мутанти bG-CSF, змінений глікозильований bG-CSF, PEG-кон'югований bGCSF, ізоформи bG-CSF, міметики bG-CSF, фрагменти bG-CSF, гібридні білки bG-CSF, гібридні білки, олігомери і мультимери, гомологи, глікозильовані варіанти, варіанти, сплайсовані варіанти і мутеїни, незалежно від їхньої біологічної активності, а також незалежно від методу їх 1 UA 110799 C2 5 10 15 20 25 30 35 40 45 синтезування або одержання, включаючи, але без обмеження ними, одержані рекомбінантними методами (продуковані з кДНК, геномної ДНК, синтетичної ДНК або нуклеїнової кислоти іншої форми), in vitro, in vivo, мікроін'єкцією нуклеїновокислотних молекул, синтетичними, трансгенними і ген-активованими методами. На додаток до цього, термін "поліпептид bG-CSF" або його варіант охоплює поліпептиди bG-CSF, які містять одну або декілька амінокислотних замін, додань або делецій. Приклади аналогів бичачого bG-CSF дивись у патенті США № 5,849,883. Послідовність зрілого поліпептиду bG-CSF довжиною 174 амінокислоти виглядає так: Крім того, поліпептид bG-CSF з початковим метіоніновим амінокислотним залишком виглядає так: Були описані заміни в найрізноманітніших положеннях амінокислот в bG-CSF. Заміни, в тому числі, але без обмеження ними, ті заміни, які модулюють фармацевтичну стабільність, підвищують агоністичну активність, підвищують стійкість до протеаз, перетворюють поліпептид на антагоніст тощо, охоплюються терміном "поліпептид bG-CSF або його варіант". Термін "поліпептид bG-CSF або його варіант" також охоплює глікозильований bG-CSF, такий як, але без обмеження ними, поліпептиди, глікозильовані в будь-якому амінокислотному положенні, N-сполучені глікозильовані форми поліпептиду або О-сполучені глікозильовані форми поліпептиду. Варіанти, які містять одиничні нуклеотидні заміни, також розглядаються як біологічно активні варіанти поліпептиду bG-CSF. Варіанти, які містять одиничні нуклеотидні заміни, також розглядаються як біологічно активні варіанти bG-CSF. Крім того, охоплюються також сплайсовані варіанти. Термін "поліпептид bG-CSF або його варіант" також охоплює гетеродимери bG-CSF, гомодимери, гетеромультимери або гомомультимери будь-якого одного або декількох bG-CSF чи будь-якого іншого поліпептиду, білка, вуглеводу, полімеру, невеликої молекули, лінкеру, ліганду або іншої активної молекули будь-якого типу, сполучену хімічним шляхом або експресовану у вигляді гібридного білка (дивись, наприклад, патенти США № 6,261,550; № 6,166,183; № 6,204,247; № 6,261,550 та № 6,017,876), а також поліпептидні аналоги, які містять, наприклад, специфічні делеції або інші модифікації, але зберігають біологічну активність (дивись, наприклад, патенти США № 6,261,550; № 6,004,548 і № 6,632,426). Поліпептиди bG-CSF та їх варіанти описані, наприклад, в заявці на патент США 12/507,237 (наразі публікації патентної заявки США 2010/0035812), яка включена до цього опису шляхом посилання. За деякими варіантами здійснення цього винаходу одна або декілька штучно закодованих амінокислот введена(-і) до складу bG-CSF в одному або декількох із таких положень: 8, 62, 69, 125, 133, 136 та будь-якій їх комбінації (зрілий поліпептид bG-CSF або відповідні амінокислоти у поліпептиді bG-CSF з початковим метіоніновим амінокислотним залишком). За деякими варіантами здійснення цього винаходу штучно закодованою амінокислотою, пара-ацетилфенілаланіном (pAF), замінена природно закодована амінокислота в одному з таких положень: S8, S62, L69, G125, Т133, A136 та будь-якій їх комбінації (зрілий поліпептид bG-CSF або відповідні амінокислоти у поліпептиді bG-CSF з початковим метіоніновим амінокислотним залишком). За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-S8pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні S8. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-S62pAF, який має послідовність: 2 UA 110799 C2 в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні S62. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-L69pAF, який має послідовність: 5 10 15 20 25 30 35 в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні L69. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-G125pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні G125. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-T133pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні Т133. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-A136pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні А136. Композиція за цим винаходом може містити поліпептид bG-CSF або його варіант, який є сполученим із лінкером, полімером або біологічно активною молекулою. Лінкери, полімери та біологічно активні молекули описані в заявці на патент США 12/507,237 (на цей час публікації патентної заявки США 2010/0035812). Термін "зв'язок" або "лінкер" вжитий у цьому описі для позначення груп або зв'язків, які зазвичай утворюються в результаті хімічної реакції, і які, як правило, є ковалентними зв'язками. Термін "гідролітично стабільні зв'язки" означає, що зв'язки є по суті стабільними у воді і не реагують із водою при застосовуваних значеннях рН, у тому числі, але без обмеження, за фізіологічних умов, протягом тривалого періоду часу, можливо, навіть необмежено довго. Термін "гідролітично нестабільні або розкладні зв'язки" означає, що зв'язки розкладаються у воді або у водних розчинах, в тому числі, наприклад, крові. Термін "ферментативно нестабільні або розкладні зв'язки" означає, що зв'язок може бути зруйнований одним або декількома ферментами. Як відомо у цій галузі, PEG і споріднені полімери можуть містити розкладні зв'язки у полімерному каркасі або в лінкерній групі між полімерним каркасом та однією або декількома кінцевими функціональними групами полімерної молекули. Наприклад, складноефірні зв'язки, утворені в результаті реакції PEG-карбонових кислот або активованих PEG-карбонових кислот зі спиртовими групами на біологічно активній речовині, як правило, гідролізуються за фізіологічних умов з вивільненням згаданої речовини. Інші гідролітично розкладні зв'язки охоплюють, але без обмеження ними, карбонатні зв'язки; імінові 3 UA 110799 C2 5 10 15 20 25 30 35 40 45 50 55 зв'язки, утворені в результаті реакції аміну та альдегіду; фосфатноскладноефірні зв'язки, утворені в результаті реакції спирту з фосфатною групою; гідразонові зв'язки, які є продуктом реакції гідразиду та альдегіду; ацеталеві зв'язки, які є продуктом реакції альдегіду і спирту; ортоскладноефірні зв'язки, які є продуктом реакції форміату та спирту; пептидні зв'язки, утворені аміногрупою, в тому числі, але без обмеження, розташованою на кінці полімеру, такого як PEG, і карбоксильною групою пептиду; та олігонуклеотидні зв'язки, утворені фосфорамідитною групою, в тому числі, але без обмеження, розташованою на кінці полімеру, та 5'-гідроксильною групою олігонуклеотиду. За деякими варіантами здійснення цього винаходу поліпептид bG-CSF або його варіант сполучений з водорозчинним полімером. У значенні, вжитому у цьому описі, термін "водорозчинний полімер" означає будь-який полімер, який є розчинним у водних розчинниках. Результатом зв'язку водорозчинних полімерів із поліпептидом bG-CSF або його варіантом можуть бути зміни, в тому числі, але без обмеження ними, підвищений або модульований період напіввиведення із сироватки, підвищений або модульований півперіод існування лікарського засобу по відношенню до немодифікованої форми, модульована імуногенність, модульовані характеристики фізичного з'єднання, такі як агрегування і утворення мультимерів, зміни зв'язування з рецептором, зміни зв'язування з одним або декількома партнерами зв'язування і зміна димеризації або мультимеризації рецептора. Водорозчинний полімер може мати або не мати своєї власної біологічної активності і може бути застосований як лінкер для зв'язування bG-CSF з іншими речовинами, у тому числі, але без обмеження ними, з одним або декількома поліпептидами bG-CSF або їх варіантами, чи з однією або декількома біологічно активними молекулами. До прийнятних полімерів належать, але без обмеження ними, поліетиленгліколь, поліетиленглікольпропіональдегід, його моно-C1-C10-алкоксиабо арилоксипохідні (описані в патенті США № 5,252,714), монометоксиполіетиленгліколь, полівінілпіролідон, полівініловий спирт, поліамінокіслоти, співполімер дивінілового простого ефіру з малеїновим ангідридом, N-(2-гідроксипропіл)метакриламід, декстран, похідні декстрану, включаючи сульфат декстрану, поліпропіленгліколь, співполімер поліпропіленоксиду/етиленоксиду, поліоксіетильований поліол, гепарин, фрагменти гепарину, полісахариди, олігосахариди, глікани, целюлоза і похідні целюлози, у тому числі, але без обмеження ними, метилцелюлоза і карбоксиметилцелюлоза, крохмаль і похідні крохмалю, поліпептиди, поліалкіленгліколь та його похідні, співполімери поліалкіленгліколей та їх похідні, полівінілетилові прості ефіри, альфа-бета-полі-[(2-гідроксіетил)-DL-аспартамід тощо, або їх суміші. До прикладів таких водорозчинних полімерів належать, але без обмеження ними, поліетиленгліколь і сироватковий альбумін. У WO 03/074087 та WO 03/074088 описане кон'югування білків або невеликих молекул з гідроксіалкілкрохмалем (HAS). До прикладів гідроксіалкілкрохмалів належать, але без обмеження ними, гідроксіетилкрохмаль. Кон'югати гідроксіалкілкрохмалю та іншої молекули, наприклад, можуть включати ковалентний зв'язок між кінцевими альдегідними групами HAS і реакційними групами іншої молекули. За деякими варіантами здійснення цього винаходу водорозчинним полімером є полі(етиленгліколева) складова. За деякими варіантами здійснення цього винаходу полі(етиленгліколева) складова має молекулярну масу від приблизно 0,1 кДа до приблизно 100 кДа. За іншим варіантом здійснення цього винаходу водорозчинний полімер має молекулярну масу від приблизно 0,1 кДа до приблизно 50 кДа. За деякими варіантами здійснення цього винаходу водорозчинний полімер має молекулярну масу від приблизно 10 кДа до приблизно 30 кДа. За іншим варіантом здійснення цього винаходу водорозчинний полімер має молекулярну масу від приблизно 15 кДа до приблизно 25 кДа. За ще одним варіантом здійснення цього винаходу водорозчинний полімер має молекулярну масу приблизно 20 кДа. Фахівцю у цій галузі буде зрозуміло, що термін "водорозчинний полімер з молекулярною масою приблизно 20 кДа" передбачає мінливість молекулярної маси, яка становить приблизно 15% (тобто від приблизно 17 кДа до приблизно 23 кДа), виходячи із детального опису та полідисперсності згаданого полімеру. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-S8pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні S8 і сполучена з полі(етиленгліколевою) складовою. Наприклад, якщо полі(етиленгліколева) 4 UA 110799 C2 5 10 15 20 25 30 35 40 складова має молекулярну масу приблизно 20 кДа, поліпептид bG-CSF або його варіант за цим варіантом здійснення може бути визначений як "bG-CSF-S8pAF-20K PEG", що вказує на те, що полі(етиленгліколева) складова, молекулярна маса якої становить 20 кДа, сполучена із заміною pAF, яка була виконана у положенні S8. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-S62pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні S62 і сполучена з полі(етиленгліколевою) складовою. Наприклад, якщо полі(етиленгліколева) складова має молекулярну масу приблизно 20 кДа, поліпептид bG-CSF або його варіант за цим варіантом здійснення може бути визначений як "bG-CSF-S62pAF-20K PEG", що вказує на те, що полі(етиленгліколева) складова, молекулярна маса якої становить 20 кДа, сполучена із заміною pAF, яка була виконана у положенні S62. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-L69pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні L69 і сполучена з полі(етиленгліколевою) складовою. Наприклад, якщо полі(етиленгліколева) складова має молекулярну масу приблизно 20 кДа, поліпептид bG-CSF або його варіант за цим варіантом здійснення може бути визначений як "bG-CSF-L69pAF-20K PEG", що вказує на те, що полі(етиленгліколева) складова, молекулярна маса якої становить 20 кДа, сполучена із заміною pAF, яка була виконана у положенні L69. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-G125pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні G125 і сполучена з полі(етиленгліколевою) складовою. Наприклад, якщо полі(етиленгліколева) складова має молекулярну масу приблизно 20 кДа, поліпептид bG-CSF або його варіант за цим варіантом здійснення може бути визначений як "bG-CSF-G125pAF-20K PEG", що вказує на те, що полі(етиленгліколева) складова, молекулярна маса якої становить 20 кДа, сполучена із заміною pAF, яка була виконана у положенні G125. За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-T133pAF, який має послідовність: в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні Т133 і сполучена з полі(етиленгліколевою) складовою. Наприклад, якщо полі(етиленгліколева) складовамає молекулярну масу приблизно 20 кДа, поліпептид bG-CSF або його варіант за цим варіантом здійснення може бути визначений як "bG-CSF-T133pAF-20K PEG", що вказує на те, що полі(етиленгліколева) складова, молекулярна маса якої становить 20 кДа, сполучена із заміною pAF, яка була виконана у положенні Т133. 5 UA 110799 C2 За одним із варіантів здійснення цього винаходу поліпептидом bG-CSF або його варіантом є bG-CSF-A136pAF, який має послідовність: 5 10 15 20 25 30 35 40 45 50 55 в якій одиночна заміна на пара-ацетилфенілаланін (pAF) виконана у положенні А136 і сполучена з полі(етиленгліколевою) складовою. Наприклад, якщо полі(етиленгліколева) складова має молекулярну масу приблизно 20 кДа, поліпептид bG-CSF або його варіант за цим варіантом здійснення може бути визначений як "bG-CSF-A136pAF-20K PEG", що вказує на те, що полі(етиленгліколева) складова, молекулярна маса якої становить 20 кДа, сполучена із заміною pAF, яка була виконана у положенні A136. У значенні, вжитому у цьому описі, терміни "стабільність" і "стабільний", вжитий вжиті разом із терміном "композиція, яка містить поліпептид bG-CSF або його варіант", означають термічне і хімічне розгортання, агрегування, деградування, денатурування, фрагментування або дестабілізування поліпептиду bG-CSF або його варіанта за певних умов виробництва, виготовлення, транспортування і зберігання. "Стабільні" композиції за цим винаходом зберігають структурну цілісність, результатом чого є збереження біологічної активності, бажано більше ніж 80%, 85%, 90%, 95%, 98%, 99% або 99,5% за певних умов виробництва, виготовлення, транспортування і зберігання. Стабільність композицій можна оцінювати за ступенем агрегування, депегілування, деградування, денатурування або фрагментування способами, відомими фахівцям в цій галузі і описаними нижче. У значенні, вжитому у цьому описі, термін "водний", вжитий разом із терміном "композиція, яка містить поліпептид bG-CSFy або його варіант", означає воду, один або декілька водорозчинних органічних розчинників або їх суміш. Термін "органічний розчинник" вживають в цьому описі у його традиційному значенні для позначення рідкої органічної сполуки, як правило, мономерної органічної речовини у вигляді рідини, за варіантом, якому віддається перевага, відносно нев'язкої рідини, молекулярна структура якої містить атоми водню, атоми вуглецю і факультативно також інші атоми, і яка здатна розчиняти тверді речовини, гази або рідини. Фармацевтичні композиції за цим винаходом можуть містити фармацевтично прийнятний носій. Фармацевтично прийнятні носії частково визначаються складом конкретної композиції, яка вводиться, а також конкретним способом, який застосовують для введення згаданої th композиції (дивись, наприклад, Remington's Pharmaceutical Sciences, 17 ed. 1985)). До відповідних фармацевтично прийнятних носіїв належать, але без обмеження ними, буферні речовини і допоміжні речовини, наприклад, такі, що містять фізіологічний розчин, забуферений фізіологічний розчин, декстрозу, воду, гліцерин, етанол та/або їх комбінації. Прийнятними носіями можуть бути буферні речовини, які містять сукцинат, фосфат, борат, ГЕПЕС, цитрат, гістидин, імідазол, ацетат, бікарбонат та інші органічні кислоти. Прийнятними носіями можуть бути допоміжні речовини, які містять багатоатомні цукрові спирти, амінокислоти, такі як аргінін, лізин, гліцин, глутамін, аспарагін, гістидин, аланін, орнітин, лейцин, фенілаланін, глутамінова кислота, треонін тощо, органічні цукри або цукрові спирти, такі як лактоза, трегалоза, стахіоза, маніт, сорбіт, ксиліт, рибіт, міоінозит, галактитол, гліцерин тощо, в тому числі циклітоли, такі як інозит; поліетиленгліколь; амінокислотні полімери; сірковмісні відновники, такі як сечовина, глутатіон, тіоктова кислота, тіогліколят натрію, тіогліцерин, -монотіогліцерин і тіосульфат натрію, низькомолекулярні поліпептиди (тобто
ДивитисяДодаткова інформація
Назва патенту англійськоюFormulations for bovine granulocyte colony stimulating factor and variants thereof
Автори англійськоюDavagnino, Juan, Kha, Catherine Ngan, Klotz, Alan Voskamh
Автори російськоюДаваньино Джуан, Кха Кэтрин Нгань, Клотц Алан Воскэмп
МПК / Мітки
МПК: A61K 38/19, A61P 29/00, C07K 14/535
Мітки: містить, стабільна, водна, колонієстимулювальний, композиція, фактор, гранулоцитарний, бичачий, яка
Код посилання
<a href="https://ua.patents.su/43-110799-stabilna-vodna-kompoziciya-yaka-mistit-bichachijj-granulocitarnijj-koloniehstimulyuvalnijj-faktor.html" target="_blank" rel="follow" title="База патентів України">Стабільна водна композиція, яка містить бичачий гранулоцитарний колонієстимулювальний фактор</a>
Попередній патент: Липка запобіжна етикетка або стрічка зі свідченням підробки
Наступний патент: Спосіб очищення терефталевої кислоти
Випадковий патент: Накладний ніготь