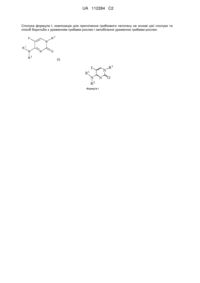
Похідні 5-фторпіримідинону
Номер патенту: 112284
Опубліковано: 25.08.2016
Автори: Бебель Тімоті, Джонсон Пітер, Брайан Крісті, Яо Ченьлінь, Оуен В., Лорсбах Бет, Салленбергер Майкл, Мейєр Кевін, Вебстер Джеффрі, Мартін Тімоті П.
Формула / Реферат
1. Сполука формули I
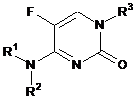 , (I)
, (I)
в якій
R1 являє собою H;
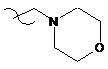 ;
;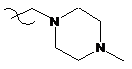 ;
; або
або 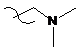 ;
;
R2 являє собою H;
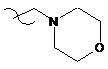 ;
;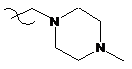 ;
; або
або 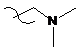 ;
;
альтернативно R1 і R2 можуть бути взяті разом з утворенням
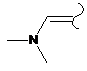 ;
;
R3 являє собою
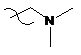 ;
;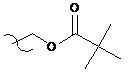 ;
; ;
;
![]() ;
;  ;
; ![]() ;
; ![]() ;
;
 ;
; 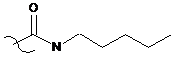 ;
; 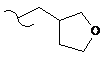 ;
;
![]() ;
; 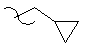 ;
;  ;
;
 ;
; 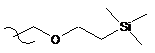 ;
; 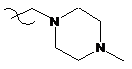 і
і 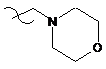 ,
,
за умови, що сполука не являє собою сполуку, в якій
обидва R1 і R2 являють собою H, і R3 являє собою ![]() ;
;
R1 являє собою H і R2 являє собою 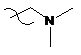 , і R3 являє собою
, і R3 являє собою 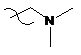 ;
;
R1 являє собою 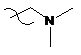 , R2 являє собою Н і R3 являє собою
, R2 являє собою Н і R3 являє собою 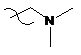 ;
;
R1 являє собою Н, R2 являє собою 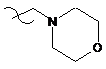 і R3 являє собою
і R3 являє собою 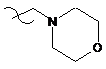 ;
;
R1 являє собою 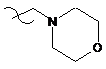 , R2 являє собою Н і R3 являє собою
, R2 являє собою Н і R3 являє собою 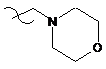 або
або
R1 і R2 являють собою H і 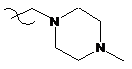 , і R3 являє собою
, і R3 являє собою 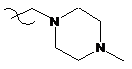 .
.
2. Сполука за п. 1, де R3 вибраний з групи, яка складається з:
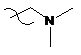 ,
, 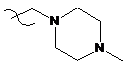 і
і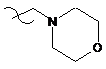 .
.
3. Сполука за п. 1, де R1 вибраний з групи, яка складається з:
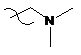 ,
, 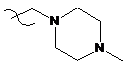 і
і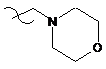 ;
;
і
R2 являє собою Н.
4. Сполука за п. 1, де R3 вибраний з групи, яка складається з:
 ,
, 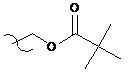 ,
,  ,
,  і
і  .
.
5. Композиція для пригнічення грибкового патогену, що містить сполуку за п. 1 і фітологічно прийнятну речовину-носій.
6. Композиція за п. 5, де грибковим патогеном є парша яблук (Venturia inaequalis), плямистість листя пшениці (Septoria tritici), плямистість листя цукрового буряка (Cercospora beticola), плямистість листя арахісу (Cercospora arachidicola і Cercosporidium personatum) і чорна Sigatoka бананів (Mycosphaerella fijiensis).
7. Спосіб боротьби з ураженням грибами рослин і запобігання ураженню грибами рослин, що включає стадії:
нанесення фунгіцидно ефективної кількості щонайменше однієї із сполук формули І щонайменше на одне з рослини, площі, сусідньої з рослиною, ґрунту, адаптованого для забезпечення росту рослини, коріння рослини, листя рослини і насіння, адаптованого для вирощування рослини:
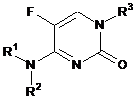 , (I)
, (I)
в якій
R1 являє собою Н;
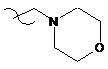 ;
;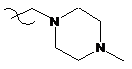 ;
; або
або 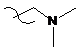 ;
;
R2 являє собою H;
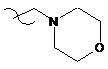 ;
;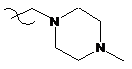 ;
; або
або 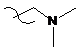 ;
;
альтернативно R1 і R2 можуть бути взяті разом з утворенням
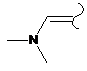 ;
;
R3 являє собою
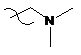 ;
;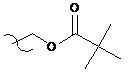 ;
; ;
;
![]() ;
;  ;
;![]() ;
;![]() ;
;
 ;
; ;
; ;
;
![]() ;
;  ;
; ;
;
 ;
;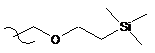 ;
;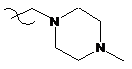 і
і 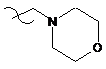 ,
,
за умови, що сполука не являє собою сполуку, в якій
обидва R1 і R2 являють собою H, і R3 являє собою ![]() ;
;
R1 являє собою H і R2 являє собою 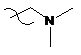 , і R3 являє собою
, і R3 являє собою 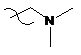 ;
;
R1 являє собою 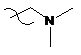 , R2 являє собою Н і R3 являє собою
, R2 являє собою Н і R3 являє собою 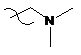 ;
;
R1 являє собою Н, R2 являє собою 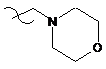 і R3 являє собою
і R3 являє собою 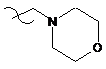 ;
;
R1 являє собою 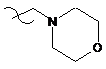 , R2 являє собою Н і R3 являє собою
, R2 являє собою Н і R3 являє собою 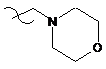 ;
;
R1 являє собою H, R2 являє собою 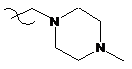 і R3 являє собою
і R3 являє собою 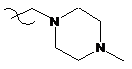 ;
;
R1 являє собою 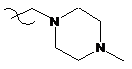 , R2 являє собою H і R3 являє собою
, R2 являє собою H і R3 являє собою 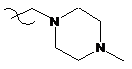 .
.
8. Спосіб за п. 7, де вказане нанесення включає нанесення сполуки формули І і фітологічно прийнятну речовину-носій.
9. Спосіб за п. 7, де грибковий патоген вибраний з групи, яка складається з парші яблук (Venturia inaequalis), плямистості листя пшениці (Septoria tritici), плямистості листя цукрового буряка (Cercospora beticola), плямистості листя арахісу (Cercospora arachidicola і Cercosporidium personatum) і чорної Sigatoka бананів (Mycosphaerella fijiensis).
10. Спосіб за п. 7, де R3 вибраний з групи, яка складається з:
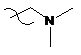 ,
, 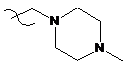 і
і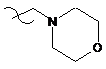 .
.
11. Сполука за п. 7, де R1 вибраний з групи, яка складається з:
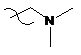 ,
, 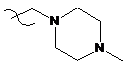 і
і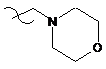 ; і
; і
R2 являє собою Н.
12. Сполука за п. 7, де R3 вибраний з групи, яка складається з:
 ,
, 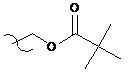 ,
,  ,
,  і
і  .
.
Текст
Реферат: (72) Винахідник(и): Бебель Тімоті (US), Брайан Крісті (US), Джонсон Пітер (US), Лорсбах Бет (US), Мейєр Кевін (US), Оуен В. (US), Салленбергер Майкл (US), Вебстер Джеффрі (US), Яо Ченлінь (US), Мартін Тімоті П. (US) (73) Власник(и): ДАУ АГРОСАЙЄНСІЗ ЕЛЕЛСІ, 9330 Zionsville Road, Indianapolis, IN 462681054, United States of America (US) (74) Представник: Мошинська Ніна Миколаївна, реєстр. №115 (56) Перелік документів, взятих до уваги експертизою: US 4 845 081, A, 04.07.1989 US 3 368 938, A, 13.02.1968 CHIACCHIO U. et al. Enantioselective Syntheses and Cytotoxicity of N,ОNucleosides// JOURNAL OF MEDICINAL CHEMISTRY, vol. 46, 2003, pp. 3696-3702 MORRIS J. ROBINS et al. A direct synthesis of 5-fluorocytosine and its nucleosides using trifluoromethyl hypofluorite// JOURNAL OF THE CHEMICAL SOCIETY, CHEMICAL COMMUNICATIONS, 1972, pp. 18-19 ARTHUR F. LEWIS et al. Synthesis and in vitro anti-human cytomegalovirus (hcmv) activity of certain alkenyl substituted cytosines and 5-halocytosines// JOURNAL OF HETEROCYCLIC CHEMISTRY, vol. 32, 1995, pp. 1513-1515 KULIKOWSKI T. et al. Methylation and tautomerism of 5-fluorocytosine nucleosides and their analogues// JOURNAL NUCLEIC ACIDS RESEARCH, SPECIAL PUBLICATION, vol. 4, 1978, pp. S7-S11 UA 112284 C2 (12) UA 112284 C2 Сполука формули І, композиція для пригнічення грибкового патогену на основі цієї сполуки та спосіб боротьби з ураженням грибами рослин і запобігання ураженню грибами рослин. F R N R 3 1 N N R 2 O (І) UA 112284 C2 5 10 15 20 25 30 35 40 45 50 Перехресне посилання на споріднені заявки Дана заявка заявляє пріоритет попередньої заявки на патент США з реєстраційним № 61/232177, зареєстрованої 7 серпня 2009 року. Рівень техніки і суть винаходу Фунгіциди є сполуками природного або синтетичного походження, які діють, захищаючи і/або усуваючи пошкодження рослин, викликані грибами. Звичайно один фунгіцид не є застосовним у всіх випадках. Тому продовжують дослідження з метою отримання фунгіцидів, які можуть мати кращу ефективність, простіші в застосуванні і мають нижчу ціну. Даний опис стосується похідних 5-фторпіримідинону і їх застосування як фунгіцидів. Сполуки даного опису можуть забезпечити захист від аскоміцетів, базидіоміцетів, дейтероміцетів і ооміцетів. Один варіант здійснення даного винаходу може включати сполуки формули I , 1 в якій R являє собою Н; 4 C1-C6алкіл, необов'язково заміщений 1-3 R ; 4 C1-C6алкеніл, необов'язково заміщений 1-3 R ; 4 C3-C6алкініл, необов'язково заміщений 1-3 R ; 5 феніл або бензил, де кожний з фенілу і бензилу може бути необов'язково заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим циклом, або конденсованою системою 5-6членних кілець, або конденсованою системою 6-6-членних кілець, причому кожна система 5 містить 1-3 гетероатоми, де кожне кільце може бути необов'язково заміщене 1-3 R , біфеніл або 5 нафтил, необов'язково заміщений 1-3 R ; 6 7 -(CHR )mOR ; 6 9 10 -(CHR )mN(R )R ; 8 -C(=O)R ; 8 -C(=S)R ; 8 -S(O)2R ; 8 -C(=O)OR ; 8 -C(=S)OR ; 6 9 10 -(CHR )mN(R )R ; 9 10 -C(=O)N(R )R або 9 10 -C(=S)N(R )R ; де m дорівнює цілому числу 1-4; 2 R являє собою Н або 4 C1-C6алкіл, необов'язково заміщений R ; 1 2 альтернативно R і R можуть бути взяті разом з утворенням 11 12 13 =CR N(R )R ; 3 R являє собою 4 C1-C6алкіл, необов'язково заміщений 1-3 R , C1-C6галогеналкіл, C1-C6гідроксіалкіл, C214 C6алкоксіалкіл, C2-C6галогеналкоксіалкіл, C2-C6алкеніл, необов'язково заміщений R , C2C6галогеналкеніл, C3-C6алкініл, феніл або бензил, де кожний з фенілу або бензилу може бути 5 необов'язково заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим циклом, або конденсованою системою 5-6-членних кілець, або конденсованою системою 6-6-членних кілець, причому кожна система містить 1-3 гетероатоми, де кожне кільце може бути необов'язково 5 5 заміщене 1-3 R , біфеніл або нафтил, необов'язково заміщений 1-3 R ; 6 7 -(CHR )mOR ; 6 8 -(CHR )mSR або 6 9 10 -(CНR )mN(R )R ; 4 R являє собою незалежно галоген, C1-C6алкіл, C1-C4галогеналкіл, C1-C4алкокси, C1C4галогеналкокси, C1-C4алкілтіо, C1-C4галогеналкілтіо, аміно, галогентіо, C1-C3алкіламіно, C2 1 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 C6алкоксикарбоніл, C2-C6алкілкарбоніл, C2-C6алкіламінокарбоніл, гідроксил, C3-C6триалкілсиліл, 5 феніл, необов'язково заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим 5 кільцем, що містить 1-3 гетероатоми, де кожне кільце може бути необов'язково заміщене 1-3 R ; 5 R являє собою незалежно галоген, C1-C6алкіл, C1-C6галогеналкіл, C1-C6алкокси, C1C6галогеналкокси, C1-C6алкілтіо, C1-C6галогеналкілтіо, галогентіо, аміно, C1-C6алкіламіно, C2C6діалкіламіно, C2-C6алкоксикарбоніл, C2-C6алкілкарбоніл, C1-C6алкілсульфоніл, нітро, гідроксил або ціано; 6 R являє собою Н, C1-C6алкіл, C1-C6алкокси, C1-C6алкоксикарбоніл, феніл або бензил, де 5 кожний з фенілу або бензилу може бути необов'язково заміщений 1-3 R ; 7 R являє собою Н, C1-C8алкіл, C2-C6алкеніл, C3-C6алкініл, C1-C6галогеналкіл, C1C6алкоксіалкіл, C2-C6триалкілсиліл, C2-C6триалкілсилілалкіл, C2-C6алкілкарбоніл, C1C6алкоксикарбоніл, феніл або бензил, де кожний з фенілу або бензилу може бути необов'язково 5 заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим циклом, або конденсованою системою 5-6-членних кілець, або конденсованою системою 6-6-членних кілець, причому кожна система містить 1-3 гетероатоми, де кожне кільце може бути необов'язково 5 5 заміщене 1-3 R , біфеніл або нафтил, необов'язково заміщений 1-3 R ; 8 R являє собою Н, C1-C6алкіл, C2-C6алкеніл, C3-C6алкініл, C1-C6галогеналкіл, C1C6алкоксіалкіл, феніл або бензил, де кожний з фенілу або бензилу може бути необов'язково 5 заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим циклом, або конденсованою системою 5-6-членних кілець, або конденсованою системою 6-6-членних кілець, причому кожна система містить 1-3 гетероатоми, де кожне кільце може бути необов'язково 5 5 заміщене 1-3 R , біфеніл або нафтил, необов'язково заміщений 1-3 R ; 9 R являє собою Н, C1-C6алкіл, C1-C6галогеналкіл, C1-C6алкоксіалкіл, C2-C6алкоксикарбоніл, 5 феніл або бензил, де кожний з фенілу або бензилу може бути необов'язково заміщений 1-3 R або системою 5- або 6-членних насичених або ненасичених кілець або конденсованою системою 5-6-членних кілець, або, конденсованою системою 6-6-членних кілець, причому кожна 5 система містить 1-3 гетероатоми, де кожне кільце може бути необов'язково заміщене 1-3 R , 5 біфеніл або нафтил, необов'язково заміщений 1-3 R ; 10 R являє собою Н, C1-C6алкіл, C1-C6галогеналкіл, C1-C6алкоксіалкіл, C2-C6алкілкарбоніл або 5 бензил, де бензил може бути необов'язково заміщений 1-3 R ; 9 10 альтернативно R і R можуть бути взяті разом з утворенням 5- або 6-членного насиченого або ненасиченого кільця, що містить 1-3 гетероатоми, де кожне кільце може бути необов'язково 5 заміщене 1-3 R ; 11 R являє собою Н або C1-C4алкіл; 12 R являє собою Н, ціано, гідроксил, C1-C4алкіл, C1-C6алкокси, C2-C6алкілкарбоніл, феніл або 5 бензил, де кожний з фенілу або бензилу може бути необов'язково заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим циклом, або конденсованою системою 5-6-членних кілець, або конденсованою системою 6-6-членних кілець, причому кожна система містить 1-3 5 гетероатоми, де кожне кільце може бути необов'язково заміщене 1-3 R ; біфеніл або нафтил, 5 необов'язково заміщений 1-3 R ; 11 12 альтернативно R і R можуть бути взяті разом з утворенням 5- або 6-членного насиченого або ненасиченого кільця, що містить 1-3 гетероатоми, де кожне кільце може бути необов'язково 5 заміщене 1-3 R ; 13 R являє собою Н, C1-C4алкіл, C1-C6алкокси, C2-C6алкілкарбоніл, феніл або бензил, де 5 кожний з фенілу або бензилу може бути необов'язково заміщений 1-3 R або 5- або 6-членним насиченим або ненасиченим циклом, або конденсованою системою 5-6-членних кілець, або конденсованою системою 6-6-членних кілець, причому кожна система містить 1-3 гетероатоми, 5 де кожне кільце може бути необов'язково заміщене 1-3 R , біфеніл або нафтил, необов'язково 5 заміщений 1-3 R ; і 12 13 альтернативно R і R можуть бути взяті разом з утворенням 5- або 6-членного насиченого або ненасиченого кільця, що містить 1-3 гетероатоми, де кожне кільце може бути необов'язково 5 заміщене 1-3 R . 14 R являє собою феніл або бензил, де кожний з фенілу або бензилу може бути 5 необов'язково заміщений 1-3 R . Інший варіант здійснення даного опису може включати фунгіцидну композицію для боротьби з ураженням грибами або для запобігання ураженню грибами, що містить описані нижче сполуки і фітологічно прийнятну речовину-носій. Ще інший варіант здійснення даного опису може включати спосіб боротьби з ураженням грибами або запобігання ураженню грибами рослин, причому спосіб включає стадії нанесення 2 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 фунгіцидно ефективної кількості однієї або декількох описаних нижче сполук щонайменше на один з грибів, рослину, площу, сусідню з рослиною, і насіння, застосовне для отримання рослини. Термін "алкіл" стосується нерозгалуженого, розгалуженого і циклічного вуглецевого ланцюга, що включає метил, етил, пропіл, бутил, ізопропіл, ізобутил, третинний бутил, пентил, гексил, циклопропіл, циклобутил, циклопентил, циклогексил і тому подібне. Термін "алкеніл" стосується нерозгалуженого, розгалуженого і циклічного вуглецевого ланцюга, що містить один або декілька подвійних зв'язків і включає етенил, пропеніл, бутеніл, ізопропеніл, ізобутеніл, циклогексеніл і тому подібне. Термін "алкініл" стосується нерозгалуженого або розгалуженого вуглецевого ланцюга, що містить один або декілька потрійних зв'язків і включає пропініл, бутиніл і тому подібне. Застосовне протягом всьому даного опису позначення "R' стосується групи, що складається з C2-C8алкілу, C3-C8алкенілу або C3-C8алкінілу, якщо не вказується інакше. Термін "алкокси" стосується замісника -OR. Термін "алкоксикарбоніл" стосується замісника -C(О)-OR. Термін "алкілкарбоніл" стосується замісника -C(О)-R. Термін "алкілсульфоніл" стосується замісника -SO2-R. Термін "галогеналкілсульфоніл" стосується замісника -SO2-R, у якого R повністю або частково заміщений Cl, F, I або Br або будь-якою їх комбінацією. Термін "алкілтіо" стосується замісника -S-R. Термін "галогеналкілтіо" стосується алкілтіо, який заміщений Cl, F, I або Br або будь-якою їх комбінацією. Термін "галогентіо" стосується сірки, заміщеної від трьох до п'яти замісниками F. Термін "алкіламінокарбоніл" стосується замісника -C(О)-N(Н)-R. Термін "диалкіламінокарбоніл" стосується замісника -C(О)-NR2. Термін "алкілциклоалкіламіно" стосується замісника циклоалкіламіно, який заміщений алкільною групою. Термін "триалкілсиліл" стосується -SiR3. Термін "ціано" стосується замісника -СN. Термін "гідроксил" стосується замісника -OH. Термін "аміно" стосується замісника -NH2. Термін "алкіламіно" стосується замісника -N(Н)-R. Термін "диалкіламіно" стосується замісника -NR2. Термін "триалкілсилілалкіл" стосується замісника -SiR3 в алкілі. Термін "алкоксіалкокси" стосується -O(CH2)nO(CH2)mCH3, де n дорівнює цілому числу 1-3 і m дорівнює 0-2. Термін "алкоксіалкіл" стосується алкоксизаміщення в алкілі. Термін "галогеналкоксіалкіл" стосується алкоксизаміщення алкілу, який повністю або частково заміщений Cl, F, Br або I або будь-якою їх комбінацією. Термін "гідроксіалкіл" стосується алкілу, який заміщений гідроксильною групою. Термін "галогеналкокси" стосується замісника -OR-X, у якого X являє собою Cl, F, Br або I або будь-яку їх комбінацію. Термін "галогеналкіл" стосується алкілу, який заміщений Cl, F, I або Br або будь-якою їх комбінацією. Термін "галогеналкеніл" стосується алкенілу, який заміщений Cl, F, I або Br або будь-якою їх комбінацією. Термін "галогеналкініл" стосується алкінілу, який заміщений Cl, F, I або Br або будь-якою їх комбінацією. Термін "галоген" або "гало" стосується одного або декількох атомів галогену, визначених як F, Cl, Br і I. Термін "гідроксикарбоніл" стосується замісника -C(О)-OH. Термін "нітро" стосується замісника -NO2. Протягом всього опису посилання на сполуки формули I означає також, що включаються оптичні ізомери і солі формули I і їх гідрати. Конкретно, коли сполуки формули I містять алкільну групу з розгалуженим ланцюгом, передбачається, що такі сполуки включають оптичні ізомери і їх рацемати. Приклади солей включають гідрохлорид, гідробромід, гідройодид і тому подібне. Крім того, сполуки формули I можуть включати таутомерні форми. Деякі сполуки, описані в даному документі, можуть існувати у вигляді одного або декількох ізомерів. Фахівцеві в даній галузі повинно бути зрозуміло, що один ізомер може бути активнішим, ніж інші. Структури, описані в даному описі, для ясності показані тільки у вигляді 3 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 однієї геометричної форми, але передбачається, що вони представляють всі геометричні і таутомерні форми молекули. Фахівцеві в даній галузі зрозуміло також, що, якщо не указано інакше, допустиме додаткове заміщення, якщо задовольняються правила хімічного зв'язування і енергії напруження. Іншим варіантом здійснення даного опису є застосування сполуки формули I для захисту рослини від ураження фітопатогенним організмом або обробки рослини, зараженої фітопатогенним організмом, що містить нанесення сполуки формули I або композиції, що містить таку сполуку, на ґрунт, рослину, частину рослини, листя і/або насіння. Крім того, іншим варіантом здійснення даного опису є композиція, застосовна для захисту рослини від ураження фітопатогенним організмом і/або обробки рослини, ураженої фітопатогенним організмом, що містить сполуку формули I і фітологічно прийнятну речовинуносій. Додаткові відмітні ознаки і переваги даного винаходу стануть очевидні фахівцеві в даній галузі при розгляді нижченаведеного докладного опису ілюстративних варіантів здійснення, що ілюструють кращий варіант здійснення винаходу, в тому вигляді, в якому він сприймається в даний час. Докладний опис винаходу Сполуки даного винаходу можна застосовувати будь-яким з різних відомих способів, або у вигляді сполук як таких, або у вигляді препаратів, що містять сполуки. Наприклад, сполуки можна наносити на коріння, насіння або листя рослин для боротьби з різними грибами, без нанесення збитку комерційній цінності рослин. Препарати можна наносити в формі будь-якого зі звичайно застосовуваних типів препаратів, наприклад, у вигляді розчинів, дустів, змочуваних порошків, текучих концентратів або емульгованих концентратів. Сполуки даного опису переважно наносять в формі препарату, що містить одну або декілька сполук формули I з фітологічно прийнятним носієм. Концентровані препарати можна диспергувати у воді або інших рідинах для нанесення на об'єкт обробки або препарати можуть бути подібними дусту або гранульованими, які потім можна наносити без додаткової обробки. Препарати можна отримувати згідно з процедурами, які є звичайними в сільськогосподарській хімічній галузі. Даний винахід розглядає всі наповнювачі, за допомогою яких з однієї або декількох сполук можна отримувати препарат для доставки і застосування його як фунгіциду. Звичайно препарати застосовують у вигляді водних суспензій або емульсій. Такі суспензії або емульсії можна отримувати з водорозчинних, диспергованих або емульгованих у воді препаратів, які є твердими речовинами, звичайно відомими як змочувані порошки; або рідинами, звичайно відомими як емульговані концентрати, водні суспензії або концентрати суспензій. Як може бути легко зрозуміло, можна застосовувати будь-яку речовину, до якої можна додати ці сполуки, за умови, що вона забезпечує необхідну придатність, без значного негативного впливу на активність цих сполук як протигрибкових агентів. Змочувані порошки, які можна пресувати з утворенням диспергованих у воді гранул, містять тісну суміш однієї або декількох сполук формули I, інертного носія і поверхнево-активних речовин. Концентрація сполуки в змочуваному порошку може бути від приблизно 10 масових процентів до приблизно 90 масових процентів з розрахунку на загальну масу змочуваного порошку, більш переважно від приблизно 25 масових процентів до приблизно 75 масових процентів. При отриманні препаратів у вигляді змочуваних порошків сполуки можна змішувати з тонкоподрібненою твердою речовиною, такою як профіліт, тальк, крейда, гіпс, фулерова земля, бентоніт, атапульгіт, крохмаль, казеїн, глютен, монтморилонітові глини, діатомові землі, очищені силікати або тому подібне. При таких операціях дрібноподрібнений носій і поверхневоактивні речовини звичайно змішують із сполукою(ами) і розмелюють. Емульговані концентрати сполук формули I можуть містити прийнятну концентрацію, таку як від приблизно 10 масових процентів до приблизно 50 масових процентів сполуки у прийнятній рідині, з розрахунку на загальну масу концентрату. Сполуки можна розчиняти в інертному носії, який є або змішуваним з водою розчинником, або сумішшю незмішуваних з водою органічних розчинників і емульгаторів. Концентрати можна розбавити водою і маслом для отримання сумішей для обприскування в формі емульсій типу масло-в-воді. Застосовні органічні розчинники включають ароматичні сполуки, особливо висококиплячі нафталінові і олефінові складові нафти, такі як важка ароматична нафта. Можна також застосовувати інші органічні розчинники, наприклад, терпенові розчинники, що включають похідні каніфолі, аліфатичні кетони, такі як циклогексанон, і "комплексні" спирти, такі як 2-етоксіетанол. Емульгатори, які можна переважно застосовувати у винаході, може легко визначити фахівець в даній галузі, вони включають різні неіоногенні, аніоногенні, катіоногенні і амфотерні 4 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 емульгатори або суміш двох або більше емульгаторів. Приклади неіоногенних емульгаторів, застосовних при отриманні емульгованих концентратів, включають поліалкіленгліколеві прості ефіри і продукти конденсації алкіл- і арилфенолів, аліфатичних спиртів, аліфатичних амінів або жирних кислот з етиленоксидом, пропіленоксидом, такі як етоксиловані алкілфеноли і ефіри карбонових кислот, солюбілізовані поліолом або поліоксіалкіленом. Катіоногенні емульгатори включають четвертинні амонієві сполуки і солі амінів жирного ряду. Аніоногенні емульгатори включають розчинні в маслі солі (наприклад, кальцію) алкіларилсульфонових кислот, розчинні в маслі солі або сульфатовані полігліколеві прості ефіри і прийнятні солі фосфатованого полігліколевого простого ефіру. Репрезентативними органічними рідинами, які можна застосовувати при отриманні емульгованих концентратів сполук даного винаходу, є ароматичні рідини, такі як ксилол, фракції пропілбензолу; або змішані нафталінові фракції, мінеральні масла, заміщені ароматичні органічні рідини, такі як діоктилфталат; гас; діалкіламіди різних жирних кислот, особливо диметиламіди жирних кислот і похідні гліколей, такі як н-бутиловий ефір, етиловий ефір або метиловий ефір діетиленгліколю і метиловий ефір триетиленгліколю і тому подібне. При отриманні емульгованого концентрату можна також застосовувати суміші двох або більше органічних рідин. Органічні рідини включають ксилол і фракції пропілбензолу, причому ксилол є найбільш переважним в деяких випадках. У рідких препаратах звичайно застосовують поверхнево-активні диспергуючі агенти в кількості від 0,1 до 20 масових процентів з розрахунку на об'єднану масу диспергуючого агента з однією або декількома сполуками. Препарати можуть містити також інші сумісні добавки, наприклад, регулятори росту рослин і інші біологічно активні сполуки, що застосовуються в сільському господарстві. Водні суспензії містять суспензії однієї або декількох нерозчинних у воді сполук формули I, диспергованих у водному наповнювачі при концентрації в діапазоні від приблизно 5 до приблизно 50 масових процентів з розрахунку на загальну масу водної суспензії. Суспензії отримують тонким подрібненням однієї або декількох сполук і енергійним перемішуванням подрібненої речовини в наповнювачі, що складається з води і поверхнево-активних речовин, вибраних з описаних вище деяких типів. Для підвищення густини і в'язкості водного наповнювача можна також додавати інші компоненти, такі як неорганічні солі і синтетичні або природні смоли. Часто найефективнішим є подрібнення і змішування одночасно з приготуванням водної суміші і гомогенізацією її в такому пристрої, як пісочний млин, кульовий млин або гомогенізатор плунжерного типу. Водні емульсії містять емульсії одного або декількох нерозчинних у воді пестицидно активних інгредієнтів, емульгованих у водному наповнювачі при концентрації звичайно в діапазоні від приблизно 5 до приблизно 50 масових процентів з розрахунку на загальну масу водної емульсії. Якщо пестицидно-активний інгредієнт є твердою речовиною, його треба розчинити у прийнятному, розчиннику, що не змішується з водою перед отриманням водної емульсії. Емульсії отримують емульгуванням рідкого пестицидно-активного інгредієнта або його розчину, що не змішується з водою, у водному середовищі, звичайно з включенням поверхневоактивних речовин, які допомагають утворенню і стабілізації емульсії, що описується вище. Це часто виконують за допомогою енергійного перемішування, що забезпечується змішувачами з високим зсувним зусиллям або гомогенізаторами. Сполуки формули I можна також застосовувати у вигляді гранульованих препаратів, які є особливо застосовними для нанесення на ґрунт. Гранульовані препарати звичайно містять від приблизно 0,5 до приблизно 10 масових процентів з розрахунку на загальну масу гранульованого препарату, сполуки(сполук), диспергованої(их) в інертному носії, який складається повністю з грубозернистого інертного матеріалу або містить як більшу частину такий інертний матеріал, як атапульгіт, бентоніт, діатоміт, глина або аналогічна недорога речовина. Такі препарати звичайно отримують розчиненням сполук у прийнятному розчиннику і нанесенням розчину на гранульований носій, який був попередньо отриманий у вигляді частинок прийнятного розміру в діапазоні від приблизно 0,5 до приблизно 3 мм. Прийнятним розчинником є розчинник, в якому сполука розчиняється в значній кількості або розчиняється повністю. Такі препарати можна також отримувати утворенням густої маси або пасти носія і сполуки і розчинника і подрібненням і сушінням її для отримання необхідних гранульованих частинок. Дусти, що містять сполуки формули I, можна отримати тісним змішуванням однієї або декількох сполук в порошкоподібній формі з дустом прийнятного сільськогосподарського носія, такого як, наприклад, каолінова глина, подрібнена вулканічна порода і тому подібне. Дусти можуть у прийнятному випадку містити від приблизно 1 до приблизно 10 масових процентів сполук з розрахунку на загальну масу дусту. 5 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 Препарати можуть додатково містити допоміжні засоби, поверхнево-активні речовини, для підвищення відкладання сполук на мішені, тобто сільськогосподарській культурі і організмі, змочування і проникнення цих сполук в таку мішень. Ці допоміжні засоби, поверхнево-активні речовини, можна необов'язково застосовувати як компонент препарату або суміші резервуара. Кількість допоміжного засобу, поверхнево-активні речовини, звичайно варіює від 0,01 до 1,0 об'ємного процента з розрахунку на об'єм води для розбризкування, переважно 0,05-0,5 об'ємного процента. Прийнятні допоміжні засоби, поверхнево-активні речовини, включають, але не обмежуються перерахованим, етоксиловані нонілфеноли, етоксиловані синтетичні або природні спирти, солі ефірів сульфобурштинових кислот, етоксиловані органосилікони, етоксиловані аміни жирного ряду і суміші поверхнево-активних речовин з мінеральними маслами або рослинними оліями. Препарати можуть включати також емульсії типу масло-вводі, такі як емульсії, описані в заявці на патент США, реєстраційному № 11/495228, опис якої спеціально включений в даний опис як посилання. Препарати можуть необов'язково включати комбінації, які містять інші пестицидні сполуки. Такими додатковими пестицидними сполуками можуть бути фунгіциди, інсектициди, гербіциди, нематоциди, мітициди, артроподициди, бактерициди або їх комбінації, які є сумісними із сполуками даного винаходу в середовищі, вибраному для застосування, і не є антагоністичними для активності даних сполук. Згідно з цим, в таких варіантах здійснення іншу пестицидну сполуку застосовують як додаткову отруйну речовину для такого ж або для іншого пестицидного застосування. Сполуки формули I і пестицидна сполука в комбінації звичайно присутні в масовому відношенні від 1:100 до 100:1. Сполуки даного винаходу можна також поєднувати з іншими фунгіцидами для отримання їх фунгіцидних сумішей і синергічних сумішей. Фунгіцидні сполуки даного опису часто застосовують в поєднанні з одним або декількома іншими фунгіцидами для боротьби з великою різноманітністю небажаних хвороб. При застосуванні в поєднанні з іншим фунгіцидом(ами) заявлені в даному описі сполуки можна вводити в препарат з іншим фунгіцидом(ами), змішати в резервуарі з іншим фунгіцидом(ами) або застосовувати послідовно з іншим фунгіцидом(ами). Такі інші фунгіциди можуть включати 2-(тіоціанатометилтіо)бензотіазол, 2-фенілфенол, сульфат 8-гідроксихіноліну, аметоктрадин, амісульбром, антиміцин, Ampelomyces quisqualis, азаконазол, азоксистробін, Bacillus subtilis, штам Bacillus subtilis QST713, беналаксил, беноміл, бентіавалікарб-ізопропіл, сіль бензиламінобензолсульфонату (BABS), бікарбонати, біфеніл, бісмертіазол, бітертанол, біксафен, бластицидин-S, боракс, суміш Bordeaux, боскалід, бромуконазол, бупіримат, полісульфід кальцію, каптафол, каптан, карбендазим, карбоксин, сарпропамід, карвон, хлазафенон, хлоронеб, хлороталоніл, хлозолінат, Coniothyrium minitans, гідроксид міді, октаноат міді, оксихлорид міді, сульфат міді, сульфат міді (триосновний), оксид міді(I), ціазофамід, цифлуфенамід, цимоксаніл, ципроконазол, ципродиніл, дазомет, дебакарб, етиленбіс(дитіокарбамат) діамонію, дихлофлуанід, дихлорофен, диклоцимет, дикломезин, дихлоран, діетофенкарб, дифеноконазол, дифензокват-іон, дифлуметорим, диметоморф, димоксистробін, диніконазол, диніконазол-M, динобутон, динокап, дифеніламін, дитіанон, додеморф, додеморфу ацетат, додин, вільна основа додину, едифенфос, енестробін, епоксіконазол, етабоксам, етоксихін, етридіазол, фамоксадон, фенамідон, фенаримол, фенбуконазол, фенфурам, фенгексамід, феноксанІл, фенпіклоніл, фенпропідин, фенпропіморф, фенпіразамін, фентин, фентину ацетат, фентину гідроксид, фербам, феримзон, флуазинам, флудіоксоніл, флуморф, флуопіколід, флуопірам, флуороімід, флуоксастробін, флухінконазол, флусилазол, флусульфамід, флутіаніл, флутоланіл, флутриафол, флуксапіроксад, фолпет, формальдегід, фосетил, фосетил-алюміній, фуберидазол, фуралаксил, фураметпір, гуазатин, гуазатину ацетати, GY-81, гексахлорбензол, гексаконазол, хімексазол, імазаліл, імазалілу сульфат, імібенконазол, іміноктадин, іміноктадину триацетат, іміноктадину тріс(альбезилат), йодокарб, іпконазол, іпфенпіразолон, іпробенфос, іпродіон, іпровалікарб, ізопротіолан, ізопіразам, ізотіаніл, казугаміцин, казугаміцину гідрохлориду гідрат, крезоксим-метил, ламінарин, манкопер, манкозеб, мандипропамід, манеб, мепанипірим, мепроніл, мептил-динокап, хлорид ртуті(II), оксид ртуті(II), хлорид ртуті(I), металаксил, мефеноксам, металаксил-M, метам, метам-амоній, метам-калій, метам-натрій, метконазол, метасульфокарб, метиліодид, метилізотіоціанат, метирам, метоміностробін, метрафенон, мілдіоміцин, міклобутаніл, набам, нітротал-ізопропіл, нуаримол, октилінон, офурас, олеїнову кислоту (жирні кислоти), орисастробін, оксадиксил, оксин-мідь, окспоконазолу фумарат, оксикарбоксин, пефуразоат, пенконазол, пенцикурон, пенфлуфен, пентахлорфенол, пентахлорфеніллаурат, пентіопірад, фенілртуті ацетат, фосфонову кислоту, фталід, пікоксистробін, поліоксин В, поліоксини, поліоксорим, калію бікарбонат, калію гідроксихінолінсульфат, пробеназол, прохлораз, процимідон, пропамокарб, пропамокарбу 6 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 гідрохлорид, пропіконазол, пропінеб, прохіназид, протіоконазол, піраклостробін, піраметостробін, піраоксистробін, піразофос, пірибенкарб, пірибутикарб, пірифенокс, піриметаніл, піріoфенон, пірохілон, хінокламін, хіноксифен, хінтозен, екстракт Reynoutria sachalinensis, седаксан, силтіофам, симеконазол, натрію 2-фенілфеноксид, натрію бікарбонат, натрію пентахлорфеноксид, спіроксамін, сірку, SYP-Z071, SYP-Z048, дьоготь, тебуконазол, тебуфлохін, текназен, тетраконазол, тіабендазол, тифлузамід, тіофанат-метил, тірам, тіадиніл, толклофос-метил, толілфлуанід, триадимефон, триадименол, триазоксид, трициклазол, тридеморф, трифлоксистробін, трифлумізол, трифорин, тритиконазол, валідаміцин, валіфеналат, валіфенал, вінклозолін, зинеб, зирам, зоксамід, Candida oleophila, Fusarium oxysporum, Gliocladium spp., Phlebiopsis gigantea, Streptomyces griseoviridis, Trichoderma spp., (RS)-N-(3,5-дихлорфеніл)-2-(метоксиметил)сукцинімід, 1,2-дихлорпропан, 1,3-дихлор-1,1,3,3тетрафторацетону гідрат, 1-хлор-2,4-динітронафталін, 1-хлор-2-нітропропан, 2-(2-гептадецил-2імідазолін-1-іл)етанол, 2,3-дигідро-5-феніл-1,4-дитіїну 1,1,4,4-тетраоксид, 2-метоксіетилртуті ацетат, 2-метоксіетилртуті хлорид, 2-метоксіетилртуті силікат, 3-(4-хлорфеніл)-5-метилроданін, 4-(2-нітропроп-1-еніл)фенілтіоціанатем, ампропілфос, анілазин, азитирам, барію полісульфід, Bayer 32394, беноданіл, бенхінокс, бенталурон, бензамакрил; бензамакрил-ізобутил, бензаморф, бінапакрил, сульфат біс(метилртуті), біс(трибутилолово)оксид, бутіобат, кадмію кальцію міді цинку хромат сульфат, карбаморф, CECA, хлорбентфіазон, хлораніформетан, хлорфеназол, хлорхінокс, клімбазол, циклафурамід, ципендазол, ципрофурам, декафентин, дихлон, дихлозолін, диклобутразол, диметиримол, диноктон, диносульфон, динотербон, дипіритіон, диталімфос, додецин, дразоксолон, EBP, ESBP, етаконазол, етем, етирим, фенаміносульф, фенапаніл, фенітропан, 5-фторцитозин і його профунгіциди, флуотримазол, фуркарбаніл, фурконазол, фурконазол-цис, фурмециклокс, фурофанат, гліодин, гризеофульвін, галакринат, Hercules 3944, гексилтіофос, ICIA0858, ізопамфос, ізоваледіон, мебеніл, мекарбінзид, метазоксолон, метфуроксам, метилртуті диціандіамід, метсульфовакс, мілнеб, мукохлорний ангідрид, міклозолін, N-3,5-дихлорфенілсукцинімід, N-3-нітрофенілітаконімід, натаміцин, N-етилмеркуріо-4-толуолсульфонанілід, нікелю біс(диметилдитіокарбамат), OCH, фенілртуті диметилдитіокарбамат, фенілртуті нітрат, фосдифен, піколінамід UK-2A і його похідні, протіокарб; протіокарбу гідрохлорид, піракарболид, піридинітрил, піроксихлор, піроксифур, хінацетол; хінацетолу сульфат, хіназамід, хінконазол, рабензазол, саліциланілід, SSF-109, сультропен, текорам, тіадифтор, тиціофен, тіохлорфенфім, тіофанат, тіохинокс, тіоксимид, триаміфос, триаримол, триазбутил, трихламід, урбацид, зариламід і будь-які їх комбінації. Крім того, сполуки даного винаходу можна комбінувати з іншими пестицидами, що включають інсектициди, нематоциди, мітициди, артроподициди, бактерициди або їх комбінації, які є сумісними із сполуками даного винаходу в середовищі, вибраному для застосування, і не є антагоністичними для активності даних сполук, з утворенням їх пестицидних сумішей і синергічних сумішей. Фунгіцидні сполуки даного опису можна застосовувати в поєднанні з одним або декількома іншими пестицидами для боротьби з ширшим рядом небажаних шкідників. При застосуванні в поєднанні з іншими пестицидами заявлені в даному описі сполуки можна вводити в препарат з іншим пестицидом(ами), змішати в резервуарі з іншим пестицидом(ами) або застосовувати послідовно з іншим пестицидом(ами). Типові інсектициди включають, але не обмежуються перерахованим: антибіотичні інсектициди, такі як алосамідин і турингієнзин; інсектициди типу макроциклічних лактонів, такі як спіносад і спінеторам; авермектинові інсектициди, такі як абамектин, дорамектин, емамектин, еприномектин, івермектин і селамектин; мілбеміцинові інсектициди, такі як лепімектин, мілбемектин, мілбеміцину оксим і моксидектин; арсенікалові інсектициди, такі як кальцію арсенат, міді ацетоарсеніт, міді арсенат, свинцю арсенат, калію арсеніт і натрію арсеніт; ботанікальні інсектициди, такі як анабазин, азадирахтин, d-лімонен, нікотин, піретрини, цинерини, цинерин I, цинерин II, жасмолін I, жасмолін II, піретрин I, піретрин II, квасіа, ротенон, гуаніа і сабадилу; карбаматні інсектициди, такі як бендіокарб і карбарил; бензофуранілметилкарбаматні інсектициди, такі як бенфуракарб, карбофуран, карбосульфан, декарбофуран і фуратіокарб; диметилкарбаматні інсектициди такі як димітан, диметилан, гіхінкарб і піримікарб; оксимкарбаматні інсектициди, такі як аланікарб, алдикарб, альдоксикарб, бутокарбоксим, бутоксикарбоксим, метоміл, нітрилакарб, оксаміл, тазимкарб, тіокарбоксим, тіодикарб і тіофанокс; фенілметилкарбаматні інсектициди, такі як аліксикарб, амінокарб, буфенкарб, бутакарб, карбанолат, клоетокарб, дикрезил, діоксакарб, EMPC, етіофенкарб, фенетакарб, фенобукарб, ізопрокарб, метіокарб, метолкарб, мексакарбат, промацил, промекарб, пропоксур, триметакарб, XMC і ксилілкарб; сикативні інсектициди, такі як борна кислота, діатомова земля і силікагель; діамідні інсектициди, такі як хлорантраніліпрол, ціантраніліпрол і флубендіамід; 7 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 динітрофенольні інсектициди, такі як динекс, динопроп, диносам і DNOC; фторні інсектициди, такі як барію гексафторсилікат, криоліт, натрію фторид, натрію гексафторсилікат і сульфлурамід; формамідинові інсектициди, такі як амітраз, хлордимеформ, форметанат і формпаранат; фумігантні інсектициди, такі як акрилонітрил, дисульфід вуглецю, тетрахлорид вуглецю, хлороформ, хлорпікрин, пара-дихлорбензол, 1,2-дихлорпропан, етилформіат, етилендибромід, етилендихлорид, етилену оксид, ціанід водень, йодметан, метилбромід, метилхлороформ, метиленхлорид, нафталін, фосфін, сульфурилфторид і тетрахлоретан; неорганічні інсектициди, такі як боракс, кальцію полісульфід, міді олеат, хлориду ртуті(I), калію тіоціанат і натрію тіоціанат; інгібітори синтезу хітину, такі як бістрифлурон, бупрофезин, хлорфлуазурон, циромазин, дифлубензурон, флуциклоксурон, флуфеноксурон, гексафлумурон, луфенурон, новалурон, новіфлумурон, пенфлурон, тефлубензурон і трифлумурон; імітатори ювенільних гормонів, такі як епофенонан, феноксикарб, гідропрен, кінопрен, метопрен, пірипроксифен і трипрен; ювенільні гормони, такі як ювенільний гормон I, ювенільний гормон II і ювенільний гормон III, агоністи гормону линяння, такі як хромафенозид, галофенозид, метоксифенозид і тебуфенозид; гормони линяння, такі як α-екдизон і екдистерон; інгібітори линяння, такі як діофенолан; прекоцени, такі як прекоцен I, прекоцен II і прекоцен III; некласифіковані регулятори росту комах, такі як дицикланіл; інсектициди, аналоги нереістоксину, такі як бенсультап, картап, тіоциклам і тіосультап; нікотиноїдні інсектициди, такі як флонікамід; нітрогуанідинові інсектициди, такі як клотіанідин, динотефуран, імідаклоприд і тіаметоксам; нітрометиленові інсектициди, такі як нітенпірам і нітіазин; піридилметиламінові інсектициди, такі як ацетаміприд, імідаклоприд, нітенпірам і тіаклоприд; хлорорганічні інсектициди, такі як бром-DDT, камфехлор, DDT, pp'-DDT, етил-DDD, HCH, гамма-НСН, ліндан, метоксихлор, пентахлорфенол і TDE; циклодієнові інсектициди, такі як альдрин, бромциклен, хлорбіциклен, хлордан, хлордекон, дильдрин, дилор, ендосульфан, альфа-ендосульфан, ендрин, НЕОD, гептахлор, HHDN, ізобензан, ізодрин, келеван і мірекс; органофосфатні інсектициди, такі як бромфенвінфос, хлорфенвінфос, кротоксифос, дихлорвос, дикротофос, диметилвінфос, фоспірат, гептенофос, метокротофос, мевінфос, монокротофос, налед, нафталофос, фосфамідон, пропафос, ТЕРР і тетрахлорвінфос; органотіофосфатні інсектициди, такі як діоксабензофос, фосметилан і фентоат; аліфатичні органотіофосфатні інсектициди, такі як ацетіон, амітон, кадузафос, хлоретоксифос, хлормефос, демефіон, демефіон-О, демефіон-S, деметон, деметон-О, деметон-S, деметон-метил, деметон-О-метил, деметон-S-метил, деметонS-метилсульфон, дисульфотон, етіон, етопрофос, IPSP, ізотіоат, малатіон, метакрифос, оксидеметон-метил, оксидепрофос, оксидисульфотон, форат, сульфотеп, тербуфос і тіометон; інсектициди типу аліфатичних амідів органічних тіофосфатів, такі як амідитіон, ціантоат, диметоат, етоат-метил, формотіон, мекарбам, ометоат, протоат, софамід і вамідотіон; оксиморганотіофосфатні інсектициди, такі як хлорфоксим, фоксим і фоксим-метил; гетероциклічні органотіофосфатні інсектициди, такі як азаметифос, кумафос, кумітоат, діоксатіон, ендотіон, меназон, морфотіон, фосалон, піраклофос, піридафентіон і хінотіон; бензотіопіранорганотіофосфатні інсектициди, такі як дитикрофос і тикрофос; бензотриазинорганотіофосфатні інсектициди, такі як азинфос-етил і азинфос-метил; ізоіндолорганотіофосфатні інсектициди, такі як діаліфос і фосмет; ізоксазолорганотіофосфатні інсектициди, такі як ізоксатіон і золапрофос; піразолопіримідинорганотіофосфатні інсектициди, такі як хлорпразофос і піразофос; піридинорганотіофосфатні інсектициди, такі як хлорпірифос і хлорпірифос-метил; піримідинорганотіофосфатні інсектициди, такі як бутатіофос, діазинон, етримфос, ліримфос, піриміфос-етил, піриміфос-метил, примідофос, піримітат і тебупіримфос; хіноксалінорганотіофосфатні інсектициди, такі як хіналфос і хіналфос-метил; тіадіазолорганотіофосфатні інсектициди, такі як атидатіон, ліфтидатіон, метидатіон і протидатіон; триазолорганотіофосфатні інсектициди, такі як ізазофос і триазофос; фенілорганотіофосфатні інсектициди, такі як азотоат, бромофос, бромофос-етил, карбофенотіон, хлортіофос, ціанофос, цитіоат, дикартон, дихлофентіон, етафос, фамфур, фенхлорфос, фенітротіон, фенсульфотіон, фентіон, фентіон-етил, гетерофос, жодфенфос, мезулфенфос, паратіон, паратіон-метил, фенкаптон, фосніхлор, профенофос, протіофос, сульпрофос, темефос, трихлорметафос-3 і трифенофос; фосфонатні інсектициди, такі як бутонат і трихлорфон; фосфонотіоатні інсектициди, такі як мекарфон; фенілетилфосфонотіоатні інсектициди, такі як фонофос і трихлоронат; фенілфенілфосфонотіоатні інсектициди, такі як ціанофенфос, EPN і лептофос; фосфорамідатні інсектициди, такі як круфомат, фенаміфос, фостіетан, мефосфолан, фосфолан і піриметафос; фосфорамідотіоатні інсектициди, такі як ацефат, ізокарбофос, ізофенфос, ізофенфос-метил, метамідофос і пропетамфос; фосфородіамідні інсектициди, такі як димефокс, мазидокс, міпафокс і шрадан; оксадіазинові інсектициди, такі як індоксакарб; оксадіазолінові інсектициди, 8 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 такі як метоксадіазон; фталімідні інсектициди, такі як діаліфос, фосмет і тетраметрин; піразолові інсектициди, такі як тебуфенпірад, толефенпірад; фенілпіразолові інсектициди, такі як ацетопрол, етипрол, фіпроніл, пірафлупрол, пірипрол і ваніліпрол; піретроїні складноефірні інсектициди, такі як акринатрин, алетрин, біоалетрин, бартрин, біфентрин, біоетанометрин, циклетрин, циклопротрин, суфлутрин, бета-суфлутрин, цигалотрин, гамма-цигалотрин, лямбдацигалотрин, циперметрин, альфа-циперметрин, бета-циперметрин, тета-циперметрин, зетациперметрин, цифенотрин, дельтаметрин, димефлутрин, диметрин, емпентрин, фенфлутрин, фенпіритрин, фенпропатрин, фенвалерат, есфенвалерат, флуцитринат, флувалінат, тауфлувалінат, фуретрин, іміпротрин, меперфлутрин, метофлутрин, перметрин, біоперметрин, трансперметрин, фенотрин, пралетрин, профлутрин, піресметрин, ресметрин, біоресметрин, цисметрин, тефлутрин, тералетрин, тетраметрин, тетраметилфлутрин, тралометрин і трансфлутрин; піретроїдні прості ефірні інсектициди, такі як етофенпрокс, флуфенпрокс, галфенпрокс, протрифенбут і силафлуофен; піримідинамінові інсектициди, такі як флуфенерим і піримідифен; піролові інсектициди, такі як хлорфенапір; інсектициди типу тетрамових кислот, такі як спіротетрамат; інсектициди типу тетронових кислот, такі як спіромезифен; тіосечовинні інсектициди, такі як діафентіурон; сечовинні інсектициди, такі як флукофурон і сулкофурон; і некласифіковані інсектициди, такі як клозантел, нафтенат міді, кротамітон, EDX, феназафлор, феноксакрим, гідраметилнон, ізопротіолан, малонобен, метафлумізон, ніфлуридид, пліфенат, піридабен, піридаліл, пірифлухіназон, рафоксанід, сульфоксафлор, триаратен і триазамат і їх комбінації. Крім того, сполуки даного винаходу можна комбінувати з гербіцидами, які є сумісними із сполуками даного винаходу в середовищі, вибраному для застосування, і не є антагоністичними для активності даних сполук, з утворенням їх пестицидних сумішей і синергічних сумішей. Фунгіцидні сполуки даного опису можна застосовувати в поєднанні з одним або декількома пестицидами для боротьби з широким рядом небажаних рослин. При застосуванні в поєднанні з гербіцидами заявлені в даному описі сполуки можна вводити в препарат з гербіцидом(ами), змішати в резервуарі з гербіцидом(ами) або застосовувати послідовно з гербіцидом(ами). Типові гербіциди включають, але не обмежуються перерахованим, амідні гербіциди, такі як алідохлор, бефлубутамід, бензадокс, бензипрам, бромобутид, кафенстрол, CDEA, ципразол, диметенамід, диметенамід-Р, дифенамід, епроназ, етніпромід, фентразамід, флупоксам, фомезафен, галозафен, ізокарбамід, ізоксабен, напропамід, напталам, петоксамід, пропізамід, хінонамід і тебутам; анілідні гербіциди, такі як хлоранокрил, цисанілід, кломепроп, ципромід, дифлуфенікан, етобензанід, фенасулам, флуфенацет, флуфенікан, мефенацет, мефлуїдид, метаміфоп, моналід, напроанілід, пентанохлор, піколінафен і пропаніл; арилаланінові гербіциди, такі як бензоїлпроп, флампроп і флампроп-М; хлорацетанілідні гербіциди, такі як ацетохлор, алахлор, бутахлор, бутенахлор, делахлор, діетатил, диметахлор, метазахлор, метолахлор, S-метолахлор, претилахлор, пропахлор, пропізохлор, принахлор, тербухлор, тенілхлор і ксилахлор; сульфонаніліні гербіциди, такі як бензофлор, перфлуїдон, піримісульфан і профлуазол; сульфонамідні гербіциди, такі як азулам, карбасулам, фенасулам і оризалін; тіоамідні гербіциди, такі як хлортіамід; антибіотичні гербіциди, такі як біланафос; гербіциди типу бензойних кислот, такі як хлорамбен, дикамба, 2,3,6-ТВА і трикамба; гербіциди типу піримідинілоксибензойної кислоти, такі як біспірибак і піримінобак; гербіциди типу піримідинілтіобензойної кислоти, такі як піритіобак; гербіциди типу фталевої кислоти, такі як хлортал; гербіциди типу піколінової кислоти, такі як амінопіралід, клопіралід і піклорам; гербіциди типу хінолінкарбонової кислоти, такі як хінклорак і хінмерас; миш'якові гербіциди, такі як какодилова кислота, СМА, DSMA, гексафлурат, МАА, МАМА, MSMA, арсеніт калію і арсеніт натрію; бензоїлциклогександіонові гербіциди, такі як мезотрион, сулкотрион, тефурилтрион і темботрион; бензофуранілалкілсульфонатні гербіциди, такі як бенфурезат і етофумезат; бензотіазолові гербіциди, такі як бензазолін; карбаматні гербіциди, такі як азулам, карбоксазол, хлорпрокарб, дихлормат, фенасулам, карбутилат і тербукарб; карбанілатні гербіциди, такі як барбан, ВСРС, карбасулам, карбетамід, СЕРС, хлорбуфам, хлорпрофам, СРРС, дезмедифам, фенізофам, фенмедифам, фенмедифам-етил, профам і свеп; гербіциди типу оксиму циклогексену, такі як алоксидим, бутроксидим, клетодим, клопроксидим, циклоксидим, профоксидим, сетоксидим, тепралоксидим і тралкоксидим; циклопропілізоксазолові гербіциди, такі як ізоксахлортол і ізоксафлутол; дикарбоксимідні гербіциди, такі як цинідон-етил, флумезин, флуміклорак, флуміоксазин і флуміпропін; динітроанілінові гербіциди, такі як бенфлуралін, бутралін, динітрамін, еталфлуралін, флухлоралін, ізопропалін, металпропалін, нітралін, оризалін, пендиметалін, продіамін, профлуралін і трифлуралін; динітрофенолові гербіциди, такі як динофенат, динопроп, диносам, диносеб, динотерб, DNOC, етинофен і мединотерб; гербіциди типу дифенілових простих ефірів, такі як етоксифен; гербіциди типу нітрофенілових 9 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 60 простих ефірів, такі як ацифлуорфен, аклоніфен, біфенокс, хлорметоксифен, хлорнітрофен, етніпромід, фтордифен, фторглікофен, фторнітрофен, фомезафен, фурилоксифен, галосафен, лактофен, нітрофен, нітрофлуорфен і оксифлуорфен; дитіокарбаматні гербіциди, такі як дазомет і метам; галогеновані аліфатичні гербіциди, такі як алорак, хлоропон, далапон, флупропанат, гексахлорацетон, йодметан, метилбромід, монохлороцтова кислота, SMA і ТСА; імідазолінонові гербіциди, такі як імазаметабенз, імазамокс, імазапік, імазапір, імазахін і імазетапір; неорганічні гербіциди, такі як сульфамат амонію, боракс, хлорат кальцію, сульфат міді, сульфат заліза(II), азид калію, ціанат калію, азид натрію, хлорат натрію і сірчана кислота; нітрильні гербіциди, такі як бромбоніл, бромоксиніл, хлороксиніл, дихлобеніл, йодобоніл, іоксиніл і піраклоніл; фосфорорганічні гербіциди, такі як аміпрофос-метил, анілофос, бенсулід, біланафос, бутаміфос, 2,4-DEP, DMPA, EBEP, фосамін, глуфосинат, глуфосинат-Р, гліфосат і піперофос; феноксигербіциди, такі як бромфеноксим, кломепроп, 2,4-DEB, 2,4-DEP, дифенопентен, дисул, ербон, етнипромід, фентеракол і трифопсим; оксадіазолінові гербіциди, такі як метазол, оксадіаргіл, оксадіазон; оксазолові гербіциди, такі як феноксасульфон; гербіциди типу феноксіоцтових кислот, такі як 4-СРА, 2,4-D, 3,4-DA, МСРА, МСРА-тіоетил і 2,4,5-Т; гербіциди типу феноксимасляних кислот, такі як 4-СРВ, 2,4-DB, 3,4-DB, МСРВ і 2,4,5-ТВ; гербіциди типу феноксипропіонових кислот, такі як клопроп, 4-СРР, дихлорпроп, дихлорпроп-Р, 3,4-DP, фенопроп, мекопроп і мекопроп-Р; гербіциди типу арилоксифеноксипропіонових кислот, такі як хлоразифоп, клодинафоп, клофоп, цигалофоп, диклофоп, феноксапроп, феноксапроп-Р, фентіапроп, флуазифоп, флуазифоп-Р, галоксифоп, галоксифоп-Р, ізоксапірифоп, метаміфоп, пропахізафоп, хізалофоп, хізалофоп-Р і трифоп; фенілендіамінові гербіциди, такі як динітрамін і продіамін; піразолові гербіциди, такі як піроксасульфон; бензоїлпіразолові гербіциди, такі як бензофенап, пірасульфотол, піразолінат, піразоксифен і топрамезон; фенілпіразолові гербіциди, такі як флуазолат, нипіраклофен, піоксаден і пірафлуфен; піридазинові гербіциди, такі як кредазин, піридафол і піридат; піридазинонові гербіциди, такі як бромпіразон, хлоридазон, димідазон, флуфенпір, метфлуразон, норфлуразон, оксапіразон і піданон; піридинові гербіциди, такі як амінопіралід, кліодинат, клопіралід, дитіопір, флуроксипір, галоксидин, піклорам, піколінафен, піриклор, тіазопір і триклопір; піримідиндіамінові гербіциди, такі як іпримідам і тіоклорим; четвертинні амонієві гербіциди, такі як циперкват, діетамкват, дифензокват, дикват, морфамкват і паракват; тіокарбаматні гербіциди, такі як бутилат, циклоат, діалат, ЕРТС, еспрокарб, етіолат, ізополінат, метіобенкарб, молінат, орбенкарб, пебулат, просульфокарб, пірибутикарб, сульфалат, тіобенкарб, тіокарбазил, триалат і вернолат; тіокарбонатні гербіциди, такі як димексано, EXD і проксан; тіосечовинні гербіциди, такі як метиурон; триазинові гербіциди, такі як дипропетрин, індазифлам, триазифлам і тригідрокситриазин; хлортриазинові гербіциди, такі як атразин, хлоразин, ціаназин, ципразин, егліназин, іпазин, мезопразин, проціазин, прогліназин, пропазин, себутилазин, симазин, тербутилазин і триетазин; метокситриазинові гербіциди, такі як атратон, метометон, прометон, секбуметон, симетон і тербуметон; метилтіотриазинові гербіциди, такі як аметрин, азипротрин, ціанатрин, дезметрин, диметаметрин, метопротрин, прометрин, симетрин і тербутрин; триазинонові гербіциди, такі як аметридіон, амібузин, гексазинон, ізометіозин, метамітрон і метрибузин; триазолові гербіциди, такі як амітрол, кафенстрол, епроназ і флупоксам; триазолонові гербіциди, такі як амікарбазон, бенкарбазон, карфентразон, флукарбазон, іпфенкарбазон, пропоксикарбазон, сульфентразон і тієнкарбазон-метил; триазолопіримідинові гербіциди, такі як клорансулам, диклосулам, флоразулам, флуметсулам, метосулам, пеноксулам і піроксулам; урацильні гербіциди, такі як бензфендизон, бромацил, бутафенацил, флупропацил, ізоцил, ленацил, сафлуфенацил і тербацил; сечовинні гербіциди, такі як бензтіазурон, кумілурон, циклурон, дихлоралсечовина, дифлуфензопір, ізонорурон, ізоурон, метабензтіазурон, монізоурон і норурон; фенілсечовинні гербіциди, такі як анізурон, бутурон, хлорбромурон, хлоретурон, хлоротолурон, хлороксурон, даймурон, дифеноксурон, димефурон, діурон, фенурон, флуометурон, флуотіурон, ізопротурон, лінурон, метіурон, метилдимрон, метобензурон, метобромурон, метоксурон, монолінурон, монурон, небурон, парафлурон, фенобензурон, сидурон, тетрафлурон і тидіазурон; піримідинілсульфонілсечовинні гербіциди, такі як амідосульфурон, азимсульфурон, бенсульфурон, хлоримурон, циклосульфамурон, етоксисульфурон, флазасульфурон, флуцетосульфурон, флупірсульфурон, форамсульфурон, галосульфурон, імазосульфурон, мезосульфурон, метазосульфурон, нікосульфурон, ортосульфамурон, оксасульфурон, примісульфурон, пропірисульфурон, піразосульфурон, римсульфурон, сульфометурон, сульфосульфурон і трифлоксисульфурон; триазинілсульфонілсечовинні гербіциди, такі як хлорсульфурон, циносульфурон, етаметсульфурон, йодосульфурон, метсульфурон, просульфурон, тифенсульфурон, триазулфурон, трибенурон, трифлусульфурон і тритосульфурон; тіадіазолілсечовинні 10 UA 112284 C2 5 10 15 20 25 30 35 40 45 50 55 гербіциди, такі як бутиурон, етидимурон, тебутіурон, тіазафлурон і тидіазурон; і некласифіковані гербіциди, такі як акролеїн, аліловий спирт, аміноциклопірахлор, азафенідин, бентазон, бензобіциклон, біциклопірон, бутидазол, кальцію ціанамід, камбендихлор, хлорфенак, хлорфенпроп, хлорфлуразол, хлорфлуренол, цинметилін, кломазон, СРMF, крезол, ціанамід, орто-дихлорбензол, димепіперат, ендотал, фтормідин, флуридон, фторхлоридон, флуртамон, флутіацет, інданофан, метилізотіоціанат, ОСН, оксазикломефон, пентахлорфенол, пентоксазон, ацетат фенілртуті, просульфалін, пірибензоксим, пірифталід, хінокламін, родетаніл, сульглікапін, тидіазимін, тридифан, триметурон, трипропіндан і тритак. Іншим варіантом здійснення даного винаходу є спосіб боротьби з ураженням грибами або запобігання ураженню грибами. Даний спосіб включає нанесення на ґрунту, рослини, коріння, листя, насіння, або вогнище поширення грибів, або місце, в якому треба запобігти зараженню (наприклад, нанесенням на злакові рослини), фунгіцидно ефективної кількості однієї або декількох сполук формули I. Сполуки є прийнятними для обробки різних рослин при фунгіцидних рівнях, виявляючи при цьому низьку фітотоксичність. Сполуки можуть бути застосовні як захисний і/або знищуючий гриби засіб. Виявлено, що сполуки мають значну фунгіцидну дію, особливо при сільськогосподарському застосуванні. Багато сполук є особливо ефективними для застосування для сільськогосподарських культур і садових рослин. Додаткові переваги можуть включати, але не обмежуються перерахованим, поліпшення здоров'я рослин; підвищення урожаю рослин (наприклад, отримання підвищеної біомаси і/або підвищеного вмісту цінних інгредієнтів); підвищення життєстійкості рослини (наприклад, досягнення підвищеного росту рослин і/або зеленішого листя); поліпшення якості рослини (наприклад, досягнення підвищеного вмісту або складу деяких інгредієнтів) і підвищення толерантності до абіотичного і/або біотичного стресу рослини. Фахівцеві в даній галузі повинно бути зрозуміло, що ефективність сполуки відносно дії на вищезгадані гриби визначає загальну застосовність сполук як фунгіцидів. Сполуки мають широкі діапазони активності проти грибкових патогенів. Зразкові патогенності можуть включати, але не обмежуються перерахованим, плямистість листя пшениці (Septoria tritici, відому також як Mycosphaerella graminicola), паршу яблук (Venturia inaequalis) і церкоспорозну плямистість листя цукрового буряка (Cercospora beticola), плямистість листя арахісу (Cercospora arachidicola і Cercosporidium personatum) і інших сільськогосподарських культур і чорної sigatoka бананів (Mycosphaerella fujiensis). Точна кількість активної речовини, що наноситься, залежить не тільки від конкретної застосовуваної речовини, але також від конкретної необхідної дії, грибкового виду, який треба придушити, і стадії його росту, а також частини рослини або іншого продукту, який контактують із сполукою. Таким чином, всі сполуки і препарати, що їх містять, не можуть бути рівно ефективними при однакових концентраціях або проти одного і того ж грибкового виду. Сполуки є ефективними при застосуванні для рослин в пригнічуючій хворобу і фітологічно прийнятній кількості. Термін "пригнічуюча хворобу і фітологічно прийнятна кількість" стосується кількості сполуки, яка усуває або пригнічує хворобу рослини, для якої пригнічення є бажаним, але яке не є значно токсичним для рослини. Ця кількість звичайно складає від приблизно 0,1 до приблизно 1000 м. ч. (мільйонні частки), причому переважною є 1-500 м. ч. Точна кількість необхідної сполуки варіює залежно від грибкової хвороби, яку пригнічують, типу застосовуваного препарату, способу застосування, конкретного виду рослини, кліматичних умов і тому подібного. Прийнятна норма введення звичайно знаходиться в діапазоні від приблизно 2 0,10 до приблизно 4 фунтів/акр (приблизно 0,01-0,45 грамів на квадратний метр, г/м ). Будь-який діапазон необхідної величини, вказаної в контексті, можна розширити або змінити без втрати результату дії, яку намагаються отримати, що очевидно фахівцеві в даній галузі внаслідок розуміння приведеного в контексті опису. Сполуки формули I можна отримати із застосуванням добре відомих хімічних процедур. Проміжні продукти, не вказані конкретно в даному описі, або є комерційно доступними, їх можна отримати шляхами, описаними в хімічній літературі, або їх можна легко синтезувати з комерційних вихідних речовин із застосуванням стандартних процедур. Нижченаведені приклади представлені для ілюстрації різних аспектів сполук даного винаходу і не повинні розглядатися як обмеження формули винаходу. Приклад 1: отримання 5-фтор-1-морфолін-4-ілметил-4-[(морфолін-4-ілметил)аміно]-1Hпіримідин-2-ону (1) 11 UA 112284 C2 5 10 15 20 25 30 35 40 Дану сполуку отримують, як описано в Int. J. Pharm. 1987, 35, 243-252. До суміші параформальдегіду (240 міліграмів (мг), 8 мілімолів (ммоль) мономера) в дихлорметані (СН 2Cl2; 20 мл) в пробірці на 25 мілілітрів (мл) з загвинчуваною кришкою додавали морфолін (697 мг, 8 ммоль). Реакційну суміш перемішували на орбітальному вібраторі протягом ночі при кімнатній температурі. Додавали 4-аміно-5-фторпіримідин-2-ол* (250 мг, 2 ммоль) і гетерогенну суміш, що утворилася, перемішували при кімнатній температурі протягом 48 годин (год.). Реакційну суміш упарювали досуха і залишок обробляли простим ефіром (Et 2O), отримуючи при цьому білу тверду речовину, яку відділяли фільтруванням і сушили, отримуючи при цьому вказану в 1 заголовку сполуку (381 мг, 65 %): т. пл. 156-158С; H ЯМР (300 MГц, CDCl3) δ 7,46 (д, J=2,5 Гц, 1Н), 5,69 (ушир. т, 1Н), 4,53 (с, 2H), 4,46 (д, J=2,6 Гц, 2H), 3,72 (м, 8H), 2,64 (м, 8H); ІЧ (ATR) -1 3483 (шир.), 3293 (шир.), 1680 (різк.), 1639 (різк.), 1574 (різк.), 1521 (різк.) см . *4-Аміно-5-фторпіримідин-2-ол можна купити в торговому джерелі. Приклад 2: отримання 5-фтор-1-(4-метилпіперазин-1-ілметил)-4-[(4-метилпіперазин-1ілметил)аміно]-1H-піримідин-2-ону (2) Цю сполуку отримували, як описано в Int. J. Pharm. 1987, 35, 243-252. До суміші параформальдегіду (240 мг, 8 ммоль мономера) в CH 2Сl2 (20 мл) в пробірці на 25 мл із загвинчуваною кришкою додавали N-метилпіперазин (813 мг, 8 ммоль). Реакційну суміш перемішували на орбітальному вібраторі протягом ночі при кімнатній температурі. Додавали 4аміно-5-фторпіримідин-2-ол (250 мг, 2 ммоль) і гетерогенну суміш, що утворилася, перемішували при кімнатній температурі протягом 48 годину. Реакційну суміш упарювали досуха і залишок обробляли Et2O, отримуючи при цьому бежеву тверду речовину, яку відділяли фільтруванням і сушили, отримуючи при цьому вказану в заголовку сполуку (247 мг, 31 %): т. 1 пл. 165-166 °C; H ЯМР (300 MГц, CDCl3) δ 7,45 (д, J=2,5 Гц, 1Н), 5,62 (ушир. т, 1Н), 4,55 (с, 2H), 4,5 (д, J=2,6 Гц, 2H), 2,69 (м, 8H), 2,44 (ушир., 8H), 2,38 (с, 6Н); ІЧ (ATR) 3465 (шир.), 1679 (різк.), -1 1646 (різк.), 1574 (різк.), 1522 (різк.) см . Сполуку 3 в таблиці I синтезували, як в прикладі 2. Приклад 3: отримання N'-[5-фтор-1-(4-фторбензил)-2-оксо-1,2-дигідропіримідин-4-іл]-N, Nдиметилформамідину (4) У ампулу на 8 мл із загвинчуваною кришкою додавали N, N-диметилформамід (ДМФ; 1,5 мл), N'-(5-фтор-2-гідроксипіримідин-4-іл)- N, N-диметилформамідин (100 мг, 0,54 ммоль), безводний карбонат калію (K2СО3; 138 мг, 1,0 ммоль) і 4-фторбензилбромід (113 мг, 0,60 ммоль). Суміш струшували і нагрівали до 70 °C протягом 2 годин і потім при кімнатній температурі протягом додаткових 16 годин. Сиру реакційну суміш фільтрували і вміщували безпосередньо в хроматографічну колонку із оберненою фазою. Після елюювання вказану в 1 заголовку сполуку виділяли у вигляді білої твердої речовини (30 мг, 20 %): т. пл. 134-136 °C; H ЯМР (300 MГц, CDCl3) δ 8,68 (с, 1Н), 8,07 (д, J=2,5 Гц, 1Н), 7,49-7,43 (м, 2H), 7,10-7,01 (м, 2H), + 5,33 (с, 2H), 3,20 (с, 3H), 3,18 (с, 3Н); ESIMS m/z 293 ([M+H] ). Сполуки 5-7 в таблиці I синтезували, як в прикладі 3. Приклад 4: отримання N-(5-фтор-1-метил-2-оксо-1,2-дигідропіримідин-4-іл)-4метилбензаміду (8) 12 UA 112284 C2 5 10 15 20 25 30 35 40 До N-(5-фтор-2-гідроксипіримідин-4-іл)-4-метилбензаміду (200 мг, 0,81 ммоль) в ДМФА (5 мл) додавали K2CO3 (224 мг, 1,6 ммоль) і йодметан (230 мг, 1,6 ммоль). Суміш перемішували і нагрівали до 60 °C протягом 30 хв і потім перемішували протягом 16 годину при кімнатній температурі. Суміш розподіляли між етилацетатом (EtOAc) і водою (H 2O). Органічну фазу сушили над сульфатом магнію (MgSO4), фільтрували і упарювали. Сиру речовину очищали хроматографією на оберненою фазою, отримуючи при цьому вказану в заголовку сполуку у 1 вигляді білої твердої речовини (17 мг, 8 %): т. пл. 229-230 °C; H ЯМР (300 MГц, CDCl3) δ 13,2 (ушир. с, 1Н), 8,23-8,15 (ушир. м, 2Н), 7,42-7,37 (ушир. м, 1H), 7,30-7,25 (ушир. м, 2H), 3,45 (с, + 3H), 2,44 (с, 3H); ESIMS m/z 262 ([M+H] ), m/z 260 ([M-H] ). Приклад 5: отримання N-(5-фтор-1-метил-2-оксо-1,2-дигідропіримідин-4-іл)- N-метил-Cфенілметансульфонаміду (9) 4-Аміно-5-фторпіримідин-2-ол (2 грами (г), 15,5 ммоль) перемішували в ацетонітрилі (CH3CN; 80 мл) при 50 °C. До нагрітої суміші додавали N, О-біс(триметилсиліл)ацетамід (BSA; 9,4 г, 46,3 ммоль) і перемішування і нагрівання продовжували протягом 1,5 години. Додавали фенілметансульфонілхлорид (3,2 г, 16,8 ммоль). Через 2 години реакційну суміш охолоджували до кімнатної температури і розподіляли між CH3CN і насиченим розчином солі. Органічну фазу сушили над MgSO4, фільтрували, упарювали і вміщували безпосередньо в колонку з силікагелем, яку елюювали (градієнт 0-100 % EtOAc в петролейному ефірі). Об'єднання фракцій, що містять основну, УФ-абсорбуючу частину суміші продукту, давало білу тверду речовину, яку застосовували без додаткового очищення. До частини цієї речовини (100 мг) додавали ДМФА (3 мл), K2CO3 (100 мг) і йодметан (100 мг) і суміш перемішували при 60 °C протягом 1 години. Реакційну суміш охолоджували до кімнатної температури і додавали надлишок гідриду натрію (NaH; 60 % дисперсія в мінеральному маслі). Всю суміш перемішували протягом 30 хв і потім нагрівали до 45 °C протягом 2,5 години. Сиру суміш фільтрували і очищали хроматографією із оберненою фазою з подальшим очищенням хроматографією на нормальній фазі (градієнт, 30-100 % EtOAc в петролейному ефірі), отримуючи при цьому 1 вказану в заголовку сполуку у вигляді білої твердої речовини (28 мг, 27 %): т. пл. 159-160С; H ЯМР (300 MГц, CDCl3) δ 7,6 (м, 1Н), 7,42-7,41 (м, 2Н), 7,38-7,36 (м, 3H), 4,8 (с, 2H), 3,5 (с, 3Н), + 2,82 (с, 3Н); ESIMS m/z 312 ([M+H] ), m/z 310 ([M-H] ). Приклад 6: отримання ізобутилового ефіру (5-фтор-1-метил-2-оксо-1,2-дигідропіримідин-4іла)карбамінової кислоти (10) і ізобутилового ефіру (5-фтор-1-метил-2-оксо-1,2дигідропіримідин-4-іл)метилкарбамінової кислоти (11) 4-Аміно-5-фторпіримідин-2-ол (0,5 г, 3,9 ммоль) і ізобутилхлорформіат (0,58 г, 4,2 ммоль) в піридині (5 мл) струшували при 60С протягом 1,5 години. Сиру суміш розподіляли між EtOAc і 1 н хлористоводневою кислотою (HCl). Органічну фазу сушили над MgSO 4, фільтрували і упарювали. З залишку в етиловому спирті (EtOH) осаджували білу тверду речовину, яку застосовували без додаткового очищення. Частину даної речовини (100 мг), K 2CO3 (125 мг) і 13 UA 112284 C2 5 10 15 20 25 30 35 40 45 йодметан (125 мг) додавали до ДМФА (3 мл) і суміш перемішували при 60С протягом 1 години. Суміш охолоджували до кімнатної температури і додавали надлишок NaH (60 % дисперсія в мінеральному маслі). Всю суміш перемішували протягом 30 хв і потім нагрівали при 45С протягом 2 годин. Сиру суміш фільтрували і очищали хроматографією із оберненою фазою, отримуючи при цьомувказані в заголовку сполуки. Ізобутиловий ефір (5-фтор-1-метил-2-оксо-1,2-дигідропіримідин-4-іла)карбамінової кислоти 1 виділяли у вигляді білої твердої речовини (16 мг): т. пл. 126-128С; H ЯМР (300 MГц, CDCl3) δ 12,2 (ушир. с, 1Н), 7,32 (ушир. с, 1Н), 3,98 (д, J=6,6 Гц, 2H), 3,4 (с, 3H), 2,02 (септ., J=6,6 Гц, 1H), + 1,01 (д, J=6,6 Гц, 6H); ESIMS m/z 244 ([M+H] ), m/z 242 ([M-H] ). Ізобутиловий ефір (5-фтор-1-метил-2-оксо-1,2-дигідропіримідин-4-іла)метилкарбамінової 1 кислоти виділяли у вигляді прозорого безбарвного масла (22 мг): H ЯМР (300 MГц, CDCl3) δ 7,52 (д, J=5,5 Гц, 1Н), 4,02 (д, J=6,8 Гц, 2Н), 3,55 (с, 3H), 3,40 (с, 3H), 1,99 (септ., J=6,8 Гц, 1H), 13 0,95 (д, J=6,8 Гц, 6H); C ЯМР (150 MГц, CDCl3) δ 158,24, 158,17, 154,7, 154,1, 140,5, 138,8, + 134,0, 133,7, 73,6, 38,6, 34,9, 27,9, 19,2; ESIMS m/z 258 ([M+H] ). Приклад 7: отримання 4-(диметиламінометиленаміно)-5-фтор-2-оксо-2H-піримідин-1ілметилового ефіру 2,2-диметилпропіонової кислоти (12) До ДМФА (3 мл) додавали N'-(5-фтор-2-гідрокспіримідин-4-ілу)-N, N-диметилформамідин (100 мг, 0,54 ммоль), карбонат цезію (196 мг, 0,6 ммоль) і хлорметилпівалат (90 мг, 0,6 ммоль) і суміш струшували при кімнатній температурі протягом 16 годин. Суміш розподіляли між EtOAc і H2О. Органічну фазу сушили над MgSO4, фільтрували і упарювали. До сирого масла, що утворилося, додавали Et2О (3,5 мл) і утворений осад збирали фільтруванням. Вказану в 1 заголовку сполуку виділяли у вигляді білої твердої речовини (37 мг, 23 %): т. пл. 193-194 °C; H ЯМР (300 MГц, ДМСО-d6) δ 8,67 (с, 1Н), 8,07 (д, J=6,3 Гц, 1Н), 5,60 (с, 2H), 3,22 (с, 3H), 3,09 (с, + 3H), 1,11 (с, 9H); ESIMS m/z 299 ([M+H] ). Сполуки 13 в таблиці I синтезували, як в прикладі 7. Приклад 8: отримання 4-аміно-1-(бензилоксиметил)-5-фторпіримідин-2(1H)-ону (14) і 1(бензилоксиметил)-4-(бензилоксиметиламіно)-5-фторпіримідин-2(1H)-ону (15) У 25-мл колбу типу колби Шленка завантажували 4-аміно-5-фторпіримідин-2-ол (500 мг, 3,87 ммоль), CH3CN (10 мл) і BSA (1,42 мл, 5,81 ммоль). Білу суспензію, що утворилася, потім нагрівали при 65 °C. Через 90 хв прозорий безбарвний розчин охолоджували до кімнатної температури і додавали бензилхлорметиловий простий ефір (1,07 мл, 7,72 ммоль), отримуючи при цьому непрозору білу суспензію. Після перемішування протягом 2 годин при кімнатній температурі реакційну суміш концентрували у вакуумі, отримуючи при цьому білий залишок, який очищали колонковою хроматографією із оберненою фазою, отримуючи при цьому 4-аміно1-(бензилоксиметил)-5-фторпіримідин-2(1H)-он (14; 433 мг, 45 %) у вигляді білої твердої 1 речовини: т. пл. 213-217ºС; H ЯМР (400 MГц, CDCl3) δ 7,98 (д, J=6,5 Гц, 1Н), 7,81 (ушир. с, 1Н), 7,56 (ушир. с, 1H), 7,24-7,36 (м, 5H), 5,11 (с, 2H), 4,54 (с, 2Н); ІЧ 3302 (інтенс.), 3082 (інтенс.), 2939 (слабка), 2869 (слабка), 1688 (інтенс.), 1619 (інтенс.), 1522 (інтенс.), 1468 (середня), 1333 -1 + (середня), 1131 (слабка), 1054 (середня) см ; ESIMS m/z 250 ([M+H] ). 1-(Бензилоксиметил)-4-(бензилоксиметиламіно)-5-фторпіримідин-2(1H)-он (15; 16,5 мг, 1 1,2 %) отримували як побічний продукт у вигляді безбарвного масла в синтезі сполуки 14: H ЯМР (400 MГц, CDCl3) δ 8,85 (т, J=5,8 Гц, 1Н), 8,08 (д, J=6,6 Гц, 1Н), 7,22-7,39 (м, 10H), 5,15 (с, 2H), 4,87 (д, J=5,8 Гц, 2Н), 4,56 (с, 2Н), 4,54 (с, 2Н); ІЧ 3248 (слабка), 3062 (слабка), 3031 (слабка), 1683 (інтенс.), 1644 (середня), 1569 (середня), 1520 (інтенс.), 1454 (слабка), 1357 -1 + (слабка), 1328 (середня), 1189 (слабка), 1069 (середня) см ; ESIMS m/z 370 ([M+H] ). Сполуки 16-23 в таблиці I синтезували, як в прикладі 8. 14 UA 112284 C2 Приклад 9: отримання N'-(5-фтор-1-метилсульфанілметил-2-оксо-1,2-дигідропіримідин-4-іл)N, N-диметилформамідину (24) 5 10 15 20 25 30 35 40 45 У 250-мл круглодонну колбу завантажували N'-(5-фтор-2-гідроксипіримідин-4-іл)-N, Nдиметилформамідин (1,00 г, 5,43 ммоль) і ДМФА (55 мл) з отриманням білої суспензії. Додавали твердий трет-бутоксид калію (1,07 г, 9,53 ммоль) і блідо-жовтої суспензії, що утворилася, давали можливість перемішуватися в атмосфері азоту при кімнатній температурі протягом 20 хв. Потім додавали хлорметилметилсульфід (682 мікролітрів (мкл), 8,14 ммоль) і суміш нагрівали при 60ºС протягом 21 години. Сиру реакційну суміш концентрували у вакуумі при 55ºС, отримуючи при цьому не зовсім білий залишок, який очищали колонковою хроматографією із оберненою фазою, отримуючи при цьому N'-(5-фтор-1метилсульфанілметил-2-оксо-1,2-дигідропіримідин-4-іл)-N, N-диметилформамідин (36 мг, 25 %) 1 у вигляді блідо-жовтої твердої речовини: т. пл. 132-136ºС; H ЯМР (400 MГц, CDCl3) δ 8,68 (с, 1Н), 8,20 (д, J=3,2 Гц, 1Н), 5,40 (с, 2H), 3,19 (с, 3H), 3,07 (с, 3H), 2,20 (с, 3Н); ІЧ 2960 (слабка), 2926 (слабка), 1640 (інтенс.), 1582 (інтенс.), 1447 (інтенс.), 1382 (середня), 1319 (середня), 1269 + (середня), 1108 (середня), 1051 (середня) см-1; ESIMS m/z 267 ([M+H] ). Приклад 10: отримання 4-аміно-5-фтор-1-(4-метилбензил)піримідин-2(1H)-ону (25) Стадія 1: до перемішуваного магнітною мішалкою розчину 4-аміно-5-фторпіримідин-2-олу (4,00 г, 31,0 ммоль) в ДМФА (100 мл) додавали диметилацеталь N, N-диметилформаміду (ДМФА-DMA; 4,00 г, 34,0 ммоль). Суміш перемішували при кімнатній температурі протягом 72 годин, розбавляли Et2О (200 мл) і фільтрували. Твердий продукт промивали гептаном, отримуючи при цьому (Е)-N'-(5-фтор-2-оксо-1,2-дигідропіримідин-4-іл)-N, N1 диметилформімідамід (5,23 г, 92 %) у вигляді білої твердої речовини: т. пл. 240-243ºС; H ЯМР (300 MГц, ДМСО-d6) δ 10,7 (ушир. с, 1Н), 8,59 (с, 1Н), 7,7 (д, J=5,6 Гц, 1H), 3,18 (с, 3H), 3,06 (с, + 3Н); ESIMS m/z 185 ([M+H] ), m/z 183 ([M-H] ). Стадія 2: порошкоподібний K2CO3 (325 меш; 2,03 г, 14,7 ммоль) додавали до суміші продукту зі стадії 1 (1,35 г, 7,35 ммоль) і α-бром-п-ксилолу (1,36 г, 7,35 ммоль) в ДМФА (20 мл) в атмосфері N2 при кімнатній температурі. Білу суспензію, що утворилася, нагрівали до 80ºС. Після перемішування при 80ºС протягом 2 годин реакційну суміш охолоджували, розбавляли ЕtOAc (150 мл) і розчин промивали Н2О (4×50 мл) і насиченим (насич.) NaCl (1×50 мл). Органічну фазу сушили (Na2SO4), фільтрували і концентрували у вакуумі, отримуючи при цьому 1,01 г блідо-жовтої твердої речовини. Сиру речовину розчиняли в суміші EtOAc/СН2Cl2 і обробляли целітом (3 г). Розчинник видаляли у вакуумі і залишок очищали хроматографією з нормальною фазою (градієнт 0-100 % EtOAc/гексани) для видалення ізомерного О-алкілованого продукту. Колонку потім елюювали розчином 90 % СН2Cl2/10 % СН3ОН, отримуючи при цьому необхідний N-алкілований продукт, N'-[5-фтор-1-(4-метилбензил)-2-оксо-1,2-дигідропіримідин-4іл]-N, N-диметилформамідин (0,668 г, 32 %) у вигляді білої твердої речовини: т. пл. 178-1795ºС; 1 H ЯМР (300 MГц, CDCl3) δ 8,82 (с, 1Н), 7,22-7,15 (м, 4Н), 4,97 (с, 2H), 3,18 (с, 3Н), 3,17 (с, 3Н), + 2,34 (с, 3Н); ESIMS m/z 289 ([M+H] ). Стадія 3: Хлорид цинку (1,24 г, 9,12 ммоль) додавали до суміші формамідинового продукту зі стадії 2 (0,656 г, 2,28 ммоль) і абсолютного EtOH (10 мл). Суміш, що утворилася, нагрівали для кип'ятіння із зворотним холодильником в атмосфері N 2. Суміш поступово перетворювалася в яскраво-жовтий гомогенний розчин. Після кип'ятіння із зворотним холодильником протягом 90 хв утворювався осад, і після 2 годин реакційній суміші давали можливість охолодитися до 15 UA 112284 C2 5 10 15 20 25 30 35 40 кімнатної температури і концентрували у вакуумі. Залишок обробляли СН 2Cl2 (75 мл, поява слабкої каламутності) і промивали Н2О (25 мл). Як тільки додавали Н2О, утворювався білий осад в обох шарах в ділильній лійці. Тверду речовину відділяли вакуумним фільтруванням. Тверду речовину промивали Н2О з подальшим промиванням Et2О. Після сушіння на повітрі протягом ночі білу тверду речовину (0,58 г) обробляли сумішшю 1:1 СН 2Cl2/MeОH (70 мл) і нагрівали для кип'ятіння із зворотним холодильником (каламутна суміш). Суміш фільтрували і фільтрат концентрували у вакуумі. Залишкову тверду речовину суспендували в суміші гексани/Et2О (3:1) і виділяли вакуумним фільтруванням, сушили на повітрі і потім сушили у вакуумній сушильній шафі (70-80ºС), отримуючи при цьому N'-(5-фтор-2-гідроксипіримідин-4ілу)-N, N-диметилформамідин (0,417 г, 78 %) у вигляді білого порошку: т. пл. 291-293ºС (розкл.); 1 H ЯМР (300 MГц, ДМСО-d6) δ 8,03 (д, J=6,9 Гц, 1Н), 7,62 (ушир. с, 1Н), 7,40 (ушир. с, 1H), 7,17 13 (д, J=7,8 Гц, 2H), 7,12 (д, J=8,1 Гц, 2H), 4,73 (с, 2H), 2,25 (с, 3Н); C ЯМР (150 MГц, ДМСО-d6) δ 158,2, 154,8, 137,3, 136,3 (д, J=240 Гц), 135,3, 131,1 (д, J=30,6 Гц), 129,7, 128,3, 51,8, 21,3; + ESIMS m/z 234 ([M+H] ), m/z 232 [M-H] ); ІЧ 3298 (середня, шир.), 3100 (середня, шир.), 1685 (інтенс.), 1619 (інтенс.), 1518 (інтенс.), 1447 (середня), 1383 (середня), 1343 (слабка), 1120 -1 (слабка), 776 (слабка) см . Приклад 11: отримання 4-аміно-5-фтор-1-(4-йодбутил)-1H-піримідин-2-ону (26) До суспензії 4-аміно-5-фторпіримідин-2-олу (0,50 г, 3,87 ммоль) в ацетонітрилі (CH3CN; 20 мл) додавали BSA (1,58 г, 7,75 ммоль) і суміш нагрівали до 70ºС протягом 1 години, отримуючи при цьому прозорий розчин. Після охолоджування до кімнатної температури додавали 1,4-дийодбутан (1,2 г, 3,87 ммоль) і суміш перемішували протягом 16 годин при кімнатній температурі і потім при 70ºС протягом 3 годин. Розчинник випаровували і залишок очищали хроматографією на нормальній фазі (24 г SiO 2; градієнт 0-15 % MeOH/СН2Cl2), отримуючи при цьому оранжеве масло. Масло розчиняли в EtOAc і розчин повільно охолоджували. Тверду речовину, що утворилася, збирали фільтруванням, промивали додатковим EtOAc і сушили, отримуючи при цьому 4-аміно-5-фтор-1-(4-йодбутил)-1H-піримідин1 2-он (0,52 г, 43 %) у вигляді рудувато-коричневої твердої речовини: т. пл. 181-184ºС; Н ЯМР (400 MГц, ДМСО-d6) δ 8,56 (с, 2H), 8,25 (д, J=6,7 Гц, 1H), 3,70 (т, J=6,7 Гц, 2H), 3,29 (т, J=6,7 Гц, + 2H), 1,73 (м, 4H); ESIMS m/z 312 ([M+H] ). Приклад 12: отримання 4-аміно-5-фтор-1-(4-[1,2,4]триазол-1-ілбутил)-1H- піримідин-2-ону (27) До суміші 1,2,4-триазолу (0,044 г, 0,64 ммоль), трет-бутоксиду калію (KOtBu; 0,072 г, 0,64 ммоль) і 18-крауну-6 (18C6; 0,008 г, 0,03 ммоль) в CH3CN (3,5 мл) додавали 4-аміно-5-фтор-1(4-йодбутил)-1H- піримідин-2-он (0,10 г, 0,32 ммоль) і суміш нагрівали до 70ºС і перемішували протягом 16 годин. Гомогенний розчин, що утворився, концентрували у вакуумі, отримуючи при цьому сирий продукт у вигляді білої твердої речовини. Очищення хроматографією із оберненою фазою (13 г C18; градієнт 0-20 % CН3CN/вода) давала 4-аміно-5-фтор-1-(4-[1,2,4]триазол-11 ілбутил)-1H-піримідин-2-он (0,023 г, 28 %) у вигляді білої твердої речовини: т. пл. 197-200ºС; H ЯМР (400 MГц, ДМСО-d6) δ 8,50 (с, 1Н), 7,94 (м, 2H), 7,56 (с, 1Н), 7,35 (с, 1H), 4,19 (т, J=6,9 Гц, + 2H), 3,61 (т, J=7,0 Гц, 2H), 1,73 (м, 2H), 1,51 (м, 2Н); ESIMS m/z 253 ([M+H] ), m/z 251 ([M-H] ). Приклад 13: отримання 4-аміно-5-фтор-1-метилпіримідин-2(1H)-ону (28) 16 UA 112284 C2 5 10 15 20 25 30 35 40 У 25-мл пробірку із загвинчуваною кришкою завантажували 4-аміно-5-фторпіримідин-2-ол (151,0 мг, 1,17 ммоль), K2CO3 (289,2 мг, 2,09 ммоль), 18C6 (278,6 мг, 0,901 ммоль) і безводний ДМФА (10 мл). Додавали метилметансульфонат (0,0814 мл, 0,961 ммоль) і суміш, що утворилася, перемішували на роторному вібраторі при 85ºС протягом 21 години. Після охолоджування до кімнатної температури сиру речовину концентрували у вакуумі і очищали колонковою хроматографією із оберненою фазою, отримуючи при цьому 4-аміно-5-фтор-1метилпіримідин-2(1H)-он (61,9 мг, 37 %) у вигляді бежевої твердої речовини: т. пл. 195ºС 1 (розкл.); Н ЯМР (400 MГц, ДМСО-d6) δ 7,94 (д, J=6,8 Гц, 1Н), 7,52 (с, 1Н), 7,32 (с, 1Н), 3,18 (с, + 3Н); ESIMS m/z 144 ([M+H] ). Сполуки 29-33 отримували, як в прикладі 13. Приклад 14: отримання (Е)-N'-(1-етил-5-фтор-2-оксо-1,2-дигідропіримідин-4-іл)-N, Nдиметилформімідаміду (34) У 25-мл пробірку із загвинчуваною кришкою завантажували (Е)-N'-(5-фтор-2гідроксипіримідин-4-іл)-N, N-диметилформімідамід (99,5 мг, 0,540 ммоль), ДМФА (2 мл) і NaH (60 % дисперсія в мінеральному маслі; 24,5 мг, 0,613 ммоль) і перемішували на роторному вібраторі при 505ºС протягом 40 хв. Після охолоджування до кімнатної температури додавали дисульфід вуглецю (0,036 мл, 0,599 ммоль) і реакційну суміш перемішували на роторному вібраторі при кімнатній температурі протягом 90 хв. У цій точці додавали йодетан (0,052 мл, 0,650 ммоль) і реакційну суміш додатково перемішували при кімнатній температурі протягом 3,5 годин, після чого сиру суміш концентрували у вакуумі. Сиру речовину очищали хроматографією з нормальною фазою (градієнт 0-30 % MeOH/СН2Cl2), отримуючи при цьому (Е)-N'-(1-етил-5фтор-2-оксо-1,2-дигідропіримідин-4-іл)-N, N-диметилформімідамід (105 мг, 67 %) у вигляді білої 1 твердої речовини: т. пл. 157-160ºС; H ЯМР (400 MГц, ДМСО-d6) δ 8,62 (с, 1Н), 8,09 (д, J=6,2 Гц, 1Н), 3,70 (кв, J=7,1 Гц, 2H), 3,20 (с, 3H), 3,07 (с, 3H), 1,18 (т, J=7,1 Гц, 3H); ESIMS m/z 213 + ([M+H] ). Сполуки 35 і 36 отримували, як в прикладі 14. Приклад 15: отримання 1-(етоксиметил)-5-фтор-4-(2-фторбензиламіно)піримідин-2(1H)-ону (37) У 25-мл пробірку із загвинчуваною кришкою завантажували 5-фтор-4-(2фторбензиламіно)піримідин-2-ол (49,7 мг, 0,210 ммоль), CH3CN (1 мл) і BSA (0,054 мл, 0,0221 ммоль) і суміш перемішували на роторному вібраторі при 65ºС протягом 30 хв. Після охолоджування до кімнатної температури додавали (хлорметоксі)етан (0,022 мл, 0,237 ммоль) і суміш, що утворилася, перемішували на роторному вібраторі при кімнатній температурі протягом 16 годин. Сиру реакційну суміш концентрували у вакуумі і очищали хроматографією з нормальною фазою (градієнт 0-25 % MeOH/СН2Cl2), отримуючи при цьому 1-(етоксиметил)-51 фтор-4-(2-фторбензиламіно)піримідин-2(1H)-он (55,0 мг, 89 %) у вигляді жовтого масла: H ЯМР (400 MГц, ДМСО-d6) δ 8,60 (т, J=5,8 Гц, 1Н), 8,05-7,95 (м, 1Н), 7,40-7,26 (м, 2H), 7,26-7,10 (м, 2H), 5,01 (с, 2H), 4,59 (д, J=5,9 Гц, 2H), 3,49 (кв, J=7,0 Гц, 2Н), 1,09 (дд, J=9,0, 5,0 Гц, 3Н); ESIMS m/z + 296 ([M+H] ), m/z 294 ([M-H] ). Приклад 16: отримання 5-фтор-4-((2-фторбензилметил)аміно)-1-(4- метилбензил)піримідин2(1H)-ону (38) 17 UA 112284 C2 5 10 15 20 25 30 35 40 У 25-мл пробірку із загвинчуваною кришкою завантажували NaH (60 % дисперсія в мінеральному маслі; 20,5 мг, 0,513 ммоль) і ДМФА (2,5 мл). Додавали 5-фтор-N-(2-фторбензил)2-(4-метилбензилокси)піримідин-4-амін (149 мг, 0,436 ммоль) і суміші давали можливість для перемішування при кімнатній температурі. Через 10 хв додавали йодметан (0,033 мл, 0,530 ммоль) і суміші, що утворилася, давали можливість перемішуватися при кімнатній температурі протягом додаткових 28 годин. Після цього часу сиру реакційну суміш концентрували у вакуумі і очищали хроматографією з нормальною фазою (градієнт 0-40 % EtOAc/гексани), отримуючи при цьому 5-фтор-4-((2-фторбензилметил)аміно)-1-(4-метилбензил)піримідин-2(1H)-он (119,7 мг, 1 77 %) у вигляді безбарвного масла: H ЯМР (400 MГц, ДМСО-d6) δ 8,16 (д, J=9,5 Гц, 1Н), 7,4513 7,06 (м, 8Н), 4,83 (с, 2H), 4,79 (с, 2H), 3,13 (д, J=3,3 Гц, 3H), 2,27 (с, 3Н); C ЯМР (101 MГц, ДМСО-d6) δ 160,1 (д, J=244,4 Гц), 154,9 (д, J=7,1 Гц), 152,9, 136,8, 136,2 (д, J=243,2 Гц), 134,2, 132,8 (д, J=37,3 Гц), 129,2 (д, J=8,2 Гц), 129,0, 128,7, 127,8, 124,6 (д, J=3,4 Гц), 124,0 (д, J=14,5 + Гц), 115,3 (д, J=21,0 Гц), 51,0, 47,7, 37,2 (д, J=8,3 Гц), 20,6; ESIMS m/z 356 ([M+H] ). Приклад 17: отримання 4-аміно-5-фтор-1-(тіофен-3-іл)піримідин-2(1H)-ону (39) А) До розчину пентасульфіду фосфору (102,6 г, 0,46 моль) в диглімі (1 л) додавали 5фторпіримідин-2,4(1H, 3H)-діон (30 г, 0,23 моль). Зі швидкістю, що визначається виділенням діоксиду вуглецю, додавали твердий гідрокарбонат натрію (NaHCO3; 77,3 г, 1,04 моль). Реакційну суміш перемішували протягом ночі при 110ºС. Жовту суміш охолоджували і виливали в 1 л холодної води. Осаджений твердий продукт виділяли фільтруванням і очищали хроматографією на нормальній фазі (градієнт 10-50 % EtOAc/петролейний ефір), отримуючи при цьому 5-фтор-4-тіоксо-3,4-дигідропіримідин-2(1H)-он (13,4 г, 40 %) у вигляді жовтої твердої 1 речовини: т. пл. 254-255ºС; Н ЯМР (301 МГц, ДМСО-d6) δ 7,81 (д, J=4,0 Гц, 1Н); ESIMS m/z 145 ([M-H] ). В) Цю речовину отримували процедурою, описаною в Tetrahedron 1985, 41, 5289-5293. До розчину 5-фтор-4-тіоксо-3,4-дигідропіримідин-2(1H)-ону (12,4 г, 84,9 ммоль) і метоксиду натрію (4,54 г, 84,9 ммоль) в MeOH (100 мл) по краплях додавали алілбромід (10,27 г, 84,9 ммоль) при кімнатній температурі. Реакційну суміш перемішували протягом ночі при кімнатній температурі. Після видалення розчинника залишок очищали хроматографією на нормальній фазі (градієнт 10-33 % EtOAc/гексан), отримуючи при цьому 4-(алілтіо)-5-фторпіримідин-2(1H)-он (6 г, 38 %) у 1 вигляді білої твердої речовини: т. пл. 150-152ºС; H ЯМР (301 MГц, ДМСО-d6) δ 11,60 (с, 1Н), 8,00 (д, J=4,5 Гц, 1Н), 5,90 (ддт, J=16,8, 10,0, 6,8 Гц, 1Н), 5,34 (дд, J=16,9, 1,4 Гц, 1Н), 5,15 (дд, + J=10,0, 0,7 Гц, 1Н), 3,83 (д, J=6,8 Гц, 2H); ESIMS m/z 187 ([M+H] ). С) Цю речовину отримували процедурою, описаною в J. Org. Chem. 2006, 71, 9183-9190. До переміщуваної суспензії сухого Cu(OAc)2 (1,02 г, 5,64 ммоль), 4-(алілтіо)-5-фторпіримідин-2(1H)ону (700 мг, 3,76 ммоль), тіофен-3-ілборонової кислоти (962 мг, 7,52 ммоль) і активованих молекулярних сит 3 Å (2 г) в сухому СН2Cl2 (30 мл) додавали піридин (595 мг, 7,52 ммоль) при кімнатній температурі. Суміш перемішували протягом 24 годин при температурі навколишнього 18 UA 112284 C2 5 10 15 20 25 30 35 40 середовища в присутності повітря. Реакційну суміш розбавляли СН2Cl2 (30 мл), фільтрували через подушку целіту і промивали водою (50 мл) в присутності етилендіамінтетраоцтової кислоти (EDTA; 700 мг, 2,4 ммоль). Безбарвну органічну фазу сушили над MgSO 4 і концентрували у вакуумі. Залишок очищали хроматографією на нормальній фазі (елюювання постійно сумішшю 2:1 петролейний ефір:EtOAc), отримуючи при цьому 4-(алілтіо)-5-фтор-1(тіофен-3-іл)піримідин-2(1H)-он (290 мг, 29 %) у вигляді жовтої твердої речовини: т. пл. 1251 127ºС; H ЯМР (301 MГц, ДМСО-d6) δ 8,52-8,35 (м, 1Н), 7,81 (с, 1Н), 7,69-7,55 (м, 1Н), 7,32 (д, J=3,5 Гц, 1Н), 6,05-5,81 (м, 1Н), 5,36 (д, J=16,9 Гц, 1Н), 5,18 (д, J=9,8 Гц, 1Н), 3,89 (д, J=6,4 Гц, + 2H); ESIMS m/z 269 ([M+H] ). D) Цю речовину отримували процедурою, описаною в J. Org. Chem. 2006, 71, 9183-9190. 4(Алілтіо)-5-фтор-1-(тіофен-3-іл)піримідин-2(1H)-он (330 мг, 1,23 ммоль) розчиняли в розчині аміаку в метанолі (7 н, 5 мл). Реакційну суміш перемішували протягом ночі при 100ºС в автоклаві. Після видалення розчинника залишок очищали препаративною тонкошаровою хроматографією, отримуючи при цьому 4-аміно-5-фтор-1-(тіофен-3-іл)піримідин-2(1H)-он (177 1 мг, 68 %) у вигляді жовтої твердої речовини: т. пл. 228-229ºС; H ЯМР (300 MГц, ДМСО-d6) δ 8,11 (д, J=6,9 Гц, 1Н), 7,89 (с, 1Н), 7,65 (д, J=1,9 Гц, 2H), 7,56 (дд, J=5,1, 3,3 Гц, 1Н), 7,29 (дд, J=5,1, + 1,0 Гц, 1Н); ESIMS m/z 212 ([M+H] ). Сполуки 40-55 отримували, як описано в прикладі 17. Приклад 18: отримання (Е)-N'-(5-фтор-2-оксо-1-(тіофен-3-іл)-1,2-дигідропіримідин-4-іл)-N, Nдиметилформімідаміду (56) 4-Аміно-5-фтор-1-(тіофен-3-іл)піримідин-2(1H)-он (140 мг, 0,66 ммоль) розчиняли в ДМФАDMA (5 мл). Реакційну суміш перемішували при кип'ятінні із зворотним холодильником протягом ночі. Залишковий розчинник ДМФА-DMA видаляли у вакуумі і залишок очищали препаративною тонкошаровою хроматографією, отримуючи при цьому (Е)-N'-(5-фтор-2-оксо-1-(тіофен-3-іл)-1,2дигідропіримідин-4-іл)-N, N-диметилформімідамід (75 мг, 43 %) у вигляді жовтої твердої 1 речовини: т. пл. 211-213ºС; H ЯМР (300 MГц, ДМСО-d6) δ 8,73 (с, 1Н), 8,22 (д, J=6,4 Гц, 1Н), 7,75 (дд, J=3,2, 1,4 Гц, 1Н), 7,60 (дд, J=5,2, 3,2 Гц, 1Н), 7,34 (дд, J=5,2, 1,4 Гц, 1Н), 3,26 (с, 3H), + 3,13 (с, 2H); ESIMS m/z 267 ([M+H] ). Сполуки 57-64 отримували, як описано в прикладі 18. Приклад 19: отримання 5-фтор-4-(2-фторбензиламіно)-1-(тіофен-3-іл)піримідин-2(1H)-ону (65) До розчину 4-(алілтіо)-5-фтор-1-(тіофен-3-іл)піримідин-2(1H)-ону (140 мг, 0,66 ммоль) в MeOH (1 мл) додавали (2-фторфеніл)метанамін (50 мг, 0,186 ммоль). Реакційну суміш нагрівали при 100ºС протягом 30 хв в мікрохвильовій печі. Після охолоджування суміш очищали препаративною тонкошаровою хроматографією, отримуючи при цьому 5-фтор-4-(2фторбензиламіно)-1-(тіофен-3-іл)піримідин-2(1H)-он (41 мг, 20 %) у вигляді білої твердої 1 речовини: т. пл. 75-78ºС; H ЯМР (300 MГц, ДМСО-d6) δ 8,70 (с, 1Н), 8,16 (д, J=7,0 Гц, 1Н), 7,66 (дд, J=3,2, 1,4 Гц, 1Н), 7,57 (дд, J=5,2, 3,2 Гц, 1Н), 7,43-7,13 (м, 5H), 4,63 (д, J=5,5 Гц, 2H); ESIMS + m/z 320 ([M+H] ). Сполуки 66-73 отримували, як описано в прикладі 19. Приклад 20: отримання 4-аміно-1-(циклопропілметил)-5-фторпіримідин-2(1H)-ону (74) 19 UA 112284 C2 5 10 15 20 25 30 35 40 До розчину (бромметил)циклопропану (1,0 г, 7,4 ммоль) в ДМФА (20 мл) додавали молекулярні сита (~2 г) і суміш, що утворилася, перемішували при кімнатній температурі. Через 1 годину додавали 4-аміно-5-фторпіримідин-2-ол (1,9 г, 14,8 ммоль) і K2CO3 (5,1 г, 37 ммоль) і реакційну суміш нагрівали при 90ºС протягом 12 годин. Після охолоджування до кімнатної температури сиру реакційну суміш фільтрували через лійку Бюхнера і твердий залишок промивали EtOAc. Зібраний фільтрат концентрували у вакуумі, отримуючи при цьому залишок, який очищали хроматографією на нормальній фазі (5 % MeOH/EtOAc, постійно). Після перекристалізації з метил-трет-бутилового простого ефіру 4-аміно-1-(циклопропілметил)-5фторпіримідин-2(1H)-он (1,12 г, 83 %) виділяли у вигляді білої твердої речовини: т. пл. 2241 226ºС; H ЯМР (400 MГц, метанол-d4) δ 7,86 (д, J=6,2 Гц, 1Н), 3,61 (д, J=7,2 Гц, 2H), 1,24 (ддд, + J=12,8, 7,6, 4,8 Гц, 1Н), 0,65-0,50 (м, 2H), 0,39 (кв, J=4,8 Гц, 2H); ESIMS m/z 184 ([M+H] ). Сполуки 75-79 отримували, як описано в прикладі 20. Приклад 21: отримання етил-1-(циклопропілметил)-5-фтор-2-оксо-1,2-дигідропіримідин-4ілкарбамату (80) 4-Аміно-1-(циклопропілметил)-5-фторпіримідин-2(1H)-он (200 мг, 1,09 ммоль) розчиняли в СН2Cl2 (0,90 мл) і піридині (172,4 мг, 2,18 ммоль) при кімнатній температурі і потім охолоджували до -20С. Потім до реакційної суміші по краплях додавали етилхлорформіат (166 мг, 1,53 ммоль), підтримуючи температуру реакції між -20 і -5ºС. Після завершення додавання реакційної суміші давали можливість повільно нагріватися до кімнатної температури і перемішували протягом 2 годин. Реакційну суміш фільтрували і тверду речовину промивали EtOAc (15 мл × 3). Фільтрат концентрували у вакуумі і очищали препаративною тонкошаровою хроматографією, отримуючи при цьому етил-1-(циклопропілметил)-5-фтор-2-оксо-1,2дигідропіримідин-4-ілкарбамат (70 мг, 30 %) у вигляді блідо-жовтої твердої речовини: т. пл. 901 , 92ºС; H ЯМР (400 MГц метанол-d4) δ 8,20 (с, 1Н), 4,26 (кв, J=7,1 Гц, 2H), 3,70 (д, J=7,2 Гц, 2H), + 1,24-1,36 (м, 4H), 0,65-0,57 (м, 2H), 0,46-0,39 (м, 2H); ESIMS m/z 256 ([M+H] ). Сполуки 81-84 отримували, як описано в прикладі 21. Приклад 22: отримання 1-(2-хлорфеніл)-3-(1-(циклопропілметил)-5-фтор-2-оксо-1,2дигідропіримідин-4-іл)сечовини (85) До перемішуваного розчину 4-аміно-1-(циклопропілметил)-5-фторпіримідин-2(1H)-ону (150 мг, 0,819 ммоль) в сухому CH 3CN (7,5 мл) при кімнатній температурі і в атмосфері азоту додавали 2-хлорфенілізоціанат (138,3 мг, 0,90 ммоль). Після перемішування протягом 1 години сиру реакційну суміш фільтрували і тверді речовини промивали CH 3CN (10 мл). Зібраний фільтрат потім концентрували у вакуумі і сушили у високому вакуумі, отримуючи при цьому 1-(2хлорфеніл)-3-(1-(циклопропілметил)-5-фтор-2-оксо-1,2-дигідропіримідин-4-іл)сечовину (160 мг, 1 58 %) у вигляді не зовсім білої твердої речовини: т. пл. 197-199ºС; Н ЯМР (400 MГц, метанолd4) δ 8,26 (д, J=6,0 Гц, 1Н), 8,21 (дд, J=8,3, 1,5 Гц, 1Н), 7,47 (дд, J=8,0, 1,4 Гц, 1Н), 7,35-7,28 (м, 1Н), 7,13 (тд, J=7,8, 1,5 Гц, 1Н), 3,74 (д, J=7,3 Гц, 2H), 1,32 (м, 1Н), 0,69-0,58 (м, 2H), 0,50-0,38 (м, + 2H); ESIMS m/z 337 ([M+H] ). 20 UA 112284 C2 Сполуки 86-93 отримували, як описано в прикладі 22. Приклад 23: отримання N-(5-фтор-2-оксо-1-((тетрагідрофуран-2-іл)метил)-1,2дигідропіримідин-4-іл)тіофен-2-карбоксаміду (94) 5 10 15 20 25 30 35 40 Цю сполуку отримували процедурою, описаною в J. Org. Chem. 2005, 70, 7459-7467. До розчину 4-аміно-5-фтор-1-((тетрагідрофуран-2-іл)метил)піримідин-2(1H)-ону (200 мг, 0,94 ммоль) в сухому ТГФ (1 мл) при кімнатній температурі додавали 1-етил-3-(3диметиламінопропіл)карбодіімід (EDC; 180 мг, 0,94 ммоль) і 1Н-бензо[d][1,2,3]триазол-1-ол (НOBt; 139 мг, 1,03 ммоль). Після перемішування протягом 10 хв додавали тіофен-2-карбонову кислоту (145 мг, 1,13 ммоль) і розчину, що утворився, надавали можливість для перемішування при кімнатній температурі протягом 12 годин. Реакційну суміш концентрували у вакуумі, гасили насиченим водним розчином NaHCO3 (10 мл) і екстрагували EtOAc (25 мл × 3). Об'єднані екстракти промивали насиченим водним розчином хлориду натрію (NaCl), сушили над Na 2SO4, фільтрували і концентрували роторним випаровуванням. Очищення хроматографією на нормальній фазі (градієнт 0-2 % MeOН/СН2Cl2), отримуючи при цьому 4-аміно-5-фтор-1((тетрагідрофуран-2-іл)метил)піримідин-2(1H)-он (60 мг, 20 %) у вигляді білої твердої речовини: 1 , т. пл. 168-170ºС; Н ЯМР (400 MГц, CDCl3) δ 12 96 (с, 1Н), 7,96 (д, J=3,7 Гц, 1Н), 7,63 (д, J=5,7 Гц, 1Н), 7,60 (д, J=4,9 Гц, 1Н), 7,16-7,11 (м, 1Н), 4,20-4,08 (м, 2H), 3,89 (дд, J=15,1, 6,9 Гц, 1Н), 3,80 (дд, J=14,5, 7,5 Гц, 1Н), 3,57 (дд, J=14,4, 7,7 Гц, 1Н), 2,10 (дт, J=12,8, 6,7 Гц, 1Н), 1,99-1,87 (м, + 2H), 0,88 (м, 1Н); ESIMS m/z 324 ([M+H] ). Сполуки 95-101 отримували, як описано в прикладі 23. Приклад 24: отримання 5-фтор-1-((тетрагідрофуран-2-іл)метил)-4-(тіофен-2ілметиламіно)піримідин-2(1H)-ону (102) Цю сполуку отримували процедурою, описаною в J. Org. Chem. 2005, 70, 7459-7467. До розчину 4-аміно-5-фтор-1-((тетрагідрофуран-2-іл)метил)піримідин-2(1H)-ону (160 мг, 0,495 ммоль) в ТГФ (4 мл) при кімнатній температурі додавали по краплях BSA (0,61 мл, 2,47 ммоль). Після завершення додання по краплях додавали комплекс боран-N, N-діізопропілетиламін (DIPEA·BH3; 0,90 мл, 4,95 мл) і розчин, що утворився, перемішували при кімнатній температурі протягом 15 хв. Реакційну суміш гасили додаванням MeOH (20 мл) і суміш концентрували у вакуумі. Суміш, що утворилася, розчиняли в суміші 1:1 (об.:об.) 17 % аміак в метанолі: 28 % аміак у воді (135 мл) і нагрівали при 50ºС протягом 13 годин. Після охолоджування до кімнатній температурі суміш екстрагували хлороформом (CHCl3; 100 мл × 2). Об'єднані екстракти промивали водним розчином NaCl, сушили над Na 2SO4, фільтрували і концентрували у вакуумі. Очищення препаративною тонкошаровою хроматографією давало 5-фтор-1-((тетрагідрофуран2-іл)метил)-4-(тіофен-2-ілметиламіно)піримідин-2(1H)-он (40 мг, 26 %) у вигляді смолистої білої 1 твердої речовини: H ЯМР (400 MГц, Ацетон-d6) δ 7,69 (д, J=6,7 Гц, 1Н), 7,52 (с, 1Н), 7,32 (дд, J=5,1, 1,2 Гц, 1Н), 7,08 (дд, J=3,4, 0,9 Гц, 1Н), 6,95 (дд, J=5,1, 3,5 Гц, 1Н), 4,85 (д, J=6,0 Гц, 2H), 4,12 (ддд, J=14,6, 7,1, 3,2 Гц, 1Н), 4,00 (дд, J=13,6, 2,8 Гц, 1Н), 3,83 (дт, J=8,1, 6,7 Гц, 1Н), 3,723,64 (м, 1Н), 3,56 (дд, J=13,6, 7,7 Гц, 1Н), 2,02-1,93 (м, 1Н), 1,86 (ддд, J=11,0, 8,1, 1,6 Гц, 2H), 1,67-1,54 (м, 1Н); ІЧ (тонка плівка) 3222, 3125, 3068, 2950, 2875, 1673, 1623, 1586, 1556, 1508, + 1368, 1329, 1186, 1139, 1065, 906 cm-1; ESIMS m/z 310 ([M+H] ). Сполуки 103 і 104 отримували, як описано в прикладі 24. Приклад 25: отримання 5-фтор-4-(2-фторбензиламіно)-1-ізобутилпіримідин-2(1H)-ону (105) 21 UA 112284 C2 5 10 15 20 25 30 A) До розчину 5-фторпіримідин-2,4(1H, 3H)-діону (5,0 г, 38 ммоль) і 1,8діазабіцикло[5.4.0]ундец-7-ену (DBU; 6,4 г, 42 ммоль) в сухому CH3CN (150 мл) при кімнатній температурі в атмосфері азоту додавали по краплях 1-бром-2-метилпропан (5,3 г, 38 ммоль). Реакційну суміш потім нагрівали для кип'ятіння із зворотним холодильником протягом 18 годин. Після охолоджування до кімнатної температури розчинник видаляли у вакуумі. Сирий залишок очищали хроматографією на нормальній фазі (градієнт 0-20 % EtOAc/петролейний ефір), отримуючи при цьому 5-фтор-1-ізобутилпіримідин-2,4(1H, 3H)-діон (2,5 г, 35 %) у вигляді білої 1 , твердої речовини: т. пл. 173-174ºС; H ЯМР (400 MГц CDCl3) δ 8,61 (с, 1Н), 7,21 (д, J=5,5 Гц, 1Н), 3,53 (д, J=7,5 Гц, 2H), 2,13-2,01 (м, 1Н), 0,98 (д, J=6,7 Гц, 6H); ESIMS m/z 185 ([M-H] ). B) Фосфорилтрихлорид (3,3 г, 21 ммоль) додавали до розчину 1,2,4-триазолу (6,7 г, 97 ммоль) в CH3CN (53 мл) в атмосфері азоту при кімнатній температурі. Суміш охолоджували до 0ºС, після чого по краплях додавали триетиламін (Et3N; 9,5 г, 92 ммоль) з подальшим додаванням розчину 5-фтор-1-ізобутилпіримідин-2,4(1H, 3H)-діону (2,0 г, 11 ммоль) в CH3CN (30 мл). Після перемішування протягом 1 години при кімнатній температурі додавали Et 3N (3,6 г, 36 ммоль) і потім воду (5 мл, 280 ммоль) і реакційну суміш перемішували протягом додаткових 10 хв. Сиру реакційну суміш потім концентрували у вакуумі. Перекристалізація з суміші EtOAc/петролейний ефір давала 5-фтор-1-ізобутил-4-(1H-1,2,4-триазол-1-іл)піримідин-2(1H)-он 1 (1,9 г, 74 %) у вигляді не зовсім білої кристалічної твердої речовини: т. пл. 150-153ºС; Н ЯМР (400 MГц, CDCl3) δ 9,26 (с, 1Н), 8,23 (с, 1Н), 7,84 (д, J=5,7 Гц, 1Н), 3,79 (д, J=7,4 Гц, 2H), 2,28 (дт, + J=13,7, 6,9 Гц, 1Н), 1,02 (д, J=6,7 Гц, 6H); ESIMS m/z 238 ([M+H] ). С) Розчин 5-фтор-1-ізобутил-4-(1H-1,2,4-триазол-1-іл)піримідин-2(1H)-ону (500 мг, 2,1 ммоль) і 2-фторбензиламіну (313 мг, 2,5 ммоль) в сухому 1,4-діоксані (10 мл) нагрівали для кип'ятіння із зворотним холодильником протягом 1 години в атмосфері азоту. Після охолоджування до кімнатної температури реакційну суміш концентрували у вакуумі. Перекристалізація з суміші ЕtOAc/метил-трет-бутиловий простий ефір давала 5-фтор-4-(2фторбензиламіно)-1- ізобутилпіримідин-2(1H)-он (545 мг, 89 %) у вигляді не зовсім білої твердої 1 , речовини; т. пл. 118-119ºС; H ЯМР (400 MГц CDCl3) δ 7,45 (тд, J=7,6, 1,7 Гц, 1Н), 7,35-7,28 (м, 2H), 7,13 (ддд, J=21,9, 13,9, 7,3 Гц, 3H), 5,58 (с, 1Н), 4,81 (д, J=5,4 Гц, 2H), 3,56 (д, J=7,5 Гц, 2H), + 2,16 (дт, J=13,6, 6,8 Гц, 1Н), 0,95 (д, J=6,7 Гц, 6H); ESIMS m/z 295 ([M+H] ). Сполуки 106-110 отримували, як описано в прикладі 25. 22 UA 112284 C2 Таблиця I Сполуки і дані характеристик, що належать до них Сполука 3 Структура Зовнішній вигляд Біла тверда речовина Т. пл. (ºС) 157-187 розклад. МС 1 а Н ЯМР (δ, розчинник) (CDCl3) 7,47 (д, J=6,1 Гц, 1Н), 5,91 (с, 1Н), 4,45 (с, 2Н), 4,38 (д, J=5,2 Гц, 2Н), 2,36 (с, 12Н) ESIMS m/z (CDCl3) 8,81 (с, 1H), + 343 ([M+H] ) 7,40 (д, J=2,3 Гц, 1H), 7,37 (д, J=8,2 Гц, 1H), 7,33 (д, J=5,6 Гц, 1H), 7,22 (дд, J=8,2, 2,3 Гц, 1H), 5,06 (с, 2H), 3,18 (с, 6H) 5 Жовте масло 6 Біла тверда речовина 186-188 ESIMS m/z (CDCl3) 8,85 (с, 1H), + 275 ([M+H] ) 7,41-7,31 (м, 5H), 7,24 (д, J=5,5 Гц, 1H), 5,04 (с, 2H), 3,22 (с, 1H), 3,21 (с, 3H) 7 Біла тверда речовина 178-179 ESIMS m/z (CDCl3) 8,85 (с, 1H), + 289 ([M+H] ) 7,26-7,17 (м, 5H), 4,99 (с, 2H), 3,21 (с, 6H), 2,37 (с, 3H) 13 Біла тверда речовина 109-111 16 Біла тверда речовина 160-163 ESIMS m/z (600 MГц, ДМСО-d6) + 285 ([M+H] ) 8,65 (с, 1H), 8,04 (д, J=6,2 Гц, 1H), 5,58 (с, 2H), 3,20 (с, 3H), 3,07 (с, 3H), 2,27 (т, J=7,3 Гц, 2H), 1,53-1,46 (м, 2H), 0,83 (т, J=7,3 Гц, 3H) ESIMS m/z (ДМСО-d6) 7,97 (д, + 218 ([M+H] ) J=6,6 Гц, 1H), 7,83 (с, 1H), 7,58 (с, 1H), 5,03 (с, 2H), 3,65-3,53 (м, 2H), 3,46-3,38 (м, 2H), 3,22 (с, 3H) 23 UA 112284 C2 Продовження таблиці I Сполука Зовнішній вигляд Не зовсім біла тверда речовина Т. пл. (ºС) 18 Не зовсім біла тверда речовина 166-170 19 Біла тверда речовина 240-245 20 Біла тверда речовина 150-154 21 Біла тверда речовина 210-214 22 Біла тверда речовина 259-264 23 Біла тверда речовина 29 Біла тверда речовина 17 Структура 24 187-192 МС 1 а Н ЯМР (δ, розчинник) ESIMS m/z (ДМСО-d6) δ 7,96 (д, + 260 ([M+H] ) J=6,6 Гц, 1H), 7,80 (с, 1H), 7,57 (с, 1H), 4,99 (с, 2H), 3,51 (дд, J=20,2, 12,2 Гц, 2H), 0,85 (т, J=7,9 Гц, 2H), -0,03 (с, 9H) ESIMS m/z (ДМСО-d6) 7,98 (д, + 272 ([M+H] ) J=6,5 Гц, 1H), 7,85 (с, 1H), 7,62 (с, 1H), 5,01 (с, 2H), 3,44 (т, J=6,4 Гц, 2H), 1,47 (м, 2H), 1,24 (м, 10H), 0,86 (т, J=5,9 Гц, 3H) ESIMS m/z (ДМСО-d6) 8,09 (д, + 270 ([M+H] ) J=6,6 Гц, 1H), 7,97 (с, 1H), 7,72 (с, 1H), 7,36 (д, J=8,8 Гц, 2H), 7,07 (д, J=8,9 Гц, 2H), 5,58 (с, 2H) ESIMS m/z (ДМСО-d6) 7,97 (с, + 260 ([M+H] ) 1H), 7,81 (д, J=6,3 Гц, 1H), 7,72 (с, 1H), 5,84 (с, 1H), 4,15 (дд, J=13,7, 6,8 Гц, 2H), 3,59 (дд, J=13,3, 6,4 Гц, 2H), 1,28-1,04 (м, 6H) ESIMS m/z (ДМСО-d6) 7,99 (м, + 230 ([M+H] ) J=6,7 Гц, 2H), 7,72 (с, 1H), 5,55 (с, 2H), 2,30 (т, J=7,2 Гц, 2H), 1,68-1,39 (м, 2H), 0,86 (т, J=7,4 Гц, 3H) ESIMS m/z (ДМСО-d6) 7,99 (д, + 244 ([M+H] ) J=6,7 Гц, 1H), 7,97 (с, 1H), 7,71 (с, 1H), 5,54 (с, 2H), 1,12 (с, 9H) ESIMS m/z (ДМСО-d6) 8,08 (д, + 246 ([M+H] ) J=7,0 Гц, 1H), 7,95 (с, 1H), 7,69 (с, 1H), 6,72 (кв, J=5,2 Гц, 1H), 4,12 (кв, J=7,0 Гц, 2H), 1,55 (д, J=6,1 Гц, 3H), 1,20 (т, J=7,1 Гц, 3H) 279 розкл. ESIMS m/z (ДМСО-d6) 7,98 (д, + 158 ([M+H] ) J=6,8 Гц, 1H), 7,57 (с, 1H), 7,39 (с, 1H), 3,63 (кв, J=7,1 Гц, 2H), 1,14 (т, J=7,1 Гц, 3H) 162-166 UA 112284 C2 Продовження таблиці I Сполука Зовнішній вигляд Біла тверда речовина Т. пл. (ºС) МС 168-189 ESIMS m/z + 264 ([M+H] ) 31 Біла тверда речовина 252-254 ESIMS m/z + 268 ([M+H] ) 32 Блідо-жовта тверда речовина 255 розклад. ESIMS m/z + 214 ([M+H] ) 33 Бежева тверда речовина 250-254 ESIMS m/z + 256 ([M+H] ) 35 Біла тверда речовина 196-200 ESIMS m/z + 311 ([M+H] ) 36 Біла тверда речовина 196-199 ESIMS m/z + 271 ([M+H] ) 40 Біла тверда 244,8-245,6 ESIMS m/z + речовина 266 ([M+H] ) 30 Структура 25 1 а Н ЯМР (δ, розчинник) (ДМСО-d6) 7,93 (д, J=3,3 Гц, 1H), 7,31 (с, 2H), 7,19 (д, J=8,6 Гц, 2H), 6,90-6,82 (м, 2H), 4,28 (т, J=6,9 Гц, 2H), 3,72 (с, 3H), 2,89 (т, J=6,9 Гц, 2H) (ДМСО-d6) 7,97 (д, J=3,5 Гц, 1H), 7,46 (с, 2H), 7,39-7,34 (м, 2H), 7,34-7,28 (м, 2H), 4,34 (т, J=6,7 Гц, 2H), 2,97 (т, J=6,7 Гц, 2H) (ДМСО-d6) 7,92 (д, J=3,2 Гц, 1H), 7,27 (с, 2H), 4,10 (дд, J=10,5, 6,7 Гц, 1H), 4,02 (дд, J=10,5, 8,0 Гц, 1H), 3,78-3,69 (м, 2H), 3,63 (дд, J=15,0, 7,8 Гц, 1H), 3,47 (дд, J=8,6, 5,6 Гц, 1H), 2,59 (дт, J=14,1, 7,2 Гц, 1H), 1,97 (дтд, J=13,8, 8,2, 5,6 Гц, 1H), 1,65-1,53 (м, 1H) (ДМСО-d6) 8,04 (д, J=6,6 Гц, 1H), 7,74 (с, 1H), 7,50 (с, 1H), 7,35-7,20 (м, 2H), 7,06 (тд, J=8,5, 1,8 Гц, 1H), 4,82 (с, 2H) (ДМСО-d6) 8,64 (с, 1H), 8,24 (д, J=6,2 Гц, 1H), 7,48-7,35 (м, 2H), 7,23-7,13 (м, 1H), 4,85 (с, 2H), 3,21 (с, 3H), 3,08 (с, 3H) (ДМСО-d6) 8,67 (с, 1H), 8,05 (д, J=6,2 Гц, 1H), 4,48 (с, 2H), 4,14 (кв, 7,1 Гц, 2H), 3,22 (с, 3H), 3,10 (с, 3H), 1,20 (т, J=7,1 Гц, Н) (ДМСО-d6) 7,98 (д, J=6,7 Гц, 1H), 7,80 (с, 1H), 7,57 (с, 1H), 7,00 (м, 2H), 6,89 (дд, J=8,6, 2,3 Гц, 1H), 3,79 (с, 3H), 3,76 (с, 3H) UA 112284 C2 Продовження таблиці I Сполука 41 42 Структура 1 а Зовнішній Т. пл. (ºС) МС Н ЯМР вигляд (δ, розчинник) Біла тверда 213,5-214,4 ESIMS m/z (ДМСО-d6) 8,28 (д, + речовина 156 ([M+H] ) J=7,1 Гц, 1H), 8,01 (с, 1H), 7,77 (с, 1H), 7,18 (дд, J=15,4, 10,3 Гц, 1H), 5,27 (д, J=16,2 Гц, 1H), 4,78 (д, J=8,0 Гц, 1H) Не зовсім 233-235 ESIMS m/z (ДМСО-d6) 8,05 (дд, + біла тверда 206 ([M+H] ) J=6,8, 1,7 Гц, 1H), речовина 7,86 (с, 1H), 7,62 (с, 1H), 7,51-7,31 (м, 5H) 43 Не зовсім біла тверда речовина 225-227 ESIMS m/z (ДМСО-d6) 8,00 (д, + 220 ([M+H] ) J=6,7 Гц, 1H), 7,83 (с, 1H), 7,59 (с, 1H), 7,25 (с, 4H), 2,34 (с, 3H) 44 Коричнева тверда речовина 230-232 45 Не зовсім біла тверда речовина 255-257 46 Блідокоричнева тверда речовина 175-178 47 Не зовсім біла тверда речовина 275-279 ESIMS m/z (ДМСО-d6) 7,99 (д, + 236 ([M+H] ) J=6,7 Гц, 1H), 7,81 (с, 1H), 7,57 (с, 1H), 7,29 (д, J=8,8 Гц, 2H), 6,98 (д, J=8,8 Гц, 2H), 3,78 (с, J=8,6 Гц, 3H) ESIMS m/z (ДМСО-d6) 8,07 (д, + 240 ([M+H] ) J=6,3 Гц, 1H), 7,93 (с, 1H), 7,68 (с, 1H), 7,51 (дд, J=8,6, 1,0 Гц, 2H), 7,43 (дд, J=8,7, 1,1 Гц, 2H) ESIMS m/z (ДМСО-d6) 8,16 (д, + 231 ([M+H] ) J=6,9 Гц, 1H), 7,987,94 (м, 1H), 7,867,82 (м, 1H), 7,827,76 (м, 1H), 7,67 (д, J=8,0 Гц, 1H) ESIMS m/z (ДМСО-d6) 7,96 (д, + 250 ([M+H] ) J=6,7 Гц, 1H), 7,82 (с, 1H), 7,57 (с, 1H), 6,99 (д, J=2,1 Гц, 1H), 6,96 (д, J=8,2 Гц, 1H), 6,82 (дд, J=8,3, 2,1 Гц, 1H), 6,08 (с, 2H) 26 UA 112284 C2 Продовження таблиці I Сполука 48 49 50 51 52 53 54 Структура Зовнішній вигляд Жовта тверда речовина Т. пл. (ºС) МС 1 а Н ЯМР (δ, розчинник) 256-258 ESIMS m/z (ДМСО-d6) 8,42 (д, + 232 ([M+H] ) J=7,2 Гц, 1H), 8,04 (с, 1H), 7,82 (с, 1H), 7,66 (д, J=15,0 Гц, 1H), 7,44 (д, J=7,9 Гц, 2H), 7,36 (т, J=7,6 Гц, 2H), 7,26 (дд, J=10,5, 4,0 Гц, 1H), 6,81 (д, J=15,0 Гц, 1H) Блідо-корич- 212-214 ESIMS m/z (ДМСО-d6) 8,24 (д, + нева тверда 246 ([M+H] ) J=7,2 Гц, 1H), 7,92 (с, речовина 1H), 7,69 (с, 1H), 7,31 (м, 2H), 7,22 (дд, J=14,9, 7,1 Гц, 3H), 7,03 (дд, J=14,5, 1,6 Гц, 1H), 5,95 (дт, J=14,5, 7,3 Гц, 1H), 3,45 (д, J=7,1 Гц, 2H) Не зовсім 244,4-245,7 ESIMS m/z (ДМСО-d6) 8,14 (д, + біла тверда 284 ([M+H] ) J=6,8 Гц, 1H), 8,04речовина 7,92 (м, 3H), 7,75 (с, J=7,8 Гц, 1H), 7,69 (д, J=8,4 Гц, 2H), 3,26 (с, 3H) Біла тверда 190,6-192,7 ESIMS m/z (ДМСО-d6) 7,75 (д, + речовина 210 ([M+H] ) J=6,6 Гц, 1H), 7,62 (с, 1H), 7,41 (с, 1H), 5,66 (т, J=3,7 Гц, 1H), 2,15 (д, J=36,9 Гц, 4H), 1,60 (дт, J=10,5, 5,0 Гц, 4H) Жовта 211,2-213,0 ESIMS m/z (ДМСО-d6) 7,97 (д, + тверда 232 ([M+H] ) J=6,5 Гц, 1H), 7,83 (с, речовина 1H), 7,60 (с, 1H), 7,45-7,24 (м, 5H), 5,86 (д, J=0,9 Гц, 1H), 5,37 (д, J=0,9 Гц, 1H) Біла тверда 152,8-153,4 ESIMS m/z (ДМСО-d6) 8,17 (д, + речовина 198 ([M+H] ) J=7,1 Гц, 1H), 7,85 (с, 1H), 7,62 (с, 1H), 6,88 (д, J=14,5 Гц, 1H), 5,74 (дт, J=14,3, 7,1 Гц, 1H), 2,06 (кв, J=7,1 Гц, 2H), 1,481,31 (м, 2H), 0,89 (т, J=7,3 Гц, 3H) Жовта 263,3-265,1 ESIMS m/z (CD3OD) 8,20 (д, + тверда 262 ([M+H] ) J=6,7 Гц, 1H), 7,55 речовина (дд, J=14,8, 1,9 Гц, 1H), 7,40 (д, J=8,7 Гц, 2H), 6,94-6,87 (м, 2H), 6,68 (д, J=14,7 Гц, 1H), 3,80 (с, 3H) 27 UA 112284 C2 Продовження таблиці I Сполука 55 57 58 59 60 61 Структура 1 а Зовнішній Т. пл. (ºС) МС Н ЯМР вигляд (δ, розчинник) Біла тверда 272,8-274,2 ESIMS m/z (ДМСО-d6) 8,17 (д, + речовина 256 ([M+H] ) J=6,7 Гц, 1H), 8,007,85 (м, 5H), 7,65 (с, 1H), 7,61-7,49 (м, 3H) Жовта тверда речовина 196,1-198,0 ESIMS m/z (ДМСО-d6) 8,72 (с, + 321 ([M+H] ) 1H), 8,09 (д, J=6,2 Гц 1H), 7,07-7,02 (м, 1H), 7,00 (с, 1H), 6,94 (дд, J=8,5, 2,3 Гц, 1H), 3,80 (с, 3H), 3,77 (с, 3H), 3,25 (с, 3H), 3,13 (с, 3H) Жовта 179,6-181,3 ESIMS m/z (ДМСО-d6) 8,69 (д, + тверда 211 ([M+H] ) J=17,4 Гц, 1H), 8,37 речовина (д, J=6,6 Гц, 1H), 7,21 (ддд, J=22,7, 11,3, 6,8 Гц, 1H), 5,41 (д, J=16,2 Гц, 1H), 4,89 (д, J=9,2 Гц, 1H), 3,25 (с, 3H), 3,11 (д, J=11,5 Гц, 3H) Біла тверда 284,6-186,9 ESIMS m/z (ДМСО-d6) 8,75 (с, + речовина 339 ([M+H] ) 1H), 8,23 (д, J=6,3 Гц, 1H), 8,01 (д, J=8,6 Гц, 2H), 7,74 (д, J=8,6 Гц, 2H), 3,27 (с, 3H), 3,26 (с, 3H), 3,14 (с, 3H) Біла тверда 173,2-174,4 ESIMS m/z (ДМСО-d6) 8,63 (с, + речовина 265 ([M+H] ) 1H), 7,87 (д, J=6,0 Гц, 1H), 5,72 (с, 1H), 3,21 (с, 3H), 3,08 (с, 3H), 2,18 (д, J=37,4 Гц, 4H), 1,62 (дд, J=29,1, 4,7 Гц, 4H) Жовта 147,0-147,9 ESIMS m/z (ДМСО-d6) 8,69 (с, + тверда 287 ([M+H] ) 1H), 8,08 (д, J=6,0 речовина Гц, 1H), 7,40-7,27 (м, 5H), 5,92 (д, J=1,2 Гц, 1H), 5,44 (д, J=1,1 Гц, 1H), 3,23 (с, 3H), 3,12 (с, 3H) 28
ДивитисяДодаткова інформація
Назва патенту англійською5-fluoropyrimidinone derivatives
Автори англійськоюBoebel, Timothy, Bryan, Kristy, Johnson, Peter, Lorsbach, Beth, Meyer, Kevin, Owen, W., Sullenberger, Michael, Webster, Jeffery, Yao, Chenglin, Martin, Timothy
Автори російськоюБебель Тимоти, Брайан Кристи, Джонсон Питер, Лорсбах Бет, Мейер Кевин, Оуен В., Салленбергер Майкл, Вебстер Джеффри, Яо Ченлинь, Мартин Тимоти
МПК / Мітки
МПК: C07D 239/47, A01P 3/00, A01N 43/54
Мітки: 5-фторпіримідинону, похідні
Код посилання
<a href="https://ua.patents.su/45-112284-pokhidni-5-ftorpirimidinonu.html" target="_blank" rel="follow" title="База патентів України">Похідні 5-фторпіримідинону</a>
Попередній патент: Пристрій для локалізації та концентрації плаваючих забруднень
Наступний патент: Сполуки та композиція як інгібітори протеїнкінази
Випадковий патент: Корпус плуга