Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки
Номер патенту: 95604
Опубліковано: 25.08.2011
Автори: Даффі Девід, Кейтс Стівен, Стюарт Кемпбелл, Остуні Емануель, Гроган Майкл, Світнем Пол, Шюллер Олівер
Формула / Реферат
1. Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, при якому:
приєднують щонайменше одну функціональну групу до відомої активної сполуки
(a) заміною неосновного залишку; або
(b) заміщенням неосновного залишку сполуки щонайменше однією функціональною групою;
де зазначеною функціональною групою є саркозиновий залишок або саркозинова похідна.
2. Спосіб за п. 1, де зазначеною фармакокінетичною властивістю є знижене неспецифічне зв'язування з білком.
3. Спосіб за будь-яким з п. 1 або 2, де зазначеною активною сполукою є Варденафіл.
4. Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, при якому:
приєднують щонайменше одну функціональну групу до відомої активної сполуки
(a) заміною неосновного залишку; або
(b) заміщенням неосновного залишку сполуки щонайменше однією функціональною групою;
де зазначена регульована сполука має наступну формулу:
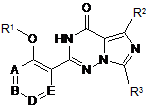 (А)
(А)
або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де
R1 являє собою нижчий алкіл;
R2 та R3 незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо;
А являє собою N або С-Н;
В являє собою N, С-Н, C-(SO2-R4) або C-CO-R4;
D являє собою N, С-Н, C-(SO2-R4) або C-CO-R4;
Е являє собою N або С-Н;
де тільки один з А, В або Е може бути N, та один з В або D являє собою С-(SO2-R4) або C-CO-R4;
R4 - група що має формулу:
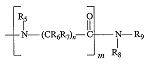 , (С)
, (С)
в якій кожний R5, R6, R7 та R8 незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо;
та додатково або альтернативно R6 та R5 разом утворюють 5- або 6-членне кільце, або R6 та R7 разом утворюють 3-6-членне кільце;
R9 незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо;
альтернативно R8 та R9 разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце; n являє собою 1-4;
та m являє собою 1-6.
5. Спосіб за п. 4, де
А являє собою С-Н;
В являє собою С-Н;
D являє собою C-(SO2-R4); та
Е являє собою С-Н.
6. Спосіб за п. 5, де m являє собою 1 або 2.
7. Спосіб за п. 6, де n являє собою 1.
8. Спосіб за п. 4, де
R1 - етил;
R2 - метил;
R3 - пропіл;
А - С-Н;
В - С-Н;
D - C-(SO2-R4); та
Е - С-Н.
9. Спосіб за п. 4, де зазначена регульована сполука має наступну формулу:
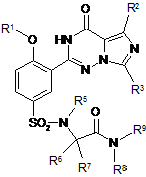 ,
,
в якій кожний R5, R6, R7 та R8 незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та додатково або альтернативно R6 та R5 разом утворюють 5- або 6-членне кільце, або R6 та R7 разом утворюють 3-6-членне кільце; R9 незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; альтернативно R8 та R9 разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце.
10. Спосіб за п. 8, де регульована сполука має наступну формулу:
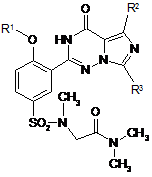 ,
,
або її фармацевтично прийнятна сіль, стереоізомер або гідрат,
де R2 та R3 незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл, може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо.
11. Спосіб за п. 4, де зазначена регульована сполука має наступну формулу:
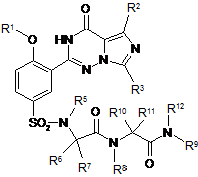 ,
,
де R1 являє собою нижчий алкіл;
R2 та R3 незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо;
R5, R6, R7, R8, R9, R10, R11 та R12 незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо;
та додатково або альтернативно R6 та R5 або R8 та R10 разом утворюють 5- або 6-членне кільце, або R6 та R7 або R10 та R11 разом утворюють 3-6-членне кільце; та R9 та R12 разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце.
12. Спосіб за п. 11, де зазначена регульована сполука має наступну формулу:
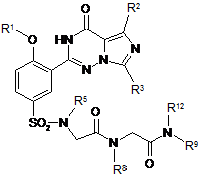 ,
,
де R1, R2, R3 R5, R8, R9 та R12 - як зазначено в п. 11.
13. Спосіб за п. 12, де зазначена регульована сполука має наступну формулу:
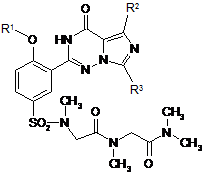 ,
,
де
R1 являє собою нижчий алкіл; та
R2 та R3 незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо.
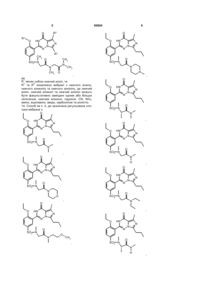
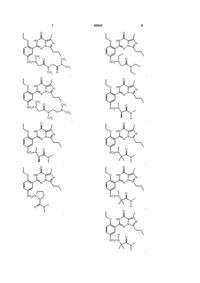
14. Спосіб за п. 4, де зазначена регульована сполука вибрана з
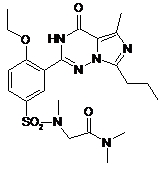 ,
, 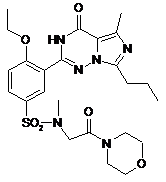 ,
, 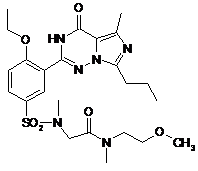 ,
,
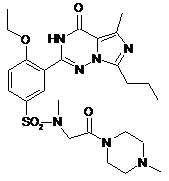 ,
, 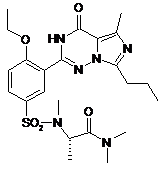 ,
,
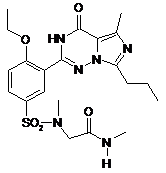 ,
, 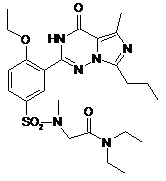 ,
, 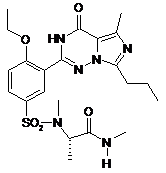 ,
,
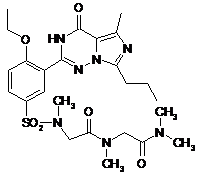 ,
, 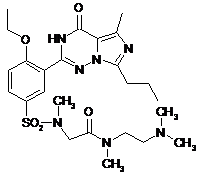 ,
, 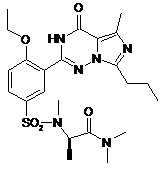 ,
,
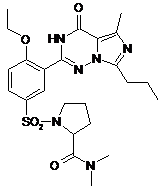 ,
, 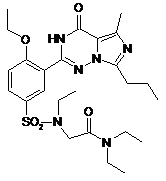 ,
, 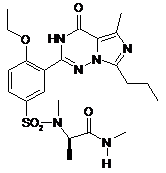 ,
,
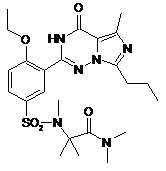 ,
, 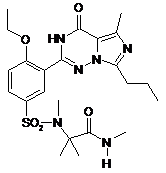 ,
, 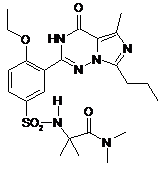 ,
,
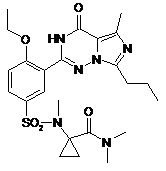 ,
, 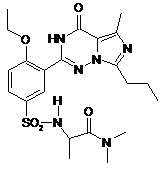 ,
, 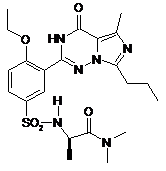 .
.
15. Спосіб за будь-яким з пп. 4-14, де фармакокінетичною властивістю є знижене неспецифічне зв'язування з білком.
16. Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, при якому:
приєднують щонайменше одну функціональну групу до відомої активної сполуки
(a) заміною неосновного залишку; або
(b) заміщенням неосновного залишку сполуки щонайменше однією функціональною групою, таким чином, поліпшуючи фармакокінетичні властивості сполуки;
де зазначена регульована сполука має наступну формулу D:
 (D)
(D)
або її фармацевтично прийнятна сіль, стереоізомер або гідрат, де
R1 являє собою нижчий алкіл; R2 та R3 незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо;
А являє собою N або С-Н;
В являє собою N, С-Н, C-(SO2-NH-R13) або C-CO-NH-R13;
D являє собою N, С-Н, C-(SO2-NH-R13) або C-CO-NH-R13;
Е являє собою N або С-Н;
де тільки один з А, В або Е може бути N, та один з В або D є C-(SO2-NH-R13) або C-CO-NH-R13;
R13 являє собою нижчий алкіл.
17. Спосіб за п. 16, де R13 - метил.
18. Спосіб за п. 16, де R2 та R3 незалежно вибрані з нижчого алкілу.
19. Спосіб за п. 16, де сполука має формулу D1:
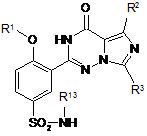 , (D1)
, (D1)
або її фармацевтично прийнятна сіль, стереоізомер, або гідрат, де
R1 являє собою нижчий алкіл;
R2 та R3 незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та
R13 вибраний з нижчого алкілу.
20. Спосіб за п. 19, де R13 - метил.
21. Спосіб за п. 19, де R2 та R3 незалежно вибрані з нижчого алкілу.
22. Спосіб за п. 19, де сполука має формулу
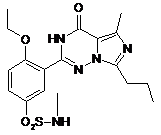 .
.
23. Спосіб за будь-яким з пп. 16-22, де фармакокінетичною властивістю є знижене неспецифічне зв'язування з білком.
Текст
1. Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, при якому: приєднують щонайменше одну функціональну групу до відомої активної сполуки (a) заміною неосновного залишку; або (b) заміщенням неосновного залишку сполуки щонайменше однією функціональною групою; де зазначеною функціональною групою є саркозиновий залишок або саркозинова похідна. 2. Спосіб за п. 1, де зазначеною фармакокінетичною властивістю є знижене неспецифічне зв'язування з білком. 3. Спосіб за будь-яким з п. 1 або 2, де зазначеною активною сполукою є Варденафіл. 4. Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, при якому: приєднують щонайменше одну функціональну групу до відомої активної сполуки (a) заміною неосновного залишку; або (b) заміщенням неосновного залишку сполуки щонайменше однією функціональною групою; де зазначена регульована сполука має наступну формулу: 2 3 8 95604 9 альтернативно R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце; n являє собою 1-4; та m являє собою 1-6. 5. Спосіб за п. 4, де А являє собою С-Н; В являє собою С-Н; 4 D являє собою C-(SO2-R ); та Е являє собою С-Н. 6. Спосіб за п. 5, де m являє собою 1 або 2. 7. Спосіб за п. 6, де n являє собою 1. 8. Спосіб за п. 4, де 1 R - етил; 2 R - метил; 3 R - пропіл; А - С-Н; В - С-Н; 4 D - C-(SO2-R ); та Е - С-Н. 9. Спосіб за п. 4, де зазначена регульована сполука має наступну формулу: R2 O R1 O HN N N N R3 R5 O SO2 N R9 N R6 R7 R8 , 7 8 в якій кожний R , R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та 6 5 додатково або альтернативно R та R разом 6 7 утворюють 5- або 6-членне кільце, або R та R 9 разом утворюють 3-6-членне кільце; R незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та 8 9 алкілтіо; альтернативно R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6членне кільце. 10. Спосіб за п. 8, де регульована сполука має наступну формулу: R2 O 5 R1 O 6 N SO2 N або її фармацевтично прийнятна сіль, стереоізомер або гідрат, 2 3 де R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл, може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо. 11. Спосіб за п. 4, де зазначена регульована сполука має наступну формулу: R2 O R1 O HN N R5 SO2 N N N R3 12 O R10 R11 R N N R6 O CH3 CH3 R9 O R8 , 1 де R являє собою нижчий алкіл; 2 3 R та R незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; 5 6 7 8 9 10 11 12 R , R , R , R , R , R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; 6 5 8 та додатково або альтернативно R та R або R 10 та R разом утворюють 5- або 6-членне кільце, 6 7 10 11 або R та R або R та R разом утворюють 3-69 12 членне кільце; та R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6членне кільце. 12. Спосіб за п. 11, де зазначена регульована сполука має наступну формулу: R2 O R1 O R7 HN N R5 SO2 N N N R3 R12 O N R9 O R8 , 1 2 3 5 8 9 12 де R , R , R R , R , R та R - як зазначено в п. 11. 13. Спосіб за п. 12, де зазначена регульована сполука має наступну формулу: R3 N N N N HN CH3 4 , 5 O HN O O N N N HN N CH3 O SO2 N N N CH3 O SO2 N N CH3 O N , де 1 R являє собою нижчий алкіл; та 2 3 R та R незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо. 14. Спосіб за п. 4, де зазначена регульована сполука вибрана з O , O O HN N O SO2 N N O N N O HN N O SO2 N N O N H HN N N N , O O HN N O SO2 N N N N O SO2 N O , N O , HN N SO2 N N N O SO2 N , O N N , HN N O N N R3 CH3 O 6 R2 O R1 95604 O N N O HN N O N O CH3 , SO2 N N N O N H , 7 95604 8 O O O HN N N CH3 O N N CH3 O SO2 N HN N N N , , O O O HN N CH3 O N N HN N CH3 O SO2 N N N N H , , O HN O N N HN N O SO2 N O SO2 N O N N N CH3 CH3 O O SO2 N CH3 O CH3 N N N N O SO2 N N N , , O O O HN N N O N HN N O SO2 N SO2 N N N N O H N , O , O HN N H SO2 N N N O N , 9 95604 O O HN N N N O SO2 N N , O O HN N H N N O SO2 N N , O O O HN N A B D E HN N N R3 SO2 NH . 15. Спосіб за будь-яким з пп. 4-14, де фармакокінетичною властивістю є знижене неспецифічне зв'язування з білком. 16. Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, при якому: приєднують щонайменше одну функціональну групу до відомої активної сполуки (a) заміною неосновного залишку; або (b) заміщенням неосновного залишку сполуки щонайменше однією функціональною групою, таким чином, поліпшуючи фармакокінетичні властивості сполуки; де зазначена регульована сполука має наступну формулу D: O R2 O O R13 N R1 R1 N N N SO2 N або її фармацевтично прийнятна сіль, стереоізомер, або гідрат, де 1 2 3 R являє собою нижчий алкіл; R та R незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; А являє собою N або С-Н; 13 В являє собою N, С-Н, C-(SO2-NH-R ) або C-CO13 NH-R ; 13 D являє собою N, С-Н, C-(SO2-NH-R ) або C-CO13 NH-R ; Е являє собою N або С-Н; де тільки один з А, В або Е може бути N, та один 13 13 з В або D є C-(SO2-NH-R ) або C-CO-NH-R ; 13 R являє собою нижчий алкіл. 13 17. Спосіб за п. 16, де R - метил. 2 3 18. Спосіб за п. 16, де R та R незалежно вибрані з нижчого алкілу. 19. Спосіб за п. 16, де сполука має формулу D1: R2 O N HN H 10 N , (D1) або її фармацевтично прийнятна сіль, стереоізомер, або гідрат, де 1 R являє собою нижчий алкіл; 2 3 R та R незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та 13 R вибраний з нижчого алкілу. 13 20. Спосіб за п. 19, де R - метил. 2 3 21. Спосіб за п. 19, де R та R незалежно вибрані з нижчого алкілу. 22. Спосіб за п. 19, де сполука має формулу O O HN N O2S NH N N N . 23. Спосіб за будь-яким з пп. 16-22, де фармакокінетичною властивістю є знижене неспецифічне зв'язування з білком. R3 (D) 11 [0001] Фізіологічні та клінічні ефекти інгібіторів фосфодіестерази, специфічної до циклічного гуанозин-3',5'-монофосфату (cGMP-специфічна PDE), дозволяють припустити, що такі інгібітори корисні при різних станах хвороби, при яких бажана модуляція функцій гладких м'язів, нирок, гемостазу, запалення, та/або ендокринної функції. Тип 5 cGMP-специфічної фосфодіестерази (PDE5) є головним ферментом, що гідролізує cGMP в гладких м'язах судин. Таким чином, інгібітор PDE5 можна призначати при лікуванні серцево-судинних розладів, включаючи, але не обмежуючись, гіпертензію, цереброваскулярні розлади та розлади сечостатевої системи, зокрема еректильну дисфункцію. [0002] На даний час існують фармацевтичні продукти, що забезпечують селективне інгібування PDE5. Варденафіл, що продається під торговою маркою Levitra®, є потужним та селективним інгібітором PDE5, який у даний час призначають при лікуванні еректильної дисфункції. Існує потреба у поліпшенні фармакокінетичних властивостей PDE5 інгібіторів. [0003] Розробка нового фармацевтичного агента вимагає обережної оптимізації хімічних та біологічних властивостей головної сполуки. Наприклад, результативний лікарський засіб-кандидат повинен бути безпечним та ефективним для його передбачуваного застосування. Крім того, сполука повинна мати бажані фармакокінетичні та фармакодинамічні профілі. Цей складний процес розробки звичайно вимагає широкого експерименту. У багатьох випадках процес визначення оптимальної сполуки часто може вимагати виготовлення тисяч структурально подібних сполук. [0004] Серед властивостей, що можуть обмежити придатність потенційного фармацевтичного агента, ступінь, з якою сполука утворює комплекс з білками in vivo. Якщо високий відсоток сполуки, що присутня in vivo, неспецифічно зв'язується, наприклад, компонентами крові та плазми крові, залишається тільки дуже невелика кількість вільної сполуки, доступна для тканини, для виконання її терапевтичної функції. Таким чином, зв'язування сполуки з різними білками та іншими компонентами плазмі можуть вимагати небажано велике дозування сполуки для досягнення бажаного терапевтичного ефекту. [0005] Традиційні підходи прагнули змінити фармакокінетичні властивості. [0006] РЕGуляція, процес кон'югації або з'єднання біомолекул та систем доставки лікарського засобу, наприклад, ліпосом, білків, ферментів, лікарських засобів, наночастинок, з поліетиленгліколем, є відомим способом зміни фармакокінетичних властивостей шляхом поліпшення півперіоду циркуляції білка та ліпосомальних фармацевтичних препаратів. (See, Bhadra et al. Pharmazie 2002 Jan; 5791:5-29) РЕGиловані лікарські засоби мають оболонку поліетиленгліколю (PEG) з великою молекулярною вагою навколо лікарського засобу, яка захищає лікарський засіб від руйнування ферментами та дозволяє лікарському засобу подолати кишку, тобто забезпечує оральну придатність, а 95604 12 також діє як захист для попередження розпізнавання РЕGилованого лікарського засобу клітинами імунної системи та захищає лікарський засіб від ниркового кліренсу. (See, Molineux, Cancer Treat Rev. 2002 Apr, 28 Suppl A: 13- 16) Як результат, РЕGиловані білки, наприклад, мають поліпшені фармакокінетичні властивості через зменшений гідроліз та довший півперіод циркуляції. Протиракові агенти мають субоптимальний фармакокінетичних профіль, що вимагає пролонгованого або багатократного введення лікарського засобу. РЕGиловат протиракові агенти, наприклад пегфілграстим, РЕGилований філграстим, показали, що для підтримування ефективності лікарського засобу та опірності пацієнта, вони є щонайменш еквівалентними такому немодифікованому філграстиму з тільки одним введенням на цикл хемотерапії. (See, Crawford, Cancer Treat Rev. 2002 Apr; 28 Suppl A:7-l 1) З'ясували, що РЕGилований ліпосомальний доксорубіцин, інший хемотерапевтичний агент, більш ефективний та менш кардіотоксичний, ніж не РЕGилований або капсулований в ліпосомах доксорубіцин. (See, Crawford, 2002). На додаток до поліпшених фармакокінетичних властивостей РЕОилований лікарські засоби дозволяють знизити схеми дозування, наприклад, фіксована доза замість дози, що залежить від ваги. (See, Yowell та Blackwell, Cancer Treat Rev. 2002 Apr; 28 Suppl A:3-6) Оскільки розмір PEG, його геометрія та ділянка прикріплення РЕGилованого терапевтичного агента, наприклад, білків, визначають фармакокінетичні властивості лікарського засобу, терапевтичні агенти повинні розроблятися за принципом білок-за-білком. (See, Harris et al. Clin. Pharmacokinet. 2001, 40(7):539- 551) Недоліком РЕGилованих агентів є потенційно знижена активність лікарського засобу на мішеневій ділянці через стеричний фактор великої молекули PEG. Розмір молекули PEG є більшою проблемою з невеликими молекулами, ніж з білками. [0007] Даний винахід стосується поліпшення сполуки шляхом розробки її такою, що вона включає, щонайменш, одну функціональну одиницю або групу, тим самим поліпшуючи свої фармакокінетичні властивості. За варіантом здійснення даний винахід стосується поліпшення фармакокінетичного профілю сполуки шляхом приєднання, щонайменш, одної функціональної одиниці або групи до сполуки, що тим самим поліпшує її характеристики неспецифічного зв'язування та фармакокінетичні властивості. За одним варіантом здійснення даного винаходу, щонайменш, один саркозиновий залишок або саркозинова похідна може приєднатися до сполуки. Саркозинова одиниця служить для зниження білкового зв'язування, що тим самим збільшує кількість вільної форми сполуки. Функціональні залишки, які приєднуються до сполуки, відрізняються за їх хімічною структурою від груп, що застосовують в методиці PEG, наприклад, функціональним залишком може бути похідна етиленгліколю, функціональні залишки мають значно меншу молекулярну вагу, наприклад, приблизно 100 дальтон у порівнянні з 5000 дальтон або більше, застосовуваним при стандар 13 тній PEGиляції. Відповідно, хімічна або біологічна активність сполук, що містять функціональні залишки за даним винаходом, не міняється через менший стеричний фактор та більшу доступність лікарського засобу до мішеневої ділянки(ділянок) сполуки. [0008] Даний винахід стосується сполук, що містять, щонайменш, одну функціональну одиницю або групу, причому функціональним залишком є гідрофобна група, ефір, оліго(етиленглікольна) група або її похідна, амін, сіль амонію, простий амід, амід на основі амінокислот, краун-ефір, цукор або нітрил. За наступним варіантом здійснення даного винаходу застосовують сполуку, що містить саркозиновий залишок або олігомер. Крім того, даний винахід стосується фармацевтичних композицій сполук, що містять, щонайменш, одну функціональну одиницю або групу. За прикладом варіанта здійснення даного винаходу забезпечується композиція, що містить саркозиновий залишок або олігомер. [0009] За іншим аспектом даний винахід стосується в основному способу регулювання фармакокінетичного та/або фармакодинамічного профілю сполуки приєднанням, щонайменш, одної функціональної одиниці або групи до сполуки, таким чином поліпшуючи її неспецифічне зв'язування та/або фармакокінетичні властивості. Приєднання функціональної одиниці або групи до сполуки утворює активний агент з поліпшеними біологічними та хімічними властивостями, переважно включаючи, але не обмежуючись, підвищену оральну абсорбцію сполуки,поліпшений метаболізм для підвищеної біодоступності, зменшене білкове зв'язування, поліпшену здатність для подолання гемоенцефалічного бар'єру або їх комбінації, без супутньої підвищеної токсичності у порівнянні з токсичністю такої модифікації попереднього рівня техніки. За переважними варіантами здійснення активний агент має поліпшену розчинність, нижчу ІС50 та/або значно менше білкове зв'язування у порівнянні з оригінальною сполукою. [0010] У цілому, функціональні групи характеризуються мінімальною кількістю донорів Нзв'язку, великою кількість акцепторів Н-зв'язку та можуть мати загальний нейтральний заряд. Сполуки даного винаходу утворюють заміщенням або переміщенням таких функціональних груп у відомих лікарських засобах або розробляють нові лікарські засоби включенням таких функціональних груп. Такі сполуки мають тенденцію відповідати правилу Ліпінського п'ять. Однак, так як такі сполуки містять функціональні групи, вони також стійкі до неспецифічних взаємодій з іншими біологічними молекулами, зокрема білками плазми. За прикладами варіантів здійснення даного винаходу функціональним залишком, що приєднується до сполуки, може бути гідрофобна група, ефір, оліго(етиленглікольна) група або її похідна, амін, сіль амонію, простий амід, амід на основі амінокислоти, краун-ефір, цукор або нітрил. За наступними прикладами варіантів здійснення даного винаходу функціональною групою, що приєднується до сполуки, може бути триметилетилендіамін, метильна 95604 14 група, ацетильна група, оксаламід, саркозиновий залишок, саркозиновий олігомер або саркозинова похідна. [0011] На Фігурі 1 зображено каркас або скелет активної сполуки (Сполука В), PDE5 інгібітор, який можна замістити функціональним залишком або групою, такою як R група, для утворення нових сполук за даним винаходом. [0012] На Фігурі 2 показано Сполуку 1 за даним винаходом. [0013] На Фігурі 3 показано різні сполуки, що представляють варіант здійснення даного винаходу. [0014] На Фігурі 4 показано Сполуку 2 за даним винаходом. [0015] На Фігурі 5 показано різні сполуки, що представляють варіант здійснення даного винаходу. [0016] На Фігурі 6 показано Сполуку 3 за даним винаходом. [0017] На Фігурі 7 показані перетворення Сполуки 3. [0018] На Фігурі 8 показано відому активну сполуку, відомим як варденафіл. [0019] На Фігурі 9 показано метаболіти Сполуки 1. [0020] На Фігурах 10А-10В показано деякі функціональні групи, які можна застосувати для виготовлення фармакокінетично поліпшених сполук за даним винаходом. (From Ostuni et al. Langmuir 2001, 17:5605-5620). Ці функціональні групи ефективні забезпечують стійкість поверхні до білків. [0021] За одним аспектом даний винахід стосується в основному способу регулювання фармакокінетичного та/або фармакодинамічного профілю сполуки шляхом приєднання, щонайменш, одної функціональної одиниці або групи до сполуки для утворення активного агента, причому активний агент має поліпшені фармакокінетичні властивості у порівнянні з немодифікованим, тобто вихідною сполукою. За прикладом варіанту здійснення даного винаходу гідрофобна група, ефір, оліго(етиленглікольна) група або її похідна, амін, сіль амонію, простий амід, амід на основі амінокислоти, краун-ефір, цукор або нітрил, аміно група, оксаламід, саркозиновий залишок, саркозиновий олігомер або саркозинова похідна може приєднатися до сполуки. За переважним варіантом здійснення саркозинову похідну приєднують до сполуки ковалентним зв'язком до N-кінцевого атому азоту саркозинового залишку або олігомера. За іншим переважним варіантом здійснення саркозин приєднують до сполуки ковалентним зв'язком з карбокси-кінця саркозинового залишку або олігомера. За конкретними варіантами здійснення активний агент має поліпшені фізико-хімічні властивості, фармакокінетичні властивості, метаболізм або профіль токсичності. За переважним варіантом здійснення активний агент має задовільну розчинність, нижчу ІС50 та/або значно менше зв'язується білком in vivo у порівнянні із сполукою, яка не має, щонайменш, одного функціонального залишку. [0022] Припускають, що група з формулою С регулює фармакокінетичний та/або фармакодинамічний профіль сполуки та може давати поліпшені 15 фармакокінетичні властивості у порівнянні з немодифікованою, тобто вихідною сполукою. За конкретними варіантами здійснення R4 являє собою активний агент, що має поліпшені фізико-хімічні властивості, фармакокінетичні властивості, метаболізм або профіль токсичності. За переважним варіантом здійснення активний агент має задовільну розчинність, нижчу ІС50 та/або значно менше зв'язується білком in vivo у порівнянні із сполукою, яка не має, щонайменш, одного функціонального залишку. [0023] За іншим аспект даний винахід стосується сполук, що містять, щонайменш, одну функціональну одиницю або групу. За прикладами варіантів здійснення сполуки, які містять, щонайменш, одну приєднану функціональну одиницю або групу, включають, але не обмежуються, хімічних сполуки, наприклад, активні агенти лікарського засобу та біоактивні речовини та білки. Хімічних сполуки включають, але не обмежуються, інгібітори та активатори білків та ферментів (наприклад, фосфодіестерази, такі як PDE5, PDE1, PDE4 та PDE6, кінази, рецептори фактору росту та протеази), та хемотерапевтичні сполуки (наприклад протинеопластичні та протиракові речовини). За прикладом варіанту здійснення даний винахід забезпечує сполуку, яка містить, щонайменш, один функціональний залишок, яким є гідрофобна група, ефір, оліго(етиленглікольна) група або її похідна, амін, сіль амонію, простий амід, амід на основі амінокислоти, краун-ефір, цукор або нітрил. За іншим прикладом варіанта здійснення даний винахід забезпечує сполуку, яка містить, щонайменш, один функціональний залишок, яким є триметилетилендіамін, оксаламід, саркозиновий залишок, саркозиновий олігомер, саркозиновий метаболіт, саркозин-етилендіамін або його розгалужений аналог. За переважним варіантом здійснення саркозиновим придатком є саркозиновий мономер або димер. За переважним варіантом здійснення, щонайменш, одна функціонально одиниця або група приєднується до сполуки ковалентним зв'язком до N-кінцевого атому азоту або ковалентним зв'язком до карбокси-кінця функціональної одиниці або групи. За прикладом варіанта здійснення саркозин приєднується до сполуки ковалентним зв'язком до N-кінцевого атому азоту саркозинового залишку або олігомеру. За іншим переважним варіантом здійснення саркозин приєднується до сполуки ковалентним зв'язком до карбокси-кінця саркозинового залишку або олігомеру. За конкретними варіантами здійснення, щонайменш, одна функціональна одиниця або група приєднується до сполуки для утворення амідної, сульфонамїдної або амінової функціональної групи. За прикладом варіанта здійснення саркозин приєднується до сполуки для утворення амідної, сульфонамїдної або амінової функціональної групи. [0024] Крім того, даний винахід стосується фармацевтичних композицій сполук, які містять, щонайменш, одну функціональну одиницю або групу. За переважним прикладом варіанта здійснення даний винахід забезпечує фармацевтичну композицію, яка містить, щонайменш, один функціональний залишок, яким є триметил-етилендіамін, 95604 16 метальна група, ацетильна група, оксаламід, саркозиновий залишок, саркозиновий олігомер, саркозиновий метаболіт, саркозин-етилендіамін, його розгалужений аналог або саркозинова похідна. [0025] Основним підходом для ідентифікації таких хімічних груп є наступне: 1) ряд хімічних груп, що підлягають оцінюванню, фіксують на твердій поверхні (пласкій або тривимірній) через відповідну групу зчеплення. Групи просторово дискретні, так що кожну можна виміряти окремо, тобто, вони знаходяться на окремому куску матриці; або на окремих кусках; або в окремих лунках мікротитрувального планшета. 2) Потім виконують аналіз або дослід на ряді хімічних груп для визначення наявності у них здатності поліпшення фармакокінетичних властивостей невеликої молекули, якщо тільки хімічна група синтетично додана до молекули. Дослід, що виконують на даному етапі на фіксованих хімічних групах, відповідає досліду, який виконують на терапевтичних засобах з невеликою молекулою, якими виміряють оптимізовану фармакокінетичну властивість. При виконанні досліду звичайно додають придатний реагент з наступним інкубаційним періодом, визначають або виміряють результат для виявлення будь-якої модифікації. Приклади властивостей та досліди наведені нижче. 3) Як тільки хімічну групу або ряд хімічних груп ідентифікують, як такі, що мають потенційно позитивну перевагу за фармакокінетичною властивістю інтересу із застосуванням дослідної системи поверхні, тоді синтезують мішеневу невелику молекулу з цією групою або групами, приєднаними у відповідному положенні, визначеної за допомогою SAR (швидкість специфічної абсорбції). Потім такі сполуки аналізують відповідним стандартним дослідом, що застосовують для вимірювання фармакокінетичної властивості інтересу. [0026] Альтернативний підхід для пласких субстратів полягає у фіксуванні хімічних груп на гранулах, причому кожна гранула забезпечує просторову ізоляцію для кожної групи протягом досліду. [0027] За даним винаходом можна розробити та синтезувати окремі сполуки, наприклад, на основі відомостей існуючих фармакофорів. Даний винахід крім того включає синтез та/або дослідження of бібліотеки of сполуки. Звичайно, бібліотека сполук містить один або більше родинних ядерних фрагментів або фармакофорів, кожний з яких комбінується з одною або більше функціональною групою. Сполуки are просторово направляються або зв'язуються з твердою основою. [0028] Відповідно, даний винахід також включає способи застосування класифікованих сполуки, наприклад у сукупностях на основі поверхні, для ідентифікації функціональних груп, які модифікують фармакофори та впливають на їх фармакокінетичні властивості бажаними способами. [0029] У цілому, класифіковані сукупності модифікованих фармакофорів застосовують способом, при якому: а) виготовляють універсальну бібліотеку модифікаторних сполук функціональних груп лікарського засобу, b) приводять в контакт або комбінують модифікаторні сполуки функціональних груп лікарського засобу з універсальної біб 17 ліотеки з фармацевтичними лікарськими засобами інтересу; та с) визначають силу взаємодії/функції модифікованих сполук лікарського засобу. Визначення на етапі (с) включає оцінювання однієї або більше фізичної та біохімічної властивості. Фізичні властивості включають, наприклад, ліпофільність, розчинність, площу полярної поверхні та подібне. Біохімічних властивості включають, наприклад, потужність, мішеневу специфічність, стабільність, біодоступність та мінімізовану неспецифічну взаємодію з молекулами хазяїна, зокрема, з такими як компоненти сироватки, які б іншим чином блокували сполуки та перешкоджали їм досягнення їх мішеней. Визначення [0030] Для зручності, наведені певні вирази, які застосовують в описі, прикладах та формулі винаходу. [0031] Вираз "функціональні одиниця або група", як застосовують тут, означає залишок, який приєднується до сполуки або білка. Залишок може бути структуральним компонентом молекули, що містить від елемента з одного атома до складної молекули, де складною молекулою є функціональний компонент, або містить множену функціональних фрагментів. За переважним варіантом здійснення функціональний залишок, який буде приєднаний як замісники або заміщений залишок відомих активних сполук, може мати мінімальну кількість донорів водню, велику кількість акцепторів водневого зв'язку та може нести нейтральний електричний заряд. Не міняючи природні функціональні властивості сполуки, в даному описі означає, що модифікація сполуки або білка, що відбувається від приєднання залишку до них, або не знижує бажану хімічну або біологічну активність сполуки або не підвищує будь-який з її шкідливих бічних ефектів, наприклад токсичність. Таку функціональну одиницю або групу можна приєднати до сполуки або білка для заміщення існуючої функціональної одиниці або групи або можна приєднати як залишок до існуючої функціональної одиниці або групи. Функціональну одиницю або групу можна приєднати до сполуки або білка ковалентними зв'язками. Функціональна одиниця або група може бути інертною до зв'язування з білком. [0032] Вираз "гетероатом", як застосовують тут, означає атом будь-якого елементу за виключенням вуглецю або водню. Переважними гетероатомами є бор, азот, кисень, фосфор, сірка та селен. [0033] Вираз "алкіл" відноситься до радикалу насичених аліфатичних груп, включаючи алкільні групи з прямим ланцюгом, алкільні групи з розгалуженим ланцюгом, циклоалкільні (аліциклічні) групи, алкіл заміщені циклоалкільні групи та циклоалкіл заміщені алкільні групи. За переважними варіантами здійснення алкіл з прямим ланцюгом або розгалуженим ланцюгом має 30 або менше атомів вуглецю в своєму скелеті (наприклад, С1С30 для прямого ланцюга, С3-С30 для розгалуженого ланцюга), та більш переважно 20 або менше. Подібним чином, переважні циклоалкіли мають 310 атомів вуглецю в їх кільцевій структурі та більш 95604 18 переважно мають 5, 6 або 7 атомів вуглецю в їх кільцевій структурі. [0034] Якщо кількість атомів вуглецю не зазначена, "нижчий алкіл", як застосовують тут, означає алкільну групу, як зазначено вище, але таку, що має від одного до десяти атомів вуглецю, більш переважно від одного до шести атомів вуглецю в своєї скелетної структурі. Подібним чином, "нижчий алкеніл" та "нижчий алкініл" мають ланцюги з подібною довжиною. Переважними алкільними групами є нижчі алкіли. За переважними варіантами здійснення замісником, зазначеним в даному описі як алкіл, є нижчий алкіл. [0035] Вираз "аралкіл", як застосовують тут, відноситься до алкільної групи, заміщеної арильною групою (наприклад, ароматичною або гетероароматичною групою). [0036] Вирази "алкеніл" та "алкініл" відносяться до ненасичених аліфатичних груп, аналогічних за довжиною та можливим заміщенням на алкіли, описані вище, але такі, що містять, щонайменш, один подвійний або потрійний зв'язок, відповідно. [0037] Вираз "арил", як застосовують тут, включає 5-, 6- та 7-членне однокільцеві ароматичні групи, які можуть включати від 0 до 4 гетероатомів, наприклад, бензол, антрацен, нафталін, пірен, пірол, фуран, тіофен, імідазол, оксазол, тіазол, тріазол, піразол, піридин, піразин, піридазин, піримідин та подібне, такі арильні групи, що мають гетероатоми в кільцевій структурі, можуть також згадуватися як "арильні гетероцикли" або "гетероароматичні." Ароматичне кільце може бути заміщеним в одній або більше кільцевих положень такими замісниками, які описані вище, наприклад, галоген, азид, алкіл, аралкіл, алкеніл, алкініл, циклоалкіл, гідроксил, алкоксил, аміно, нітро, сульфгідрил, іміно, амідо, фосфонат, фосфінат, карбоніл, карбоксил, силіл, простий ефір, алкілтіо, сульфоніл, сульфонамідо, кетон, альдегід, складний ефір, гетероцикліл, ароматичні або гетероароматичні фрагменти, -CF3, -CN або подібне. Вираз "арил" також включає поліциклічні кільцеві системи, що мають два або більше циклічних кілець, в яких два або більше атомів вуглецю є спільними для двох сусідніх кілець (кільця є "злитими кільцями"), де, щонайменш, одне з кілець є ароматичним, наприклад, іншими циклічними кільцями можуть бути циклоалкіли, циклоалкеніли, циклоалкініли, арили та/або гетероцикліли. [0038] Вирази орто, мета та пара застосовують до 1,2-, 1,3- та 1,4-дизаміщених бензолів, відповідно. Наприклад, назви 1,2-диметилбензол та ортодиметилбензол є синонімами. [0039] Вирази "гетероцикліл" або "гетероциклічна група" відноситься до 3- - 10-членних кільцевих структур, більш переважно до 3- - 7-членних кільць, які включають один - чотири гетероатоми. Гетероцикли також можуть бути поліциклами. Гетероциклільни групи включають, наприклад, тіофен, тіантрен, фуран, піран, ізобензофуран, хромен, ксантен, феноксатіїн, пірол, імідазол, піразол, ізотіазол, ізоксазол, піридин, піразин, піримідин, піридазин, індолізин, ізоіндол, індол, індазол, пурин, хінолізин, ізохінолін, хінолін, фталазин, нафтіридин, хіноксалін, хіназолін, цинолін, птерідин, 19 карбазол, карболін, фенантридин, акрідин, піримідин, фенантролін, феназин, фенарсазин, фенотіазин, фуразан, феноксазин, піролідин, оксолан, тіолан, оксазол, піперидин, піперазин, морфолін, лактони, лактами, такі як азетідинони та піролідинони, султами, султани та подібне. Гетероциклічне кільце може бути заміщеним в одному або більше положенні такими замісниками, що описані вище, як наприклад, галоген, алкіл, аралкіл, алкеніл, алкініл, циклоалкіл, гідроксил, аміно, нітро, сульфгідрил, іміно, амідо, фосфонат, фосфінат, карбоніл, карбоксил, сіліл, ефір, алкілтіо, сульфоніл, кетон, альдегід, складний ефір, гетероцикліл, ароматичний або гетероароматичний компонент, -CF3, -CN або подібне. [0040] Вирази "поліцикліл" або "поліциклічна група" відноситься до двох або більше кілець (наприклад, циклоалкіли, циклоалкеніли, циклоалкініли, арили та/або гетероцикліли,) в яких два або більше атомів вуглецю є загальними для двох сусідніх кілець, наприклад, кільцями є "злиті кільця". Кільця, які з'єднані через не сусідні атоми називають "з'єднаними містковим зв'язком" кільцями. Кожне з кілець поліциклу може бути заміщеним такими замісниками, які описані вище, як наприклад, галоген, алкіл, аралкіл, алкеніл, алкініл, циклоалкіл, гідроксил, аміно, нітро, сульфгідрил, іміно, амідо, фосфонат, фосфінат, карбоніл, карбоксил, силіл, простий ефір, алкілтіо, сульфоніл, кетон, альдегід, складний ефір, гетероцикліл, ароматичний або гетероароматичний компонент, -CF3, -CN або подібне. [0041] Як застосовують тут, вираз "нітро" означає -NO2; вираз "галоген" означає - F, -СІ, -Вr або І; вираз "сульфгідрил" означає -SH; вираз "гідроксил" означає -ОН; а вираз "сульфоніл" означає SO2-. [0042] Вирази "амін" та "аміно" є прийнятими в даній галузі та відносяться до незаміщених та заміщених амінів, наприклад, до компоненту, який можна представити загальною формулою: де R, R' та R" кожний незалежно представляє групу, дозволену правилами валентності, переважно Н, алкіл, алкеніл, алкініл, аралкіл, арил та гетероциклічну групу. [0043] Вираз "ациламіно" є прийнятим в даній галузі та відноситься до компоненту, який можна представити загальною формулою: де R та R' зазначені вище. [0044] Вираз "амідо" є прийнятим в даній галузі як аміно-заміщений карбоніл та включає компонент, який можна представити загальною формулою: 95604 20 де R та R' зазначені вище. Переважні варіанти здійснення аміду не будуть включати іміди, які можуть бути не стабільними. [0045] Вираз "алкілтіо" відноситься до алкільної групи, як зазначено вище, що має радикал сірки, що приєднується. За переважними варіантами здійснення "алкілтіо" компонент представлений одним з -S-алкілу, -S-алкенілу, -S-алкінілу та -S(CH2)m-R8, де m та R8 зазначені вище. Представники алкілтіо груп включають метилтіо, етилтіо та подібне. [0046] Вираз "карбоніл" прийнятий в даній галузі та включає такі фрагменти, які можна представити загальною формулою: де X являє собою зв'язок або представляє кисень або сірку, a R та R' зазначені вище. Де X являє собою кисень, a R або R' не є воднем, формула представляє "складний ефір". Де X являє собою кисень, a R зазначений вище, компонент згадують тут як карбоксильну групу, та зокрема де R являє собою водень, формула представляє "карбонову кислоту". Де X являє собою кисень, та R' являє собою водень, формула представляє "форміат". У цілому, де атом кисню згаданої вище формули заміщений сіркою, формула представляє "тіолкарбонільну" групу. Де X являє собою сірку, a R або R' не є воднем, формула представляє "тіольний складний ефір." Де X являє собою сірку, a R являє собою водень, формула представляє "тіолкарбонову кислоту." де X являє собою сірку, a R' являє собою водень, формула представляє "тіолформіат." З іншого боку, де X являє собою зв'язок, a R не є воднем, зазначена вище формула представляє "кетонну" групу. Де X являє собою зв'язок, a R являє собою водень, зазначена вище формула представляє "альдегідну" групу. [0047] Вирази "алкоксил" або "алкокси", як застосовують, тут відноситься до алкільної групи, як зазначено вище, яка має кисеневий радикал, що приєднується до неї. Представлені алкоксильні групи включають метокси, етокси, пропілокси, трет-бутокси та подібне. "Ефір" являє собою два вуглеводню, ковалентно зв'язаних киснем. [0048] Вираз "сульфонат" є прийнятим в даній галузі та включає компонент, який можна представити загальною формулою: в який R41 являє собою електронну пару, водень, алкіл, циклоалкіл або арил. [0049] Вирази трифліл, тозил, мезил та нонафліл прийняті в даній галузі та відноситься до трифторметансульфонільну, ртолуолсульфонільну, метансульфонільну та нонафторбутансульфонільну групи, відповідно. Вирази трифлат, тозилат, мезилат та нонафлат прийняті в даній галузі та відносяться до трифторметансульфонатного складного ефіру, р 21 толуолсульфонатного складного ефіру, метансульфонатного складного ефіру, та нонафторбутансульфонатного складного ефіру функціональних груп та молекул, що містять зазначені групи, відповідно. [0050] Абревіатури Me, Et, Ph, Tf, Nf, Ts, Ms представляють метил, етил, феніл, трифторметансульфоніл, нонафторбутансульфоніл, ртолуолсульфоніл та метансульфоніл, відповідно. Більш повний список абревіатур, що застосовуються хіміками-органіками в даній галузі, з'являється у першому випуску кожного тому журналу з органічної хімії; цей список звичайно представлений в таблиці, озаглавлений як Стандартний список абревіатур. Абревіатури зазначеного списку та усі абревіатури, що застосовуються хімікамиорганіками в даній галузі, включені посиланням. [0051] Вираз "сульфат" прийнятий в даній галузі та включає компонент, який можна представити загальною формулою: в якій R41 зазначений вище. [0052] Вираз "сульфоніламіно" прийнятий в даній галузі та включає компонент, який можна представити загальною формулою: [0053] Вираз "сульфамоїл" прийнятий в даній галузі та включає компонент, який можна представити загальною формулою: [0054] Вираз "сульфоніл", як застосовують тут, відноситься до компоненту, який можна представити загальною формулою: в якому R44 вибраний з групи, що містить водень, алкіл, алкеніл, алкініл, циклоалкіл, гетероцикліл, арил або гетероарил. [0055] Вираз "сульфоксидо" як застосовують тут, відноситься до компоненту, який можна представити загальною формулою: в якому R44 вибраний з групи, що містить водень, алкіл, алкеніл, алкініл, циклоалкіл, гетероцикліл, аралкіл або арил. [0056] "Селеноалкіл" відноситься до алкільної групи, що має заміщену селено групу, приєднану 95604 22 до неї. Приклади "селеноефірів", які можна замістити алкілом, вибрані з одного з -Se-алкілу, -Seалкенілу, -Se-алкінілу та -Se-(CH2)m-R7, m та R7 зазначені вище. [0057] Аналогічні замісники можна виконати до алкенільних та алкінІльних груп для утворення, наприклад, аміноалкенілів, аміноалкінілів, амідоалкенілів, амідоалкінілів, іміноалкенілів, іміноалкінілів, тіоалкенілів, тіоалкінілів, карбоніл-заміщених алкенілів або алкінілів. [0058] Як застосовують тут, визначення кожного виразу, наприклад, алкіл, m, n та подібне, коли він з’являється більш ніж один раз у будь-якій структурі, призначений бути незалежним від його визначення у другому місці тієї самої структури. [0059] Буде зрозуміло, що "замісник" або "заміщений" включає не визначену безпосередньо умову, що таких замісник являє собою, у відповідності за дозволом валентності, заміщений атом та замісник, та що замісник дає стабільну сполуку, наприклад, яка спонтанно не піддається перетворенню, такому як перестановка, циклізація, елімінування та подібне. [0060] Як застосовують тут, вираз "заміщений" передбачає включати усі дозволені замісники органічних сполук. У широкому аспекті дозволені замісники включають ациклічні та циклічні, розгалужені та нерозгалужені, карбоциклічні та гетероциклічні, ароматичні та неароматичні замісники органічних сполук. Ілюстративні замісники включають, наприклад, описані вище. Придатні замісники можуть бути одним або більше та однаковими або різними для відповідних органічних сполук. За даним винаходом гетероатоми, такі як азот, можуть мати водневі замісники та/або будь-які придатні замісники органічних сполук, описані тут, як відповідають валентностям гетероатомів. Даний винахід не призначений бути обмеженим будьяким способом придатними замісниками органічних сполук. [0061] Вираз "захисна група", як застосовують тут, означає тимчасові замісники, які захищають потенційно реактивні функціональні групи від небажаних хімічних перетворень. Приклади таких захисних груп включають складні ефіри карбонових кислот, сілільні ефіри спиртів, ацеталі та кеталі альдегідів та кетонів, відповідно. Галузь хімії захисних груп роздивлялася (Greene, T. W.; Wuts, n P.G.M. Protective Groups in Organic Synthesis, 2 ed.; Wiley: New York, 1991). [0062] Як застосовують тут, вираз "метаболіт" відноситься до сполуки, яка перетворюється при обміні речовин в організмі. Наприклад, за варіантом здійснення даного винаходу Сполука 1 (Фігура 2) перетворюється при обміні речовин в організмі на метаболіти, показані на Фігурі 9. [0063] Даний винахід також включає метаболіти будь-якої із зазначених вище сполук. Переважні метаболіти включають сполуки, що мають формули: 23 95604 24 або [0064] Таблиці 1-3 наводять певні біологічні та фармакологічні властивості зазначених вище модифікованих сполук А. Таблиця 3 включає індекс селективності до деяких PDE. Зв'язування з білком, проникність та розчинність зазначених вище сполук сформульовані в Таблиці 2. Сполуки даного винаходу [0065] Певні сполуки за даним винаходом можуть існувати в конкретних геометричних або стереоізомерних формах. Даний винахід передбачає усі такі сполуки, включаючи цис- та транс-ізомери, R- та (S-енантіомери, діастереомери, (D)-ізомери, (L)-ізомери, їх рацемічні суміші та їх інші суміші, що знаходяться у межах даного винаходу. В заміснику, такому як алкільна група, можуть бути присутніми додаткові асиметричні атоми вуглецю. Усі такі ізомери, а також їх суміші, призначені бути включеними в даний винахід. Наприклад, за одним варіантом здійснення сполука або фармацевтична композиція являє собою перетворення Сполуки 2, яка має структуру: [0067] Крім того, якщо, наприклад, конкретний енантіомер сполуки за даним винаходом є бажаним, його можна виготовити асиметричним синтезом або утворенням похідної з хіральною добавкою, де утворену діастереомерну суміш розділяють, а добавлену групу відщеплюють для забезпечення чистих бажаних енантіомерів. Альтернативно, якщо молекула містить основну функціональну групу, таку як аміно, або кислотну функціональну групу, таку як карбоксильну, діастереомерні солі утворюються з придатних оптично активних кислоти або основи, з наступним розчиненням діастереомерів, утворених фракційною кристалізацією або хроматографічними засобами, добре відомими в даній галузі, та послідовним відновленням чистих енантіомерів. [0068] Передбачені еквіваленти сполук, описаних вище, включають сполуки які іншім чином їм відповідають, та які мають однакові загальні властивості їх (наприклад, функція анальгетиків), де зроблено одну або більше простих варіацій замісників, які не впливають несприятливо на ефективність сполуки у зв'язуванні з сигма рецепторами. У цілому, сполуки за даним винаходом можна виготовити способами, ілюстрованими в загальних схемах реакції, як, наприклад, в описаних нижче, або їх модифікаціями звикористанням готових придатних стартових матеріалів, реагентів та традиційних методик синтезу. В цих реакціях також можливо застосування варіантів, які відомі, але не згадуються тут. [0069] Для цілей даного винаходу хімічні елементи ідентифікують у відповідності за періодичною таблицею елементів, версією CAS (Хімічна Реферативна Служба), Handbook of Chemistry та Physics, 67th Ed., 1986-87, внутрішня частина обкладинки. [0070] За одним варіантом здійснення даний 1 винахід забезпечує сполуку формули А : [0066] Наступні ізомери цієї сполуки включені в даний винахід: 25 O R1 N A B D R2 HN O 95604 N N E R3 (А) або фармацевтично прийнятну сіль, стереоі1 зомер або її гідрат, де R являє собою нижчий алкіл; R та R незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; А являє собою N або С-Н; 4 В являє собою N, С-Н, C-(SO2-R ) або C-CO4 R; 4 D являє собою N, С-Н, C-(SO2-R ) або C-CO4 R; Е являє собою N або С-Н; де тільки один з А, В або Е може бути N, а 4 один з В або D являє собою C-(SO2-R ) або C-CO4 R; 4 R являє собою групу, що має формулу: 5 6 7 8 в якій кожний R , R , R та R незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та 6 5 додатково або альтернативно R та R разом 6 7 утворюють 5- або 6-членне кільце, або R та R 9 разом утворюють 3-6 членне кільце; R незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбоніл та алкілтіо; 8 9 альтернативно R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце; n-1-4; та m-1-6. За переважним варіантом 2 3 здійснення R та R незалежно вибрані з нижчого алкілу. [0071] Припускають, що група, яка має формулу С регулює фармакокінетичний та/або фармакодинамічний профіль сполуки та може поліпшувати фармакокінетичні властивості у порівнянні з немодифікованою, тобто вихідною сполукою. За конк4 ретними варіантами здійснення R являє собою активний агент, що має поліпшені фізико-хімічні властивості, фармакокінетичні властивості, метаболізм або профіль токсичності. За переважним варіантом здійснення активний агент має кращу розчинність, нижчу ІС50 та/або значно менше зв'язування з білком in vivo у порівнянні із сполукою яка не має, щонайменш, одного функціонального залишку. 26 [0072] Сполуки за даним винаходом, які модифіковані шляхом приєднання до них, щонайменш, одного залишку формули С, забезпечують модифіковані фармакокінетичні властивості, включаючи модифіковане неспецифічне in vivo зв'язування з білком. Такі оптимальні фармакокінетичні властивості не ставлять під загрозу ні селективність, ні активність модифікованої сполуки. [0073] Сполуки за даним винаходом можна розробити утримуючими функціональну одиницю або групу, або існуюча сполука(и) може бути модифікована шляхом приєднання до неї, щонайменш, одної функціональної одиниці або групи, тобто залишку; такі останні сполуки включають речовини, які являють собою хімічно або біологічно активні молекули. Такі сполуки також включають терапевтичні лікарські засоби або білки, бажана активність яких відома фахівцям в даній галузі. Потенційні сполуки ідентифікуються фахівцем за присутністю функціональних груп, які забезпечують бажані in vivo характеристики активності лікарського засобу, розчинність та придатне зв'язування з білком, необхідне для терапевтичної ефективності при мінімальній терапевтично ефективній кількості сполуки. Додаткові властивості сполуки, що враховуються, включають оральну абсорбцію, метаболізм, здатність подолання гемоенцефалічного бар'єру та токсичність сполуки. Потенційні сполуки для модифікації шляхом приєднання, щонайменш, одного функціонального залишку, взаємозамінно згадуються тут як "вихідні" сполуки. [0074] Вихідні сполуки містять основну структуру, каркас або скелет, тобто фармакофор, до якого приєднуються замісники, типово залишки, які не потрібні для хімічної або біологічної активності сполуки, але які можуть впливати на властивості, включаючи, але не обмежуючись, розчинність та/або in vivo зв'язування з білком. Наприклад, потенційні вихідні сполуки можна вибрати для модифікації із залишками за даним винаходом за присутністю замісника, наприклад, піперазинової групи або морфолінової групи. Група замісника сама може бути заміщеною залишком або альтернативно, бути заміщеною залишком для утворення сполуки за даним винаходом. [0075] Крім того, сполуки даного винаходу можна розробити de novo. Наприклад, скелети, що містять функціональні групи, які забезпечують стійкість до зв'язування з білком, можна вибрати як вихідну точку для розробки лікарського засобу. Альтернативно такі скелети можуть бути основою для комбінаційних бібліотек для дослідження сполук інтересу. [0076] Сполуки за даним винаходом, які модифіковані шляхом приєднання до них, щонайменш, одного залишку забезпечують модифіковані фармакокінетичні властивості, включаючи модифіковане неспецифічне in vivo зв'язування з білком. Такі оптимальні фармакокінетичні властивості не порушують ні селективність, ні активність модифікованої сполуки. Фармакокінетично поліпшені сполуки даного винаходу переважно дозволяють вводити мінімальну ефективну кількість сполуки для досягнення бажаного терапевтичного ефекту не 27 зв'язаної сполуки, таким чином знижуючи кількість дозування (та можуть поліпшати дотримання пацієнтом схеми прийому). Сполуки забезпечують поліпшені фармакокінетичні властивості над вихідною сполукою завдяки модифікації неспецифічного in vivo зв'язування сполуки з білком. Приєднання, щонайменш, одного залишку може знизити неспецифічне зв'язування з білком деяких сполук. Інші поліпшені фармакокінетичні властивості сполук за даним винаходом включають розчинність, оральну придатність, метаболізм, здатність подолання гемоенцефалічного бар'єру та забезпечення бажаного тканинного розподілу, тобто у мішеневій тканині(ах). [0077] Модифікація зв'язування з білком заснована на поверхневій технології, тобто виготовлення та дослідження поверхонь на їх здатність протидіяти абсорбції білків з розчину. Поверхні, які є стійкими до абсорбції білків з розчину, відомі фахівцю в даній галузі як "стійкі до білка" поверхні. Функціональні групи можна досліджувати для ідентифікації групи(груп), що присутні на стійких до білка поверхонь, як описано в, наприклад, Chapman et al. Surveying for Surfaces that Resist the Adsorption of Proteins, J. Am. Chem. Soc. 2000, 122:8303-8304; Ostuni et al. A Survey of StructureProperty Relationships of Surfaces that Resist the Adsorption of Protein, Langmuir 2001, 17:5605-5620; Holmlin, et al. Zwitterionic SAMs that Resist Nonspecific Adsorption of Protein from Aqueous Buffer, Langmuir 2001, 17:2841-2850; and Ostuni et al. S elf- Assembled Monolayers that Resist the Adsorption of Proteins and the Adhesion of Bacterial and Mammalian Cells, Langmuir 2001, 17:6336-6343. [0078] За переважними прикладами варіантів здійснення даного винаходу функціональні залишки включають, але не обмежуються, гідрофобну групу, ефір, оліго(етиленглікольну) групу або її похідну, амін, сіль амонію, простий амід, амід на основі амінокислот, краун-ефір, цукор або нітрил та інші придатні функціональні групи, наведені нижче, як описано у роботі Ostuni et al. Langmuir 2001, 17:5605-5620, вміст якої включений в даний опис в усій її повноті, специфічно функціональні групи, які були зокрема ефективні при перетворення поверхонь на такі, що не абсорбують білок, тобто стійкі до білка. На Фігурах 10А-10В показані деякі з різних функціональних груп, які можна приєднати до каркасів або скелетів активних сполук для утворення сполук за даним винаходом. [0079] Хімічні сполуки за даним винаходом містять мінливий основний каркас або скелетну структуру відомої активної сполуки, тобто вихідної сполуки, для якої модифікації можна здійснити шляхом приєднання, щонайменш, одного замісника, який являє собою, щонайменш, одну функціональну групу, переміщенням та/або заміщенням існуючої неосновної групи(груп) замісника, як обговорювалося вище. Мінливий основний каркас або скелетну структуру згадують тут як "А" або як радикал активної сполуки, каркас або радикал якої може утворювати ковалентні зв'язки із, щонайменш, одним функціональним залишком. Скелет або каркас хімічно або біологічно активних молекул, включаючи відомі терапевтичні лікарські за 95604 28 соби або білки, що мають бажану активність, включають, але не обмежуються, скелетні структури циклічних гуанозин-3',5'-монофосфатфосфодіестераз, cGMP PDE, наприклад cGMP PDE5, як описано, наприклад, в опублікованих РСТ заявках WO 00/24745 (Bunnage et al.), WO 01/27112 (Allerton et al), WO 02/074312 (Allerton et al.) та патентах США №№ 6440982 Bl (Maw et al.) та 6583147 Bl (Yoo et al.). [0080] За одним варіантом здійснення сполука має наступну формулу: 5 6 7 8 в якій кожний R , R , R та R незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та 6 5 додатково або альтернативно R та R разом 6 7 утворюють 5- або 6-членне кільце, або R та R 9 разом утворюють 3-6-членне кільце; R незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкіл8 9 тіо; альтернативно R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6членне кільце. [0081] Переважно функціональна група, що приєднується до сульфонільної групи, являє собою саркозинову похідну або олігомер. Переважний варіант здійснення має формулу: 1 2 3 в якій R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо. [0082] За найбільш переважним варіантом здійснення каркас або скелет можуть бути PDE5 інгібітором, що має формулу (В): 29 95604 де R представляє, щонайменш, один функціональний залишок, який заміщує оригінальний піперазин приєднуючись до сірки вихідної сполуки ковалентним зв'язком. 4 [0083] В сполуці А або В, R може бути сполукою, що має формулу С: 5 6 7 30 4 [0086] За іншим варіантом здійснення R являє собою 2-метиламіно-2-триметил-пропіонамід, утворюючи сполуку, що має формулу III: 8 де кожний R , R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та дода6 5 тково або альтернативно R та R разом утворю6 7 ють 5- або 6-членне кільце, або R та R разом 9 утворюють 3-6-членне кільце; R незалежно вибраний з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; альтернативно R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце; n-1-4; a m-1-6. 4 [0084] За переважним варіантом здійснення R являє собою метил-аміно-диметилацетамід, утворюючи сполуку, що має формулу І: . [0087] За іншими переважними варіантами 4 здійснення m являє собою 1 або 2 для R (Формула С), який приєднується до Сполуки А. Переважно, п являє собою 1. [0088] За наступним варіантом здійснення сполука має наступну формулу: 1 . 4 [0085] За іншим варіантом здійснення R являє собою метил-аланін-диметиламід, утворюючи сполуку, що має формулу II: 2 3 5 6 7 8 9 10 11 в якій R , R , R R , R , R , R , R , R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; та додатково або альтернативно 6 5 8 10 R та R , або R та R разом утворюють 5- або 66 7 10 11 членне кільце, або R та R , або R та R разом 9 1 утворюють 3-6-членне кільце; a R та R разом з азотом, до якого вони приєднуються, утворюють 5або 6-членне кільце. [0089] Для зазначеного вище варіанту здійс6 7 10 11 нення переважно R , R , R , та R кожний являє собою водень. Більш переважно саркозиновий димер приєднується до сульфонільної групи, а сполука має формулу: 12 31 1 2 3 в якій R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщений одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо. За , найбільш переважним варіантом здійснення 1 2 3 R є етилом, R є метилом, a R є пропілом. [0090] Таблиця 1 підсумовує певні властивості вище зазначених модифікованих сполук В, включаючи ІС50 та CLogP. [0091] Таблиця 2 підсумовує певні властивості модифікованих сполук, включаючи зв'язування з білком, розчинність та неспецифічне зв'язування. Індекс селективності до декількох PDE вище зазначених сполук сформульовані в Таблиці 3. [0092] Даний винахід стосується способу регулювання фармакокінетичних та/або фармакодинамічних властивостей сполуки, що містить: приєднання, щонайменш, одного функціонального залишку, де, щонайменш, один функціональний залишок знижує неспецифічне зв'язування з білком, до відомої активної сполуки шляхом (а) переміщенням неосновного залишку, тобто варіантного каркасу, сполуки із, щонайменш, одним функціональним залишком, або (b) заміщенням неосновного залишку сполуки, щонайменш, одним функціональним залишком, що таким чином поліпшує фармакокінетичні властивості сполуки. [0093] За переважним варіантом здійснення зазначеного вище способу функціональний залишок, який буде приєднуватися як замісник або як заміщений залишок, містить мінімальну кількість донорів водню, велику кількість акцепторів водневого зв'язку та несе нейтральний електричний заряд. [0094] У зазначеному вище способі, щонайменш, один функціональний залишок, який приєднується до відомої активної сполуки, може бути гідрофобною групою, ефіром, оліго(етиленглікольною) групою або її похідною, аміном, сіллю амонію, простим амідом, амідом на 95604 32 основі амінокислот, краун-ефіром, цукром або нітрилом, амінною групою, оксаламідом, саркозиновим залишком, саркозиновою похідною або саркозиновим олігомером. За переважним варіантом здійснення фармакокінетичною властивістю є неспецифічне зв'язування з білком. [0095] Даний винахід стосується способу регулювання фармакокінетичних та/або фармакодинамічних властивостей сполуки, що містить: приєднання залишку від групи, що містить гідрофобну групу, ефір, оліго(етиленглікольну) групу або її похідну, амін, сіль амонію, простий амід, амід на основі амінокислот, краун-ефір, цукор або нітрил, амінну групу, оксаламід, саркозиновий залишок, саркозинову похідну або саркозиновий олігомер, до відомої активної сполуки для утворення другої сполуки. [0096] Загалом, зв'язування з білком оцінюють вимірюванням здатності молекул даного винаходу зв'язуватися з одним або більше компонентом сироватки людини або його імітаціями. За одним варіантом здійснення придатні функціональні залишки можна ідентифікувати дослідженням поверхонь, що містять такі залишки, на їх здатність до стійкості проти абсорбції компонентів сироватки, включаючи, але не обмежуючись білки сироватки та переважно білки сироватки людини. Кандидатні залишки можна досліджувати безпосередньо приєднанням їх до твердої конструкції та аналізувати конструкцію на стійкість до білка. Альтернативно, кандидатні залишки включені в або зв'язані з молекулами фармацевтичного інтересу. Такі сполуки можна синтезувати на твердій конструкції або зв'язати з твердою конструкцією після синтезу. У не обмежуючому прикладі досліду безпосереднього зв'язування фіксовані кандидатні функціональні залишки або молекули, що включають такі залишки, аналізують на їх здатність зв'язувати компоненти сироватки. Компоненти сироватки можна помітити сигнальним компонентом для визначення або можна застосовувати мічений вторинний реагент, який зв'язується з такими компонентами сироватки. [0097] Поверхні, стійкі до абсорбції білків з розчину, відомі як "стійкі до білків" поверхні. Функціональні групи можна дослідити для ідентифікації групи(груп), що присутні в поверхнях, стійких до білків, як описано, наприклад, у Chapman et al. Surveying for Surfaces that Resist the Adsorption of Proteins, J. Am. Chem. Soc. 2000, 122:8303-8304; Ostuni et al. A Survey of Structure-Property Relationships of Surfaces that Resist the Adsorption of Protein, Langmuir 2001, 17:5605-5620; Holmlin, et al. Zwitterionic SAMs that Resist Nonspecific Adsorption of Protein from Aqueous Buffer, Langmuir 2001, 17:2841-2850; and Ostuni et al. SelfAssembled Monolayers that Resist the Adsorption of Proteins and the Adhesion of Bacterial and Mammalian Cells, Langmuir 2001, 17:6336-6343. [0098] При ідентифікації функціонального залишку, який забезпечує таку стійкість до білків, фахівець в даній галузі легко визначить придатну хімічну структуру або скелет відомої біологічно або хімічно активної сполуки, до якої функціональні залишок можна приєднати або заміщенням функ 33 ціональної групи активної сполуки, або заміщенням неосновної функціональної групи активної сполуки. Наприклад, як обговорювалося вище, присутність піперазинової групи в сполуці покаже, що таку групу можна або перемістити або замістити функціональним залишком. Фахівець в даній галузі, наприклад, медичний хімік, розпізнає інші придатні групи в відомих активних сполуках, які можна перемістити або замістити, щонайменш, одним функціональним залишком. Відповідно, комбінаторну бібліотеку сполук можна створити як описано нижче, де сполуки є модифікованими сполуками, що містять кон'югат активної ділянки сполуки (основний скелет сполуки, що має конкретну бажану активність), наприклад, сполука А та, щонайменш, один функціональний залишок, що приєднується до неї, де кожний кон'югат має різний функціональний залишок, що приєднується до нього, наприклад, залишки, що мають формулу С, де R група вибрана з різних груп, описаних тут, або різних функціональних груп, показаних на Фігурах 10А -10В. Відповідно, бібліотеку можна застосовувати для дослідження ряду різних функціональних залишків на поліпшені фармакокінетичні та/або фармакодинамічні властивості, включаючи неспецифічне зв'язування з білком модифікованої сполуки. [0099] За переважними варіантами здійснення тверду конструкцію вибирають або модифікують для мінімізації її взаємодії з компонентами сироватки. Приклади таких конструкцій та дослідних систем описані в міжнародних заявках на патенти WO 02/48676, WO 03/12392, WO 03/18854, WO 03/54515, які включені в даний опис шляхом посилань. Альтернативно, молекули даного винаходу можна змішати з одним або більше компонентом сироватки в рідкій фазі та визначити кількість незв'язаних молекул. [0100] Аналіз прямого зв'язування можна також виконати в рідкій фазі. Наприклад, аналізовані сполуки можна змішати з одним або більше компонентом сироватки в рідкій фазі та визначити незв'язані молекули. [0101] В прикладі переважного варіанту здійснення молекули, що мають знижене зв'язування з білком, ідентифікують наступним чином: самоагрегований моношар тіолових молекул з ангідридними групами на кінці утворюють на золотій поверхні. Ряд невеликих молекул з амінними групами на кінці та з групами, що розроблені для стійкості до зв'язування з альбуміном, наприклад, на іншому кінці, потім приєднують до поверхні шляхом реакції між аміном та ангідридом. Ряд молекули наносять на просторово роздільні ділянки на золотій поверхні для створення серії молекул, які могли б бути стійкими до зв'язування з білком. Потім серію піддають дії розчину, що містить флуоресцентно мічений альбумін. Після придатного інкубаційного періоду золоту поверхню промивають та вивчають на флуоресцентному сканері. Фіксовані хімічні групи, що зв'язується з альбуміном, будуть ідентифіковані за присутністю флуоресцентного сигналу; групи, які стійкі до зв'язування з альбуміном, будуть мати низьку флуоресцентність в тієї частині серії. Якщо флуоресцентний білок не доступний, 95604 34 тоді антитіла до білка інтересу в комбінації з флуоресцентними вторинними антитілами можна застосувати для визначення зв'язування білка з хімічними групами. Якщо антитіло не доступне, тоді для ідентифікації присутності білка на окремих елементах в серії можна застосовувати спосіб визначення без мітки, такий як поверхневий плазмонний резонанс (SPR) або мас-спектрометрія MALDI (лазерна іонізація та дезорбція з матриці). SPR також має перевагу забезпечення кінетичної інформації у зв'язуванні білка з хімічними групами. [0102] Застосування цієї системи не обмежується альбуміном; будь-який білок фармакокінетичного інтересу можна аналізувати на потенційне зв'язування. Наприклад, білки крові, що зв'язують невеликі молекули, такі як а-кислотнй глікопротеїн (AAG, AGP) та ліпопротеїни, можна піддати серії та визначенню зв'язування з білком. [0103] За варіантом здійснення даного винаходу хімічні групи можна ідентифікувати як стійкі до зв'язування з Р-глікопротеїном (PGP) та тому такі, що мають потенціал для зниження продукту реакції, коли вони приєднуються до невеликої молекули терапевтичного засобу. Це зокрема важливо для розробки протиракових лікарських засобів, що забезпечують ефективне лікування при розвитку стійкості до ряду лікарських засобів (MDR). [0104] Спосіб також можна застосувати для ідентифікації хімічних груп, які стійкі до зв'язування з білками, такими як тромбін, протитромбін та Фактор Ха, та тому мають потенціал для регулювання коагуляції. [0105] Спосіб також можна застосувати для ідентифікації груп, які поліпшують терапевтичні засоби, які розроблені як допоміжні або заміщені терапії, де зв'язування з білком та фармакокінетичні властивості дуже важливі, наприклад, гормони та білки, що їх зв'язують, та стероїди та білки, що їх зв'язують, такі як тестостерон та глобулін, що зв'язує статеві гормони (SHBG). [0106] За іншим аспектом даний винахід стосується способу регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки, що містить етапи, при яких: приєднують першу сполуку, вибрану з групи, що містить будь-які з вище зазначених відомих структур або скелетів активних сполук, включаючи, але не обмежуючись, активні агенти лікарського засобу, біоактивні речовини, білки та хімікат, до залишку, представленого формулою С для утворення другої сполуки, , 5 6 7 8 9 де R , R , R , R та R можуть бути Н та нижчим алкілом, де нижчий алкіл може бути заміщеним галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; a 6 5 R та R разом утворюють 5- або 6-членне кільце, 6 7 або R та R разом утворюють 3-6 членне кільце; 35 8 95604 9 36 або її фармацевтично прийнятна сіль, стереоі1 2 3 зомер або гідрат, де R , R та R незалежно вибрані з Н, нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо, при якому: 4 приєднують R , що має формулу С: , 5 6 7 8 9 де R , R , R , R та R можуть бути Н та нижчим алкілом, де нижчий алкіл може бути заміщеним галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо; a 6 5 R та R разом утворюють 5- або 6-членне кільце, 6 7 або R та R разом утворюють 3-6-членне кільце; 8 9 R та R разом з азотом, до якого вони приєднуються утворюють 5- або 6-членне кільце; n являє собою 1-4; a m являє собою 1-6, для утворення другої сполуки. [0110] За конкретними варіантами здійснення даний винахід стосується вище згаданого способу, де друга сполука має формулу: 1 2 1 R та R разом з азотом, до якого вони приєднуються, утворюють 5- або 6-членне кільце; n являє собою 1-4; a m являє собою 1-6. [0107] За певними варіантами здійснення даний винахід стосується вище згаданого способу, де m являє собою 1 або 2. [0108] За конкретними варіантами здійснення даний винахід стосується вище згаданого способу, де n являє собою 1. [0109] За конкретними варіантами здійснення даний винахід стосується способу регулювання фармакокінетичної та/або фармакодинамічної 1 властивості сполуки, де сполука має формулу А : 2 3 де R , R та R незалежно вибрані з Н, нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо. [0111] За певними варіантами здійснення даний винахід стосується вище згаданого способу, де друга сполука має формулу: 3 де R , R та R незалежно вибрані з Н та нижчого алкілу, де нижчий алкіл може бути факультативно заміщеним одним або більше галогеном, нижчим алкокси, гідрокси, CN, NO2, аміно, ациламіно, амідо, карбонілом та алкілтіо. [0112] За певними варіантами здійснення даний винахід стосується вище згаданого способу, де сполука має формулу В: [0113] За конкретними варіантами здійснення даний винахід стосується вище згаданого способу, 4 де R являє собою метил-аміно-диметилацетамід, для утворення сполуки, що має формулу І: [0114] За конкретними варіантами здійснення, даний винахід стосується вище згаданого способу, 4 де R - метил-аланін-диметилацетамід, для утворення сполуки, що має формулу II: , 37 [0115] За конкретними варіантами здійснення, даний винахід стосується вище згаданого способу, 4 де R являє собою 2-метиламіно-2-триметилпропіонамід, для утворення сполуки, що має формулу III: 95604 38 А являє собою N або С-Н; 13 В являє собою N, С-Н, C-(SO2-NH-R ) або C13 CO-NH-R ; 13 D являє собою N, С-Н, C-(SO2-NH-R ) або C13 CO-NH-R ; Е являє собою N або С-Н; де тільки один з А, В або Е може бути N, а 13 один з В або D являє собою С-(SO2-NH-R ) або C13 CO-NH-R ; 13 R являє собою нижчий алкіл. 2 [0119] За переважним варіантом здійснення R 3 та R незалежно вибрані з нижчого алкілу. За до13 датковим переважним варіантом здійснення R метил. [0120] Переважний метаболіти включають сполуки, що мають формулу D1: 1 [0116] За конкретними варіантами здійснення даний винахід стосується вище згаданих способів, 4 де m являє собою 1 або 2 для R (Формула С), який приєднується до Сполуки А. Переважно, n являє собою 1. [0117] За конкретними варіантами здійснення даний винахід стосується вище згаданого способу, де зазначена перша сполука є відомою структурою або скелетом активних сполук, включаючи, але не обмежуючись, активні агенти лікарського засобу, біоактивні речовини, білки та хімічні сполуки. Наприклад, сполука може бути сполукою з формулою А або В. [0118] Даний винахід також стосується вище згаданих способів, які включають метаболіти будьякої із зазначених вище сполук. За одним варіантом здійснення даного винаходу метаболіт може мати, структуру, представлену формулою D: 1 R являє собою нижчий алкіл; 2 3 R та R незалежно вибрані з нижчого алкілу, нижчого алкенілу та нижчого алкінілу, де нижчий алкіл, нижчий алкеніл та нижчий алкініл можуть бути факультативно заміщені одним або більше галогеном, нижчим алкокси, гідрокси, CN, Ж)2, аміно, ациламіно, амідо, карбонілом та алкілтіо; 2 3 де R , R та R зазначені вище для Сполуки А, 13 та R вибраний з нижчого алкілу, переважно метилу. Переважні варіанти здійснення включають сполуку формули [0121] Сполуки формули D та D1 або їх фармацевтично прийнятні солі, стереоізомери, гідрати або пролікарські засоби можна вводити безпосередньо пацієнту. Альтернативно, сполуки формули D та Di можуть бути утворені в організмі пацієнта після введення вихідної сполуки або пролікарського засобу. Таким чином за одним варіантом здійснення даний винахід спрямований на способи інгібування PDE, зокрема PDE5, введенням людині сполук формули D або D1. Додатковий варіант здійснення даного винаходу спрямований на способи інгібування PDE, зокрема PDE5, введенням людині, пролікарський засіб утворює сполуку формули D або D1 in vivo, наприклад, як результат перетворення при обміні речовин. [0122] Певні сполуки, утворені вище згаданими способами за даним винаходом, можуть існувати в конкретних геометричних або стереоізомерних формах. Даний винахід передбачає усі такі сполуки, включаючи цис- та транс-ізомери, R-та Sенантіомери, діастереомери, (Б)-ізомери, (Ь) 39 95604 40 ізомери, їх рацемічні суміші та інші їх суміші, як потрапляють у межі даного винаходу. Додаткові асиметричні атоми вуглецю можуть бути присутніми в заміснику, такому як алкільна група. Усі такі ізомери, а також їх суміші, включені в даний винахід. Наприклад, за одним варіантом здійснення сполука або фармацевтичні композиція є перетворенням Сполуки 2, що має структуру: [0123] Наступні ізомери такої сполуки включені в даний винахід: [0124] Крім того, якщо, наприклад, бажаний конкретний енантіомер сполуки за даним винаходом, його можна виготовити асиметричним синтезом або деривацією з хіральним допоміжним засобом, де утворену діастереомерну суміш розділяють, а допоміжну групу відщеплюють для забезпечення чистих бажаних енантіомерів. Альтернативно, якщо молекула містить основну функціональну групу, таку як аміно, або кислотну функціональну групу, таку як карбоксильну, діастереомерні солі утворюють з придатної оптично активної кислоти або основи з наступним розчиненням діастереомерів, таким чином утворених фракційною кристалізацією або хроматографічними засобами, добре відомими в даній галузі, та наступним відновленням чистих енантіомерів. [0125] Синтетичні невеликі молекули часто мають низьку розчинність, яка обмежує їх здатність розчинятися в кишці, абсорбуватися організмом та досягати терапевтичну мішень. Навпаки, деякі молекули є настільки гідрофільними, що вони не можуть подолати гідрофобну мембрану, яка оточує клітини, та тому не здатні досягти їх терапевтичну мішень. Тому бажані хімічні групи, що дозволяють хімікам або підвищувати розчинність, або знижувати гідрофільність невеликих молекул. [0126] Далі описується спосіб, оснований на поверхні, для ідентифікації груп, що можуть поліпшати розчинність невеликих молекул. Самоагрегований моношар тіолових молекул з ангідридними групами на кінці утворюють на золотій поверхні. Ряд невеликих молекул з тіольними групами на одному кінці та гідрофільними групами на іншому кінці потім приєднують до поверхні шляхом реакції між тіолом та малеімідом. Ряд молекул наносять на просторово розділені ділянки на золотій поверхні для утворення серії молекул, що можуть підвищувати розчинність невеликої молекули. Краплини полярних (наприклад, вода) та гідрофобних (наприклад, октанол) рідин потім поміщають до кожного елемента серії. Контактні кути двох рідин на кожному елементі потім виміряють для кожного елемента серії за допомогою гоніометра. Альтернативно, здатність до змочування конкретної рідини на поверхні, що представляє хімічну групу, можна визначити, вимірюючи площу поверхні, покриту краплиною, якщо дивитися зверху (високий кут контакту буде давати краплини невеликої площі; низькі кути контакту вкриють більші площі). Кут контакту рідини на поверхні, що представляє хімічну групу, зворотно пропорційний здатності цієї хімічної групи змішуватися з рідиною (розчинником). Наприклад, хімічна група, для якої вода має високий кут контакту, коли вона присутня на поверхні, така як метил (СН3), має низьку здатність змішуватися з водою, тобто, вона буде мати схильність до зниження розчинності невеликої молекули. Навпаки, хімічна група, для якої вода має низький кут контакту, коли вона присутня на поверхні, така як карбоксил (СООН), має високу здатність змішуватися з водою, тобто, вона буде мати схильність до підвищення розчинності невеликої молекули. Ряди хімічних груп, таким чином, можна швидко досліджувати за допомогою кутів контакту на поверхні для ідентифікації груп, що підвищують розчинність або знижують гідрофільність. Цей підхід можна застосувати для посилення впливу на розчинність хімічних групи за даним винаходом. 41 [0127] Загальним параметром для здатності невеликої молекули долати ліпідну мембрану клітини є logP, де Р являє собою коефіцієнт розподілу сполуки між октанолом та водою. Відносний кут контакту поверхні, що представляє хімічні групи для октанолу та води, тому пропонує швидкий, емпіричний спосіб для оцінювання великих рядів хімічних групи на їх потенційний вплив на logP сполуки. [0128] Можна застосовувати рН залежність розчинності невеликих молекул у способі шляхом вимірювання кутів контакту розчинів в різнихрН. Параметр, еквівалентний logP у цьому випадку, являє собою logD, де D - коефіцієнт розподілу, визначений як співвідношення суми концентрацій усіх видів сполуки в октанолі до суми концентрацій усіх видів сполуки у воді в різних рН. Тому, кути контакту, виміряні при різних рН, пропонують можливість еквівалентної міри до logD. [0129] Також буде корисним дослідити кандидатці сполуки на їх здатність активно переноситися крізь клітинні мембрани та клітини або на їх стійкість до такого перенесення. Наприклад, відомо, що фармацевтично корисні протиракові молекули можуть бути обмежені за їх ефективністю через активне перенесення з мішеневих пухлинних клітин. Таким же чином, моношари ендотеліальних клітин мозкових капілярів, як спостерігають, переносять вінкристин в одному напрямку з базального кінця до апікального кінця, ефективно перешкоджаючи потрапляння протиракового агента до центральної нервової системи. В деяких випадках цінні хімічні групи на додаток до зниження неспецифічного зв'язування з білком будуть поліпшувати фармакокінетичні властивості, посилюючи пасивне або активне перенесення до їх ділянки дії та/або інгібуючи перенесення від ділянки дії. [0130] Мозок являє собою одну з найбільш складних тканин для проникнення невеликих молекул. Нейроваскулярні сполучення щільні та містять дуже небагато активних носіїв, які, головним чином, відповідають за виведення невеликих молекул з мозку. Параклітинний шлях (міжклітинне сполучення) не доступний для невеликих молекул, для них існує тільки трансклітинний шлях (крізь клітинні мембрани). Класично, молекули, для яких мішенню є мозок, такі як бензодіазепіни, являються гідрофобними, що дозволяє їм проникати крізь клітинні мембрани. Даний винахід являє відповідає вимогам пошуку хімічних груп, які забезпечують стійкість до білка та полегшують загальну проблему надмірного зв'язування з білком, асоційованого з молекулами, такими як бензодіазепіни; це вимагає високого дозування через зв'язування з білками сироватки значного відсотка. Підходи, описані раніше, для ідентифікації зв'язувачів PGP допоможуть оптимізувати молекули для поліпшення часу знаходження в мозку. [0131] Доступні декілька модельних систем, що застосовують моношари різних типів клітин для оцінювання активного перенесення фармацевтично активних речовин. Наприклад, моношари кишкових епітеліальних клітин Сасо-2 можна застосовувати для оцінювання активного перенесення речовини між кишкою та кровотоком. Нанесенні на 95604 42 поверхню, яка дозволяє потік матеріалу від апікального кінця до базілатерального та навпаки, клітини утворюють біологічну мембрану, яку можна застосувати для моделювання фізіологічної абсорбції та біопридатності. За іншим прикладом лінію капілярних ендотеліальних клітин мозку миші (МВЕС) стабілізували для оцінювання активного перенесення в та з центральної нервової системи. Іншим прикладом таких клітин є клітини карциноми прямої кишки людини НТ29. Крім того, моношари, що експресують окремі транспортні білки, можна стабілізувати з використанням трансфектованих клітин. Наприклад, Sasaki et аію (2002) J. Biol. Chem. 8:6497 застосовували моношар двічі трансфектованих клітин нирки собаки Madin-Darby для дослідження перенесення органічних аніонів. [0132] Можна звичайно застосовувати альтернативи клітинним моношарам для перевірки проникності. Альтернативи типово містять біологічну структуру, здатну до активного перенесення, та включають, але не обмежуються, органи травного тракту, отримані від лабораторних тварин, та відновлені органи або мембрани, створені in vitro від клітин, висіяних на штучному середовище. [0133] Багато невеликих молекул, що є потенційними терапевтичними засобами, не ефективні в організмі, тому що ферменти організму, особливо печінки та кишок, метаболізують їх. Наприклад, ферменти CYP450 спричиняють Фазу І окислення невеликих молекул, тим самим, змінюючи їх фізичні та біологічні властивості, що може нести позитивний або негативний вплив на їх терапевтичну дію. Хімічні групи, стійкі до окислення ферментами CYP450, можна застосовувати при модуляції метаболізму невеликих молекул без загрози їх ефективності до терапевтичної мішені. Альтернативно, бажано для ідентифікації хімічних груп, які діють як захисні мішені для окисних ферментів, що таким чином відхиляють шлях метаболізму від активного фармакофору. Цей підхід може дати нові пролікарські засоби та/або метаболічні захисні групи для сприйнятливих до метаболізму фармакофорів. [0134] Шляхом для ідентифікації хімічних груп, які модулюють метаболічний профіль невеликих молекул, є наступне: самоагрегований моношар тіолових молекул з ангідридними групами на кінцях формують на золотій поверхні. Ряд невеликих молекул з амінними групами на одному кінці та групами, що забезпечують стійкість до окислення CYP450, наприклад, на іншому кінці, потім приєднують до поверхні шляхом реакції між аміном та ангідридом. Цей ряд молекул наносять на просторово розділені ділянки золотої поверхні для створення серії молекул, стійких до ферментативного окислення. Цю серію потім обробляють розчином, що містить фермент CYP450, наприклад, мікросомальний препарат. Такі мікросоми доступні для усіх з основних ізоферментів в класі CYP450. Як тільки встановили серію ферменту протягом придатного інкубаційного періоду, золоту поверхню промили та помістили до MALDI мас-спектрометру (MS). Хімічні композиції ряду хімічних груп, зафіксованих на поверхні, потім визначили масспектрометричним аналізом для кожного елементу 43 в серії на золоті (див. попередні описи). Якщо хімічні групи були модифіковані ферментом, тоді це буде виявлено змінами їх мас-спектру. Якщо хімічні групи не були модифіковані CYP450, тоді їх мас-спектр не буде змінюватися до обробки ферментом. Групи, стійкі до модифікації, є гарними кандидатами для заміщення груп в невеликих молекулах, сприйнятливих до окислення CYP450. Метаболічна стабільність або профіль [0135] Цей підхід не обмежений мікросомами, що містять ферменти CYP450 людського походження. Цей підхід можна застосовувати з природними мікросомальними препаратами від багатьох видів, щоб дослідити в масі для прогнозування (та врахування) різних метаболічних шляхів для різних видів. Ці дані допомогли б у виборі найбільш релевантних видів тварин для предклінічної перевірки. [0136] Подібним чином, групи, стійкі до модифікації іншими ферментами Фази І, що викликають відновлення та гідроліз невеликих молекул, можна було б ідентифікувати обробкою серій цими ферменти та дослідженням серії на MALDI-MS. Групи, стійкі до кон'югації, та синтез ферментами Фаза II можна ідентифікувати обробкою серії ферментом та ко-фактором та дослідженням серії на MALDIMS. [0137] Взаємодії лікарських засобів. Подібним чином, поверхневий серійний підхід можна застосовувати для ідентифікації небезпечної взаємодії лікарський засіб-лікарський засіб, яка може підвищувати токсичність терапевтичних засобів з невеликими молекулами. За цим способом ряд загальних "метаболічних" мотивів, виявлених в існуючих лікарських засобах (наприклад, аспірин та протигістаміни), фіксують на поверхні. Потім поверхню обробляють мікросомою CYP450, змішаною з потенційним терапевтичним засобом, та потім аналізують метаболізм фіксованих мотивів, за допомогою MALDI-MS. Якщо аналізована сполука взаємодіє з метаболізмом фіксованих груп CYP450, то цей результат буде свідчити про потенційні взаємодії лікарських засобів. Оскільки цей приклад не підпадає під категорію ідентифікації хімічних груп для поліпшення фармакокінетичної властивості, він дійсно показує широку придатність поверхневого серійного підходу. Токсичність [0138] Можна також застосовувати цей формат для визначення, які CYP450 включені в метаболізм конкретної хімічної групи. Ця інформація допомогла б розробити лікарські засоби для конкретних субпопуляцій з певними мутаціями в їх CYP450. [0139] Невеликі молекули часто зазнають невдачу як терапевтичні засоби, тому що вони токсичні до клітин. Групи, що знижують токсичність, були б корисними для поліпшення таких молекул. Наступне описує спосіб дослідження впливу на токсичність ряду хімічних груп. Розчини хімічних груп наносять та висушують на серіях на пласкому субстраті. Потім на серію наносять клітинний тип інтересу як моношар. Потім ряд молекул електропорують крізь клітинний моношар та в клітини. Після періоду інкубація серію досліджують на жит 95604 44 тєздатність клітин. Будь-які зони, що містять мертві клітини, покажуть, що електропоровані хімічні групи токсичні. Фармацевтичні композиції [0140] За іншим аспектом даний винахід забезпечує фармацевтично прийнятні композиції, які містять терапевтично ефективну кількість одної або більше сполук за даним винаходом, включаючи, але не обмежуючись, сполуки, описані вище, та ті, що показані на Фігурах, сформульовані разом з одним або більше фармацевтично прийнятним носієм (адитивом) та/або розріджувачем. Як детально описано нижче, фармацевтичні композиції за даним винаходом можуть бути спеціально сформульовані для введення в твердій або рідкій формі, включаючи адаптовані для: (1) орального введення, наприклад, великі дози (водні або неводні розчини або суспензії), таблетки, наприклад, для букальної, під'язичної та системної абсорбція, болюси, порошки, гранули, пасти для нанесення на язик; (2) парентерального введення, наприклад, підшкірною, внутрішньо м'язовою, внутрішньовенною або епідуральною ін'єкцією, наприклад, як стерильний розчин або суспензія, або формуляція тривалого вивільнення; (3) місцевого нанесення, наприклад, як крем, мазь, або пластир контрольованого вивільнення або спрей для шкіри; (4) внутрішньовагінально або внутрішньоректально, наприклад, як вагінальний супозиторій, крем або пінка; (5) під'язично; (6) внутрішньоочно; (7) через шкіру; або (8) назально. [0141] Вираз "терапевтично ефективна кількість", як застосовують тут, означає таку кількість сполуки, матеріалу або композиції, що містить сполуку за даним винаходом, яка ефективна для створення деякого бажаного терапевтичного ефекту щонайменш в субпопуляції клітин тварини при придатному співвідношенні користь/ризик при будь-якому медичному лікуванні, наприклад придатні бічні ефекти при будь-якому медичному лікуванні. [0142] Вираз "фармацевтично прийнятний", як застосовують тут, відноситься до таких сполук, матеріалів, композицій та/або дозованих форм, які у межах медичного обговорення придатні для застосування в контакті з тканинами людей та тварин з токсичністю, подразненням, алергічною реакцією або іншими проблеми або ускладненнями, з придатним співвідношенням користь/ризик. [0143] Вираз "фармацевтично прийнятний носій", як застосовують тут, означає фармацевтично прийнятний матеріал, композицію або транспортний засіб, такий як а рідкий або твердий наповнювач, розріджувач, формоутворювач, технологічна добавка (наприклад, змащувач, магнієвий тальк, кальцію або цинку стеарат або стерична кислота), або розчинник, що інкапсулює матеріал, що залучається до перенесення або транспортування даної сполуки від одного органу або частини тіла до іншого органу або частини тіла. Кожний носій має бути "прийнятним", тобто є сумісним з іншими інгредієнти формуляції та не шкідливий для пацієнта. Деякі приклади матеріалів, які можуть служити фармацевтично прийнятними носіями, включають: (1) цукри, такі як лактоза, глюкоза та сахароза; (2) 45 крохмалі, такі як кукурудзяний крохмаль та картопляний крохмаль; (3) целюлоза та її похідні, такі як натрію карбоксиметилцелюлоза, етилцелюлоза та целюлози ацетат; (4) порошковий трагакант; (5) солод; (6) желатин; (7) тальк; (8) формоутворювачі, такі як масло какао та супозиторні воски; (9) олії, такі як арахісова олія, бавовняна олія, сафлорова олія, кунжутова олія, оливкова олія, кукурудзяна олія та соєва олія; (10) гліколі, такі як пропіленгліколь; (11) поліоли, такі як гліцерин, сорбітол, манітол та поліетиленгліколь; (12) складні ефіри, такі як етил олеат та етил лаурат; (13) агар; (14) буферні агенти, такі як магнію гідроксид та алюмінію гідроксид; (15) альгінова кислота; (16) апірогенна вода; (17) ізотонічний сольовий розчин; (18) розчин Рінгеру; (19) етиловий спирт; (20) рН буферізовані розчини; (21) поліефіри, полікарбонати та/або поліангідриди; та (22) інші нетоксичні сумісні речовини, що застосовуються у фармацевтичних формуляціях. [0144] Як зазначено вище, певні варіанти здійснення даних сполук можуть включати основну функціональну групу, таку як аміно або алкіламіно, та, таким чином, здатні утворювати фармацевтично прийнятні солі з фармацевтично прийнятними кислотами. Вираз "фармацевтично прийнятні солі", у цьому відношенні, означає відносно нетоксичні, неорганічні та органічні кислотно-адитивні солі сполук за даним винаходом. Такі солі можна отримати in situ у процесі виготовлення транспортного засобу для введення або дозованої форми, або окремо реакцією очищеної сполуки за даним винаходом в формі її вільної основи з придатною органічною або неорганічною кислотою, та виділенням солі, утвореної таким чином утвореної, протягом послідовної очистки. Типові солі включають гідробромід, гідрохлорид, сульфат, бісульфат, фосфат, нітрат, ацетат, валерат, олеат, пальмітат, стеарат, лаурат, бензоат, лактат, фосфат, тозилат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтілат, мезилат, глікогептонат, лактобіонат та лаурилсульфонатні солі та подібне. (See, наприклад, Berge et al. (1977) "Pharmaceutical Salts", J. Pharm. ScL 66:1-19). [0145] Фармацевтично прийнятні солі даних сполуки включають традиційні нетоксичні солі або четвертинні амонійні солі сполук, наприклад, нетоксичних органічних або неорганічних кислот. Наприклад, такі традиційні нетоксичні солі включають похідні з неорганічних кислот, такі як гідрохлорид, гідробромід, сірчана, сульфамінова, фосфорна, азотна та подібне; та солі, отримані з органічних кислот, таких як оцтова, пропіонова, сукцинова, глікольна, стеаринова, лактамова, яблучна, винна, лимонна, аскорбінова, пальмітинова, малеїнова, гідроксималеїнова, фенілоцтова, глутамова, бензольна, саліцилова, сульфанільна, 2іцетоксибензойна, фумарова, толуолсульфонова, метансульфонова, етандисульфонова, оксалінова, ізотіонова та подібне. [0146] В інших випадках сполуки за даним винаходом можуть містити одну або більше кислотних функціональних груп та, таким чином, здатні утворювати фармацевтично прийнятні солі з фармацевтично прийнятними основами. Вираз "фар 95604 46 мацевтично прийнятні солі" у цих випадках відноситься до відносно нетоксичних, неорганічних та органічних основно-адитивних солей сполук за даним винаходом. Такі солі можна отримати in situ у процесі виготовлення транспортного засобу для введення або дозованої форми, або окремо реакцією очищеної сполуки за даним винаходом в формі її вільної кислоти з придатною основою, такою як гідроксид, карбонат або бікарбонат фармацевтично прийнятного металевого катіону, з амонієм або з фармацевтично прийнятним органічним первинним, вторинним або третинним аміном. Типові солі лужних або лужноземельних солей включають солі літію, натрію, калію, кальцію, магнію, алюмінію та подібне. Типові органічні аміни, застосовані для утворення основно-адитивних солей включають етиламін, діетиламін, етилендіамін, етаноламін, діетаноламін, піперазин та подібне. (See, наприклад, Berge et al., вище). [0147] В композиції також можуть бути присутніми зволожуючі агенти, емульсифікатори та змащувачі, такі як натрію лаурил сульфат та магнію стеарат, а також барвники, агенти, що регулюють вивільнення, агенти покриття, підсолоджувачі, смакові та ароматичні агенти, консерванти та антиоксиданти. [0148] Приклади фармацевтично прийнятних антиоксидантів включають: (1) розчинні у воді антиоксиданти, такі як аскорбінова кислота, цистеїн гідрохлорид, натрію бісульфат, натрію метабісульфіт, натрію сульфіт та подібне; (2) розчинні в олії антиоксиданти, такі як аскорбіл пальмітат, бутильований гідроксианізол (ВНА), бітильований гідрокситолуол (ВНТ), лецитін, пропіл галат, альфа-токоферол та подібне; та (3) метал хелатоутворюючі агенти, такі як лимонна кислота, етилендіамін тетраоцтова кислота (EDTA), сорбітол, винна кислота, фосфорна кислота та подібне. [0149] Формуляції за даним винаходом включають придатні для орального, назального, місцевого (включаючи букальне та під'язичне), ректального, вагінального та/або парентерального введення. Формуляції звичайно можуть знаходитися в одиничній дозованій формі та можуть бути виготовлені будь-якими способами, добре відомими в даній фармацевтичній галузі. Кількість активного інгредієнту, який можна комбінувати з матеріалом носія для утворення окремої дозованої форми, буде змінюватися в залежності від пацієнта, що потребує лікування, конкретного способу введення. Кількість активного інгредієнту, який можна комбінувати з матеріалом носія для утворення окремої дозованої форми, буде кількістю сполуки, яка створює терапевтичний ефект. В основному, від ста відсотків ця кількість буде змінюватися від близько 0,1% до близько 99% активного інгредієнту, переважно від близько 5% до близько 70%, найбільш переважно від близько 10% до близько 30%. [0150] За конкретними варіантами здійснення формуляція за даним винаходом містить формоутворювач, вибраний з групи, що містить циклодекстрини, целюлози, ліпосоми, агенти, що утворюють міцели, наприклад, жовчні кислоти, та полімерні носії, наприклад, поліефіри та поліангід 47 риди; та сполуку за даним винаходом. За конкретними варіантами здійснення вищезгадана формуляція представляє орально біодоступну сполуку за даним винаходом. [0151] Способи виготовлення таких формуляцій або композицій включають етап приведення в асоціацію сполуки за даним винаходом з носієм та, факультативно, одним або більше додатковим інгредієнтом. У цілому, формуляції виготовляють однорідним та безпосереднім приведенням в асоціацію сполуки за даним винаходом з рідкими носіями або з точно розподіленими твердими носіями, або з обома, а потім, якщо необхідно, формують продукт. [0152] Формуляції даного винаходу, придатні для орального введення, можуть бути у формі капсул, саше, пілюлі, таблеток, ромбовидних таблеток (із застосуванням смакової основи, звичайно сахароза та акацієва або трагакантова камеді), порошків, гранул, абояк розчин, або суспензія у водній або неводній рідині, або як рідка емульсія олія-у-воді або вода-в-олії, або як еліксир або сироп, або як пастилки (із застосуванням інертної основи, такої як желатин та гліцерин, або сахароза та акацієва камедь) та/або як рідина для полоскання ротової порожнини, та подібне, кожне з яких містить попередньо визначену кількість сполуки за даним винаходом як активний інгредієнт. Сполуку за даним винаходом можна також вводити як болюс, електуарій або пасту. [0153] В твердих дозованих формах даного винаходу для орального введення (капсули, таблетка, пілюлі, драже, порошки, гранули, пласкі таблетки та подібне) активний інгредієнт змішують з одним або більше фармацевтично прийнятним носієм, таким як натрію цитрат або дикальцію фосфат, та/або з будь-яким з: (1) наповнювачів або сухих розріджувачів, таких як крохмалі, лактоза, сахароза, глюкоза, манітол та/або саліцилова кислота; (2) зв'язувачів, таких як, наприклад, карбоксиметилцелюлоза, альгінати, желатин, полівінілпіролідон, сахароза та/або акацієва камедь; (3) зволожувачів, таких як гліцерол; (4) агентів, що дезінтегрують, таких як агар-агар, кальцію карбонат, картопляний або маніоковий крохмаль, альгінова кислота, деякі силікати та натрію карбонат; (5) агентів, що затримують розчинення, таких як парафін; (6) прискорювачів абсорбції, таких як четвертинні амонійні сполуки, та сурфактантів, таких як полоксамер та натрію лаурил сульфат; (7) зволожуючих агентів, таких як, наприклад, цетиловий спирт, гліцерол моностеарат, та неіонних сурфактантів; (8) абсорбентів, таких як каолін та бентонітова глина; (9) змащувачів, таких як тальк, кальцію стеарат, магнію стеарат, тверді поліетиленгліколі, натрію лаурил сульфат, цинку стеарат, натрію стеарат, стеаринова кислота та їх суміші; (10) барвників; та (11) агентів, що регулюють вивільнення, таких як кросповідон або етилцелюлоза. У випадку капсул, таблеток та пілюль фармацевтичні композиції можуть також містити буферні агенти. Тверді композиції подібного типу також можна застосовувати як наповнювачі для м'яких та твердих желатинових капсул із застосуванням таких формоутворювачів як лактоза або молочні 95604 48 цукри, а також поліетиленгліколі з великою молекулярною масою та подібне. [0154] Таблетку можна виготовити пресуванням або штампуванням факультативно з одним або більше додатковим інгредієнтом. Пресовані таблетки можна виготовити з використанням зв'язувача (наприклад, желатину або гідроксипропілметилцелюлози), змащувача, інертного розріджувача, консерванту, дезінтегранта (наприклад, натрію крохмаль гліколяту або перехресно зшитої карбоксиметилцелюлози натрію), поверхнево активного або дисперсного агента. Пресовані таблетки можна виготовити штампуванням в придатному апараті суміші порошкової сполуки, зволоженої інертним рідкім розріджувачем. [0155] Таблетки та інші тверді дозовані форми фармацевтичних композицій за даним винаходом, такі як драже, капсули, пілюлі та гранули, можна факультативно виконати з насічкою або виконати з покриттями та оболонками, такими як кишковорозчинні покриття та інші покриття, добре відомі в фармацевтичній галузі. їх можна також сформулювати із забезпеченням повільного або регульованого вивільнення активного інгредієнту за даним винаходом, наприклад, із гідроксипропілметилцелюлозою в різних пропорціях для забезпечення бажаного профілю вивільнення профіль, з іншими полімерними матрицями, з застосуванням ліпосом та/або мікросфер. Їх можна сформулювати для швидкого вивільнення, наприклад, ліофілізованими. Їх можна стерилізувати, наприклад, фільтрацією крізь фільтр, що затримує бактерії, або включенням агентів, що стерилізують, у форму стерильних твердих композицій, які можна розчинити в стерильній воді, або деяких інших стерильних середовищ для ін'єкції безпосередньо перед застосуванням. Такі композиції можуть також факультативно містити непрозорі агенти та можуть бути композицією, що вивільняє активний інгредієнт(и) тільки, або переважно, в певній частині травного тракту, факультативно, уповільненим способом. Приклади включених композицій, які можна застосовувати, містять полімерні речовини та воски. Активний інгредієнт також може бути в мікроінкапсульованій формі, якщо потрібно, з одним або більше яз зазначених вище формоутворювачів. [0156] Рідкій дозовані форми для орального введення сполук даного винаходу включають фармацевтично прийнятні емульсії, мікроемульсії, розчини, суспензії, сиропи та еліксири. На додаток до активного інгредієнту рідкі дозовані форми можуть містити інертні розріджувачі, що звичайно застосовують в даній галузі, такі як, наприклад, вода або інші розчинники, агенти, що посилюють розчинність, та емульсифікатори, такі як етиловий спирт, ізопропіловий спирт, етил карбонат, етил ацетат, бензиловий спирт, бензил бензоат, пропіленгліколь, 1,3-бутиленгліколь, олії (зокрема, бавовняна, арахісова, кукурудзяна, зародкова, оливкова, касторова та кунжутова олії), гліцерол, тетрагідрофуриловий спирт, поліетиленгліколі, жирнокислотні складні ефіри сорбітану та їх суміші. 49 [0157] Крім інертних розріджувачів оральні композиції можуть також включати допоміжні агенти, такі як зволожуючі агенти, емульсійні та суспензійні агенти, підсолоджувачі, смакові добавки, барвники, ароматизатори та консерванти. [0158] Суспензії на додаток до активних сполук можуть містити суспензійні агенти як, наприклад, етоксильовані ізостеарилові спирти, поліоксиетилен сорбітол та сорбітанові складні ефіри, мікрокристалічну целюлозу, алюмінію метагідроксид, бентоніт, агар-агар, трагакант та їх суміші. [0159] Формуляції фармацевтичних композицій даного винаходу для ректального або вагінального введення можуть бути у формі супозиторію, який можна виготовити змішуванням одної або більше сполуки даного винаходу з одним або більше придатним неподразнюючим формоутворювачем або носієм, що містить, наприклад, масло какао, поліетиленгліколь, супозиторний віск або саліцилат, та який є твердим при кімнатній температурі, але рідкім при температурі тіла, та, таким чином, буде плавитися в ректальній або вагінальній порожнині та вивільняти активну сполуку. [0160] Формуляції за даним винаходом, які придатні для вагінального введення також включають вагінальні супозиторії, тампони, креми, гелі, пасти, пінки або спреєві формуляції, що містять носії, що, як відомо придатні в даній галузі. [0161] Дозовані форми для місцевого або трансдермального введення сполуки за даним винаходом включають порошки, спреї, мазі, пасти, креми, лосьйони, гелі, розчини, пластири та інгаляції. Активна сполука може бути змішаною в стерильних умовах з фармацевтично прийнятним носієм та з будь-якими консервантами, буферами або пропелентами, які вимагаються. [0162] Мазі, пасти, креми та гелі можуть містити на додаток до активної сполуки за даним винаходом формоутворювачі, такі як тваринні та рослинні жири, олії, воски, парафіни, крохмаль, трагакант, похідні целюлози, поліетиленгліколі, силікони, бентоніти, кремнієву кислоту, тальк та оксид цинку або їх суміші. [0163] Порошки та спреї можуть містити на додаток до сполуки за даним винаходом формоутворювачі, такі як лактоза, тальк, кремнієва кислота, алюмінію гідроксид, кальцію силікати та поліамідний порошок або суміші цих речовин. Спреї можуть додатково містити традиційні пропеленти, такі як хлорофторовуглеводні та леткі незаміщені вуглеводні, такі як бутан та пропан. [0164] Трансдермальні пластирі мають додаткові переваги, що забезпечують регульовану доставку сполуки за даним винаходом в організмі. Такі дозовані форми можна виготовити розчиненням або диспергуванням сполуки у відповідному середовище. Посилювачі абсорбції також можна застосовувати для підвищення потоку сполуки крізь шкіру. Швидкість такого потоку можна регулювати або за допомогою мембрани, що регулює швидкість, або дисперсійної сполуки в полімерному матриксі або гелі. [0165] Офтальмологічні формуляції, очні мазі, порошки, розчини та подібне, також передбачаються об'ємом даного винаходу. 95604 50 [0166] Фармацевтичні композиції за даним винаходом, придатні для парентерального введення, містять одну або більше сполуку даного винаходу в комбінації з одним або більше фармацевтично прийнятними стерильними ізотонічними водними або неводними розчинами, дисперсіями, суспензіями або емульсіями або стерильними порошками, які можна відновити в стерильні розчини для ін'єкцій або дисперсії перед застосуванням, які можуть містити цукри, спирти, антиоксиданти, буфери, бактеріостатичні агенти, розчини, які роблять формуляцію ізотонічною з кров'ю визначеного реципієнта, або суспензійні, або агенти, що загущують. [0167] Приклади придатних водних та неводних носіїв, які можна застосовувати у фармацевтичних композиціях даного винаходу, включають воду, етанол, поліоли (такі як гліцерол, пропіленгліколь, поліетиленгліколь та подібне) та їх придатні суміші, рослинні олії, такі як оливкова олія, та органічні складні ефіри для ін'єкцій, такі як етил олеат. Потрібну плинність можна підтримати, наприклад, застосуванням матеріалів покриття, таких як лецитин, забезпеченням потрібного розміру частинок у випадку дисперсій, та за допомогою сурфактантів. [0168] Такі композиції можуть також містити додаткові агенти, такі як консерванти, зволожуючі агенти, емульсифікатори та дисперсійні агенти. Попередження дії мікроорганізмів на зазначені сполуки можна забезпечити включенням різних протибактеріальних та протигрибкових агентів, наприклад, парабену, хлорбутанолу, фенол сорбінової кислоти та подібного. Також може бути бажаним включення в композиції ізотонічних агентів, таких як цукри, натрію хлорид та подібне. Крім того, пролонговану абсорбцію ін'єкційної фармацевтичної форми можна забезпечити включенням агентів, які затримують абсорбцію, таких як алюмінію моностеарат та желатин. [0169] В деяких випадках для пролонгованої дії лікарського засобу бажана повільна абсорбція лікарського засобу з підшкірної або внутрішньо м'язової ін'єкції. Це можна виконати застосуванням рідкої суспензії кристалічного або аморфного матеріалу, який погано розчиняється уводі. Швидкість абсорбції лікарського засобу тоді залежить від швидкості його розчинення, яка, в свою чергу, може залежати від розміру кристалів та кристалічної форми. Альтернативно, затримана абсорбція парентерально введеної форми лікарського засобу досягається розчиненням або суспендуванням лікарського засобу у масляному транспортному засобі. [0170] Ін'єкційні форми уповільненого всмоктування виготовляють утворенням мікроінкапсульованих матриці даних сполук в полімерах, що біологічно руйнуються, таких як полілактид-полігліколід. В залежності від співвідношення лікарського засобу до полімеру та природи конкретного застосовуваного полімеру можна регулювати швидкість вивільнення лікарського засобу. Приклади інших полімерів, що біологічно руйнуються, включають полі(ортоефіри) та полі(ангідриди). Ін'єкційні формуляції уповільненого всмоктування також виготовляють включенням лікарського засобу в ліпосоми 51 або мікроемульсії, які сумісні з тканиною організму. [0171] Якщо сполуки за даним винаходом вводити як фармацевтичні засоби людям та тваринам, їх можна приймати в чистому вигляді або як фармацевтичну композицію, що містить, наприклад, 0,1-99% (більш переважно 10-30%) активного інгредієнту у комбінації з фармацевтично прийнятним носієм. [0172] Препарати за даним винаходом можна приймати орально, парентерально, місцево або ректально. Звісно, їх приймають у формах, придатних для кожного способу введення. Наприклад, їх вводять в таблетках або капсульній формі, ін'єкцією, інгаляцією, очними краплями, маззю, супозиториєм та т. д., вводять ін'єкцією, інфузією або інгаляцією; місцево лосьйоном або маззю; та ректально супозиторіями. Оральні введення є переважними. [0173] Вирази "парентеральне введення" та "вводити парентерально", як застосовують тут, означає способи введення, за виключенням ентерального та місцевого введення, звичайно ін'єкцією, та включає, без обмеження, внутрішньовенну, внутрішньо м'язову, внутрішньоартеріальну, внутрішньотекальну, внутрішньокапсулярну, внутрішньоочну, внутрішньокардіальну, внутрішньодермальну, внутрішньоперітоніальну, через трахею, підшкірну, під кутикулу, внутрішньосуглобову, підкапсулярну, субарахноїдальну, внутрішньоспінальну та внутрішньочеревну ін'єкцію та інфузію. [0174] Вирази "системне введення", "вводити систематично", "периферійне введення" та "вводити периферійно", як застосовують тут, означають введення сполуки, лікарського засобу або іншого матеріалу, за виключенням безпосередньо в центральну нервову систему, так що вона потрапляє у систему пацієнта та, таким чином, стає суб'єктом метаболізму та інших подібних процесів, наприклад, підшкірне введення. [0175] Ці сполуки можна вводити людям та тваринам для лікування будь-яким придатним способом введення, включаючи орально, назально, у вигляді, наприклад, спрею, ректально, внутрішньовагінально, парентерально, внутрішньоцистернально та місцево у вигляді порошків, мазей або крапель, включаючи букально та під'язично. [0176] Незалежно від вибраного способу введення, сполуки за даним винаходом, які можна застосувати в придатній гідратній формі, та/або фармацевтичні композиції за даним винаходом сформульовані в фармацевтично прийнятних дозованих формах традиційними способами, відомими фахівцю в даній галузі. [0177] Фактичні рівні дозування активних інгредієнтів у фармацевтичних композиціях за даним винаходом можуть бути різними, щоб отримати кількість активного інгредієнта, яка ефективна для досягнення бажаного терапевтичного ефекту для конкретного пацієнта, композицію та спосіб введення, що не є токсичними для пацієнта. [0178] Вибраний рівень дозування буде залежати від ряду факторів, включаючи активність конкретної застосовуваної сполуки за даним винаходом або її складного ефіру, солі або аміду, 95604 52 способу введення, часу введення, швидкості виведення або метаболізму конкретної застосовуваної сполуки, швидкості та ступеню абсорбції, тривалості лікування, інших лікарських засобів, сполук та/або матеріалів, застосованих в комбінація з конкретною застосовуваною сполукою, віку, статі, ваги, стану, стану здоров'я та історії хвороби пацієнта, що потребує лікування, та подібних факторів, добре відомих в медицині. [0179] Терапевт або ветеринар, що є звичайним фахівцем в даній галузі, може легко визначити та призначити потрібну ефективну кількість фармацевтичної композиції. Наприклад, терапевт або ветеринар можуть призначити початкові дози сполук даного винаходу, застосованих у фармацевтичній композиції, при рівнях, нижчих ніж ті, що вимагаються для досягнення бажаного терапевтичного ефекту та поступово підвищувати дозування до досягнення бажаного ефекту. [0180] У цілому, придатною щоденною дозою сполуки даного винаходу буде кількість сполуки, яка є мінімальною дозою, ефективною для утворення терапевтичного ефекту. Така ефективна доза буде в основному залежати від факторів, описаних вище. В основному, оральні, внутрішньовенні, внутрішньоцеребровентрикулярні та підшкірні дози сполук за даним винаходом для пацієнта при застосуванні для виражених анальгетичних ефектів буде змінюватися від близько 0,0001 до близько 100мг на кг ваги тіла на день. [0181] Якщо потрібно, ефективну щоденну дозу активної сполуки можна вводити у вигляді двох, трьох, чотирьох, п'яти, шести або більше субдоз, що вводять окремо з придатними інтервалами протягом дня, факультативно, в одиничних дозованих формах. Переважним дозуванням є одне введення на день. [0182] Крім того, можливо сполуку за даним винаходом вводити окремо, переважним є введення сполуки у вигляді фармацевтичної формуляції (композиції). [0183] Сполуки за даним винаходом можуть бути сформульовані для введення будь-яким традиційним шляхом для застосування в медицині або ветеринарії за аналогією з іншими фармацевтичними засобами. [0184] За іншим аспектом даний винахід забезпечує фармацевтично прийнятні композиції, які містять терапевтично ефективну кількість одної або більше даних сполук, описаних вище, сформульованих разом з одним або більше фармацевтично прийнятними носіями (адитивами) та/або розріджувачами. Як описано в деталях нижче, фармацевтичні композиції за даним винаходом можуть бути спеціально сформульовані для введення в твердій або рідкій формі, включаючи адаптовані для: (1) орального введення, наприклад, великі дози (водні або неводні розчини або суспензії), таблетки, болюси, порошки, гранули, пасти для нанесення на язик; (2) парентерального введення, наприклад, підшкірна, внутрішньом'язова або внутрішньовенна ін'єкція, наприклад, як стерильний розчин або суспензія; (3) місцевого застосування, наприклад, як крем, мазь або спрей, що наносять на шкіру, легені або слизові оболон 53 ки; або (4) внутрішньовагінального або внутрішньоректального, наприклад, як вагінальний супозиторій, крем або пінка; (5) під'язичного або букального; (6) внутрішньоочнго; (7) через шкіру; або (8) назально. [0185] Вираз "лікування" охоплює також профілактику, терапію та лікування. [0186] Пацієнтом, що отримує таке лікування, є будь-яка тварина, що потребує такого лікування, включаючи приматів, конкретно людей, та інших ссавців, таких як коні, рогата худоба, свиня та вівця; та домашня птиця та домашні тварини у цілому. [0187] Сполуку даного винаходу можна вводити окремо або у суміші з фармацевтично прийнятним носієм та також можна вводити разом з протимікробними агентами, такими як пеніциліни, цефалоспоріни, аміноглікозиди та глікопептиди. Кон'юктивна терапія, таким чином, включає послідовне, одночасне та окреме введення активної сполуки таким чином, що терапевтичні ефекти першого введення не зникають до наступного введення. [0188] Додавання активної сполуки даного винаходу до корму тваринам переважно виконують виготовленням придатного кормового преміксу, що містить активну сполуку в ефективній кількості, та включенням преміксу в повний раціон. [0189] Альтернативно, проміжний концентрат або кормова добавка, що містить активний інгредієнт можна додавати до корму. Спосіб, яким можна виготовити та вводити такі кормові премікси та повні раціони, описані в довідниках (таких як "Applied Animal Nutrition", W.H. Freedman and CO., San Francisco, U.S.A., 1969 або "Livestock Feeds and Feeding" О and В books, Corvallis, Ore., U.S.A., 1977). Міцели [0190] Останнім часом в фармацевтичній промисловості запровадили мікроемульсіфікаційну технологію для поліпшення біодоступності деяких ліпофільних (нерозчинних у воді) фармацевтичних агентів. Приклади включають Триметрин (Dordunoo, S. K., et al., Drug Development and Industrial Pharmacy, 17(12), 1685-1713, 1991 and REV 5901 (Sheen, P. C, et al., J Pharm Sci 80(7), 712-714, 1991). Серед іншого, мікроемульсіфікація забезпечує посилену біодоступність, переважно спрямовуючи абсорбцію до лімфатичної системи замість циркуляційної системи, яка таким чином обходить печінку та попереджує руйнування сполук в гепатобіліарній циркуляції. [0191] За одним аспектом даного винаходу формуляції містять міцели, утворені із сполуки за даним винаходом та, щонайменш, одного амфіфільного носія, де міцели мають середній діаметр менш ніж близько 100нм. Більш переважні варіанти здійснення забезпечують міцели, що мають середній діаметр менш ніж близько 50нм, та ще більш переважні варіанти здійснення забезпечують міцели, що мають середній діаметр менш ніж близько 30нм або навіть менш ніж близько 20нм. [0192] Оскільки передбачені усі придатні амфіфільні носії, у даний час переважні носії в основному мають статус визнаних повністю безпечни 95604 54 ми (GRAS), та це може розчинити сполуку за даним винаходом та мікроемульсифікувати її на більш пізній стадії, коли розчин контактує із складною водною фазою (такою як виявлена у гастроінтестинальному тракті людини). Звичайно, амфіфільні інгредієнти, що відповідають таким вимогам мають значення HLB (гідрофільно-ліпофільного балансу) 2-20, а їх структури містять аліфатичні радикали з прямим ланцюгом від С-6 до С-20. Прикладами є поліетилен-гліколізовані жирні гліцериди та поліетиленгліколі. [0193] Зокрема переважними амфіфільними носіями є насичені та мононенасичені поліетиленгліколізовані жирнокислотні гліцериди, такі як отримані з повністю або частково гідрогенізованих різних олій. Такі олії можуть переважно включати три-, ди- та моно- жирнокислотні гліцериди та дита моно-поліетиленгліколеві складні ефіри відповідних жирних кислот, із зокрема переважною жирнокислотною композицією, включаючи капринову кислоту 4-10, капринову кислоту 3-9, лаурилову кислоту 40-50, міристинову кислоту 14-24, пальмітинову кислоту 4-14 та стеаринову кислоту 5-15%. Інший застосовуваний клас амфіфільних носіїв включає частково етеріфікований сорбітан та/або сорбітол з насиченими або мононенасиченими жирними кислотами (SPAN-серія) або відповідними етоксильованими аналогами (TWEEN-серія). [0194] Зокрема передбачаються комерційно доступні амфіфільні носії, включаючи Gelucireсерия, лабрафіл, лабразол або лаурогліколь (усі виготовлені та розповсюджуються Gattefosse Corporation, Saint Priest, Франція), PEG-моноолеат, PEG-діолеат, PEG-монолаурат та дилаурат, лецитин, полісорбат 80 та т. д. (виготовляються та розповсюджуються рядом компаній в СІЛА та світі). Полімери [0195] Гідрофільні полімери, придатні для застосування за даним винаходом, є такими, що легко розчиняються у воді, можуть ковалентно приєднуватися до ліпіду, що утворює везикулу, та переносяться in vivo без токсичних ефектів (тобто, є біосумісними). Придатні полімери включають поліетиленгліколь (PEG), полімолочну (також позначаються як полілактид), полігліколеву кислоту (також позначаються як полігліколід), полімолочної-полігліколевої кислоти сополімер та полівініловий спирт. Переважні полімери мають молекулярну масу від близько 100 або 120 дальтон до близько 5000 або 10000 дальтон та більш переважно від близько 300 дальтон до близько 5000 дальтон. За зокрема переважним варіантом здійснення полімером є поліетиленгліколь, що має молекулярну масу від близько 100 до близько 5000 дальтон та більш переважно, що має молекулярну масу від близько 300 до близько 5000 дальтон. За зокрема переважним варіантом здійснення полімером є поліетиленгліколь 750 дальтон (PEG(750)). Полімери за даним винаходом мають значно меншу молекулярну масу, приблизно 100 дальтон, у порівнянні з великою молекулярною масою 5000 дальтон або більшу, що застосовується в стандартних технологіях РЕGиляції. Полімери також можна визначити за числом їх мономерів; в переважному варіанті здійснення даного винаходу 55 застосовують полімер, щонайменш, із близько трьома мономерами, такі PEG полімери, що містять три мономери (приблизно 150 дальтон). [0196] Інші гідрофільні полімери, які можуть бути придатними для застосування в даному винаході, включають полівінілпіролідон, поліметоксазолін, поліетилоксазолін, полігідроксипропіл метакриламід, поліметакриламід, полідиметилакриламід та дериватизовані целюлози, такі як гідроксиметилцелюлоза або гідроксиетилцелюлоза. [0197] За конкретними варіантами здійснення формуляція за даним винаходом включає біосумісний полімер, вибраний з групи, що містить поліаміди, полікарбонати, поліалкілени, полімери акрилового та метакрилового складних ефірів, полівінілові полімери, полігліколіди, полісілоксани, поліуретани та їх сополімери, целюлози, поліпропілен, поліетилени, полістирини, полімери молочної кислоти та гліколевої кислоти, поліангідриди, полі(орто)ефіри, полі(масляна кислота), полі(валеріанова кислота), полі(лактид-сокапролактон), полісахариди, білки, полігіалуронові кислоти, поліціаноакрилати та поєднання, суміші або сополімери їх. Циклодекстрини [0198] Циклодекстрини є циклічними олігосахаридами, що містять 6, 7 або 8 глюкозних одиниць, що позначаються грецькими літерами альфа, бета або гама, відповідно. Не відомо існування циклодекстринів з менше ніж шістьома глюкозними одиницями. Глюкозні одиниці зв'язані альфа- 1,4-глікозидними зв'язками. У результаті конфігурації крісла цукрових одиниць, усі вторинні гідроксильні групи (при С-2, С-3) розташовані на одній стороні кільця, тоді як усі первинні гідроксильні групи при С-6 розташовані на іншій стороні. Як результат, зовнішні поверхні є гідрофільними, що робить циклодекстрини розчинними у воді. Навпаки, заглиблення циклодекстринів є гідрофобними, оскільки вони вирівняні воднем атомів С-3 та С-5 та атомами кисню подібно ефіру. Ці матриці дозволяють комплексоутворення з рядом відносно гідрофобних сполук, включаючи, наприклад, стероїдні сполуки, такі як 17-бета-естрадіол (див., наприклад, van Uden et al. Plant Cell Tiss. Org. Cult. 38:1-3-113 (1994)). Комплексоутворення відбувається шляхом Ван-дер-Ваальсових взаємодій та утворенням водневого зв'язку. Для загального огляду хімії циклодекстринів, дивись Wenz, Agnew. Chem. Int. Ed. Engl., 33:803-822 (1994). [0199] Фізико-хімічні властивості похідних циклодекстринів строго залежить від виду та ступеню замісника. Наприклад, їх розчинність у воді змінюється від відсутності розчинності (наприклад, триацетил-бкта-циклодекстрин) до 147% розчину (вага/об'єм) (G-2-бета-циклодекстрин). Крім того, вони розчинні у багатьох органічних розчинниках. Властивості циклодекстринів дають можливість контролювати розчинність різних компонентів формуляції, посилюючи або знижуючи їх розчинність. [0200] Описані чисельні циклодекстрини та способи їх виготовлення. Наприклад, Parmeter (I), et al. (патент США №3453259) та Gramera, et al. (патент США №3459731) описали електронейтра 95604 56 льні циклодекстрини. Інші похідні включають циклодекстрини з катіонними властивостями (Parmeter (II), патент США № 3453257), нерозчинні перехресно зшиті циклодекстрини (Solms, патент США №3420788), та циклодекстрини з аніонними властивостями (Parmeter (III), патент США №3426011). Серед циклодекстринових похідних з аніонними властивостям отримані приєднанням до вихідних циклодекстринів карбонових кислот, фосфористих кислот, фосфінових кислот, фосфонових кислот, фосфорних кислот, тіофосфонових кислот, тіосульфінових кислот та сульфонових кислот (див., Parmeter (III), вище). Крім того, сульфоалкільні ефірні циклодекстринові похідні описані Stella, et al. (патент США №5134127). Ліпосоми [0201] Ліпосоми складаються із, щонайменш, одної ліпідної двошарової мембрани, що включає водні внутрішній простір. Ліпосоми можна характеризувати за типом мембрани та за розміром. Невеликі одношарові везикули (SUV) мають одну мембрану та типово мають діаметр від 0,02 до 0,05мкм; великі одношарові везикули (LUV) типово більше ніж 0,05мкм. Оліголамелярні великі везикули та багатошарові везикули мають багато, звичайно концентричних, мембранних шарів та типово більше ніж 0,1мкм. Ліпосоми з кількома неконцентричними мембранами, тобто, кілька менших везикул, що находяться в більшій везикулі, називають мультивезикулярними везикулами. [0202] Один аспект даного винаходу стосується формуляцій, які включають ліпосоми, що містять сполуку за даним винаходом, де ліпосомна мембрана сформульована для забезпечення ліпосоми підвищеною транспортною здатністю. Альтернативно або додатково, сполука за даним винаходом може знаходитися в або абсорбуватися на подвійному шарі ліпосоми. Сполука за даним винаходом може агрегуватися з ліпідним сурфактантом та переноситися у внутрішній простір ліпосоми; у цих випадках ліпосомна мембрана сформульована стійкою до руйнуючих ефектів агрегації активного агента з сурфактантом. [0203] За одним варіантом здійснення даного винаходу ліпідний подвійний шар ліпосоми містить ліпіди, дериватизовані з поліетиленгліколем (PEG), так що ланцюги PEG виходять з внутрішньої поверхні ліпідного подвійного шару у внутрішній простір ліпосоми, та виходять із зовнішнього ліпідного подвійного шару в оточуюче середовище. [0204] Активні агенти, що включені в ліпосоми за даним винаходом, знаходяться у розчинній формі. Агрегати сурфактанта та активного агенту (такі як емульсії або міцели, що містять активний агент інтересу) можуть бути захоплені у внутрішній простір ліпосом за даним винаходом. Сурфактант служить для диспергування та розчинення активного агенту та можуть бути вибраний з будь-якого придатного аліфатичного, циклоаліфатичного або ароматичного сурфактанта, включаючи, але не обмежуючись, біосумісний лізофосфатидилхоліни (LPC) з ланцюгами різної довжини (наприклад, від близько С.суб.14 до близько С.суб.20). Полімердериватизовані ліпіди, такі як PEG-ліпіди, також 57 можна застосовувати для утворення міцели, оскільки вони будуть діяти як інгібітори злиття міцели з мембраною, та оскльки додавання полімеру до сурфактантних молекул знижує CMC (критична концентрація міцелоутворення) сурфактанта та допомагає в утворенні міцел. Переважними є сурфактанти with CMC у мікромолярному діапазоні; сурфактанти з більшою CMC можна застосовувати для виготовлення міцел, замкнених у ліпосоми за даним винаходом, однак, сурфактантні мономери міцели можуть впливати на стабільність подвійного шару ліпосом та будуть враховуватися при розробці ліпосоми з бажаною стабільністю. [0205] Ліпосоми за даним винаходом можна виготовити будь-яким з ряду методик, відомих в даній галузі. Дивись, наприклад, патент США №4235871; Опубліковану РСТ заявку WO 96/14057; New RRC, Liposomes: A practical approach, IRL Press, Oxford (1990), pages 33-104; Lasic DD, Liposomes from physics to applications, Elsevier Science Publishers BV, Amsterdam, 1993. [0206] Наприклад, ліпосоми за даним винаходом можна виготовити дифузією ліпіду, дериватизованого з гідрофільним полімером, в попередньо сформовані ліпосоми, наприклад, піддаючи попередньо сформовані ліпосоми впливу міцел, що утворені з ліпід-щеплених полімерів, при ліпідних концентраціях, що відповідають фінальному молярному відсотку дериватизованого ліпіду, який є бажаним в ліпосомі. Ліпосоми, що містять гідрофільний полімер, також можна утворити методиками гомогенізації, гідратації пласкої ліпідної мембрани або екструдування, що відомі в даній галузі. [0207] За іншим прикладом методики формуляції активний агент спочатку диспергують ультразвуком в лізофосфатидилхоліні або іншому сурфактанті з низькою CMC (включаючи полімерщеплені ліпіди), що легко розчиняє гідрофобні молекули. Утворену міцелярну суспензію активного агента потім застосовують для регідратації сухого ліпідного зразка, що містить придатний молярний відсоток полімер-щеплених ліпідів або холестерол. Суспензію ліпіду та активного агента потім формують в ліпосоми за допомогою методик екструдування, відомих в даній галузі, та утворені ліпосоми виділяють з неінкапсульованого розчину стандартним колонковим розділенням. [0208] За одним аспектом даного винаходу ліпосоми виготовляють із головним чином однорідними розмірами у вибраному діапазоні розмірів. Один ефективний спосіб обробки в розмір включає екструдування водної суспензії ліпосом крізь серію полікарбонатних мембран, що мають пори вибраного однакового розміру; розмір пор мембрани приблизно буде відповідати найбільшим розмірам ліпосом, утворених екструдуванням крізь таку мембрану. Дивись, наприклад, патент США №4737323 (12.04.1988). Модифікатори вивільнення [0209] Характеристики вивільнення формуляції за даним винаходом залежать від інкапсульованого матеріалу, концентрація лікарського засобу, поміщеного в капсули, та присутності модифікатори вивільнення. Наприклад, вивільнення можна регулювати за допомогою залежності від 95604 58 рН, наприклад, за допомогою покриття, чуттєвого до рН, яке вивільняє тільки при низькому рН, як у шлунку, або при більш високому рН, як у кишці. Покриття, розчинне у кишці, можна застосовувати для попередження вивільнення, яке відбувається до проходження шлунку. Складні покриття або суміші ціанаміду, інкапсульовані в різних матеріалах, можна застосовувати для забезпечення початкового вивільнення у шлунку, а потім пізнішого вивільнення у кишці. Вивільнення також можна регулювати включенням солей або агентів, що утворюють пори, які можуть підвищувати всмоктування води або вивільнення лікарського засобу дифузією з капсули. Формоутворювачі, які модифікують розчинність лікарського засобу, можна також застосовувати для регулювання швидкості вивільнення. Також можуть бути включені агенти, що посилюють деградацію матриксу або вивільнення з матриксу. їх можна додати до лікарського засобу, як окрему фазу (тобто, як частинки), або можна сумісно розчинити в полімерній фазі, в залежності від сполуки. В усіх випадках кількість повинна бути у межах 0,1 30% (вага/вага полімеру). Типи агентів, що посилюють деградацію, включають неорганічні солі, такі як амонію сульфат та амонію хлорид, органічні кислоти, такі як лимонна кислота, бензойна кислота та аскорбінова кислота, неорганічні основи, такі як натрію карбонат, калію карбонат, кальцію карбонат, цинку карбонат та цинку гідроксид, та органічні основи, такі як протаміну сульфат, спермін, холін, етаноламін, діетаноламін та триетаноламін, та сурфактанти, такі як Tween® та Pluronic®. Агенти, що утворюють пори, які додають матриксам мікроструктуру (тобто, водорозчинні сполуки, такі як неорганічні солі та цукри), додають як частинки. Діапазон повинен складати 1-30% (вага/вага полімеру). [0210] Всмоктування також можна регулювати, змінюючи час перебування частинок в кишці. Цього можна досягти, наприклад, покриттям частинки або застосуванням у якості інкапсульованого матеріалу полімеру, адгезивного до слизової. Приклади включають більшість полімерів з вільними карбоксильними групами, такими як хітозан, целюлози та особливо поліакрилати (як застосовують тут, поліакрилати означають полімери, що включають акрилатні групи та модифіковані акрилатні групи, такі як ціаноакрилати та метакрилати). Комбінаторні бібліотеки [0211] Дані сполуки можна синтезувати способами комбінаторного синтезу, описаного в даному розділі. Комбінаторні бібліотеки сполук можна застосовувати для дослідження фармацевтичної, агрохімічної або іншої біологічної або терапевтичної активності або якостей, що залежать від матеріалу. Комбінаторна бібліотека для цілей даного винаходу являє собою суміш хімічно зв'язаних сполук, які можна досліджувати разом на бажану властивість; зазначені бібліотеки можуть бути у розчині або ковалентно зв'язані з твердою конструкцією. Виготовлення багатьох зв'язаних сполук в одній реакції значно знижує та спрощує число процесів дослідження, які потрібно виконати. Дослідження на придатну біологічну, фармаце 59 втичну, агрохімічну або фізичну властивість можна виконати традиційними способами. [0212] Різноманітності в бібліотеці можна досягти різноманітністю на різних рівнях. Наприклад, субстратні арильні групи, застосовувані в комбінаторному підході, можуть бути різними в арильному компоненті ядра, наприклад, мозаїчність в кільцевій структурі, та/або можуть бути різними по відношенню інших замісників. [0213] В даній галузі для утворення комбінаторних бібліотек невеликих органічних молекул застосовують ряд методик. Дивись, наприклад, Blondelle et al. (1995) Trends Anal. Chem. 14:83; Affymax патенти США №№5359115 та 5362899: Ellman патент США №5288514: Still et al. PCT публікація WO 94/08051; Chen et al. (1994) JACS 116:2661: Kerr et al. (1993) JACS 115:252; PCT публікації WO92/10092, WO93/09668 та WO91/07087; та Lemer et al. PCT публікація WO93/20242). Відповідно, ряд бібліотек з близько 16-1000000 або більше різновидів можна синтезувати та дослідити на конкретну активність або властивість. [0214] За прикладом варіанту здійснення бібліотеку заміщених різновидів можна синтезувати з використанням даних реакцій, адаптованих для методик, описаних Still et al. в PCT публікації WO 94/08051, наприклад, зв'язування з полімерною гранулою групою, що гідролізується або фотолізується, наприклад, розташованою в одному положенні субстрату. За методикою Still et al. бібліотеку синтезують на наборі гранул, кожна гранула включає набір міток, що ідентифікують конкретний різновид на цій гранулі. За одним варіантом здійснення, який є зокрема придатним для виявлення інгібіторів ферментів, гранули можна диспергувати на поверхні проникної мембрани, та різновиди вивільняються з гранули лізисом лінкеру гранули. Різновид з кожної гранули буде дифундувати крізь мембрану до дослідної зони, де він буде взаємодіяти з ферментом досліду. Детальні описи ряду комбінаторних методик наведені нижче. Безпосереднє визначення характеристик [0215] Зростаюча тенденція в галузі комбінаторної хімії повинна застосовувати чутливість методик, таких як мас-спектрометрія (MS), наприклад, які можна використовувати для характеристики субфемтомолярних кількостей сполуки та безпосереднього виявлення хімічного складу сполуки, вибраної з комбінаторної бібліотеки. Наприклад, якщо бібліотека створена на нерозчинному конструкційному матриксі, дискретні популяції сполук можуть спочатку вивільнятися з конструкції та характеризуватися за допомогою MS. За іншими варіантами здійснення як частину методики підготовки зразка MS можна застосовувати такі методики MS як MALDI для вивільнення сполуки з матриксу, зокрема якщо спочатку застосовують лабільний зв'язок, для фіксування сполуки на матриксі. Наприклад, гранулу, вибрану з бібліотеки, можна ірадіювати на етапі MALDI для вивільнення різновиду з матриксу та іонізувати різновиду для аналізу MS. Багатошпильковий синтез [0216] В бібліотеках даного способу застосовують формат багатошпилькової бібліотеки. Коро 95604 60 тко, Geysen та співробітники (Geysen et al. (1984) PNAS 81:3998-4002) запровадили спосіб для створення бібліотек сполук паралельним синтезом на поліакриловій кислоті на поліетиленових шпильках, розташованих на форматі мікротитрувального планшету. Методику Geysen можна застосовувати для синтезу та дослідження тисяч сполук за тиждень із застосуванням багатошпилькового способу, та зафіксовані сполуки можна повторно застосовувати в багатьох дослідах. Придатні лінкерні фрагменти також можна приєднати до шпильок, щоб сполуки могли відщепитися від конструкцій після синтезу для оцінювання чистоти та додаткового оцінювання (c.f, Bray et al. (1990) Tetrahedron Lett 31:5811-5814; Valerio et al. (1991) Anal Biochem 197:168-177; Bray et al. (1991) Tetrahedron Lett 32:6163-6166). Розподіл-з'єднання-рекомбінація [0217] За ще одним варіантом здійснення різноманітну бібліотеку сполук можна забезпечити на наборі гранул за допомогою принципу розподілз'єднання-рекомбінація (див., наприклад, Houghten (1985) PNAS 82:5131-5135; та патенти США №№№ 4631211; 5440016; 5480971). Коротко, як припускає назва, на кожному етапі синтезу, де в бібліотеку вводять виродження, гранули розділяють на окремі групи, рівні числу різних замісників, яких додадуть в конкретне положення в бібліотеці, причому різні замісники, з'єднуються в окремих реакціях, а гранули рекомбіновані в одну групу для наступної ітерації. [0218] За одним варіантом здійснення принцип розподіл-з'єднання-рекомбінація можна здійснити за допомогою аналогічного підходу так званого способу "чайного пакетику", вперше розробленого Houghten, де синтез сполуки відбувається на смолі, що міститься всередині пористих поліпропіленових пакетів (Houghten et al. (1986) PNAS 82:5131-5135). Замісники приєднуються до смол, що несуть сполуку, при поміщенні пакетиків у відповідні реакційні розчини, тоді як всі традиційні етапи, такі як відмивання смоли і зняття захисних груп, проводять одночасно в реакційному резервуарі. В кінці синтезу кожний пакетик містить окрему сполуку. Комбінаторні Бібліотеки by Light-Directed, Просторово Addressable Parallel Хімічних. Синтез [0219] Схема комбінаторного синтезу, в якому ідентичність сполуки отримують шляхом визначення її місцеположення на субстраті для синтезу, називається просторово-доступний синтез. За одним варіантом здійснення комбінаторний процес проводять шляхом регулювання додавання хімічного реагенту до специфічних місцеположень на твердій основі (Dower et al. Cl 991) Annu Rep Med Chem 26:271-280; Fodor, S.P.A. (1991) Science 251:767; Pirrung et al. (1992) Патент США № 5,143,854; Jacobs et al. (1994) Trends Biotechnol 12:19-26). Просторове розрішення фотолітографії забезпечує мініатюризацію. Ця методика може бути проведена з використанням реакцій захищення/зняття захисту з фотолабільними захисними групами. [0220] Ключові етапи цієї технології проілюстровані у Gallop et al. (1994) J Med Chem 37:1233
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod of modulating the pharmacokinetic and/or pharmacodynamic properties of a compound
Автори англійськоюDuffy David, Grogan Michael, Kates Steven, Ostuni Emanuele, Schueller Olivier, Sweetnam Paul, Stewart Campbell
Назва патенту російськоюСпособ регулирования фармакокинетического и/или фармакодинамического свойства соединения
Автори російськоюДаффи Девид, Гроган Майкл, Кейтс Стивен, Остуни Эмануэль, Шюллер Оливер, Свитнем Пол, Стюарт Кемпбелл
МПК / Мітки
МПК: A61K 31/53
Мітки: регулювання, спосіб, фармакодинамічної, фармакокінетичної, сполуки, властивості
Код посилання
<a href="https://ua.patents.su/45-95604-sposib-regulyuvannya-farmakokinetichno-ta-abo-farmakodinamichno-vlastivosti-spoluki.html" target="_blank" rel="follow" title="База патентів України">Спосіб регулювання фармакокінетичної та/або фармакодинамічної властивості сполуки</a>
Попередній патент: Спосіб, пристрій і система для надання візуальних ознак, що ідентифікують фінансові рахунки
Наступний патент: Спосіб візування цифровою камерою
Випадковий патент: Гумова суміш для шумозахисного матеріалу