Ціаноантраніламідні сполуки, композиція та спосіб регулювання кількості шкідників
Номер патенту: 81791
Опубліковано: 11.02.2008
Автори: Стівенсон Томас Мартін, Селбі Томас Пол, Хьюз Кеннет Ендрю, Лам Джордж Філіп
Формула / Реферат
1. Сполука формули І, її N-оксид або сіль
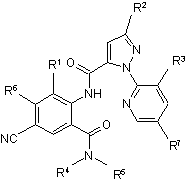 ,I
,I
де
R1 є Ме, Cl, Br aбo F;
R2 є F, Сl, Вr, С1-С4 галоалкіл або С1-С4 галоалкокси;
R3 є F, Сl або Вr;
R4 є Н; С1-С4 алкілом; С3-С4 алкенілом, С3-С4 алкінілом, С3-С5 циклоалкілом або С4-С6 циклоалкілалкілом, кожний з яких необов’язково заміщений одним замісником, вибраним з групи, що складається з галогену, CN, SMе, S(O)Me, S(O)2Me та OМe;
R5 є Н або Me;
R6 є H, F або Сl; і
R7 є H, F або Сl.
2. Сполука за п. 1, яка відрізняється тим, що
R1 є Mе або Сl;
R2 є Сl, Вr, CF3, OCF2H, OCF3 або OCH2CF3; та
R4 є Н, Ме, Et, i-Pr, t-Bu, CH2CN, СН(Me)СН2SMе або C(Me)2CH2SMe.
3. Сполукa за п. 2, яка відрізняється тим, що
R2 є Сl, Вr, CF3 або OCH2CF3;
R4 є Н, Me, Et або і-Рr; та
R5 є H.
4. Композиція для регулювання кількості безхребетних шкідників, що містить біологічно ефективну кількість сполуки за п. 1 та принаймні один додатковий компонент, вибраний з групи, яка складається з поверхнево-активної речовини, твердого розріджувача та рідкого розріджувача.
5. Композиція за п. 4, яка відрізняється тим, що додатково містить ефективну кількість принаймні однієї додаткової біологічно активної сполуки або агента.
6. Композиція за п. 5, яка відрізняється тим, що принаймні одна біологічно активна сполука або агент вибрані із інсектицидів групи, яка складається з піретроїду, карбамату, неонікотиноїду, нейронного блокатора натрієвих каналів, інсектицидного макроциклічного лактону, антагоністу γ-аміномасляної кислоти (GABA), інсектицидної сечовини, міметика ювенільного гормону, члена Bacillus thuringiensis, Bacillus thuringiensis дельта ендотоксину та природного або генетично модифікованого вірусного інсектициду.
7. Композиція за п. 5, яка відрізняється тим, що принаймні одна біологічно активна сполука або агент вибрані із групи, яка містить абамектин, ацефат, ацетаміприд, ацетопрол, амідофлумет (S-1955), авермектин, азадирактин, азинфос-метил, біфентрин, біфеназат, бістрифлурон, бупрофезин, карбофуран, хлорфенапір, хлорфлуазурон, хлорпірифос, хлорпірифос-метил, хлормафенозид, клотіанідин, цифлутрин, бета-цифлутрин, цигалотрин, ламбда-цигалотрин, циперметрин, циромазин, дельтаметрин, діафентіурон, діазинон, дифлубензурон, диметоат, динотефуран, діофенолан, емамектин, ендосульфан, есфенвалерат, етипрол, фенотікарб, феноксикарб, фенпропатрин, фенвалерат, фіпроніл, флонікамід, флюцитринат, тау-флувалінат, флуфенерим (UR-50701), флуфеноксурон, гамма-калотрин, галофенозид, гексафлумурон, імідаклоприд, індоксакарб, ізофенфос, луфенурон, малатіон, метальдегід, метамідофос, метидатіон, метоміл, метопрен, метоксихлор, метоксифенозид, метофлутрин, монокротофос, метоксифенозид, новалурон, новіфлумурон (XDE-007), оксаміл, паратіон, паратіон-метил, перметрин, форат, фосалон, фосмет, фосфамідон, піримікарб, профенофос, профлутрин, протрифенбут, піметрозин, піридаліл, пірипроксифен, ротенон, S 1812 (Vаlent) спіносад, спіромезифен (BSN 2060), сульпрофос, тебуфенозид, тефлубензурон, тефлутрин, тербуфос, тетрахлорвінфос, тіаклоприд, тіаметоксам, тіодикарб, тіосультап-натрій, толфенпірад, тралометрин, трихлорфон та трифлумурон, алдикарб, фeнаміфос, амітраз, кінометіонат, хлоробензилат, цигексатин, дикофол, дієнохлор, етоксазол, феназахін, фенбутатин оксид, фенпіроксимат, гекситіазокс, пропаргіт, піридабен, тебуфенпірад, Bacillus thuringiensis aizawai, Bacillus thuringiensis kurstaki, Bacillus thuringiensis дельта ендотоксин, бакуловірус, ентомопатогенні бактерії, ентомопатогенні віруси та ентомопатогенні грибки.
8. Композиція за п. 5, яка відрізняється тим, що принаймні одна біологічно активна сполука або агент вибрані із групи, яка містить ацетаміприд, циперметрин, цигалотрин, цифлутрин та бета-цифлутрин, есфеквалерат, фенвалерат, тралометрин, фенотикарб, метоміл, оксаміл, тіодикарб, клотіанідин, імідаклоприд, тіаклоприд, індоксакарб, спіносад, абамектин, авермектин, емамектин, ендосульфан, етипрол, фіпроніл, флуфеноксурон, трифлумурон, діофенолан, пірипроксифен, піметрозин, амітраз,. Bacillus thuringiensis aizawai, Bacillus thuringiensis kurstaki, Bacillus thuringiensis дельта ендотоксин та ентомопатогенні грибки.
9. Композиція за п. 4, яка відрізняється тим, що має форму рідкого препарату з можливістю просочування через грунт.
10. Композиція за п. 4, яка відрізняється тим, що має форму спреєвої композиції, де рідким розріджувачем є пропелант.
11. Композиція за п. 4, яка відрізняється тим, що має форму приманкової композиції, де рідкий розріджувач містить один або більше харчових матеріалів та вибірково містить атрактант та/або зволожувач.
12. Спосіб регулювання кількості безхребетних шкідників, що включає етап, на якому біологічно ефективну кількість сполуки за п. 1 або композицію за п. 4 піддають контакту з безхребетними шкідниками або їх оточенням.
13. Спосіб за п. 12, який відрізняється тим, що безхребетним шкідником є тарган, мурашка або терміт, та контакт здійснюють шляхом уживання шкідником композиції у формі приманкової композиції.
14. Спосіб за п. 12, який відрізняється тим, що безхребетним шкідником є москіт, скатопсид, жигалка осіння, жигалка оленяча, жигалка кінська, оса, жовта личинка, шершень, кліщ, павук, мурашка або комар, та контакт здійснюють шляхом розпилювання композиції у формі спреєвої композиції із контейнера зі спреем.
15. Спосіб за п. 12, який відрізняється тим, що контакт композиції з рослиною здійснюють шляхом просочування ґрунту композицією у формі рідкого препарату.
Текст
1. Сполука формули І, її N-оксид або сіль R2 C2 2 (19) 1 3 81791 4 фенотікарб, феноксикарб, фенпропатрин, фенвалерат, фіпроніл, флонікамід, флюцитринат, тау-флувалінат, флуфенерим (UR-50701), флуфеноксурон, гамма-калотрин, галофенозид, гексафлумурон, імідаклоприд, індоксакарб, ізофенфос, луфенурон, малатіон, метальдегід, метамідофос, метидатіон, метоміл, метопрен, метоксихлор, метоксифенозид, метофлутрин, монокротофос, метоксифенозид, новалурон, новіфлумурон (XDE-007), оксаміл, паратіон, паратіон-метил, перметрин, форат, фосалон, фосмет, фосфамідон, піримікарб, профенофос, профлутрин, протрифенбут, піметрозин, піридаліл, пірипроксифен, ротенон, S 1812 (Vаlent) спіносад, спіромезифен (BSN 2060), сульпрофос, тебуфенозид, тефлубензурон, тефлутрин, тербуфос, те трахлорвінфос, тіаклоприд, тіаметоксам, тіодикарб, тіосультап-натрій, толфенпірад, тралометрин, трихлорфон та трифлумурон, алдикарб, фeнаміфос, амітраз, кінометіонат, хлоробензилат, цигексатин, дикофол, дієнохлор, етоксазол, феназахін, фенбутатин оксид, фенпіроксимат, гекситіазокс, пропаргіт, піридабен, тебуфенпірад, Bacillus thuringiensis aizawai, Bacillus thuringiensis kurstaki, Bacillus thuringiensis дельта ендотоксин, бакуловірус, ентомопатогенні бактерії, ентомопатогенні віруси та ентомопатогенні грибки. 8. Композиція за п. 5, яка відрізняється тим, що принаймні одна біологічно активна сполука або агент вибрані із групи, яка містить ацетаміприд, циперметрин, цигалотрин, цифлутрин та бетацифлутрин, есфеквалерат, фенвалерат, тралометрин, фенотикарб, метоміл, оксаміл, тіодикарб, клотіанідин, імідаклоприд, тіаклоприд, індоксакарб, спіносад, абамектин, авермектин, емамектин, ендосульфан, етипрол, фіпроніл, флуфеноксурон, трифлум урон, діофенолан, пірипроксифен, піметрозин, амітраз,. Bacillus thuringiensis aizawai, Bacillus thuringiensis kurstaki, Bacillus thuringiensis дельта ендотоксин та ентомопатогенні грибки. 9. Композиція за п. 4, яка відрізняється тим, що має форму рідкого препарату з можливістю просочування через грунт. 10. Композиція за п. 4, яка відрізняється тим, що має форму спреєвої композиції, де рідким розріджувачем є пропелант. 11. Композиція за п. 4, яка відрізняється тим, що має форму приманкової композиції, де рідкий розріджувач містить один або більше харчових матеріалів та вибірково містить атрактант та/або зволожувач. 12. Спосіб регулювання кількості безхребетних шкідників, що включає етап, на якому біологічно ефективну кількість сполуки за п. 1 або композицію за п. 4 піддають контакту з безхребетними шкідниками або їх о точенням. 13. Спосіб за п. 12, який відрізняється тим, що безхребетним шкідником є тарган, мурашка або терміт, та контакт здійснюють шляхом уживання шкідником композиції у формі приманкової композиції. 14. Спосіб за п. 12, який відрізняється тим, що безхребетним шкідником є москіт, скатопсид, жигалка осіння, жигалка оленяча, жигалка кінська, оса, жовта личинка, шершень, кліщ, павук, мурашка або комар, та контакт здійснюють шляхом розпилювання композиції у формі спреєвої композиції із контейнера зі спреем. 15. Спосіб за п. 12, який відрізняється тим, що контакт композиції з рослиною здійснюють шляхом просочування ґрунту композицією у формі рідкого препарату. Даний винахід стосується деяких антраніламідів, їх N-оксидів, солей та композицій, що придатні для сільськогосподарських або несільськогосподарських застосувань, включаючи застосування, які перелічені нижче, та способу їх використання для регулювання кількості безхребетних шкідників у сільськогосподарському та несільськогосподарському середовищах. Регулювання кількості безхребетних шкідників є надзвичайно важливим у досягненні високої ефективності врожаїв. Шкода, що наноситься безхребетними шкідниками зростаючим сільськогосподарським культурам та культурам, що зберігаються, може спричинити суттєве зниження продуктивності і таким чином зумовити підвищену вартість для споживачів. Важливим є також контроль безхребетних шкідників у галузях лісівництва, оранжерейних культур, декоративних культур, розсадникових культур, зберігання харчових та волоконних продуктів, скотарстві, домашньому господарстві, важливим є також здоров'я людей та тварин. Багато продуктів для цих цілей є у продажу, але потреба у нових сполуках, котрі є більш ефективними, більш дешевими, менш токсичними, більш безпечними для довкілля та з різними способами дії, зберігається. [WO 01/070671] розкриває похідні N-ацил антранілової кислоти Формули і як артроподициди де, зокрема, А та В являють собою, незалежно, О або S; J являє собою заміщене, при потребі, фенільне кільце, 5- або 6-членне гетероароматичне кільце, нафтильну кільцеву систему або ароматичну 8-, 9- або 10-членну злиту 5 81791 гетеробіциклічну кільцеву систему; R1 та R3 являють собою, незалежно, Η або заміщений, при потребі, С1-С6 алкіл; R2 являє собою Η або С1-С6 алкіл; кожна R4 являє собою, незалежно, Н, С1-С6 алкіл, С1-С6 галоалкіл, галоген або CN; і n дорівнює 1-4. Даний винахід стосується сполук Формули 1, їх N-оксидів або солей де R1 являє собою Me, Cl, Вr або F; R2 являє собою F, СІ, Вr, С1-С4 галоалкіл або С1-С4 галоалкокси; R3 являє собою F, СІ або Вr; R4 являє собою Н; С1-С4 алкіл; С3-С4 алкеніл, С3-С4 алкініл, С3-С5 циклоалкіл, або С4-С6 циклоалкілалкіл, кожна заміщена, при потребі, одним замісником, що вибирається із групи, яка складається із галогену, CN, SMe, S(O)Me, S(O)2 Me та ОМе; R5 являє собою Η або Me; R6 являє собою Н, F або СІ; і R7 являє собою Н, F або СІ. Даний винахід також стосується композиції для контролю безхребетних шкідників, що містить біологічно ефективну кількість сполуки Формули 1 та принаймні один додатковий компонент, котрий вибирається із групи, яка складається із поверхнево-активної речовини, твердого розріджувача та рідкого розріджувача, і, при потребі, ефективної кількості принаймні однієї додаткової біологічно активної сполуки або агента. Цей винахід також стосується способу регулювання кількості безхребетних шкідників, що включає контактування зазначеного безхребетного шкідника або його оточення з біологічно ефективною кількістю сполуки Формули 1 (наприклад, як композиції, що тут описана). Даний винахід також стосується способу контролю безхребетних шкідників, що включає контактування зазначеного безхребетного шкідника або його оточення з біологічно ефективною кількістю композиції, котра містить біологічно ефективну кількість сполуки Формули 1 та принаймні один додатковий компонент, який вибирається із групи, що складається із 6 поверхнево-активної речовини, твердого розріджувача та рідкого розріджувача, зазначена композиція додатково включає, при потребі, ефективну кількість принаймні однієї додаткової біологічно активної сполуки або агента. Даний винахід додатково стосується розпилювальної композиції, що містить сполуку Формули 1 і диспергатор, та приманкової композиції, яка містить сполуку Формули 1, один або кілька харчових продуктів, при потребі, атрактант, та, при потребі, зволожувач. Даний винахід також стосується пристрою для регулювання кількості безхребетних шкідників, що включає зазначену приманкову композицію та корпус, пристосований для розміщення зазначеної приманкової композиції, де зазначений корпус має принаймні один отвір, розмір якого дозволяє даному безхребетному шкіднику проходити через зазначений отвір, так що даний безхребетний шкідник може скористатись доступом до зазначеної приманкової композиції із місця знаходження поза даним корпусом, і де зазначений корпус додатково пристосований для розміщення в/поблизу осередку потенційної або відомої діяльності зазначеного безхребетного шкідника. У наведеному вище тексті вираз "алкіл", коли він використовується окремо або у словосполученнях, таких як "алкілтіо" або "галоалкіл", включає прямий або розгалужений алкіл, такий як метил, етил, n-пропіл, і-пропіл або різні ізомери бутилу. Вираз "галоген", коли він використовується окремо або у словосполученнях, таких як "галоалкокси", включає фтор, хлор, бром або йод. Крім того, при використанні у словосполученнях, таких як "галоалкіл" або "галоалкокси", зазначений алкіл або алкокси може бути частково або повністю заміщений атомами галогену, котрі можуть бути однаковими або різними. Приклади "галоалкілу" включають F3C, СlСН2, CF3CH2 та CF3CCI2. Приклади "галоалкокси" включають CF3O, HCF2O, ССl3СН2О, HCF2CH2CH2O та CF3CH2O. Фахівцеві у даній галузі зрозуміло, що не всі гетероцикли, котрі містять азот, можуть утворювати N-оксиди, оскільки азот потребує наявної окремої пари для окиснення до даного оксиду; фа хівець у даній галузі розпізнає саме ті гетероцикли, що містять азот, котрі можуть утворювати N-оксиди. Фахівець у даній галузі також розпізнає третинні аміни, котрі утворюють Nоксиди. Синтетичні методи для одержання Nоксидів гетероциклів та третинних амінів дуже добрі відомі фахівцям у даній галузі, включаючи окиснення гетероциклів та третинних амінів пероксикислотами, такими як пероцтова та nхлоропербензойна кислота (МСРВА), пероксидом водню, алкіл гідропероксидами, такими як t-бутил гідропероксид, перборатом натрію та діокстранами, такими як диметидіоксиран. Зазначені методи для одержання N-оксидів широко описані та оглянуті у літературі, дивись, наприклад, [T.L. Gilchrist in Comprehensive Organic Synthesis, vol.7, pp.748-750, S.V. Ley, Ed., Pergamon Press; M. Tisler and B. Stanovnik in 7 81791 Comprehensive Heterocyclic Chemistry, vol.3, pp.1820, A.J. Boulton and A. McKillop, Eds., Pergamon Press; M.R. Grimmett and B.R.T. Keene in Advances in Heterocyclic Chemistry, vol.43, pp.149-161, A.R. Katritzky, Ed., Academic Press; M. Tisler and B. Stanovnik in Advances in Heterocyclic Chemistry, vol.9, pp.285-291, A.R. Katritzky and A.J. Boulton, Eds., Academic Press; and G.W.H. Cheeseman and E.S.G. Werstiuk in Advances in Heterocyclic Chemistry, vol.22, pp.390-392, A.R. Katritzky and A.J. Boulton, Eds., Academic Press]. Сполуки даного винаходу можуть існувати як один або кілька стереоізомерів. Різні стереоізомери включають енантіомери, діастереомери, атропізомери та геометричні ізомери. Фахівцеві у даній галузі зрозуміло, що один стереоізомер може бути більш активним та/або може виявляти сприятливі ефекти, коли їм збагатити (відносно іншого(ших)) суміш або коли його відокремити від іншого(ших) стереоізомерів. Крім того, фахівцеві у даній галузі відомо, яким чином відокремити, збагатити та/або селективно одержати зазначені стереоізомери. Відповідно, даний винахід включає сполуки, що вибираються із сполук Формули 1, їх N-оксидів та солей. Сполуки даного винаходу можуть бути присутніми як суміш стереоізомерів, окремі стереоізомери або як оптично активна форма. Солі сполук даного винаходу включають кислі солі приєднання неорганічних або органічних кислот, таких як бромистоводнева, хлористоводнева, азотна, фосфорна, сірчана, оцтова, масляна, фумарова, молочна, малеїнова, малонова, щавлева, пропіонова, саліцилова, винна, 4-толуолсульфонова або валеріанова кислота. У композиціях та методах даного винаходу солі сполук даного винаходу придатні, краще, для сільськогосподарських та/або несільськогосподарських застосувань, що описані в даному тексті. Заслуговують на ува гу сполуки Формули 1, де R4 являє собою Η або С1-С4 алкіл, заміщений, при потребі, одним замісником, що вибирається із групи, яка складається із CN, SMe та ОМе; R5 являє собою Η або Me; R6 являє собою Н; і R7 являє собою Н. Сполуки, яким віддається перевага виходячи із вартості, легкості синтезу та/або біологічної ефективності, є наступними: "Яким віддається перевага 1". Сполуки Формули 1, де R1 являє собою Me або СІ; R2 являє собою СІ, Вr, CF3, OCF2H, OCF3 або OCH2CF3; і R4 являє собою Н, Me, Et, і-Рr, t-Bu, CH 2CN, CH(Me)CH2SMe або C(Me)2CH2SMe. "Яким віддається перевага 2". Сполуки, "Яким віддається перевага 1", де R2 являє собою СІ, Вr, CF 3 або OCH2CF3 ; R4 являє собою Н, Me, Et або і-Pr; та R5 являє собою Н. Заслуговують на увагу сполуки "Яким віддається перевага 1" та сполуки "Яким 8 віддається перевага 2", де R6 являє собою Н; і R7 являє собою Н. Композиціями даного винаходу, яким віддається перевага, є такі, що включають вищенаведені сполуки, яким віддається перевага. Способи застосування, яким віддається перевага, є ті, що включають вищенаведені сполуки, яким віддається перевага. Сполуки Формули 1 можуть бути одержані з використанням одного або кількох наступних способів або їх варіацій, як показано на Схемах 120. Коли не зазначено інше, визначення R 1, R2, R3 R4 та R5 у сполуках Формул 1-24 нижче є такими, що визначені вище у розділі Стислий виклад винаходу. Сполуки Формули 1 можуть бути одержані шляхом реакції бензоксазинонів Формули 2 з аміном Формули HNR4R5 як окреслено на Схемі 1. Ця реакція може відбуватись у чистому вигляді або у різновиді придатних розчинників, включаючи тетрагідрофуран, діетиловий ефір, діоксан, толуол, ди хлорометан або хлороформ, при оптимальних температурах, що варіюють від кімнатної температури до температури відгонки даного розчинника. Загальна реакція бензоксазинонів з амінами для одержання антраніламідів добре документована у хімічній літературі. Для огляду хімії бензоксазинонів дивись [Jakobsen et al., Bioorganic and Medicinal Chemistry 2000, 8, 2095-2103 та посилання у цій роботі. Дивись також G,M, Coppola, J. Heterocyclic Chemistry 1999, 36, 563-588]. Сполуки Формули 1 можуть бути також отримані із галоантранілових діамідів Формули 3 (де X являє собою галоген, краще, йод або бром) способом сполучення, показаним на Схемі 2. Реакція сполуки Формули 3 з ціанідом металу (наприклад, ціанідом одновалентної міді, ціанідом цинку або ціанідом калію), при потребі, з (або без нього) придатним паладієвим каталізатором [наприклад, тетракіс(трифенілфосфін)паладій(0) або дихлоробіс(трифенілфосфін)паладій(II)], з (або без) галогенідом металу (наприклад, йодидом одновалентної міді, йодидом цинку або йодидом калію) у придатному розчиннику, такому як ацетонітрил, Ν,Ν-диметилформамід або Nметилпіролідинон, при потребі, при температурах, що варіюють від кімнатної температури до температури відгонки даного розчинника, дає сполуки Формули 1. Придатний розчинник може також бути те трагідрофураном або діоксаном, коли у зазначеній реакції сполучення використовується паладієвий каталізатор. 9 81791 Ціанобензоксазинони Формули 2 можуть бути одержані за способом, що окреслений на Схемі 3. Реакція галобензоксазинону Формули 4 (де X являє собою галоген, краще, йод або бром) з ціанідом металу з використанням схожого методу, як описано вище для Схеми 2 (при потребі, з або без паладієвого каталізатора та, при потребі, з або без галогеніду металу) дає сполуку Формули 2. Ціанобензоксазинони Формули 2 можуть бути також одержані за способом, що деталізований на Схемі 4, шляхом сполучення піразолкарбонової кислоти Формули 5 з ціаноантраніловою кислотою Формули 6. Ця реакція включає послідовне додавання метансульфонілхлориду у присутності третинного аміну, такого як триетиламін, або піридину до піразолкарбонової кислоти Формули 5, з наступним додаванням ціаноантранілової кислоти Формули 6, з наступним другим додаванням третинного аміну та метансульфонілхлориду. Схема 5 зображує інший спосіб одержання бензоксазинонів Формули 2, що включає сполучення ізатинового ангідриду Формули 7 з піразоловим хлорангідридом Формули 8. Для цієї реакції годяться такі розчинники як піридин або піридин/ацетонітрил. Хлорангідриди Формули 8 можуть отримуватись із відповідних кислот Формули 5 з використанням відомих методів, таких як хлорування тіонілхлоридом або оксалілхлоридом. 10 Як показано на Схемі 6, галоантранілові діаміди Формули 3 можуть бути одержані за реакцією бензоксазинонів Формули 4, де X являє собою галоген, з аміном Формули HNR4R5 з використанням схожого способу, який описаний вище для Схеми 1. Умови цієї реакції подібні до таких, що визначені на Схемі 1. Як показано на Схемі 7, галобензоксазинони Формули 4 (де X являє собою галоген) можуть бути одержані шляхом прямого сполучення піридилпіразолкарбонової кислоти Формули 5 з галоантраніловою кислотою Формули 9 (де X являє собою галоген) з використанням способу, подібного до описаного вище для Схеми 4. Дана реакція включає послідовне додавання метансульфонілхлориду у присутності третинного аміну, такого як триетиламін, або піридину до піразолкарбонової кислоти Формули 5, з наступним додаванням галоантранілової кислоти Формули 9, з наступним другим додаванням третинного аміну та метансульфонілхлориду. Цей спосіб звичайно дає високі виходи бензоксазинону. Як показано на Схемі 8, галобензоксазинон Формули 4 може бути також одержаний шляхом сполучення ізатинового ангідриду Формули 10 (де X являє собою галоген) з піразоловим хлорангідридом Формули 8 за методом, подібним до того, що описаний вище для Схеми 5. 11 81791 12 трифосген) або алкіл хлороформіатом, наприклад, метил хлороформіатом, у придатному розчиннику, такому як толуол або тетрагідрофуран. Ціаноантранілові кислоти Формули 6 можуть бути одержані із галоантранілових кислот Формули 9, як окреслено на Схемі 9. Реакція галоантранілової кислоти Формули 9 (де X являє собою галоген) з ціанідом металу з використанням тієї ж самої процедури сполучення, що описана вище для Схеми 2 (при потребі, з або без паладієвого каталізатора та, при потребі, з або без галогеніду металу) дає сполуку Формули 6. Піридилпіразолкарбонові кислоти Формули 5 можуть бути одержані з використанням способу, окресленого на Схемі 13. Реакція піразолу 12 з 2галопіридином Формули 13 у присутності придатної основи, такої як карбонат калію, у розчиннику, такому як Ν,Ν-диметилформамід або ацетонітрил, дає високі виходи 1-піридилпіразолу 14 з високою специфічністю щодо потрібної регіохімії. Металування 14 літій діізопропіламідом (LDA) з наступним гасінням літієвої солі діоксидом вуглецю дає піразолкарбонову кислоту Формули 5. Як показано на Схемі 10, ціаноізатинові ангідриди Формули 7 можуть бути одержані із ціаноантранілових кислот Формули 6 за реакцією з фосгеном (або еквівалентом фосгену, таким як трифосген) або алкіл хлороформіатом (наприклад, метил хлороформіатом) у придатному розчиннику, такому як толуол або тетрагідрофуран. Як показано на Схемі 11, галоантранілові кислоти Формули 9 можуть бути одержані шляхом прямого галогенування незаміщеної антранілової кислоти Формули 11 N-хлоросукцинімідом (NCS), N-бромосукцинімідом (NBS) або Nйодосукцинімідом (NIS), відповідно, у розчинниках, таких як Ν,Ν-диметилформамід (DMF), з одержанням відповідної галоген-заміщеної кислоти Формули 9. Як проілюстровано на Схемі 12, галоізатинові ангідриди Формули 10 можуть бути одержані із галоантранілових кислот Формули 9 за реакцією з фосгеном (або еквівалентом фосгену, таким як Вихідні піразоли 12, де R2 являє собою CF3, СІ або Вr, є відомими сполуками. Піразол 12, де R2 являє собою CF3, може бути одержаний згідно з процедурами, що описані у літературі [J. Fluorine Chem.1991, 53(1), 61-70]. Піразоли 12, де R2 являє собою СІ або Вr, також можуть бути одержані за способами, що відомі із літератури [Н. Reimlinger and A. Van Overstraeten, Chem. Ber. 1966, 99(10), 3350-7]. Корисний альтернативний спосіб одержання 12, де R2 являє собою СІ або Вr, поданий на Схемі 14. Металування сульфамоїлпіразолу 15 n-бутиллітієм з наступним прямим галогенуванням даного аніону гексахлороетаном (коли R2 являє собою СІ) або 1,2-дибромотетрахлороетаном (коли R2 являє собою Вr) дає галогеновані похідні 16 (де R 2 являє собою СІ або Вr). Вилучення сульфамоїльної групи трифторооцтовою кислотою (TFA) при кімнатній температурі проходить чисто і з високим виходом, з утворенням піразоліл 12, де R2 являє собою СІ або Вr, відповідно. 13 81791 Як альтернатива до способу, що проілюстрований на Схемі 13, піразолкарбонові кислоти Формули 5, де R2 являє собою CF3, можуть бути також одержані за способом, що окреслений на Схемі 15. Реакція сполуки 17 (де R8 являє собою С 1-С4 алкіл) з придатною основою у 13 придатному органічному розчиннику дає циклізований продукт Формули 18 після нейтралізації кислотою, такою як оцтова кислота. Придатною основою може бути, наприклад, але не обмежуючись цим, гідрид натрію, калій tбутоксид, димзил натрію (CH3S(O)CH2-Na+), карбонати або гідроксиди лужного металу (такого як літій, натрій або калій), фториди або гідроксиди тетраалкіл (такий як метил, етил або бутил) амонію, або 2-трет-бутиламіно-2-діетиламіно-1,3диметил-пергідро-1,3,2-діазафосфонін. Придатним органічним розчинником може бути, наприклад, але не обмежуючись цим, ацетон, ацетонітрил, тетрагідрофуран, дихлорометан, диметилсульфоксид, або Ν,Ν-диметилформамід. Реакція циклізації звичайно проводиться у температурних межах від приблизно 0 до 120°С. Ефекти розчинника, основи, температури та часу введення взаємозв'язані, і вибір умов реакції важливий для мінімізації утворення супутніх продуктів. Основою, якій віддається перевага, є тетрабутиламоній фторид. Дегідратація сполуки Формули 18 з утворенням сполуки Формули 19, з наступним гідролізом карбонільно-ефірної групи до карбонової кислоти дає сполуку Формули 5. Дегідратація проводиться шляхом обробки каталітичною кількістю придатної кислоти. Ця каталітична кислота може являти собою, наприклад, але не обмежуючись цим, сірчану кислоту. Дана реакція проводиться, загалом, з використанням органічного розчинника. Як відомо фа хівцеві у даній галузі, реакції дегідратації можуть здійснюватись у широкому різновиді розчинників, наприклад, оцтовій кислоті, у температурному інтервалі, загалом, від приблизно 0 до 200°С, краще, від 0 до 100°С. Карбонові ефіри Формули 19 можуть бути перетворені у карбонові кислоти Формули 5 з використанням множини способів, включаючи нуклеофільне розщеплення за безводних умов або гідролітичні методи, включаючи використання кислот або основ [дивись огляд методів у роботі T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 2nd ed., John Wiley & Sons, Inc., New York, 1991, pp.224-269]. Для способу Схеми 15 перевага віддається гідролітичним методам, що каталізуються основою. Придатні основи включають 14 гідроксиди лужних металів (таких як літій, натрій або калій). Наприклад, даний ефір може бути розчинений у суміші води та спирту, 14 такого як етанол. Після обробки гідроксидом натрію або гідроксидом калію даний ефір омилюється з одержанням натрієвої або калієвої солі даної карбонової кислоти. Підкислення сильною кислотою, такою як хлористоводнева кислота або сірчана кислота, дає карбонову кислоту Формули 5. Сполуки Формули 17, де R2 являє собою CF3, можуть бути отримані за способом, що окреслений на Схемі 16. Обробка гідразинової сполуки Формули 20 кетоном Формули CH3COR2 у розчиннику, такому як вода, метанол чи оцтова кислота, дає гідразон Формули 21. Фахівцеві у даній галузі зрозуміло, що дана реакція може потребувати каталізу, при потребі, за допомогою кислоти та може також потребувати застосування підвищених температур, у залежності від схеми молекулярного заміщення гідразону Формули 21. Реакція даного гідразону Формули 21 з алкілхлорооксалатом у придатному органічному розчиннику, такому як, наприклад, але не обмежуючись цим, дихлорометан або тетрагідрофуран, у присутності поглинача кислоти, такого як триетиламін, дає сполуку Формули 17. Дана реакція звичайно проводиться при температурі у межах від приблизно 0 до 100°С. Гідразинові сполуки Формули 20 можуть бути одержані з використанням стандартних способів, таких як за реакцією відповідного галопіридину Формули 13 з гідразином. Як альтернатива до способу, що ілюструється Схемою 13, піразолкарбонові кислоти Формули 5, де R2 являє собою СІ або Вr, можуть також бути одержані за способом, що окреслений на Схемі 17. Окиснення сполуки Формули 22, при потребі, у присутності кислоти, дає сполуку Формули 19, де R2 являє собою СІ або Вr. Гідроліз даної карбоново-ефірної групи до карбонової кислоти запроваджує сполуку Формули 5. де R8 являє собою С 1-С4 алкіл. Окиснювальним агентом для перетворення сполуки Формули 22 у сполуку Формули 19 може бути пероксид водню, органічні пероксиди, персульфат калію, персульфат натрію, персульфат амонію, моноперсульфат калію (наприклад, Оксон (Охоnе®)) або перманганат 15 81791 калію. Для одержання повного перетворення слід використовува ти принаймні один еквівалент окиснювального агента щодо сполуки Формули 22, краще, від одного до двох еквівалентів. Зазначене окиснення здійснюється, типово, у присутності розчинника. Даним розчинником може бути простий ефір, такий як тетрагідрофуран, р-діоксан і таке подібне, органічний складний ефір, такий як етилацетат, диметилкарбонат і таке подібне, або полярний апротонний органічний розчинник, такий як Ν,Ν-диметилформамід, ацетонітрил і таке подібне. Кислоти, придатні для використання на стадії окиснення, включають неорганічні кислоти, такі як сірчана кислота, фосфорна кислота і таке подібне, та органічні кислоти, такі як оцтова кислота, бензойна кислота і таке подібне. Може використовува тись від одного до п'яти еквівалентів кислоти. Окиснювачем, якому віддається перевага, є персульфат калію, і зазначене окиснення проводиться, краще, у присутності сірчаної кислоти. Дана реакція може проводитись шляхом змішування сполуки Формули 22 у потрібному розчиннику та кислоті, якщо остання використовується. Потім даний окиснювач може додаватись при зручній швидкості. Температура реакції, звичайно, варіює від 0°С до температури кипіння даного розчинника для досягнення прийнятного часу протікання даної реакції до її завершення. Способи, що придатні для перетворення ефіру Формули 19 у карбонову кислоту Формули 5, вже описані для Схеми 15. Сполуки Формули 22, де R2 являє собою галоген, і R8 являє собою С 1-С4 алкіл, можуть бути одержані із відповідних сполук Формули 23 як показано на Схемі 18. де R8 являє собою С 1-С4 алкіл. Обробка сполуки Формули 23 агентом галогенування, звичайно, у присутності розчинника, дає відповідну гало сполуку Формули 22. Реагенти галогенування, що можуть бути використані, включають оксигалогеніди фосфору, тригалогеніди фосфору, пентагалогеніли фосфор у, тіонілхлорид, дигалотриалкілфосфорани, дигалодифенілфосфорани, оксалілхлорид та фосген. Перевага віддається оксигалогенідам фосфор у та пентагалогенідам фосфору. Для досягнення повного перетворення слід використовува ти принаймні 0,33 еквіваленти оксигалогеніду фосфор у щодо сполуки Формули 23, краще, від приблизно 0,33 до 1,2 еквіваленти. Для досягнення повного перетворення слід 16 використовува ти принаймні 0,20 еквіваленти пентагалогеніду фосфору щодо сполуки Формули 23, краще, від приблизно 0,20 до 1,0 еквіваленти. Типові розчинники для зазначеного галогенування включають галогеновані алкани, такі як дихлорометан, хлороформ, хлоробутан і таке подібне, ароматичні розчинники, такі як бензол, ксилол, хлорбензол і таке подібне, прості ефіри, такі як тетрагідрофуран, р-діоксан, діетиловий ефір і таке подібне, та полярні апротонні розчинники, такі як ацетонітрил, Ν,Νдиметилформамід і таке подібне. При потребі, може бути додана органічна основа, така як триетиламін, піридин, Ν,Ν-диметиланілін або таке подібне. Крім того, можливе додавання каталізатора, такого як Ν,Ν-диметилформамід. Перевага віддається процесу, в якому зазначеним розчинником є ацетонітрил, і основа відсутня. Типово, коли використовується ацетонітрильний розчинник, нема потреби ані в основі, ані в каталізаторі. Перевага віддається процесу, в якому сполука Формули 23 розмішується в ацетонітрилі. Потім протягом зручного періоду часу додається галогенуючий реагент, і дану суміш витримують при потрібній температурі до завершення даної реакції. Температура реакції лежить, звичайно, у межах від 20°С до точки кипіння ацетонітрилу, і час реакції складає, типово, менше 2 годин. Потім дану реакційну масу нейтралізують неорганічною основою, такою як бікарбонат натрію, гідроксид натрію і таке подібне, або органічною основою, такою як ацетат натрію. Потрібний продукт Формули 22 може бути виділений з використанням способів, відомих фа хівцям у даній галузі, включаючи кристалізацію, екстракцію та дистиляцію. Як альтернатива, сполуки Формули 22, де R2 являє собою Вr або СІ, можуть бути одержані шляхом обробки відповідних сполук Формули 22, де R2 являє собою відмінний галоген (наприклад, СІ для Формули 22, де R2 являє собою Вr) або сульфонатну груп у, таку як р-толуолсуль фонат, бензолсудьфонат та метансульфонат, бромистим воднем або хлористим воднем, відповідно. За даним способом R2 галогеновий або сульфонатний замісник у сполуці Формули 22 заміщується Вr або СІ із бромистого водню або хлористого водню, відповідно. Дана реакція проводиться у придатному розчиннику, такому як дибромометан, дихлорометан, оцтова кислота, етилацетат або ацетонітрил. Дана реакція може проводитись при атмосферному тиску або близькому до нього, або при тиску, ви ще атмосферного, в автоклаві. Галогенуючий реагент може додаватись у формі газу до даної реакційної суміші, що містить сполуку Формули 23 та розчинник. Коли R2 у ви хідній сполуці Формули 22 являє собою галоген, такий як СІ, дана реакція проводиться, краще, у такий спосіб, що барботаж або інший придатний засіб сприяє вилученню галогеніду водню, який генерується зазначеною реакцією. Як альтернатива, зазначений галогенуючий реагент може бути спочатку розчинений в інертному розчиннику, в якому він добре розчиняється (такому як оцтова кислота), 17 81791 перед контактуванням зі сполукою Формули 23 у чистому вигляді або в розчині. Дана реакція може проводитись при температурах від приблизно 0 до 100°С, найбільш зручно, при температурі, близькій до температури довкілля (наприклад, від приблизно 10 до 40°С), і ще краще, у межах від приблизно 20 до 30°С. Додавання каталізатору на основі кислот Льюїса (такого як трибромід алюмінію для приготування сполук Формули 22, де R2 являє собою Вr) може полегшити протікання даної реакції. Продукт Формули 22 виділяється з використанням відомих способів, що відомі фа хівцям у даній галузі, включаючи екстракцію, дистиляцію та кристалізацію. Вихідні сполуки Формули 22, де R2 являє собою сульфонатну гр упу, можуть бути одержані із відповідних сполук Формули 23 з використанням стандартних способів, таких як обробка сульфонілхлоридом (наприклад, ртолуолсульфонілхлоридом) та основою, такою як третинний амін (наприклад, триетиламін), у відповідному розчиннику, такому як дихлорометан. Як альтернатива до способу, що проілюстрований Схемою 13, піразолкарбонові кислоти Формули 5, де R2 являє собою галоалкокси, можуть бути також одержані за способом, окресленим на Схемі 19. Сполука Формули 23 окиснюється до сполуки Формули 24. Умови реакції для цього окиснення описані для перетворення сполуки Формули 22 у сполуку Формули 19 на Схемі 17. де R2 являє собою галоалкокси, і R8 є С1-С4 алкілом. Проміжна сполука Формули 24 потім піддається алкілуванню з утворенням сполуки Формули 19 (де R2 являє собою галоалкокси) шляхом реакції з відповідним агентом галоалкілування, таким як галоалкілгалогенід або сульфонат. Дана реакція проводиться у присутності принаймні одного еквівалента основи. Придатні основи включають неорганічні основи, такі як карбонати, гідроксиди та гідриди лужних металів (таких як літій, натрій або калій), або органічні основи, такі як триетиламін, діізопропілетиламін та 1,8діазабіцикло[5,4,0]ундец-7-ен. Дана реакція, загалом, проводиться у розчиннику, котрий може включати спирти, такі як метанол та етанол, галогеновані алкани, такі як дихлорометан, ароматичні розчинники, такі як бензол, толуол та хлоробензол, прості ефіри, такі як тетрагідрофуран, і полярні апротонні розчинники, такі як ацетонітрил, Ν,Ν-диметилформамід, і таке подібне. З неорганічними основами краще використовува ти спирти та полярні апротонні 18 розчинники. Перевага віддається такій основі як карбонат калію, та такому розчиннику як Ν,Νдиметилформамід або ацетонітрил. Дана реакція, загалом, проводиться у межах температур від 0 до 150°С, найбільш типово, між навколишньою температурою та 100°С. Ефір Формули 24 потім може бути перетворений у карбонову кислоту Формули 5 з використанням способів, що вже описані для перетворення сполуки Формули 19 у сполуку Формули 5 на Схемі 15. Сполуки Формули 23 можуть бути одержані із сполук Формули 20 як окреслено на Схемі 20. У цьому методі гідразинова сполука Формули 20 піддається реакції зі сполукою Формули 25 (може застосовуватись фумаратний ефір або малеатний ефір, або суміш обох) у присутності основи та розчинника. де R8 являє собою С 1-С4 алкіл. Основа, використана на Схемі 20, являє собою, типово, металалкоксидну сіль, таку як натрій етоксид, калій етоксид, натрій етоксид, калій етоксид, калій трет-бутоксид, літій третбутоксид і таке подібне. Можуть застосовуватись полярні протонні та полярні апротонні органічні розчинники, такі як спирти, ацетонітрил, тетрагідрофуран, Ν,Ν-диметилформамід, диметилсульфоксид і таке подібне. Розчинники, яким віддається перевага, являють собою спирти, такі як метанол та етанол. Особлива перевага віддається тому, щоб даний спирт був тим самим, що утворює фумаратний або малеатний ефір, та алкоксидну основу. Дана реакція, типово, проводиться шляхом перемішування сполуки Формули 20 та основи у даному розчиннику. Дана суміш може підігріватись або охолоджуватись до потрібної температури, і сполука Формули 25 додається протягом деякого часу. Типово, температури реакції варіюють між 0°С та температурою кипіння застосованого розчинника. Дана реакція може проводитись під тиском, що перевищує атмосферний, з метою підвищення точки кипіння даного розчинника. Загалом, перевага віддається температурам у межах від приблизно 30 до 90°С. Потім дана реакційна суміш може бути підкислена шляхом додавання органічної кислоти, такої як оцтова кислота і таке подібне, або неорганічної кислоти, такої як хлористоводнева, сірчана і таке подібне. Потрібний продукт Формули 23 може бути виділений з використанням способів, що відомі фа хівцям у даній галузі, таких як кристалізація, екстракція або дистиляція. Визнано, що деякі реагенти та умови реакції, описані вище для одержання сполук Формули 1, можуть бути несумісними з деякими 19 81791 функціональними групами, що присутні у проміжних сполуках. У цих випадках уведення у схему даного синтезу послідовностей протектування/депротектування або взаємоперетворень функціональних груп посприяє одержанню бажаних продуктів. Застосування та вибір даних захисних груп будуть зрозумілими фа хівцям у даній галузі [дивись, наприклад, T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 2nd ed.; Wiley: New York, 1991]. Фахівцеві у даній галузі зрозуміло, що у деяких випадках після введення даного реагенту, як показано на будь-якій індивідуальній схемі, може виникнути потреба у здійсненні додаткових рутинних синтетичних стадій, які детально не описані, для завершення синтезу сполук Формули 1. Фахівцеві у даній галузі також зрозуміло, що може виникнути потреба у реалізації комбінації стадій, які проілюстровані на вищенаведених схемах, у порядку, що відмінний від передбаченого конкретною поданою послідовністю для одержання сполук Формули 1. Без подальших уточнень, можна вважати, що фа хівець у даній галузі, з використанням попереднього опису зможе використати даний винахід у всій його повноті. Тому наступні Приклади слід розглядати просто як ілюстративні і не такі, що у будь-якій мірі обмежують якимсь чином розкриття даного винаходу. Стадії у наступних Прикладах ілюструють процедуру для кожної стадії у повному синтетичному перетворенні, і вихідний матеріал для кожної стадії необов'язково був одержаний з використанням специфічного препаративного способу, що описаний в інших Прикладах чи Стадіях. Відсотки подані як вагові відсотки, за виключенням сумішей хроматографічних розчинників, або коли зазначено інше. Частки та відсотки для сумішей хроматографічних розчинників подані, якщо не зазначено інше, в об'ємних одиницях. 1ЯМР спектри наведені умлн -1 у напрямі уздовж енергетичного спектра від тетраметилсилану; "s" означає синглет, "d" означає дублет, "t" означає триплет, "q" означає квартет, "m" означає мультиплет, "dd" означає дублет дублетів, "dt" означає дублет триплетів, та "br s" означає широкий синглет. Приклад 1 Одержання 1-(3-хлоро-2-піридиніл)-N-[4-ціано2-метил-6-(аміно карбоніл)феніл]-3(трифторометил)-1Н-піразол-5-карбоксаміду Стадія А: Одержання 2-аміно-3-метил-5йодобензойної кислоти До розчину 2-аміно-3-метилбензойної кислоти (Aldrich, 5г, 33ммоль) у Ν,Ν-диметилформаміді (30мл) додавали N-йодосукцинімід (7,8г, 34,7ммоль), і дану реакційну суміш суспендували на 75°С масляній бані протягом ночі. Тепло вилучали, і дану реакційну суміш потім повільно виливали у льодяну воду (100мл) з осадженням світло-сірої твердої речовини. Дану тверду речовину відфільтровували та промивали чотири рази водою і потім помішували у вакуумну піч при 70°С для висушування протягом ночі. Потрібна 20 проміжна сполука була виділена у вигляді світлосірої твердої речовини (8,8г). 1 Η ЯМР (DNSO-d6): δ 7,86 (d, 1H), 7,44 (d, 1H), 2,08 (s, 3H). Стадія В: Одержання 3-хлоро-2-[3(трифторометил)-1Н-піразол-1-іл]піридину До суміші 2,3-дихлоропіридину (99,0г, 0,67моль) та 3-(трифторометил)-піразолу (83г, 0,61моль) у безводному Ν,Ν-диметилформаміді (300мл) додавали карбонат калію (166,0г, 1,2моль), і дану реакційну суміш потім нагрівали до 110-125°С протягом 48 годин. Дану реакційну суміш охолоджували до 100°С та фільтрували через целітовий (Celite®) діатомовий фільтр для вилучення твердих речовин. Ν,Νдиметилформамід та надлишок дихлоропіридину вилучались шляхом дистиляції при атмосферному тиску. Дистиляція даного продукту під зниженим тиском (Ткип. 139-141°С, 7мм) дала 113,4г потрібної проміжної сполуки у вигляді прозорого жовтого масла. 1 Η ЯМР (CDCl3): δ 8,45 (d, 1H), 8,15 (s, 1H), 7,93 (d, 1H), 7,36 (t, 1H), 6,78 (s, 1H). Стадія С: Одержання 1-(3-хлоро-2-піридиніл)3-(трифторометил)-1Н-піразол-5-карбонової кислоти До розчину 3-хлоро-2-[3-(трифторометил)-1Нпіразол-1-іл]піридину (тобто піразольного продукту зі Стадії В) (105,0г, 425ммоль) у безводному тетрагідрофурані (700мл) при температурі -75°С додавали через канюлю охолоджений до -30°С розчин діізопропіламіду літію (425ммоль) у безводному тетрагідрофурані (300мл). Темночервоний розчин перемішували протягом 15 хвилин, після чого через нього при -63°С перепускали діоксид вуглецю доти, поки даний розчин не став блідо-жовтим, і екзотермічна реакція припинилась. Дану реакційну суміш перемішували додатково протягом 20 хвилин і потім гасили водою (20мл). Розчинник вилучали під зниженим тиском, і дану реакційну суміш розподіляли між ефіром та 0,5N водним розчином гідроксиду натрію. Водні екстракти промивали ефіром (3х), фільтрували через целітовий (Celite®) діатомовий фільтр для вилучення залишкових твердих речовин, потім підкислювали до рН приблизно 4, при досягненні якого утворилось помаранчеве масло. Водну суміш енергійно перемішували і вводили додаткову кислоту для зниження рН до 2,5-3. Зазначене помаранчеве масло застигало у гранульовану тверду речовину, котру відфільтровували, промивали послідовно водою та 1N хлористоводневою кислотою і висушували під вакуумом при 50°С з одержанням 130г титульного продукту у вигляді білуватої твердої речовини. Продукт із наступної партії після схожої процедури плавився при 175-176°С. 1 Η ЯМР (DNSO-d6): δ 7,61 (s, 1H), 7,76 (dd, 1H), 8,31 (d, 1H), 8,60 (d, 1H). Стадія D: Одержання 2-[1-(3-хлоро-2піридиніл)-3-(трифторометил)-1Н-піразол-5-іл]-6йодо-8-метил-4Н-3,1-бензоксазин-4-ону До розчину метансульфонілхлориду (2,91мл, 37,74ммоль) в ацетонітрилі (50мл) додавали по краплях суміш 1-(3-хлоро-2-піридиніл)-3 21 81791 (трифторометил)-1Н-піразол-5-карбонової кислоти (тобто продукту карбонової кислоти зі Стадії С) (10,0г, 34,31ммоль) та триетиламіну (4,78мл, 34,31ммоль) в ацетонітрилі (50мл) при -5°С. Потім реакційну температуру підтримували при 0°С підчас послідовного додавання реактивів. Після перемішування протягом 20 хвилин додавали 2аміно-3-метил-5-йодобензойну кислоту (тобто продукт зі Стадії А) (9,51г, 34,31ммоль), і перемішування продовжували ще протягом 10 хвилин. Потім по краплях додавали розчин триетиламіну (9,56мл, 68,62ммоль) в ацетонітрилі (15мл), і дану реакційну суміш перемішували протягом 30 хвилин з наступним додаванням метансульфонілхлориду (2,91мл, 37,74ммоль). Потім дану реакційну суміш підігрівали до кімнатної температури та перемішували протягом 2 годин. Розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням 8,53г титульної сполуки у вигляді жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,59 (dd, 1H), 8,35 (d, 1H), 8,15 (s, 1H), 7,97 (dd, 1H), 7,86 (d, 1H), 7,49 (m, 2H), 1,79 (s,3H). Стадія Ε: Одержання 2-[1-(3-хлоро-2піридиніл)-3-(трифторометил)-1Н-піразол-5-іл]-6ціано-8-метил-4Н-3,1-бензоксазин-4-ону До розчину 2-[1-(3-хлоро-2-піридиніл)-3(трифторометил)-1Н-піразол-5-іл]-6-йодо-8-метил4Н-3,1-бензоксазин-4-ону (тобто беноксазинонового продукту зі Стадії D) (500мг, 0,94ммоль) у тетрагідрофурані (10мл) додавали послідовно при кімнатній температурі йодид міді (І) (180мг, 0,094ммоль), тетракіс(трифенілфосфін)паладій (0) (5,4мг, 0,047ммоль) та ціанід міді (І) (420мг, 4,7ммоль). Після нагрівання даної реакційної суміші зі зворотним холодильником протягом ночі додавали додатково ціанід міді (І) (420мг, 4,7ммоль), йодид міді (І) (107мг, 0,56ммоль) та тетракіс(трифенілфосфін)паладій (0) (325мг, 0,28ммоль), і нагрівання зі зворотним холодильником продовжували протягом 1 години. Дана реакційна суміш набула чорного кольору, і у цей момент тонкошарова хроматографія на силікагелі підтвердила завершення даної реакції. Потім дану реакційну суміш розводили етилацетатом (20мл) та фільтрували через целіт (Celite®) з наступним промиванням три рази 10% водним розчином бікарбонату натрію та один раз розсолом. Даний органічний екстракт осушували (MgSO4) та концентрували під зниженим тиском з одержанням 410мг титульної сполуки у вигляді неочищеної жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,59 (dd, 1Н), 8,33 (d, 1H), 8,03 (dd, 1H), 7,95 (d, 1H), 7,56 (m, 2H), 1,88 (s, 3H). Стадія F: Одержання 1-(3-хлоро-2-тридиніл)-N[4-ціано-2-метил-6-(аміно карбоніл)феніл]-3(трифторометил)-1Н-піразол-5-карбоксаміду До розчину 2-[1-(3-хлоро-2-тридиніл)-3(трифторометил)-1Н-піразол-5-іл]-6-ціано-8-метил4Н-3,1-бензоксазин-4-ону (тобто ціанобензоксазинонового продукту зі Стадії Е) (200мг, 0,46ммоль) у тетрагідрофурані 95мл) 22 додавали по краплях гідроксид амонію (0,5мл, 12,8ммоль) при кімнатній температурі. Потім дану реакційну суміш перемішували протягом 5 хвилин, і в цей момент тонкошарова хроматографія на силікагелі підтвердила завершення даної реакції. Тетрагідрофурановй розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням 620мг титульної сполуки, сполуки даного винаходу, у вигляді твердої речовини з Тпл 200-202°С. 1 Η ЯМР (CDCl3): δ 10,65 (s, 1H), 8,43 (dd, 1H), 7,9 (dd, 1H), 7,67 (s, 1H), 7,63 (s, 1H), 7,45 (m, 1H), 7,25 (s, 3H), 6,21 (bs, 1H), 5,75 (bs, 1H), 2,26 (s, 3H). Приклад 2 Одержання 1-(3-хлоро-2-піридиніл)-N-[4-ціано2-метил-6-[(метиламіно)карбоніл]феніл]-3(трифторометил)-1Н-піразол-5-карбоксаміду Стадія А: Одержання 1-(3-хлоро-2-піридиніл)N-[4-йодо-2-метил-6-](метиламін)карбоніл]феніл]3-(трифторометил)-1Н-піразол-5-карбоксаміду До розчину 2-[1-(3-хлоро-2-піридиніл)-3(трифторометил)-1Н-піразол-5-іл]-6-йодо-8-метил4Н-3,1-бензоксазин-4-ону (тобто бензоксазинонового продукту Прикладу 1, Стадія D) (500мг, 0,94ммоль) у тетрагідрофурані (15мл) додавали по краплях метиламін (2,0Μ розчин у THF, 1,4мл, 2,8ммоль), і дану реакційну суміш перемішували протягом 3 годин, і в цей момент тонкошарова хроматографія на силікагелі підтвердила завершення даної реакції. Тетрагідрофурановий розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням 400мг титульної сполуки у вигляді твердої жовтої речовини. 1 Η ЯМР (CDCl3): δ 10,25 (s, 1H), 8,45 (dd, 1Н), 7,85 (dd, 1H), 7,55 (s, 1H), 7,50 (s, 1H), 7,46 (s, 1H), 7,40 (m, 1H), 6,15 (d, 1H), 2,93 (d, 3H), 2,12 (s, 3H). Стадія В: Одержання 1-(3-хлоро-2-піридиніл)N-[4-ціано-2-метил-6[(метиламіно)карбоніл]феніл]-3-(трифторометил)1Н-піразол-5-карбоксаміду До розчину 1-(3-хлоро-2-піридиніл)-N-[4-йодо2-метил-6-[(метиламіно)карбоніл]феніл]-3(трифторометил)-1Н-піразол-5-карбоксаміду (тобто діамідного продукту зі Стадіїї А) (410мг, 0,72ммоль) у тетрагідрофурані (8мл) додавали послідовно при кімнатній температурі йодид міді (І) (24мг, 0,126ммоль), тетракіс(трифенілфосфін)паладій (0) (70мг, 0,060ммоль) та ціанід міді (І) (640мг, 7,2ммоль). Дану реакційну суміш нагрівали зі зворотним холодильником протягом 4,5 годин. Тонкошарова хроматографія на силікагелі підтвердила завершення даної реакції. Потім дану реакційну суміш розводили етилацетатом (20мл) та фільтрували через целіт (Celite®), з наступним промиванням три рази 10% водним розчином бікарбонату натрію та один раз розсолом. Даний органічний екстракт осушували (MgSO4) та концентрували під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням 114мг титульної 23 81791 сполуки, сполуки даного винаходу, у вигляді білої твердої речовини з Тпл. 214-216°С. 1 Η ЯМР (CDCl3): δ 10,70 (s, 1Н), 8,46 (dd, 1H), 7,87 (dd, 1H), 7,57 (s, 2H), 7,45 (m, 1H), 7,31 (s, 1H), 6,35 (d, 1H), 2,98 (d, 3H), 2,24 (s, 3H). Приклад 3 Одержання 3-хлоро-1-(3-хлоро-2-піридиніл)-N[4-ціано-2-метил-6-[(метиламіно)карбоніл]феніл]1Н-піразол-5-карбоксаміду Стадія А: Одержання 3-хлоро-N,N-диметил1Н-піразол-1-сульфонаміду До розчину N-диметилсульфамоїлпіразолу (188,0г, 1,07моль) у безводному тетрагідрофурані (1500мл) при -78°С по краплях додавали розчин 2,5Μ n-бутиллітію (472мл, 1,18моль) у гексані при підтриманні температури нижче -65°С. По завершенню додавання дану реакційну суміш витримували при -78°С протягом додаткових 45 хвилин, після чого по краплях додавали розчин гексахлороетану (279г, 1.18моль) у тетрагідрофурані (120мл). Дану реакційну суміш витримували при -78°С протягом однієї години, підігрівали до -20°С і потім гасили водою (1л). Дану реакційну суміш екстрагували метиленхлоридом (4x500мл); органічні екстракти осушували над сульфа том магнію та концентрували. Неочищений продукт додатково очищали методом хроматографії на силікагелі з використанням метиленхлориду як елюенту з одержанням 160г титульної сполуки у вигляді жовтого масла. 1 Η ЯМР (CDCl3): δ 7,61 (s, 1H), 6,33 (s, 1H), 3,07 (d, 6H). Стадія В: Одержання 3-хлоропіразолу До трифторооцтової кислоти (290мл) додавали по краплях 3-хлоро-N,N-диметил-1Нпіразол-1-сульфонамід (тобто хлоропіразольний продукт зі Стадії А) (160г), і дану реакційну суміш перемішували при кімнатній температурі протягом 1,5 години, і потім концентрували під зниженим тиском. Залишок розчиняли у гексані, нерозчинні тверді речовини відфільтровували, і гексан концентрували з одержанням неочищеного продукту у ви гляді масла. Даний неочищений продукт додатково очищали методом хроматографії на силікагелі з використанням суміші ефір/гексан (40:60) як елюенту з одержанням 64,44г титульного продукту у вигляді жовтого масла. 1 Η ЯМР (CDCl3): δ 6,39 (s, 1H), 7,66 (s, 1H), 9,6 (br s, 1H). Стадія С: Одержання 3-хлоро-2-(3-хлоро-1Нпіразол-1-іл)піридину До суміші 2,3-дихлоропіридину (92,60г, 0,629моль) та 3-хлоропіразолу (тобто продукту зі Стадіїї В) (64,44г, 0,629моль) у Ν,Νдиметилформаміді (400мл) додавали карбонат калію (147,78г, 1,06моль), і дану реакційну суміш потім нагрівали до 100°С протягом 36 годин. Дану реакційну суміш охолоджували до кімнатної температури і повільно виливали у льодяну воду. Осаджені тверді речовини відфільтровували та промивали водою. Твердий осад на фільтрі розчиняли в етилацетаті, осушували над сульфатом магнію і концентрували. Неочищену 24 тверду речовину піддавали хроматографуванню на силікагелі з використанням 20% етилацетат/гексан як елюенту з одержанням 39,75г титульного продукту у ви гляді білої твердої речовини. 1 ЯМР (CDCl3): δ 6,43 (s, 1Н), 7,26 (m, 1H), 7,90 (d, 1H), 8,09 (s, 1H), 8,41 (d, 1H). Стадія D: Одержання 3-хлоро-1-(3-хлоро-2піридиніл)-1Н-піразол-5-карбонової кислоти До розчину 3-хлоро-2-(3-хлоро-1Н-піразол-1іл)піридину (тобто піразольного продукту зі Стадії С) (39,75г, 186ммоль) у безводному тетрагідрофурані (400мл) при -78°С додавали по краплях розчин 2,0Μ літію діізопропіламіду (93мл, 186ммоль) у тетрагідрофурані. Через даний бурштиновий розчин перепускали діоксид вуглецю протягом 14 хвилин, після чого даний розчин набув блідого коричнево-жовтого кольору. Дану реакційну суміш робили основною за допомогою 1N водного розчину гідроксиду натрію та екстрагували ефіром (2x500мл). Водні екстракти підкислювали 6Ν хлористоводневою кислотою з наступною екстракцією етилацетатом (3x500мл). Етилацетатні екстракти осушували над сульфатом магнію та концентрували з одержанням 42,96г титульного продукту у вигляді білуватої твердої речовини. Продукт із іншої партії, отриманий у такий самий спосіб, плавився при 198-199°С. 1 Η ЯМР (DMSO-d6): δ 6,99 (s, 1H), 7,45 (m, 1H), 7,93 (d, 1H), 8,51 (d, 1H). Стадія Ε: Одержання 2-[3-хлоро-1-(3-хлоро-2піридиніл)-1Н-піразол-5-іл]-6-йодо-8-метил-4Н-3,1бензоксазин-4-ону До розчину метансульфонілхлориду (0,63мл, 8,13ммоль) в ацетонітрилі (10мл) додавали по краплях суміш 3-хлоро-1-(3-хлоро-2-піридиніл)-1Нпіразол-5-карбонової кислоти (тобто продукту карбонової кислоти зі Стадії D) (2,0г, 7,75ммоль) та триетиламіну (1,08мл, 7,75ммоль) в ацетонвтрилі (5мл) при 0°С. Потім дану реакційну суміш перемішували протягом 15 хвилин при 0°С. Потім додавали 2-аміно-3-метил-5-йодобензойну кислоту (тобто продукт із Прикладу 1, Стадія А) (2,14г, 7,75ммоль), і перемішування продовжували протягом ще 5 хвилин. Потім по краплях додавали розчин триетиламіну (2,17мл, 15,15ммоль) в ацетонітрилі (5мл), підтримуючи температуру нижче 5°С. Дану реакційну суміш перемішували протягом 40 хвилин при 0°С, і потім додавали метансульфонілхлорид (0,63мл, 8,13ммоль). Потім дану реакційну суміш підігрівали до кімнатної температури та перемішували протягом ночі. Потім реакційну суміш розводили водою (50мл) та екстрагували етилацетатом (3x50мл). Об'єднані етилацетатні екстракти промивали послідовно 10% водним розчином бікарбонату натрію (1x20мл) та розсолом (1x20мл), осушували (MgSO4) та концентрували з одержанням 3,18г титульного продукту у вигляді неочищеної жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,55 (dd, 1Н), 8,33 (s, 1H), 7,95 (dd, 1H), 7,82 (d, 1H), 7,45 (m, 1H), 7,16 (s, 1H), 1,77 (s,3H). 25 81791 Стадія F: Одержання 2-[3-хлоро-1-(3-хлоро-2піридиніл)-1Н-піразол-5-іл]-6-ціано-8-метил-4Н-3,1бензоксазин-4-ону До розчину 2-[3-хлоро-1-(3-хлоро-2-піридиніл)1Н-піразол-5-іл]-6-йодо-8-метил-4Н-3,1бензоксазин-4-ону (тобто бензоксазинонового продукту зі Стадії Е) (600мг, 1.2ммоль) у тетрагідрофурані (15мл) послідовно при кімнатній температурі додавали йодид міді (І) (137мг, 0,72ммоль), тетракіс(трифенілфосфін)паладій (0) (416мг, 0,36ммоль) та ціанід міді (І) (860мг. 9,6ммоль). Потім дану реакційну суміш нагрівали зі зворотним холодильником протягом ночі. Реакційна суміш набула чорного кольору, і у цей момент тонкошарова хроматографія на силікагелі підтвердила завершення даної реакції. Дану реакційну суміш розводили етилацетатом (20мл) та фільтрували через целіт (Celite®) з наступним промиванням три рази 10% водним розчином бікарбонату натрію та один раз розсолом. Органічний екстракт осушували (MgSO 4) та концентрували під зниженим тиском з одержанням 397мг титульної сполуки у вигляді неочищеної жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,50 (q, 1Н), 8,22 (d, 1H), 7,90 (dd, 1H), 7,67 (d, 1H), 7,45 (m, 1H), 7,15 (s, 1H), 1,79 (s,3H). Стадія G: Одержання 3-хлоро-1-(3-хлоро-2піридиніл)-N-[4-ціано-2-метил-6(метиламіно)карбоніл]феніл]-1Н-піразол-5карбоксаміду До розчину 2-[3-хлоро-1-(3-хлоро-2-піридиніл)1Н-піразол-5-іл]-6-ціано-8-метил-4Н-3,1бензоксазин-4-ону (тобто ціанобензоксазинонового продукту зі Стадії F) (100мг, 0,25ммоль) у тетрагідрофурані (5мл) додавали по краплях метиламін (2,0Μ розчин у THF, 0,5мл, 1,0ммоль), і дану реакційну суміш перемішували протягом 5 хвилин, і в цей момент тонкошарова хроматографія на силікагелі засвідчила завершення даної реакції. Тетрагідрофурановий розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням титульної сполуки, сполуки даного винаходу, у вигляді білої твердої речовини (52мг), котра розкладалась у приладі для плавлення при температурі вище 140°С. 1 Η ЯМР (CDCl3): δ 10,55 (s, 1H), 8,45 (dd, 1H), 7,85 (dd, 1H), 7,55 (d, 2H), 7,40 (m, 1H), 6,97 (d, 1H), 6,30 (d, 1H), 2,98 (d, 3H), 2,24 (d, 3H). Приклад 4 Одержання 3-хлоро-1-(3-хлоро-2-піридиніл)-N[4-ціано-2-метил-6-(аміно карбоніл)феніл]-1Нпіразол-5-карбоксаміду До розчину 2-[3-хлоро-1-(3-хлоро-2-піридиніл)1Н-піразол-5-іл]-6-ціано-8-метил-4Н-3,1бензоксазин-4-ону (тобто ціанобензоксазинонового продукту із Прикладу 3, Стадія F) (100мг, 0,25ммоль) у тетрагідрофурані (5мл) додавали по краплях гідроксид амонію (0,5мл, 12,8ммоль) при кімнатній температурі. Потім дану реакційну суміш перемішували протягом 5 хвилин, і в цей момент тонкошарова хроматографія на силікагелі засвідчила 26 завершення даної реакції. Тетрагідрофурановий розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням 55мг титульної сполуки, сполуки даного винаходу, у вигляді білої твердої речовини, що розкладалась у приладі для плавлення при температурі вище 255°С. 1 Η ЯМР (CDCl3): δ 10,50 (s, 1Н), 8,45 (dd, 1H), 7,85 (dd, 1H), 7,66 (d, 1H), 7,61 (s, 1H), 7,41 (m, 1H), 6,95 (s, 1H), 6,25 (bs, 1H), 5,75 (bs, 1H), 2,52 (s, 3H). Приклад 5 Одержання 3-бромо-1-(3-хлоро-2-піридиніл)-N[4-ціано-2-метил-6-[(метиламіно)карбоніл]феніл]1Н-піразол-5-карбоксаміду Стадія А: Одержання 3-бромо-N,N-диметил1Н-піразол-1-сульфонаміду До розчину Ν,Ν-диметилсульфамоїлпіразолу (44,0г, 0,251моль) у безводному тетрагідрофурані (500мл) при -78°С по краплях додавали розчин nбутиллітію (2,5Μ у гексані, 105,5мл, 0,264моль) при підтриманні температури на рівні нижче -60°С. Підчас цього додавання утворилась щільна тверда речовина. По завершенню введення дану реакційну суміш витримували додатково протягом 15 хвилин, після чого по краплях додавали розчин 1,2-дибромотетрахлороетану (90г, 0,276моль) у тетрагідрофурані (150мл) при підтриманні температури нижче -70°С. Дана реакційна суміш стала прозорою і набула оранжевого кольору; перемішування було подовжено ще на 15 хвилин. Баня з температурою -78°С була вилучена, і дану реакцію гасили водою (600мл). Дану реакційну суміш екстрагували метиленхлоридом (4х), і органічні екстракти осушували над сульфатом магнію та концентрували. Неочищений продукт піддавали додатковій очистці методом хроматографії на силікагелі з використанням суміші метиленхлорид-гексан (50:50) як елюенту з одержанням 57,04г титульного продукту у вигляді прозорого безбарвного масла. 1 Η ЯМР (CDCl3): δ 3,07 (d, 6Н), 6,44 (m, 1H), 7,62 (m, 1H). Стадія В: Одержання 3-бромопіразолу До трифторооцтової кислоти (70мл) повільно додавали 3-бромо-N,N-диметил-1Н-піразол-1сульфонамід (тобто бромопіразольний продукт зі Стадії А) (57,04г). Дану реакційну суміш перемішували при кімнатній температурі протягом 30 хвилин і потім концентрували під зниженим тиском. Даний залишок розчиняли в гексані, нерозчинні тверді речовини відфільтровували, і гексан випарювали з одержанням неочищеного продукту у ви гляді масла. Даний неочищений продукт додатково очищали методом хроматографії на силікагелі з використанням суміші етилацетат/дихлорометан (10:90) як елюенту з одержанням масла. Дане масло розчиняли у дихлорометані, нейтралізували водним розчином бікарбонату натрію, екстрагували метиленхлоридом (3х), осушували над сульфатом магнію та концентрували з одержанням 25,9г титульного продукту у вигляді білої твердої речовини, Тпл 61-64°С. 27 1 81791 Η ЯМР (CDCl3): δ 6,37 (d, 1H), 7,59 (d, 1H), 12,4 (br s, 1H). Стадія С: Одержання 2-(3-бромо-1Н-піразол-1іл)3-хлоропіридину До суміші 2,3-дихлоропіридину (27,4г, 185ммоль) та 3-бромопіразолу (тобто продукту зі Стадії В) (25,4г, 176ммоль) у безводному Ν,Νдиметилформаміді (88мл) додавали карбонат калію (48,6г, 352ммоль), і дану реакційну суміш нагрівали до 125°С протягом 18 годин. Дану реакційну суміш охолоджували до кімнатної температури та виливали у льодяну воду (800мл). Випав осад. Осаджені тверді речовини перемішували протягом 1,5 години, фільтрували та промившій водою (2x100мл). Твердий осад на фільтрі розчиняли у метиленхлориді та промивали послідовно водою, 1N хлористоводневою кислотою, насиченим водним розчином бікарбонату натрію та розсолом. Органічні екстракти потім осушували сульфатом магнію та концентрували з одержанням 39,9г рожевої твердої речовини. Неочищену тверду речовину суспендували у гексані та перемішували енергійно протягом 1 години. Дані тверді речовини фільтрували, промивали гексаном та висушували з одержанням титульного продукту у вигляді білуватого порошку (30,4г), який, за даними ЯМР, мав чистоту >94%. Цей матеріал був використаний на Стадії D без додаткової очистки. 1 Η ЯМР (CDCI3): δ 6,52 (s, 1Н), 7,30 (dd, 1H), 7,92 (d, 1H), 8,05 (s, 1H), 8,43 (d, 1H). Стадія D: Одержання 3-бромо-1-(3-хлоро-2піридиніл)-1Н-піразол-5-карбонової кислоти До розчину 2-(3-бромо-1Н-піразол-1-іл)-3хлоропіридину (тобто піразольному продукту зі Стадії С) (30,4г, 118ммоль) у безводному тетрагідрофурані (250мл) при -76°С додавали по краплях розчин літій діізопропіламіду (118ммоль) у тетрагідрофурані з такою швидкістю, щоб температура підтримувалась на рівні нижче -71°С. Дану реакційну суміш перемішували протягом 15 хвилин при -76°С, і потім через неї перепускали діоксид вуглецю протягом 10 хвилин, що спричинило нагрівання до -57°С. Дану реакційну суміш підігрівали до -20°С та гасили водою. Дану реакційну суміш концентрували і потім розчиняли у воді (1л) та ефірі (500мл), і потім додавали водний розчин гідроксиду натрію (1N, 20мл). Водні екстракти промивали ефіром та підкислювали хлористоводневою кислотою. Осаджені тверді речовини фільтрували, промивали водою та висушували з одержанням 27,7г титульного продукту у вигляді жовто-коричневої твердої речовини. Продукт з іншої партії, отриманий за аналогічною процедурою, плавився при 200201°С. 1 Η ЯМР (DMSO-d6): δ 7,25 (s, 1Н), 7,68 (dd, 1H), 8,24 (d, 1H), 8,56 (d, 1H). Стадія Е: Одержання 2-[3-бромо-1-(3-хлоро-2піридиніл)-1Н-піразол-5-іл]-6-йодо-8-метил-4Н-3,1бензоксазин-4-ону До розчину метансульфонілхлориду (0,54мл, 6,94ммоль) в ацетонітрилі (15мл) додавали по краплях суміш 3-бромо-1-(3-хлоро-2-піридиніл)-1Hпіразол-5-карбонової кислоти (тобто продукту 28 карбонової кислоти зі Стадії D) (2,0г, 6,6ммоль) та триетиламіну (0,92мл, 6,6ммоль) в ацетонітрилі (5мл) при 0°С. Потім дану реакційну суміш перемішували протягом 15 хвилин при 0°С. Потім додавали 2-аміно-3-метил-5-йодобензойну кислоту (тобто продукт із Прикладу 1, Стадія А) (1,8г, 6,6ммоль), і перемішування продовжували ще протягом 5 хвилин. Потім по краплях додавали розчин триетиламіну (1,85мл, 13,2ммоль) в ацетонітрилі (5мл), підтримуючи температуру на рівні нижче 5°С. Дану реакційну суміш перемішували протягом 40 хвилин при 0°С, і потім додавали метансульфонілхлорид (0,54мл, 6,94ммоль). Потім реакційну суміш підігрівали до кімнатної температури та перемішували протягом ночі. Потім дану реакційну суміш розводили водою (50мл) та екстрагували етилацетатом (3x50мл). Об'єднані етилацетатні екстракти промивали послідовно 10% водним розчином бікарбонату натрію (1x20мл) та розсолом (1x20мл), осушували (MgSO4) та концентрували з одержанням 2,24г титульного продукту у вигляді неочищеної жовтої речовини. 1 Η ЯМР (CDCl3): δ 8,55 (dd, 1H), 8,33 (d, 1H), 7,95 (dd, 1H), 7,85 (s, 1H), 7,45 (m, 1H), 7,25 (s, 1H), 1,77 (s,3H). Стадія F: Одержання 2-[3-бромо-1-(3-хлоро-2піридиніл)-1Н-піразол-5-іл]-6-ціано-8-метил-4Н-3,1бензоксазин-4-ону До розчину 2-[3-бромо-1-(3-хлоро-2-піридиніл)1H-піразол-5-іл]-6-йодо-8-метил-4Н-3,1бензоксазин-4-ону (тобто бензоксазинонового продукту зі Стадії Е) (600мг, 1,1ммоль) у тетрагідрофурані (15мл) послідовно при кімнатній температурі додавали йодид міді (І) (126мг, 0,66ммоль), тетракіс(трифенілфосфін)паладій (0) (382мг, 0,33ммоль) та ціанід міді (І) (800мг, 8,8ммоль). Потім дану реакційну суміш нагрівали зі зворотним холодильником протягом ночі. Дана реакційна суміш набула чорного кольору, і в цей момент тонкошарова хроматографія на силікагелі засвідчила завершення даної реакції. Реакційну суміш розводили етилацетатом (20мл) та фільтрували через целіт (Celite®) з наступним промиванням три рази 10% розчином бікарбонату натрію та один раз розсолом. Органічний екстракт осушували (MgSO4) та концентрували під зниженим тиском з одержанням 440мг титульної сполуки у вигляді неочищеної жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,55 (m, 1Н), 8,31 (d, 1H), 7,96 (dd, 1H), 7,73 (s, 1H), 7,51 (m, 1H), 7,31 (s, 1H), 1,86 (s,3H). Стадія G: Одержання 3-бромо-1-(3-хлоро-2піридиніл)-N-[4-ціано-2-метил-6[(метиламіно)карбоніл] феніл]-1Н-піразол-5карбоксаміду До розчину 2-[3-бромо-1-(3-хлоро-2-піридиніл)1Н-піразол-5-іл]-6-ціано-8-метил-4Н-3,1беноксазин-4-ону (тобто ціанобензоксазинонового продукту зі Стадії F) (100мг, 0,22ммоль) у тетрагідрофурані (5мл) додавали по краплях метиленамін (2,0Μ розчин у THF, 0,5мл, 1,0ммоль), і дану реакційну суміш перемішували протягом 5 хвилин, і в цей момент тонкошарова 29 81791 хроматографія на силікагелі засвідчила завершення даної реакції. Тетрагідрофурановий розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням титульної сполуки, сполуки даного винаходу, у вигляді білої твердої речовини (41мг), котра розкладалась у приладі для плавлення при температурі вище 180°С. 1 Η ЯМР (CDCl3): δ 10,55 (s, 1Н), 8,45 (dd, 1H), 7,85 (dd, 1H), 7,57 (s, 2H), 7,37 (m, 1H), 7,05 (s, 1H), 6,30 (d, 1H), 2,98 (d, 3H), 2,24 (s, 3H). Приклад 6 Одержання 3-бромо-1-(3-хлоро-2-піридиніл)-N[4-ціано-2-метил-6-(аміно карбоніл)феніл]-1Нпіразол-5-карбоксаміду До розчину 2-[3-бромо-1-(3-хлоро-2-піридиніл)1Н-піразол-5-іл]-6-ціано-8-метил-4Н-3,1бензоксазин-4-ону (тобто ціанобензоксазинонового продукту Прикладу 5, Стадія F) (100мг, 0,22ммоль) у тетрагідрофурані (5мл) додавали по краплях гідроксид амонію (0,5мл, 12,8ммоль) при кімнатній температурі. Потім дану реакційну суміш перемішували протягом 5 хвилин, і в цей момент тонкошарова хроматографія на силікагелі засвідчила завершення даної реакції. Тетрагідрофурановий розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням титульної сполуки, сполуки даного винаходу, у вигляді білої твердої речовини (36мг) з точкою плавлення вище 255°С. 1 Η ЯМР (CDCl3): δ 10,52 (s, 1Н), 8,45 (dd, 1H), 7,85 (dd, 1H), 7,65 (s, 1H), 7,60 (s, 1H), 7,40 (m, 1H), 7,05 (s, 1H), 6,20 (bs, 1H), 5,75 (bs, 1H), 2,25 (s, 3H). Приклад 7 Одержання 3-хлоро-1-(3-хлоро-2-піридиніл)-N[2-хлоро-4-ціано-6-[(метиламіно)карбоніл]феніл]1H-піразол-5-карбоксаміду Стадія А: Одержання 2-аміно-3-хлоро-5йодобензойної кислоти До розчину 2-аміно-3-хлоробензойної кислоти (Aldrich, 5г, 29,1ммоль) у Ν,Ν-диметилформаміді (30мл) додавали N-йодосукцинімід (5,8г, 26ммоль), і реакційну суміш нагрівали до 60°С протягом ночі. Джерело тепла вилучали, і реакційну суміш потім повільно виливали у льодяну воду (100мл) з осадженням світлокоричневої твердої речовини. Тверду речовину фільтрували та промивали чотири рази водою і потім помішували у вакуумну піч при 70°С для сушіння протягом ночі. Потрібну проміжну сполуку виділяли у вигляді світло-коричневої твердої речовини (7,2г). 1 Η ЯМР (D MSO-d): δ 7,96 (d, 1H), 7,76 (t, 1H). Стадія В: Одержання 8-хлоро-2-[3-хлоро-1-(3хлоро-2-піридиніл)-1H-піразол-5-іл]-6-йодо-4Н-3,1бензоксазин-4-ону До розчину метансульфонілхлориду (0,31мл, 4,07ммоль) в ацетонітрилі (10мл) додавали по краплях суміш 3-хлоро-1-(3-хлоро-2-піридиніл)-1Нпіразол-5-карбонової кислоти (тобто продукту карбонової кислоти із Прикладу 3, Стадія D) (1,0г, 30 3,87ммоль) та триетиламіну (0,54мл, 3,87ммоль) в ацетонітрилі (5мл) при 0 °С. Потім дану реакційну суміш перемішували протягом 15 хвилин при 0°С. Потім додавали 2-аміно-3-хлоро-5-йодобензойну кислоту (тобто продукт зі Стадії А) (1,15г, 3,87ммоль), і перемішування продовжували протягом ще 5 хвилин. Потім по краплях додавали розчин триетиламіну (1,08мл, 7,74ммоль) в ацетонітрилі (5мл), підтримуючи температуру нижче 5°С. Дану реакційну суміш перемішували протягом 40 хвилин при 0°С, і потім додавали метансульфонілхлорид (0,31мл, 4,07ммоль). Потім реакційну суміш підігрівали до кімнатної температури та перемішували протягом ночі. Потім дану реакційну суміш розводили водою (50мл) та екстрагували етилацетатом (3x50мл). Об'єднані етилацетатні екстракти промивали послідовно 10% водним розчином бікарбонату натрію (1x20мл) та розсолом (1x20мл), осушували (MgSO4) та концентрували під зниженим тиском. Залишкову тверду речовину очи щали методом хроматографії на силікагелі з одержанням 575мг титульної сполуки у вигляді неочищеної жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,55 (q, 1H), 8,39 (d, 1H), 8,04 (d, 1H), 7,94 (dd, 1H), 7,45 (m, 1H), 7,19 (s, 1H). Стадія С: Одержання 8-хлоро-2-[3-хлоро-1-(3хлоро-2-піридиніл)-1Н-піразол-5-іл]-6-ціано-4Н-3,1бензоксазин-4-ону До розчину 8-хлоро-2-[3-хлоро-1-(3-хлоро-1-(3хлоро-2-піридиніл)-1Н-піразол-5-іл]-6-йодо-4Н-3,1бензоксазин-4-ону (тобто бензоксазинонового продукту зі Стадії В) (575мг, 1,1ммоль) у тетрагідрофурані (15мл) послідовно при кімнатній температурі додавали йодид міді (І) (840мг, 0,44ммоль), тетракіс(трифенілфосфін)паладій (0) (255мг, 0,22ммоль) та ціанід міді (І) (500мг, 5,5ммоль). Потім дану реакційну суміш нагрівали зі зворотним холодильником протягом ночі. Дана реакційна суміш набула чорного кольору, і в цей момент тонкошарова хроматографія на силікагелі підтвердила завершення даної реакції. Дану реакційну суміш розводили етилацетатом (20мл) та фільтрували через целіт (Celite®) з наступним промиванням три рази 10% водним розчином бікарбонату натрію та один раз розсолом. Органічний екстракт осушували (MgSO 4) та концентрували під зниженим тиском з одержанням 375мг титульної сполуки у вигляді неочищеної жовтої твердої речовини. 1 Η ЯМР (CDCl3): δ 8,55 (q, 1H), 8,36 (d, 1H), 7,95 (m, 2H), 7,5 (m, 1H). Стадія D: Одержання 3-хлоро-1-(3-хлоро-2піридиніл)-N-[2-хлоро-4-ціано-6[(метиламіно)карбоніл]феніл]-1Н-піразол-5карбоксаміду До розчину 8-хлоро-2-[3-хлоро-1-(3-хлоро-2піридиніл)-1Н-тразол-5-іл]-6-ціано-4Н-3,1бензоксазин-4-ону (тобто ціанобензоксазинонового продукту зі Стадії С) (187мг, 0,446ммоль) у тетрагідрофурані (5мл) по краплях додавали метиламін (2,0Μ розчин у THF, 0,5мл, 1,0ммоль), і дану реакційну суміш перемішували протягом 5 хвилин, і в цей момент тонкошарова хроматографія на силікагелі 31 81791 підтвердила завершення даної реакції. Тетрагідрофурановий розчинник випарювали під зниженим тиском, і залишкову тверду речовину очищали методом хроматографії на силікагелі з одержанням 49мг титульної сполуки, сполуки даного винаходу, у вигляді білої твердої речовини, котра плавилась при 197-200°С. 1 Η ЯМР (CDCl3): δ 10,05 (bs, 1Н), 8,45 (q, 1H), 7,85 (dd, 1H), 7,70 (d, 1H), 7,59 (d, 1H), 7,38 (m, 1H), 7,02 (s, 1H), 6,35 (d, 1H), 2,94 (d, 3H). З використанням описаних тут процедур та методів, що відомі у даній галузі, можуть бути одержані наступні сполуки Таблиці 1. У наступних Таблицях використовуються наступні скорочення: t означає третинний, s означає вторинний, n означає нормальний, і означає ізо, Me означає метил, Et означає етил, Рr означає пропіл, і-Pr означає ізопропіл, Вu означає бутил і CN означає ціано. 32 33 81791 34 вологість та температура. Корисні препарати містять рідини, такі як розчини (включаючи здатні до емульсіфікації концентрати), суспензії, емульсії (включаючи мікроемульсії та/або суспоемульсії), і таке подібне, що може загустіти у гелі. Корисні препарати також включають тверді речовини, такі як дуети, порошки, гранули, грудки, таблетки, плівки і таке подібне, що може бути здатним до диспергування у воді ("змочувальним") або водорозчинним. Активний інгредієнт може бути (мікро)інкапсульований і, крім того, сформований у суспензію або твердий препарат; як альтернатива, увесь даний препарат активного інгредієнта може бути інкапсульований (або "перекритий"). Застосування інкапсуляції може сприяти контрольованому виділенню або виділенню із затримкою активного інгредієнта. Розпилювальні препарати можуть поширюватись у придатних середовищах і застосовуватись у розпилювальних об'ємах від приблизно одного до кількох сотень літрів на гектар. Висококонцентровані композиції використовуються, головним чином, як проміжні речовини для складання наступних препаратів. Дані препарати, типово, містять ефективні кількості активного інгредієнта, розріджувача та поверхнево-активної речовини у наступних приблизних межах, що у сумі складають 100 відсотків за вагою. В Активний інгредієнт Дисперговані у воді та водорозчинні гранули, таблетки та порошки 5-90 Суспензії, емульсії, розчини (включаючи здатні до емульсіфікації концентрати) 5-50 Дусти Гранули та гр удки Висококонцентровані композиції Препарати /Застосування Сполуки даного винаходу призначені, загалом, для використання як препарат або композиція з носієм, що придатний для сільськогосподарських або несільськогосподарських застосувань, котрий містить, принаймні, один рідкий розріджувач, твердий розріджувач або поверхнево-активну речовину. Інгредієнти даного препарату або композиції вибираються таким чином, щоб узгоджуватись з фізичними властивостями даного активного інгредієнта, способом застосування та такими чинниками довкілля як тип грунту, Типові тверді розріджувачі описані у роботі [Watkins, et al., Handbook of Insecticide Dust Diluents and Carriers, 2nd Ed., Dorland Books, Caldwell, New Jersey]. Типові рідкі розріджувачі описані у роботі [Marsden, Solvents Guide, 2nd Ed., Interscience, New York, 1950. McCutcheon's Detergents and Emulsifiers Annual, Allured Publ. Corp., Ridgewood, New Jersey, так само як і у Sisely and Wood, Encyclopedia of Surface Active Agents, Chemical Publ. Co., Inc., New York, 1964, де подано також перелік поверхнево-активних речовин та рекомендовані застосування. Усі препарати можуть містити незначні кількості добавок для зниження піноутворення, грудкоутворення, корозії, 1-25 0,01-99 90-99 Р 35 81791 мікробіологічного росту і такого подібного, або загусники для підвищення в'язкості. Поверхнево-активні речовини включають, наприклад, поліетоксильовані спирти, поліетоксильовані алкілфеноли, поліетоксильовані ефіри сорбітан жирних кислот, діалкіл сульфосукцинати, алкілсульфати, алкілбензольні сульфонати, кремнійорганічні речовини, Ν,Νдіалкілтаурати, лігнінсульфонати, нафталінсульфонатні формальдегідні конденсати, полікарбоксилати та блоксополімери поліоксиетилен/поліоксипропілену. Тверді розріджувачі включають, наприклад, глини, такі як бентоніт, монтморилоніт, атапульгіт та каолін, крохмаль, цукор, кремнезем, тальк, діатомові землі, сечовину, карбонат кальцію, карбонат та бікарбонат натрію та сульфат натрію. Рідкі розріджувачі включають, наприклад, воду, Ν,Νдиметилформамід, диметилсульфоксид, Nалкілпіролідон, етиленгліколь, поліпропіленгліколь, парафіни, алкілбензоли, алкілнафталіни, олії, такі як оливкова, касторова, лляна, тунгова, кунжутна, кук урудзяна, арахісова, бавовняна, соєва, ріпакова та кокосова, ефіри жирних кислот, кетони, такі як циклогексанон, 2гептанон, ізофорон, та 4-гідрокси-4-метил-2пентанон, і спирти, такі як метанол, циклогексанон, деканон та тетрагідрофурфуриловий спирт. Розчини, включаючи здатні до емульсіфікації концентрати, можуть бути одержані шляхом простого змішування зазначених інгредієнтів. Дуети та порошки можуть бути одержані шляхом змішування та, звичайно, розмелювання у молотковомумлині або рідинно-енергетичному млині. Суспензії, звичайно, одержують шляхом мокрого розмелювання; дивись, наприклад, [US 3060084]. Гранули та грудки можуть бути виготовлені шляхом напилення активного матеріалу на попередньо сформовані гранулярні носії або з використанням агломераційних методів. Дивись, наприклад, [Browning, :Agglomeration", Chemical Engineering, December 4, 1967, pp.147-48, Perry's Chemical Engineer's Handbook, 4th Ed., McGraw-Hill, New York, 1963, pages 8-57 та наступні, і РСТ публікацію [WO 91/13546]. Грудки можуть бути виготовлені згідно з [US 4172714]. Дисперговані у воді та водорозчинні гранули можуть бути одержані як зазначено у [US 4144050, US 3920442 та DE 3246493]. Таблетки можуть бути виготовлені згідно з [US 5180587, US 5232701 та US 5208030]. Плівки можуть бути одержані згідно з [GB 2095558 та US 3299566]. Додаткову інформацію, що стосується галузі складання композицій, можна почерпнути у роботі [T,S, Woods, "The Formulator's Toolbox - Product Forms for Modern Agriculture " in Pesticide Chemistry and Biodcience, The Food-Environment Challenge, T. Brooks and T.R. Roberts, Eds., Proceedings of the 9 th International Congress on Pesticide Chemistry, The Royal Society of Chemistry, Cambridge, 1999, pp.120-133]. Дивись також [US 3235361, стовпчик 6, рядок 16 - стовпчик 7, рядок 19 та Приклади 8, 12, 15, 39, 41, 52, 53, 58, 132, 13-140, 162-164, 166, 167 та 169-182; US 2891855, стовпчик 3, рядок 66 стовпчик 5, рядок 17 та Приклади 1-4; Klingman, 36 Weed Control as a Science, John Wiley and Sons, Inc., New York, 1961, pp.81-96; та Hance et al., Weed Control Handbook, 8th Ed., Blackwell Scientific Publications, Oxford, 1989]. У наступних Прикладах усі відсотки є ваговими відсотками, і всі препарати одержані за допомогою звичайних методів. Номери сполук відповідають таким у вказівній таблиці А. Приклад А Змочувальний порошок Сполука 1 65,0 % додецилфенол поліетиленгліколевий ефір 2,0% натрій лігнинсульфонат 4,0% натрій алюмосилікат 6,0% монтморилоніт (кальцинований) 23,0 % Приклад В Гранули Сполука 1 гранули атапульгіту (низьколетюча речовина, 0,71/0,30мм; USS. Сита No.25-50) Приклад С Екструдовані грудки Сполука 1 безводний сульфат натрію неочищений лігнинсульфонат кальцію алкілнафталінсульфонат натрію кальцій/магній бентоніт Приклад D Здатний до емульсіфікації концентрат Сполука 1 суміш розчинних у маслі сульфонатів та поліоксиетиленових ефірів ізофорон 10% 90% 25,0% 10,0% 5,0% 1,0% 59,0% 0,5% 10,0% 70,0% Приклад Ε Гранули Сполука 1 0,5% целюлоза 2,5% лактоза 4,0% кукурудзяне борошно 93,0% Сполуки даного винаходу характеризуються сприятливими метаболічною та/або грунтовозалишковою моделями і виявляють активність, що контролює спектр сільськогосподарських та несільськогосподарських безхребетних шкідників. Сполуки даного винаходу також характеризуються сприятливою системністю щодо листяного та або ґрунтового внесення у рослинах, що виявляють переміщення, сприяючи захисту листя та інших частин рослин, які не контактують прямо з інсектицидними композиціями, котрі містять сполуки даного винаходу. (У контексті даної заявки "контроль безхребетних шкідників" означає таке інгібування розвитку безхребетних шкідників (включаючи смертність), що спричинює значне 37 81791 зниження живлення або іншого ушкодження чи шкоди, заподіяної даним шкідником; аналогічним чином визначаються й інші вирази). Як застосовується у даному тексті, вираз "безхребетний шкідник" включає членистоногих, черевоногих молюсків та нематод, у практичному сенсі як шкідників. Вираз "членистоногі" включає комах, кліщів, павуків, скорпіонів, багатоніжок, двопарноногих, мокриць та симфіланів. Вираз "черевоногі молюски" включає слимаків, слизовиків та інших Stylommatophora. Вираз "нематоди" включає всіх гельмінтів, таких як круглі черв'яки, серцеподібні черв'яки, та травоїдні нематоди (Nematoda), трематоди (Trematoda), Acanthocephala та стрічкові черв'яки (Cestoda). Фахівцеві у даній галузі зрозуміло, що не всі сполуки у рівній мірі ефективні проти усіх шкідників. Сполуки даного винаходу виявляють активність супроти практично важливих сільськогосподарських та несільськогосподарських шкідників. Вираз "сільськогосподарський" стосується продукування польових культур, таких, що призначені для харчування та виробництва волокон, і включає вирощування злакових культур (наприклад, пшениці, вівса, ячменю, жита, рису, кукурудзи), соєви х бобів, овочеви х культур (наприклад, латуку, капусти, томатів, бобів), картоплі, батату, винограду, бавовни, деревних фр уктів (наприклад, яблук, кісточкових фруктів та цитрусови х). Вираз "несільськогосподарський" стосується інших садових рослин (наприклад, лісових, оранжерейних, розсадникових або декоративних рослин, що не вирощуються у полі), трав (комерційних, для гольфа, житлових, рекреаційних і т.д.), деревинних продуктів, громадського (людини) здоров'я та здоров'я тварин, домашніх та комерційних будівель, домашнього господарства, застосувань, пов'язаних зі зберіганням продуктів від шкідників. Із міркувань спектра контролю безхребетних шкідників та економічної важливості захист (від шкоди або ушкоджень, спричинених безхребетними шкідниками) сільськогосподарських культур, таких як бавовна, кукурудза, соєві боби, рис, овочевих культур, таких як картопля, батат, виноград та деревинних фр уктів шляхом контролю безхребетних шкідників відноситься до варіантів даного винаходу, яким віддається перевага. Сільськогосподарські або несільськогосподарські шкідники включають личинки ряду лускокрилих Lepidoptera, таких як "похідних" черв'яків, совок, п'ядениць та геліотинів родини совок Noctuidae (наприклад, осінній "похідний" черв'як (Spodoptera fugiperda J.E. Smith), буряковий "похідний" черв'як (Spodoptera exigua Hubner), чорна совка (Agrotis ipsilon Hufnagel), капустяна п'ядениця (Trichoplusia пі Hubner), тютюнова листовійка (Heliothis virescens Fabricius)); свердлувальники, чохлоноски, павутинна гусінь, ковпачковоподібні черв'яки, мермітиди та шкідники, що скелетують листя, із родини вогневок Pyralidae (наприклад, європейський зерновий свердлувальник (Ostrinia nubilalais Hubner), "пупкова" цитрусова гусінь (Amyelois transitella Walker), зернова коренева 38 павутинна гусінь (Crambus caliginosellus Clemens), дернинна павутинна гусінь (Herpetogramma licarsisalis Walker)); трубкокрути, листовійки, шкідники насіння, та фр уктові шкідники із родини листовійок Torticidae (наприклад, плодожерка яблунева (Cydia pomonella Linnaeus), листовійка виноградна (Endopiza viteana Clemens), листовійка східна персикова (Grapholita molesta Busck)); та багато інших економічно важливих лускокрилих (наприклад, капустяна міль (Plutella xylostella Linnaeus), рожевий короб очний черв'як бавовни (Pectinophora gossypiella Saunders), непарний шовкопряд (Lymantria dispar Linnaeus)); німфи та дорослі особини ряду Blattodea, включаючи тарганів родин Blattellidae та Blattidae (наприклад, чорний тарган (Blatta orientalis Linnaeus), азіатський тарган (Blattella asahinai Mizukubo), прусак (Blattella germanica Linnaeus), бурострічковий тарган (Supella longipalpa Fabricius), американський тарган (Periplaneta Americana Linnaeus), коричневий тарган (Periplaneta brunnea Burmeister), тарган Мадейри (Leucophaea maderae Fabricius); личинки та дорослі особини, що живляться листям, ряду твердокрилих Coleoptera, включаючи довгоносиків родин Anthribidae, Bruchidae та Curculionidae (наприклад, довгоносик бавовни (Anthonomus grandis Boheman), довгоносик рисовий водяний (Lissorhoptrus oryzophilus Kuschel), довгоносик комірний (Sitophilus granaries Linnaeus), довгоносик рисовий (Sitophilus oryzae Linnaeus); земляні блошиці, колорадські жуки, черв'яки коренеїди, листяні жуки, та молі-мінери родини Chrysomelidae (наприклад, колорадський картопляний жук (Leptinotarsa decemlineata Say), блошиця довговуса (Diabrotica virgifera LeConte)); хр ущі та інші жуки родини Scaribaeidae (наприклад, хрущик японський (Роріlliа japonica Newman) та європейський хрущ (Rhizotrogus majalis Razumowsky)); шкіроїди родини Dermestidae; дротяники родини Elateridae; короїди родини Scolytidae та хрущаки великі борошняні родини Tenebrionidae. Крім того, сільськогосподарські та несільськогосподарські шкідники включають: дорослі особини та личинки ряду Dermaptera, включаючи вуховійки родини Forficulidae (наприклад, вуховійка звичайна (Forficula auricularia Linnaeus), чорна вуховійка (Chelisoches morio Fabricius); дорослі особини та німфи рядів Hemiptera та Homoptera, такі як клописліпняки родини Miridae, цикади родини Cicadidae, цикадки (наприклад, видів Empoasca) із родини Cicadellidae, дельфациди із родин Fulgoroidae та Delphacidae, горбатки із родини Membracidae, листоблошиці із родини Psyllidae, алейродіди із родини Aleyrodidae, попелиці родини Aphididae, філоксера родини Phylloxeridae, червеці родини Pseudococcidae, щитівки родин Coccidae, Diaspididae та Margarodidae, клопи-мереживниці родини Tingidae, клопи-щитники родини Pentatomidae, клопи білокрилі (наприклад, видів Blissus) та інші насіннєві клопи родини Lygaeidae, пінниці родини Cercopidae, гарбузові клопи родини Coreidae та червоноклопи і червоноклопи бавовни родини Pyrrhocoridae. Також включені як 39 81791 сільськогосподарські та несільськогосподарські шкідники дорослі особини та личинки ряду Асаrі (кліщі), такі як кліщики павутинні та червоні кліщі родини Tetranychidae (наприклад, павутинні кліщики (Panonychus ulmi Koch), кліщики павутинні двоплямисті (Tetranychus uricae Koch), кліщики МакДеніела (McDaniel) (Tetranychus mcdanieli McGregor)), плоскі кліщики родини Tenuipalpidae (наприклад, кліщик плоский цитрусовий (Brevipalpus lewisi McGregor)), іржасті та брунькові кліщики родини Eriophyidae та інші кліщики, що живляться листям, і кліщики, важливі щодо здоров'я людей та тварин, тобто пилкові кліщі родини Epidermoptidae, залізниці родини Demodicidae, зернові кліщі родини Glycyphagidae, іксодові кліщі ряду Ixodidae (наприклад, кліщі оленя (Ixodes scapularis Say), австралійські паралізуючі кліщі (Ixodes holocyclus Neumann), іксодовий кліщ мінливий (Dermacentor variabilis Say), однозірковий іксодовий кліщ (Amblyomma americanum Linnaeus), кінський та коростяний кліщі родин Psoroptidae, Pyemotidae та Sarcoptidae; дорослі та незрілі особини ряду Orthoptera, включаючи сарану, кобилок та цвіркунів (наприклад, кобилки (наприклад, Melanoplus sanguinipes Fabricius, M.differentialis Thomas), сарана американська (наприклад, Schistocerca Americana Drury), пустельні кобилки (Schistocerca gregaria Forskal), мігруючі кобилки (Locusta migratoria Linnaeus), чагарникові кобилки (видів Zonocerus), цвіркун домовий (Acheta domesticus Linnaeus), кротові цвіркуни (видів Gryllotalpa)); дорослі та незрілі особини ряду Diptera, у тому числі молі-мінери, галіци, дрозофіли (Tephritidae), мушки шведські (наприклад, Oscinella frit Linnaeus), грунтові личинки комах, домашні мухи (наприклад, Muska domestica Linnaeus), малі домашні мухи (наприклад, Fannia canicularis Linnaeus, F. femoralis Stein), жигалки осінні (наприклад, Stomoxys calcitrans Linnaeus), лицьові мухи, жигалки коров'ячі малі, яєчні мухи (наприклад, видів Chrysomya, Phormia), та інші справжні мушині шкідники, конячі мухи (наприклад, видів Tabanus), оводові мухи (наприклад, видів Gastrophilus, Oestrus), червоподібні личинки скота (наприклад, видів Hypoderma), оленячі мухи (наприклад, видів Chrysops), рунці вівці (наприклад, Melophagus ovinus Linnaeus) та інші Brachycera, москіти (наприклад, видів Aedes, Anopheles, Culex), скатопсиди (наприклад, видів Prosimulium, Simulium), мокреці, мошки, скіаріди та інші Nematocera; дорослі та незріли особини ряду Thysanoptera, включаючи трипс тютюновий {Thrips tabaci Lindeman), трипси пшеничні (видів Frankliniella), та інші трипси, що живляться листям; комашині шкідники ряду Hymenoptera, включаючи мурашок (наприклад, рудий мурахадеревоточильник (Camponotus ferrugineus Fabricius), мураха-деревоточильник пенсільванський (Camponotus pennsylvanicus De Geer), фараонова мураха (Monomorium pharaonis Linnaeus), васманія (Wasmannia auropunctata Roger), мураха Ріхтера (Solenopsis geminata Fabricius), руда мураха Ріхтера (Solenopsis invicta Buren), мураха аргентинська (Iridomyrmex humilis 40 Ma yr), паратрехіна (Paratrechina longicornis Latreille), мураха дернова (Tetramorium caespitum Linnaeus), мураха кукурудзяного поля (Lastius alienus Forster), мураха (Таріпота sessile Say)), бджоли (включаючи бджіл-теслярів), оси, жовті личинки, справжні оси та пилярі справжні (видів Neodiprion; Cephus); комашині шкідники роду Isoptera, включаючи термітів жовтоногих (Reticulitermes flavipes Kollar), термітів (Reticulitermes Hesperus Banks), термітів (Coptotermes formosanus Shiraki), вест-індських термітів сухостою (Incisitermes immigrants Snyder) та інших важливих з економічної точки зору термітів; комашині шкідники ряду Thysanura, такі як лускунниця (Lepisma saccharina Linnaeus) та лускунниця домашня (Thermobia domestica Packard); комашині шкідники ряду Mallophaga, і включаючи вошу головну (Pediculus humanus capitis De Geer), вошу тілесну (Pediculus humanus humanus Linnaeus), пухоїда (Menacanthus stramineus Nitszch), волосоїда собачого (Trichodectes canis De Geer), пухоїда курячого строкаточеревного (Goniocotes gallinae De Geer), вошу вівці (Bo vicola ovis Schrank), вошу бичачу коротконосу (Haematopinus eurysternus Nitzsch), вошу великої рогатої худоби довгоносу кровосисну (Linognathus viruli Linnaeus) та інші сисні або жуйні паразитичні воші, що нападають на людину та тварин; комашині шкідники ряду Siphonoptera, включаючи щурячу східну блоху (Xenopsylla cheopis Rothschild), блоху котячу (Ctenocephalides felis Bouche), блоху собачу (Ctenocephalides canis Curtis), блоху курячу (Ceratophyllus gallinae Schrank), присисну блоху (Echidnophaga gallinacea Westwood), блоху людську (Pulex irritans Linnaeus) та інших блох, що турбують ссавців та птахів. Додаткові безхребетні шкідники, що охоплюються даним винаходом, включають: павуків ряду Аrаnеае, таких як коричневий павук-самітник (Loxosceles reclusa Gertsch & Mulaik) та "чорну удову" (Latrodectus mactans Fabricius), та губоногих ряду Scutigeromorpha, таких як мухоловка звичайна (Scutigera coleoptrata Linnaeus). Сполуки даного винаходу виявляють також активність щодо членів класів Nematoda, Cestoda, Trematoda та Acanthocephala, включаючи важливі в економічному плані члени рядів Strongylida, Ascaridida, Oxyurida, Rhabditida, Spirurida та Enoplida, такі як, проте не обмежуючись цим, економічно важливі сільськогосподарські шкідники (тобто нематоди кореневого наросту роду Meloidogyne, нематодишкідники роду Pratylenchus, приземкуватокореневі нематоди роду Trichodorus і т.д.), та шкідники, що зашкоджують здоров'ю людей та тварин (тобто всі економічно важливі трематоди, стрічкові черв'яки та круглі черв'яки, такі як Strongylus vulgaris у коней, Toxocara canis у собак, Haemonchus contortus у овець, Dirofilaria immitis Leidy у собак, Anoplocephala perfoliata у коней, Fasciola hepatica Linnaeus у жуйних тварин, і т.д.). Сполуки даного винаходу виявляють особливо високу активність проти шкідників ряду Lepidoptera (наприклад, Alabama argillacea Hubner (гусінь совки бавовни американська), Archips argyrospila 41 81791 Walker (трубкокрути листя фруктови х дерев), A. rosana Linnaeus (листовійки європейські) та інші види Archips, Chilo suppressalis Walker (свердлувальники рисового стебла), Cnaphalocrosis medianalis Guenee (листовійки рисові), Crambus caliginosellus Clemens (вогневки), Crambus teterrellus Zincken (вогневка), Cydia pomonella Linnaeus (плодожерка яблунева), Earias insulana Boisduval (колючий коробочний черв'як бавовни), Earias vittella Fabricius (плямистий коробочний черв'як бавовни), Helicoverpa armigera Hubner (американський коробочний черв'як бавовни), Helicoverpa zea Boddie (совка бавовни), heliothis virescens Fabricius (тютюнова листовійкабрунькоїд), Herpetogramma licarsisalis Walker (лучні метелики), Lobesia botrana Denis & Schiffermuller (листовійка виноградна), Pectinofora gossypiella Saunders (рожевий коробочний черв'як бавовни), Phyllocnistis citrella Stainton (мільмінер цитрусова), Pieris brassicae Linnaeus (великий білий метелик), Pieris rapae Linnaeus (малий білий метелик), Plutella xylostella Linnaeus (капустяна міль), Spodoptera exigua Hubner (буряковий "похідний" черв'як), Spodoptera litura Fabricius (тютюнова совка, кластер гусені), Spodoptera fugiperda J.E. Smith (осінній "похідний" черв'як), Trichoplusia nі Hubner (капустяна п'ядениця) та Tuta absoluta Me yrick (молі-мінери томатів). Сполуки даного винаходу також мають комерційно значиму активність щодо членів ряду Homoptera, включаючи Acyrthisiphon pisum Harris (тля горохова), Aphis craccivora Koch (тля чорна люцернова), Aphis fabae Scopoli (тля чорна бобова), Aphis gossypii Glover (тля бавовни), Aphis pomi De Geer (тля яблунева), Aphis spraecola Patch (тля таволгова), Aulacorthum solani Kaltenbach (тля в'юнкова), Chaetosiphon fragaefolii Cockerell (тля суниці), Diuraphis noxia Kurdjumov/Mord vilko (тля пшениці російська), Dysaphis plantaginea Paaserini (тля розова), Eriosoma lanigerum Hausmann (тля кров'яна яблунева), Hyalopterus pruni Geoffroy (тля борошниста сливова), Lipaphis erysimi Kaltenbach (тля псевдокапустяна), Metopolophium dirrhodum Walker (тля зернова), Macrosipum euphorbiae Thomas (тля картопляна листяна), Myzus persicae Sulzer (тля персиково-картопляна, тля персикова), Nasonovia ribisnigri Mosley (тля салатна), видів Pemphigus (коренева тля та галоутворююча тля), Rhopalosiphum maidis Fitch (тля кукурудзяна листяна), Rhopalosiphum padi Linnaeus (тля вівсяна), Schizaphis graminum Rondani (тля злакова звичайна), Sitobion avenue Fabricius (тля злакова), Therioaphis maculata Buckton (тля плямиста люцерни). Toxoptera aurantii Boyer de Fonscolombe) (тля чайна), та Toxoptera citricida Kirkaldy (тля цитрусова), видів Adelges (хермес), Phylloxera devastatrix Pergande (філоксера гікорі); Bemisia tabaci Gennadius (білокрилка тютюнова, білокрилка батату), Bemisia argentifolii Bellows & Perring (білокрилки леукофілуму), Dialeurodes citri Ashmead (білокрилка цитрусова) та Trialeurodes vaporariorum Westwood (білокрилка теплична); Empoasca fabae Harris (цикадка картопляна), Laodelphax striatellus Fallen (малі дельфациди), Macrolestes quadrilineatus Forbes (цикадка зіркова), 42 Nephotettix cinticeps Uhler (цикадка зелена), Nephotettix nigropictus Stal (цикадка рисова), Nilaparvata lugens Stal (коричневі дельфациди), Peregrinus maidis Ashmead (зернові дельфациди), Sogatella furcifera Horvath (білоспинні дельфациди), Sogatodes orizicola Muir (рисові дельфациди), Typhlocyba pomaria McAtee (цикадка яблунева), видів Erythroneoura (цикадка виноградна); Magicidada septendecin Linnaeus (цикада періодична), leery a purchasi Maskell (червець австралійський жолобчастий), Quadraspidiotus perniciosus Comstock (червець Сан-Хосе), Planococcus citri Risso (червець виноградний борошнистий); видів Pseudococcus (інший комплекс червеців); Cacopsylla pyricola Foerster (мідяниця грушева), Trio za diospyri Ashmead (листоблошиця хурмова). Ці сполуки також виявляють активність щодо членів ряду Hemiptera, включаючи: Acrosternum hilare Say (клопів-щитників звичайних), Anasa tristis De Geer (клопів гарбузових), Bissus leucopterus leucopterus Say (клопів білокрилих), Corythuca gossypii Fabricius (клопів бавовни), Cyrtopeltis modesta Distant (клопів томатів), Dysdercus suturellus Herrich-Schaffer (червоноклопів бавовни), Euchistus servus Say (клопів-щитників коричневих), Euchistus variolarius Palisot de Beauvois (клопівщитників одноплямистих), видів Graptosthetus (комплекс клопів насіннєвих), Leptoglossus corculus Say (клопів-краєвиків соснових), Lygus lineolaris Palisot de Beauvois (клопиків лучних), Nezara viridula Linnaeus (клопів-щитників злакових південних), Oebalus pugnax Fabricius (клопівщитників рисових), Oncopeltus fasciatus Dallas (клопів молочайних великих), Pseudatomoscelis seriatus Reuter (блошиць бавовни). Інші ряди комах, що контролюються сполуками даного винаходу, включають Thysanoptera (наприклад, Frankiniella occidentalis Pergande (трипс пшеничний західний), Scirthothrips citri Moulton (трипс цитрусовий), Sericothrips variabilis Beach (трипс соєвий), та Thrips tabaci Lindeman (трипс тютюновий); та ряд Coleoptera (наприклад, Leptinotarsa decemlineata Say (колорадський картопляний жук), Epilachna varivestis Mulsant (мексиканський бобовий жук) та дротяники родів Agriotes, Athous або Limonius). Сполуки даного винаходу можуть також змішува тись з однією або кількома іншими біологічно активними сполуками або агентами, включаючи інсектициди, фунгіциди, нематоциди, бактерициди, акарициди, регулятори росту, такі як стимулятори укорінення, хемостерилізатори, семіохімікати, репеленти, атрактанти, феромони, живильні стимулятори, інші біологічно активні сполуки або ентомопатогенні бактерії, віруси або грибки, з утворенням багатокомпонентного пестициду, що дає навіть ширший спектр сільськогосподарського або несільськогосподарського застосування. Таким чином, даний винахід також стосується композиції, що включає біологічно ефективну кількість сполуки Формули 1 та ефективну кількість принаймні однієї додаткової біологічно активної сполуки або агента, і, крім того, включає принаймні одну поверхнево 43 81791 активну речовину, твердий розріджувач або рідкий розріджувач. Приклади таких біологічно активних сполук або агентів, з якими можуть бути змішані сполуки даного винаходу, наступні: інсектициди, такі як абамектин, ацефат, ацетаміприд, ацетопрол, амідофлумет (S-1955), авермектин, азадирактин, азинфос-метил, біфентрин, біфеназат, бістрифлурон, бупрофезин, карбофуран, хлор фенапір, хлорфлуазурон, хлорпірифос, хлорпірифос-метил, хлормафенозид, клотіанідин, цифлутрин, бетацифлутрин, цигалотрин, ламбда-цигалотрин, циперметрин, циромазин, дельтаметрин, діафентіурон, діазинон, дифлубензурон, диметоат, динотефуран, діофенолан, емамектин, ендосульфан, есфенвалерат, етипрол, фенотікарб, феноксикарб, фенпропатрин, фенвалерат, фіпроніл, флонікамід, флюцитринат, тау-флувалінат, флуфенерім (UR-50701), флуфеноксурон, гамма-калотрин, галофенозид, гексафлумурон, імідаклоприд, індоксакарб, ізофенфос, луфенурон, малатіон, метальдегід, метамідофос, метидатіон, метоміл, метопрен, метоксихлор, метоксифенозид, метофлутрін, монокротофос, метоксифенозид, новалурон, новіфлумурон (XDE-007), оксаміл, паратіон, паратіон-метил, перметрин, форат, фосалон, фосмет, фосфамідон, піримікарб, профенофос, профлутрин, протрифенбут, піметрозин, піридаліл, пірипроксифен, ротенон, S 1812 (Valent) спіносад, спіромезифен (BSN 2060), сульпрофос, тебуфенозид, тефлубензурон, тефлутрин, тербуфос, те трахлорвінфос, тіаклоприд, тіаметоксам, тіодикарб, тіосультап-натрій, толфенпірад, тралометрин, трихлорфон та трифлумурон; фунгіциди, такі як ацибензолар, Sметил, азоксистробін, беналазі-М, бентіавалікарб, беноміл, бластицидин-S, бордоська суміш (триосновний сульфат міді), боскалід, бромуконазол, бутіобат, карпропамід, каптафол, каптан, карбендазім, хлоронеб, хлороталоніл, клотримазол, охксихлорид міді, солі міді, цимоксаніл, ціазофамід, цифлуфенамід, ципроконазол, ципродиніл, диклоцимет, дикломезин, диклоран, дифеноконазол, диметоморф, димоксистробін, диніконазол, диніконазол-М, додин, едифенфос, епоксиконазол, етабоксам, фамоксадон, фенаримол, фенбуконазол, фенгексамід, феноксаніл, фенпіклоніл, фенпропідин, фенпропіморф, фентин ацетат, фентин гідроксид, флуазинам, флудіоксоніл, флуморф, флуоксастробін, флухінконазол, флузілазол, флутоланіл, флутріафол, фолпет, фозетил-алюміній, фуралаксил, фураметапір, гуазатін, гексаконазол, гімексазол, імазаліл, імібенконазол, іміноктадин, іпконазол, шпробенфос, іпродіон, іпровалікарб, ізоконазол, ізопротіолан, касугаміцин, ксероксимметил, манкозеб, манеб, мефеноксам, мепанапірим, мепроніл, металаксил, метконазол, метоміностробін/феноміностробін, метрафенон, міконазол, міклобутаніл, нео-азорин (метанарсонат заліза III), нуаримол, оризастробін, оксадиксил, окспоконазол, пенконазол, пенцикурон, пікобензамід, пікоксистробін. 44 пробеназол. прохлораз, пропамокарб, пропіконазол, прохіназид, протіоконазол, піраклостробін, піриметаніл, пірифенокс, пірохілон, хіноксифен, силтіофам, симеконазол, сипконазол, спіроксамін, сірка, тебуконазол, тетраконазол, тіадиніл, тіабендазол, тифлузамід, тіофанатметил. тіарам, толілфлуанід, триадимефон, триадименол, триаримол, трициклазол, трифлоксистробін, трифлумізол, трифорин, тритиконазол, уніконазол, валідаміцин, винклозолін та зоксамід; нематоциди, такі як алдикарб, оксаміл та фенаміфос; бактерициди, такі як стрептоміцин; акарициди, такі як амітраз, кінометіонат, хлоробензилат, цигексатин, дикофол, дієнохлор, етоксазол, феназахін, фенбутатин оксид, фенпропатрин, фенпіроксимат, гекситіазокс, пропаргіт, пірідабен та тебуфенпірад; та біологічні агенти, такі як Bacillus thuringiensis, включаючи види aizawai та kurstaki, Bacillus thuringiensis дельта ендотоксин, бакуловірус, та ентомопатогенні бактерії, віруси та грибки. Сполуки даного винаходу та їх композиції можуть застосовуватись до рослин, генетично трансформованих для експресії білків, токсичних щодо безхребетних шкідників (таких як токсин Bacillus thuringiensis). Ефект екзогенно нанесених сполук даного винаходу для контролю безхребетних шкідників може бути синергічним з експресованими токсиновими білками. Загальні посилання на зазначені засоби захисту сільськогосподарських культур можна знайти у роботі [The Pesticide Manual, 12th Edition, C.D.S. Tomlin, Ed., British Crop Protection Council, Farnham, Surrey, U.K., 2000]. Інсектициди та акарициди для змішування зі сполуками даного винаходу, яким віддається перевага, включають піретроїди, такі як ацетаміприд, циперметрин, цигалотрин, цифлутрин, бета-цифлутрин, есфенвалерат, фенвалерат та тралометрин; карбамати, такі як фенотикарб, метоміл, оксаміл та тіодикарб; неонікотиноїди, такі як клотианідин, імідаклоприд та тіаклоприд; нейронні блокатори натрієвих каналів, такі як індоксакарб; інсектицидні макроциклічні лактони, такі як спіносад, абамектин, авермектин та емамектин; антагоністи γ-аміномасляної кислоти (GABA), такі як ендосульфан, етипрол та фіпроніл; інсектицидні сечовини, такі як флуфеноксурон та трифлумурон; міметики ювенільного гормону, такі як діофенолан та пірипроксифен; піметрозин; та амітраз. Біологічні агенти для змішування зі сполуками даного винаходу, яким віддається перевага, включають Bacillus thuringiensis та Bacillus thuringiensis дельта ендотоксин, так само як і природні, генетично модифіковані вірусні інсектициди, включаючи членів родини Baculoviridae, так само як і ентомофагові грибки. Суміші, яким віддається найбільша перевага, включають суміш сполуки даного винаходу з цигалотрином; суміш сполуки даного винаходу з бета-цифлутрином; суміш сполуки даного винаходу зесфенвалератом; суміш сполуки даного винаходу з метомілом; суміш сполуки даного винаходу з імідаклопридом; суміш сполуки даного 45 81791 винаходу з тіаклопридом; суміш сполуки даного винаходу з індоксакарбом; суміш сполуки даного винаходу з абамектином; суміш сполуки даного винаходу з ендосульфаном; суміш сполуки даного винаходу з етипролом; суміш сполуки даного винаходу з фіпронілом; суміш сполуки даного винаходу з флуфеноксуроном; суміш сполуки даного винаходу з пірипроксифеном; суміш сполуки даного винаходу з піметрозином; суміш сполуки даного винаходу з амітразом; суміш сполуки даного винаходу з Bacillus thuringiensis aizawai або Bacillus thuringiensis kurstaki, та суміш сполуки даного винаходу з Bacillus thuringiensis дельта ендотоксином. У деяких випадках особливо вигідними для контролю резистентності є комбінації зі сполуками або агентами проти безхребетних шкідників, що мають схожий спектр контролю, але відмінний спосіб дії. Таким чином, композиції даного винаходу можуть додатково включати біологічно ефективну кількість принаймні однієї додаткової сполуки для контролю безхребетних шкідників або агента, що має схожий спектр контролю, але відмінний спосіб дії. Контактування рослини, що була генетично модифікована для експресії захисної сполуки (наприклад, білка), або ділянки рослини з біологічно ефективною кількістю сполуки даного винаходу може також запровадити ширший спектр захисту рослини і може бути сприятливим для контролю резистентності. Контроль безхребетних шкідників у сільськогосподарських та несільськогосподарських галузях здійснюється шляхом застосування однієї або кількох сполук даного винаходу, в ефективній кількості, до навколишнього середовища, де перебувають зазначені шкідники, включаючи сільськогосподарський та/або несільськогосподарський осередок ураження, до ділянки, що має захищатись, або безпосередньо до даних шкідників, які мають контролюватись. Таким чином, даний винахід також стосується способу контролю безхребетних шкідників у сільськогосподарських та/або несільськогосподарських галузях, що включає контактування даних шкідників або їх середовища перебування з біологічно ефективною кількістю однієї або кількох сполук даного винаходу, або з композицією, що включає принаймні одну таку сполуку або композицію, яка містить принаймні одну таку сполуку та ефективну кількість принаймні однієї додаткової біологічно активної сполуки або агента. Приклади придатних композицій, що містять сполуку даного винаходу та ефективну кількість принаймні однієї додаткової біологічно активної сполуки або агента, включають гранульовані композиції, де зазначена додаткова біологічно активна сполука присутня у тій самій гранулі де й сполука даного винаходу, або в окремих гранула х. Способом контактування, якому віддається перевага, є розпилення. Як альтернатива, гранульована композиція, що включає сполуку даного винаходу, може наноситись на листя даної рослини або на грунт. Сполуки даного винаходу також ефективно доставляються шляхом 46 поглинання рослиною через контакт даної рослини з композицією, яка містить сполуку даного винаходу, шляхом просочування грунту рідким препаратом, внесення гранульованого препарату у грунт, обробки ящика розсадника або протравлювання саджанців. Сполуки даного винаходу також ефективні при місцевому застосуванні композиції, що містить сполуку даного винаходу, до осередку ураження. Інші способи контактування включають нанесення сполуки або композиції даного винаходу прямим та непрямим розбризкуванням, розпиленням аерозолю, нанесенням гелю, нанесенням покриття на насіння, мікрокапсулюванням, системним поглинанням, за допомогою приманок, серг, харчових гр удок, аерозольних генераторів, фумігантів, дуетів та з використанням інших способів. Сполуками даного винаходу можуть бути також просочені матеріали, що йдуть на виготовлення пристроїв для контролю за шкідниками (наприклад, ловильних сіток для комах). Сполука даного винаходу може бути введена у композицію приманки, котра уживається безхребетним шкідником або застосовується у пристроях, таких як пастки, пристрої для приманювання і таке подібне. Така приманкова композиція може бути у формі гранул, що включають (а) активний інгредієнт, а саме, сполуку Формули 1, її N-оксид або сіль, (b) один або кілька харчових матеріалів, (с) при потребі, атрактант, і (d) при потребі, один або кілька зволожувачів. Привертають увагу гранули або приманкові композиції, котрі містять приблизно від 0,001 до 5% активного інгредієнта, приблизно 40-99% харчового матеріалу та/або атрактанту, і, при потребі, приблизно 0,05-10% зволожувачів; ці композиції ефективні в плані контролю ґрунтових безхребетних шкідників при дуже низьких нормах внесення, зокрема, при дозах активного інгредієнта, що є летальними, скоріше, при заковтуванні, а не при прямому контакті. Примітно, що деякі харчові матеріали можуть діяти одночасно як джерело їжі та як атрактант. Харчові матеріали включають вуглеводні, білки та ліпіди. Прикладами харчових матеріалів є рослинне борошно, цукор, крохмалі, тваринний жир, рослинна олія, дріжджові екстракти та тверді молокопродукти. Прикладами атрактантів є одоранти та ароматизатори, такі як фруктові або рослинні екстракти, парфуми або інші тваринні чи рослинні компоненти, феромони або інші агенти, відомі як засоби для приманювання безхребетних шкідників, з якими проводиться боротьба. Прикладами зволожувачів, тобто агентів, що зберігають вологу, є гліколі та інші поліоли, гліцерин та сорбіт. Примітною є приманкова композиція (та спосіб, де використовується така композиція), що застосовується для контролю безхребетних шкідників, включаючи, окремо або у комбінації, мурашок, термітів та тарганів. Пристрій для контролю за безхребетними шкідниками може включати приманкову композицію даного винаходу та корпус, пристосований для розміщення зазначеної приманкової композиції, де зазначений 47 81791 корпус має принаймні один отвір, розмір якого дозволяє даному безхребетному шкіднику проходити через зазначений отвір, так що даний безхребетний шкідник може скористатись доступом до зазначеної приманкової композиції із місця знаходження поза даним корпусом, і де зазначений корпус додатково пристосований для розміщення в/поблизу осередку потенційної або відомої діяльності зазначеного безхребетного шкідника. Сполуки даного винаходу можуть наноситись у своєму чистому стані, але найбільш часто дана аплікація буде являти собою препарат, що включає одну або кілька сполук з придатними носіями, розріджувачами та поверхнево-активними речовинами, та, можливо, у комбінації з їжею, у залежності від потрібного кінцевого застосування. Спосіб нанесення, якому віддається перевага, включає розпилення водної дисперсії або очищеного масляного розчину даних сполук. Комбінації аерозольних масел, аерозольних масляних концентратів, розпилених зв'язувальних речовин, ад'ювантів, інших розчинників та синергистів, таких як піперонілбутоксид, у багатьох випадках підсилюють ефективність даної сполуки. Для несільськогосподарських застосувань такі спреї можуть наноситись із аерозольних контейнерів, таких як банки, пляшки або інші посудини, або з використанням помпи, або шляхом вивільнення із герметизованого контейнера, наприклад, герметизованого аерозольного балончика. Такі спреєві композиції можуть набувати різних форм, наприклад, спреїв, дисперсій, туманів, пін, димів або туманів. Такі спреєві композиції можуть додатково містити пропеланти, піноутворювачі і т.д., у залежності від потреби. Заслуговує на увагу спреєва композиція, що містить сполуку або композицію даного винаходу та пропелант. Репрезентативні пропеланти включають, проте не обмежуючись цим, метан, етан, пропан, ізопропан, бутан, ізобутан, бутен, пентан, ізопентан, неопентан, пентен, фторовуглеводні, хлорофторовуглеці, диметиловий ефір, та суміші із зазначеного вище. Заслуговує на увагу спреєва композиція (та спосіб застосування такої спреєвої композиції, що розливається із посудини, котра містить спрей), що використовується для контролю безхребетних шкідників, включаючи, окремо або у комбінації, москітів, скатопсидів, ос, жовтих личинок, шершнів, кліщів, павуків, мурашок, комарів і такого подібного. Норма внесення, потрібна для ефективного контролю (тобто "біологічно ефективна кількість"), буде залежати від таких чинників як вид безхребетного шкідника, що має контролюватись, життєвий цикл даного шкідника, стадія розвитку, розміри, місце знаходження, час року, хазяйська культура або тварина, характер живлення, парувальна поведінка, вологість довкілля, температура і таке подібне. За нормальних умов норми внесення від приблизно 0,01 до 2кг активного інгредієнту на гектар є достатніми для контролю шкідників в сільськогосподарських екосистемах, але може також бути достатнім лише 48 0,0001кг/га або аж до 8кг/га. Для цілей несільськогосподарського призначення ефективні норми застосування можуть варіювати приблизно від 1,0 до 50мг/м 2, але може бути також достатнім лише 0,1мг/м 2 або аж до 150мг/м 2. Фахівець у даній галузі легко визначить біологічно ефективну кількість, що потрібна для забезпечення потрібного рівня контролю безхребетних шкідників. Наступні тести демонструють ефективність контролю специфічних шкідників за допомогою сполук даного винаходу. "Ефективність контролю" представляє собою інгібування розвитку безхребетних шкідників (включаючи смертність), що суттєво знижує живлення. Захист від шкідників, що забезпечується даними сполуками, проте, не обмежується зазначеними видами. Дивись Вказівні Таблиці А, В та С щодо опису сполук. У даних Вказівних Таблицях використовуються наступні скорочення: і відповідає ізо, t відповідає третинному, Me відповідає метилу, Et відповідає етилу, Рr відповідає пропілу, і-Рr відповідає ізопропілу, с-Pr відповідає циклопропілу, Вu відповідає бутилу, і CN відповідає ціано. Під скороченням "Ехр" мається на думці "Приклад", і наступний за ним номер вказує, в якому прикладі одержана дана сполука. 49 81791 50 (У даній Таблиці "compound" відповідає "сполуці", "m.p." відповідає Тпл.; * Див. Вказівну таблицю С щодо 1H Я МР даних) ВКАЗІВНА ТАБЛИЦЯ С (У даній Таблиці шапка: Сполука № 1H ЯМР дані (якщо не зазначено інше, розчин CDCl3) 51 81791 Біологічні приклади винаходу теста Для оцінки контролю капустяної молі (Plutella xylostella) використовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 12-14 денною рослиною редиски. Вона була попередньо інфікована 10-15 новонародженими личинками на шматку корму комахи з використанням пробовідбірника для перенесення пробки з личинками та їжею у випробувальну комірку. Дані личинки рухались по випробуваній рослині у міру висихання корму. Випробувані сполуки компонували з використанням розчину, що містив 10% ацетону, 90% води та 300млн -1 неіонної поверхневоактивної речовини Х-77® Spreader Lo-Foam Formula, що містила алкіларилполіоксиетилен, вільні жирні кислоти, гліколі та ізопропанол (фірма Loveland Industries, Inc. Greeley, Colorado, USA). Препарати даних сполук наносились в 1мл рідини через розпилювальну форсунку SUJ2 1/8 JJ звичайної конструкції (Spraying Systems Co. Wheaton, Illinois, USA), розміщену на відстані 1,27см (0,5дюйм) над верхньою частиною кожної випробувальної комірки. Усі експериментальні сполуки у цих тестах розпилювали при 50млн -1 з трикратним повторенням. Після розпилення препарату випробуваної сполуки кожну комірку піддавали сушінню протягом 1 години і потім накривали чорним сітчастим ковпачком. Зазначені випробувальні комірки витримували протягом 6 діб у ростовій камері при 25°С та 70% відносній вологості. Шкоду, завдану рослині, оцінювали потім візуально, виходячи із кількості спожитого листя. Із випробуваних сполук наступні забезпечували від дуже добрих до чудови х рівнів захисту рослин (ушкодження живлення 20% або менше): 1, 2, 3, 4, 5, 6, 7 , 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 88, 89, 90, 91, 92, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103,106, 108, 109, 110, 111 та 112. Тест В Для оцінки контролю осінніх "похідних" черв'яків (Spodoptera frugiperda) застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 4-5 денною рослиною кукурудзи (маїсу). Вона була 52 попередньо інфікована (з використанням пробовідбірника) 10-15 1-денними личинками на шматку корму комахи. Випробувані сполуки складали та розпилювали при 50млн -1 як описано для Тесту А. Аплікації проводили три рази. Після розпилення випробувальні комірки витримувались у ростовій камері і потім візуально оцінювались як описано для Тесту А. Із випробуваних сполук наступні забезпечували чудові рівні захисту рослин (ушкодження живлення 20% або менше): 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 63, 64, 65, 66, 67, 68, 70, 73, 74, 76, 78, 88, 91, 92, 94, 95, 96, 98, 99, 100, 101, 102, 103, 106, 109, 110, 111 та 112. Тест С Для оцінки контролю тлі персикової (Muzus persicae) шляхом контакту та/або за допомогою системних засобів застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 12-15 денною рослиною редиски. Вона була попередньо інфікована шляхом поміщення на лист випробуваної рослини 30-40 тлей на шматку листа, вирізаного з культурної рослини (метод зрізу листа). Дані личинки рухались по випробуваній рослині у міру десикації даного шматка листа. Після зазначеного попереднього інфікування грунт випробувальної комірки був покритий шаром піску. Випробувані сполуки компонували з використанням розчину, що містив 10% ацетону, 90% води та 300млн -1 неіонної поверхневоактивної речовини Х-77® Spreader Lo-Foam Formula, що містила алкіларилполіоксиетилен, вільні жирні кислоти, гліколі та ізопропанол (фірма Loveland Industries, Inc. Greeley, Colorado, USA). Препарати даних сполук наносились в 1мл рідини через розпилювальну форсунку SUJ2 1/8 JJ звичайної конструкції (Spraying Systems Co.), розміщену на відстані 1,27см (0,5дюйм) над верхньою частиною кожної випробувальної комірки. Усі експериментальні сполуки у цьому тестуванні розпилювались при 250млн -1 з 3кратним повторенням. Після розпилення препарату випробуваної сполуки кожну комірку піддавали сушінню протягом 1 години і потім накривали чорним сітчастим ковпачком. Зазначені випробувальні комірки витримували протягом 6 діб у ростовій камері при 19-21°С та 50-70% відносній вологості. Потім проводили візуальну оцінку кожної випробувальної комірки щодо смертності комах. Із випробуваних сполук наступні давали принаймні 80% смертність: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 40, 41, 43, 44, 46, 47, 48, 49, 50, 51, 52, 53, 55, 56, 63, 65, 66, 67, 68, 69, 70, 73, 74, 76, 78, 88, 89, 90, 91, 92, 94, 95, 96, 98, 99, 100, 101, 102, 103, 106, 108, 109, 110, 111 та 112. Тест D 53 81791 Для оцінки контролю цикадки картопляної (Empoasca fabae Harris) шляхом контакту та/або за допомогою системних засобів застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 5-6 денною рослиною бобів Longio (з вже сформованими первинними листками). Перед аплікацією на верхню частину ґрун ту насипали білий пісок, і один із первинних листків був підданий ексцизії. Випробувані сполуки готувались та розпилювались при 250млн-1 з 3-кратним повторенням як описано для Тесту С. Після розпилення випробувальні комірки піддавали сушінню протягом 1 години перед тим як постінфікувати 5 картопляними цикадками (18-21 денні дорослі особини). На верхню частину циліндра помішували чорний сітчастий ковпачок. Зазначені випробувальні комірки витримували протягом 6 діб у ростовій камері при 19-21°С та 50-70% відносній вологості. Потім проводили візуальну оцінку кожної випробувальної комірки щодо смертності комах. Із випробуваних сполук наступні давали принаймні 80% смертність: 1, 3, 4, 5, 6, 8, 9, 10, 12, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 32, 33, 34, 35, 37, 38, 40, 41, 43, 44, 46, 47, 48, 49, 50, 51, 52, 53, 55, 56, 63, 66, 67, 68, 70, 73, 76, 88, 89, 90, 94, 95, 98, 99, 101, 103, 106, 108, 109, 110, 111 та 112. Тест Е Для оцінки контролю тлі бавовни (Aphis gossypii) шляхом контакту та/або за допомогою системних засобів застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 6-7 денною рослиною бавовни. Вона була попередньо інфікована 30-40 комахами на шматку листа згідно з методом зрізу листа, описаним для Тесту С, і грунт випробувальної комірки був покритий шаром піску. Випробувані сполуки готувались та розпилювались при 250млн-1 з 3-кратним повторенням як описано для Тесту D. Після розпилення випробувальні комірки витримували у ростовій камері і потім візуально оцінювали як описано для Тесту D. Із випробуваних сполук наступні давали принаймні 80% смертність: 1, 2, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 24, 25, 26, 27, 28, 29, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 43, 44, 46, 47, 48, 49, 50, 51, 52, 53, 55, 56, 63, 69, 71, 72, 74, 76, 78, 79, 81, 84, 88, 89, 90, 91, 92, 95, 96, 97, 98, 99, 100, 101, 102,103, 106, 108, 109, 110, 111 та 112. Тест F Для оцінки контролю цикади кукурудзяної (Peregrinus maidis) через контакт або з використанням системних засобів застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 3-4 денною рослиною (колосом) кукурудзи (маїсу). Перед аплікацією на верхню частину ґрунту насипали білий пісок. Випробувані сполуки готувались та розпилювались при 250млн -1 з 3кратним повторенням як описано для Тесту С. 54 Після розпилення випробувальні комірки піддавали сушінню протягом 1 години перед тим як пост-інфікувати 10-20 цикадами кукурудзяними (18-20 денні німфи) шляхом їх насипання на пісок за допомогою солонки. На верхню частину циліндра помішували чорний сітчастий ковпачок. Зазначені випробувальні комірки витримували протягом 6 діб у ростовій камері при 19-21°С та 50-70% відносній вологості. Потім проводили візуальну оцінку кожної випробувальної комірки щодо смертності комах. Із випробуваних сполук наступні давали принаймні 80% смертність: 1, 2, 3, 4, 5, 6, 8, 10, 11, 12, 13, 18, 20, 24, 25, 26, 27, 28, 29, 32, 33, 35, 37, 38, 39, 40, 41, 43, 45, 46, 47, 48, 49, 50, 51, 53, 56, 88, 89, 90, 91, 94, 95, 108 та 109. Тест G Для оцінки контролю білокрилки леукофілуму (Bemisia tabaci) застосовувалась випробувальна комірка, що містила 14-21 денну рослину бавовни, яка вирощувалась у середовищі Redi-earth® (Scotts Co.), з принаймні двома справжніми листками, котрі були інфіковані німфами 2-ої та 3ої вікових стадій на нижній частині даних листків. Випробувані сполуки компонувались у не більше, ніж 2мл ацетону і потім розводились водою до 25-30мл. Складені композиції наносились з використанням плоскої вентиляторно-повітряної форсунки (Spraying Systems 122440) під тиском 10 фунт/кв.дюйм (69кПа). Рослини опилювались до стікання на поворотному розпилювачі. Усі експериментальні сполуки у цьому тестуванні розпилювались при 250млн -1, і це повторювалось три рази. Після розпилення випробуваної сполуки випробувальні комірки витримувались протягом 6 діб у ростовій камері при 50-60% відносній вологості та температурі 28°С вдень і при 24°С вночі. Потім листки вилучали, і мертві та живі німфи підраховувались для визначення відсотку смертності. Із випробуваних сполук наступні давали принаймні 80% смертність: 2, 3, 4, 5, 7, 8, 9, 10, 24, 25, 26, 27, 28, 30, 32, 33, 34, 35, 38, 41, 46, 48, 49, 51, 52, 53, 66, 67, 70, 73, 88, 92 та 98. Тест H Для оцінки переміщення сполук у рослинах та контролю тлі персикової (Muzus persicae) і цикадки картопляної (Empoasca fabae) після листяного переміщення сполуки через дану рослину застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 12-15 денною рослиною редиски (для тесту на тлю персикову) або з 5-6 денною рослиною бобів Longio (для тесту на цикадку картопляну). Випробувані сполуки компонували з використанням розчину, що містив 10% ацетону, 90% води та 600млн -1 неіонної поверхневоактивної речовини Х-77® Spreader Lo-Foam Formula, що містила алкіларилполіоксиетилен, вільні жирні кислоти, гліколі та ізопропанол (фірма Loveland Industries, Inc.). Препарати даних сполук наносились у 20мкл піпеткою на два більших фотосинтетично активних листки. Усі експериментальні сполуки у цих тестах 55 81791 наносились при 1000млн -1, і тести повторювали три рази. Після нанесення препарату випробуваної сполуки грунт у кожній випробувальній комірці покривали шаром піску, і кожну зазначену комірку піддавали сушінню протягом 1 години і потім накривали чорним сітчастим ковпачком. Зазначені випробувальні комірки витримували у ростовій камері при приблизно 20°С та 50-70% відносній вологості. За 2 доби оброблені листки покривали з двох боків тонкою пластиковою сіткою, але з незайманим черешком, який залишався прикріпленим до даної рослини і забезпечував нормальний васкулярний рух та фотосинтез. Потім дані рослини були інфіковані 20-30 тлями (редиска) або 20 цикадками картопляними (боби) і витримувались у ростовій камері ще 8 діб. Потім кожну випробувальну комірку оцінювали візуально щодо смертності даних комах, котрі контактували та живились на необроблених тканинах рослин. Результати щодо смертності тлі персикової (% GPA М) та смертності цикадки картопляної (% PLH Μ) наведені у Таблиці А. Таблиця А Відсоток смертності комах Сполука 1 3 4 5 6 26 27 % PLH M 58 96 93 96 77 73 13 % GPA M 87 81 78 94 100 67 57 ТЕСТ І Для оцінки переміщення сполук у рослинах та контролю тлі персикової (Muzus persicae) і цикадки картопляної (Empoasca fabae) після переміщення сполуки через ксилему із ґрунтової аплікації вверх через коріння у листя застосовувалась випробувальна комірка, що складалась із невеликого відкритого контейнера з 12-15 денною рослиною редиски (для тесту на тлю персикову) або з 5-6 денною рослиною бобів Longio (для тесту на цикадку картопляну). Випробувані сполуки компонували з використанням розчину, що містив 10% ацетону, 90% води та 600млн -1 неіонної поверхневоактивної речовини Х-77® Spreader Lo-Foam Formula, що містила алкіларилполіоксиетилен, вільні жирні кислоти, гліколі та ізопропанол (фірма Loveland Industries, Inc.). Препарати даних сполук наносились у 1мл розчині піпеткою у гр унт поблизу даної рослини. Усі експериментальні сполуки у цих тестах наносились при 1000млн -1, і тести повторювали три рази. Після нанесення препарату випробуваної сполуки кожну зазначену комірку піддавали сушінню протягом 1 години. Грунт у кожній випробувальній комірці покривали шаром піску, і потім верхню частину комірки накривали чорним сітчастим ковпачком. Зазначені випробувальні комірки витримували у ростовій 56 камері при приблизно 20°С та 50-70% відносній вологості. За 2 доби дані рослини були інфіковані 20-30 тлями (редиска) або 20 цикадками картопляними (боби) і витримувались у ростовій камері ще 5 діб. Потім кожну випробувальну комірку оцінювали візуально щодо смертності даних комах, котрі контактували та живились на необроблених тканинах рослин. Результати щодо смертності тлі персикової (% GPA М) та смертності цикадки картопляної (% PLH Μ) наведені у Таблиці В. Таблиця В Відсоток смертності комах Сполука 1 2 5 6 % PLH M 100 56 95 100 % GPA M 64 64 40 59
ДивитисяДодаткова інформація
Назва патенту англійськоюCyanoantranilamide compounds, composition and methods for controlling number of pests
Автори англійськоюHughes Kenneth Andrew, Lahm George Philip, Selby Thomas Paul, Stevenson Thomas Martin
Назва патенту російськоюЦианоанраниламидные соединения, композиция и способ регуляции количества вредителей
Автори російськоюХьюз Кеннет Эндрю, Лам Джордж Филип, Сэлби Томас Пол, Стивенсон Томас Мартин
МПК / Мітки
МПК: A01P 7/04, C07D 401/12, C07D 405/12, C07D 401/04
Мітки: сполуки, композиція, кількості, спосіб, ціаноантраніламідні, шкідників, регулювання
Код посилання
<a href="https://ua.patents.su/28-81791-cianoantranilamidni-spoluki-kompoziciya-ta-sposib-regulyuvannya-kilkosti-shkidnikiv.html" target="_blank" rel="follow" title="База патентів України">Ціаноантраніламідні сполуки, композиція та спосіб регулювання кількості шкідників</a>
Попередній патент: Заміщені піролопіразольні похідні як інгібітори кінази
Наступний патент: Спосіб та установка для термічної обробки твердих матеріалів, що містять оксид заліза
Випадковий патент: Спосіб діагностики доклінічної стадії діабетичної нефропатії












