Спосіб профілактики порушень мікробіоценозу, обумовлених антибактеріальною терапією асоційованих ускладнених форм урогенітального хламідіозу
Формула / Реферат
Спосіб профілактики порушень мікробіоценозу, обумовлених антибактеріальною терапією асоційованих ускладнених форм урогенітального хламідіозу, що включає проведення специфічної і неспецифічної терапії, який відрізняється тим, що як неспецифічний засіб використовують мультипробіотики групи "симбітер" за наступною схемою: I етап: Апібакт - 1 доза 1 раз на добу, під час їжі, 10 діб; II етап: Симбітер-2 - 1 доза 1 раз на добу, під час вечері, 10 діб, а також інтравагінально (інтрауретрально) 1 раз на добу, 10 діб; III етап: Симбітер концентрований - 1 доза 1 раз на добу, під час їжі, 10 діб; ІV етап: Симбівіт - 500 мг 1 раз на добу, 30 діб, Симбітер-2 - інтравагінально (інтрауретрально) 1 раз на добу, 1 раз на тиждень, 30 діб.
Текст
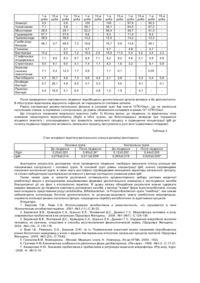
Корисна модель, що заявляється відноситься до медицини, а саме до способу профілактики порушень біоценозу, обумовленого антибактеріальною терапією асоційованих ускладнених форм урогенітального хламідіозу і може бути використаний, у венерології, гінекології, урології, гастроентерології. Урогенітальні інфекції відносяться до однієї із найважливіших медико-соціальних проблем сучасності, займаючи провідне місце серед захворювань органів сечостатевої системи [5, 8, 13, 23]. Основними методами лікування запальних процесів статевого шляху інфікування, визваних, як моно інфекцією, так і асоційованими формами, залишаються антибактеріальні і антифунгальні засоби, кортикостероїди та препарати сульфаніламідного ряду [8, 9, 11, 12, 13, 14, 16]. На превеликий жаль фармакологічні препарати з протизапальними властивостями неблагоприємно впливають на життєдіяльність, не тільки патогенної та умовно-патогенної мікрофлори, а й на стан симбіонтів, підтримуючих екологічну рівновагу з макроорганізмом [1, 3, 6, 15, 18, 20]. Необхідно підкреслити виникнення та розвиток дисбіозів під впливом потужної дії на організм екзотоксикантів фізичного (променева енергія, кліматичні і метеорологічні умови) та хімічного походження (консерванти, барвники, харчові домішки, пестициди). До екзогенних факторів порушення фізіологічної мікрофлори відносяться також промислові відходи використання забрудненої води, не правильне харчування, хронічні не інфекційні хвороби, то що [2, 9, 4, 18, 20, 21]. Не аби яке значення має шлях введення протизапальних засобів (місцеве, ентеральне або парантеральне). У багатьох випадках дисбіози мають первинну природу, де основними факторами ризику являються внутрішньоутробні, та післяпологові інфекції, патологія вагітних, штучне вигодовування немовлят. Поєднання цих негативних факторів дає можливість формувати небезпечну замкнуту систему, вагітність – новонароджені популяція дорослих індивідуумів з порушеним симбіозом - розповсюдження дисбіозів серед населення погіршення інтегрального здоров'я [1, 2, 3, 4, 17, 22]. Дисбіоз - це не хвороба одного якогось мікробіотопа, це патологічний стан усього організму, де однією із невід'ємних систем, являється саме симбіонта ендоекосистема, слугуюча в якості найбільш чутливого індикатора будь-якого неблагоприємного впливу на організм. Роль еволюційно-сформованого бар'єру між клітинами організму і навколишнім середовищем виконують шкіряні покрови та слизові оболонки, вистилаючі різноманітні трубчасті і полосні органи, де найбільш значимими являються органи урогенітального, шлунково-кишкового та дихального трактів. Проте, не дивлячись на різнобічні функціональні особливості, вони мають загальні структурні риси, забезпечуючи фізіологічний та екологічний бар'єр, котрий унеможливлює проникнення патологічних агентів у середину організму, як за рахунок конкурентних відносин між профільною і патогенною або умовно-патогенною мікрофлорою, так і за рахунок лімфоїдних утворень, основною функцією яких є формування антитіл (імуноглобулінів А), котрі попадаючи до складу секрету, створюють захисні умови: оксонізація та аглютинація мікроорганізмів, попередження адгезивних процесів мікроорганізмів до епітелію, тим самим перешкоджаючи проникненню їх в глибину слизових оболонок, нейтралізація ендотоксинів, а також вплив на рухливість, або життєдіяльність патогенних мікроорганізмів низькомолекулярними метаболітами [3, 7, 10, 18, 20]. Алгоритм профілактики і лікування дисбіотичних змін передбачає використання лікарських засобів, складовими яких є живі або інактивовані бактерії, їх компоненти тощо, що відносяться до групи мікробіологічних препаратів - пробіотиків, або вакцин, котрі сприяють відновленню мікробного ценозу і регулюють механізми впливу різних негативних чинників на фізіологічну мікрофлору. Це насамперед стосується мікробіологічних препаратів включаючих дружню для людини мікрофлору, до якої відносяться аспорогенні анаеробні сахаролітики рядів Bifidobacterium, Lastobacillus, Lactococcus і Propionibacberium. Згідно цього способу, на фоні використання фармпрепаратів специфічної протизапальної та імунокорегуючої терапії, проводиться профілактика дисбіозів біотопів урогенітального тракту засобами до складу, яких входять ліофізовані молочнокислі бактерії. Найближчим аналогом способу профілактики та лікування дисбіотичних порушень є метод вакцинації, впровадженого в лікарську практику у вигляді препараті "Солко-Триховак", який представляє собою ліофілізат інактивованих, морфологічно змінених L. acidophilus, ізольованих із вагіни жінок хворих на урогенітальний трихомоніаз. Механізм дії вакцини заключається в індукції синтезу гуморальних антитіл, протиаберантних лактобактерій, проти умовно-патогенної або патогенної флори, стимуляції локального накопичення секреторних антитіл, формування стану для оптимального розмноження паличок Додерлейна активно продукуючих Н 2О 2, молочну кислоту і лізоцим, відтворюючи РН середовища до фізіологічних значень, забезпечуючи умови до витіснення патогенної та умовно патогенної флори з біотопу вагіни, даючи можливість розвитку сапрофітній мікрофлорі [2, 7, 10, 17]. Однак, при лікуванні дисбіозів сечостатевого тракту солкотриховаком не береться до уваги той факт, що порушення в будь-якому біотопі не протікає ізольовано від інших мікроекосистем, і в першу чергу пов'язані з біотопом шлунково-кишкового тракту, як основного резервуару мікрофлори людини, та має здатність стимулювати ріст гардлерен, бактерій роду Mobiluncus, збільшуючи їхній титр в секреті трубча тих та полосних сечостатевих органів. І навпаки, навіть такі мікроорганізми, як Mobiluncus, Gardnerella, Mycoplasma hominis, котрі раніше виключно рахувались дисбіозною флорою урогенітального тракту, сьогодні достатньо часто виділяються із кишківника незалежно від віку і статі. Тому вакцинація солкотрихоголом не зможе привести до стійкого клінічного ефекту без паралельної корекції складу біоценозу кишківника та інших біотопів. Невтішним являється і факт заборони вакцинації в період вагітності, лактації та дітям до п'ятнадцяти років, незважаючи на те, що урогенітальний біоценоз це не просто совокупність мікроорганізмів, а еволюційно сформована складна мікробна популяція тісно пов'язана з іншими біотопами мікроекологічної системи, з структурно-функціональними компонентами сечостатевих органів, з їх імунною та ендокринною функціями, тощо. І саме фертильний період життя найбільш уразливий по відношенню до фізіологічної мікрофлори під впливом гормональної перебудови, імунологічних змін. Аргументованим протипоказанням застосування вакцинації являються інфекційні захворювання, особливо які супроводжуються підвищенням температури, а також захворювання з порушенням кровотворення та аутоімунні процеси [9]. Винахід, що заявляється, вирішує задачу конструювання технології терапії асоційованих форм урогенітальних хламідіозів з використанням мультипробіотичних засобів у комбінації зі специфічним лікуванням, що буде сприяти суттєвому зростанню ефективності лікування та профілактиці порушення біоценозу в різних біотопах організму. Технічний результат, що досягається корисною моделлю, полягає у підвищенні регуляторних функцій імунної системи, як системно, так і на локальному рівні (на слизових оболонках вагіни, уретри, носоглотки, бронхів кишківника), підвищенні антагоністичної активності щодо широкого спектра патогенних і умовно-патогенних бактерій, грибів, а також індукції синтезу вітамінів, органічних кислот, ферментів, екзополісахаридів, бактеріоцину та лізоциму, завдяки мультипробіотикам групи "симбітер" науково-виробничої компанії "РД. Пролісок". Поставлена задача вирішується тим, що запропонований спосіб профілактики порушень лікробіоценозуу, обумовлених антибактеріальною терапією асоційованих ускладнених форм уроенітального хламідіозу, який включає проведення специфічної і неспецифічної терапії, згідно корисної моделі в якості неспецифічного засобу використовують мультипробіотики групи "симбітер" по слідуючій схемі: І етап: Апібакт – 1 доза ´ 1 раз на добу, під час їжі – 10 діб. II етап: Симбітер-2 - 1 доза - 1 раз на добу, під час вечері - 10 діб; Симбітер-2 інтравагінально (інтрауретрально) попередньо розводячи вміст флакона охолодженою кип'яченою водою (35-37°С) у співвідношенні 1:2´1 раз на добу. Курс лікування 10 діб. III е тап: Симбітер концентрований - 1 доза´1 раз на добу. Курс лікування 10 діб. Симбітер-2 - інтравагінально (інтрауретрально) ´ 1 раз через добу. Курс лікування 30 діб. ІV етап: Симбівіт - 500мг. ´ 1 раз на добу. Курс лікування 30 діб. Симбітер-2 - інтравагінально (інтрауретрально) 1 раз на добу, 1 раз на тиждень. Курс лікування 30 діб. Відмінними ознаками запропонованого способу профілактики дисбіозів є підвищення регуляторних функцій імунної системи, як на локальному так і системному рівнях, підвищення антагоністичної активності по відношенню до широкого кола патогенних та умовно-патогенних мікроорганізмів (Salmonella, Shigella, Esherichia, Staphylococcus, Candida, Gardnerella, Mycoplasma, Mobiluncus, тощо) за рахунок "живої" форми мультипробіотиків, основу яких складають представники роду Bifidobagterium, Lactobacillus, Lactococcus Propionibacterium, тобто найбільш фізіологічних представників людської нормофлори. Комплексна система терапії має аргументовані можливості впливати на різні складові імунної системи з різними формами передачі сигналів лімфоцитами імунної системи одного біотопу, іншому і навпаки. Ці компоненти пов'язані між собою хоч і різняться своєрідністю імунологічних реакцій. Роль медіаторів в клітинних комунікаціях взаємодії обох складових імунної системи виконують цитокіни, реагуючі на збудників, що звільняються від компонентів клітинної мембрани або продуктів їх метаболізму і можуть бути активовані дією пробіотичних засобів у відповідності з патогенетичними особливостями розвитку і перебігу захворювань. Враховуючи антиоксидантні та імуномодулюючі властивості прополісу, а також унікальну комбінацію симбіозу пробіотичних бактерій (14 видів) першу сходинку на етапі комплексної терапії займає препарат апібакт до складу якого включені вищенаведені компоненти, котрі нівелюють процеси запалення, ініційовані і підтримані макрофагами і Т-лімфоцитами, інгібіруючі інтерлейкіни - 1,6 та стимулюючі продукцію інтерлейкіну - 2 з гаммаінтерферонами. В подальшому становлення нормального імунного балансу препаратами симбітер-2 та симбітер концетрований відбувається в результаті непатогенно-специфічної активізації імуноглобулінів А до відповідних бактерій. Значно підвищується вміст лізоциму в слизових оболонках, відбувається підвищення фагоцитарної активності, порманізація РН, інших метаболічних процесів. На фоні активації продукції специфічних імуноглобулінів типу А, в лімфоїдних тканинах слизових оболонок, індукуються компоненти місцевого імунітету за рахунок синтезу секреторного імуноглобуліну А, де не останню роль відіграє мультипробіотик симбітер-2 при колонізації його компонентами біотопів урогенітального тракту. Постійне вживання кисломолочного продукту симбівіт, на етапі реабілітації, виготовленого з використанням бакпрепарату симбітер, є надійною запорукою активного тренінгу імунної системи бактеріями в рамках мікробіологічної терапії, а також запорукою кількісного та якісного складу симбіонтів різних біотопів, створюючи тим самим екологічну рівновагу між мікро- і макроорганізмом та підтримуючи на відповідному рівні процеси саморегуляції, детоксикації, особливо під впливом постійного токсичного навантаження в умовах інтерактивної амбівалентної дії факторів потенційного екологічного ризику. Приклади конкретного виконання запропонованого способу. Приклад 1. Хвора Б, 21 рік. Діагноз: Хронічний двосторонній аднексіт, ендодервиціт хламідійної етіології. Бактеріальний вагіноз. Супутні хвороби - хронічний гастродуоденіт, синдром порушеного всмоктування. Отримала слідуючи лікування: 1. Вільпрофен 500мг.´2р/д 7 діб. 2. Траумель 22мл.´1р/д, п/ш №5. 3. Апібакт, 1 доза ´1 раз на добу, 10 діб. Через 10 діб Симбімер-2´1 доза, 1 раз на добу, 10 діб, плюс інтравагіально ´ 1 раз на добу. Через 10 діб Симбітер концентрований, 1 доза ´1 раз на добу, 10 діб, плюс Симбітер-2 інтравагінально ´1 раз через день. 4. Магнітотермія №5 через добу. Приклад 2. Хвора Н, 23 роки. Діагноз: Лівосторонній аднексит. Бактеріальний вагіноз. Супутні хвороби: хронічний ангіохоліт, панкреатит. Отримала слідуюче лікування: 1. Вільпрофен 500мг.´2р/д 7 діб. 2. Граумель 22мл.´1р/д. п/ш №5. 3. Апібакт, 1 доза ´1 раз на добу, 10 діб. Через 10 діб Симбітер -концентрований, 1 доза ´1 раз на добу, 10 діб. 4. Магнітотермія №5 через добу. За період лікування побічних реакцій не відмічалось. Результати клінічних, лабораторних та інструментальних досліджень, в динаміці, мали позитивні зрушення. Моніторинг, протягом одного місяця, ні клінічного ні біологічного рецидиву не зафіксував. У Київському обласному шкірновенерологічному диспансері було проліковано 42 хворі за технологією розробленого методу. Середній вік пацієнток складав 24,7 років. Контрольну гр упу складали 24 особи. Хворі, що спостерігались в основній і контрольних групах за віком, давністю захворювання, частотою загострень, клінічними проявами та супутніми захворюваннями практично не відрізнялись поміж собою. Стан мікрофлори біотопу кішківника оцінювали, в динаміці, за допомогою бактеріологічного дослідження фекальних мас з застосуванням методики Знаменського [1986]. Кількісний склад мікрофлори визначали в колонії утворюючих одиницях (КУО) на 1г. дослідженого матеріалу. Всі хворі обстежувались по стандартній схемі: зшкребок із уретри, вагіни та цервікального каналу з подальшою цитоморфологічною оцінкою, бактеріологічним дослідженням, з визначенням чутливості, а також імунологічні дослідження з використанням люмінесцентної діагностики [19]. Паралельно враховували показники РН піхвового слизу, результати амінового тесту. Для вивчення стану локального імунітету, методом імуноферментного аналізу визначали рівень показників секреторного імуноглобуліну та Ig M. Препарати групи "симбітер" застосовували у комплексному лікуванні хворим жінкам з асоційованими формами урогенітального хламідіозу, що склали основну груп у. До гр упи порівняння ввійшли хворі жінки, яким лікування проводилось в рамках традиційних схем з використанням солкотриховаку, 1 раз на добу, через кожні два тижні. На курс - три вн утрішньом'язові ін'єкції. Критеріями оцінки являлись порівняльні результати, до і після лікування, лабораторно-інструментальних досліджень. При проведенні статистичної обробки, усіх результатів дослідження, використовували середні величини з послідуючою оцінкою достовірності. Проаналізувавши результати досліджень, в динаміці, необхідно зробити висновки, що методи лікування, проведені в обох гр упах, являються достатньо дієвими. Однак, варіант терапії, в основній групі, з застосуванням технології запропонованого способу, дозволяє доказово аргументовано віднести його за соціальними, медичними та психологічними критеріями оцінки, до найпривабливіших. При вивченні стану лікробіоценозу біотопу кишківника, необхідно підкреслити, що у пацієнток основної групи відмічається достовірне підвищення вмісту лактобактерій з достатньо високою ферментативною активністю. Значне підвищення вмісту фізіологічної мікрофлори призвело до одночасної елімінації умовнопатогенних мікроорганізмів, грибів роду Candida, стафілококів, гемолітичних штамів кишкових паличок і на заключну добу моніторингу достовірно перевищувала рівень показників пацієнток контрольної групи (табл.1). Таблиця 1 Показники лікробіоценозу біотопу кишківника до і після проведеної терапії Види мікроорганізмів Лактобактерії Біфідобактерії Гриби роду кандіда Гемолітична кишкова паличка Стафілокок Рівень мікроорганізмів в біотопі кишківника КУО/г. Основна група n=42 Контрольна група n=24 1-а доба 15-а доба 1-а доба 15-а доба 7,9±0,2 9,4±0,3 7,4±0,3 7,6±0,3 7,7±0,3 8,4±0,3 7,8±0,1 8,0±0,3 3,3±0,5 1,4±0,2 3,7±0,4 3,6±0,4 4,3±0,3 2,6±0,4 4,2±0,3 3,7±0,5 4,1±0,3 2,1±0,4 3,1±0,2 3,0±0,3 Дані про лікробіоценоз біотопу урогенітального тракту представлені в табл. 2. У мікробіологічному спектрі сечостатевих органів переважала умовно-патогенна флора в поєднанні з інфекціями, які передаються статевим шляхом. Концентрація мікроорганізмів, тільки у секреті піхви, до проведення лікування, коливалась в межах 10 5107КУО/мл, що рахується в якості високого рівня патологічного обсіменіння. Таблиця 2 Показники контамінації слизових оболонок різних біотопів урогенітального тракту мікрофлорою у жінок основної і контрольної групи в динаміці Біотоп піхви Основна група Контрольна n=42 група n=24 Біотоп цервікального каналу Основна група Контрольна n=42 група n=24 Біотоп уретри Основна Контрольна група n=42 група n=24 Хламідії Уреаплазми Мікоплазми Гарднарели Трихомонади Гриби роду Кандіда Гонококи Бактероїди Стафілококи епідермальні Стрептококи Кишкова паличка гемолітична Лактобацили Біофідумбактерії Пропіонібактерії 1-а доба 0,5 7,1 28,5 57,1 38,5 15-а доба 1-а доба 0,6 5,9 29,1 57,6 38,5 15-а доба 1-а доба 100 38,1 52,3 9,6 14,2 15-а доба 1-а доба 100 38,1 56,4 8,3 12,5 15-а доба 1-а доба 97,6 64,0 49,7 11,0 14,2 15-а доба 1-а доба 95,2 67,2 51,3 8,3 12,3 15-а доба 46,1 0,7 48,5 7,3 16,6 16,7 0,8 13,8 26,1 14,2 2,1 9,5 7,2 4,7 18,5 2,5 4,7 18,9 11,0 4,8 5,4 4,2 4,7 3,4 2,3 7,1 9,5 8,3 8,7 6,9 7,1 8,2 8,2 4,6 5,1 4,9 4,9 9,5 9,1 9,5 4,1 7,4 1,1 8,3 1,6 3,2 8,1 0,9 7,1 0,3 12,3 1,7 0,6 1,1 0,1 0,05 4,7 35,7 4,6 7,3 9,6 4,4 2,1 2,8 5,2 0,4 0,8 5,7 26,1 4,9 6,0 0,7 5,3 4,0 9,1 0,1 4,2 18,5 5,1 6,4 2,8 1,2 1,9 0,7 Після проведеного комплексного лікування лікробіоценоз урогенітальних органів змінився в бік фізіологічного. В обох гр упах відмічалась відсутність інфекцій, які передаються статевим шляхом. Рівень контамінації умовно-патогенною флорою в основній групі був нижче 103КУО/мл., що не являється патогенним станом, в порівнянні з контрольною, де рівень обсіменіння коливався в межах 10 3-105КУО/мл. Що стосується показників локального імунітету (табл. 3) біотопу вагіни, до лікування, то відмічалось чітке зниження секреторного імуноглобуліну (SlgA) в обох гр упах, що безпосередньо засвідчує про порушення місцевого імунітету і опосередковано про тривалість запального процесу, а підви щення концентрації lgM до початку лікування підкреслює активність запального процесу, виступаючи в ролі його індикативної складової. Таблиця 3 Стан місцевого імунітету вагінального слизу в динаміці моніторингу SIgA IgM Основна група До лікування Після лікування 0,25±0,023 0,85±0,24* 0,078±0,014 0,011±0,006* Контрольна група До лікування Після лікування 0,12±0,032 0,44±0,035 0,065±0,018 0,025±0,005* Аналізуючи результати досліджень після проведеного лікування, необхідно визначити істотну різницю між показниками контрольної і основної групи. В основній групі рівень концентрації lgM, значно перевищував показники контрольної групи, в свою чергу достовірно підтверджував зменшення характеру запального процесу, та клініко-лабораторної критеріальної активності у вигляді наглядного зниження рівня lgM. Таким чином один із аспектів досягнення оптимального аргументованого вибору системи медичної реабілітації хворих з ускладненими асоційованими формами урогенітального хламідіозу є застосування засобів біокорегуючої дії на фоні з етіотропною терапією. В цьому зв'язку обнадійливі результати можна одержати завдяки введенню до лікування комплексу допоміжних засобів, у вигляді "живих" форм мультипробіотиків, основу яких складають представники роду Lactobacillus, Bifidobacterium, та Propionibacberium групи "симбітер", тим самим забезпечуючи колонізацію біотопів урогенітального та шлунково-кишкового тракту симбіотною мікрофлорою, сприяючи еліпінації умовно-патогенної флори, покращенню перебігу метаболічних та адаптивних процесів. Література. 1. Барсова Т.М., Леви С.Б. Использование антибиотиков и резистентность, что скрывается в тени //Клиническая антибиотикотерапия. -2001.-№3 (11).-С.30-32. 2. Бережной В.В., Крамаров С.А., Шунько Е.Е., Яновеький Д.С., Дымент Г.С. Микрофлора человека и роль современных пробиотиков в ее регуляции //Здоровье Женщины. - 2004. -№1 (№7). -С.134-139. 3. Бережной В.В., Янковский Д.С., Крамаров С.А., Шунько Е.Е., Дымент Г.С. Нарушения микробной экологии человека, их причины, следствия и способы восстановления физиологической нормы //Здоровье Женщины. 2004. -№2 (18). -С.170-178. 4. Вовк І.Б., Ревенько О.О., Борисик О.Ю. та ін. Порівняльний кількісний аналіз показників лікробіоценозу різних біологічних середовищ у жінок з вірусно-бактеріальною етіологією запальних процесів геніталій //Здоровье Женщины. -2005. -№3 (23). -С.79-82. 5. Гранилов В.М. Хламидиозы. - Москва: Медицин, книга. Н. -Новгород.; Из-во НГМА, -2000. -192с. 6. Грачева Н.М. Клинические особенности различных форм дисбактериоза. //Леч.врач. -1999. -№2-3. -С.17-21. 7. Каширская Н.Ю. Значение пробиотиков и пребиотиков в регуляции кишечной микрофлоры //Рус.мед. журн. –2000. -8. -№13-14. 8. Козлова В.И., Пухнер А.Ф. Вирусные, хламидийные и микоплазменные заболевания гениталий. -М.: Медицина. -2003. -438с. 9. Компендіум 2000/2001 лікарські препарати/ Коваленко В.М., Вікторов О.П.-К: Моріол, -2000. -1456с. 10. Коршунов В.М., Володин Н.Н., Агафонова С.А., Коршунова О.В. Влияние пробиотиков и биотерапевтических препаратов на имунную систему организма-хозяина //Педиатрия. -2002. -№5. -С.92-100. 11. Лебедюк М.М., Коляденко В.Г., Степаненко B.I. Клініка, діагностика і раціональне лікування урогенітального хламідіозу у жінок на сучасному етапі //Журн. дерматологія и венерологія ім. Н.А. Торсуєва. 2003. -№1 (5).-С.4-12. 12. Лобанов Г.Ф., Лобанов М.Г., Сазонович В.В. Принципи системогенезного підходу в лікуванні урогенітальних хламідіозів //Імунологія та алергологія. -2001. -№1. -С.80-81. 13. Лобанов Г.Ф. Особливості розвитку та перебігу урогенітального хламідіозу у жінок, що мешкають на територіях підвищеного екологічного ризику // Дерматовенерологія, косметологія, сексологія. -2005. -3-4 (8). -С.98102. 14. Лобанов Г.Ф., Чикалова І.Г., Лобанов М.Г. Особливості реабілітації хвори х урогенітальним хламідіозом в умовах інтерактивної амбівалентної дії факторів потенційного екологічного ризику. //Журн. дерматовенерології, косметології ім. М.О. Торсуєва. -2006. -№1-2 (12).-С.81-87. 15. Ликова Е.А. Дисбактериоз кишечника при антибактериальной терапии и перспективы лечения антибиотикорезистентными пробиотиками //Антибиотики и химиотер. -2001. -46. -№3. -С.21-25. 16. Мавров И.И., Мальцева Т.В. Хламидийная инфекция: Клинические проявления и характер осложнений //Дерматологія та венерологія. -2005. -№4 (30).-С.3-10. 17. Применение пробиотипов в комплексной терапии и профилактике воспалительных заболеваний в акушерстве и гинекологии: Методические рекомендации //Венцковский Б.М., Товстановская В.А., Г уцуляк В.В., Янковский Д.С., Дымент Г.С. -К., -2002., -20с. 18. Назарова Е.К., Гиммельфарб Е.И., Сазаева Л.Г. Микробиоценоз влагалища и его нарушения, этиология, патогенез, клиника, лабораторная диагностика //Антибиотики и химиотер. -2002. -47. -№ 4. -С.34-42. 19. Уніфікація методів дослідження в діагностиці захворювань, що передаються статевим шляхом: Методичні рекомендації //Мавров I.I., Бєлозіров О.П., Тацька Л.С., Кутова В.В. і спів.авт. -Харків. -2000. -217с. 20. Янковский Д.С. Состав и функции микробиоценозов различных биотопов человека //Здоровье женщины. 2003. - №4 (16). -С.145-158. 21. Янковский Д.С. Микробная екология человека. Современные возможности ее поддержания и восстановления. - К: Експорт ЛТД. -2005. -362с. 22. Kagermeier-Callaway A.S. International Committee on sistematic bacteriology. Subcommitee in the taxonomy of Bifidobacterium, Lactobacillus and related organisms Minutes of the meetings, 4 and 6 juli 1994, Prague, Czeck. Republie //Int. J. Syst. Evol. Vicrobiol -2000. -VI 50 (3). - P. 1991-1992. 23. Whittington W.L.Y.. Bent Ch., Kissinger P.et al. Determinants of persistent and recurrent Chlamyolix trachomatis infection in yond women. Results of multicenter control sbudy//STD.-2001. -P. 117-123.
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for preventing impaired microbiocenosis because of antibacterial therapy of associated complications of urogenital chlamidiosis
Автори англійськоюLobanov Hennadii Feodosiiovych
Назва патенту російськоюСпособ профилактики нарушений микробиоценоза, обусловленных противобактериальной терапией ассоциированных осложненных форм урогенитального хламидиоза
Автори російськоюЛобанов Геннадий Федосеевич
МПК / Мітки
МПК: A61P 13/00, A61K 35/74
Мітки: профілактики, форм, мікробіоценозу, порушень, терапією, ускладнених, спосіб, хламідіозу, асоційованих, обумовлених, урогенітального, антибактеріальною
Код посилання
<a href="https://ua.patents.su/5-22838-sposib-profilaktiki-porushen-mikrobiocenozu-obumovlenikh-antibakterialnoyu-terapiehyu-asocijjovanikh-uskladnenikh-form-urogenitalnogo-khlamidiozu.html" target="_blank" rel="follow" title="База патентів України">Спосіб профілактики порушень мікробіоценозу, обумовлених антибактеріальною терапією асоційованих ускладнених форм урогенітального хламідіозу</a>
Попередній патент: Спосіб лікування генералізованого пародонтиту
Наступний патент: Обмежувач швидкості, що приводить клини-уловлювачі в дію без троса
Випадковий патент: Упорний підшипник ковзання для валів заглибних відцентрових електронасосів