Спосіб контролю та коригування полірувальної здатності електроліту для електрохімічного полірування ніобію
Номер патенту: 23120
Опубліковано: 30.06.1998
Автори: Устименко Валерій Миколайович, Хрульова Ольга Димитровна, Федоренко Олександр Михайлович
Формула / Реферат
1. Способ контроля и корректировки полирующей способности электролита для электрохимического полирования ниобия, включающих введение добавки реагентов в электролят на основе фтористоводородной и серной кислот, отличающийся тем, что введение добавки осуществляют до совпадения значений пиковых токов при снятии на вольтамперных характеристиках рабочего и эталонного растворов электролита причем наличие участков токовых колебаний на вольтамперной характеристике является обязательным.
2. Способ по п. 1, отличающийся тем, что при корректировке в качестве добавки в злектролит вводят фтористоводородную кислоту, либо ее смесь с концентрированной серной кислотой или с олеумом.
3. Способ по п. 1, отличающийся тем, что при корректировке в качестве добавки в электролит вводят фтористоводородную кислоту, либо ее смесь с органическими веществами карбамидного ряда, например, ацетилкарбамид, - метилацетилкарбамид, карбамид.
Текст
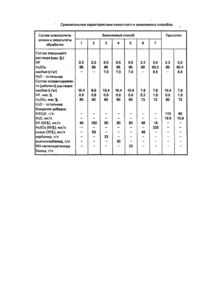
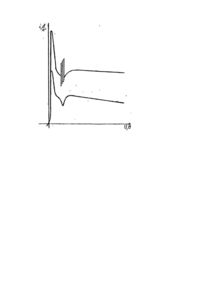
Способ относится к области электрохимической обработки металлов, в частности ниобия, и может быть использован для контроля и корректировки электролитов на основе плавиковой и серной кислот. В качестве прототипа выбран "Способ восстановления состава раствора для электролитического полирования изделий из ниобия" [1], согласно которому в раствор, содержащий фтористоводородную и серную кислоты и воду, по мере снижения в нем концентрации фтористоводородной кислоты вводят фторсерную кислоту и воду в эквимолярных количествах до восстановления концентрации фтористоводородной кислоты, а содержание воды в растворе сохраняется, в основном, постоянным. Основными недостатками этого способа являются технические затруднения при синтезе (получении) и хранении запасов фторсерной кислоты, а также необходимость принятия специальных мер защиты при операции смешивания ее с водой, в ходе которой выделяется большое количество тепла, сопровождаемое вскипанием и разбрызгиванием раствора (возможен взрыв смеси). Другим недостатком прототипа является большая погрешность и длительность процесса анализа раствора для определения концентрации в нем фтристоводородной кислоты, поскольку большой вклад в эту ошибку вносят фторсодержащие соединения ниобия, которые накапливаются в растворе при его эксплуатации. Кроме того, по известному прототипу восстановить состав раствора полностью принципиально невозможно из-за непрерывного накопления в нем ниобия при отсутствии рекомендаций по извлечению из раствора исключительно ниобия. В результате, даже при восстановлении в растворе начальной концентрации фтористоводородной кислоты, полирующие свойства раствора могут значительно отличаться от полирующи х свойств первоначального рабочего раствора по скорости эффективности и по режиму ЭХП. Таким образом, рассмотренные способы не позволяют эффективно контролировать и корректировать именно полирующие свойства электролита так, чтобы практически полностью воспроизводился технологический режим ЭХП ниобия. В основу изобретения поставлена задача упрощения способа корректировки электролита, в котором за счет сравнительной оценки вольтамперных характеристик исходного и рабочего электролитов осущест-вляюг контроль за восстановлением полирующих свойств раствора и одновременно воспроизводят технологический режим процесса, т.е. получают более простой метод корректировки свойств рабочего электролита. Поставленная задача решается таким образом, что в способе контроля и корректировки электролита на основе фтористоводородной и серной кислот для ЭХП ниобия, включающем введение в рабочий электролит добавок, дополнительно осуществляют съем вольтамперных характеристик эталонного и рабочего растворов, проводят их сравнительную оценку, и корректировку осуществляют добавлением реагентов в рабочий раствор электролита так, чтобы совпали значения пиковых токов на вольтамперных характеристиках обоих растворов, при этом наличие участков токовых колебаний на ВАХ является обязательным. В качестве добавки в электролит вводят плавиковую кислоту либо ее смесь с концентрированной серной кислотой или олеумом. Кроме того, в качестве добавок вместо названных кислот используют органические. вещества карбамидного ряда, например, ацетилкарбамид, N,N-метилацетилкарбамид, карбамид. Реализация способа иллюстрируется с помощью чертежа и таблицы с описанием примеров выполнения. ВАХ эталонного и рабочего растворов получали с помощью потенциостата ПИ-50-1.1 и самопишущего потенциометра ПДП4-002 в комплексе с электрохимической ячейкой. Эффективность полирования оценивали по величине скорости съема ниобия с поверхности (Vn , мкм×мин-1) и величиной логарифмического показателя эффективности W (час-1); рассчитываемого по формуле R W = 01 / t, R02 где R01, R02 - коэффициенты шероховатости поверхности до и после ее обработки (ЭХП). Чем больше значения этих величин, тем эффективнее осуществляется ЭХП. Коэффициент шероховатости измеряли с помощью профиломера 287. ЭХП поверхности осуществлялось по способу Диперса. Как видно из таблицы, после проведения корректировки электролитов по заявляемому способу эффективность ЭХП по сравнению с ЭХП в эталонных растворах воспроизводилась полностью и иногда даже усиливалась, в то время как корректировка по известному способу не восстанавливала полностью полирующих свойств электролитов. Примеры конкретного выполнения. Пример 1. В качестве эталонного выбран раствор, приготовленный смешиванием концентрированных HF и H2SO4 кислот в объемном отношении 1:9. ВАХ этого раствора имела вид кривой 1 согласно рисунку. Пиковый ток характеризовался величиной его плотности 550 А/м 2. Скорость съема ниобия с поверхности при ЭХП составляла 0,24 мкм/мин. Логарифмический показатель эффективности ЭХП имел величину 0,14 час-1. Корректируемый электролит, содержащий в 1 кг помимо фтористоводородной и серной кислот растворенный в нем ниобий массой 10,42, после обработки соответствующей площади изделий имел ВАХ, подобную кривой 2 на рисунке. Пиковый ток характеризовался величиной его плотности 157 А/м 2. Электролит не обладал полирующими свойствами, имел нулевой показатель эффективности ЭХП. К 500 мл корректируемого электролита добавили 20 мл 50%-ного раствора HF. Через 30 мин. после перемешивания ВАХ откорректированного раствора имела вид кривой 1 согласно рисунка. Плотность пикового тока составила 545 А/м 2. Ниобиевая пластина была подвергнута ЭХП по способу Дисперса в течение 60 мин при 6 В. Скорость съема ниобия составила 0,24 мкм/мин, показатель эффективности ЭХП имел величину 0,14 час-1. Пример 2. Эталонный раствор был такой же, как в примере 1. Корректируемый электролит содержал в 1 кг 8,6 г ниобия и имел ВАХ, подобную кривой 2 согласно рисунка. Плотность пикового тока была 230 А/м 2. Эффективность ЭХП в таком электролите была нулевой. К 1 л корректируемого раствора добавили 100 мл 40%-ной HF. После перемешивания и выдержки в течение суток электролит имел ВАХ, подобную кривой I согласно рисунку, однако, плотность пикового тока была небольшой - 300 А/м 2. Операция корректировки была продолжена. К откорректированному электролиту добавили дополнительно 50 мл 40%-ной HF и 50 мл 30 %-ного олеума. ВАХ повторно откорректированного электролита также имела вид кривой 1, согласно рисунку, но плотность пикового тока возросла до величины 450 А/м 2, т.е. достигнуто было воспроизведение ВАХ по эталонному раствору на 82%. В таком откорректированном электролите пластина ниобия была подвергнута ЭХП по способу Диперса. Скорость съема ниобия составила 0,24 мкм/мин, показатель эффективности ЭХП - 0,16 час-1. Пример 3. В качестве эталонного был взят повторно откорректированный электролит из примера 2, характеризуемый плотностью пикового тока 450 А/м 2. Корректируемый рабочий электролит содержал в 1 кг 10,4 г ниобия и имел ВАХ, подобную кривой 2 согласно рисунку. Плотность пикового тока составляла 160 А/м 2. Электролит не обладал полирующими свойствами, К 500 мл корректруемого электролита добавили 40 мл 50%-ного раствора HF. После перемешивания и выдержки его в течение суток электролит имел ВАХ, подобную кривой 1 на рисунке. Плотность пикового тока оказалась 510 А/м 2, т.е. выше требуемой по технологическому регламенту. К откорректированному электролиту добавили 11 г карбамида. ВАХ повторно корректированного электролита сохранила вид кривой 1, как на рисунке, и плотность пикового тока достигла требуемой величины 450 А/м 2. Ниобиевая пластина была подвергнута ЭХП по способу Диперса. Скорость съема ниобия составила 0,24 мкм/мин, показатель эффективности ЭХП - 0,16 час-1. Пример 4. В качестве эталонного был взят повторно откорректированный электролит из примера 2, характеризуемый плотностью пикового тока 450 А/м 2. Корректируемый рабочий электролит содержал в 1 кг 10,4 г ниобия и имел ВАХ, подобную кривой 2 согласно рисунку. Плотность пикового тока составляла 180 А/м 2. Электролит не обладал полирующими свойствами. К 500 мл корректирумого электролита добавили 40 мл 50%-ного раствора плавиковой кислоты. После перемешивания и выдержки его в течение суток электролит имел ВАХ, подобную кривой 1 на рисунке. Плотность пикового тока оказалась 550 А/м 2, т.е. выше требуемого по технологическому регламенту. К откорректированному электролиту добавили 11 г ацетилкарбамида. ВАХ повторно корректированного электролита сохранила вид кривой 1, как на рисунке, и плотность пикового тока достигла требуемой величины 450 А/м 2. В таком электролите скорость съема ниобия при ЭХП по способу Диперса составила 0,24 мкм-мин, а коэффициент эффективности ЭХП - 0,18 час-1 . Пример 5. В качестве эталонного был взят повторно откорректированный электролит из примера 2, характеризуемый плотностью пикового тока 450 А/м 2. Корректируемый рабочий электролит содержал в 1 кг 10,4 г ниобия и имел ВАХ, подобную кривой 2 согласно рисунку. Плотность пикового тока составляла 200 А/м 2. Электролит не обладал полирующими свойствами. К 500 мл корректируемого электролита добавили 40 мл 50%-ного раствора плавиковой кислоты. После перемешивания и выдержки его в течение суток электролит имел ВАХ, подобную кривой 1 на рисунке. Плотность пикового тока оказалась 600 А/м 2, т.е. выше требуемого по технологическому регламенту. К откорректированному электролиту добавили 11 г NN-метилацетилкарбамида. ВАХ повторно корректированного электролита сохранила вид кривой 1, как на рисунке, и плотность пикового тока достигла требуемой величины 450 А/м 2. В таком электролите скорость съема ниобия при ЭХП по способу Диперса составила 0,24 мкм/мин, а коэффициент эффективности ЭХП - 0,17 час-1 . Пример 6. В качестве эталонного был выбран эталонный электролит из примера 1. Корректируемый электролит содержал в 1 кг 7,8 г ниобия, имел ВАХ, подобную кривой 1 согласно рисунку, но обладал слабо выраженными полирующими свойствами с низким показателем эффективности ЭХП (0,01 час"1); плотность пикового тока имела значение 300 А/м. К 500 мл корректируемого раствора добавили 24 мл 40%-ной HF и 24 мл 30%-ного олеума. ВАХ откорректированного электролита также имела вид кривой 1 согласно рисунку, но плотность пикового тока возросла до 450 А/м 2, т.е. достигн уто было воспроизведение ВАХ на 82% по эталонному раствору. В таком электролите скорость съема ниобия при ЭХП по способу Диперса составила 0,24 мкм/мин, а коэффициент эффективности ЭХП - 0,16 час-1 , Пример 7. В качестве эталонного был взят электролит, содержащий в 1 кг 6,6 ниобия, 30 г HF и 800 г H2SO4. ВАХ для этого раствора имела вид кривой 1 согласно рисунку. Плотность пикового тока имела величину 400 А/м 2. Скорость съема ниобия с поверхности при ЭХП составила 0,20 мкм/мин, а показатель эффективности ЭХП - 0,12 час-1. Корректируемый электролит содержал в 1 кг 7,8 г ниобия и имел ВАХ, подобную кривой 1 на рисунке, с величиной пикового тока 300 А/м 2. Э ффективность ЭХП в нем составляла 0,005 час-1. К 500 мл корректируемого электролита добавили 180 мл смеси 50%-ной НF и 96%-ной H2SO4 кислот, взятых в объемном соотношении 1:9. Через 30 мин после перемешивания ВАХ откорректированного электролита также имела вид кривой 1 согласно рисунку, но плотность пикового тока возросла до требуемой величины 400 А/м 2. Ниобиевая пластина была подвергнута ЭХП по способу Диперса. Скорость съема ниобия составила 0,21 мкм/мин, а показатель эффективности ЭХП возрос до значения 0,14 час-1. Предложенный способ позволяет контролировать и корректировать именно полирующее свойства электролита, прост, удобен и безопасен.
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for control and correction of electrolyte polishing ability for electrochemical polishing niobium
Автори англійськоюFedorenko Oleksandr Mykhailovych, Khruliova Olha Dmytrivna, Ustimenko Valerii Mykolaiovych
Назва патенту російськоюСпособ контроля и корректирование полировочной способности электролита для электрохимического полирования ниобия
Автори російськоюФедоренко Александр Махайлович, Хрулева Ольга Дмитриевна, Устименко Валерий Николаевич
МПК / Мітки
МПК: C25F 7/00
Мітки: електроліту, електрохімічного, коригування, ніобію, полірувальної, здатності, спосіб, полірування, контролю
Код посилання
<a href="https://ua.patents.su/5-23120-sposib-kontrolyu-ta-koriguvannya-poliruvalno-zdatnosti-elektrolitu-dlya-elektrokhimichnogo-poliruvannya-niobiyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб контролю та коригування полірувальної здатності електроліту для електрохімічного полірування ніобію</a>
Попередній патент: Білково-вітамінний харчовий продукт
Наступний патент: Пристрій для багаторазового запису та зчитування інформації
Випадковий патент: Спосіб безперервного розливання для одержання металевої заготовки