Похідні цитизину, що містять фосфор
Номер патенту: 59365
Опубліковано: 15.09.2003
Автори: Газалієв Арстан Маулєновіч, Гуляєв Алєксандр Євгєньєвіч, Вітік Андрєй Зіновьєвіч
Формула / Реферат
1. Фосфорсодержащие производные цитизина общей формулы
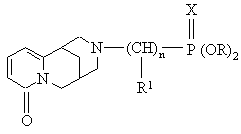 ,
,
где n = 0, 1 при n = 0, Х = S, О
R = СН3, С2Н5, С3Н7, i-С3Н7, С4Н9
при n = 1, X = О
R = СН3
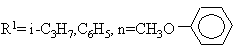
в качестве гепатопротектора
2. Фосфорсодержащие производные цитизина по п. 1 общей формулы
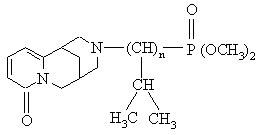 ,
,
где n = 0, 1 в качестве гепатопротектора
3. Фосфорсодержащие производные цитизина по любому из пп. 1, 2, где n = 1 для использования в качестве медикамента.
4. Фосфорсодержащие производные цитизина по любому из пп. 1, 2, отличающиеся тем, что они предназначены для использования в производстве медикаментов для гепатопротективного лечения.
Текст
1 Фосфорсодержащие производные цитизина общей формулы X R = СНз, С2Н5, C3H7, 1-C3H7, C4HC при п = 1, Х = О N—(СН)—Р(ОСН3)2 н,с сн, где п = 0, 1 в качестве гепатопротектора 3 Фосфорсодержащие производные цитизина по любому из пп 1, 2, где п = 1 для использования в качестве медикамента 4 Фосфорсодержащие производные цитизина по любому из пп 1, 2, отличающиеся тем, что они предназначены для использования в производстве медикаментов для гепатопротективного лечения ю (О ГО о> ю N—(СН)—P(OR). Изобретение относится к новым химическим соединениям, в частности к фосфорсодержащим производным цитизина, проявляющим гепатопротекторную и антиферментную активность Известно, что алкалоид цитизин (1) впервые выделенный из семян ракитника и термопсиса в настоящее время широко используется в медицинской практике в виде 0,15% водного раствора О (цититон) в качестве аналептического средства (Машковский М Д «Лекарственные средства», М , 1977г, ч 1, стр 123) 59365 4 Синтез О,О-диалкил-1\1-цитизинилфосфатов (п - О, X - О соединения 4 а д ) осуществляли взаимодействием д и ал кил фосфитов с цитизином в условиях реакции Тодда-Атертона по следующей схеме •K-P(QR}2 ,& О О О О Ъ где R - C2.s Характерным свойством цитизина является способность его возбуждать дыхание, связанная с рефлекторной стимуляцией дыхательного центра усиленными импульсами, поступающими от каротидных клубочков Одновременное возбуждение симпатических узлов и надпочечников приводит к повышению артериального давления В связи с этим цитизин рекомендуют использовать в случаях остановки дыхания и сердечной деятельности при интоксикациях Цитизин широко распространен в природе Он найден во многих растениях и извлечение его из растительного сырья ионообменным методом является главным промышленным способом получения цитизина В работах (Докл АН Узб ССР, 1978г, № 9, стр 39 - 42, Докл АН Узб ССР, 1977, № 7, стр 40 43) описан синтез фосфорсодержащих N-[p(диалкоксифосфинил) меркаптоэтил] цитизинов (2) и их иодметилатов (3) Авторы показали, что все синтезированные соединения обладают необратимой ингибирующей активностью в случае ацетилхолинэстеразы и проявляют эффект избирательного торможения каталитической активности бутирилхолинэстеразы Сведения о других фосфорсодержащих производных цитизина нами в литературе не обнаружены В связи с тем, что исходный алкалоид цитизин проявляет значительную биологическую активность, можно предположить, что и другие его фосфорсодержащие производные будут интересны с этой точки зрения Целью заявляемого изобретения является получение новых фосфорсодержащих производных цитизина, в частности, обладающих повышенной биологической активностью Поставленная цель достигается тем, что получены фосфорсодержащие производные цитизина общей формулы (б) где п -0, 1 при n - O X - S , О R -СНз(а), С2Н5(б), С3Н7(в), 1-С3Н7(г), С4Н9(д) при П - 1 Х - 0 Rl-l-C3H7(a); С6Н5(б); п (в) Синтез О.О-диалкил-Nцитизинилтиофосфатов (п - 0, X - S соединения 5 а На первой стадии д ) осуществляли в две стадии при взаимодействии цитизина с диалкилхлорфосфитом (синтез описан в работе Нифантьев Э В «Химия фосфорорганических соединений, М Наука, 1983г — стр 85) в среде бензола, в токе сухого аргона и в присутствии триэтиламина образуется промежуточный О.О-диалкил-Nцитизинилфосфит, который затем реагирует с эквимолярным количеством элементной серы с образованием О.О-диалкил-Nцитизинилтиофосфата (RG)aPCf О 5 Диметил - (N-цитизинил) алкил (арил) фосфонаты (п - 1 , X - О, R-СНз соединения 6 а в) получены взаимодействием цитизина с альдегидами и диметилфосфитом в условиях реакции КабачникаФилдса б D Следующие примеры поясняют изобретение подробнее, не ограничивая его этим Примеры 1 Синтез О,О-диметил-І\І-цитизинил фосфата (4а) В колбу помещают смесь 2,86г (0,026 моль) диметилфосфита и 15,5мл (0,16 моль) четыреххлористого углерода в 100мл бензола и при перемешивании прикалывают к ней смесь 5г (0,026 моль) цитизина и 2,63г (0,026 моль) триэтиламина в 230мл сухого бензола с такой скоростью, чтобы температура раствора не превышала 20°С После окончания прикалывания реакционную смесь перемешивают при комнатной температуре в течение 6 часов Выпавшие кристаллы солянокислого триэтиламина отфильтровывают, растворитель отгоняют на вакуумном испарителе Получают 5,64г (выход 72,5% от теоретического) кристаллического вещества (перекристаллизация из бензола) с температурой плавления Т пл 158 159°С ИК спектр, v, с м 1 1270 (Р-О), 1050 (Р-О-С), 830(P-N-C), 1658 (N-CO) 59365 этого ряда (таблица) 2 Синтез О.О-диметил-N5 0Гц), 7,23дд(1Н, СНе, 3JHH 3,2ГЦ), 6,1 2Д (1Н, цитизинилтиофосфата (5а) СН„), 3,341 (6Н, СНзО, СН,Р 13,2 Гц) В колбу помещают 5г (0,026моль) цитизина и 2,63г (0,026моль) триэтиламина в 200мл абсолютЯМП р 5 р -9,1м д ного бензола При энергичном перемешивании в Найдено, % С 52,05, Н 6,24, N 9,30, Р 10,36, токе сухого аргона и при комнатной температуре C13P19N2O4P прибавляют 3,33г (0,026моль) диметилхлорфосВычислено, % С 52,36, Н 6,37, N 9,40, Р 10,40 фита Перемешивают 5 часов Выпавший осадок По данным рентгеноструктурного анализа когидрохлорида триэтиламина отфильтровывают, ординация атома фосфора в молекуле 0,0промывая порциями абсолютного бензола Фильтдиметил-Ы-цитизинилфосфата - искаженная тетрат и расчетное количество серы 0,83г раэдрическая, обычная для фосфатных группиро(0,026моль) помещают в колбу и продолжают певок Дигидропиридиновый цикл - плоский с точноремешивать при комнатной температуре еще 2 часа Затем смесь отгоняют в роторном испаритестью ± 0,01 А, карбонильный атом кислорода ле и остаток перекристаллизовывают из бензола отклоняется от этой плоскости незначительно (на Получают 8,01г (выход 97%) кристаллического 0.07А) Тетрагидропиридиновый цикл принимает вещества с Тпл 164-165°С 3 конформацию кресла (ДС S2,7°) с выходом мостиИК спектр, v, с м 1 1030 (Р-О-С), 1670 (N-CO), кового атома С из средней плоскости остальных 820 (P-S)/ на 0.75А Пиперидиновый цикл имеет почти идеСпектр ПМР, 5, м д 6,23д (1Н, СН а , 3 J H H альную конформацию кресла (ДС3 s0,5°) Метиль6,0Гц), 7,16дд (1Н, СНр, \ J H H 5,8Гц), 5,8д (1Н, ные группы СНз имеют гош-ориентацию относиСНТ), тельно связей Р-0 и Р-0 соответственно Аналогично получены другие соединения 4б в Спектр ПМР, 5, м д 6,23д (1Н, СН а , J H H Таблица Физико-химические константы и данные элементного анализа заявляемых соединений С Н N Р Брутто Формула С H N P % 52,08 6,27 9,48 10,26 Ci 3 Hi 9 N 2 O 4 P 52,36 6,37 9,40 10,40 72,5 1,5258 55,39 1,5027 57,72 7,13 7,69 8,65 7,82 9,66 8,83 C 1 5 H 2 3N 2 O 4 P C17H27N2O4P 55,21 57,62 7,05 7,62 8,59 7,91 9,51 8,75 68,4 69,7 57,81 7,74 7,87 8,86 C17H27N2O4P 57,62 7,62 7,91 8,75 70,5 1,4836 59,77 8,19 7,28 8,20 C,gH3,N 2 O 4 P 59,68 8,11 7,33 8,11 63,8 49,91 6,18 8,87 9,69 C 1 3 H,gN 2 O3PS 49,68 6,05 8,91 9,87 97,0 1,5486 1,5463 1,5446 52,72 55,24 55,19 57,38 6,79 7,41 7,38 7,86 8,14 7,50 7,49 7,01 9,17 8,43 8 47 7,91 Сі5П 2 зН 2 ОзРЗ C, 7 H 2 7 N 2 O3PS C, 7 H 2 7 N 2 O3PS C,gH3,N 2 O 3 PS 52,63 55,13 55,13 57,28 6,72 7,30 7,30 7,79 8,19 7,57 7,57 7,04 9,06 8,38 8,38 7,79 92,5 87,3 75,1 82,0 57,70 7,72 8,03 8,67 C17H27N2O4P 57,56 7,58 7,90 8,52 78,1 61,87 6,47 7,19 7,99 C20H25N2O4P 61,85 6,44 7,21 7,98 85,2 60,18 6,74 6,56 7 37 C21H2BN2O5P 60,14 6,68 6,68 7,39 87,0 Соединение Тпл °С N20 158159 115116 164165 99- 100 137139 190192 186188 4а 46 4в 4г 4д 5а 56 5в 5г 5д 6а 66 6в Найдено, % 3,40д (6Н, СНзО, J C h 3 p 12,0Гц) 31 ЯМР Р 5 Р -10,22м д Найдено, % С 49,91, Н6.13, N8,87, Р 9,69, C13H19N2O3SP Вычислено, % С 49,68, Н 6,05, N 8,91, Р 9,87 Аналогично получены и соединения 5б-д этого ряда Результаты приведены в таблице 3 Синтез диметил-2-(І\І-цитизинил)-2изобутилфосфоната (6а) Смесь 3,8г (0,02моль) цитизина, 1,24г (0,02моль) изомасляного альдегида, 2,2г (0,02моль) диметилфосфита и каталитического количества 18-краун-6 в 100мл бензола кипятят 3 часа с одновременной отгонкой образующейся в ходе реакции воды После отгонки растворителя Вычислено, % Выход по окончании реакции остаток промывают гексаном и перекристаллизовывают из смеси бензолэфир Получают 5,52г (выход 78,1%) кристаллического вещества с Т пл 138°С 1 ИК спектр, v, см 1220 (Р-О), 1070 (Р-О-С) 3 Спектр ПМР, 5, м д 6,72д (1Н, СН а , J H H 3 8,6Гц), 7,10дд (1Н, СНр, J H H 6,4ГЦ), 6 , 5 1 Д (1Н, СНТ), 3,31д (6Н, СНзО, J C H p 12,6Гц), 0,50 д (ЗН, СНз-С), Найдено, % С 57,70, Н 7,72, N 8,03, Р 8,67, C17H27N2O4P Вычислено, % С 57,56, Н 7,58, N 7,90, Р 8,52 Аналогично получены и соединения 66-в этого ряда (табл) Биологическая активность заявляемых соеди 8 59365 нении Проведенные фармакологические исследования показали, что синтезированные соединения проявляют гепатопротекторную и антиферментную активности I Изучение гепатопротекторной активности Острая токсичность соединения Средне-летальную дозу LDso определяли на мышах белых рандомбредных (320 голов по 18 20 грамм каждая) Препарат вводили однократно внутривенно в физиологическом растворе или перорально в крахмальной 1% взвеси Период наблюдения - 14 дней Ежедневно проверяли общее состояние животных, в течение периода наблюдения 3 раза животных взвешивали, проводили вскрытие павших животных и макроскопическое описание Определение LDso проводили методом проб и анализа В результате проведенных экспериментов получили, что LD50 - 4300мг/кг (3200 - 5800) при пероральном введении соединения и LD50 1800мг/кг (1250 - 2550) при внутривенном введении Приведена средняя арифметическая величина и доверительный полуинтервал при Р - 95% Гепатопротекторная активность при остром токсическом гепатите у крыс По мнению фармакологов, наиболее эффективным гепатопротекторным препаратом в настоящее время является препарат «Эссенциале» (ФРГ), который и был использован в следующих экспериментах в качестве препарата сравнения Этот препарат представляет собой сложный комплекс веществ и содержит в своем составе сумму флаваноидов, фосфолипидов, никотинамид и различные витамины Изучение гепатопротекторной активности заявляемого препарата при остром токсическом гепатите проводили на 4 группах самцов белых рандомбредных крыс массой 120 - 150 грамм по 10 особей в каждой Первая группа - животным вводили внутривенно 0,1мл изотонического раствора хлорида натрия и через час внутрибрюшинно 0,4мл вазелинового масла Вторая группа - внутривенно 0,1мл изотонического раствора хлористого натрия и через час внутрибрюшинно 0,4мл 40% раствора гепатотропного яда - четыреххлористого углерода в вазелиновом масле Третья группа - внутривенно 0,1мл раствора «Эссенциале» (50мг/кг) и через час внутрибрюшинно 0,4мл 40% раствора ССЦ в вазелиновом масле Четвертая группа - внутривенно 0,1мл водного раствора заявляемого вещества (50мл/кг) и затем, через час внутрибрюшинно 0,4мл 40% раствор ССЦ в вазелиновом масле Все инъекции повторяли один раз в сутки на протяжении четырех дней, после чего под эфирным наркозом животные были декапитированы Гепатопротекторную активность заявляемого препарата и препарата сравнения при отравлении крыс четыреххлористым углеродом оценивали по изменению биохимических и гистологических показателей, характеризующих степень повреждения (разрушения) клеток при отравлении Исследовали активность фермента аланинаминотрансферазы (АЛаТ) и уровень общего билирубина в крови, хемолюминисценцию эритроцитов и морфометрически объемную долю некрозов, внутридольковой инфильтрации, регенерирующих и дистрофированных клеток в срезах ткани печени При изучении хемолюминисценции эритроциты, выделенные из крови суспензировали в изотоническом растворе хлорида натрия (по 1мл 10% взвеси эритроцитов в пробе) свечение стимулировали 0,1мл 5% Н2О2 и определяли среднеарифметические показатели интегральной площади под кривой хемолюминисценции Группа АЛаТ млмольхчас/литр Билирубин микромоль/литр 1 2 3 4 215 ±8,1 1828 ±34,6 1291 ±10,5 445,4 ±11,7 8,06 ±0,4 31,12 ± 1,09 20,84 ± 0,25 12,90 ±0,32 Группа 1 2 3 4 Дистрофия, % 2,6 20,5 12,8 8,2 Некроз, % 0,2 4,3 0,9 0,5 Приведенные данные показывают, что заявляемое вещество обладает гепатопротекторной активностью при отравлении крыс четыреххлористым углеродом, причем действует более активно, чем препарат «Эссенциале» использованный в качестве препарата сравнения Действие на выживаемость мышей при отравлении их гепатотропным ядом 1 Для изучения действия препарата на выживаемость мышей при отравлении гепатотропным ядом использовались мыши белые рондомбред Инфильтрация, % 0,35 0,6 0,4 0,3 Площадь под кривой хемолюминисценции 4,34 9,395 7,35 5,386 Регенерация, % 1,4 0,652 1,03 1,48 ные, самцы массой 1 8 - 2 0 грамм, три группы по 10 мышей в каждой Первой группе животных внутрибрюшинно вводили 0,1мл изотонического раствора хлорида натрия Второй группе - внутривенно 0,1мл раствора «Эссенциале» в дозе 50мг/кг Третьей группе - внутрибрюшинно 0,1мл раствора заявляемого вещества в водном растворе (100мг/кг) Через час после первого введения всем животным внутрибрюшинно ввели 0,1мл 50% раствора четыреххлористого углерода в вазелиновом 59365 10 лошади с удельной активностью 9,6Ед/мг Активмасле ность АХЭ и БуХЭ определяли калориметричеИнъекции проводили однократно Срок наским методом Элл мана при 25°С в 0,2М Naблюдения 5 суток Выживаемость через 5 суток фосфатном буфере, рН 7,5 В качестве субстрата составила использовали илдид ацетилтиохолина фирмы «Chemapol» (ЧСФР) Эффективность обратимых Число выживших жиГруппа Выживание, % ингибиторов определяли по методу А П Бресткивотных на и характеризовали величиной обобщенной ин1 0 0 гибиторной константы (К,), которая при смешанном 2 2 20 типе торможения связана с конкурентной (К,) и о 8 80 1 бесконкурентной (К ,) составляющими соотноше1 нием 1/К, - 1/К, + 1/К , Полученные результаты показывают, что Активность цитохрома Р450 определяли двупредлагаемое соединение в большей степени, мя методами по скорости гидроксилирования 3,4чем «Эссенциале» защищает животных от гибели бенз/а/пирена, путем флуориметрического опрепри отравлении их гипототропным ядом деления образующегося 4-гидроксибенз/а/пирена Таким образом, мы установили, что соединеи по скорости диэтилирования 7-этоксикумарина ние обладает умеренной токсичностью и его гепапутем флуориметрического определения, обратопротекторное действие в эксперименте на жизующегося 7-гидроксикумарина Ингибирующее вотных значительно превосходит действие влияние исследуемых веществ на ЦТ Р450 оценипрепарата «Эссенциале» вали по величинам pJso, представляющим собой 2 Хорошие результаты по выживаемости мыобратный логарифм концентрации агента, вызышей при отравлении их гепатопротекторным ядом вающей активности на 50% показало и еще одно из заявляемых фосфорсоУстановлено, что цитизинилфосфаты и цитидержащих производных цитизина зинилтиофосфаты являются ингибиторами АХЭ Процент выживаемости для этого соединения средней силы и весьма эффективными ингибитов эксперименте, аналогичном вышеописанному, рами БуХЭ Наибольшую избирательность по отсоставил 80% ношению к БуХЭ наблюдали для производных II Изучение антиферментной активности тиофосфата (рК 1 - 6,7 и рК 1 - 6,1 соответственПри исследовании антиферментной активноно) сти синтезированных соединений изучали их Выявлены сильные ингибиторы цитохрома взаимодействие с ацетилхолинэстеразой (АХЭ) и Р450, имеющие перспективу для практического бутирилхолинэстеразой (БуХЭ) Использовали использования, среди них - соединение с pJso АХЭ из эритроцитов крови человека с удельной 5,55 и соединение с pJso - 5,70 активностью 1,2Ед/мг и БуХЭ из сыворотки крови Комп'ютерна верстка А Крулевський Підписано до друку 06 10 2003 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюPhosphorus containing cethysine derivatives
Назва патенту російськоюПроизводные цитизина, содержащие фосфор
МПК / Мітки
МПК: C07F 9/6561
Мітки: фосфор, містять, похідні, цитизину
Код посилання
<a href="https://ua.patents.su/5-59365-pokhidni-citizinu-shho-mistyat-fosfor.html" target="_blank" rel="follow" title="База патентів України">Похідні цитизину, що містять фосфор</a>
Попередній патент: Радіатор, зокрема для систем опалення, з високим опором внутрішньому тиску
Наступний патент: Спосіб та пристрій, що діють у реальному часі, для виявлення, визначення місця знаходження, швидкості та напряму руху ділянки відносного переміщення в сцені
Випадковий патент: Тара-гра з упакуваннями для дрібнофасованих виробів









