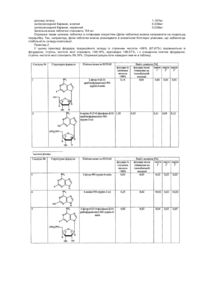
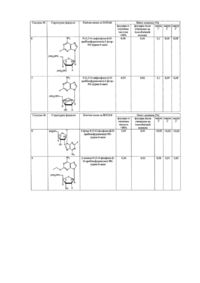
Таблетована композиція із швидким вивільненням надчистої флудари та її застосування
Номер патенту: 78741
Опубліковано: 25.04.2007
Автори: Хайль Вольфганг, Так Йоханнес-Вільгельм, Ліпп Ральф, Тільштам Ульф
Формула / Реферат
1. Таблетована композиція із швидким вивільненням діючої речовини, яка містить як діючу речовину флудару із ступенем чистоти >99,19 % у кількості від 1 до 100 мг у сполученні з моногідратом лактози, колоїдним діоксидом кремнію, мікрокристалічною целюлозою (Avicel), натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) і стеаратом магнію, яка відрізняється тим, що процентний вміст домішок у флударі не перевищує наступних значень:
0,02 % 2-фтор-9-(![]() -D-арабінофуранозил)-9Н-пурин-6-аміну,
-D-арабінофуранозил)-9Н-пурин-6-аміну,
0,12 % 6-аміно-9-(5-O-фосфоно-![]() -D-арабінофуранозил)-9Н-пурин-2-олу,
-D-арабінофуранозил)-9Н-пурин-2-олу,
0,02 % 2-фтор-9Н-пурин-6-аміну,
0,02 % 6-аміно-9Н-пурин-2-олу,
0,05 % 2-фтор-9-(5-O-фосфоно-![]() -D-рибофуранозил)-9Н-пурин-6-аміну,
-D-рибофуранозил)-9Н-пурин-6-аміну,
0,1 % 9-(3,5-O-дифосфоно-![]() -D-арабінофуранозил)-2-фтор-9Н-пурин-6-
-D-арабінофуранозил)-2-фтор-9Н-пурин-6-
аміну,
0,1 % 9-(2,5-O-дифосфоно-![]() -D-арабінофуранозил)-2-фтор-9Н-пурин-6-
-D-арабінофуранозил)-2-фтор-9Н-пурин-6-
аміну,
0,02 % 2-фтор-9-(5-O-фосфоно-![]() -D-арабінофуранозил)-9Н-пурин-6-аміну,
-D-арабінофуранозил)-9Н-пурин-6-аміну,
0,06 % 2-етокси-9-(5-O-фосфоно-![]() -D-арабінофуранозил)-9Н-пурин-6-
-D-арабінофуранозил)-9Н-пурин-6-
аміну,
0,02 % 2-(6-аміно-9Н-пурин-2-іл)-9-(5-O-фосфоно-![]() -D-арабінофуранозил)-
-D-арабінофуранозил)-
9Н-пурин-6-аміну й O,O'-біс[2-(6-аміно-2-фтор-9Н-пурин-9-іл)-5-
дезокси-![]() -D-арабінофураноз-5-ил]фосфату,
-D-арабінофураноз-5-ил]фосфату,
0,1 % 9-(2-хлор-2-дезокси-5-фосфоно-![]() -D-арабінофуранозил)-2-фтор-9Н-
-D-арабінофуранозил)-2-фтор-9Н-
пурин-6-аміну й
0,1 % 9-(2,5-ангідро-![]() -D-арабінофуранозил)-2-фтор-9Н-пурин-6-аміну.
-D-арабінофуранозил)-2-фтор-9Н-пурин-6-аміну.
2. Таблетована композиція із швидким вивільненням діючої речовини за п. 1, яка містить як діючу речовину флудару із ступенем чистоти >99,19 % у кількості від 1 до 70 мг разом з моногідратом лактози в кількості від 50 до 100 мг, колоїдним діоксидом кремнію в кількості від 0,1 до 5 мг, мікрокристалічною
целюлозою (Avicel) у кількості від 40 до 100 мг, натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозу) у кількості від 1 до 10 мг і стеаратом магнію в кількості від 0,5 до 10 мг.
3. Таблетована композиція із швидким вивільненням діючої речовини за п. 1 або 2, яка містить як діючу речовину флудару із ступенем чистоти >99,19 % у кількості від 1 до 50 мг разом з моногідратом лактози в кількості від 60 до 90 мг, колоїдним діоксидом кремнію в кількості від 0,5 до 1 мг, мікрокристалічною целюлозою (Avicel) у кількості від 50 до 90 мг, натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) у кількості від 1,5 до 5 мг і стеаратом магнію в кількості від 1 до 3 мг.
4. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-3, яка містить як діючу речовину флудару із ступенем чистоти >99,19 % у кількості 10 мг разом з моногідратом лактози в кількості 74,75 мг, колоїдним діоксидом кремнію в кількості 0,75 мг, мікрокристалічною целюлозою (Avicel) у кількості 60,00 мг, натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) у кількості 3,00 мг і стеаратом магнію в кількості від 1,5 до 2,00 мг.
5. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-4, яка містить як діючу речовину флудару із ступенем чистоти >99,37 %.
6. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-5, яка містить як діючу речовину флудару із ступенем чистоти >99,57 %.
7. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-6, яка містить як діючу речовину флудару із ступенем чистоти >99,80 %.
8. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-7, яка містить як діючу речовину флудару із ступенем чистоти >99,85 %.
9. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-8, яка відрізняється тим, що на серцевини таблеток нанесене покриття, яке містить наступні компоненти: гідроксипропілметилцелюлозу в кількості від 1 до 5 мг, тальк у кількості від 0,1 до 1 мг, діоксид титану в кількості від 0,1 до 5 мг, жовтий залізооксидний барвник у кількості від 0,01 до 0,1 мг і червоний залізооксидний барвник у кількості 0,01 до 0,1 мг.
10. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-9, яка відрізняється тим, що на серцевини таблеток нанесене покриття, яке містить наступні компоненти: гідроксипропілметилцелюлозу в кількості від 1 до 3 мг, тальк у кількості від 0,1 до 0,8 мг, діоксид титану в кількості від 0,1 до 2 мг, жовтий залізооксидний барвник у кількості від 0,01 до 0,05 мг і червоний залізооксидний барвник у кількості від 0,01 до 0,05 мг.
11. Таблетована композиція із швидким вивільненням діючої речовини за будь-яким з пп. 1-10, яка відрізняється тим, що на серцевину таблеток нанесене покриття, яке містить наступні компоненти: гідроксипропілметилцелюлозу в кількості 2,250 мг, тальк у кількості 0,450 мг, діоксид титану в кількості 1,187 мг, жовтий залізооксидний барвник у кількості 0,036 мг і червоний залізооксидний барвник у кількості 0,036 мг.
12. Застосування таблетованої композиції за будь-яким з пп. 1-11 для одержання медикаменту, призначеного для лікування раку.
Текст
Даний винахід стосується таблетованої композиції із швидким вивільненням діючої речовини, як яку вона містить флудару із ступенем чистоти >99,19% (надчисту флудару) с певним складом залишкових домішок. Таблетування композиції на основі флудари із ступенем чистоти 99,5% й у яких така діюча речовина характеризується певним складом присутніх у ній домішок, дотепер не були відомі. Діюча речовина флудара із ступенем чистоти >99,19% відома із заявки WO 99/29710. Однак й у цій заявці не міститься ніяких відомостей про конкретний склад чистої флудари, яка присутня в лікарській композиції. Виходячи з вищевикладеного, в основу даного винаходу була покладена задача запропонувати стабільну таблетовану композицію, які містила б флудар у з високим ступенем чистоти та із строго визначеною концентрацією в ній залишкових домішок й яка була б швидкорозчинною й завдяки цьому швидко вивільняла б діюну речовину. При створенні винаходу було встановлено, що застосування в складі таблетованої композиції як діючої речовини флудари із ступенем чистоти >99,19% у не мікронізованій, а в просіяній формі із строго визначеною концентрацією в ній залишкових домішок дозволяє подолати недоліки відомих таблеток. Вміст діючої речовини в запропонованій у винаході таблетованій композиції становить від 5 до 100 мг, переважно від 8 до 75 мг, більш переважно від 10 до 50 мг, найбільш переважно від 10 до 20 мг. До числа переважних речовин (ад'ювантів і добавок), які включаються до складу лікарської композиції, належать лактоза, колоїдний діоксид кремнію, мікрокристалічна целюлоза (Avicel), натрієва сіль кроскармелози (натрійкарбоксиметилцелюлоза) і стеарат магнію. Разом з тим до складу лікарської композиції можна включати й інші відомі фахівцям речовини, які використовуються в технології приготування лікарських засобів. Загальний вміст подібних використовуваних у те хнології приготування лікарських засобів речовин (ад'ювантів і добавок) у складі таблетки становить від 100 до 250 мг, переважно від 120 до 200 мг, найбільш переважно від 130 до 180 мг. Відповідно до цього об'єктом даного винаходу є таблетована композиція із швидким вивільненням діючої речовини, яка містить флудар у як діючу речовину із ступенем чистоти >99,19% у кількості від 1 до 100 мг у сполученні з моногідратом лактози, колоїдним діоксидом кремнію, мікрокристалічною целюлозою (Avicel), натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) і стеаратом магнію і яка відрізняється тим, що процентний вміст домішок у флударі не перевищує наступних значень: 0,02% 2-фтор-9-(b-D-арабінофуранозил)-9Н-нурин-6-аміну, 0,12% 6-аміно-9-(5-О-фосфоно-b-D-арабінофуранозил)-9Н-пурин-2-олу, 0,02% 2-фтор-9Н-пурин-6-аміну, 0,02% 6-аміно-9Н-пурин-2-олу, 0,05% 2-фтор-9-(5-О-фосфоно-b-D-рибофуранозил)-9Н-пурин-6-аміну, 0,1% 9-(3,5-О-дифосфоно-b-D-арабінофуранозил)-2-фтор-9Н-пурин-6-аміну, 0,1% 9-(2,5-О-дифосфоно-b-D-арабінофуранозил)-2-фтор-9Н-нурин-6-аміну, 0,02% 2-фтор-9-(5-О-фосфоно-b-D-арабінофуранозил)-9Н-нурин-6-аміну, 0,06% 2-етокси-9-(5-О-фосфоно-b-D-арабінофуранозил)-9Н-нурин-6-аміну, 0,02% 2-(6-аміно-9Н-пурин-2-іл)-9-(5-О-фосфоно-b-D-арабінофуранозил)-9Н-пурин-6-аміну й О,О'-біс[2-(6аміно-2-фтор-9Н-пурин-9-іл)-5-дезокси-a-D-арабінофураноз-5-ил]фосфату, 0,1% 9-(2-хлор-2-дезокси-5-фосфоно-b-D-арабінофуранозил)-2-фтор-9Н-нурин-6-аміну й 0,1% 9-(2,5-ангідро-b-D-арабінофуранозил)-2-фтор-9Н-пурин-6-аміну. Переважна таблетована композиція із швидким вивільненням діючої речовини, яка містить як діючу речовину флудар у із ступенем чистоти >99,19% у кількості від 1 до 70,00 мг разом з моногідратом лактози в кількості від 50 до 100 мг, колоїдним діоксидом кремнію в кількості від 0,1 до 5 мг, мікрокристалічною целюлозою (Avicel) у кількості від 40 до 100 мг, натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) у кількості від 1 до 10 мг і стеаратом магнію в кількості від 0,5 до 10 мг. До особливо переважних належать ті таблетовані композиції із швидким вивільненням діючої речовини, які містять як діючу речовину флудару із ступенем чистоти >99,19% у кількості від 1 до 50,00 мг разом з моногідратом лактози в кількості від 60 до 90 мг, колоїдним діоксидом кремнію в кількості від 0,5 до 1 мг, мікрокристалічною целюлозою (Avicel) у кількості від 50 до 90 мг, натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) у кількості від 1,5 до 5 мг і стеаратом магнію в кількості від 1 до 3 мг. Найбільш переважною є таблетована композиція із швидким вивільненням діючої речовини, яка містить як діючу речовину флудару із ступенем чистоти >99,19% у кількості 10 мг разом з моногідратом лактози в кількості 74,75 мг, колоїдним діоксидом кремнію в кількості 0,75 мг, мікрокристалічноюцелюлозою (Avicel) у кількості 60,00 мг, натрієвою сіллю кроскармелози (натрійкарбоксиметилцелюлозою) у кількості 3,00 мг і стеаратом магнії в кількості від 1,5 до 2,00 мг. Переважні також ті композиції, які містять флудару як діючу речовину із ступенем чистоти >99,37%. Більше переважні ті композиції, які містять флудару як діючу речовину із ступенем чистоти >99,57%. До особливо переважних належать ті композиції, які містять флудару як діючу речовину із ступенем чистоти >99,80%. Найбільш переважні ті композиції, які містять флудар у як діюну речовину із ступенем чистоти >99,85%. Запропоновані у винаході композиції за загальновідомими методами переробляють у пресувальні маси, з яких потім пресують серцевини таблеток. На такі серцевини таблеток далі можна наносити покриття за загальновідомими методами. Для нанесення покриттів у принципі можуть використовуватися всі відомі фа хівцям з їх застосування в ци х цілях матеріали. Одне із переважних покриттів може містити, наприклад, такі компоненти: гідроксипропілметилцелюлозу в кількості від 1 до 5 мг, переважно від 1 до З мг, найбільш переважно 2,250 мг, тальк у кількості від 0,1 до 1 мг, переважно від 0,1 до 0,8 мг, найбільш переважно 0,450 мг, діоксид титану в кількості від 0,1 до 5 мг, переважно 0,1 до 2 мг, найбільш переважно 1,187 мг, жовтий залізооксидний барвник у кількості від 0,01 до 0,1 мг, переважно від 0,01 до 0,05 мг, найбільш переважно 0,036 мг, і червоний залізооксидний барвник у кількості від 0,01 до 0,1 мг, переважно від 0,01 до 0,05 мг, найбільш переважно 0,036 мг. Подібні покриття також є об'єктом даного винаходу. Запропоновані у винаході таблетовані композиції можуть використовува тися для одержання медикаменту, призначеного для лікування раку. Відповідно до цього даний винахід стосується також застосування запропонованих у ньому композицій для одержання медикаменту, призначеного для лікування раку. У наступних прикладах описаний спосіб одержання запропонованих у винаході таблетованих композицій з надчистою флударою, а також дається порівняльний аналіз флудари звичайного складу із ступенем чистоти 99,19%. Приклад 1 Одержання таблетованої композиції Для одержання запропонованої у винаході таблетованої композиції діючу речовину флудар у (флударабіну фосфа т) спочатку просіюють, після чого разом з моногідратом лактози, мікрокристалічною целюлозою (Avicel) і колоїдним діоксидом кремнію переробляють у приблизно 30%-ну суху суміш. Цю суміш потім також просіюють. Якість, відповідно величину частинок перевіряють шляхом ситового аналізу. Після цього до сухої суміші на наступних стадіях змішування послідовно додають натрієву сіль кроскармелози (натрійкарбоксиметилцелюлозу) і стеарат магнію. Отриману пресувальну масу спресовують у серцевини таблеток. Отримана таким шляхом таблетована композиція містить, наприклад, такі окремі компоненти: надчиста флудара із ступенем чистоти >99,19% 10,00мг моногідрат лактози 74,75мг колоїдний діоксид кремнію 0,75мг мікрокристалічна целюлоза (Avicel) 60,00мг натрієва сіль кроскармелози (натрійкарбоксиметилцелюлоза) 3,00мг стеарат магнію 1,5-2,00мг На завершення на серцевини таблеток наносять лакове плівкове покриття з водної суспензії. Подібне плівкове покриття містить, наприклад, такі компоненти: гідроксипропілметилцелюлоза 2,250мг тальк 0,450мг діоксид титану 1,187мг залізооксидний барвник, жовтий 0,036мг залізооксидний барвник, червоний 0,036мг Загальна маса таблетки становить 154 мг. Отримані таким шляхом таблетки із плівковим покриттям (філм-таблетки) можна направляти на подальшу переробку. Так, наприклад, філм-таблетки можна упаковувати в алюмінієві блістерні упаковки, що забезпечує стабільність складу композиції. Приклад 2 У цьому прикладі флудара традиційного складу із ступенем чистоти 99,19%, відповідно >99,57%, і з очищеною іонітом флударою, ступінь чистоти якої становить 99,19%. Отримані результати наведені нижче в таблиці. Отримані в цьому прикладі результати свідчать про те, що композиція з комерційно доступною флударою (флударою з максимальним ступенем чистоти 97,67%) або композиція з очищеною іонітом флударою (флударою з максимальним ступенем чистоти 99,19%) містить значно більшу кількість побічних продуктів як забруднюючих домішок в порівнянні із запропонованою у винаході композицією з надчистою флударою (флударою із ступенем чистоти від >99,37% до >99,57%). Традиційні методи очищення, такі, наприклад, як винятково ефективна іонообмінна хроматографія, дозволяють одержати продукт лише з порівняно помірним ступенем чистоти. Запропоновані у винаході композиції із флударою містять отриману через утворення натрієвої солі надчисту флудару, як це вже описано в заявці WO 99/29710. Флудару із ще більш високим ступенем чистоти можна одержати через утворення калієвої солі (ступінь чистоти 99,8%) або літієвої солі (ступінь чистоти 99,85%).
ДивитисяДодаткова інформація
Назва патенту англійськоюFast releasing tablet formulation containing ultrapure fludara and its use
Автори англійськоюHeil Wolfgang, Lipp Ralph
Назва патенту російськоюТаблетированная композиция с быстрым высвобождением сверхчистой флудары и ее применение
Автори російськоюХайль Вольфганг, Липп Ральф
МПК / Мітки
МПК: A61P 35/00, A61K 9/28, A61K 9/20, A61K 31/70
Мітки: таблетована, застосування, вивільненням, швидким, флудари, композиція, надчистої
Код посилання
<a href="https://ua.patents.su/5-78741-tabletovana-kompoziciya-iz-shvidkim-vivilnennyam-nadchisto-fludari-ta-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Таблетована композиція із швидким вивільненням надчистої флудари та її застосування</a>
Попередній патент: Спосіб стабілізації індивідуального субстрату для спектрального визначення злоякісності
Наступний патент: Похідні бензотіазину і бензотіадіазину, спосіб їх одержання і фармацевтична композиція, яка їх містить
Випадковий патент: Спосіб формування протистенотичного кінце-кінцевого анастомозу на трубчастих органах травного тракту