Композиція, яка містить 11b-галогенстероїд, який має андрогенну дію, і гестаген, та чоловічий контрацептив на основі цієї композиції
Номер патенту: 78834
Опубліковано: 25.04.2007
Автори: Хабеніхт Урсула-Фрідеріке, Больманн Рольф, Нуббемайер Райнхард
Формула / Реферат
1. Композиція, яка містить 11 β -галогенстероїд загальної формули І, який має андрогенну дію:
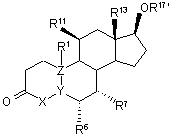 , І
, І
у якій
X-Y-Z являє собою групу однієї з обох структур СН=С-С або СН2-С=С,
R1 може знаходитися в ![]() і
і ![]() -положенні і являє собою водень, R або зв'язане через Р з циклічним каркасом угруповання P-Q-R, де Р і Q означають прямоланцюгові або розгалужені С1-С8алкіленові, С1-С8алкеніленові, С1-С8алкініленові групи або їх фторовані похідні і можуть мати ідентичні або різні значення, і де R означає залишок СН3 або СF3, за умови, що при Z відсутній замісник R1, якщо X-Y-Z являє собою групу СН2-С=С,
-положенні і являє собою водень, R або зв'язане через Р з циклічним каркасом угруповання P-Q-R, де Р і Q означають прямоланцюгові або розгалужені С1-С8алкіленові, С1-С8алкеніленові, С1-С8алкініленові групи або їх фторовані похідні і можуть мати ідентичні або різні значення, і де R означає залишок СН3 або СF3, за умови, що при Z відсутній замісник R1, якщо X-Y-Z являє собою групу СН2-С=С,
R6 являє собою атом водню або може мати значення, вказані для R7,
R7 являє собою R або зв'язане через Р з циклічним каркасом угруповання Р-Q-R, де групи, які утворюють це угруповання, мають вказані вище значення,
R11 являє собою галоген,
R13 являє собою метил або етил, і
R17' являє собою водень або C(O)-R18, де
R18 являє собою прямоланцюговий або розгалужений С1-С18алкільний, С1-С18алкенільний, С1-С18алкінільний або арильний залишок, або являє собою зв'язане через Р з С(O)-групою угруповання T-U-V, де Т і U означають прямоланцюгові або розгалужені С1-С18алкіленові, С1-С18алкеніленові, С1-С18алкініленові групи, аліциклічні С3-С12-групи або арильні групи і мають ідентичні або різні значення, а V означає прямоланцюговий або розгалужений С1-С18алкільний, С1-С18алкенільний, С1-С18алкінільний або арильний залишок, або
R18 має одне з вищевказаних значень і додатково заміщений однією або декількома групами NR19R20 або однією або декількома групами SOxR21, при цьому х означає 0, 1 або 2, а R19, R20 і R21 кожний являє собою відповідно водень або зв'язане через Т з N, S угруповання Т-U-V, яке має вказані вище значення, за умови, що, крім того, дані поняття включають фізіологічно сумісні кислотно-адитивні солі з неорганічними й органічними кислотами,
і гестаген наступної формули
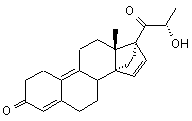 .
.
2. Композиція за п. 1, яка відрізняється тим, що 11 ![]() -галогенстероїд загальної формули І являє собою сполуку 11
-галогенстероїд загальної формули І являє собою сполуку 11 ![]() -фтор-17
-фтор-17 ![]() -гідрокси-7
-гідрокси-7 ![]() -метилестр-4-ен-3-он.
-метилестр-4-ен-3-он.
3. Фармацевтичний препарат, який містить композицію за п. 1, а також фармацевтично прийнятний носій і/або допоміжні речовини.
4. Фармацевтичний препарат за п. 3, який відрізняється тим, що 11 ![]() -галогенстероїд загальної формули І являє собою сполуку 11
-галогенстероїд загальної формули І являє собою сполуку 11 ![]() -фтор-17
-фтор-17 ![]() -гідрокси-7
-гідрокси-7 ![]() -метилестр-4-ен-3-он.
-метилестр-4-ен-3-он.
5. Чоловічий контрацептив, який містить фармацевтичний препарат за п. 3.
6. Чоловічий контрацептив, який містить фармацевтичний препарат за п. 4.
7. Чоловічий контрацептив за п. 5 або 6, який відрізняється тим, що сполука загальної формули І, яка входить до його складу і яка має андрогенну дією, вводиться в організм за допомогою відповідного імплантата безперервно протягом тривалого проміжку часу.
8. Чоловічий контрацептив за п. 5 або 6, який відрізняється тим, що сполука загальної формули І, яка входить до його складу і яка має андрогенну дію, вводиться в організм перорально.
9. Чоловічий контрацептив за п. 5 або 6, який відрізняється тим, що сполука загальної формули І, яка входить до його складу і яка має андрогенну дію, вводиться в організм за допомогою трансдермальної системи протягом тривалого проміжку часу.
10. Чоловічий контрацептив за будь-яким з пп. 5-9, який відрізняється тим, що андроген, який входить до його складу, вводиться в організм за допомогою відповідного імплантата безперервно протягом тривалого проміжку часу.
11. Чоловічий контрацептив за будь-яким з пп. 5-9, який відрізняється тим, що гестаген є компонентом трансдермальної системи.
12. Чоловічий контрацептив за будь-яким з пп. 5-9, який відрізняється тим, що гестаген вводиться перорально.
Текст
Даний винахід стосується композиції, яка містить 11b-галогенстероїд, який має андрогенну дію, вибраний із групи сполук загальної формули І I у якій X-Y-Z являє собою групу однієї з обох структур СН=С-С або СН2-С=С, R1 може знаходитися в a- і b-положенні і являє собою водень, R або зв'язане через Ρ з циклічним каркасом угруповання P-Q-R, де Ρ і Q означають прямоланцюгові або розгалужені С1-С8алкіленові, С1С8алкеніленові, С1-С8алкініленові групи або їх фторовані похідні і можуть мати ідентичні або різні значення і де R означає залишок СН3 або CF3, за умови, що при Ζ відсутній замісник R1, якщо Χ-Υ-Ζ являє собою групу СН2С=С R6 являє собою атом водню або може мати значення, вказані для R7, R7 являє собою R або зв'язане через Ρ з циклічним каркасом угруповання Р-Q-R, де групи, які утворюють це угруповання, мають вказані вище значення, R11 являє собою галоген, R13 являє собою метил або етил і R17' являє собою водень або C(O)-R18, де R18 являє собою прямоланцюговий або розгалужений С 1-С18алкільний, С1-С18алкенільний, С1С18алкінільний або арильний залишок, або являє собою зв'язане через Ρ з С(О)-групою угруповання T-U-V, де Τ і U означають прямоланцюгові або розгалужені С1-С18алкіленові, С1-С18алкеніленові, С1-С18алкініленові групи, аліциклічні С3-С12групи або арильні групи і мають ідентичні або різні значення, а V означає прямоланцюговий або розгалужений С1-С18алкільний, С1-С18алкенільний, С1-С18алкінільний або арильний залишок, або R18 має одне з вищевказаних значень і додатково заміщений однією або декількома групами NR19R20 або однією або декількома групами SOxR21, при цьому x означає 0, 1 або 2, a R19, R20 і R21 кожний являє собою відповідно водень або зв'язане через Τ з N, S угруповання Т-U-V, яке має вказані вище значення, за умови, що, крім того, дані поняття включають фізіологічно сумісні кислотно-адитивні солі з неорганічними й органічними кислотами, і гестаген наступної формули Дана композиція придатна для одержання фармацевтичних препаратів. Відповідно до цього даний винахід стосується фармацевтичних препаратів, які містять вищезгадану композицію, до складу якої входять 11b-галогенстероїд, який має андрогенну дію, і гестаген формули а також фармакологічно прийнятний носій і/або допоміжні речовини. Переважний як 11b-галогенстероїд, який має андрогенну дію, як для композиції, так і для фармацевтичного препарату 11b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-он. Об'єктом даного винаходу є далі чоловічий контрацептив на основі запропонованої у винаході композиції. Відповідно до одного з варіантів здійснення винаходу до складу чоловічого контрацептиву як 11bгалогенстероїд, який має андрогенну дію, входить 11b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-он. Відповідно до одного з особливо переважних варіантів здійснення даного винаходу як 11b-галогенстероїд, який має андрогенну дію, так і гестаген представлені в чоловічому контрацептиві або у вигляді загального імплантата, або двох окремих імплантатів і можуть застосовуватися відповідно в такій формі з метою забезпечити вивільнення активних сполук в організмі чоловіка протягом тривалого проміжку часу (тобто забезпечити пролонговану дію). Безперервне вивільнення гестагену протягом тривалого проміжку часу можна забезпечити також за допомогою трансдермальної системи, у яку занурений гестаген. Відповідно до винаходу передбачається й інший підхід, а саме: одну з діючих речовин вводити в організм у складі перорального препарату, а іншу діючу речовину вводити у вигляді імплантата або черезшкірно. Можливий і такий варіант, коли обидві діючі речовини вводяться перорально. І наприкінці слід назвати ще одну можливість: призначати один або обидва компоненти запропонованої у винаході композиції для букального застосування або для введення через слизову оболонку. Концепція контролю чоловічої фертильності відповідає проголошеним Всесвітньою організацією охорони здоров'я (ВООЗ) глобальним цілям під гаслом "За здорову репродуктивну здатність" [Reproductive Health, див. WHO Task Force on Methods for the Regulation of Male Fertility, 1990, Contraceptive efficacy of testosteroneinduced azoospermia in normal men, Lancet 336, cтop.955-959; WHO Task Force on Methods for the Regulation of Male Fertility, 1993, Comparison of two androgens plus depot-medroxyprogesterone acetate for suppression to azoospermia in Indonesian men, Fertil. Steril. 60, с.1062; WHO Task Force on Methods for the Regulation of Male Fertility, 1995, Rate of testosterone-induced suppression to severe oligozoospermia or azoospermia in two multinational clinical studies, Int. J. Androl. 18, с.157-165; WHO Task Force on Methods for the Regulation of Male Fertility, 1996, Contraceptive efficacy of testosterone-induced azoospermia and oligozoospermia in normal men, Fertil. Steril. 65, стор.821-829] Невід'ємною складовою частиною цієї стратегії є протизаплідні засоби для чоловіків та жінок. Але оскільки насамперед задовільні методи чоловічої контрацепції дотепер відсутні, їх розробка розглядається як одна з насущних задач [Andrologie, Grundlagen und Klinik der reproduktiven Gesundheit des Mannes, під ред. Ε. Nieschlag, H.M. Behre, вид-во Springer-Verlag, 2-е вид., 2000, стор.442 і далі]. Найбільш значний прогрес досягнутий у розробці гормональних методів контролю чоловічої фертильності. Ці методи відрізняються підтвердженою практикою оборотністю й ефективністю. Гормональна чоловіча контрацепція заснована на пригніченні (припиненні) сперматогенезу, що в кінцевому рахунку приводить до азооспермії і тим самим до (тимчасової) безплідності чоловіків. З механістичної точки зору відбувається істотне пригнічення обох гонадотропінів - ЛГ (лютеїнізуючого гормону) і ФСГ (фолікулостимулювального гормону), тобто концентрація цих обох гормонів у сироватці крові знаходиться в даному випадку нижче меж виявлення. Наслідком інгібування ЛГ є також пригнічення продукування яєчниками тестостерону (обидва гормони належать до ендокринної системи регуляції). Повне пригнічення всіх трьох гормонів є неодмінною умовою інгібування сперматогенезу. Істотним недоліком описаного методу є дефіцит андрогенів і зумовлені цим відповідні симптоми і наслідки, які спостерігаються в чоловіків. Методи чоловічої контрацепції спрямовані на пригнічення ЛГ, ФСГ і внутрішньотестикулярного тестостерону і тим самим на інгібуванні сперматогенезу, тоді як периферичний тестостерон заміщається на андроген, який вводиться зовні. Як андроген дотепер використовували тестостерон, відповідно ефіри тестостерону (наприклад енантат тестостерону, буциклат тестостерону). Ендокринний тестостерон призначений для підтримання на необхідному рівні лібідо, потенції, "чоловічої поведінки", метаболізму білків, і еритропоезу й інших функцій, таких як обмін мінеральних речовин і обмін речовин у кістковій тканині. Іншими словами, мета полягає в тому, щоб знизити вміст тестостерону в яєчках до рівня, типового для нього в периферичній крові, підтримувати його вміст у загальній циркуляційній системі на постійному рівні. Пригнічення сперматогенезу за допомогою тільки тестостерону або ефірів тестостерону вважалося в перший момент ідеальним протизаплідним методом, однак, як було встановлено пізніше, він виявився недостатньо ефективним, і в ряді випадків до початку необхідної дії був потрібний значний проміжок часу (аж до 6 місяців). Крім того, доводилося враховувати і такий фактор, як етнічні особливості. Введення занадто високих доз супроводжувалося очевидними, небажаними побічними ефектами. При використанні тестостерону були зафіксовані такі побічні ефекти, як насамперед збільшення передміхурової залози за рахунок росту числа клітин і залоз строми (ДГП, доброякісна гіперплазія простати). При опосередкованому 5аредуктазою метаболізмі тестостерону утворюється дигідротестостерон (ДГТ), який може серед іншого сприяти появі ДГП [Cummings і ін., див. вище; заявка WO 99/13883 А1]. Оскільки тестостерон у придатних для перорального застосування формах зараз відсутній, доводиться використовувати інші, альтернативні лікарські форми (внутрішньом'язові, пластири і т.п.). З метою прискорити настання необхідної дії, так само як і підвищити ефективність тестостерон стали комбінувати з іншими речовинами, які пригнічують гонадотропіни, з GnRH-антагоністами (від англ. "Gonadotropin Releasing Hormone", гонадотропін-рилізінг-гормон). Завдяки цій комбінації вдалося значно поліпшити азооспермію і скоротити час до настання передбаченої дії. Однак наявні зараз GnRH-антагоністи представлені в такій формі, що їх доводиться вводити в організм щодня (внутрішньом'язово або підшкірно, пероральні форми відсутні), і їх одержання вимагає чималих витрат. З цієї причини вказана комбінація не знайшла широкого поширення. Застосування прогестинів, таких як ацетат ципротерону або левоноргестрел, або виявлялося неефективним при пригніченні сперматогенезу, або приводило при високих дозуваннях до значного зниження числа еритроцитів (Merrigiola і ін., 1998; Merrigiola і ін., 1997; Merrigiola і ін., 1996; Bebb і ін., 1996). Застосування суміші двох сполук, одного естрогену з іншим естрогеном, у комбінації між собою [описане в патенті US 4210644]. Також був описаний метод, спрямований на інгібування сперматогенезу шляхом черезшкірного або перорального введення тестостерону і перорального введення ацетату норетистерону (Guerin i Rollet, 1998). Однак для досягнення азооспермії потрібні достатньо високі дози обох компонентів. Для заміни тестостерону при чоловічій контрацепції був запропонований 7а-метил-19-нортестостерон (МеНТ), який, по-перше, характеризується більш високою в порівнянні з тестостероном ефективністю, оскільки має більш високу афінність до андрогенних рецепторів, і, по-друге, завдяки стеричному бар'єру, утвореному 7ос-метильною групою, ймовірно, перешкоджає метаболізуванню під дією 5ос-редуктази [Cummings і ін., див. вище, WO 99/13883 А1, WO 99/13812 А1, US 5342834]. Завдяки другій з вищезгаданих властивостей, як очікується, буде забезпечений помітно більш сприятливий у порівнянні з тестостероном профіль побічних ефектів, особливо у відношенні передміхурової залози. Про комбінацію 7a-метил-19-нортестостерону і гестагену у вказаних джерелах не говориться. Серед інших, порівнянних з 7a-метил-19-нортестостероном за їх вибірною андрогенною дією, сполук слід назвати запропоновані відповідно до винаходу до використання 11b-галогенстероїди загальної формули І, які мають андрогенну дію, насамперед 11b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-он. Вказані сполуки вперше [описані в заявці DE 10104327.9]. Ці сполуки мають у порівнянні з 7a-метил-19-нортестостероном більш високу метаболічну стабільність. [DE 10104327.9] є неопублікованою заявкою. При описі замісників у сполуках загальної формули І і розкритті їх значень даються посилання на цей документ. Названі сполуки пропонується застосовувати для чоловічої контрацепції, їх можна використовувати разом з гестагенами, однак більш докладна інформація, про які саме гестагенах при цьому йдеться, відсутня. З урахуванням вищевикладеного в основу даного винаходу була покладена задача запропонувати протизаплідний засіб для чоловіків (чоловічий контрацептив) на основі андрогену/гестагену без використання тестостерону як андрогену. Одночасно з цим передбачалося, що завдяки гестагену вдається мінімізувати дозу використовуваного андрогену і як наслідок зменшити побічні ефекти. Покладена в основу винаходу задача вирішується завдяки вказаній вище комбінації з 11b-галогенстероїду, який має андрогенну дію, насамперед 17b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-ону, і гестагену формули Цей гестаген [описаний у заявці WO 96/20209 (DE 4447401.6)]. Однак у даній заявці нічого не зазначається про спільне застосування з андрогеном для досягнення (тимчасової) чоловічої безплідності. Мова йде лише про гестаген, який виявляє винятково високу ефективність після перорального введення. Разом з тим у названій публікації пропонуються й інші шляхи введення в організм. Крім того, [у заявці ЕР 00250449.6] описана трансдермальна система, яка містить цей гестаген. Застосування запропонованої в даному винаході комбінації як чоловічого контрацептиву дозволяє інгібувати у достатньому ступені продукування сперматозоїдів у яєчку й одночасно з цим забезпечити відносно низьку дозу заміщення андрогену. Іншими словами, досягається синергетичний ефект. За допомогою запропонованої у винаході як чоловічого контрацептиву композиції при низькому дозуванні обох компонентів, які входять до її складу, вдається знизити вміст ЛГ, ФСГ і тестостерону до рівня нижче меж виявлення, відповідно до рівня втрати ними активності. Таке зниження концентрації ЛГ і ФСГ відбувається одночасно. Для досягнення необхідної дії запропонованого у винаході контрацептиву і його прийнятності для чоловіків вирішальне значення при цьому має відносно швидке зниження вмісту вказаних найбільш важливих для надійності контрацептиву параметрів (тобто ЛГ і ФСГ). Відповідно до винаходу для настання дії запропонованого контрацептиву передбачається приблизно З місяці після початку його використання. Принципових і "особистісних" обмежень у тривалості використання запропонованого у винаході контрацептиву нема, тобто це може продовжуватися до того моменту, коли користувачу більше не потрібна контрацепція. З іншого боку, запропонований у винаході контрацептив у будь-який момент гарантує користувачу відновлення його репродуктивної здатності. Дозування 11b-галогенстероїду загальної формули І, який має андрогенну дію, насамперед 11b-фтор-17bгідрокси-7a-метилестр-4-ен-3-ону, і гестагену вибирають з таким розрахунком, щоб вміст ЛГ, тестостерону і ФСГ найпізніше через 3 місяці після початку використання контрацептиву знаходився на рівні за межами активності цих параметрів. Для 11b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-оу достатнім є добова ефективна кількість, яка дорівнює 0,7-1,5мкг, переважно 0,7-1,0мкг. При визначенні ефективної кількості андрогенного стероїду формули І слід враховувати, що ефективність 11b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-ону приблизно в 10 разів перевищує цей показник тестостерону. У випадку застосування імплантату або якої-небудь іншої системи, яка вивільняє діючу речовину протягом тривалого проміжку часу, цю систему необхідно формувати таким чином, щоб забезпечити щоденне вивільнення певної, вказаної кількості діючої речовини. При дозуванні застосовуваного відповідно до винаходу гестагену можна виходити з того, що його вибрана кількість виявляє на пригнічення сперматогенезу дію, порівнянну з дією левоноргестрелу в добовій дозі, що дорівнює 200-300мкг. Переважною є кількість, еквівалентна ефективній кількості левоноргестрелу при пероральному введенні останнього в добовій дозі, що дорівнює 240-260мкг. Еквівалентні ефективні кількості левоноргестрелу і застосовуваного відповідно до винаходу гестагену визначають за методами, відомим фахівцям у даній галузі, наприклад у дослідах із збереження вагітності в щура. При формуванні обох діючих речовин з метою їх використання в контрацептиві за винаходом можна керуватися даними, наведеними в вказаних вище джерелах, у яких ці діючі речовини описані як такі і на які у даному описі робляться посилання. Технологія формування андрогенів, відповідно гестагенів для наступного вивільнення цих діючих речовин протягом тривалого проміжку часу відома з рівня техніки, так, зокрема, можна назвати імплантовані системи для гестагенів Norplant і Jardelle. Далі, при формуванні застосовуваного відповідно до винаходу гестагену можна послатися [на заявки WO 00/21570 (разом з циклодекстрином) і WO 02/49622 (трансдермальна система, яка містить застосовуваний відповідно до винаходу гестаген)]. Концентрацію ЛГ, ФСГ, так само як і тестостерону визначають за відомими методами. Ефективність запропонованої у винаході композиції підтверджується - визначенням концентрації ЛГ у сироватці крові молодих самців щура після обробки протягом 1 тижня при підшкірному введенні комбінації сполук А і В (див. діаграму 1) і - визначенням концентрації тестостерону в сироватці крові дорослих самців щура після обробки протягом 1 тижня при підшкірному введенні комбінації сполук А і В (див. діаграму 2). В обох випадках вказані параметри вже після закінчення одного тижня знаходяться нижче меж виявлення (швидкий початок дії). Сполука А являє собою 11b-фтор-17b-гідрокси-7a-метилестр-4-ен-3-он, a сполука В являє собою застосовуваний відповідно до винаходу гестаген. Вказані дози вводили щодня з розрахунку на кг ваги тіла. В інших дослідах на самцях щура було встановлено, що за допомогою запропонованої у винаході комбінації (сполука А із сполукою В; дозування, ідентична до вказаної на діаграмах 1 і 2) після шеститижневої обробки/при шеститижневій обробці вдається - залежно від гормонального статусу зменшити масу релевантних органів (передміхурової залози, придатків яєчка, сім'яного пухирця і яєчка); - знизити кількість сперматозоїдів до рівня менш є 10% від контрольного значення; - підтримувати постійно показники концентрації гормонів ЛГ і тестостерону також після завершення обробки, яка здійснювалася впродовж вказаного проміжку часу на рівні нижче меж виявлення (тобто, отже, як при швидкому настанні дії (див. вище), так і при уповільненій (пролонгованій) дії). Бібліографія: Е. Nieschlag і Н.М. Behre, Testosterone in Male Contraception, під ред. Ε. Nieschlag і Н.М. Behre, Testosterone: action, deficiency, substitution, вид-во Springer, Berlin, 1998, стор.513-528; Μ.С. Merrigiola, W.J. Bremner, A. Constantino, A. Pavani, M. Capelli і С. Flamigni, Low Dose of Cyproterone Acetate and Testosterone Enanthate for Contraception in Men, Hum Reprod. 13, 1998, стор.1225-1229; Μ.С. Merrigiola, W.J. Bremner, A. Constantino, A. Pavant, M. Capelli і С. Flamigni, An Oral Regimen of Cyproterone Acetate and Testosterone Undecanoate for Spermatogenic Suppression in Men, Fertil. Steril. 68, 1997, стор.840-850; M.C. Merrigiola, W.J. Bremner, C.A. Paulsen, A. Valdiserri, L. Incorvaia, R. Motta, A. Pavani, M. Capelli і С. Flamigni, A Combined Regimen of Cyproterone Acetate and Testosterone Enanthate as a Potentially Highly Effective Male Contraceptive, J. Clin. Endocrinol. 81, 1996, стор.3018-3023; R.A. Bebb, B.D. Anawalt, R.B. Christensen, C.A. Paulsen, W.J. Bremner і A.M. Matsumoto, Combined Administration of Levonorgestrel and Testosterone Induces More Rapid and Effective Suppression of Spermatogenesis than Testosterone Alone, A Promising Contraceptive Approach, J. Clin Endocriniol. Metab. 81, 1996, стор.757-762; J.F. Guenn і J. Rollet, International Journal of Andrology 11, 1988, стор.187-199; Hadgraft i Guy, Transdermal Drug Delivery, Developmental Issues and Research Initiatives, вид-во Marcel Dekker Inc., 1989; M. Ottel і Е. Schillinger (під ред.), Handbook of Experimental Pharmacology, том 135/11, Androgens і Antiestrogens /1, Pharmacology and Clinical Applications of Estrogens and Antiestrogens, K.-H. Fritzemeier і С. Hegele-Hartung, In Vitro and In Vivo Models to Characterize Estrogens and Antiestrogens, вид-во Springer-Verlag, Berlin, Heidelberg, 1999; F. Neuman, F. Daher, J. Brotherton, K.-J. Graf, S.H. Hasan, H.J. Horn, A. Hughes, G.W. Oertel, H. Steinheck, H.E. Voss, R.K. Wagner, Androgens // and AntiAndrogens, вид-во Springer-Verlag, Berlin, Heidelberg, 1974; Fuhrmann, Bengston, Repenthin і Schillinger, J. SteroidBiochem. Мої. Biol. 42(8), 1992, с.787; Lancet 336, 1990, стор.955-959; Fertil. Steril. 60, 1993, стор.1062; Int. J. Androl. 18, 1995, стор.157-165; Fertil. Steril. 65, 1996, стор.821-829; Andrologie, Grundlagen und Klinik der reproduktiven Gesundheit des Mannes, під ред. Ε. Nieschlag, H.M. Behre, вид-во Springer-Verlag, 2-е вид., 2000, стор.442 і далі.
ДивитисяДодаткова інформація
Назва патенту англійськоюComposition containing androgenic 11-beta-halogen steroid and gestagen, pharmaceutical composition and male contraceptive
Автори англійськоюNubbemeyer Reinhard, Bohlmann Rolf
Назва патенту російськоюКомпозиция, содержащая 11-бета-галогенстероид, который обладает андрогенным действием, и гестаген, мужской контрацептив на основе этой композиции
Автори російськоюНуббемайер Райнхард, Больманн Рольф
МПК / Мітки
МПК: C07J 53/00, C07J 1/00, A61P 15/16, C07J 9/00, A61K 31/565
Мітки: яка, композиції, контрацептив, чоловічий, дію, містить, цієї, основі, андрогенну, гестаген, має, композиція, 11b-галогенстероїд
Код посилання
<a href="https://ua.patents.su/5-78834-kompoziciya-yaka-mistit-11b-galogensterod-yakijj-maeh-androgennu-diyu-i-gestagen-ta-cholovichijj-kontraceptiv-na-osnovi-cieh-kompozici.html" target="_blank" rel="follow" title="База патентів України">Композиція, яка містить 11b-галогенстероїд, який має андрогенну дію, і гестаген, та чоловічий контрацептив на основі цієї композиції</a>
Попередній патент: Пружна муфта
Наступний патент: Фіточай “енергія життя”
Випадковий патент: Спосіб діагностики поширених мутацій гена трбм









