Композиції на основі антитіла проти cd3
Формула / Реферат
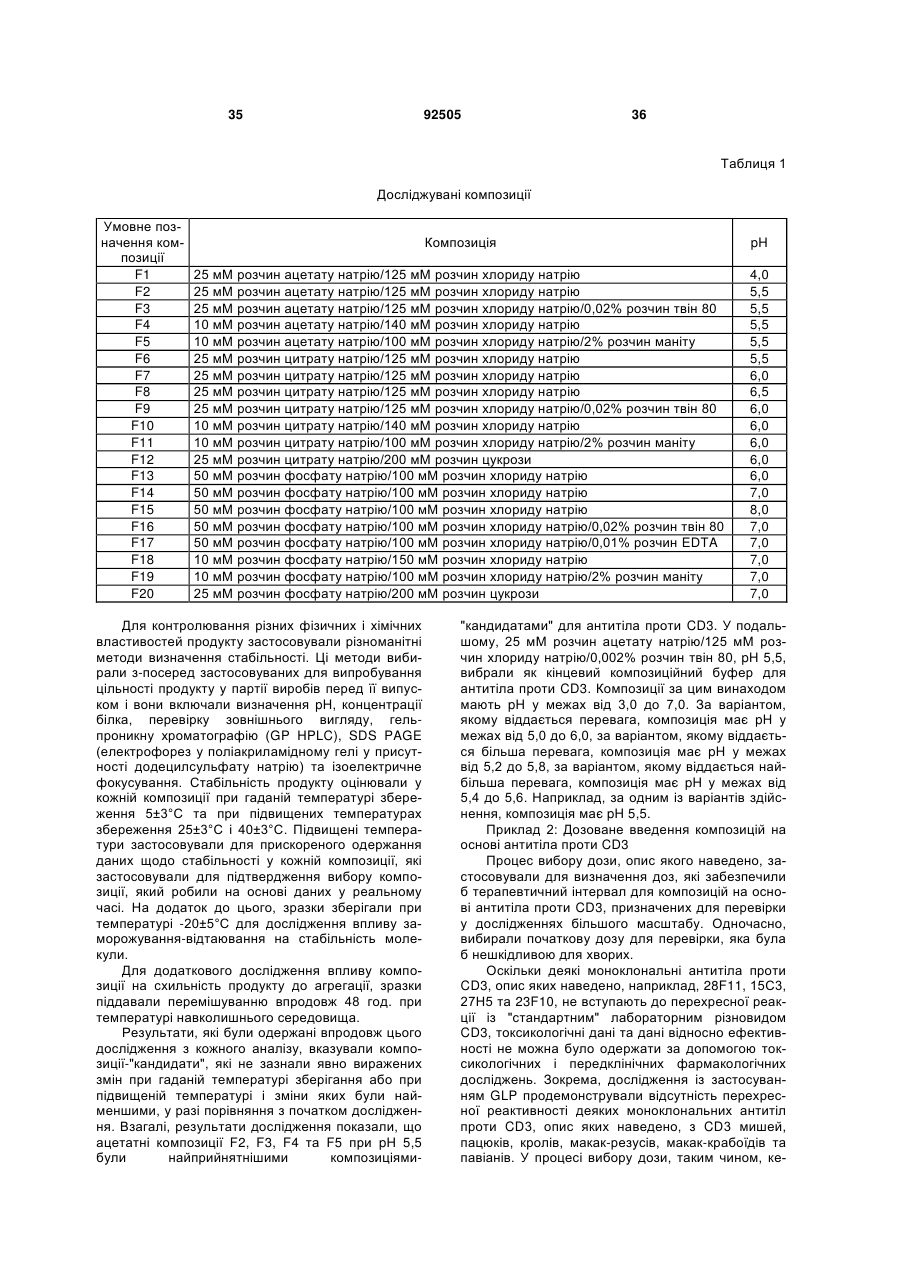
1. Фармацевтична композиція на основі антитіла проти CD3, яка містить такі суттєві інгредієнти:
a) рН-буферну речовину, концентрація якої становить від 10 мМ до 50 мМ, яка забезпечує рН від 5,0 до 6,0, причому згадана рН-буферна речовина являє собою ацетат натрію;
b) хлорид натрію, концентрація якого становить від 100 мМ до 140 мМ;
c) 0,02 % (у відношенні маси до об'єму) поверхнево-активної речовини; та
d) фармацевтично ефективну кількість антитіла проти CD3.
2. Композиція за п. 1, яка відрізняється тим, що концентрація хлориду натрію становить 125 мМ.
3. Композиція за п. 1, яка відрізняється тим, що згадана поверхнево-акгивна речовина являє собою іоногенну, аніоногенну або цвітеріонну поверхнево-активну речовину.
4. Композиція за п. 3, яка відрізняється тим, що згадана іоногенна поверхнево-активна речовина являє собою полісорбат.
5. Композиція за п. 4, яка відрізняється тим, що згаданий полісорбат являє собою полісорбат 80.
6. Композиція за п. 1, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,2 до 5,8.
7. Композиція за п. 1, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,4 до 5,6.
8. Композиція за п. 1, яка відрізняється тим, що рН-буферна речовина забезпечує рН 5,5.
9. Композиція за п. 1, яка відрізняється тим, що вміст поверхнево-активної речовини становить 0,02 % (у відношенні маси до об'єму), та тим, що згадана поверхнево-активна речовина являє собою полісорбат 80.
10. Композиція за п. 1, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,05 мг до 10 мг.
11. Композиція за п. 1, яка відрізняється тим, шо фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,1 мг до 5,0 мг.
12. Композиція за п. 1, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,5 мг до 3,0 мг.
13. Композиція за п. 1, яка відрізняється тим, що антитілом проти CD3 є:
антитіло 28F11, яке включає варіабельну ділянку 1 (CDR1) важкого ланцюга, що має амінокислотну послідовність SEQ ІD NО: 27, варіабельну ділянку 2 (CDR2) важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 28, варіабельну ділянку 3 (CDR3) важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 29, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 30, CDR2 легкого ланцюга, що має амінокислотну послідовність SEO ID NO: 31, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 32;
антитіло 27Н5, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 27, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 28, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 29, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 30, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 31, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 32;
антитіло 23F10, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 34, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 36, SEQ ID NO: 39 або SEQ ID NO: 43, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 37, SEQ ID NO: 40 або SEQ ID NO: 42, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 38 або SEQ ID NO: 41;
антитіло 15С3, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 44, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30 або SEQ ID NO: 39, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 31 або SEQ ID NО: 46, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 45 або SEQ ID NО: 47;
Orthoclone ОКТ3, людське ОКТ3γ1 (НОКТ3γ1) або ChAglyCD3.
14. Фармацевтична композиція на основі антитіла проти CD3, яка містить такі суттєві інгредієнти:
a) рН-буферну речовину, яка містить ацетат натрію, концентрація якого становить 25 мМ, що забезпечує рН у діапазоні від 5,0 до 6,0;
b) хлорид натрію, концентрація якого становить 125 мМ;
c) поверхнево-активну речовину, яка містить полісорбат; та
d) фармацевтично ефективну кількість антитіла проти CD3.
15. Композиція за п. 14, яка відрізняється тим, що згаданий полісорбат являє собою полісорбат 80.
16. Композиція за п. 14, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,2 до 5,8.
17. Композиція за п. 14, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,4 до 5,6.
18. Композиція за п. 14, яка відрізняється тим, що рН-буферна речовина забезпечує рН 5,5.
19. Композиція за п. 14, яка відрізняється тим, що вміст поверхнево-активної речовини становить 0,02 % (у відношенні маси до об'єму).
20. Композиція за п. 14, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,05 мг до 10 мг.
21. Композиція за п. 14, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,1 мг до 5,0 мг.
22. Композиція за п. 14, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,5 мг до 3,0 мг.
23. Композиція за п. 14, яка відрізняється тим, що антитілом проти CD3 є:
антитіло 28F11, яке включає варіабельну ділянку 1 (CDR1) важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 27, варіабельну ділянку 2 (CDR2) важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 28, варіабельну ділянку 3 (CDR3) важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 29, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 31, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 32;
антитіло 27Н5, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 27, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 28, CDR3 важкого ланіцога, що має амінокислотну послідовність SEQ ID NO: 29, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 31, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 32;
антитіло 23F10, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 34, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 36, SEQ ID NO: 39 або SEQ ID NO: 43, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 37, SEQ ID NO: 40 або SEQ ID NO: 42, та CDR3 легкого ланцюга, що має амінокислотну послідовнісіь SEQ ID NО: 38 або SEQ ID NO: 41;
антитіло 15С3, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 44, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30 або SEQ ID NO: 39, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 31 або SEQ ID NО: 46, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 45 або SEQ ID NО: 47;
Orthoclone ОКТ3, людське ОКТ3γ1 (НОКТ3γ1) або ChAglyCD3.
24. Фармацевтична композиція на основі антитіла проти CD3, яка містить такі суттєві інгредієнти:
a) ефективну кількість антитіла проти CD3 від 0,5 мг до 3,0 мг на дозу;
b) від 1 мг до 3мг ацетату натрію;
c) від 5 мг до 9 мг хлориду натрію;
d) від 0,1 мкг до 0,3 мкг полісорбату 80,
доведена до 1,0 мл за допомогою води.
25. Фармацевтична композиція за п. 24, яка містить 2,05 мг ацетату натрію, 7,31 мг хлориду натрію і 0,216 мкг полісорбату 80.
26. Фармацевтична композиція за п. 24, яка має рН 5,5.
27. Спосіб лікування автоімунного захворювання або запального розладу, який включає введення особі, яка потребує такого лікування, ефективної дози антитіла проти CD3, причому кількість антитіла на добову дозу становить від 0,1 мг до 5,0 мг, впродовж п'яти діб.
28. Спосіб за п. 27, який відрізняється тим, що згадана кількість становить від 0,5 мг до 3,0 мг.
29. Спосіб за п. 27, який відрізняється тим, що згадане введення здійснюють внутрішньовенним шляхом.
30. Спосіб лікування або запобігання відторгнення трансплантата в особи, який включає введення згаданій особі ефективної дози антитіла проти CD3 у кількості від 0,1 мг до 5,0 мг на дозу.
31. Спосіб за п. 30, який відрізняється тим, що згадане введення здійснюють внутрішньовенним шляхом.
32. Спосіб за п. 30, який відрізняється тим, що згадана ефективна доза антитіла проти CD3 забезпечує рівень виділення цитокінів, менший за 3 за шкалою рівнів токсичності ВООЗ.
33. Спосіб за п. 30, який відрізняється тим, що згадане введення здійснюють після трансплантації або одночасно з нею.
Текст
1. Фармацевтична композиція на основі антитіла проти CD3, яка містить такі суттєві інгредієнти: a) рН-буферну речовину, концентрація якої становить від 10 мМ до 50 мМ, яка забезпечує рН від 5,0 до 6,0, причому згадана рН-буферна речовина являє собою ацетат натрію; b) хлорид натрію, концентрація якого становить від 100 мМ до 140 мМ; c) 0,02 % (у відношенні маси до об'єму) поверхнево-активної речовини; та d) фармацевтично ефективну кількість антитіла проти CD3. 2. Композиція за п. 1, яка відрізняється тим, що концентрація хлориду натрію становить 125 мМ. 3. Композиція за п. 1, яка відрізняється тим, що згадана поверхнево-активна речовина являє собою іоногенну, аніоногенну або цвітеріонну поверхнево-активну речовину. 4. Композиція за п. 3, яка відрізняється тим, що згадана іоногенна поверхнево-активна речовина являє собою полісорбат. 5. Композиція за п. 4, яка відрізняється тим, що згаданий полісорбат являє собою полісорбат 80. 6. Композиція за п. 1, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,2 до 5,8. 7. Композиція за п. 1, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,4 до 5,6. 8. Композиція за п. 1, яка відрізняється тим, що рН-буферна речовина забезпечує рН 5,5. 2 (19) 1 3 NО: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 34, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 36, SEQ ID NO: 39 або SEQ ID NO: 43, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 37, SEQ ID NO: 40 або SEQ ID NO: 42, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 38 або SEQ ID NO: 41; антитіло 15С3, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 44, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30 або SEQ ID NO: 39, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 31 або SEQ ID NО: 46, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 45 або SEQ ID NО: 47; Orthoclone ОКТ3, людське ОКТ3γ1 (НОКТ3γ1) або ChAglyCD3. 14. Фармацевтична композиція на основі антитіла проти CD3, яка містить такі суттєві інгредієнти: a) рН-буферну речовину, яка містить ацетат натрію, концентрація якого становить 25 мМ, що забезпечує рН у діапазоні від 5,0 до 6,0; b) хлорид натрію, концентрація якого становить 125 мМ; c) поверхнево-активну речовину, яка містить полісорбат; та d) фармацевтично ефективну кількість антитіла проти CD3. 15. Композиція за п. 14, яка відрізняється тим, що згаданий полісорбат являє собою полісорбат 80. 16. Композиція за п. 14, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,2 до 5,8. 17. Композиція за п. 14, яка відрізняється тим, що рН-буферна речовина забезпечує діапазон рН від 5,4 до 5,6. 18. Композиція за п. 14, яка відрізняється тим, що рН-буферна речовина забезпечує рН 5,5. 19. Композиція за п. 14, яка відрізняється тим, що вміст поверхнево-активної речовини становить 0,02 % (у відношенні маси до об'єму). 20. Композиція за п. 14, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,05 мг до 10 мг. 21. Композиція за п. 14, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,1 мг до 5,0 мг. 22. Композиція за п. 14, яка відрізняється тим, що фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу від 0,5 мг до 3,0 мг. 23. Композиція за п. 14, яка відрізняється тим, що антитілом проти CD3 є: 92505 4 антитіло 28F11, яке включає варіабельну ділянку 1 (CDR1) важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 27, варіабельну ділянку 2 (CDR2) важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 28, варіабельну ділянку 3 (CDR3) важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 29, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 31, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 32; антитіло 27Н5, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 27, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 28, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 29, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 31, та CDR3 легкого ланцюга, що має амінокислотнупослідовність SEQ ID NO: 32; антитіло 23F10, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 34, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 36, SEQ ID NO: 39 або SEQ ID NO: 43, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 37, SEQ ID NO: 40 або SEQ ID NO: 42, та CDR3 легкого ланцюга, що має амінокислотну послідовнісіь SEQ ID NО: 38 або SEQ ID NO: 41; антитіло 15С3, яке включає CDR1 важкого ланцюга, що має амінокислотну послідовність SEQ ID NO: 33, CDR2 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 44, CDR3 важкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 35, CDR1 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 30 або SEQ ID NO: 39, CDR2 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 31 або SEQ ID NО: 46, та CDR3 легкого ланцюга, що має амінокислотну послідовність SEQ ID NО: 45 або SEQ ID NО: 47; Orthoclone ОКТ3, людське ОКТ3γ1 (НОКТ3γ1) або ChAglyCD3. 24. Фармацевтична композиція на основі антитіла проти CD3, яка містить такі суттєві інгредієнти: a) ефективну кількість антитіла проти CD3 від 0,5 мг до 3,0 мг на дозу; b) від 1 мг до 3мг ацетату натрію; c) від 5 мг до 9 мг хлориду натрію; d) від 0,1 мкг до 0,3 мкг полісорбату 80, доведена до 1,0 мл за допомогою води. 25. Фармацевтична композиція за п. 24, яка містить 2,05 мг ацетату натрію, 7,31 мг хлориду натрію і 0,216 мкг полісорбату 80. 26. Фармацевтична композиція за п. 24, яка має рН 5,5. 27. Спосіб лікування автоімунного захворювання або запального розладу, який включає введення особі, яка потребує такого лікування, ефективної дози антитіла проти CD3, причому кількість антиті 5 92505 6 ла на добову дозу становить від 0,1 мг до 5,0 мг, впродовж п'яти діб. 28. Спосіб за п. 27, який відрізняється тим, що згадана кількість становить від 0,5 мг до 3,0 мг. 29. Спосіб за п. 27, який відрізняється тим, що згадане введення здійснюють внутрішньовенним шляхом. 30. Спосіб лікування або запобігання відторгнення трансплантата в особи, який включає введення згаданій особі ефективної дози антитіла проти CD3 у кількості від 0,1 мг до 5,0 мг на дозу. 31. Спосіб за п. 30, який відрізняється тим, що згадане введення здійснюють внутрішньовенним шляхом. 32. Спосіб за п. 30, який відрізняється тим, що згадана ефективна доза антитіла проти CD3 забезпечує рівень виділення цитокінів, менший за 3 за шкалою рівнів токсичності ВООЗ. 33. Спосіб за п. 30, який відрізняється тим, що згадане введення здійснюють після трансплантації або одночасно з нею. Галузь, до якої належить винахід Цей винахід стосується дозування і композиції на основі антитіла проти CD3, а також способів застосування таких композицій та доз. Передумови створення винаходу Антитіла проти сигнальної молекули іпсилон CD3 рецепторного комплексу Т-клітин довели свою придатність як імуносупресори та для лікування автоімунних розладів. Таким чином, корисними були б поліпшені способи одержання антитіл проти CD3, способи очищення антитіл проти CD3 і фармацевтичні композиції, які містять антитіла проти CD3. Суть винаходу Цей винахід пропонує дозування і композицію на основі моноклональних антитіл, специфічно спрямованих проти CD3. Цей винахід пропонує також способи одержання моноклональних антитіл проти CD3 і способи очищення антитіл проти CD3. Фармацевтичні композиції на основі антитіла проти CD3, опис яких наводиться, містять pHбуферну речовину, ефективну у діапазоні від 3,0 до 6,2; сіль; поверхнево-активну речовину; і фармацевтично ефективну кількість антитіла проти CD3. Згадана сіль являє собою, наприклад, хлорид натрію; згаданою поверхнево-активною речовиною є, наприклад, іоногенна, аніоногенна або цвітеріонна поверхнево-активна речовина. Наприклад, поверхнево-активна речовина являє собою іоногенну поверхнево-активну речовину, таку як полісорбат, наприклад, полісорбат 80. Згадана pHбуферна речовина являє собою, наприклад, ацетат натрію. За деякими варіантами здійснення, pHбуферна речовина вибрана з-посеред цитрату натрію/лимонної кислоти і ацетату натрію/оцтової кислоти. pH-буферна речовина є ефективною у діапазоні від 10 мМ до 50 мМ. pH-буферна речовина, яку застосовують у композиціях, опис яких наведено, забезпечує діапазон pH у межах 5,0-6,0. Наприклад, pH-буферна речовина забезпечує діапазон pH у межах 5,2-5,8. За деякими варіантами здійснення, pH-буферна речовина забезпечує діа пазон pH у межах 5,4-5,6. Наприклад, pH-буферна речовина забезпечує pH приблизно 5,5. У композиціях, опис яких наведено, сіль присутня у діапазоні від 100 мМ до 140 мМ. Вміст поверхнево-активної речовини становить 0,02% (у відношенні масидо об'єму). Фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу у межах від 0,05 мг до 10 мг. За деякими варіантами здійснення, фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу у межах від 0,1 мг до 5,0 мг. Наприклад, фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу у межах від 0,5 мг до 3,0 мг. У композиціях на основі антитіла проти CD3, опис яких наведено, згаданим антитілом проти CD3 є, наприклад, 28F11, 27Н5, 23F10, 15С3, Orthoclone ОКТ3, людське ОКТ3 1 (НОКТ3 1) або ChAg1yCD3. Фармацевтичні композиції на основі антитіла проти CD3, запропоновані цим винаходом, містять pH-буферну речовину, яка містить ацетат натрію, ефективну у діапазоні від 3,0 до 6,2, хлорид натрію, поверхнево-активну речовину, яка містить полісорбат, і фармацевтично ефективну кількість антитіла проти CD3. Згаданим полісорбатом є, наприклад, полісорбат 80. pH-буферна речовина є ефективною у діапазоні від 10 мМ до 50 мМ. pHбуферна речовина, яку застосовують у композиціях, опис яких наведено, забезпечує діапазон pH у межах 5,0-6,0. Наприклад, pH-буферна речовина забезпечує діапазон pH у межах 5,2-5,8. За деякими варіантами здійснення, pH-буферна речовина забезпечує діапазон pH у межах 5,4-5,6. Наприклад, pH-буферна речовина забезпечує pH приблизно 5,5. У фармацевтичних композиціях, опис яких наведено, сіль є присутня у діапазоні від 100 мМ до 140 мМ. Вміст поверхнево-активної речовини становить 0,02% (у відношенні маси до об'єму). Фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість анти 7 тіла проти CD3 на дозу у межах від 0,05 мг до 10 мг. За деякими варіантами здійснення, фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу у межах від 0,1 мг до 5,0 мг. Наприклад, фармацевтично ефективною кількістю антитіла проти CD3 є така кількість, яка забезпечує кількість антитіла проти CD3 на дозу у межах від 0,5 мг до 3,0 мг. Антитілом проти CD3 є, наприклад, 28F11, 27Н5, 23F10, 15С3, Orthoclone OKT3, людське ОКТ3 1 (НОКТ3 1) або ChAglyCD3. За одним із варіантів здійснення композицій на основі антитіла проти CD3, запропонованих цим винаходом, фармацевтична композиція містить ефективну кількість антитіла проти CD3 на дозу у межах від 0,5 мг до 3,0 мг, ацетат натрію у межах від 1 мг до 3 мг, хлорид натрію у межах від 5 мг до 9 мг і полісорбат 80 у межах від 0,1 мкг до 0,3 мкг, за умови що об'єм композиції за допомогою води доводять до рівня 1,0 мл. Наприклад, фармацевтична композиція містить 2,05 мг ацетату натрію, 7,31 мг хлориду натрію і 0,216 мкг полісорбату 80. pH фармацевтичної композиції дорівнює, наприклад, 5,5. Цим винаходом запропоновані також способи лікування автоімунного захворювання або запального розладу у суб'єкта шляхом введення суб'єкту, який потребує цього, ефективної дози композиції на основі антитіла проти CD3 для забезпечення кількості антитіла проти CD3 на дозу у межах від 0,05 мг до 10 мг на добу впродовж періоду часу тривалістю п'ять днів. Наприклад, ефективною дозою антитіла проти CD3 є така доза, яка містить кількість антитіла проти CD3 на дозу у межах від 0,1 мг до 5,0 мг на добу впродовж періоду часу тривалістю п'ять днів. За варіантом, якому віддається перевага, ефективною дозою антитіла проти CD3 є така доза, яка містить кількість антитіла проти CD3 на дозу у межах від 0,5 мг до 3,0 мг на добу впродовж періоду часу тривалістю п'ять днів. За способами, опис яких наведено, композицію на основі антитіла проти CD3 вводять внутрішньовенним шляхом. Наприклад, композицію вводять шляхом безперервного внутрішньовенного вливання. Цим винаходом запропоновані також способи лікування або запобігання відторгнення трансплантату у суб'єкта шляхом введення згаданому суб'єкту, після або одночасно з трансплантатом, антитіла проти CD3 у ефективній дозі і підвищення у подальшому дози кожного дня доти, доки не буде досягнуто 50% або більшого рівня насичення TCRCD3, з подальшим введенням 5 добових доз, причому загальний курс лікування не повинен перевищувати восьми днів. За способами, опис яких наведено, композицію на основі антитіла проти CD3 вводять внутрішньовенним шляхом. Наприклад, композицію вводять шляхом безперервного внутрішньовенного вливання. За варіантом, якому віддається перевага, ефективна доза антитіла проти CD3 забезпечує рівень виділення цитокінів менший від 3 за шкалою токсичності ВООЗ (Всесвітня організація охорони здоров'я). Композиції на основі антитіла проти CD3, запропоновані цим винаходом, вводять у дозі у діа 92505 8 пазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній зпосеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. Прикладами моноклональних антитіл є 28F11, 27Н5, 23F10 та 15С3, опис яких наведено, а також Orthoclone OKT3, людське ОКТ3 1 (НОКТ3 1) та ChAglyCD3. За варіантом, якому віддається перевага, моноклональним антитілом є антитіло, яке зв'язується з тією самою антигенною детермінантою, що і 28F11, 27Н5, 23F10 або 15С3. За варіантом, якому також віддають перевагу, згадані антитіла є повністю людськими антитілами ("людські антитіла проти CD3" ("huCD3 антитіла")). Антитіло проти CD3 має одну або декілька з наведених нижче характеристик: антитіло зв'язується з СD3позитивними (CD3+) клітинами, але не з СD3негативними (CD3-) клітинами; антитіло проти CD3 індукує антигенну модуляцію, яка охоплює зміну (наприклад, зниження) рівня поверхневоклітинної експресії або активності CD3 чи Т-клітинного рецептора (TcR); антитіло проти CD3 пригнічує зв'язування мишачого анти-людського ОКТ3 моноклонального антитіла з Т-лімфоцитами; або антитіло проти CD3 зв'язує антигенну детермінанту CD3, яка повністю або частково включає амінокислотну послідовність EMGGITQTPYKVSISGT (ПОСЛІДОВНІСТЬ № 57). Антитіло проти CD3 конкурує з мишачим анти-СD3 антитілом ОКТ3 за зв'язування з CD3, і піддання дії антитіла проти CD3 видаляє або маскує CD3 та/або TcR без негативної дії на поверхневоклітинну експресію CD2, CD4 або CD8. Пригнічення зв'язування мишачого антилюдського моноклонального антитіла ОКТ3 з Тлімфоцитом визначається як зменшення здатності мишачого антитіла ОКТ3 до утворення комплексу з CD3 на клітинній поверхні Т-лімфоцита. Антитіло проти CD3 включає варіабельну ділянку важкого ланцюга, що має амінокислотну послідовність, представлену ПОСЛІДОВНОСТЯМИ № 2, № 6, № 10 або № 22, і варіабельну ділянку легкого ланцюга, яка має амінокислотну послідовність, представлену ПОСЛІДОВНОСТЯМИ № 4, № 8, № 16-20 або № 25-26. За варіантом, якому віддається перевага, три гіперваріабельні ділянки (CDR) важкого ланцюга включають амінокислотну послідовність, яка є щонайменше на 90%, 92%, 95%, 97%, 98%, 99% або більше ідентичною послідовності, вибраній з групи, яку складають GYGMH (ПОСЛІДОВНІСТЬ №27); VIWYDGSKKYYVDSVKG (ПОСЛІДОВНІСТЬ №28); QMGYWHFDL (ПОСЛІДОВНІСТЬ №29); SYGMH (ПОСЛІДОВНІСТЬ №33); IIWYDGSKKNYADSVKG (ПОСЛІДОВНІСТЬ № 34); GTGYNWFDP (ПОСЛІ 9 ДОВНІСТЬ № 35) та AIWYNGRKQDYADSVKG (ПОСЛІДОВНІСТЬ №44), і легкий ланцюг з трьома гіперваріабельними ділянками, які включають амінокислотну послідовність, яка є щонайменше на 90%, 92%, 95%, 97%, 98%, 99% або більше ідентичною послідовності, вибраній з групи, яку складають амінокислотна послідовність RASQSVSSYLA (ПОСЛІДОВНІСТЬ № 30); DASNRAT (ПОСЛІДОВ-НІСТЬ № 31); QQRSNWPPLT (ПОСЛІДОВНІСТЬ № 32); RASQSVSSSYLA (ПОСЛІДОВНІСТЬ № 36); GASSRAT (ПОСЛІДОВНІСТЬ № 37); QQYGSSPIT (ПОСЛІДОВНІСТЬ № 38); RASQGISSALA (ПОСЛІДОВНІСТЬ №39); YASSLQS (ПОСЛІДОВНІСТЬ № 40); QQYYSTLT (ПОСЛІДОВНІСТЬ № 41); DASSLGS (ПОСЛІДОВНІСТЬ №42); WASQGISSYLA (ПОСЛІДОВНІСТЬ № 43); QQRSNWPWT (ПОСЛІДОВНІСТЬ №45); DASSLES (ПОСЛІДОВНІСТЬ №46) та QQFNSYPIT (ПОСЛІДОВНІСТЬ № 47). Згадане антитіло зв'язує CD3. Антитіло проти CD3 за цим винаходом демонструє щонайменше дві або декілька (тобто дві або декілька, три або декілька, чотири або декілька, п'ять або декілька, шість або декілька, сім або декілька, вісім або декілька, дев'ять або декілька, десять або декілька, одинадцять або декілька) з наведених нижче характеристик: антитіло містить варіабельну ділянку важкого ланцюга (VH), яка кодується послідовністю людського VH-гена DP50 зародкового типу або нуклеїновокислотною послідовністю, яка є гомологічною до послідовності людського VH-гена DP50 зародкового типу; антитіло містить варіабельну ділянку легкого ланцюга (VL), яка кодується послідовністю людського VLгена L6 зародкового типу або нуклеїновокислотною послідовністю, яка є гомологічною до послідовності людського VL-гена L6 зародкового типу; антитіло містить VL, яка кодується послідовністю людського VL-гена L4/18a зародкового типу або нуклеїновокислотною послідовністю, яка є гомологічною до послідовності людського VL-гена L4/18a зародкового типу; антитіло включає гіперваріабельну ділянку 1 (CDR 1) VH, яка містить амінокислотну послідовність YGMH (ПОСЛІДОВНІСТЬ № 58); антитіло включає гіперваріабельну ділянку 2 (CDR 2) VH, яка містить амінокислотну послідовність DSVKG (ПОСЛІДОВНІСТЬ № 59); антитіло включає гіперваріабельну ділянку 2 (CDR 2) VH, яка містить амінокислотну послідовність IWYX1GX2X3X4X5YX6DSVKG (ПОСЛІДОВНІСТЬ № 60); антитіло включає гіперваріабельну ділянку 3 (CDR 3) VH, яка містить амінокислотну послідовність XAXBGYXCXDFDXE (ПОСЛІДОВНІСТЬ № 61); антитіло включає гіперваріабельну ділянку 3 (CDR 3) VH, яка містить амінокислотну послідовність GTGYNWFDP (ПОСЛІДОВНІСТЬ № 62) або амінокислотну послідовність QMGYWHFDL (ПОСЛІДОВНІСТЬ № 63); антитіло включає амінокислотну послідовність VTVSS (ПОСЛІДОВНІСТЬ № 64) у положенні, яке є С-кінцевим відносно гіперваріабельної ділянки 3 (CDR 3), причому згадане положення знаходиться у межах варіабельної ділянки, яка є С-кінцевою відносно гіперваріабельної ділянки 3 (CDR 3); антитіло включає амінокислотну послідовність GTLVTVSS (ПОСЛІДОВНІСТЬ № 65) у 92505 10 положенні, яке є С-кінцевим відносно гілерваріабельної ділянки 3 (CDR 3), причому згадане положення знаходиться у межах варіабельної ділянки, яка є С-кінцевою відносно гіперваріабельної ділянки 3 (CDR 3); антитіло включає амінокислотну послідовність WGRGTLVTVSS (ПОСЛІДОВНІСТЬ № 66) у положенні, яке є С-кінцевим відносно гіперваріабельної ділянки 3 (CDR 3), причому згадане положення знаходиться у межах варіабельної ділянки, яка є С-кінцевою відносно гіперваріабельної ділянки 3 (CDR 3); антитіло зв'язує антигенну детермінанту, яка повністю або частково включає амінокислотну послідовність EMGGITQTPYKVSISGT (ПОСЛІДОВНІСТЬ № 57); і антитіло включає мутацію у важкому ланцюзі на залишку амінокислоти у положенні 234, 235, 265 або 297 або їх комбінаціях і де виділення цитокінів з Т-клітини у присутності згаданого антитіла зменшується, порівняно з виділенням цитокінів з Тклітини у присутності антитіла, яке не включає мутації у важкому ланцюзі у положенні 234, 235, 265 або 297 або їх комбінаціях. Номенклатура залишків важкого ланцюга, наведена у цьому описі, відповідає номенклатурі Індексу Європейської Спільноти (дивись Кебот (Kabat) та інші, "Proteins of Immunological Interest", US Dept. of Health & Human. Services (1983)), як показано, наприклад, у патентах США №№ 5,624,821 та 5,648,260, які у повному обсязі включено до цього опису, шляхом посилання. Антитіло проти CD3 може містити амінокислотну мутацію. Згадана мутація, як правило, знаходиться у межах константної ділянки. Наслідком мутації є антитіло, яке має змінену ефекторну функцію. Ефекторна функція антитіла змінюється шляхом зміни, тобто збільшення або зменшення, спорідненості згаданого антитіла до ефекторної молекули, наприклад, рецептора Fc-фрагмента або складової комплементу. Наслідком згаданої мутації є, наприклад, антитіло, яке є здатним до зменшення виділення цитокінів із Т-клітини. Згадана мутація знаходиться, наприклад, у межах важкого ланцюга на залишку амінокислоти 234, 235, 265 або 297 чи їх комбінаціях. За варіантом, якому віддається перевага, наслідком згаданої мутації є залишок аланіну у положенні 234, 235, 265 чи 297 або залишок глутамату у положенні 235, або їх комбінація. Термін "цитокін" означає усі людські цитокіни, відомі у цій галузі, які зв'язують позаклітинні рецептори, експресовані на поверхні клітини і, тим самим, модулюють функцію клітини, у > тому числі (але без обмеження) IL-2 (інтерлейкін-2), IFN (гамма-інтерферон), TNF-α (фактор некрозу пухлин), IL-4, IL-5, IL-6, IL-9, IL-10 та IL-13. За варіантом, якому віддається перевага, антитіло проти CD3, запропоноване цим винаходом, містить одну або декілька мутацій, які запобігають опосередкованому константною ділянкою важкого ланцюга виділенню одного або декількох цитокінів in vivo. Повністю людські антитіла проти CD3 за цим винаходом включають, наприклад, мутацію L234L235 A234E235 на ділянці Fc, завдяки чому виділення цитокінів, у разі піддання дії антитіла проти CD3, значно зменшується або припиняється. Як 11 92505 12 описано нижче у Прикладі 4, мутація L234L235 A234E235 на ділянці Fc антитіл проти CD3 за цим винаходом зменшує або припиняє виділення цитокінів у разі піддання антитіл проти CD3 дії людських лейкоцитів, у той час як описані нижче мутації підтримують здатність до значного виділення цитокінів. Наприклад, значне зменшення виділення цитокінів виявляється при порівнянні виділення цитокінів у разі піддання дії антитіла проти CD3, яке має мутацію L234L235 A234E235 на ділянці Fc, з рівнем виділення цитокінів у разі піддання дії іншого антитіла проти CD3, яке має одну або декілька мутацій, опис яких наведено нижче. До числа інших мутацій на Fc-фрагменті належать, наприклад, L234L235 A234A235, L235 E235, N297 A297 та D265 A265. За альтернативним варіантом, антитіло проти CD3 кодується нуклеїновою кислотою, яка включає одну або декілька мутацій, які замінюють залишок нуклеїнової кислоти на залишок нуклеїнової кислоти зародкового типу. Словосполучення "за лишок нуклеїнової кислоти зародкового типу" означає залишок нуклеїнової кислоти, який є природно присутнім у гені зародкового типу, який кодує константну або варіабельну ділянку. Таким чином, антитіла за цим винаходом включають одну або декілька мутацій, які замінюють нуклеїнову кислоту на залишок нуклеїнової кислоти зародкового типу. Гени антитіла зародкового типу включають, наприклад, DP50 (номер депонування: IMGT/EMBL/GenBank/DDBJ:L06618), L6 (номер депонування: IMGT/EMBL/GenBank/DDBJ:X01668) та L4/18a (номер депонування: EMBL/GenBank/DDBJ:Z00006). Важкий ланцюг huCD3 антитіла є похідним Vгена (ген варіабельної ділянки імуноглобуліну) зародкового типу, наприклад гена DP50 зародкового типу. Нуклеїновокислотні і амінокислотні послідовності гена DP50 зародкового типу включають, наприклад, нуклеїновокислотні і амінокислотні послідовності, наведені нижче: huCD3 антитіла включають варіабельну ділянку важкого ланцюга (VH), яка кодується послідовністю людського VH-гена DP50 зародкового типу. Послідовність VH-гена DP50 зародкового типу представлена, наприклад, ПОСЛІДОВНІСТЮ № 48 на Фіг.5. huCD3 антитіла за цим винаходом включають варіабельну ділянку важкого ланцюга (VH), яка кодується нуклеїновокислотною послідовністю, яка є щонайменше на 80% гомологічною до послідовності VH-гена DP50 зародкового типу. За варіантом, якому віддається перевага, згадана нуклеїновокислотна послідовність є щонайменше на 90%, 95%, 96%, 97% гомологічною до послідовності VH-гена DP50 зародкового типу, а за варіантом, якому віддається більша перевага, щонайменше на 98%, 99% гомологічною до послідовності VHгена DP50 зародкового типу. VH huCD3 антитіла є щонайменше на 80% гомологічною до амінокислотної послідовності VH, яка кодується послідовністю VH-гена DP50 зародкового типу. За варіантом, якому віддається перевага, згадана амінокислотна послідовність VH huCD3 антитіла є щонайменше на 90%, 95%, 96%, 97% гомологічною до амінокислотної послідовності, яка кодується послідовністю VH-гена DP50 зародкового типу, а за варіантом, якому віддається більша перевага, щонайменше на 98%, 99% гомологічною до послідовності, яка кодується послідовністю VH-гена DP50 зародкового типу. huCD3 антитіла включають також варіабельну ділянку легкого ланцюга (VL), яка кодується послідовністю людського VL-гена L6 або L4/18a зародкового типу. Послідовність людського VL-гена L6 зародкового типу представлена, наприклад, ПОСЛІДОВНІСТЮ № 56 на Фіг.6, а послідовність людського VL-гена L4/18а зародкового типу представлена, наприклад, ПОСЛІДОВНІСТЮ № 53 на Фіг.7. За альтернативним варіантом, huCD3 антитіла включають варіабельну ділянку легкого ланцюга (VL), яка кодується нуклеїновокислотною послідовністю, яка є щонайменше на 80% гомологічною до послідовності VL-гена L6 або L4/18a зародкового типу. За варіантом, якому віддається перевага, згадана нуклеїновокислотна послідовність є щонайменше на 90%, 95%, 96%, 97% гомологічною до послідовності VL-гена L6 або L4/18a зародкового типу, а за варіантом, якому віддається більша перевага, щонайменше на 98%, 99% гомологічною до послідовності VL-гена L6 або L4/18a зародкового типу. VL huCD3 антитіла є щонайменше на 80% гомологічною до амінокислотної послідовності VL, яка кодується послідовністю VL-гена L6 або L4/18a зародкового типу. За варіантом, якому віддається перевага, згадана амінокислотна послідовність VL huCD3 антитіла є щонайменше на 90%, 95%, 96%, 13 97% гомологічною до амінокислотної послідовності, яка кодується послідовністю VL-гена L6 або L4/18a зародкового типу, а за варіантом, якому віддається більша перевага, щонайменше на 98%, 99% гомологічною до послідовності, яка кодується послідовністю VL-гена L6 або L4/18a зародкового типу. huCD3 антитіла мають, наприклад, частково консервативні амінокислотні послідовності, які є похідними DP50 зародкового типу. Наприклад, гіперваріабельна ділянка 1 (CDR 1) huCD3 антитіл за цим винаходом має щонайменше суміжну амінокислотну послідовність YGMH (ПОСЛІДОВНІСТЬ № 58). Гіперваріабельна ділянка 2 (CDR 2) антитіл проти CD3 включає, наприклад, принаймні суміжну амінокислотну послідовність DSVKG (ПОСЛІДОВНІСТЬ № 59). Наприклад, гіперваріабельна ділянка 2 (CDR 2) включає суміжну амінокислотну послідовність IWYX1GX2X3X4X5YX6DSVKG (ПОСЛІДОВНІСТЬ № 60), де Х1 Х2, Х3, Χ4, Χ5 та Х6 представляють будь-яку амінокислоту. Наприклад, Х1 Х2, Х3 та Х4 є гідрофільними амінокислотами. У деяких антитіл проти CD3 за цим винаходом Χ1 є аспарагіном або аспартатом, Х2 є аргініном або серином, Х3 є лізином або аспарагіном, Х4 є лізином або глутаміном, Х5 є аспартатом, аспарагіном або тирозином і/або Х6 є валіном або аланіном. Наприклад, VH CDR 2 містить амінокислотну послідовність, вибрану з групи, яка складається з AIWYNGRKQDYADSVKG (ПОСЛІДОВНІСТЬ №69), IIWYDGSKKNYADSVKG (ПОСЛІДОВНІСТЬ №70), VIWYDGSKKYYVDSVKG (ПОСЛІДОВНІСТЬ №71) та VIWYDGSNKYYADSVKG (ПОСЛІДОВНІСТЬ № 72). Гіперваріабельна ділянка 3 (CDR 3) антитіл проти CD3 містить, наприклад, принаймні суміжну амінокислотну послідовність XAXBGYXCXDFDXE (ПОСЛІДОВНІСТЬ № 61), де ХА, ХВ, ХС, XD та ХЕ представляють будь-яку амінокислоту. У деяких антитіл проти CD3 за цим винаходом ХА та ХВ є нейтральними амінокислотами, XD є ароматичною амінокислотою і/або ХЕ є гідрофобною амінокислотою. Наприклад, ХА є гліцином або глутаміном, ХВ є треоніном або метіоніном, ХС є аспарагіном або триптофаном, XD є триптофаном або гістидином і/або ХЕ є проліном або лейцином. Наприклад, CDR 3 містить суміжну амінокислотну послідовність GTGYNWFDP (ПОСЛІДОВНІСТЬ № 62) або суміжну амінокислотну послідовність QMGYWHFDL (ПОСЛІДОВНІСТЬ № 63). Антитіла проти CD3 включають каркасну ділянку 2 (FRW 2), яка містить амінокислотну послідовність WVRQAPGKGLEWV (ПОСЛІДОВНІСТЬ № 73). Антитіла проти CD3 за цим винаходом включають каркасну ділянку 3 (FRW 3), яка містить амінокислотну послідовність RFTISRDNSKNTLYLQMNSLRAEDTAVYYCA (ПОСЛІДОВНІСТЬ № 74). Деякі антитіла проти CD3 містять суміжну амінокислотну послідовність VTVSS (ПОСЛІДОВНІСТЬ № 64) у положенні, яке є С-кінцевим відносно гіперваріабельної ділянки 3 (CDR 3). Наприклад, антитіло містить суміжну амінокислотну послідовність GTLVTVSS (ПОСЛІДОВНІСТЬ № 92505 14 65) у положенні, яке є С-кінцевим відносно гіперваріабельної ділянки 3 (CDR 3). Інші антитіла проти CD3 містять суміжну амінокислотну послідовність WGRGTLVTVSS (ПОСЛІДОВНІСТЬ № 66) у положенні, яке є С-кінцевим відносно гіперваріабельної ділянки 3 (CDR 3). Залишок аргініну у ПОСЛІДОВНОСТІ № 66 є показаним, наприклад, у VH послідовностях людського антитіла 28F11 проти CD3 (ПОСЛІДОВНІСТЬ №2) і людського антитіла 23F10 проти CD3 (ПОСЛІДОВНІСТЬ № 6). За іншим аспектом, винахід пропонує способи лікування, запобігання або полегшення симптому імунопатології шляхом введення суб'єкту композиції на основі антитіла проти CD3. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі у межах від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі у межах від 0,1 мг/доба до 5,0 мг/доба, і за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі у межах від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять хворому, який страждає на запальну хворобу кишечнику, неспецифічний виразковий коліт, хворобу Крону, розсіяний склероз, ревматоїдний артрит або діабет типу І, або є схильним до цих захворювань. Композицію вводять, наприклад, внутрішньовенним шляхом. Передбачаються інші шляхи введення. Наприклад, композиції на основі антитіла проти CD3 вводять підшкірним, пероральним, парентеральним, назальним, внутрішньом'язовим шляхом або будь-якою комбінацією цих шляхів введення. За іншим аспектом, цим винаходом запропоновані способи лікування або запобігання відторгнення трансплантату шляхом введення суб'єкту антитіла проти CD3 у дозі у межах від 0,05 мг/доба до 10 мг/доба після трансплантування і підвищення кожного подальшого дня згаданої дози доти, доки не буде досягнуто 50% або більшого рівня насичення TCR-CD3, з подальшим введенням 5 добових доз, причому загальний курс лікування не повинен перевищувати восьми днів. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі у межах від 0,1 мг/доба до 5,0 мг/доба, і за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі у межах від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 15 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 застосовують для лікування або запобігання відторгнення нирок після трансплантації органу або тканини. Згадану композицію вводять із профілактичною метою (наприклад, перед гострим кризом відторгнення для запобігання кризу) та/або згадану композицію застосовують як лікарський засіб проти гострого кризу відторгнення після трансплантації. Композицію вводять, наприклад, внутрішньовенним шляхом. Передбачаються інші шляхи введення. Наприклад, композиції на основі антитіла проти CD3 вводять підшкірним, пероральним, парентеральним, назальним, внутрішньом'язовим шляхом або будь-якою комбінацією цих шляхів введення. Композиції на основі антитіла проти CD3 за цим винаходом зберігають у придатних контейнерах, наприклад, флаконах, таким чином, що доза композиції на основі антитіла проти CD3 на контейнер знаходиться у діапазоні від 1 мг/контейнер до 10 мг/контейнер. Наприклад, доза композиції на основі антитіла проти CD3 на контейнер знаходиться у діапазоні 2-5 мг/контейнер. За варіантом, якому віддається перевага, доза на контейнер знаходиться у діапазоні 3,5-4,5 мг/контейнер, наприклад, доза на контейнер дорівнює 4 мг/контейнер. Факультативно пацієнту додатково вводять другий препарат, наприклад (але без обмеження), протизапальні сполуки або імуносупресорні сполуки. До числа придатних сполук належить (але без обмеження) метотрексат, циклоспорин А (з включенням, наприклад, мікроемульсії циклоспорину), такролімус (tacrolimus), кортикостероїдні препарати, статини, інтерферони типу І, ремікад (Remicade (інфліксімаб (Infliximab)), енбрел (Enbrel (етанерцепт (Etanercept)) та гуміра (Humira (адалімумаб (Adalimumab)). Наприклад, суб'єктам, хворим на діабет типу І або латентний автоімунний діабет дорослих (LADA), також вводять другий препарат, наприклад, GLP-1 (глюкагоноподібний пептид), або сполуку, яка переводить бета-клітини у стан спокою (тобто сполуку, яка знижує або іншим чином пригнічує виділення інсуліну, наприклад, відкривачі калієвих каналів). За іншим аспектом, винахід пропонує способи очищення антитіла проти CD3 засобами афінної хроматографії, іонообмінної хроматографії та гідроксиапатитної хроматографії. Наприклад, афінною хроматографією є хроматографія білка А. Іонообмінною хроматографією є, наприклад, аніонообмінна хроматографія. Короткий опис фігур Фіг.1A-1D - ряд зображень нуклеотидної послідовності і амінокислотних послідовностей варіабельних ділянок легких ланцюгів і варіабельних ділянок важких ланцюгів huCD3 антитіла 28F11, де гіперваріабельні ділянки виділені рамками. Фіг.2A-2D - ряд зображень нуклеотидної послідовності і амінокислотних послідовностей варіабельних ділянок легких ланцюгів і варіабельних ділянок важких ланцюгів huCD3 антитіла 23F10. 92505 16 Фіг.3А-3D - ряд зображень нуклеотидної послідовності і амінокислотних послідовностей варіабельних ділянок легких ланцюгів і варіабельних ділянок важких ланцюгів huCD3 антитіла 27Н5. На Фіг.3Е представлено впорядковане розміщення п'яти легких ланцюгів клону 27Н5, де зірочка (*) означає консервативну амінокислоту; двокрапка (:) означає консервативну мутацію; крапка (.) означає напівконсервативну мутацію. Фіг.4A-4D - ряд зображень нуклеотидної послідовності і амінокислотних послідовностей варіабельних ділянок легких ланцюгів і варіабельних ділянок важких ланцюгів huCD3 антитіла 15С3. Фіг.5 - впорядковане розміщення, яке відображає варіабельні ділянки важких ланцюгів huCD3 антитіл 15С3, 27Н5 та 28F11, а також послідовність DP50 зародкового типу, послідовність людського J-фрагмента 5-02 важкого ланцюга і послідовність людського J-фрагмента 2 важкого ланцюга. Для кожної послідовності вказані гіперваріабельні ділянки. Фіг.6 - впорядковане розміщення, яке відображає варіабельні ділянки VkIII huCD3 антитіл 15С3 (варіабельна ділянка 1 легкого ланцюга, тобто "VL1") та 28F11, а також послідовність L6 зародкового типу, послідовність людського J-фрагмента каппа 4 і послідовність людського J-фрагмента каппа 1. Для кожної послідовності вказані гіперваріабельні ділянки. Фіг.7 - впорядковане розміщення, яке відображає варіабельні ділянки VkI VL2 huCD3 антитіл 15С3 (варіабельна ділянка 2 легкого ланцюга, тобто "VL2") та 27Н5, а також послідовність L4/18a зародкового типу, послідовність людського Jфрагмента каппа 4 і послідовність людського Jфрагмента каппа 5. Для кожної послідовності вказані гіперваріабельні ділянки. Фіг.8 - впорядковане розміщення, яке відображає варіабельні ділянки VkII VL1 huCD3 антитіла 27Н5 та DPK22, а також послідовність людського J-фрагмента каппа 5. Для кожної послідовності вказані гіперваріабельні ділянки. Докладний опис Цей винахід пропонує композиції і дозування моноклональних антитіл, наприклад, повністю людських моноклональних антитіл, специфічних проти ланцюга CD3 типу іпсилон (CD3 ). Повністю людські антитіла за цим винаходом називають huCD3 антитілами. Композиції за цим винаходом мають pH у межах від 3,0 до 7,0. За варіантом, якому віддається перевага, композиція має pH у межах від 5,0 до 6,0, і за варіантом, якому віддається більша перевага, композиція має pH у межах від 5,2 до 5,8, і за варіантом, якому віддається найбільша перевага, композиція має pH у межах від 5,4 до 5,6. Наприклад, за одним із варіантів здійснення, композиція має pH 5,5. Антитіла проти CD3 за цим винаходом зв'язуються з CD3, який повністю або частково містить амінокислотні залишки від положення 27 до положення 43 іпсилон-субодиниці процесованого людського CD3 (тобто без лідерної послідовності). Амінокислотна послідовність іпсилон-субодиниці людського CD3 представлена, наприклад, номе 17 рами депонування GenBank NP_000724; ААА52295; Р07766; А32069; САА27516; та ААН49847. Наприклад, антитіло проти CD3 зв'язує антигенну детермінанту CD3, яка повністю або частково містить амінокислотну послідовність EMGGITQTPYKVSISGT (ПОСЛІДОВНІСТЬ № 57). Зразковим huCD3 моноклональним антитілом, яке зв'язується з цією антигенною детермінантою, є антитіло 28F11, опис якого наведено. Антитіло 28F11 включає варіабельну ділянку важкого ланцюга (ПОСЛІДОВНІСТЬ № 2), яке кодується нуклеїновокислотною послідовністю, яка представлена нижче ПОСЛІДОВНІСТЮ № 1, і варіабельну ділянку легкого ланцюга (ПОСЛІДОВНІСТЬ № 4), яка кодується нуклеїновокислотною послідовністю, яка представлена ПОСЛІДОВНІСТЮ № 3 (Фіг.1A-1D). Амінокислоти, які входять до складу гіперваріабельних ділянок (CDR), як визначено Чотья (Chothia) та іншими, 1989, Е.А. Кебот (Е.А. Kabat) та іншими, 1991, виділені рамками на Фіг.1В та Фіг.1D і Фіг.5 та Фіг.6). (Дивись Чотья К. (Chothia С.) та інші, Nature 342:877-883 (1989); Кебот Е.А. (Kabat Е.А.) та інші, Sequences of Proteins of Immunological Interest, 5-е видання, US Department of Health and Human Services, US Government Printing Office (1991)). Гіперваріабельні ділянки важкого ланцюга антитіла 28F11 мають наведені нижче послідовності: GYGMH (ПОСЛІДОВНІСТЬ № 27), VIWYDGSKKYYVDSVKG (ПОСЛІДОВНІСТЬ № 28) та QMGYWHFDL (ПОСЛІДОВНІСТЬ № 29). Гіперваріабельні ділянки легкого ланцюга антитіла 28F11 мають наведені нижче послідовності: RASQSVSSYLA (ПОСЛІДОВНІСТЬ № 30), DASNRAT (ПОСЛІДОВНІСТЬ № 31) та QQRSNWPPLT (ПОСЛІДОВНІСТЬ № 32). Як показано на Фіг.2A-2D, антитіло 23F10 включає варіабельну ділянку важкого ланцюга (ПОСЛІДОВНІСТЬ № 6), яка кодується нуклеїновокислотною послідовністю, яка представлена ПОСЛІДОВНІСТЮ № 5, і варіабельну ділянку легкого ланцюга (ПОСЛІДОВНІСТЬ № 8), яка кодується нуклеїновокислотною послідовністю, яка представлена ПОСЛІДОВНІСТЮ № 7. Амінокислоти, - які входять до складу гіперваріабельних ділянок, як визначено Чотья (Chothia) та іншими, 1989, Е.А. Кебот (Е.А. Kabat) та іншими, 1991, виділені рамками на Фіг.2В, Фіг.2D. Гіперваріабельні ділянки важкого ланцюга антитіла 23F10 мають наведені нижче послідовності: GYGMH (ПОСЛІДОВНІСТЬ № 27), VIWYDGSKKYYVDSVKG (ПОСЛІДОВНІСТЬ №28) та QMGYWHFDL (ПОСЛІДОВНІСТЬ № 29). Гіперваріабельні ділянки легкого ланцюга антитіла 23F10 мають наведені нижче послідовності: RASQSVSSYLA (ПОСЛІДОВНІСТЬ № 30), DASNRAT (ПОСЛІДОВНІСТЬ № 31) та QQRSNWPPLT (ПОСЛІДОВНІСТЬ № 32). Як показано на Фіг.3A-3D, антитіло 27Н5 включає варіабельну ділянку важкого ланцюга (ПОСЛІДОВНІСТЬ № 10), яка кодується нуклеїновокислотною послідовністю, яка представлена ПОСЛІДОВНІСТЮ № 9, і варіабельну ділянку легкого ланцюга, вибрану з-посеред амінокислотних послідовностей, представлених ПОСЛІДОВНОСТЯМИ № 16-20, які кодуються нуклеїновокислотними послідовностями, які представлені ПОСЛІ 92505 18 ДОВНОСТЯМИ № 11-15. Амінокислоти, які входять до складу гіперваріабельних ділянок, як визначено Чотья (Chothia) та іншими, 1989, Е.А. Кебот (Е.А. Kabat) та іншими, 1991, виділені рамками на Фіг.3В, Фіг.3D, Фіг.5 та Фіг.7-8. Гіперваріабельні ділянки важкого ланцюга антитіла 27Н5 мають наведені нижче послідовності: SYGMH (ПОСЛІДОВНІСТЬ № 33), IIWYDGSKKNYADSVKG (ПОСЛІДОВНІСТЬ № 34) та GTGYNWFDP (ПОСЛІДОВНІСТЬ № 35). Гіперваріабельні ділянки легкого ланцюга антитіла 27Н5 мають наведені нижче послідовності: RASQSVSSSYLA (ПОСЛІДОВНІСТЬ № 36); GASSRAT (ПОСЛІДОВНІСТЬ № 37); QQYGSSPIT (ПОСЛІДОВНІСТЬ № 38); RASQGISSALA (ПОСЛІДОВНІСТЬ № 39); YASSLQS (ПОСЛІДОВНІСТЬ № 40); QQYYSTLT (ПОСЛІДОВНІСТЬ №41); DASSLGS (ПОСЛІДОВНІСТЬ №42) та WASQGISSYLA (ПОСЛІДОВНІСТЬ № 43). Як показано на Фіг.4A-4D, антитіло 15С3 включає варіабельну ділянку важкого ланцюга (ПОСЛІДОВНІСТЬ № 22), яка кодується нуклеїновокислотною послідовністю, яка представлена ПОСЛІДОВНІСТЮ № 21, і варіабельну ділянку легкого ланцюга, вибрану з-посеред амінокислотних послідовностей, представлених ПОСЛІДОВНОСТЯМИ № 25-26, які кодуються нуклеїновокислотними послідовностями, які представлені ПОСЛІДОВНОСТЯМИ № 23-24. Амінокислоти, які входять до складу гіперваріабельної ділянки, як визначено Чотья (Chothia) та іншими, 1989, Е.А. Кебот (Е.А. Kabat) та іншими, 1991, виділені рамками на Фіг.4В, Фіг.4D і Фіг.5-7. Гіперваріабельні ділянки важкого ланцюга антитіла 15С3 мають наведені нижче послідовності: SYGMH (ПОСЛІДОВНІСТЬ № 33), AIWYNGRKQDYADSVKG (ПОСЛІДОВНІСТЬ №44) та GTGYNWFDP (ПОСЛІДОВНІСТЬ № 35). Гіперваріабельні ділянки легкого ланцюга антитіла 15С3 мають наведені нижче послідовності: RASQSVSSYLA (ПОСЛІДОВНІСТЬ №30); DASNRAT (ПОСЛІДОВНІСТЬ №31); QQRSNWPWT (ПОСЛІДОВНІСТЬ № 45); RASQGISSALA (ПОСЛІДОВНІСТЬ № 39); DASSLES (ПОСЛІДОВНІСТЬ № 46); QQFNSYPIT (ПОСЛІДОВНІСТЬ № 47). Антитіла проти CD3 за цим винаходом включають також антитіла, які містять амінокислотну послідовність варіабельної ділянки важкого ланцюга, яка є щонайменше на 90%, 92%, 95%, 97%, 98%, 99% або більше ідентичною до амінокислотної послідовності, представленої ПОСЛІДОВНІСТЮ № 2, № 6, № 10 або № 22, і/або амінокислотну послідовність варіабельної ділянки легкого ланцюга, яка є щонайменше на 90%, 92%, 95%, 97%, 98%, 99% або більше ідентичною до амінокислотної послідовності, представленої ПОСЛІДОВНІСТЮ № 4, № 8, № 16-20 або № 25-26. За альтернативним варіантом, моноклональним антитілом є антитіло, яке зв'язує ту саму антигенну детермінанту, що і 28F11, 27Н5, 23F10 або 15С3. У разі відсутності інших визначень, наукові та технічні терміни, що вживаються у зв'язку з цим винаходом, будуть мати значення, які традиційно розуміються пересічними фахівцями у цій галузі. 19 На додаток до цього, якщо тільки іншого не потребує контекст, терміни у однині будуть включати множину, а терміни у множині будуть включати однину. Взагалі, умовні позначення, що вживаються у зв'язку з культурами клітин і тканин, молекулярною біологією та хімією білків і оліго- або полінуклеотидів, а також гібридизацією та методиками, опис яких наводиться, є добре відомими і традиційно вживаними у цій галузі. Для одержання рекомбінантної ДНК, синтезу олігонуклеотидів, культивування і трансформування тканин застосовують стандартні методи (наприклад, електропорацію, ліпофекцію). Ферментативні реакції і методи очищення здійснюють за рекомендаціями виробника або за традиційними методами, прийнятими у цій галузі або описаними у цьому описі. Вищезгадані способи і процедури здійснюють, як правило, за традиційними методиками, добре відомими у цій галузі, та за описом у різних загальних і більш конкретніших джерелах, на які посилаються і які обговорюються у цьому описі. Дивись, наприклад, Сембрук (Sambrook) та інші, Molecular Cloning: A Laboratory Manual (2-е видання, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1989)). Термінологія, вживана у зв'язку з аналітичною хімією, хімією органічного синтезу, медичною і фармацевтичною хімією та лабораторними процедурами і методами, опис яких наведено, являє собою термінологію, добре відому і широко вживану у цій галузі. Для проведення хімічного синтезу, здійснення хімічних аналізів, виготовлення фармацевтичних препаратів, лікарських форм, їх доставки та лікування хворих застосовують стандартні методи. Слід розуміти, що наведені нижче терміни, які вживаються у зв'язку з розкриттям, наведеним у цьому описі, якщо не зазначено інше, мають такі значення: Термін "антитіло", який вживають у цьому описі, означає імуноглобулінові молекули та імунологічно активні частини імуноглобулінових (Ig) молекул, тобто молекул, які містять антигензв'язувальний центр, який специфічно зв'язує (вступає до імунної реакції з) антиген(-ом). Такі антитіла включають (але без обмеження) поліклональні, моноклональні, химерні, одноланцюгові антитіла, Fab, Fab', Р(аb')2-фрагменти та бібліотеку експресованих послідовностей Fab. Словосполучення "специфічно зв'язує" або "вступає до імунної реакції з" означає, що згадане антитіло реагує з однією або декількома антигенними детермінантами бажаного антигену і не реагує (тобто не зв'язується) з іншими поліпептидами або зв'язується з іншими поліпептидами з набагато нижчою спорідненістю (Kd>10-6). Відомо, що основна структурна одиниця антитіла включає тетрамер. Кожен тетрамер складається з двох ідентичних пар поліпептидних ланцюгів, де кожна пара має один "легкий" ланцюг (приблизно 25 кДа) і один "важкий" ланцюг (приблизно 50-70 кДа). Амінокінцева частина кожного ланцюга включає варіабельну ділянку, яка складається приблизно з 100-110 або більше амінокислот і яка відповідає, головним чином, за розпізнавання антигену. Карбоксикінцева частина кожного лан 92505 20 цюга визначає константну ділянку, яка відповідає, головним чином, за ефекторну функцію. Людські легкі ланцюги класифікуються як каппа і лямбда легкі ланцюги. Важкі ланцюги класифікуються як мю, дельта, гамма, альфа або іпсилон і визначають ізотип антитіла як, відповідно, IgM, IgD, IgA та IgE. У межах легких і важких ланцюгів варіабельні і константні ділянки сполучаються "J''-фрагментом, який містить приблизно 12 або більше амінокислот, причому важкий ланцюг включає також "D''фрагмент, який складається приблизно з 10 або більше амінокислот. Дивись, взагалі, Fundamental Immunology, глава 7 (редактор Пол В. (Paul W.), 2е видання, Raven Press, Ν.Υ. (1989)). Варіабельні ділянки кожної пари легкий/важкий ланцюги утворюють антигензв'язувальний центр антитіла. Термін "моноклональне антитіло" (МАb) або словосполучення "композиція на основі моноклонального антитіла", які вживають у цьому описі, означає популяцію молекул антитіл, яка включає молекули антитіл лише одного різновиду, які являють собою специфічний продукт гена легкого ланцюга і специфічний продукт гена важкого ланцюга. Зокрема, гіперваріабельні ділянки (CDR) моноклонального антитіла є ідентичними в усіх молекул згаданої популяції. Моноклональні антитіла містять антигензв'язувальний центр, здатний до вступання до імунної реакції з конкретною антигенною детермінантою антигену, який характеризується специфічною зв'язувальною спорідненістю до неї. Як правило, молекули антитіл, одержані від людей, належать до будь-якого з класів IgG, IgM, IgA, IgE та IgD, які відрізняються один від одного природою важкого ланцюга, присутнього у молекулі. Певні класи мають також підкласи, наприклад, IgG1, IgG2 тощо. На додаток до цього, легкий ланцюг у людей може бути каппа-ланцюгом або лямбда-ланцюгом. Термін "антигенна детермінанта", який вживають у цьому описі, включає будь-яку білкову детермінанту, здатну до специфічного зв'язування з імуноглобуліном, scFv або рецептором Т-клітини. Термін "антигенна детермінанта", який вживають у цьому описі, включає будь-яку білкову детермінанту, здатну до специфічного зв'язування з імуноглобуліном або рецептором Т-клітини. Антигенні детермінанти, як правило, являють собою хімічно активні поверхневі угруповання молекул, наприклад, амінокислот або бічних ланцюгів цукрів і, як правило, мають специфічні об'ємні структурні характеристики, а також специфічні зарядні характеристики. Кажуть, що антитіло специфічно зв'язує антиген у тому разі, коли константа дисоціації є 1 мкМ; за варіантом, якому віддається перевага, 100 нМ і за варіантом, якому віддається найбільша перевага, 10 нМ. Словосполучення "імунологічне зв'язування" та "властивості імунологічного зв'язування", які вживаються у цьому описі, означають нековалентні взаємодії того типу, які відбуваються між молекулою імуноглобуліну і антигеном, для якого згаданий імуноглобулін є специфічним. Сила або спорідненість імунологічних зв'язувальних взаємодій може виражатись за допомогою константи ди 21 соціації (Kd) взаємодії, де менше значення Kd представляє більшу спорідненість. Кількісне визначення властивостей імунологічного зв'язування вибраних поліпептидів здійснюють за допомогою способів, добре відомих у цій галузі. Одним із таких способів є визначення швидкості утворення і дисоціації комплексів антигензв'язувальна ділянка/антиген, де згадана швидкість залежить від концентрації партнерів, які утворюють комплекс, спорідненості взаємодії та геометричних параметрів, які рівною мірою впливають на згадану швидкість у обох напрямках. Таким чином, як "константа збільшення швидкості" (Kon), так і "константа зменшення швидкості" (Koff) можуть бути визначені шляхом обчислення концентрацій і фактичної швидкості асоціації та дисоціації. (Дивись Nature 361:186-187 (1993)). Співвідношення Kon/Koff надає можливість відміни усіх параметрів, не пов'язаних зі спорідненістю, і дорівнює константі дисоціації Kd. (Дивись, у цілому, Девіс (Davies) та інші, (1990), Annual Rev. Biochem. 59:439-473). Кажуть, що антитіло за цим винаходом специфічно зв'язується з антигенною детермінантою CD3 у тому разі, коли константа зв'язування у стані рівноваги (Kd) є 1 мкМ; за варіантом, якому віддається перевага, є 100 нМ, за варіантом, якому віддається більша перевага, є 10 нМ і за варіантом, якому віддається найбільша перевага, знаходиться у межах від 100 пМ до приблизно 1 пМ, за даними аналізів, наприклад, аналізів зв'язування лігандів, мічених радіоактивним ізотопом, або подібних аналізів, відомих фахівцям у цій галузі. Фахівцям у цій галузі буде зрозумілою можливість визначення, без зайвого експериментування, чи має людське моноклональне антитіло таку саму специфічність, що й людське моноклональне антитіло за цим винаходом (наприклад, моноклональне антитіло 28F11, 27Н5, 23F10 або 15С3) шляхом визначення того, чи перше згадане антитіло перешкоджає зв'язуванню другого згаданого антитіла з антигенним поліпептидом CD3. Якщо людське моноклональне антитіло, яке піддають випробуванню, конкурує з людським моноклональним антитілом за цим винаходом, як показує зниження зв'язування людським моноклональним антитілом за цим винаходом, у такому разі два моноклональні антитіла зв'язуються з тією самою, або тісно спорідненою, антигенною детермінантою. Інший спосіб визначення, чи людське моноклональне антитіло має специфічність людського моноклонального антитіла за цим винаходом, полягає у попередньому інкубуванні людського моноклонального антитіла за цим винаходом з антигенним поліпептидом CD3, з яким воно, за нормальних обставин, реагує, з подальшим доданням людського моноклонального антитіла, яке піддають випробуванню, для визначення, чи пригнічується здатність людського моноклонального антитіла, яке піддають випробуванню, до зв'язування антигенного поліпептиду CD3. Якщо людське моноклональне антитіло, яке піддають випробуванню, пригнічується, у такому разі, з усією ймовірністю, воно має таку саму, або функціонально еквіваленту епітопну специфічність, що і моноклональне антитіло за цим винаходом. 92505 22 Термін "ідентичність послідовностей" означає, що дві полінуклеотидні або амінокислотні послідовності є ідентичними (тобто на основі порівняння нуклеотидів або залишків) у порівняльному вікні. "Відсоток ідентичності послідовностей" обчислюють шляхом порівняння двох оптимально впорядковано розміщених послідовностей у порівняльному вікні, з визначенням кількості положень, у яких у обох послідовностях знаходяться ідентичні нуклеїновокислотні основи (наприклад, А, Т, С, G, U або І) або залишки, з одержанням кількості суміщених положень, ділення кількості суміщених положень на загальну кількість положень у порівняльному вікні (тобто розмір вікна) і множення результату на 100 для одержання відсотка ідентичності послідовностей. Термін "суттєва ідентичність", який вживається у цьому описі, означає характеристику полінуклеотидної або амінокислотної послідовності, де згаданий полінуклеотид або амінокислота містить послідовність, яка має щонайменше 85 відсоткову ідентичність послідовностей, за варіантом, якому віддається перевага, щонайменше 90-95 відсоткову ідентичність послідовностей, частіше щонайменше 99 відсоткову ідентичність послідовностей, порівняно з еталонною послідовністю у порівняльному вікні із щонайменше 18 нуклеотидних (6 амінокислотних) положень, часто у вікні із щонайменше 24-48 нуклеотидних (8-16 амінокислотних) положень, де відсоток ідентичності послідовностей обчислюють шляхом порівняння еталонної послідовності з послідовністю, яка може включати делеції або додання, які у цілому становлять 20% або менше від еталонної послідовності у порівняльному вікні. Згадана еталонна послідовність може бути підгрупою більшої послідовності. У значенні вживаному у цьому описі, двадцять традиційних амінокислот і їх скорочення відповідають традиційному застосуванню. Дивись Immunology - A Synthesis (друге видання, Е.С. Голуб (E.S. Golub) та Д.Р. Грен (D.R. Gren) (редактори), Sinauer Associates, Sunderland 7, штат Массачусетс (1991)). Стереоізомери (наприклад, Dамінокислоти) двадцяти традиційних амінокислот, штучні амінокислоти, наприклад, -, -двозаміщені амінокислоти, N-алкільні амінокислоти, молочна кислота та інші нетрадиційні амінокислоти, можуть також бути придатними складовими для поліпептидів за цим винаходом. Приклади нетрадиційних амінокислот включають: 4-гідроксипролін, карбоксиглутамат, -Ν,Ν,Ν-триметиллізин, -Νацетиллізин, О-фосфосерин, N-ацетилсерин, Nформілметіонін, 3-метилгістидин, 5-гідроксилізин, σ-Ν-метиларгінін та інші подібні амінокислоти та імінокислоти (наприклад, 4-гідроксипролін). У позначенні поліпептидів, який вживається у цьому описі, лівостороннім напрямком є амінокінцевий напрямок, а правостороннім напрямком є карбоксикінцевий напрямок, відповідно до стандартного застосування і звичаю. Консервативні амінокислотні заміни означають взаємозамінність залишків, які мають однакові бічні ланцюги. Наприклад, групою амінокислот, які мають аліфатичні бічні ланцюги, є гліцин, аланін, валін, лейцин та ізолейцин; групою амінокислот, 23 які мають аліфатично-гідроксильні бічні ланцюги, є серин і треонін; групою амінокислот, які мають амідовмісні бічні ланцюги, є аспарагін і глутамін; групою амінокислот, які мають ароматичні бічні ланцюги, є фенілаланін, тирозин і триптофан; групою амінокислот, які мають основні бічні ланцюги, є лізин, аргінін і гістидин; і групою амінокислот, які мають сірковмісні бічні ланцюги, є цистеїн та метіонін. Замісними консервативними амінокислотними групами, яким віддають перевагу, є: валінлейцин-ізолейцин, фенілаланін-тирозин, лізинаргінін, аланін-валін, глутамінова кислотааспарагінова кислота і аспарагін-глутамін. Як обговорюється у цьому описі, незначні зміни амінокислотних послідовностей антитіл або молекул імуноглобулінів передбачаються як такі, що охоплюються цим винаходом, за умови, що у разі змін, амінокислотна послідовність зберігається щонайменше на 75%, за варіантом, якому віддається перевага, щонайменше на 80%, 90%, 95%, а за варіантом, якому віддається найбільша перевага, на 99%. Передбачаються, зокрема, консервативні амінокислотні заміни. Консервативними замінами є заміни, які відбуваються у сімействі амінокислот, які є спорідненими за своїми бічними ланцюгами. Генетично закодовані амінокислоти, у цілому, підрозділяються на сімейства: (1) кислими амінокислотами є аспартат, глутамат; (2) основними амінокислотами є лізин, аргінін, гістидин; (3) неполярними амінокислотами є аланін, валін, лейцин, ізолейцин, пролін, фенілаланін, метіонін, триптофан, і (4) незарядженими полярними амінокислотами є гліцин, аспарагін, глутамін, цистеїн, серин, треонін, тирозин. До гідрофільних амінокислот належать аргінін, аспарагін, аспартат, глутамін, глутамат, гістидин, лізин, серин і треонін. До гідрофобних амінокислот належать аланін, цистеїн, ізолейцин, лейцин, метіонін, фенілаланін, пролін, триптофан, тирозин і валін. Іншими сімействами амінокислот є (і) серин і треонін, які являють собою аліфатично-гідроксильне сімейство; (іі) аспарагін і глутамін, які являють собою амідовмісне сімейство; (ііі) аланін, валін, лейцин і ізолейцин, які являють собою аліфатичне сімейство; та (iv) фенілаланін, триптофан і тирозин, які являють собою ароматичне сімейство. Термін "агент" вживають у цьому описі для позначення хімічної сполуки, суміші хімічних сполук, біологічної макромолекули або екстракту, одержаного з біологічних матеріалів. Термін "хворий" охоплює людину і ветеринарні суб'єкти. Цей винахід включає також Fv, Fab, Fab' та F(ab')2 фрагменти антитіла проти CD3, одноланцюгові антитіла проти CD3, біспецифічні антитіла проти CD3 і гетерокон'юговані антитіла проти CD3, триспецифічні антитіла, імунокон'юговані та їхні фрагменти. Біспецифічними антитілами є антитіла, які мають зв'язувальні специфічності щонайменше до двох різних антигенів. У цьому разі, однією зі зв'язувальних специфічностей є зв'язувальна специфічність до CD3. Другою зв'язувальною мішенню є будь-який другий антиген і, за варіантом, якому 92505 24 віддається перевага, поверхневий мембранний білок або рецептор чи субодиниця рецептора. Введення терапевтичних засобів і композицій Буде зрозуміло, що терапевтичні засоби за цим винаходом будуть вводитись із відповідними носіями, наповнювачами та іншими компонентами, які включають до складу композицій для забезпечення поліпшеного перенесення, доставки, прийнятності тощо. Численні придатні композиції можна знайти у фармакологічному довіднику, відомому усім фахівцям у галузі фармацевтичної хімії: Remington's Pharmaceutical Sciences (15-е видання, Mack Publishing Company, Easton, штат Пенсільванія (1975), зокрема, у його розділі 87 (Блау (Blaug), Сеймур (Seymour)). Ці композиції охоплюють, наприклад, порошки, пасти, мазі, желе, які містять лікарські засоби, воски, масла, ліпіди, ліпіди (катіонні або аніонні), які містять мікросфери (наприклад, Lipofectin™), кон'югати ДНК, безводні абсорбційні пасти, емульсії типу масло у воді і вода у маслі, емульсії карбоваксу (поліетиленгліколі різної молекулярної маси), напівтверді гелі і напівтверді суміші, які містять карбовакс. Будь-яка з вищезгаданих сумішей може бути придатною для лікування за цим винаходом, за умови, що активна складова композиції не інактивується у згаданій композиції, а згадана композиція є фізіологічно прийнятною і сумісною зі шляхом введення. Дивись також Балдрік П. (Baldrick P.), "Pharmaceutical excipient development: the need for preclinical guidance". Regul Toxicol Pharmacol., 32(2):210-218 (2000), Ванг В. (Wang W.), "Lyophilization and development of solid protein Pharmaceuticals". Int. J. Pharm. 203(1-2): 1-60 (2000), Чармен B.H. (Charman W.N.), "Lipids, lipophilic drugs, and oral drug delivery-some emerging concepts", J. Pharm. Sci., 89 (8):967-978 (2000), Пауелл (Powell) та інші, "Compendium of excipients for parenteral formulations", PDA J. Pharm. Sci. Technol., 52:238311 (1998) та посилання у цьому описі для додаткової інформації відносно композицій, наповнювачів та носіїв, добре відомих фахівцям із фармацевтичної хімії. Композиції, за варіантом, якому віддається перевага, є по суті чистими. Словосполучення "по суті чистий", яке вживають у цьому описі, означає, що переважним присутнім різновидом є цільовий різновид (тобто на молярній основі кількість цього різновиду є більшою за кількість будь-якого іншого окремо взятого різновиду у цій композиції), а за варіантом, якому віддається перевага, по суті очищеною фракцією є композиція, де цільовий різновид становить щонайменше приблизно 50% (на молярній основі) від усіх присутніх макромолекулярних різновидів. Взагалі, по суті чиста композиція буде містити більше за приблизно 80% від усіх макромолекулярних різновидів, присутніх у згаданій композиції, за варіантом, якому віддається більша перевага, більше за приблизно 85%, 90%, 95% та 99%. За варіантом, якому віддається найбільша перевага, цільовий різновид очищають до суттєвої однорідності (забруднювальні різновиди не можуть бути виявлені у згаданій композиції за допомогою традиційних способів виявлення), причому згадана 25 композиція складається по суті з одного макромолекулярного різновиду. Терапевтичні композиції за цим винаходом, які містять анти-СD3 антитіло за цим винаходом, застосовують для лікування або полегшення інтенсивності симптому, пов'язаного з імунопатологією, наприклад, з автоімунним захворюванням або запальним розладом. Автоімунні захворювання включають, наприклад, синдром набутого імунодефіциту (СНІД, який являє собою вірусне захворювання з автоімунною складовою), вогнищеву алопецію, анкілозивний спондилоартрит, антифосфоліпідний синдром, автоімунну хворобу Аддісона, автоімунну гемолітичну анемію, автоімунний гепатит, автоімунне захворювання внутрішнього вуха (AIED), автоімунний лімфопроліферативний синдром (ALPS), автоімунну тромбоцитопенічну пурпуру (АТР), хворобу Бехчета, кардіоміопатію, синдром черевної мальабсорбції - герпетоформний дерматит; синдром хронічного перевтомлення з дисфункцією імунної системи (CFIDS), хронічну запальну демієлінізуючу поліневропатію (CIPD), рубцевий пемфігоїд, синдром холодової аглютинації, синдром CRST, хворобу Крона, хворобу Дего, юнацький дерматоміозит, дискоїдний червоний вовчак, ідіопатичну кріоглобулінемію змішаного типу, фіброміалгіюфіброміозит, хворобу Грейвса, хворобу ГійєнаБарре, тиреоїдит Хашимото, ідіопатичний фіброз легень, ідіопатичну тромбоцитопенічну пурпуру (ІТР), нефропатію IgA-типу, інсулінозалежний цукровий діабет, юнацький інфекційний артрит (хвороба Стілла-Шоффара), юнацький ревматоїдний артрит, хворобу Меньєра, дифузну хворобу сполучної тканини змішаного типу, розсіяний склероз, важку псевдопаралітичну міастенію, злоякісну анемію, нодозний поліартеріїт, поліхондрит, плюригландулярний синдром, ревматичну поліміалгію, поліміозит і дерматоміозит, початкову агаммоглобулінемію, первинний біліарний цироз печінки, псоріаз, псоріатичний артрит, феномен Рейно, синдром Рейтера, ревматизм, ревматоїдний артрит, саркоїдоз, склеродермію (прогресуючий системний склероз (PSS), відомий також як системний склероз (SS)), синдром Гужеро-Шегрена, синдром ригідної людини, системний червоний вовчак, синдром Такаясу, темпоральний артеріїт/гігантоклітинний артеріїт, неспецифічний виразковий коліт, увеїт, вітиліго і гранулематоз Вегенера. Запальні розлади включають, наприклад, хронічні і гострі запальні розлади. Приклади запальних розладів включають хворобу Альцгеймера, астму, атопічну алергію, алергію, атеросклероз, бронхіальну астму, екзему, гломерулонефрит, реакцію "трансплантат проти хазяїна", гемолітичну анемію, остеоартрит, сепсис, інсульт, трансплантацію тканини і органів, васкуліт, діабетичну ретинопатію і пошкодження легень, викликане апаратом штучного вентилювання легень. Композиції на основі антитіла проти CD3 вводять суб'єкту, який страждає на імунопатологічний розлад, наприклад, автоімунне захворювання або запальний розлад. Суб'єкта, який страждає на автоімунне захворювання або запальний розлад, 92505 26 встановлюють за допомогою способів, відомих у цій галузі. Наприклад, суб'єктів, які страждають на автоімунне захворювання, наприклад, хворобу Крона, неспецифічний виразковий коліт або запальну хворобу кишечнику, встановлюють за допомогою будь-якого із цілого ряду клінічних та/або лабораторних аналізів, наприклад, об'єктивного обстеження, рентгенографічного дослідження і аналізів крові, сечі і калу, для оцінки імунного статусу. Наприклад, хворих, які страждають на розсіяний склероз, встановлюють, наприклад, за допомогою магнітного резонансу з візуалізацією присутності пошкоджень центральної нервової системи (ЦНС), які є розсіяними у часі та просторі (тобто трапляються у різних частинах ЦНС із щонайменше тримісячною різницею у часі). Хворих, які страждають на ревматоїдний артрит, встановлюють, наприклад, за допомогою аналізів крові та/або рентгенографічного дослідження чи обстежень з одержанням зображень. Хворих, які страждають на діабет типу І, встановлюють, наприклад, коли будь-які три з наведених нижче проб дають позитивний результат, із подальшою другою позитивною пробою у інший день: (1) рівень глюкози у плазмі натщесерце більший за або такий що дорівнює 126 мг/дл із симптомами діабету; (2) випадковий рівень глюкози у плазмі (що визначається у будь-яку годину дня) більший за або такий що дорівнює 200 мг/дл із симптомами діабету; або (3) показник пероральної проби на толерантність до глюкози (OGTT) більший за або такий що дорівнює 200 мг/дл, який визначається з інтервалом у дві години (показник OGTT наводять для тригодинного проміжку часу). Введення композиції на основі антитіла проти CD3 хворому, який страждає на імунопатологічний розлад, наприклад, автоімунне захворювання або запальний розлад, вважається успішним, якщо досягається будь-який із численних лабораторних або клінічних результатів. Наприклад, введення композиції на основі антитіла проти CD3 хворому, який страждає на імунопатологічний розлад, наприклад, автоімунне захворювання або запальний розлад, вважається успішним, якщо полегшується інтенсивність, ослаблюється, пригнічується або не розвивається до подальшого, тобто гіршого, стану один або декілька симптомів, пов'язаних із розладом. Введення композиції на основі антитіла проти CD3 хворому, який страждає на імунопатологічний розлад, наприклад, автоімунне захворювання або запальний розлад, вважається успішним, якщо розлад, наприклад, автоімунний розлад, вступає до стадії ремісії або не розвивається до подальшого, тобто гіршого, стану. Композиції на основі антитіла проти CD3 за цим винаходом застосовують для лікування, діагностування та/або запобігання запальної хвороби кишечнику (IBD). Запальна хвороба кишечнику являє собою хронічне запалення і подразнення тканини шлунково-кишкового (GI) тракту. Запальна хвороба кишечнику пов'язується з такими симптомами, як судоми черевної порожнини і біль у черевній порожнині, діарея, ректальна кровотеча, гарячка та підвищене число лейкоцитів. Композиції на основі антитіла проти CD3 за цим винаходом вво 27 дять суб'єкту, який страждає на запальну хворобу кишечнику, у якого була діагностована запальна хвороба кишечнику або який є схильним до запальної хвороби кишечнику. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі, яка є достатньою для полегшення щонайменше одного симптому запальної хвороби кишечнику, для лікування запальної хвороби кишечнику, для запобігання запальної хвороби кишечнику та/або для запобігання розвитку запобігання запальної хвороби кишечнику у суб'єкта до подальшої стадії хвороби. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2.4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. За іншим варіантом здійснення, композиції на основі антитіла проти CD3 за цим винаходом застосовують для лікування, діагностування та/або запобігання неспецифічного виразкового коліту. Неспецифічний виразковий коліт являє собою хронічне запалення і подразнення товстої кишки. Неспецифічний виразковий коліт пов'язується з такими симптомами, як анемія; втомлюваність; втрата маси; втрата апетиту; ректальна кровотеча; втрата загальної рідини організму і живильних речовин; ураження шкіри; біль у суглобах; порушення росту (особливо у дітей). Композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту, який страждає на неспецифічний виразковий коліт, у якого він був діагностований або який є схильним до нього. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі, яка є достатньою для полегшення щонайменше одного симптому неспецифічного виразкового коліту, для лікування неспецифічного виразкового коліту, для запобігання неспецифічного виразкового коліту та/або для запобігання розвитку неспецифічного виразкового коліту у суб'єкта до подальшої стадії хвороби. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, яку вибирають зпосеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 92505 28 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. За іншим варіантом здійснення, композиції на основі антитіла проти CD3 за цим винаходом застосовують для лікування, діагностування та/або запобігання хвороби Крону. Хвороба Крону являє собою хронічне запалення і подразнення кишечнику. Хвороба Крону пов'язується з такими симптомами, як біль у черевній порожнині, діарея, втрата маси, поганий апетит, гарячка, нічна пітливість, ректальний біль та ректальна кровотеча. Композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту, який страждає на хворобу Крону, у якого вона була діагностована або який є схильним до неї. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі, яка є достатньою для полегшення щонайменше одного симптому хвороби Крону, для лікування хвороби Крону, для запобігання хвороби Крону та/або для запобігання розвитку хвороби Крону у суб'єкта до подальшої стадії хвороби. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній зпосеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. За іншим варіантом здійснення, композиції на основі антитіла проти CD3 за цим винаходом застосовують для лікування, діагностування та/або запобігання розсіяного склерозу (MS). Розсіяний склероз являє собою хронічне запальне захворювання, яке уражає центральну нервову систему (ЦНС). Симптоми розсіяного склерозу включають, наприклад, зміну у сфері відчуттів, проблеми зору, м'язову слабкість, депресію, труднощі з координацією та мовою і біль. Композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту, який страждає на розсіяний склероз, у якого він був діагностований або який є схильним до нього. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі, яка є достатньою для полегшення щонайменше одного симптому розсіяного склерозу, для лікування розсіяного склерозу, для запобігання розсіяного склерозу та/або для запобігання розвитку розсіяного склерозу у суб'єкта до подальшої стадії хвороби. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба 29 до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній зпосеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. За іншим варіантом здійснення, композиції на основі антитіла проти CD3 за цим винаходом застосовують для лікування, діагностування та/або запобігання інсулінозалежного цукрового діабету (діабет типу І). Діабет типу І являє собою захворювання, яке відрізняється стійкою гіперглікемією (високі рівні цукру у крові), яка є наслідком невідповідної секреції гормону інсуліну. Діабет типу І характеризується втратою інсулінопродукуючих бета-клітин острівців Лангерганса підшлункової залози. Діабет типу І являє собою автоімунне захворювання, у разі якого власна імунна система організму нападає на бета-клітини острівців Лангерганса підшлункової залози з їх знищенням або пошкодженням у достатній мірі для зменшення або припинення продукування інсуліну. Симптоми діабету типу І включають, наприклад, підвищене відчуття спраги, підвищене сечовипускання, втрату маси незважаючи на підвищений апетит, нудоту, блювання, біль у черевній порожнині і втомлюваність. Композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту, який страждає на діабет типу І, у якого він був діагностований або який є схильним до нього. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі, яка є достатньою для полегшення щонайменше одного симптому діабету типу І, для лікування діабету типу І, для запобігання діабету типу І та/або для запобігання розвитку діабету типу І у суб'єкта до подальшої стадії хвороби. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. За іншим варіантом здійснення, композиції на основі антитіла проти CD3 за цим винаходом застосовують для лікування, діагностування та/або запобігання ревматоїдного артриту (RA). Ревматоїдний артрит являє собою автоімунне захворювання, яке спричинює хронічне запалення суглобів. Ревматоїдний артрит може також викликати запалення тканини довкола суглобів, а також інших органів у тілі. Ревматоїдний артрит пов'язується з такими симптомами як втомлюваність, від 92505 30 сутність апетиту, слабка гарячка, біль у м'язах і суглобах та тугорухливість. Композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту, який страждає на ревматоїдний артрит, у якого він був діагностований або який є схильним до нього. Композиції на основі антитіла проти CD3 за цим винаходом вводять у дозі, яка є достатньою для полегшення щонайменше одного симптому ревматоїдного артриту, для лікування ревматоїдного артриту, для запобігання ревматоїдного артриту та/або для запобігання розвитку ревматоїдного артриту у суб'єкта до подальшої стадії хвороби. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. Цей винахід пропонує також способи лікування або полегшення симптому, пов'язаного з імунопатологічним розладом або симптому, пов'язаного з відторгненням після трансплантації органу. Наприклад, композиції за цим винаходом застосовують для лікування або полегшення симптому будь-яких автоімунних захворювань і запальних розладів, опис яких наведено. Терапевтичні композиції за цим винаходом застосовують також як імуносупресорні агенти у разі трансплантації органів або тканин. Термін "імуносупресорний агент", який вживають у цьому описі, означає агент, результатом дії якого на імунну систему є негайне або уповільнене зниження активності щонайменше одного шляху, залученого до імунної реакції, незалежно від того, чи ця реакція відбувається природним шляхом, чи є штучно ініційованою, незалежно від того, чи ця реакція відбувається як частина вродженої імунної системи, адаптивної імунної системи, чи обох. Ці імуносупресорні композиції на основі антитіла проти CD3 вводять суб'єкту перед, під час та/або після трансплантації органу або тканини. Наприклад, композицію на основі антитіла проти CD3 за цим винаходом застосовують для лікування або запобігання відторгнення після трансплантації органу або тканини. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі у діапазоні від 0,05 мг/доба до 10 мг/доба. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 31 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. За варіантом, якому віддається перевага, терапевтичні композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту внутрішньовенним або підшкірним шляхом. Передбачаються інші шляхи введення. Наприклад, композиції на основі антитіла проти CD3 вводять внутрішньовенним, підшкірним, пероральним, парентеральним, назальним, внугрішньом'язовим шляхом або будь-якою комбінацією цих шляхів введення. За одним із варіантів здійснення, композиції на основі антитіла проти CD3 за цим винаходом вводять у поєднанні з другим агентом, наприклад, GLP-1 (глюкагоноподібний пептид) або сполукою, яка переводить бета-клітини у стан спокою (тобто сполукою, яка знижує або іншим чином пригнічує виділення інсуліну, наприклад, відкривачі калієвих каналів). Приклади придатних GLP-1 сполук описують, наприклад, у опублікованій заявці на патент США № 20040037826, а придатні сполуки, які переводять бета-клітини у стан спокою, описують у опублікованій заявці на патент США № 20030235583, обидві з яких у повному обсязі включено до цього опису шляхом посилання. За іншим варіантом здійснення, композиції на основі антитіла проти CD3, які застосовуються для лікування імунопатологічного розладу, вводять у комбінації з будь-яким із численних відомих протизапальних та/або імуносупресорних сполук. До числа придатних відомих сполук належать (але без обмеження) метотрексат, циклоспорин А (з включенням, наприклад, мікроемульсії циклоспорину), такролімус (tacrolimus), кортикостероїдні препарати, статини, бета-інтерферон, ремікад (Remicade (інфліксімаб (Infliximab))), енбрел (Enbrel (етанерцепт (Etanercept))) та гуміра (Humira (адалімумаб (Adalimumab))). Наприклад, при лікуванні ревматоїдного артриту, композиції на основі антитіла проти CD3 за цим винаходом можуть вводитись разом із кортикостероїдними препаратами, метотрексатом, циклоспорином А, статинами, ремікадом (інфліксімабом), енбрелом (етанерцептом) та/або гуміра (адалімумабом). При лікуванні увеїту, композиції на основі антитіла проти CD3 можуть вводитись разом, наприклад, із кортикостероїдними препаратами, метотрексатом, циклоспорином А, циклофосфамідом та/або статинами. Подібним же чином, хворі, уражені таким захворюванням, як хвороба Крона або псоріаз, можуть лікуватись комбінацією композиції на основі антитіла проти CD3 за цим винаходом і ремікаду (інфліксімабу) та/або гуміра (адалімумабу). Хворі на розсіяний склероз можуть одержувати комбінацію композиції на основі антитіла проти CD3 за цим винаходом, наприклад, з ацетатом глатирамеру (копаксон (Copaxone)), бетаінтерфероном 1а (авонекс (Avonex)), бета 92505 32 інтерфероном 1а (ребіф (Rebif)), бетаінтерфероном 1b (бетасерон (Betaseron) або бетаферон (Betaferon)), мітоксантроном (mitoxantrone) (новантрон (Novantrone)), дексаметазоном (декадрон (Decadron)), метилпреднізолоном (депо-медрол (Depo-Medrol)) та/або преднізоном (дельтазон (Deltasone)) та/або статинами. За одним із варіантів здійснення, імуносупресивні композиції на основі антитіла проти CD3 за цим винаходом вводять у поєднанні з другим агентом, наприклад, GLP-1 (глюкагоноподібний пептид) або сполукою, яка переводить бета-клітини у стан спокою, як описано вище. За іншим варіантом здійснення, ці імуносупресивні композиції на основі антитіла проти CD3 вводять у комбінації з будь-яким із цілого ряду відомих протизапальних та/або імуносупресивних сполук. До числа придатних протизапальних та/або імуносупресивних сполук для застосування з антитілами проти CD3 за цим винаходом належить (але без обмеження) метотрексат, циклоспорин А (з включенням, наприклад, мікроемульсії циклоспорину), такролімус, кортикостероїдні препарати і статини. За ще іншим варіантом здійснення цього винаходу, антитіло проти CD3 вводять людині у разі виявлення присутності у організмі згаданої людини автоантитіл. Такі автоантитіла відомі у цій галузі як антитіла зі зв'язувальною спорідненістю до одного або декількох білків, які експресуються ендогенно у організмі людини. За одним з аспектів цього винаходу, людину перевіряють на присутність автоантитіл, специфічно залучених до одного або декількох автоімунних захворювань, як добре відомо у цій галузі. За одним зі специфічних варіантів здійснення, людину перевіряють на присутність антитіл проти інсуліну, глутамінової кислоти, декарбоксилази та/або ІА-2 білка з подальшим введенням антитіла проти CD3 у разі позитивного виявлення одного або декількох таких автоантитіл. За іншим варіантом здійснення цього винаходу, антитіло проти CD3 вводять людині для запобігання, зниження або зменшення рекрутингу імунокомпетентних клітин до людських тканин. Антитіло проти CD3 за цим винаходом вводять суб'єкту, який потребує цього, для запобігання або лікування станів, пов'язаних із патологічним або порушеним рекрутингом імунокомпетентних клітин до тканин людини, уражених хворобою. За іншим варіантом здійснення цього винаходу, антитіло проти CD3 вводять людині для запобігання, зниження або зменшення ефектів, які опосередковуються вивільненням цитокінів у межах людського тіла. Термін "цитокін" означає усі людські цитокіни, відомі у цій галузі, які зв'язують позаклітинні рецептори, експресовані на поверхні клітини і, тим самим, модулюють функцію клітини, у тому числі (але без обмеження) IL-2 (інтерлейкін2), -IFN (гамма-інтерферон), TNF- (фактор некрозу пухлин), IL-4, IL-5, IL-6, IL-9, IL-10 та IL-13. За іншим варіантом здійснення цього винаходу, проти CD3 антитіло водять людині для запобігання, зменшення або зниження ефектів, опосередкованих вивільненням рецепторів цитокінів у людському тілі. Термін "рецептор цитокінів" озна 33 чає усі людські рецептори цитокінів, відомі у цій галузі, які зв'язують один або декілька цитокінів, як визначено у цьому описі, з включенням (але без обмеження) рецепторів вищезгаданих цитокінів. Так, проти CD3 антитіло за цим винаходом вводять для лікування та/або запобігання станів, які опосередковуються шляхом патологічної активації, зв'язування або лікування одного або декількох рецепторів цитокінів у людському тілі. Додатково передбачається, що введення проти CD3 антитіла in vivo знизить рівень внутрішньоклітинної передачі сигналів, опосередкованої рецептором(-ами) цитокінів у організмі такої людини. За одним з аспектів цього винаходу, проти CD3 антитіла вводять людині у разі зниження функціонування панкреатичних бета-клітин. За одним із варіантів здійснення, індивіда перевіряють на функціонування бета-клітин, секрецію інсуліну або рівні С пептиду, як відомо у цій галузі. У подальшому, у разі виявлення достатнього рівня зниження будь-якого зі згаданих індикаторів, людині, за відповідною схемою приймання лікарського засобу, вводять проти CD3 антитіло для запобігання подальшого прогресування автоімунного руйнування функціонування бета-клітин. Діагностичні і профілактичні композиції Композиції на основі антитіла проти CD3 (які у цьому описі називають також композиціями на основі антитіла) за цим винаходом застосовують у діагностичних і профілактичних композиціях. За одним із варіантів здійснення, композицію на основі моноклонального антитіла проти CD3 за цим винаходом вводять хворим, які належать до групи ризику розвитку одного з вищезгаданих автоімунних захворювань. Схильність хворого до одного або декількох із вищезгаданих автоімунних захворювань може визначатись за допомогою генотипових, серологічних або біохімічних маркерів. Наприклад, присутність конкретних підтипів HLA (головний комплекс гістосумісності людини) і серологічних автоантитіл (проти інсуліну, GAD65 та ІА-2) вказує на діабет типу І. За іншим варіантом здійснення цього винаходу, композицію на основі антитіла проти CD3 вводять людям, у яких діагностоване одне або декілька з вищезгаданих автоімунних захворювань. У разі постановки діагнозу, антитіло проти CD3 вводять для полегшення або звернення ефектів автоімунітету. За одним із таких прикладів, людині, у якої діагностували діабет типу І, вводять достатню дозу антитіла проти CD3 для відновлення функції 92505 34 підшлункової залози і зведення до мінімального рівня пошкодження унаслідок автоімунної інфільтрації до підшлункової залози. За іншим варіантом здійснення, людині, у якої діагностували ревматоїдний артрит, вводять антитіло проти CD3 для зменшення інфільтрації імунокомпетентних клітин до та руйнування суглобів кінцівок. За варіантом, якому віддається перевага, терапевтичні, діагностичні та/або профілактичні композиції на основі антитіла проти CD3 за цим винаходом вводять суб'єкту внутрішньовенним або підшкірним шляхом. Передбачаються інші шляхи введення. Наприклад, композиції на основі антитіла проти CD3 вводять внутрішньовенним, підшкірним, пероральним, парентеральним, назальним, внутрішньом'язовим шляхом або будь-якою комбінацією цих шляхів введення. Усі публікації та патентні документи, згадані у цьому описі, включені до нього шляхом посилання таким чином, як нібито кожна окрема публікація або документ були б конкретно та індивідуально призначені до включення шляхом посилання. Згадування публікацій і патентних документів не призначене для визнання того, що будь-який з них належить до відомого рівня техніки, і не представляє жодного визнання щодо їх вмісту або дати публікації. Після наведення письмового опису цього винаходу, фахівцям у цій галузі буде зрозуміло, що цей винахід може бути практично втіленим цілим рядом варіантів здійснення і що вищенаведений опис і наведені нижче приклади мають ілюстративне призначення, а не обмеження формули винаходу, яка додається. Приклади Наведені нижче приклади, у тому числі проведені експерименти і одержані результати, наведені виключно з ілюстративною метою і не повинні розглядатись як такі, що обмежують обсяг цього винаходу. Приклад 1: Розробка і аналіз композицій При дослідженні композицій, опис якого наведено, стабільність антитіла проти CD3 у 20 композиціях контролювали при визначених температурах впродовж періоду часу тривалістю три місяці. Досліджувані композиції містили ацетатний, цитратний і фосфатний буферні розчини, які забезпечували pH у діапазоні від pH 4,0 до pH 8,0, а також вибрані наповнювачі твін 80, маніт, EDTA (етилендіамінтетраоцтова кислота), хлорид натрію і цукрозу. Досліджувані композиції подані у наведеній нижче таблиці: 35 92505 36 Таблиця 1 Досліджувані композиції Умовне позначення композиції F1 F2 F3 F4 F5 F6 F7 F8 F9 F10 F11 F12 F13 F14 F15 F16 F17 F18 F19 F20 Композиція pH 25 мМ розчин ацетату натрію/125 мМ розчин хлориду натрію 25 мМ розчин ацетату натрію/125 мМ розчин хлориду натрію 25 мМ розчин ацетату натрію/125 мМ розчин хлориду натрію/0,02% розчин твін 80 10 мМ розчин ацетату натрію/140 мМ розчин хлориду натрію 10 мМ розчин ацетату натрію/100 мМ розчин хлориду натрію/2% розчин маніту 25 мМ розчин цитрату натрію/125 мМ розчин хлориду натрію 25 мМ розчин цитрату натрію/125 мМ розчин хлориду натрію 25 мМ розчин цитрату натрію/125 мМ розчин хлориду натрію 25 мМ розчин цитрату натрію/125 мМ розчин хлориду натрію/0,02% розчин твін 80 10 мМ розчин цитрату натрію/140 мМ розчин хлориду натрію 10 мМ розчин цитрату натрію/100 мМ розчин хлориду натрію/2% розчин маніту 25 мМ розчин цитрату натрію/200 мМ розчин цукрози 50 мМ розчин фосфату натрію/100 мМ розчин хлориду натрію 50 мМ розчин фосфату натрію/100 мМ розчин хлориду натрію 50 мМ розчин фосфату натрію/100 мМ розчин хлориду натрію 50 мМ розчин фосфату натрію/100 мМ розчин хлориду натрію/0,02% розчин твін 80 50 мМ розчин фосфату натрію/100 мМ розчин хлориду натрію/0,01% розчин EDTA 10 мМ розчин фосфату натрію/150 мМ розчин хлориду натрію 10 мМ розчин фосфату натрію/100 мМ розчин хлориду натрію/2% розчин маніту 25 мМ розчин фосфату натрію/200 мМ розчин цукрози 4,0 5,5 5,5 5,5 5,5 5,5 6,0 6,5 6,0 6,0 6,0 6,0 6,0 7,0 8,0 7,0 7,0 7,0 7,0 7,0 Для контролювання різних фізичних і хімічних властивостей продукту застосовували різноманітні методи визначення стабільності. Ці методи вибирали з-посеред застосовуваних для випробування цільності продукту у партії виробів перед її випуском і вони включали визначення pH, концентрації білка, перевірку зовнішнього вигляду, гельпроникну хроматографію (GP HPLC), SDS PAGE (електрофорез у поліакриламідному гелі у присутності додецилсульфату натрію) та ізоелектричне фокусування. Стабільність продукту оцінювали у кожній композиції при гаданій температурі збереження 5±3°С та при підвищених температурах збереження 25±3°С і 40±3°С. Підвищені температури застосовували для прискореного одержання даних щодо стабільності у кожній композиції, які застосовували для підтвердження вибору композиції, який робили на основі даних у реальному часі. На додаток до цього, зразки зберігали при температурі -20±5°С для дослідження впливу заморожування-відтаювання на стабільність молекули. Для додаткового дослідження впливу композиції на схильність продукту до агрегації, зразки піддавали перемішуванню впродовж 48 год. при температурі навколишнього середовища. Результати, які були одержані впродовж цього дослідження з кожного аналізу, вказували композиції-"кандидати", які не зазнали явно виражених змін при гаданій температурі зберігання або при підвищеній температурі і зміни яких були найменшими, у разі порівняння з початком дослідження. Взагалі, результати дослідження показали, що ацетатні композиції F2, F3, F4 та F5 при pH 5,5 були найприйнятнішими композиціями "кандидатами" для антитіла проти CD3. У подальшому, 25 мМ розчин ацетату натрію/125 мМ розчин хлориду натрію/0,002% розчин твін 80, pH 5,5, вибрали як кінцевий композиційний буфер для антитіла проти CD3. Композиції за цим винаходом мають pH у межах від 3,0 до 7,0. За варіантом, якому віддається перевага, композиція має pH у межах від 5,0 до 6,0, за варіантом, якому віддається більша перевага, композиція має pH у межах від 5,2 до 5,8, за варіантом, якому віддається найбільша перевага, композиція має pH у межах від 5,4 до 5,6. Наприклад, за одним із варіантів здійснення, композиція має pH 5,5. Приклад 2: Дозоване введення композицій на основі антитіла проти CD3 Процес вибору дози, опис якого наведено, застосовували для визначення доз, які забезпечили б терапевтичний інтервал для композицій на основі антитіла проти CD3, призначених для перевірки у дослідженнях більшого масштабу. Одночасно, вибирали початкову дозу для перевірки, яка була б нешкідливою для хворих. Оскільки деякі моноклональні антитіла проти CD3, опис яких наведено, наприклад, 28F11, 15С3, 27Н5 та 23F10, не вступають до перехресної реакції із "стандартним" лабораторним різновидом CD3, токсикологічні дані та дані відносно ефективності не можна було одержати за допомогою токсикологічних і передклінічних фармакологічних досліджень. Зокрема, дослідження із застосуванням GLP продемонстрували відсутність перехресної реактивності деяких моноклональних антитіл проти CD3, опис яких наведено, з CD3 мишей, пацюків, кролів, макак-резусів, макак-крабоїдів та павіанів. У процесі вибору дози, таким чином, ке 37 рувались даними, які були одержані in vitro на людських Т-клітинах, шляхом порівняння антитіла проти CD3, яке не вступало до перехресної реакції зі стандартним лабораторним різновидом CD3 (тобто "антитіло проти CD3, яке не вступає до перехресної реакції"), з іншими існуючими на ринку антитілами проти CD3, шляхом застосування опублікованої інформації відносно антитіл проти CD3, які зараз розробляються або існують на ринку (дивись, наприклад, Orthoclone marketed sheet; Woodle Transplantation 1999; Friend Transplantation 1999; Herold NEJM 2002; Keymeulen NEJM 2005): - дози Orthoclone OKT3, hOKT3 1 (Ala-Ala) та ChAglyCD3, застосовані при проведенні клінічних досліджень, були ефективними у межах від 5 мг до 25 мг/ін'єкцію з досягненням 80% або більшого ступеня модуляції молекул CD3 з поверхні Тклітин і забезпечували середній сироватковий рівень >800 нг/мл; - тривалість лікування із застосуванням Orthoclone OKT3, hOKT3 1 (Ala-Ala) та ChAglyCD3 коливалась у межах 10-14, 7-14 та 6 послідовних днів, відповідно; - in vitro дослідження з визначенням модуляції рецепторів CD3 та TCR на людських Т-клітинах постійно показували, що ІС50 антитіла проти CD3, яке не вступає до перехресної реакції, у 2-3 рази перевищує відповідний показник для Orthoclone; - in vitro дослідження з визначенням проблем безпечності, наприклад, CRS (синдром виділення цитокінів), постійно демонстрували, що антитіла проти CD3, які не вступають до перехресної реакції, спричинюють мінімальну індукцію або зовсім не індукують TNF , IFN , IL-6 або IL-2, порівняно з Orthoclone, після інкубації з людськими лейкоцитами периферичної крові. Параметри in vitro аналі 92505 38 зу імітували клінічний вплив лейкоцитів у периферичній крові хворих. Індукція цитокіну антитілом проти CD3, яке не вступає до перехресної реакції, є на декілька порядків величини нижчою, аніж у разі Orthoclone. Таким чином, для визначення імунологічної і попередньої терапевтичної ефективності у межах терапевтичного інтервалу, хворі будуть одержувати 5 добових послідовних доз антитіла проти CD3, яке не вступає до перехресної реакції. Діапазон застосовуваних доз, впродовж п'яти послідовних днів, у хворих буде становити від 0,5 мг/доба до 5,0 мг/доба, що є значно нижче, аніж ефективна доза Orthoclone, але буде індукувати (якщо буде взагалі) мінімальний CRS. За варіантом, якому віддається перевага, діапазон застосовуваних впродовж п'яти послідовних днів доз становить від 0,7 мг/доба до 2 мг/доба. Наприклад, діапазон застосовуваних впродовж п'яти послідовних днів доз становить 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба або 2,0 мг/доба. Наслідком застосування діапазону доз за цим винаходом є значно легший CRS, виходячи з in vitro даних. Приклад 3: Виготовлення і очищення композицій на основі антитіла проти CD3 Нижче наведена схема послідовності операцій, на якій зображені стадії загального процесу одержання антитіл проти CD3. Подробиці щодо стадій процесу та контролю якості продукції у процесі виготовлення, до якого вдавались на кожній стадії процесу, подані у табличній формі у Таблицях 2-4. 39 92505 40 41 92505 42 Таблиця 2 Культивування клітин і збирання клітин, які виросли у культурі Стадія Стадія процесу Умови № 1 Одержання посівного матеріалу: Живильне середовище - Колби і бутелі, вміст яких педля вирощування СМ41 ремішується під час їх обертання Одержання посівного матеріалу: Живильне середовище - Мішки для клітин(25 л) для вирощування СМ41 2 Стадія напрацювання посівного Живильне середовище матеріалу: для вирощування СМ42 - Промисловий біореактор 2 Основна необроблена маса: - Промисловий біореактор 3 Збирання клітин, що виросли у культурі/очищення Фільтрування (0,2 мкм) після збирання клітин, які виросли у культурі 4 Клітини і дебрис, видалені шляхом фільтрування Фільтрування очищеного супернатанту у стерильні контейнери. Зберігання при температурі5±3°С. Максимальний час зберігання14 днів. Контроль якості продукції у процесі виготовлення Визначення загальної кількості, кількості життєздатних клітин і відсотка життєздатності Візуальна перевірка на відсутність мікробного забруднення Температура Швидкість качалки/шейкера Визначення загальної кількості, кількості життєздатних клітин і % життєздатності Відсутність мікробного росту Температура Потік газу Кут качання Частота качання Кількість генерацій Щоденно: Визначення загальної кількості, кількості життєздатних клітин і відсотка життєздатності Відсутність мікробного росту Температура pH Розчинений кисень Швидкість потоку газоподібного азоту Тиск газоподібного азоту Швидкість потоку газоподібного діоксиду вуглецю Тиск газоподібного діоксиду вуглецю Швидкість потоку повітря Тиск потоку повітря Швидкість подачі День збирання клітин, що виросли у культурі Біонавантаження Мікоплазми: - Барвник Hoechst - Культура Віруси: - In vitro віруси CMRC-5, VERO, CHOK1) - "Мінут-віруси" мишей групи парвовірусів за допомогою Q-ПЛР Кількість ретровірусоподібних частинок/мл нерозбавлених клітин, що виросли у культурі (електронний мікроскоп) Біонавантаження (перед і після фільтрування) Ендотоксин (після фільтрування) Титр білка А (високоефективна рідинна хроматографія) Перевірка цілісності кінцевих фільтрів 43 92505 44 Таблиця 3 Очищення і реакції модифікування Стадія Стадія процесу № 5 Очищення засобами mabSelect хроматографії 6 7 8 9 10 11 12 Контроль якості продукції у процесі виготовлення рН Температура 12°С Електропровідність Промивання 50 мМ розчином Температура Na3PO4/250 мМ розчином NaCl, буфер pH 7,0 та 50 мМ розчином Na3PO4/1,0 M Концентрація білка (Хроматографія білка А) розчином NaCl, буфер pH 7,0 Біонавантаження Елюювання 10 мМ розчином форміату Концентрація білка (А280) натрію, буфер pH 3,5 Максимальне завантаження 21 г/л РН обробка Довести до 3,7±0,10 за допомогою 2,0 Μ Концентрація білка (А280) розчину оцтової кислоти з подальшим Біонавантаження повторним доведенням до7,20±0,20 за SDS PAGE1 допомогою основного трис-буферу Концентрування і діафі- Концентрування до приблизно10,0±1,0 Концентрація білка (А280) льтрування г/л із подальшим діафільтруванням до pH 10 мМ розчину Na3PO4, буфер pH 7,0 Електропровідність Біонавантаження Очищення хроматогра- Температура 12°С pH фією на колонках Q Попереднє урівноважування за допомо- Електропровідність Ceramic Hyper DF гою 0,1 Μ розчину фосфату натрію, pH Температура Концентрація білка (А280) 7,0 Промивання/елюювання за допомогою Біонавантаження SDS PAGE1 10 мМ розчину Na3PO4, буфер pH 7,0 Промивання після елюювання за допомогою 10 мМ розчину Na3PO4/2,0 M розчину NaCl, буфер pH 7,0 Максимальне завантаження 50 г/л Очищення гідроксіапа- Температура 12°С pH титною хроматографією Попереднє урівноважування за допомо- Електропровідність гою 0,1 Μ розчину фосфату натрію, pH Температура Концентрація білка (А280) 6,5 Промивання за допомогою 15 мМ розчи- Біонавантаження SDS PAGE1 ну Na3PO4, буфер pH 6,5 Елюювання за допомогою 15 мМ розчину Na3PO4/375 мМ розчину NaCl, буфер рН6,5 Максимальне завантаження 20 г/л Промивання після елюювання за допомогою 0,5 Μ розчину фосфату натрію, pH 6,5 Фільтрування для вида- 20 нм патронний фільтр19°С±4°С, 0,98 Концентрація білка (А280) лення вірусів (Pianova бар промивання 15 мМ розчином фосТемпература 20 Ν) фату натрію/375 мМ розчином NaCl, бу- Вхідний тиск Перевірка цілісності фільтра пісфер pH 6,5 ля застосування Умови Концентрування і діафі- Концентрування з подальшим діафільт- Концентрація білка (А280) льтрування руванням до25 мМ розчину ацетату на- pH трію/125 мМ розчину NaCl, буфер рН5,5 Електропровідність Біонавантаження Додання наповнювача 10% розчин полісорбату 80 Концентрація білка (А280) Кінцева концентрація6,0 мг/мл+0,6 мг/мл pH Електропровідність 1 - є необхідним лише у разі здійснення більше 1 циклу і профілі елюату не порівнюються лише візуальним аналізом 45 92505 При завершенні кожної стадії очищення і під час фасування до контейнера для нерозбавленого очищеного продукту, продукт, який знаходиться у процесі обробки, фільтрують (0,2 мкм). Для кожної стадії очищення, час між видаленням продукту, який знаходиться у процесі обробки, із зберіганням при температурі 5±3°С, здійсненням стадії очищення і поверненням обробленого профільтрованого (0,2 мкм) продукту до холодильної камери не повинен перевищувати 36 год. 46 Склад кінцевого композиційного буфера виглядає наведеним нижче чином: Складова буфера Ацетат натрію Хлорид натрію Полісорбат 80 Концентрація 25 мМ розчин 125 мМ розчин 0,02% (у об'ємному відношенні) Таблиця 4 Кінцеве фільтрування і випуск Стадія Стадія процесу № 13 Кінцеве фільтрування (0,2 мкм) і фасування 14 Перевірка і випуск Контроль якості продукції у процесі виготовлення Фільтрування при температурі Біонавантаження (перед фільтрунавколишнього середовища. ванням) Карантинне зберігання при Перевірка цілісності фільтра після температурі 5±3°С застосування Не застосовуються За специфікацією нерозбавленого очищеного продукту Сировина, застосована у процесі одержання антитіла проти CD3 Живильне середовище СМ34, яке містить основні розчини, застосовують під час зберігання клітин у банку. Початковий головний банк клітин є кріоконсервованим у живильному середовищі СМ34, доповненому диметилсульфоксидом. Живильне середовище СМ41, яке містить основні розчини і хімікати, застосовують під час одержання посівного матеріалу. На додаток до цього, до основного живильного середовища перед застосуванням додають Додаток Е, яке містить солі. Живильне середовище СМ42, яке містить основні розчини, хімікати і амінокислоти, застосовують на стадії напрацювання посівного матеріалу. Живильне середовище СМ42 доповнюють підкормками SF31, SF32 і Домішкою Е. Ці підкормки містять основи у формі порошку, солі, амінокислоти, глюкозу, вітаміни, хімікати і мікроелементи. Усі амінокислоти, застосовані у живильних середовищах і підкормочних композиціях, одержують із джерел нетваринного походження. Приклад 4: Схема лікування для застосування композицій на основі антитіла проти CD3 при лікуванні автоімунного захворювання Композицію на основі антитіла проти CD3 або відповідне плацебо вводять шляхом внутрішньо Умови венного вливання у 1-5 дні проведення експерименту у дозі у межах від 0,05 мг/доба до 10 мг/доба або плацебо. За варіантом, якому віддається перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,1 мг/доба до 5,0 мг/доба, а за варіантом, якому віддається більша перевага, композицію на основі антитіла проти CD3 вводять у дозі від 0,5 мг/доба до 3,0 мг/доба. Наприклад, композицію на основі антитіла проти CD3 вводять у дозі, вибраній з-посеред 0,5 мг/доба, 0,6 мг/доба, 0,7 мг/доба, 0,8 мг/доба, 0,9 мг/доба, 1,0 мг/доба, 1,1 мг/доба, 1,2 мг/доба, 1,3 мг/доба, 1,4 мг/доба, 1,5 мг/доба, 1,6 мг/доба, 1,7 мг/доба, 1,8 мг/доба, 1,9 мг/доба, 2,0 мг/доба, 2,1 мг/доба, 2,2 мг/доба, 2,3 мг/доба, 2,4 мг/доба, 2,5 мг/доба, 2,6 мг/доба, 2,7 мг/доба, 2,8 мг/доба, 2,9 мг/доба та 3,0 мг/доба. Якщо рівень дози пов'язується зі значною модуляцією CD3 комплексу на Т-клітинах та/або із значним синдромом виділення цитокінів, замість однієї або декількох доз більш високого рівня випробують одну або декілька доз нижчого рівня. Результатом введення дози композиції на основі антитіла проти CD3 бажаного рівня є рівень виділення цитокінів, який є меншим за "3" за шкалою ВООЗ для виділення цитокінів. Критерії для рівня 3 за шкалою ВООЗ для симптомів виділення цитокінів наведені нижче у Таблиці 5. 47 92505 48 Таблиця 5 Критерії ВООЗ рівнів токсичності Грипоподібні симптоми (симптоми виділення цитокінів) Гарячка за відсу- Немає тності інфекції, (104,0°F (40°С)) 37,1°С38,0°С 98,7°F100,4°F Озноб Немає Незначний або нетривалий Міалгія/ артралгія Нормальний стан Незначна Пітливість Нездужання Грипоподібні симптоми Приріст маси тіла Втрата маси тіла Нормальний рівень Відсутнє 40,0°С (104,0°F) Впродовж год >40,0°С впродовж>24 год 50% часу неспання Прикутість до ліжка або нездатність подбати про себе Тяжкі Загрозливі для життя 20% 20% нення згаданої цілі, згадану дозу вводять впродовж 5 днів, але максимальна загальна тривалість лікування не повинна перевищувати 8 днів. Композицію на основі антитіла проти CD3 вводять шляхом внутрішньовенного (iv) вливання. За варіантом, якому віддається перевага, внутрішньовенне вливання є безперервним вливанням впродовж періоду часу у межах від 30 хв. до 3 год., за варіантом, якому віддається більша перевага, у межах від 1 год. до 2 год. Наприклад, композицію на основі антитіла проти CD3 вводять шляхом безперервного внутрішньовенного вливання впродовж 2 год кожного дня. Пересічним фахівцям у цій галузі буде зрозуміло, що тривалість безперервного внутрішньовенного вливання безпосередньо пов'язується з дозою композиції, яка вводиться, і об'ємом мішечка для внутрішньовенного вливання. Обчислення необхідного часу для безперервного вливання при даному рівні дози і об'ємі мішечка знаходиться у межах пересічного рівня можливостей цієї галузі. Інші варіанти здійснення Незважаючи на наведений докладний опис винаходу, вищенаведений опис призначено для ілюстрації, а не для обмеження обсягу винаходу, який визначається обсягом формули винаходу, яка додається. Інші аспекти, переваги і модифікації входять до обсягу формули винаходу, яка додається. 49 92505 50 51 92505 52 53 92505 54 55 92505 56 57 92505 58 59 92505 60
ДивитисяДодаткова інформація
Назва патенту англійськоюAnti-cd3 antibody formulations
Автори англійськоюElson Greg, Dean Yann, Kosco-Vilbois Marie
Назва патенту російськоюКомпозиции на основе антитела против cd3
Автори російськоюЭлсон Грег, Дин Ян, Коско-Вильбуа Мари
МПК / Мітки
МПК: A61K 39/395, C07K 16/28, A61P 37/06
Мітки: антитіла, композиції, основі
Код посилання
<a href="https://ua.patents.su/54-92505-kompozici-na-osnovi-antitila-proti-cd3.html" target="_blank" rel="follow" title="База патентів України">Композиції на основі антитіла проти cd3</a>
Попередній патент: Антиміостатинове моноклональне антитіло
Наступний патент: Універсальна вакуумна сушарка
Випадковий патент: Амортизаційний стояк для гідравлічного приводу коліс