Похідні ізоксазоліну, спосіб їх одержання (варіанти), гербіцидна композиція та спосіб контролю рослин
Номер патенту: 92210
Опубліковано: 11.10.2010
Формула / Реферат
1. Похідні ізоксазоліну формули (І)
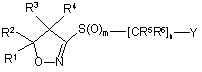 , (І)
, (І)
де
R1 і R2, кожен незалежно від іншого, являє собою водень, С1-10алкіл, С1-10галогеналкіл, С3-8циклоалкіл або С3-8циклоалкіл-С1-3алкіл, або
R1 і R2 разом з атомом вуглецю, з яким вони зв'язані, утворюють С3-7кільце,
R3 і R4, кожен незалежно від іншого, являє собою водень, С1-10алкіл, С1-10галогеналкіл, С3-8циклоалкіл або С3-8циклоалкіл-С1-10алкіл або С1-6алкоксі-С1-10алкіл, або
R3 і R4 разом з атомом вуглецю, з яким вони зв'язані, утворюють С3-7кільце, або
R1 з R3 або R4 і разом з атомом вуглецю, з яким вони зв'язані, утворюють С5-8кільце, або
R2 з R3 або R4 і разом з атомом вуглецю, з яким вони зв'язані, утворюють С5-8кільце;
R5 являє собою галоген або С1-6галогеналкіл;
R6 являє собою водень, ціано, С1-6алкіл, С1-6алкоксикарбоніл, галоген або С1-6галогеналкіл;
m дорівнює 0, 1 або 2;
n дорівнює 1, 2 або 3; і
Y являє собою одну з наступних груп
 ,
, 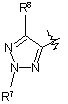 ,
, 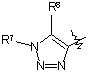 ,
,
де
R7 являє собою водень, С1-10алкіл, С1-10алкілкарбоніл, форміл, С1-10галогеналкілкарбоніл, С1-10алкоксикарбоніл, С1-10галогеналкіл, ціано, С2-10алкеніл, С2-10алкініл, С3-10циклоалкіл, С3-10циклоалкіл-С1-10алкіл, С1-10алкілкарбоніл-С1-10алкіл, С1-10алкілсульфоніл, С1-10галогеналкілсульфоніл, С1-10алкоксі-С1-10алкіл або феніл, що необов'язково заміщений 1-5 замісниками, вибраними з ціано, С1-10алкілу, С1-10галогеналкілу або галогену; або
R7 являє собою -CONR13R14 або -SO2NR13R14, де R13 і R14, кожен незалежно від іншого, являють собою водень, С1-6алкіл, С1-6галогеналкіл, С1-6циклоалкіл С1-6алкілкарбоніл, С1-6галогеналкілкарбоніл, С1-6алкілсульфоніл, С1-6галогеналкілсульфоніл, або R13 і R14 разом утворюють С3-8алкіленову групу, що необов'язково містить один кисень, сірку, аміно- або С1-6алкіламіногрупу;
R8 являє собою водень, С1-10алкіл, С1-10алкілкарбоніл, форміл, С1-10галогеналкілкарбоніл, С1-10алкоксикарбоніл, С1-10галогеналкіл, С2-10алкеніл, С2-10алкініл, С3-10циклоалкіл, С3-10циклоалкіл-С1-10алкіл, галоген, ціано, С1-10алкокси або С1-10галогеналкокси; або
R8 являє собою -CONR15R16, -SO2NR15R16 або NR15R16, де R15 і R16, кожен незалежно від іншого, являють собою водень, С1-6алкіл, С1-6галогеналкіл, С1-6циклоалкіл, С1-6алкілкарбоніл, С1-6галогеналкілкарбоніл, С1-6алкілсульфоніл, С1-6галогеналкілсульфоніл, або R15 і R16 разом утворюють С3-8алкіленову групу, що необов'язково містить один кисень, сірку, аміно- або С1-6алкіл аміногрупу;
і N-оксиди, солі й оптичні ізомери сполук формули І.
2. Похідні ізоксазоліну за п. 1, де R1 і R2 незалежно являють собою С1-10алкіл або С1-10галогеналкіл.
3. Похідні ізоксазоліну за п. 1 або 2, де R1 і R2, обидва являють собою метил.
4. Похідні ізоксазоліну за будь-яким з пп. 1-3, де R3 і R4 незалежно являють собою водень, С1-10алкіл або С1-10галогеналкіл.
5. Похідні ізоксазоліну за будь-яким з пп. 1-4, де R3 і R4, обидва являють собою водень.
6. Похідні ізоксазоліну за будь-яким з пп. 1-5, де R5 являє собою галоген або трифторметил.
7. Похідні ізоксазоліну за будь-яким з пп. 1-6, де R5 являє собою фтор або хлор.
8. Похідні ізоксазоліну за будь-яким з пп. 1-7, де R6 являє собою водень, метоксикарбоніл, С1-6алкіл або галоген.
9. Похідні ізоксазоліну за будь-яким з пп. 1-8, де R6 являє собою водень або фтор.
10. Похідні ізоксазоліну за будь-яким з пп. 1-9, де m дорівнює 1 або 2.
11. Похідні ізоксазоліну за будь-яким з пп. 1-10, де m дорівнює 2.
12. Похідні ізоксазоліну за будь-яким з пп. 1-11, де n дорівнює 1.
13. Похідні ізоксазоліну за будь-яким з пп. 1-12, де Y являє собою одну з наступних груп
 ,
, 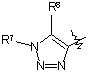 .
.
14. Похідні ізоксазоліну за будь-яким з пп. 1-13, де R7 являє собою водень, С1-10алкіл, С1-10галогеналкіл, С2-10алкеніл, С2-10алкініл, С3-10циклоалкіл, С3-10циклоалкіл-С1-10алкіл, С1-10алкоксі-С1-10алкіл або феніл, що необов'язково заміщений 1-5 замісниками, вибраними з ціано, С1-10алкілу, С1-10галогеналкілу або галогену.
15. Похідні ізоксазоліну за будь-яким з пп. 1-14, де R7 являє собою водень, метил, етил, ізопропіл, трет-бутил, монофторметил, дифторметил, трифторметил, аліл, пропаргіл, циклопропіл, циклопентил, циклопропілметил, циклобутилметил, метоксиметил, 2-метоксіетил або феніл.
16. Похідні ізоксазоліну за будь-яким з пп. 1-15, де R8 являє собою водень, С1-10алкіл, С1-10алкілкарбоніл, форміл, С1-10алкоксикарбоніл, С1-10галогеналкіл, С3-10циклоалкіл, галоген, ціано, С1-10алкокси або С1-10галогеналкокси.
17. Похідні ізоксазоліну за будь-яким з пп. 1-16, де R8 являє собою водень, метил, етил, ацетил, форміл, метоксикарбоніл, монофторметил, дифторметил, трифторметил, бромдифторметил, 1-фторетил, циклопропіл, фтор, хлор, бром, ціано, метокси, дифторметокси, трифторметокси або 2,2,2-трифторетокси.
18. Спосіб одержання сполуки формули (Id)
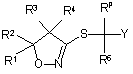 , (Id)
, (Id)
який включає взаємодію сполуки формули VIII
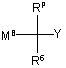 , (VIII)
, (VIII)
де
R6 і Y є такими, як визначено в п. 1,
RP являє собою водень, галоген або С1-6галогеналкіл, і
МB вибирають із групи: MgCl, MgBr, ZnBr і Li,
зі сполукою формули IX
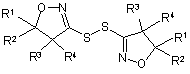 , (IX)
, (IX)
де
R1, R2, R3 і R4 є такими, як визначено в п. 1, необов'язково в присутності розріджувача.
19. Спосіб одержання сполуки формули (Id)
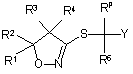 , (Id)
, (Id)
який включає взаємодію сполуки формули IІа
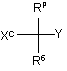 , (IIa)
, (IIa)
де
R6 і Y є такими, як визначено в п. 1,
RP являє собою водень, галоген або С1-6галогеналкіл, і
XC являє собою функціональну групу, що може бути вилучена у вигляді радикала
зі сполукою формули IX
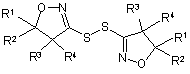 , (IX),
, (IX),
де R1, R2, R3 і R4 є такими, як визначено в п. 1,
за допомогою ініціатора радикальної реакції або його попередника необов'язково в присутності основи і необов'язково в присутності розріджувача.
20. Спосіб одержання сполуки формули (Id)
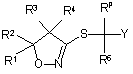 , (Id)
, (Id)
який включає взаємодію сполуки формули II, де R6 і Y є такими, як визначено в п. 1, RP являє собою водень, галоген або С1-6галогеналкіл, і XA являє собою відхідну групу, вибрану з групи, яка складається з галогену, алкілсульфонату, арилсульфонату і галогеналкілсульфонату,
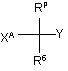 (II)
(II)
зі сполукою формули IX
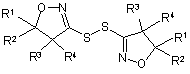 , (IX)
, (IX)
де R1, R2, R3 і R4 є такими, як визначено в п. 1,
у присутності відновлювального агента, необов'язково в присутності основи і необов'язково в присутності розріджувача.
21. Проміжна сполука формули IX
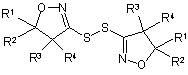 , (IX)
, (IX)
де R1, R2, R3 і R4 є такими, як визначено в п. 1.
22. Гербіцидна композиція, що містить гербіцидно ефективну кількість сполуки формули І за пп. 1-17 та на додаток до допоміжних речовин.
23. Композиція за п. 22, що містить додатковий гербіцид на додаток до сполуки формули І.
24. Композиція за п. 22, що містить антидот на додаток до сполуки формули І.
23. Спосіб контролю рослин, що включає внесення гербіцидно ефективної кількості сполуки формули І пп. 1-17 або композиції за. 22, що містить таку сполуку, на рослину або її локус.
Текст
, сполука формули І+бенкарбазон (CAS RN 173980-17-1), сполука формули І+бенфлуралін (59), сполука формули І+бенфуресат (61), сполука формули І+бенсульфурон-метил (64), сполука формули І+бенсулід (65), сполука формули І+бентазон (67), сполука формули І+бензфендізон (CAS RN 158755-95-4), сполука формули І+бензобіциклон (69), сполука формули І+бензофенап (70), сполука формули І+біфенокс (75), сполука формули І+біланафос (біалафос) (77), сполука формули І+біспірибакнатрій (82), сполука формули І+боракс (86), сполука формули І+бромацил (90), сполука формули І+бромбутид (93), сполука формули І+бромфеноксим (CAS RN 13181-17-4), сполука формули І+бромоксиніл (95), сполука формули І+бутахлор (100), сполука формули І+бутафенацил (101), сполука формули І+бутаміфос (102), сполука формули І+бутралін (105), сполука формули І+бутроксидим (106), сполука формули І+бутилат (108) , сполука формули І+какодилова кислота (CAS RN 75-60-5), сполука формули І+хлорат кальцію (CAS RN 10137-74-3), сполука формули І+кафенстрол (110), сполука формули І+карбетамід (117), сполука формули І+карфентразонетил (121), сполука формули I+CDEA (CAS RN 2315-36-8), сполука формули І+СЕРС (CAS RN 587-56-4), сполука формули І+хлорбромурон (CAS RN 13360-45-7), сполука 45 формули І+хлорфлуренолметил (133), сполука формули І+хлоридазон (134), сполука формули І+хлоримуронетил (135), сполука формули І+хлороцтова кислота (138), сполука формули І+хлортолурон (143), сполука формули І+хлорпрофам (144), сполука формули І+хлорталдиметил (148), сполука формули І+цинідонетил (152), сполука формули І+цинметилін (153), сполука формули І+цисанілід (CAS RN 34484-77-0), сполука формули І+клефоксидим (CAS RN 211496-02-5), сполука формули І+клетодим (155), сполука формули І+кломепроп (160), сполука формули І+клопіралід (162), сполука формули І+СМА (CAS RN 5902-954), сполука формули І+4-СРВ (CAS RN 3547-07-7), сполука формули I+CPMF, сполука формули І+4СРР (CAS RN 3307-39-9), сполука формули І+СРРС (CAS RN 2150-32-5), сполука формули І+крезол (CAS RN 1319-77-3), сполука формули І+кумілурон (180), сполука формули І+ціанамід (182), сполука формули І+цикланілід (186), сполука формули І+циклоат (187), сполука формули І+циклосульфурон (189), сполука формули І+циклоксидим (190), сполука формули І+цихалофоп-бутил (195), сполука формули I+2,4D (211), сполука формули I+3,4-DA (CAS RN 58822-7), сполука формули І+даімурон (213), сполука формули І+далапон (214), сполука формули І+дазомет (216), сполука формули I+2,4-DB (217), сполука формули I+3,4-DB, сполука формули І+2,4-DEB (CAS RN 94-83-7), сполука формули І+десмедифам (225), сполука формули І+десметрин (CAS RN 1014-69-3), сполука формули І+дикамба (228), сполука формули І+дихлобеніл (229), сполука формули І+ортодихлорбензол (CAS RN 95-50-1), сполука формули І+пара-дихлорбензол (CAS RN 106-46-7), сполука формули І+дихлорпроп (234), сполука формули І+дихлорпроп-Р (235), сполука формули І+диклофопметил (238), сполука формули І+диклозулам (241), сполука формули І+дифезокватметилсульфат (248), сполука формули І+дифлуфеникам (251), сполука формули І+дифлуфензопір (252), сполука формули І+димефурон (256), сполука формули І+димепіперат (257), сполука формули І+диметахлор (258), сполука формули І+диметенамід (260), сполука формули І+диметенамід-Р, сполука формули І+диметипін (261), сполука формули І+какодилова кислота (264), сполука формули І+динітрамін (268), сполука формули І+динотерб (272), сполука формули І+дифенамід (274), сполука формули І+дипропетрин (CAS RN 4147-51-7), сполука формули І+дикват дибромід (276), сполука формули І+дитіопір (280), сполука формули І+діурон (281), сполука формули I+DNOC (282), сполука формули I+3,4-DP (CAS RN 3307-41-3), сполука формули I+DSMA (CAS RN 144-21-8), сполука формули І+ЕВЕР, сполука формули І+ендотал (295), сполука формули І+ЕРТС (299), сполука формули І+еспрокарб (303), сполука формули І+еталфлуралін (305), сполука формули І+етефон (307), сполука формули І+етофумесат (311), сполука формули І+етоксифен (CAS RN 188634-90-4), 92210 46 сполука формули І+етоксифен-етил (CAS RN 131086-42-5), сполука формули І+етоксисульфурон (314), сполука формули І+етобензанід (318), сполука формули І+феноксапроп-р-етил (339), сполука формули І+фентразамід (348), сполука формули І+сульфат заліза (353), сполука формули І+флампроп, сполука формули І+флампроп-М (355), сполука формули І+флорасулам (359), сполука формули І+флуазифоп-бутил (361), сполука формули І+флуазифоп-Р-бутил (362), сполука формули І+флуазолат (ізопропазол) (CAS RN 174514-07-9), сполука формули І+флукарбазоннатрій (364), сполука формули І+флуцетосульфурон (CAS RN 412928-75-7), сполука формули І+флухлоралін (365), сполука формули І+флуфенацет (BAY FOE 5043) (369), сполука формули І+флуфенпіретил (371), сполука формули І+флуметралін (373), сполука формули І+флуміклорак-пентил (375), сполука формули І+флуміпропін (флуміпропін) (CAS RN 84478-52-4), сполука формули І+фторметурон (378), сполука формули І+фторглікофенетил (380), сполука формули І+флупоксам (CAS RN 11912615-7), сполука формули І+флупропацил (CAS RN 120890-70-2), сполука формули І+флупропанат (383), сполука формули І+флупирсульфуронметилнатрій (384), сполука формули І+флуренол (387), сполука формули І+флуридон (388), сполука формули І+фторхлоридон (389), сполука формули І+флуроксипір (390), сполука формули І+флуртамон (392), сполука формули І+флутіацетметил (395), сполука формули І+фосамін (406), сполука формули формули І+НС252 (429), мазасульфурон (456), сполука формули І+інданофан (462), сполука формули І+йодметан (CAS RN 74-88-4), сполука формули ГНоксиніл (467), сполука формули І+ізопротурон (475), сполука формули І+ізоурон (476), сполука формули І+ізоксабен (477), сполука формули І+ізоксахлортол (CAS RN 141112-06-3), сполука формули І+ізоксапірифоп (CAS RN 87757-18-4), сполука формули І+карбутилат (482), сполука формули І+лактофен (486), сполука формули І+ленацил (487), сполука формули І+лінурон (489), сполука формули І+МАА (CAS RN 124-58-3), сполука формули І+МАМА (CAS RN 2321-53-1), сполука формули І+МСРА (499), сполука формули І+МСРА-тіоетил (500), сполука формули І+МСРВ (501), сполука формули І+мекопроп (503), сполука формули І+мекопроп-Р (504), сполука формули І+мефенацет (505), сполука формули І+мефлуидид (507), сполука формули І+мезосульфурон-метил (514), сполука формули І+метам (519), сполука формули І+метаміфоп (мефлуоксафоп) (520), сполука формули І+метабензтіазурон (526), сполука формули І+метазол (CAS RN 20354-26-1), сполука формули І+метиларсонова кислота (536), сполука формули І+метилдимрон (539), сполука формули І+метилізотіоціанат (543), сполука формули І+метобензурон (547), сполука формули І+метобромурон (CAS RN 3060-89-7), сполука формули І+метосулам (552), сполука формули І+метоксурон (553), сполука формули І+МК-616 47 (559), сполука формули І+молінат (560), сполука формули І+монолінурон (562), сполука формули I+MSMA (CAS RN 2163-80-6), сполука формули І+напроаналід (571), сполука формули І+напропамід (572), сполука формули І+напталам (573), сполука формули І+небурон (574), сполука формули І+нипіраклофен (CAS RN 99662-11-0), сполука формули І+н-метилгліфосат, сполука формули І+нонанова кислота (583), сполука формули І+норфлуразон (584), сполука формули І+олеїнова кислота (жирні кислоти) (593), сполука формули І+орбенкарб (595), сполука формули І+ортосульфамурон (CAS RN 213464-77-8), сполука формули І+оризалін (597), сполука формули І+оксадіаргіл (599), сполука формули І+оксадіазон (600), сполука формули І+оксацикломефон (604), сполука формули І+оксифлуорфен (610), сполука формули І+пебулат (617), сполука формули І+пеноксулам (622), сполука формули І+пентахлорфенол (623), сполука формули І+пентанохлор (624), сполука формули І+пентоксазон (625), сполука формули І+петоксамід (627), сполука формули І+петролейні масла (628), сполука формули І+фенмедифам (629), сполука формули І+піклорам (645), сполука формули І+піколінафен (646), сполука формули І+піперофос (650), сполука формули І+арсеніт калію (CAS RN 10124-50-2), сполука формули І+азид калію (CAS RN 20762-80-1), сполука формули І+претилахлор (656), сполука формули І+продіамін (661), сполука формули І+профлуазол (CAS RN 190314-43-3), сполука формули І+профоксидим (663), сполука формули І+прогексадіон кальцій (664), сполука формули І+пропахлор (667), сполука формули І+пропаніл (669), сполука формули І+пропаквізафоп (670), сполука формули І+пропам (674), сполука формули І+пропізохлор (667), сполука формули І+пропоксикабзаноннатрій (прокарбазоннатрій) (679), сполука формули І+пропізамід (681), сполука формули І+просульфокарб (683), сполука формули І+піраклоніл (піразогіл) (CAS RN 158353-15-2), сполука формули І+пірафлуфенетил (691), сполука формули І+пірасульфотол (CAS RN 365400-11-9), сполука формули І+піразолінат (692), сполука формули І+піразосульфурон-етил (694), сполука формули І+піразоксифен (695), сполука формули І+пірибензоксим (697), сполука формули І+пірибутикарб (698), сполука формули І+піридафол (CAS RN 40020-01-7), сполука формули І+піридат (702), сполука формули І+пірифталід (704), сполука формули І+піримінобакметил (707), сполука формули І+піримісульфан (CAS RN 221205-90-9), сполука формули І+піроксасульфон (CAS RN 447399-55-5), сполука формули І+піроксулам (трифлосулам) (CAS RN 422556-08-9), сполука формули І+квінклорак (712), сполука формули І+квінмерак (713), сполука формули І+квінокламін (714), сполука формули І+квізалофоп (717), сполука формули І+квізалофоп-Р (718), сполука формули І+секвестрен, сполука формули І+сетоксидим (726), сполука формули І+сидурон (727), сполука формули I+SMA (CAS RN 3926-62-3), сполука формули І+арсеніт натрію (CAS RN 7784-46-5), сполука формули І+азид натрію (CAS RN 26628-22-8), 92210 48 сполука формули І+хлорат натрію (734), сполука формули І+сульфометурон-метил (751), сполука формули І+сульфосат (CAS RN 81591-81-3), сполука формули І+сірчана кислота (755), сполука формули І+дьогтьові масла (758), сполука формули І+2,3,6-ТВА (759), сполука формули І+ТСАнатрій (760), сполука формули І+тебутам (CAS RN 35256-85-0), сполука формули І+тебутиурон (765), сполука формули І+тепралоксидим (771), сполука формули І+тербацил (772), сполука формули І+тефурилтрион (CAS RN 473278-76-1), сполука формули І+тенілхлор (789), сполука формули І+тидиазимин (CAS RN 123249-43-4), сполука формули І+тиазафлурон (CAS RN 25366-23-8), сполука формули І+тіазопір (793), сполука формули І+тіобенкарб (797), сполука формули І+тіокарбацил (807), сполука формули І+тралкоксидим (811), сполука формули І+триалат (816), сполука формули І+триазифлам (819), сполука формули І+трикамба (CAS RN 2307-49-5), сполука формули І+триклопір (827), сполука формули І+трифлусульфурон-метил (837), сполука формули І+тригідрокситриазин (CAS RN 108-80-5), сполука формули І+тринексапак-етил (CAS RN 95266-40-3) і сполука формули І+тритосульфурон (843). Партнери по суміші сполуки формули І можуть також бути у вигляді ефірів і солей, як приведено в The Pesticide Manual, 13th Edition (BCPC), 2003. Посилання на ацифлуорфеннатрій також застосовне до ацифлуорфену, і посилання на бенсульфуронметил також застосовне до бенсульфурону і т.д. Відношення компонента формули І до партнера по змішуванню складає переважно від 1:100 до 1000:1. Суміші можна з успіхом використовувати в згаданих вище композиціях (у тому випадку «активний інгредієнт» належить до відповідного суміші сполуки формули І і партнера по змішуванню). Сполуку формули І відповідно до даного винаходу можна також використовувати в комбінації з одним або декількома антидотами. Аналогічно, суміші сполуки формули І, відповідно до даного винаходу, з одним або декількома додатковими гербіцидами можна також використовувати в комбінації з одним або декількома антидотами. Антидотами можуть бути AD 67 (MON 4660) (11), беноксакор (63), клоквінтоцетметил (163), циометриніл і відповідний (Z) ізомер, ципросульфамід (CAS RN 221667-31-8), дихлормід (231), фенхлоразолетил (331), фенхлорим (332), флуразол (386), флуксофенім (399), фурилазол (413) і відповідний R ізомер, ізоксадифенетил (478), мефенпірдіетил (506), оксабетриніл (598), нафталіновий ангідрид (CAS RN 81-84-5) і N-ізопропіл-4-(2метоксибензоїлсульфамоїл)бензамід (CAS RN 221668-34-4). Особливо переважними є суміші сполуки І з беноксакором (наприклад, сполука формули І+беноксакор). Антидоти сполуки формули І можуть також бути у вигляді ефірів або солей, як приведено, наприклад, у The Pesticide Manual, 13th Edition (BCPC), 2003. Посилання на клоквінтоцетметил також застосовне до літію, натрію, калію, кальцію, магнію, алюмінію, залізу, амонію, четвер 49 92210 50 тинного амонію, їх сульфонієвої або фосфонієвої солей, як описано в WO 02/34048, і посилання на фенхлоразолетил також застосовне до фенхлоразолу і т. д. Переважне відношення в суміші сполуки формули І до антидота складають від 100:1 до 1:10, особливо від 20:1 до 1:1. Суміші можна з успіхом використовувати в приведених вище композиціях (у тому випадку «активний інгредієнт» належить до відповідної суміші сполуки формули І і антидота). Переважні суміші сполуки формули І з додатковими гербіцидами й антидотами включають: Суміші сполуки формули І із триазином і антидотом. Суміші сполуки формули І з гліфосатом і антидотом. Суміші сполуки формули І із глюфосинатом і антидотом. Суміші сполуки формули І з ізоксафлутолом і антидотом. Суміші сполуки формули І з ізоксафлутолом і триазином і антидотом. Суміші сполуки формули І з ізоксафлутолом і гліфосатом і антидотом. Суміші сполуки формули І з ізоксафлутолом і глюфосинатом і антидотом. Суміші сполуки формули І з мезотрионом і антидотом. Суміші сполуки формули І з мезотрионом і триазином і антидотом. Суміші сполуки формули І з мезотрионом і гліфосатом і антидотом. Суміші сполуки формули І з мезотрионом і глюфосинатом і антидотом. Суміші сполуки формули І із сулкотрионом антидотом. Суміші сполуки формули І із сулкотрионом і триазином і антидотом. Суміші сполуки формули І із сулкотрионом і глифосинатом і антидотом. Суміші сполуки формули І із сулкотрионом і глюфосинатом і антидотом. Наступні приклади додатково ілюструють, але не обмежують даний винахід. Приклади одержання 1) Способи одержання 5,5-диметил-4,5дигідроізоксазольних похідних Приклад II: Одержання гідроксімінооцтової кислоти Гідроксімінооцтову кислоту (приклад II) (107г, 1,2моль) розчиняли в 1,2-диметоксіетані (1,4л) і нагрівали до 70°С. Додавали порціями протягом 1 години при 70°С N-хлорсукцинімід (NCS) (320,4г, 2,4моль). Реакційну суміш перемішували при 70°С протягом 1 години. Реакційну суміш охолоджували до 5°С і додавали гідрокарбонат калію (535г, 4,45ммоль) і воду (54г). У суспензію вводили 2метилпропен (134,6г, 2,4моль) протягом 20 хвилин при 5°С. Реакційну суміш нагрівали до кімнатної температури і перемішували при кімнатній температурі протягом 18 годин. Реакційну суміш вили вали у воду (1,5л) і суміш екстрагували гексаном (3 500мл). Об'єднані органічні екстракти промивали насиченим розчином солі, сушили над сульфатом натрію і концентрували. Залишок переганяли, з одержанням 3-хлор-5,5-диметил-4,5дигідроізоксазолу у вигляді рідини (60,7г, 37,8% вихід). 1 Н-NMR (400МГц, CDCI3): 1,47 (с, 6Н, Me), 2,92 (с, 2Н, СН2) м. ч. Приклад I3: Одержання 5,5диметилізоксалідин-3-ону Натрій (1,72г, 75ммоль) розчиняли в метанолі (30мл) при кімнатній температурі. Повільно додавали гідроксисечовину (3,8г, 50ммоль), потім додавали по краплях етилдиметилакрилат (6,4г, 50ммоль). Реакційну суміш витримували при кімнатній температурі протягом 18 годин. Твердий залишок видаляли фільтруванням і фільтрат кон центрували. Залишок розчиняли у воді і перемішували протягом 15 хвилин, потім додавали по краплях водну хлористоводневу кислоту (2М), для підкислення суміші. Водний розчин екстрагували хлороформом. Органічний екстракт промивали насиченим розчином солі, сушили над сульфатом магнію і концентрували, з одержанням 5,5 Водну гліоксилову кислоту (50% по масі) (11,9моль) і гідрохлорид гідроксиламіну (627г, 9моль) змішували і концентрували. Додавали ацетонітрил (1л), розчин охолоджували до 5°С і фільтрували. Маточний розчин концентрували до 50% об'єму, залишали на ніч при 5°С і повторно фільтрували. Процедуру повторювали двічі. Тверді залишки об'єднували і сушили, з одержанням гідроксімінооцтової кислоти у вигляді білих кристалів (546г, 68%). Приклад I2: Одержання 3-хлор-5,5-диметил4,5-дигідроізоксазолу 51 диметилізоксалідин-3-ону у вигляді білої твердої речовини (2,8г, 49% вихід). 1 Н-ЯМР (400МГц, CDCI3): 1,43 (с, 6Н, Me), 2,58 (с, 2Н, СН2) м. ч. Приклад I4: Одержання 3-хлор-5,5-диметил4,5-дигідроізоксазолу 92210 52 (10мл) і кип'ятили зі зворотним холодильником протягом 5 годин. Реакційну суміш концентрували і залишок розподіляли між водою і діетиловим ефіром. Фази розділяли й органічну фазу промивали насиченим розчином солі, сушили над сульфатом магнію і концентрували, з одержанням 3-хлор-5,5іметил-4,5-дигідроізоксазолу у вигляді коричневого, текучого масла (0,4г, 69% вихід). Приклад I5: Одержання 2-(5,5-диметил-4,5дигідроізоксазол-3-іл)дисульфіду 5,5-Диметилізоксалідин-3-он (приклад I3) (0,5г, 0,57ммоль) розчиняли в оксихлориді фосфору Гідрохлорид 2-(5,5-диметил-4,5дигідроізксазол-3-іл)ізотіосечовини (29г, 138ммоль) (отриманий, як описано в WO 06/068092) і карбонат калію (39г, 416ммоль) розчиняли в метанолі (250мл) і додавали порціями при кімнатній температурі йод (18г, 100ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 1 години. Реакційну суміш концентрували, залишок розчиняли у воді і водній суміші екстрагували декілька разів етилацетатом. Об'єднані органічні екстракти промивали водою і насиченим розчином солі, сушили над сульфатом магнію і концентрували, з одержанням 2-(5,5диметил-4,5-дигідроізоксазол-3-іл)дисульфіду у вигляді блідо-жовтої твердої речовини (14,1г, 78% вихід). 2) Способи одержання триазольних похідних Синтез етилового ефіру 1-трет-бутил-1Н[1,2,3]триазол-4-карбонової кислоти описана в Synthesis, 1985, 178-180. Етиловий ефір 1-трет-бутил-1Н-[1,2,3]триазол4-карбонової кислоти відновлюють, як описано в прикладі I6, з одержанням 1-трет-бутил-1Н[1,2,3]триазол-4-іл]метанолу. 1 Н-ЯМР (400МГц, CDCI3): 1,65 (с, 9Н, Me), 4,76 (с, 2Н, СН2), 7,60 (с, 1Н, СН) м. ч. 1-трет-бутил-1Н-[1,2,3]триазол-4-іл]метанол бромують, як описано в прикладі I7, з одержанням 4-бромметил-1-трет-бутил-1Н-[1,2,3]триазолу. 1 Н-ЯМР (400МГц, CDCI3): 1,65 (с, 9Н, Me), 4,58 (с, 2Н, СН2), 7,63 (с, 1Н, СН) м. ч. Синтез метилового ефіру 5-(дифторметил)-2метил-2Н-[1,2,3]триазол-4-карбонової кислоти описана в WO 2004/018438. Приклад I6: Одержання (5-фторметил-2метил-2Н-[1,2,3]триазол-4-іл)метанолу і (2,5диметил-2Н-[1,2,3]триазол-4-іл)метанолу До розчину літійалюмінійгідриду (2М у ТГФ) (2,83мл, 5,65ммоль) у тетрагідрофурані (10мл) додавали по краплях розчин метилового ефіру 5фторметил-2-метил-2Н-[1,2,3]триазол-4карбонової кислоти (отриманої, як описано в WO 04/018438) (978мг, 5,65ммоль) у тетрагідрофурані (10мл) при 0°С. Реакційну суміш нагрівали до кімнатної температури і перемішували при кімнатній температурі протягом 40 хвилин. Реакційну суміш гасили послідовним додаванням води (200мкл), водного гідроксиду натрію (2М) (350мкл) і води (400мкл). Осад видаляли фільтруванням і фільтрат упарювали, з одержанням суміші 4:1 (5фторметил-2-метил-2Н-[1,2,3]триазол-4іл)метанолу і (2,5-диметил-2Н-[1,2,3]триазол-4іл)метанолу у вигляді блідо-жовтої рідини (610мг, 76% вихід). 1 Н-ЯМР (400МГц, CDCI3): 4,19 (д, 3Н, Me), 4,83 (с, 2Н, СН2), 5,52 (д, 2Н, СН2) м. ч. 1 Н-ЯМР (400МГц, CDCI3): 2,31 (с, 3Н, Me), 4,11 (с, 3Н, Me), 4,72 (с, 2Н, СН2) м. ч. Аналогічну методику використовували з етиловим ефіром 2-метил-5-трифторметил-2Н[1,2,3]триазол-4-карбонової кислоти (отриманої, як описано в WO 04/018438) як вихідну сполуку, з одержанням (2-метил-5-трифторметил-2Н[1,2,3]триазол-4-іл)метанолу. 1 Н-ЯМР (400МГц, CDCI3): 2,03 (т, 1Н, ОН), 4,24 (с, 3Н, Me), 4,84 (д, 2Н, СН2) м. ч. Приклад I7: Одержання 4-бромметил-5фторметил-2-метил-2Н-[1,2,3]триазолу і 4бромметил-2,5-диметил-2Н-[1,2,3]триазолу 53 Суміш 4:1 (5-фторметил-2-метил-2Н[1,2,3]триазол-4-іл)метанолу і (2,5-диметил-2Н[1,2,3]триазол-4-іл)метанолу (610мг, 4,21ммоль) (приклад I6) розчиняли в діетиловому ефірі (10мл) в атмосфері аргону при кімнатній температурі і додавали трибромід фосфору (395мкл, 4,21ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 24 годин. Реакційну суміш гасили додаванням холодної води і суміш екстрагували три рази етилацетатом. Об'єднані органічні екстракти промивали насиченим розчином солі, сушили над сульфатом магнію і концентрували, з одержанням суміші 4:1 4-бромметил-5фторметил-2-метил-2Н-[1,2,3]триазолу і 4бромметил-2,5-диметил-2Н-[1,2,3]триазолу у вигляді жовтогарячої рідини (954мг). 1 Н-ЯМР (400МГц, CDCI3): 4,18 (д, 3Н, Me), 4,57 (с, 2Н, СН2), 5,51 (д, 2Н, СН2) м. ч. 1 Н-ЯМР (400МГц, CDCI3): 2,31 (с, 3Н, Me), 4,11 (с, 3Н, Me), 4,50 (с, 2Н, СН2) м. ч. Аналогічну методику використовували з (2метил-5-трифторметил-2Н-[1,2,3]триазол-4іл)метанолом як вихідну сполуку, з одержанням 4бромметил-2-метил-5-трифторметил-2Н[1,2,3]триазолу. 1 Н-ЯМР (400МГц, CDCI3): 4,19 (с, 3Н, Me), 4,49 (с, 2Н, СН2) м. ч. Приклад I8: Одержання оксиму 3(метилгідразон)бутан-2-ону Монооксим бутан-2,3-діону (2,6г, 25,8ммоль) розчиняли в етанолі (100мл), потім додавали при кімнатній температурі метилгідразин (1,13г, 24,5ммоль). Реакційну суміш перемішували при 80°С протягом 2 годин. Додавали метилгідразин (0,6г, 12ммоль) і реакційну суміш перемішували при 80°С протягом 1,5 годин, потім при кімнатній температурі протягом 48 годин. Реакційну суміш концентрували, з одержанням оксиму 3(метилгідразон)бутан-2-ону у вигляді блідо-жовтої, кристалічної твердої речовини (3,3г, 100% вихід). 1 Н-ЯМР (400МГц, CDCI3): 1,89 (с, 3Н, Me), 2,11 (с, 3Н, Me), 3,09 (с, 3Н, Me), 4,8-5,3 (ушир.с, 1Н, ОН) м. ч. Приклад I9: Одержання 2А5-триметил-2Н[1,2,3]триазол-1-оксиду Оксим 3-(метилгідразон)бутан-2-ону (3,3г, 25,8ммоль) (приклад I8) розчиняли в тетрагідро 92210 54 фурані (135мл), потім додавали водний піридин (15%) (157мл, 0,29моль), з наступним додаванням суспензії сульфату міді (II) (15,7г, 62,8ммоль) у воді (35мл). Реакційну суміш перемішували при 80°С протягом 2 годин, потім охолоджували до кімнатної температури й екстрагували три рази етилацетатом. Об'єднані органічні екстракти промивали водним сульфатом міді (II) (10%), сушили над сульфатом магнію і концентрували. Залишок очищали колонковою хроматографією на силікагелі (градієнт: метанол/дихлорметан), з одержанням 2,4,5-триметил-2Н-[1,2,3]триазол-1-оксиду у вигляді безбарвної рідини (0,7г, 21% вихід). 1 Н-ЯМР (400 МГц3 CDCI3): 2,19 (с, 3Н, Me), 2,23 (с, 3Н, Me), 3,93 (с, 3Н, Me) м. ч. Приклад I10: Одержання 5-бромметил-2,4Диметил-2Н-[1,2,3]триазол-1-оксиду N-Бромсукцинімід (NBS) (186мг, 1,0ммоль) і 2,2'-азобісізобутиронітрил (AIBN) (14мг, 0,087ммоль) додавали до розчину 2,4,5-триметил2Н-[1,2,3]триазол-1-оксиду (110мг, 0,87ммоль) (приклад I9) у тетрахлориді вуглецю (7мл). Реакційну суміш нагрівали при 70°С протягом 1 години, потім охолоджували до кімнатної температури і фільтрували. Розчинник видаляли, з одержанням 5-бромметил-2,4-диметил-2Н-[1,2,3]триазол-1оксиду у вигляді коричневої смоли. 1 Н-ЯМР (400МГц, CDCI3): 2,31 (с, 3Н, Me), 3,95 (с, 3Н, Me), 4,42 (с, 2Н, СН2) м. ч. Приклад I11: Альтернативне одержання 4бромметил-2,5-диметил-2Н-[1,2,3]триазолу 5-бромметил-2,4-диметил-2Н-[1,2,3]триазол-1оксид (4,83г, 23,3ммоль) (приклад I10) розчиняли в тетрахлориді вуглецю (50мл), потім додавали по краплях трихлорид фосфору (6,8мл, 77,8моль). Реакційну суміш перемішували при 75°С протягом 2,5 годин. Реакційну суміш гасили повільним додаванням до гарячої води, потім охолоджували і розбавляли холодною водою. Фази розділяли і водну фазу екстрагували двічі дихлорметаном. Об'єднані органічні екстракти промивали водою і насиченим розчином солі, сушили над сульфатом магнію і концентрували. Залишок очищали колонковою хроматографією на силікагелі (градієнт: метанол/дихлорметан), з одержанням 4бромметил-2,5-диметил-2Н-[1,2,3]триазол у вигляді жовтої олії (1,47г, 33% вихід). 55 92210 56 1 Н-ЯМР (400МГц, CDCI3): 2,3 (с, 3Н, Me), 4,1 (с, 3Н, Me), 5,5 (с, 2Н, СН2) м. ч. Приклад I12: Одержання метилового ефіру 1(4-метоксибензил)-5-метил-1Н-[1,2,3]триазол-4 карбонової кислоти і метилового ефіру 3-(4метоксибензил)-5-метил-3Н-[1,2,3]триазол-4карбонової кислоти 4-метоксибензилазид (отриманий, як описано, наприклад, у J. Chem. Soc, Perkin Trans. 1, 1982 (2), 627-630) (5,47г, 33,6ммоль) розчиняли в толуолі (20мл) і додавали по краплях при кімнатній температурі протягом 5 хвилин метил-2-бутиноат (6,72мл, 67,1ммоль). Реакційну суміш нагрівали при 100°С протягом 14 годин. Розчин охолоджували до кімнатної температури і розчинник упарювали, з одержанням світло-жовтої рідини, що очищали колонковою хроматографією на силікагелі (градієнт: 0-50% етилацетат у гексані), з одержанням суміші метилового ефіру 1-(4-метоксибензил)5-метил-1H-[1,2,3]триазол-4-карбонової кислоти і метилового ефіру 3-(4-метоксибензил)-5-метил3Н-[1,2,3]триазол-4-карбонової кислоти у вигляді світло-жовтої олії (7,35г, 85% вихід). Ізомер 1 (основний) 1Н-ЯМР (400МГц, CDCI3): 2,46 (с, 3Н, Me), 3,79 (с, 3Н, Me), 3,94 (с, 3Н, Me), 5,47 (с, 2Н, СН2), 6,82-6,88 (м, 2Н, СН), 7,13 (д, 2Н, СН) м. ч. Ізомер 2 (неосновний) 1Н-ЯМР (400МГц, CDCI3): 2,51 (с, 3Н, Me), 3,77 (с, 3Н, Me), 3,90 (с, 3Н, Me), 5,80 (с, 2Н, СН2), 6,82-6,88 (м, 2Н, СН), 7,28 (д, 2Н, СН) м. ч. Аналогічну методику використовували з етиловим ефіром пент-2-инової кислоти як вихідної сполуки, з одержанням суміші етилового ефіру 5етил-1-(4-метоксибензил)-1Н-[1,2,3]триазол-4карбонової кислоти й етилового ефіру 5-етил-3-(4метоксибензил)-3Н-[1,2,3]триазол-4-карбонової кислоти. Ізомер 1 (основний) 1Н-ЯМР (400МГц, CDCI3): 1,00 (т, 3Н, Me), 1,42 (т, 3Н, Me), 2,88-2,96 (м, 2Н, СН2), 3,79 (с, 3Н, Me), 4,42 (кв, 2Н, СН2), 5,48 (с, 2Н, СН2), 6,82-6,87 (м, 2Н, СН), 7,14 (д, 2Н, СН) м. ч. Ізомер 2 (неосновний) 1Н-ЯМР (400МГц, CDCI3): 1,29 (т, 3Н, Me), 1,36 (т, 3Н, Me), 2,88-2,96 (м, 2Н, СН2), 3,78 (с, 3Н, Me), 4,35 (кв, 2Н, СН2), 5,81 (с, 2Н, СН2), 6,82-6,87 (м, 2Н, СН), 7,28 (д, 2Н, СН) м. ч. Приклад I13: Одержання метилового ефіру 5метил-2Н-[1,2,3]триазол-4-карбонової кислоти Суміш метилового ефіру 1-(4-метоксибензил)5-метил-1Н-[1,2,3]триазол-4-карбонової кислоти і метилового ефіру 3-(4-метоксибензил)-5-метил3Н-[1,2,3]триазол-4-карбонової кислоти (приклад I12) (7,35г, 28,6ммоль) розчиняли в суміші ацетонітрил/вода (9:1) (100мл) і додавали церій(IV)амонійнітрат (CAN) (31,4г, 57,2ммоль). Розчин перемішували при кімнатній температурі протягом 16 годин. Розчинник упарювали і залишок розподіляли між водою і етилацетатом. Фази розділяли і водну фазу екстрагували двічі великою кількістю етилацетату. Об'єднані органічні екстрак ти промивали насиченим розчином солі, сушили над сульфатом магнію і концентрували. До залишку додавали дихлорметан (50мл), що викликав випадання білого твердого осаду (1,77г, 40% вихід). Тверду речовину виділяли фільтруванням. Маточний розчин упарювали і залишок знову обробляли дихлорметаном (50мл). Це приводило до випадання більшої кількості білого твердого осаду. Осад відділяли фільтруванням і об'єднані осади сушили, з одержанням метилового ефіру 5-метил2Н-[1,2,3]триазол-4-карбонової кислоти (2,6г, 59% вихід). 57 1 Н-ЯМР (400МГц, CDCI3): 2,62 (с, 3Н, Me), 4,0 (с, 3Н, Me) м. ч. Аналогічну методику використовували із сумішшю етилового ефіру 5-етил-1-(4-метоксибензил)1H-[1,2,3]триазол-4-карбонової кислоти й етилового ефіру 5-етил-3-(4-метоксибензил)-3Н[1,2,3]триазол-4-карбонової кислоти, як вихідні сполуки, з одержанням етилового ефіру 5-етил2Н-[1,2,3]триазол-4-карбонової кислоти. 1 Н-ЯМР (400МГц, CDCI3): 1,36 (т, 3Н, Me), 1,42 (т, 3Η, Me), 3,08 (кв, 2Н, СН2), 4,44 (кв, 2Н, СН2) м. ч. Приклад I14: Одержання метилового ефіру 2етил-5-метил-2Н-[1,2,3]триазол-4-карбонової кислоти, метилового ефіру 3-етил-5-метил-3Н[1,2,3]триазол-4-карбонової кислоти і метилового ефіру 1-етил-5-метил-1Н-[1,2,3]триазол-4карбонової кислоти Метиловий ефір 5-метил-2Н-[1,2,3]триазол-4карбонової кислоти (1,77г, 12,6ммоль) (приклад I13) розчиняли в Ν,Ν-диметилформаміді (12мл) і додавали при 0°С етилйодид (16,3ммоль, 1,31мл) і карбонат калію (2,26г, 16,3ммоль). Реакційну суміш нагрівали до кімнатної температури і перемішували протягом 5 годин в атмосфері азоту. Розчин розподіляли між водою і діетиловим ефіром. Фази розділяли, водну фазу екстрагували двічі великою кількістю діетилового ефіру. Об'єднані органічні екстракти промивали насиченим розчином солі, сушили над сульфатом магнію і концентрували, з одержанням суміші метилового ефіру 2етил-5-метил-2Н-[1,2,3]триазол-4-карбонової кислоти, метилового ефіру 3-етил-5-метил-3Н[1,2,3]триазол-4-карбонової кислоти і метилового ефіру 1-етил-5-метил-1Н-[1,2,3]триазол-4карбонової кислоти у вигляді жовтого масла (1,10г, 52% вихід). Ізомер 1 (основний) 1Н-ЯМР (400МГц, CDCI3): 1,6 (т, 3Н, Me), 2,52 (с, 3Н, Me), 3,95 (с, 3Н, Me), 4,45 (кв, 2Н, СН2) м. ч. Ізомер 2 (середній по кількості) 1Н-ЯМР (400МГц, CDCI3): 1,5 (т, 3Н, Me), 2,54 (с, 3Н, Me), 3,96 (с, 3Н, Me), 4,73 (кв, 2Н, СН2) м. ч. Ізомер 3 (неосновний) 1Н-ЯМР (400МГц, CDCI3): 1,53 (т, 3Н, Me), 2,6 (с, 3Н, Me), 3,95 (с, 3Н, Me), 4,35 (кв, 2Н, СН2) м. ч. Аналогічну методику використовували з етиловим ефіром 5-метил-2Н-[1,2,3]триазол-4карбонової кислоти як вихідну сполуку (отриманий, як описано в прикладі I12 з етил-2-бутиноату, з наступним видаленням захисної групи, як описано в прикладі I13) і ізопропілйодидом як реагентом, з одержанням етилового ефіру 2-ізопропіл-5-метил2Н-[1,2,3]триазол-4-карбонової кислоти, етилового ефіру 3-ізопропіл-5-метил-3Н-[1,2,3]триазол-4карбонової кислоти й етилового ефіру 1-ізопропіл5-метил-1Н-[1,2,3]триазол-4-карбонової кислоти. Ізомер 1 (основний) 1Н-ЯМР (400МГц, CDCI3): 1,38-1,44 (м, 3Н, Me), 1,56-1,63 (м, 6Н, Me), 2,52 (с, 92210 58 3Н, Me), 4,31-4,45 (м, 2Н, СН2), 4,83 (септ, 1Н, СН) м. ч. Ізомер 2 (середній по кількості) 1Н-ЯМР (400МГц, CDCI3): 1,38-1,44 (м, 3Н, Me), 1,56-1,63 (м, 6Н, Me), 2,53 (с, 3Н, Me), 4,31-4,45 (м, 2Н, СН2), 5,44 (септ, 1Н, СН) м. ч. Ізомер 3 (неосновний) 1Н-ЯМР (400МГц, CDCI3): 1,38-1,44 (м, 3Н, Me), 1,56-1,63 (м, 6Н, Me), 2,59 (с, 3Н, Me), 4,31-4,45 (м, 2Н, СН2), 4,58 (септ, 1Н, СН) м. ч. Аналогічну методику використовували з етиловим ефіром 5-етил-2Н-[1,2,3]триазол-4карбонової кислоти як вихідну сполуку і метилйодидом як реагентом, з одержанням етилового ефіру 5-етил-2-метил-2Н-[1,2,3]триазол-4-карбонової кислоти. 1 Н-ЯМР (400МГц, CDCI3): 1,32 (т, 3Н, Me), 1,41 (т, 3Н, Me), 2,95 (кв, 2Н, СН2), 4,20 (с, 3Н, Me), 4,42 (кв, 2Н, СН2) м. ч. Аналогічну методику використовували з етиловим ефіром 5-етил-2Н-[1,2,3]триазол-4карбонової кислоти як вихідну сполуку і етилйодидом як реагентом, з одержанням етилового ефіру 2,5-діетил-2Н-[1,2,3]триазол-4-карбонової кислоти. 1 Н-ЯМР (400МГц, CDCI3): 1,2-1,30 (м, 3Н, Me), 1,35-1,45 (м, 3Н, Me), 1,41 (т, 3Н, Me), 2,95 (кв, 2Н, СН2), 4,38-4,44 (м, 4Н, СН2) м. ч. Ефіри відновлювали, як описано в прикладі I6, спирти брому вали, як описано в прикладі I7, і бромметильні проміжні сполуки конденсували, як описано в прикладі I39. Приклад I15: Одержання етилового ефіру 2дифторметил-5-метил-2Н-[1,2,3]триазол-4карбонової кислоти й етилового ефіру 3дифторметил-5-метил-3Н-[1,2,3]триазол-4карбонової кислоти Гідрид натрію (60% суспензія в мінеральному маслі) (570мг, 14,2ммоль) промивали в атмосфері азоту ізогексаном і суспендували в сухому тетрагідрофурані (50мл) у тригорлій колбі, оснащеній холодильником із сухим льодом. Додавали по краплях розчин етилового ефіру 5-метил-2Н[1,2,3]триазол-4-карбонової кислоти (2г, 12,9ммоль) (приклад I13) у тетрагідрофурані (10мл). Реакційну суміш перемішували при кімнатній температурі протягом 30 хвилин. Хлордифторметан пропускали через розчин протягом 10 хвилин і реакційну суміш перемішували при кімнатній температурі протягом 1,5 годин. Більшу кількість хлордифторметану пропускали через розчин протягом декількох хвилин і реакційну суміш перемішували протягом додаткових 1,5 годин. Реакцію гасили додаванням води і суміш екстрагували етилацетатом. Об'єднані органічні екстракти промивали водою і насиченим розчином солі, сушили над сульфатом магнію і концентрували. Залишок очищали колонковою хроматографією на силікагелі (градієнт: етилацетат/ізогексан), з одержанням етилового ефіру 2-дифторметил-5-метил-2Н 59 92210 60 [1,2,3]триазол-4-карбонової кислоти (1,3г, 49% вихід) і суміші 1:2 етилового ефіру 2-дифторметил5-метил-2Н-[1,2,3]триазол-4-карбонової кислоти й етилового ефіру 3-дифторметил-5-метил-3Н[1,2,3]триазол-4-карбонової кислоти (250мг, 9% вихід). Ізомер 1 (основний) 1Н-ЯМР (400МГц, CDCI3): 1,44 (т, 3Н, Me), 2,80 (с, 3Н, Me), 4,47 (кв, 2Н, СН2), 7,64 (т, 1Н, CHF2) м. ч. Ізомер 2 (неосновний) 1Н-ЯМР (400МГц, CDCI3): 1,45 (т, 3Н, Me), 2,60 (с, 3Н, Me), 4,47 (кв, 2H, CH2), 7,33 (т, 1Н, CHF2) м. ч. Ефіри відновлювали, як описано в прикладі I6, спирти бромували, як описано в прикладі I7, і бромметильні проміжні сполуки конденсували, як описано в прикладі I39. Приклад I16: Одержання етилового ефіру 1-(4метоксибензил)-5-трифторметил-1H[1,2,3]триазол-4-карбонової кислоти й етилового ефіру 3-(4-метоксибензил)-5-трифторметил-3Н[1,2,3]триазол-4-карбонової кислоти Етил 4,4,4-трифтор-2-бутинкарбоксилат (отриманий відповідно до Organic Syntheses, 1992, 70, 246-55) (1,65г, 10,1ммоль) додавали до розчину 4-метоксибензилазиду (отриманий, як описано, наприклад, у J. Chem. Soc, Perkin Trans. 1, 1982 (2), 627-630) (1,65г, 9,9ммоль) у толуолі (10мл) і реакційну суміш перемішували при кімнатній температурі протягом 16 годин. Суміш концентрували і залишок очищали колонковою хроматографією на силікагелі (градієнт: етилацетат/ізогексан), з одержанням суміші 1,4:1 етилового ефіру 1-(4метоксибензил)-5-трифторметил-1Н[1,2,3]триазол-4-карбонової кислоти й етилового ефіру 3-(4-метоксибензил)-5-трифторметил-3Н [1,2,3]триазол-4-карбонової кислоти (2,85г, 87% вихід). Ізомер 1 (неосновний) 1Н-ЯМР (400МГц, CDCI3): 1,4 (т, 3Н, Me), 3,8 (с, 3Н, Me), 4,4 (кв, 2Н, СН2), 5,85 (с, 2Н, СН2), 6,9 (д, 2Н, СН), 7,35 (д, 2Н, СН) м. ч. Ізомер 2 (основний) 1Н-ЯМР (400МГц, CDCI3): 1,4 (т, 3Н, Me), 3,8 (с, 3Н, Me), 4,45 (кв, 2Н, СН2), 5,7 (с, 2Н, СН2), 6,85 (д, 2Н, СН), 7,2 (д, 2Н, СН) м. ч. Приклад I17: Одержання етилового ефіру 5трифторметил-2Н-[1,2,3]триазол-4-карбонової кислоти Суміш 1,4:1 етилового ефіру 1-(4метоксибензил)-5-трифторметил-1Н[1,2,3]триазол-4-карбонової кислоти й етилового ефіру 3-(4-метоксибензил)-5-трифторметил-3Н[1,2,3]триазол-4-карбонової кислоти (2,85г, 8,66ммоль) (приклад I16) розчиняли в трифтороцтовій кислоті (TFA) (15мл) і суміш нагрівали при 60°С протягом 2 годин. Реакційну суміш концентрували і залишок очищали колонковою хроматографією на силікагелі (градієнт: метанол/дихлорметан), з одержанням етилового ефіру 5-трифторметил-2Н-[1,2,3]триазол-4-карбонової кислоти (1,75г, 96,6% вихід). 1 Н-ЯМР (400МГц, CDCI3): 1,4 (т, 3Н, Me), 4,5 (кв, 2Н, СН2), 12,2-12,6 (ушир.с, 1Н, NH) м. ч. Приклад I18: Одержання етилового ефіру 2метил-5-трифторметил-2Н-[1,2,3]триазол-4кабонової кислоти, етилового ефіру 3-метил-5трифторметил-3Н-[1,2,3]триазол-4-карбонової кислоти й етилового ефіру 1-метил-5-трифторметил1Н-[1,2,3]триазол-4-карбонової кислоти
ДивитисяДодаткова інформація
Назва патенту англійськоюIsoxazoline compounds, prosess for the preparation thereof (variants), herbicidal composition and method to control plants
Автори англійськоюBoehmer Jutta Elisabeth, Mclachlan Matthew Murdoch Woodhead
Назва патенту російськоюПроизводные изоксазолина, способ их получения (варианты), гербицидная композиция и способ контроля растений
Автори російськоюБемер Ютта Элизабет, Маклечлен Меттью Мердоч Вудхед
МПК / Мітки
МПК: A01N 43/80, C07D 261/04, C07D 413/12, A01P 13/00
Мітки: спосіб, композиція, похідні, ізоксазоліну, рослин, гербіцидна, одержання, варіанти, контролю
Код посилання
<a href="https://ua.patents.su/58-92210-pokhidni-izoksazolinu-sposib-kh-oderzhannya-varianti-gerbicidna-kompoziciya-ta-sposib-kontrolyu-roslin.html" target="_blank" rel="follow" title="База патентів України">Похідні ізоксазоліну, спосіб їх одержання (варіанти), гербіцидна композиція та спосіб контролю рослин</a>
Попередній патент: Одноразовий інструмент для видалення сторонніх тіл із зовнішньої оболонки очного яблука та його придатків
Наступний патент: Інфрачервоний піроелектричний газоаналізатор
Випадковий патент: Кристалічний (r)-(e)-2-(4-(2-(5-(1-(3,5-дихлорпіридин-4-іл)етоксі)-1н-індазол-3-іл)вініл)-1н-піразол-1-іл)етанол












