Спосіб визначення додецилсульфату натрію
Номер патенту: 19579
Опубліковано: 25.12.1997
Автори: Наджафова Оксана Юріївна, Сухан Василь Васильович, Верба Валентина Вікторівна, Запорожець Ольга Антонівна
Формула / Реферат
Спосіб визначення додецил сульфату натрію шляхом вилучення органічним реагентом з водного розчину в Іншу фазу та наступного вимірювання світлопоглинання розчину, який відрізняється тим, що вилучення здійснюють з водного розчину з рН 3-8 перемішуванням протягом 30 хвилин на магнітній мішалці з 0,02 г силікагелю, модифікованого йодидом дидециламіноетил-b-тридециламонію та метиловим оранжевим, з наступним відокремленням сорбенту фільтруванням та вимірюванням світлопоглинання фільтрату.
Текст
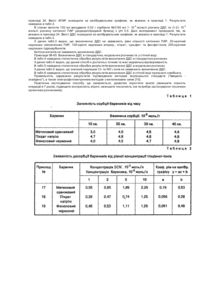
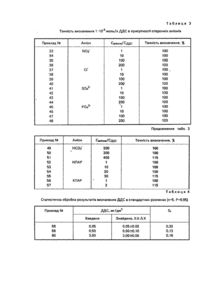
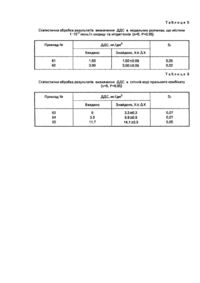
Запропонований винахід відноситься до аналітичної хімії і стосується визначення додецилсульфату натрію (ДДС) при вмісті його у розчині 0,05 - 3,0 мг/дм 3(об'єм проби 50 см 3), що може бути використано для аналізу вод різних категорій: природної, питної та стічної. Для визначення мікрокількостей ДДС у воді використовують екстракційно-фотометричні методи [1-9]. Вони грунтуються на екстрактції органічними розчинниками іонних асоціатів ДДС з барвниками катіонного типу та вимірюванні світлопоглинання органічної фази. Межа визначення складає 0,1 мг/дм 3. Основними недоліками цих методів є застосування токсичних органічних розчинників, тривалість та трудомісткість аналізу, що зумовлені багаторазовою екстракцією, а також недостатня вибірковість визначення ДДС. Найбільш близьким за технічною сутністю та результатом, що досягається, є екстракційно-фотометричний метод з використанням метиленового синього [10]. В основі методу лежить утворення іонного асоціату ДДС з метиленовим синім, що екстрагується хлороформом. Сам барвник хлороформом не екстрагується. Визначенню ДДС заважають сульфіди, сульфіти та інші відновники, що відновлюють метиленовий синій, а також великі кількості хлоридів, нітратів, тіоціанатів та білків. Заважаючий вплив цих речовин усувають, проводячи екстракцію у лужному середовищі (рН 10), потім сполучені хлороформні екстракти промивають підкисленим розчином метиленового синього. Для аналізу відбирають такий об'єм стічної води, який містить від 20 до 300 мкг ДДС. Якщо в 100 см 3 стічної води міститься менше 20 мкг ДДС, відбирають відповідно більший об'єм і випарюють до об'єма менше 100 см 3. Це призводить до ускладнення аналізу. Чутливість цього способу складає 0,05 мг/дм 3, що дозволяє надійно визначати ДДС, при вмісті їх в воді на рівні ГДК 0.5 мг/дм 3 [11]. Недоліком вказаного методу є застосування токсичних органічних розчинників, тривалість та трудомісткість аналізу, що обумовлені необхідністю випарювання проби, флотації та багаторазової екстракцією, а також недостатня вибірковість визначення ДДС. В основу винаходу поставлено задачу підвищення експресності та вибірковості, зменшення трудомісткості та токсичності визначення ДДС із збереженням чутливості. Вирішення задачі досягається тим, що в способі визначення ДДС шляхом попереднього вилучення з водного розчину в іншу фаз у органічним реагентом з наступним вимірюванням оптичної густини розчину вилучення здійснюють при рН 3-8 силікагелем, модифікованим четвертинною амонійною сіллю йодидом дидециламіноетил-b-тридециламонію та метиловим оранжевим. Використання способа визначення ДДС у воді, що заявляється, дає позитивний ефект у порівнянні з відомим способом, полягає в підвищенні експресності в три рази (35-40 хв замість 120 хв за прототипом), збільшенні вибірковості (не заважають сульфіди, сульфіти та Інші відновники, 100-кратний надлишок хлоридів, нітратів та тіоціанатів, білки, що заважають за прототипом), зменшенні токсичності (не застосовуються вогненебезпечні токсичні органічні розчинники - хлороформ, етилацетат, метанол) та трудомісткості (кількість операцій 5 - замість 36 за прототипом). Оптимальні умови визначення ДДС: сорбент №1 - силікагель "Chemapol" L 100/250 для хроматографії, модифікований йодидом дидециламіноетил-b-тридециламонію (ДДАТД). Ємність сорбенту за ДДАТД становить 0,24 ммоль/г; сорбент №2 - силікагель "Chemapol" L 100/250 для хроматографії, модифікований ДДАТД та метиловим оранжевим. Ємність силікагеля за ДДАТД та метиловим оранжевим складає 0,24 та 0,216 ммоль/г відповідно; Оптимальне рН водного розчину ДДС 3-10. Калібрувальний графік лінійний в Інтервалі концентрацій ДДС 0,05 - 3,0 мг/дм 3 при об'ємі проби 50 см 3. Границя визначення складає 0,05 мг/дм 3. Таким чином суттєвими ознаками способу, що пропонується, є те, що виділення ДДС з водної фази здійснюється при рН 3-8 силікагелем, модифікованим четвертинною амонійною сіллю йодидом дидециламіноетил-b-тридециламонію та метиловим оранжевим. Застосування силікагелю, модифікованого йодидом дидециламіноетил-β-тридециламинію та метиловим оранжевим для визначення ДДС в літературі не знайдено, що дозволяє вважати запропонований спосіб, як такий, що відповідає ознакам "новизна" та "суттєві відмінності". Приклад 1. В стакан ємністю 150 мл вміщували 0,02 г сорбенту №2 і 50 мл розчину ДДС з концентраціями 0,05-3,0 мг/дм 3 з рН 5,5. Розчин перемішували на магнітній мішалці протягом 30 хвилин. Потім розчин відфільтровували через фільтр "червона" стрічка і вимірювали оптичну густин у фільтрату на КФК-2 при l = 440 нм, І= 1см проти розчину порівняння. Розчин порівняння готували наступним чином. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл дистильованої води з рН 5,5. Розчин перемішували на магнітній мішалці протягом 30 хвилин. Потім розчин відфільтровували через фільтр "Червона" стрічка. Вміст ДДС знаходили за калібрувальним графіком, побудованим в координатах - оптична густина концентрація ДДС. Рівняння графіка - А440 - 0.0538С (мг/дм 3) + 0,14. Лінійність калібрувального графіка зберігається в інтервалі 0,05 - 3,0 мг/дм 3. Границя визначення складає - 0,05 мг/дм 3. Одержання модифікованого силікагелю. Приклади 2-4. Модифікація ДДАТД-силікагеля барвниками аніонного типу. В стакан ємністю 150 мл вміщували 0,5 г сорбенту №1 і 50 мл 5×10-3 моль/л розчину метилового оранжевого. Розчин перемішували на магнітній мішалці протягом 30 хвилин, потім відфільтровували через фільтр "червона" стрічка. Сорбент модифікований барвником промивали дистильованою водою на фільтрі до безбарвних промивних вод. Силікагель підсушували на повітрі, а потім в сушильній шафі при t=80°С [12]. Концентрацію метилового оранжевого на поверхні визначали, як різницю між вихідною та залишковою концентраціями барвника в розчині, вимірюючи фотометричним методом при l=440 нм та І=1 см. Ємність сорбента за метиловим оранжевим становила 0,216 ммоль/г. В стакан ємністю 150 мл вміщували 0,5 г сорбента. №1 і 50 мл 5 ·10-3 моль/л розчину пікрату натрію. Далі експеримент проводили так, як вказано в прикладі 2. Концентрацію пікрату натрію на поверхні визначали як в прикладі 2, вимірюючи оптичну густину фільтрату при l =364 нм та І= 1 см. Ємність сорбента за пікратом натрію становила 0,23 ммоль/г. В стакан ємністю 150 мл вміщували 0.5 г сорбента №1 і 100 мл насиченого розчину фенолового червоного. Далі експеримент проводили так, як вказано в прикладі 2. Концентрацію фенолового червоного на поверхні визначали як вказано в прикладі 2, вимірюючи оптичну густину фільтрату при l =400 нм та І= 1 см. Ємність сорбента за феноловим червоним становила 0,26 ммоль/г. Таким чином, метиловий оранжевий, пікрат натрію та феноловий червоний закріплюються на поверхні ДДАТД-силікагеля, ємність відповідно становить 0,216, 0,23 та 0,26 ммоль/г. Приклади 5-8. Обгрунтування часу сорбціт метилового оранжевого. В стакан ємністю 150 мл вміщували 0,02 г сорбента №1 і 50 мл 2×10-5 моль/л розчину метилового оранжевого. Розчин перемішували на магнітній мішалці протягом 10 хвилин і відфільтровували через фільтр "червона" стрічка. Концентрацію метилового оранжевого на поверхні визначали, як вказано в прикладі 2. Ємність сорбента за метиловим оранжевим становила - 3,0 х10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 5. Розчин перемішували протягом 20 хвилин, відфільтровували і визначали ємність сорбенту, як вказано в прикладі 2. Ємність сорбента за метиловим оранжевим становила - 4,0×10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 5. Розчин перемішували протягом 20 хвилин, відфільтровували і визначали ємність сорбенту, як вказано в прикладі 2. Ємність сорбента за метиловим оранжевим становила - 4,5×10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 5. Розчин перемішували протягом 40 хвилин, відфільтровували і визначали ємність сорбенту, як вказано в прикладі 2. Ємність сорбента за метиловим оранжевим становила - 4,6· 10-5 моль/г. Таким чином, за 30 хвилин досягається максимальна сорбція метилового оранжевого. Приклади 9-12. Обгрунтування часу сорбції пікрату натрію. В стакан ємністю 150 мл вміщували 0,02 г сорбента №1 і 50 мл 2· 10-5 моль/л розчину пікрату натрію. Далі експеримент проводили, як вказано в прикладі 5. Концентрацію пікрату натрію на поверхні визначали, як вказано в прикладі 3. Ємність сорбента за пікратом натрію становила - 4,7· 10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 9. Розчин перемішували протягом 20 хвилин, відфільтровували і визначали ємність сорбента, як вказано в прикладі 5. Ємність сорбента за пікратом натрію становила - 4,8 х 10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 9. Розчин перемішували протягом 30 хвилин, відфільтровували і визначали ємність сорбента, як вказано в прикладі 3. Ємність сорбента за пікратом натрію становила - 4,8· 10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 9. Розчин перемішували протягом 40 хвилин, відфільтровували і визначали ємність сорбента, як вказано в прикладі 3. Ємність сорбента за пікратом натрію становила - 4,8· 10-5 моль/г. Приклади 13-16. Обгрунтування часу сорбції фенолового червоного. В стакан ємністю 150 мл вміщували 0,02 г сорбента №1 і 50 мл 2· 10-5 моль/л фенолового червоного. Далі експеримент проводили, як вказано в прикладі 5. Концентрацію фенолового червоного на поверхні визначали, як вказано в прикладі 4. Ємність сорбента за феноловим червоним становила - 4,0 ·10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 13. Розчин перемішували протягом 20 хвилин, відфільтровували і визначали ємність сорбента, як вказано в прикладі 4. Ємність сорбента за феноловим червоним становила - 4,5· 10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 13. Розчин перемішували протягом 30 хвилин, відфільтровували і визначали ємність сорбента, як вказано в прикладі 4. Ємність сорбента за феноловим червоним становила - 4,7· 10-5 моль/г. В стакан ємністю 150 мл вміщували всі компоненти, як вказано в прикладі 13. Розчин переміщували і визначали ємність сорбенту, як вказано в прикладі 4. Ємність сорбенту за феноловим червоним становила 4,8· 10-5 моль/г. Результати наведено в табл.1 (приклади 5-16). Таким чином, з наведених даних видно, що за 30 хвилин відбувається практично повна модифікація силікагелю барвниками. Приклади 17-19. Обгрунтування придатності сорбентів, модифікованих ДДАТД та барвниками для визначення аніонів на прикладі тіоціанату, В стакан ємністю 150 мл вміщували 0,05 г сорбента №2, додавали 5 мл розчину тіоціанату калію з різною концентрацією (1-10)×10-3 моль/л. Розчин перемішували на магнітній мішалці протягом 30 хвилин. При цьому в розчин переходить з поверхні силікагелю еквімолярна кількість барвника. Потім розчин відфільтровували через фільтр "червона" стрічка і вимірювали оптичну густин у фільтрату на КФК-2 при l =440 нм та І= 1см проти розчину порівняння дистильованої води. Концентрацію метилового оранжевого у фільтраті визначали за калібрувальним графіком побудованим в координатах оптична густина - концентрація тіоціанат-іонів. Рівняння графіка А440 = 0.19С (10-3 моль/л) + 0,53, коефіцієнт чутли вості а = 0,19. Одержані результати наведено в табл.2. Видно, що із збільшенням концентрації аніону в розчині зростає ступінь десорбції метилового оранжевого з сорбента №2. В стакан ємністю 150 мл вміщували 0,05 г сорбента, модифікованого ДДАТД та пікратом натрію, додавали 5 мл розчину тіоціанату калію з різною концентрацією (1-10) · 10-3 моль/л. Далі експеримент проводили так, як вказано в прикладі 17. Оптичну густин у фільтрату вимірювали при l= 364 нм та І= 1 см. Концентрацію пікрату натрію у фільтраті визначали за калібрувальним графіком, як вказано в прикладі 17. Рівняння графіка – А364 =0.096С (10-3 моль/л) + 0,28, коефіцієнт чутливості - а =0,096. Одержані результати наведено в табл.2. Видно, що із збільшенням концентрації аніону в розчині зростає ступінь десорбції пікрату натрію з сорбента. В стакан ємністю 150 мл вміщували 0,05 г сорбента, модифікованого ДДАТД та феноловим червоним, додавали 5 мл розчину тіоціанату калію з різною концентрацією (1-10)×10-3 моль/л. Далі експеримент проводили так, як вказано в прикладі 17. Оптичну густин у фільтрату вимірювали при l=400 нм та І= 1 см. Концентрацію фенолового червоного у фільтраті визначали за калібрувальним графіком, як вказано в прикладі 17. Рівняння графіка – А400=0,091С (10-3 моль/л) + 0,43, коефіцієнт чутливості - а = 0,091. Одержані результати наведено в табл.2. Видно, що Із збільшенням концентрації аніону в розчині зростає ступінь десорбції фенолового червоного з сорбента. З даних табл.2 видно, що найбільший коефіцієнт чутли вості (а = 0.19) спостерігається для сорбенту, модифікованого метиловим оранжевим. Приклади 20-23. Обгрунтування часу десорбції метилового оранжевого. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 5,5. Розчин перемішували на магнітній мішалці протягом 10 хвилин. Розчин відфільтровували через фільтр "червона" стрічка і вимірювали оптичну густин у фільтрату на КФК 2 при l=440 нм, І= 1см проти дистильованої води. Концентрацію метилового оранжевого в фільтраті визначали за калібрувальним графіком побудованим: в координатах - оптична густина - концентрація метилового оранжевого. Процент десорбції - 75%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС ! з рН 5,5. Розчин перемішували на магнітній мішалці протягом 20 хвилин. Далі експеримент проводили так, як вказано в прикладі 20. Процент десорбції - 92%. В стакан ємністю 150 мл вміщували 0,02 г ! сорбента №2 І 50 мл 1,5 мг/дм 3 розчину ДДС з рН 5,5. Розчин перемішували на магнітній мішалці протягом 30 хвилин. Далі експеримент проводили так, як вказано в прикладі 20. Процент десорбції - 99%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 150 мл 1,5 мг/дм 3 розчину ДДС з рН 5,5. Розчин перемішували на магнітній мішалці протягом 40 хвилин. Далі експеримент проводили так, як вказано в прикладі 20. Процент десорбції - 100%. З наведених даних видно, що 30 хвилин достатньо для десорбції барвника з поверхні модифікованого силікагеля. Приклади 24-33. Обгрунтування оптимального інтервалу рН для визначення ДДС. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 150 мл 1,5 мг/дм розчину ДДС з рН 2. Розчин перемішували на магнітній ! мішалці протягом 30 хвилин. Розчин відфільтровували через фільтр "червона" стрічка 1 вимірювали оптичну густин у фільтрату на КФК 2 при l= 440 нм, І= 1см проти дистильованої води. Концентрацію ДДС у фільтраті визначали за калібрувальним графіком, побудованим в координатах оптична густина - концентрація ДДС. Точність визначення - 150%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 3. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 150 мл 1,5 мг/дм 3 розчину ДДС з рН 4. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 5. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 6. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначений - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 7. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента № 2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 3. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 9. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм 3 розчину ДДС з рН 10. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення - 100%. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1,5 мг/дм розчину ДДС з рН 11. Далі експеримент проводили так, як вказано в прикладі 24. Точність визначення -150%. Приклади 33-57. Заважаючий вплив. В стакан ємністю 150 мл вміщували 0,02 г сорбента № 2 і 50 мл 1· 10-5 моль/л розчину ДДС та 1· 10-5 - 2-· -3 10 моль/л розчину NaNO3 з рН 5,5. Розчин перемішували на магнітній мішалці протягом 30 хвилин. Розчин відфільтровували через фільтр "червона" стрічка і вимірювали оптичну густин у фільтрату на КФК-2 при l = 440 нм, І=1см проти розчину порівняння, приготованого, як вказано в прикладі 1. Вміст ДДС знаходили за калібрувальним графіком, як вказано в прикладі 1. Результати наведені в табл.3. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1 · 10-5 моль/л розчину ДДС та 1· 10-5- 2-· -3 10 моль/л розчину NaCI з рН 5,5. Далі експеримент проводили так, як вказано в прикладі 24. Вміст ДДС знаходили за калібрувальним графіком, як вказано в прикладі 1. Результати наведено в табл.3. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1 ·10-5 моль/л розчину ДДС та 1· 10-5 - 2· -3 10 моль/л розчину Na2SO4 з рН 5,5. Далі експеримент проводили так, як вказано в прикладі 24. Вміст ДДС знаходили за калібрувальним графіком, як вказано в прикладі 1. Результати наведено в табл.3. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1 ·10-5 моль/л розчину ДДС та 1· 10-5 - 2· 10-3 моль/л розчину Na3РО4 з рН 5,5. Далі експеримент проводили так, як вказано в прикладі 24. Вміст ДДС знаходили за калібрувальним графіком, як вказано в прикладі 1. Результати наведено в табл.3. В стакан ємністью 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1· 10-5 моль/л розчину ДДС та 2· 10-3 - 4· -3 10 моль/л розчину NaCO3 з рН 5,5. Далі експеримент проводили так, як вказано в прикладі 24. Вміст ДДС знаходили за калібрувальним графіком, як вказано в прикладі 1. Результати наведено в табл.3. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2 і 50 мл 1· 10-5 моль/л розчину ДДС та 1· 10-5 - 3· -4 10 моль/л розчину неіоногенної ПАР (тритон Х-305) з рН 5,5. Далі експеримент проводили так, як вказано в прикладі 24. Вміст АПАР знаходили за калібрувальним графіком, як вказано в прикладі 1. Результати наведено в табл.3. В стакан ємністю 150 мл вміщували 0,02 г сорбента №2150 мл 1· 10-5 моль/л розчину ДДС та (1-2)· 10-5 моль/л розчину катіонної ПАР (додецилпіридиній бромід) з рН 5,5. Далі експеримент проводили так, як вказано в прикладі 24. Вміст ДДС знаходили за калібрувальнимграфіком, як вказано в прикладі 1. Результати наведено в табл.3. З даних табл.3 видно, що визначенню ДДС не заважають рівні кількості катіонних ПАР, 20-кратний надлишок неіоногенних ПАР, 100-кратні надлишки хлорид-, нітрат-, сульфат- та фосфат-іонів, 200-кратний надлишок гідрокарбонатів. Катіони металів не заважають визначенню ДДС. Приклади 58-65. Визначення ДДС в стандартних, модельних розчинах та у стічній воді. В табл.4 наведена статистична обробка результатів визначення ДДС в стандартних розчинах. З даних табл.4 видно, що даний спосіб є достатньо точним та має задовільну відтворюваність. В табл.5 наведена статистична обробка результатів визначення ДДС в модельних розчинах. З даних табл.5 видно, що значний надлишок СІ- та NO-3 іонів не заважають визначенню ДДС. В табл.6 наведена статистична обробка результатів визначення ДДС в стічній воді прального комбінату. Правильність одержаних результатів підтверджено методом внутрішнього стандарта ("введено знайдено"), а також спектрофотометричним методом з метиленовим синім [10]. Практичне застосування способу, що заявляється, дозволяє спростити аналіз (зменшити кількість операцій в 7 разів), підвищити експресність втричі, зменшити токсичність (не потребує застосування токсичних органічних розчинників).
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for determination of sodium dodecylsulphate
Автори англійськоюZaporozhets Olha Antonivna, Verba Valentyna Viktorivna, Sukhan Vasyl Vasyliovych
Назва патенту російськоюСпособ определеня додецилсульфата натрия
Автори російськоюЗапорожец Ольга Антоновна, Верба Валентина Викторовна, Сухан Василий Васильевич
МПК / Мітки
МПК: B01J 41/00, G01N 30/96, C07C 305/00, C07C 7/00
Мітки: додецилсульфату, спосіб, натрію, визначення
Код посилання
<a href="https://ua.patents.su/6-19579-sposib-viznachennya-dodecilsulfatu-natriyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення додецилсульфату натрію</a>
Попередній патент: Спосіб визначення істинності отрути сірої медоносної бджоли apis mellifera
Наступний патент: Трифазний антирезонансний трансформатор напруги
Випадковий патент: Спосіб лікування нагноєних радикулярних кіст