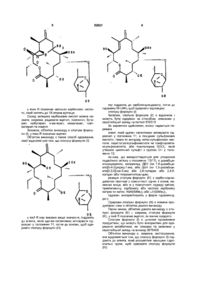
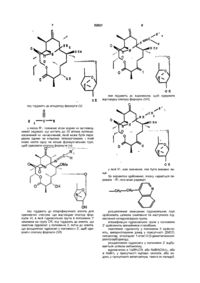
Похідні 5-o-дезозамініл-6-o-метил еритроноліду а та спосіб їх одержання
Формула / Реферат
1. Соединение формулы (I):
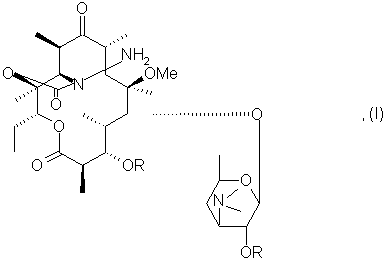
в которой R представляет собой остаток карбоновой кислоты, содержащий до 18 атомов углерода.
2. Соединение по п. 1, в котором R представляет собой ацетил.
3. Способ получения соединения формулы (I), отличающийся тем, что соединение формулы (II):
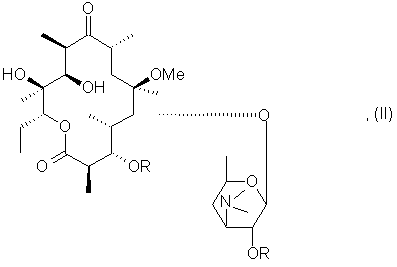
в которой R имеет указанное выше значение, подвергают воздействию агента, способного селективно активировать гидроксил в положении 11, затем воздействию основания, чтобы получить соединение формулы (III):
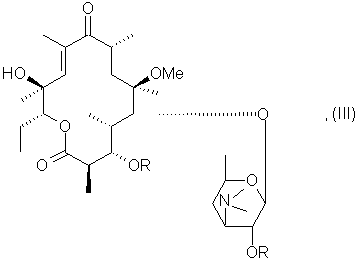
которое подвергают воздействию карбонилдиимидазола, затем воздействию гидразина NH2NH2, чтобы получить соответствующее соединение формулы (I).
4. Соединение формулы (III) как промежуточный продукт для получения соединения формулы (I).
5. Соединение по п. 4, в котором R представляет собой ацетил.
6. Способ получения соединения формулы (VIII):
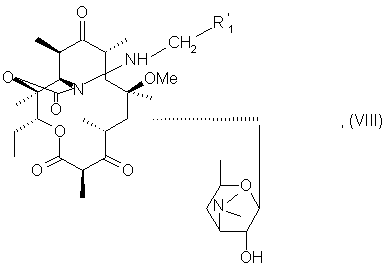
в которой R’1 обозначает атом водорода или углеводородный радикал, содержащий до 23 атомов углерода, насыщенный или ненасыщенный, который может быть прерван одним или несколькими гетероатомами и может нести одну или несколько функциональных групп, заключающийся в том, что соединение формулы (I):

в которой R представляет собой остаток карбоновой кислоты, содержащий до 18 атомов углерода, подвергают воздействию агента, расщепляющего защищенные гидроксильные группы, чтобы получить соединение формулы (IV):
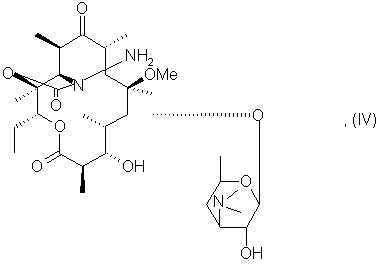
которое подвергают воздействию альдегида формулы (V):
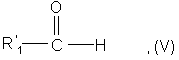
в которой R’1 имеет указанное выше значение, с получением соединения формулы (VI):
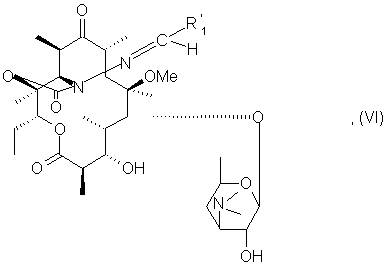
которое подвергают действию агента этерификации для получения соединения, соответствующего соединению формулы VI, в которой гидроксильная группа в положении 2’ заменена на группу OR,
которое подвергают воздействию диимида в присутствии диметилсульфоксида для окисления гидроксила в положении 3, затем воздействию агента, расщепляющего гидроксил в положении 2’, чтобы получить соединение формулы (VII):
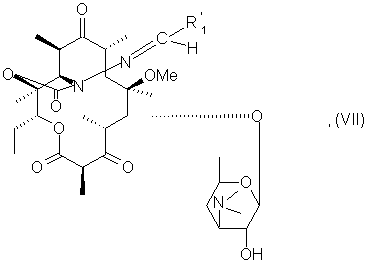
которое подвергают воздействию восстановителя, чтобы получить соответствующее соединение формулы (VIII).
7. Способ по п. 6, в котором R’1 обозначает радикал
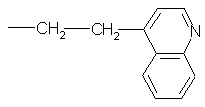 .
.
Текст
1 Соединение формулы (І) ОМе (і) но ОМе (III) OR которое подвергают воздействию карбонилдиимидазола, затем воздействию гидразина NH2NH2, чтобы получить соответствующее соединение формулы (I) 4 Соединение формулы (III) как промежуточный продукт для получения соединения формулы (I) 5 Соединение по п 4, в котором R представляет собой ацетил 6 Способ получения соединения формулы (VIII) о OR в которой R представляет собой остаток карбоновой кислоты, содержащий до 18 атомов углерода 2 Соединение по п 1, в котором R представляет собой ацетил 3 Способ получения соединения формулы (I), отличающийся тем, что соединение формулы (II) о (II) в которой R имеет указанное выше значение, подвергают воздействию агента, способного селективно активировать гидроксил в положении 11, затем воздействию основания, чтобы получить соединение формулы (III) (VIII) (О ю в которой R'i обозначает атом водорода или углеводородный радикал, содержащий до 23 атомов углерода, насыщенный или ненасыщенный, который может быть прерван одним или несколькими гетероатомами и может нести одну или несколько функциональных групп, заключающийся втом, что соединение формулы (I) 52621 ОМе (VI) OR в которой R представляет собой остаток карбоновой кислоты, содержащий до 18 атомов углерода, подвергают воздействию агента, расщепляющего защищенные гидроксильные группы, чтобы получить соединение формулы (IV) о ОМе (IV) которое подвергают действию агента этерификации для получения соединения, соответствующего соединению формулы VI, в которой гидроксильная группа в положении 2 заменена на группу OR, которое подвергают воздействию диимида в присутствии диметилсульфоксида для окисления гидроксила в положении 3, затем воздействию агента, расщепляющего гидроксил в положении 2, чтобы получить соединение формулы (VII) о он (VII) которое подвергают воздействию альдегида формулы (V) О R, С Н (V) в которой R'i имеет указанное выше значение, с получением соединения формулы (VI) Даний винахід стосується нових похідних 5-0дезозамініл 6-0-метил еритроноліду А, способу їх одержання та їх застосування при одержанні біологічно активних продуктів Об'єктом винаходу є сполуки формули (І) которое подвергают воздействию восстановителя, чтобы получить соответствующее соединение формулы (VIII) 7 Способ по п 6, в котором R'I обозначает радикал 52621 OR ОН у яких R позначає залишок карбонової кислоти, який містить до 18 атомів вуглецю Серед залишків карбонових кислот можна назвати, зокрема, радикали ацетил, пропюніл, бутирил, ізобутирил, н-ваперил, ізовалерил, третвалерил та піваліл Зокрема, об'єктом винаходу є сполуки формули (І), у яких R позначає ацетил Об'єктом винаходу є також спосіб одержання, який відрізняється тим, що сполуку формули (II) ОПе OR у якій R має вказане вище значення, піддають дії агента, який здатен селективно активувати гідроксил у положенні 11, потім дії основи, щоб одержати сполуку формули (III) яку піддають дії карбонілдимідазолу, потім дії гідразину NH2NH21 щоб одержати відповідну сполуку формули (І) Загалом, сполуки формули (II) є відомими і можуть бути одержані за способом, описаним у європейській заявці на патент 619319 За варіантом здійснення, якому надається перевага агент, який здатен селективно активувати гідроксил у положенні 11, є похідним сульфонової кислоти, таким як ангідрид метансульфонової кислоти, па ратолуолсульфо кислоти чи трифторметансульфокислоти, або тюнілхлорид SOCb, який утворює циклічний сульфіт з групою ОН у положенні 12, основа, що використовується для утворення подвійного зв'язку у положенні 10(11), є діазабіциклоундеценом, наприклад, ДБУ (чи 1,8-діазабіцикло[5-4-0]ундец-7-ен), або ДБН (чи 1,5-діазабіцикло[4,3,0]нон-5-ен) або 2,6-лутидин або 2,4,6колідин аботетраметилгуанідин, реакція сполуки формули (III) з карбонілдммідазолом протікає у присутності однієї з основ, названих вище, або ж у присутності гідриду натрію, триетиламшу, карбонату або кислого карбонату натрію чи калію, NaNfSiMesh або LiNfSiMesh, гідразин використовують у формі пдразинпдрату Одержані сполуки формули (III) є новими продуктами і самі є об'єктом даного винаходу Таким чином, об'єктом даного винаходу є сполуки формули (III) і, зокрема, сполука формули (III), у якій R позначає ацетил, як ХІМІЧНІ продукти Сполуки формули (І) є цінними проміжними продуктами, що можуть бути використані для одержання антибіотиків, які описано та заявлено у європейській заявці на винахід 0676409 Об'єктом винаходу є, зокрема, застосування, яке відрізняється тим, що сполуку формули (І) піддають дії агента, який розщеплює захищені гідроксильні групи, щоб одержати сполуку формули (IV) 52621 оме А І он яке піддають дії відновника, щоб одержати відповідну сполуку формули (VIII) яку піддають дм альдегіду формули (V) 'Н у якому R'i позначає атом водню чи вуглеводневий радикал, що містить до 23 атомів вуглецю, насичений чи ненасичений, який може бути перервано одним чи кількома гетероатомами, і який може нести одну чи кілька функціональних груп, щоб одержати сполуку формули (vi) ще у якій R'I має значення, яке було вказано ви За варіантом здійснення, якому надається перевага - R'I позначає радикал о ••^ ™'у П о N \ . яку піддають дії етерифікуючого агента для одержання сполуки, що відповідає сполуці формули VI, в якій гідроксильна група в положенні 2 замінена на групу OR, яку піддають дії агента, що окислює гідроксил у положенні 3, потім дії агента, що розщеплює гідроксил у положенні 2', щоб одержати сполуку формули (VII) «Ш.ІИІЦГ розщеплення захищених гідроксильних груп здійснюють шляхом омилення та наступного підкислення складноефірної групи, етерифікацію гідроксильної групи у положенні 2 здійснюють звичайними способами, окислення гідроксилу у положенні 3 здійснюють, використовуючи дммід у присутності ДМСО, наприклад, хлорпдрат 1-етил-3-(3-диметиламшопропіл)карбодиміду, розщеплення гідроксилу у положенні 2 відбувається шляхом метанолізу, відновником є NaBbbCN, або І\ІаВН(ОАс)з, або ж ІЧаВЬЦ у присутності оцтової кислоти, або водень у присутності каталізатора, такого як паладій, 52621 платина і, можливо, у присутності кислоти, такої як соляна кислота чи оцтова кислота Продукти формули (VII) є антибіотиками з цінними властивостями, які описано та заявлено у європейському патенті 0676409 ПРИКЛАД 1 2',3-діацетат 11,12-дідезокси-Зде(2,6-дідезокси-3-С-метил-3-О-метил-альфа-І_рибогексопіранозил)-11,12(пдразоно(карбонілокси)-б-О-метил-еритроміцину СТАДІЯ А 2',3-діацетат 11-дезокси-10,11дідепдро-3-де(2,6-дідезокси-3-С-метил-3-О-метилальфа-І_-рибогексопіранозил)-6-О-метилеритроміцину Розчин, що містить 9,45г 2',3-діацетату 3де(2,6-дідезокси-3-С-метил-3-О-метил-альфа-І_рибогексопіранозил)-6-О-метил-еритроміцину та 112мл піридину, витримують при перемішуванні протягом 15 хвилин при 0°С Протягом 10 хвилин додають 1,52мл тюнілхлориду Продовжують перемішування протягом ночі при кімнатній температурі Зневоднюють і сушать До суміші вливають 150мл етилацетату і 200мл бікарбонату натрію Перемішують протягом 10 хвилин Декантують, екстрагують етилацетатом та сушать Одержують 10,7г продукту Суміш 10,7г цього продукту та 124мл диметилформаміду перемішують при 50°С Протягом 5 хвилин додають 2,53мл ДБУ Перемішують 48 годин при 50°С, виливають до води Додають 100см3 етилацетату Декантують, промивають водою (1,25л), екстрагують етилацетатом (400мл) і сушать над сульфатом магнію, фільтрують і фільтрат упарюють досуха Потім додають приблизно 50мл простого ізопропілового ефіру, залишають кристалізуватись на протязі 72 годин, фільтрують, промивають і сушать Одержують 5,514г шуканого продукту, який плавиться при 174°С СТАДІЯ Б 2',3-діацетат 11,12-дідезокси-Зде(2,6-дідезокси-3-С-метил-3-О-метил-альфа-І_рибогексопіранозил)-11,12-(пдразоно(карбонілокси)-6-О-метил-еритроміцину Перемішують суміш, яка містить 2,623г продукту, одержаного на попередній стадії, 972мг карбонілдммідазолу, ЗОмл дихлорметану і бОмкл ДБУ Продовжують перемішування протягом 4 годин Додають 404мкл пдразинпдрату Перемішують протягом 24 годин, додають 50мл 0,5М кислого фосфату натрію Декантують, екстрагують метиленхлоридом, сушать Вбирають ізопропіловим ефіром Залишають кристалізуватись на протязі ночі Фільтрують, промивають простим ізопропіловим ефіром і сушать Одержують 2,415г шуканого продукту Спектр ЯМР, CDCI3, м ч 0,84 (т) СН3СН2, 1,00 (д) 1,10 (д) 1,12 (д)-1,15 (д) СН-Ме, 1,23(д) 1,28(с) 6 і 12 Me 1,40(с) 2,09 (с) 2,18 (с) 2,26 (с) 2,61 (м) 2,88 (м) %3,06(м) ОАс, NMe 2 Н 8 1 Н'з, Н2 Ню, 10 3.02 (с) С-ОМе, 3,33 (м) H' 5l 3,67 (с) Нц, 3,69 (д) Н5, 4.03 (д) Н'і акс, 4,53(з пошир) (2Н) NH 2 , 4,73 (дд) Н'2 акс, 5,03 (д) Нз, 5,13 (дд) Н13 ЗАСТОСУВАННЯ 11,12-дідезокси-3-де((2,6дідезокси-3-С-метил-З-О-метил-альфа-і-рибогексопіранозил)окси) 6-О-метил-3-оксо-11,12-(оксикарбоніл(2-(3-(4-хшолшіл)2-пропіл)пдразоно))еритроміцин СТАДІЯ А 11,12-дідезокси-3-де(2,б-дідезокси3-С-метил-3-О-метил-апьфа-І_рибогексопіранозил)-11, 12(пдразоно(карбонілокси)-б-О-метил-еритроміцин Перемішують протягом ЗО хвилин суміш, яка містить 714мг продукту стадії Б прикладу 1, 7,5мл ізопропанолу і 2мл 1N гідроксиду натрію Витримують реакційну суміш на протязі 48 годин при кімнатній температурі Додають 2мл нормального розчину соляної кислоти Випарюють досуха Одержаний продукт хроматографують на дюксиді кремнію, елююючи сумішшю етилацетат-триетиламш (9-1) Одержують ЗООмг шуканого продукту СТАДІЯ Б 2'-ацетат 11,12-дідезокси-3-де(2,6дідезокси-3-С-метил-3-О-метил-альфа-І_-рибогексопіранозил)11,12-(оксикарбоніл(3-(4-хшолшіл) пропіліден)пдразоно)-6-О-метил еритроміцину Витримують при перемішуванні в атмосфері азоту протягом 4 годин 281 мл 4-хшолшілпропанальдепду, 10,2мл толуолу, 802мг продукту, одержаного на попередній стадії, і ЗОбмкл оцтової кислоти Випарюють досуха Одержаний продукт піддають хроматографії на дюксиді кремнію, елююючи сумішшю етилацетат-триетиламш (95-5), потім сумішшю етилацетат-триетиламш (90-10) Одержують 916мг продукту Витримують при перемішуванні на протязі ночі 839мг цього продукту, 10мл метиленхлориду і 121мкл оцтового ангідриду Додають 8,55мл аміачної води Перемішують протягом 10 хвилин, екстрагують метиленхлоридом і сушать Одержують 846г шуканого продукту СТАДІЯ В 11,12-дідезокси-3-де((2,6-дідезокси3-С-метил-3-О-метил-альфа-І_рибогексопіранозилокси)3-оксо-11,12-(оксикарбоніл(3-(4-хшолшіл)пропіліден)пдразоно)-6-О-метил еритроміцин Перемішують протягом 15 хвилин суміш, яка містить 1,783г хлорпдрату 1-етил-3-(3-диметиламшопропілкарбодиміду), 1,67мл ДМСО і 11 мл метиленхлориду Додають 781 мг продукту, одержаного на попередній стадії, і 8мл метиленхлориду Витримують при перемішуванні протягом 1,30 години і додають 1,8г трифторацетату піридинію Перемішують протягом 3 годин при кімнатній температурі і додають ЗОмл гідроксиду амонію Витримують при перемішуванні на протязі 15 хвилин, екстрагують метиленхлоридом і сушать над сульфатом магнію Піддають хроматографії на дюксиді кремнію, елююючи сумішшю етилацетаттриетиламш (9-1) Одержують 647мг продукту 52621 12 11 Витримують на протязі ночі при перемішуванні до рН 8-9 за допомогою 28%-ного розчину аміаку суміш 566мг цього продукту і 18мл метанолу і одеДекантують, промивають водою, сушать, фільтруржують 540мг шуканого продукту ють і випарюють досуха Одержують 0,37г продукту, який піддають хроматографії на дюксиді кремСТАДІЯ Г 11,12-дідезокси 3-де((2,6-дідезокси нію, елююючи сумішшю етилацетат-триетиламш З-С-метил 3-О-метил-альфа-І_-рибогексопірано96-4 Одержують 127мг продукту (Rf = 0,25), який зил)окси)6-О-метил-3-оксо-11,12 (оксикарбоніл(2зневоднюють, промивають і сушать Одержують (3-(4-хінолшіл)2-проліл)пдразоно))еритроміцин 90мг шуканого продукту з температурою плавленУ Юмл етилацетату розчиняють 0,38г продукня 189°С ту, одержаного на попередній стадії, і 38мг оксиду платини Гідрують при інтенсивному перемішуванСпектр ЯМР, CDCI3, м ч , 300МГц ні на протязі 24 годин Фільтрують, промивають 1,34 (с) -1, 48 (с) 6 і 12 СНз, 2,30 (с) N(CH3)2, етилацетатом і випарюють при зниженому тиску 2,65 (с) 6-ОСНз, 3,06 (дк) Н4, 3,19 (к) Ню, 3,74 (с) Одержують 0,375г продукту, який витягають у 5 мл НЦ, 5,50 (т мобільний) NH-CH 2 , 7,30 (д) Н3 ХІНОметанолу, 175 мкл оцтової кислоти і 90 мг борпдЛІН, 7,53-7,68 (дт) Н6-Н7 ХІНОЛІН, 8,10 (м) Н5-Н8 риду натрію Перемішують 3 години при кімнатній ХІНОЛІН, 8,79 (д) ЬІ2 ХІНОЛІН температурі Випарюють метанол і витягають за допомогою суміші метиленхлорид-вода Доводять ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійською5-o-disosaminyl -6-o-methyl erythronolide a derivatives and the process of preparation thereof
Назва патенту російськоюПроизводные 5-o-дезозаминил-6-o-метил еритронолида а и способ их получения
МПК / Мітки
МПК: C07H 17/08, C07H 17/00
Мітки: одержання, спосіб, 5-o-дезозамініл-6-o-метил, еритроноліду, похідні
Код посилання
<a href="https://ua.patents.su/6-52621-pokhidni-5-o-dezozaminil-6-o-metil-eritronolidu-a-ta-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Похідні 5-o-дезозамініл-6-o-метил еритроноліду а та спосіб їх одержання</a>
Попередній патент: Фенілоксазолідинони, що мають с-с-зв’язок з 4-8-членними гетероциклічними кільцями
Наступний патент: Спосіб визначення дози іонізуючого випромінювання
Випадковий патент: Саморозвантажувальний вагон для перевозки сипких вантажів