Ферментний біосенсор для визначення аніонних поверхнево-активних речовин у водних розчинах
Номер патенту: 55939
Опубліковано: 27.12.2010
Автори: Павлюченко Олексій Сергійович, Кукла Олександр Леонідович, Солдаткін Олексій Петрович, Шелякіна Маргарита Костянтинівна, Архіпова Валентина Миколаївна, Солдаткін Олександр Олексійович, Дзядевич Сергій Вікторович
Формула / Реферат
Ферментний біосенсор для визначення концентрації аніонних поверхнево-активних речовин у водних розчинах, який складається з потенціометричного датчика на основі двох рН-чутливих польових транзисторів, на один з яких нанесена робоча ферментна мембрана на основі ацетилхолінестерази, що є чутливою до аніонних поверхнево-активних речовин, на другий нанесена референтна мембрана, вказаний біосенсор розташований у вимірювальній кюветі для досліджуваного розчину, де встановлений і електрод порівняння, виходи датчиків призначені для підключення до відповідних входів приладу для вимірювання сигналів потенціометричних датчиків на основі іон-селективних польових транзисторів, а виходи згаданого приладу призначені для підключення до відповідних входів комп'ютера.
Текст
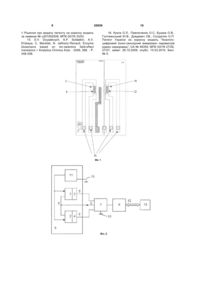
Ферментний біосенсор для визначення концентрації аніонних поверхнево-активних речовин у 3 нуються в природі. Деякі штами бактерій мають ферментні системи, здатні розкладати ПАР [1], але частина ПАР не руйнується і згодом у небезпечних кількостях накопичується в довкіллі та у живих організмах. Небезпеку також становить здатність ПАР розчиняти токсиканти, що призводить до концентрації токсикантів у воді [2]. У зв'язку з вищевикладеним, постійний ефективний контроль наявності цих токсинів (перевищення допустимих концентрацій) в навколишньому середовищі та продуктах споживання є необхідним для охорони природи та покращення якості життя. Відомі стандартні методи для визначення аніонних поверхнево активних речовин базуються на формуванні комплексу між ПАР та метиленом синім, послідуючою екстракцією в хлороформі та спектрофотометричним вимірюванням [3]. Також подібним чином застосовуються етил фіолетовий [4], малахіт зелений [5], метил помаранчевий [6] та похідні пиридіну [7-9]. Всі ці методи потребують багато часу, велику низку процедур екстракції за допомогою розчинників [3-6, 8, 10], а їхні результати сильно залежать від присутності інтерферуючих речовин, таких як органічні сульфати, сульфонали, карбоксилати, фенолати, нітрати, іони хлору тощо [3, 7, 8]. З іншого боку, застосування цих методів потребує використання складних систем проточного аналізу [5, 6, 8], фазового конвертера, сегментора, сепаратора та спеціального обладнання для здійснення двофазного процесу екстракції [4, 5]. Крім того, існує обмеження застосування цих методів для кольорових та мутних розчинів. Не менш важливим фактором також є використання при аналізі токсичних розчинників. Таким чином, всі сучасні стандартні методи високоточного визначення токсичних речовин, а саме рідинна хроматографія, спектрофотометрія, колориметрія, різноманітні хімічні та фізичні методи потребують наявності кваліфікованого персоналу та складного і дорогого обладнання. Ще одним недоліком наведених методів аналізу є необхідність в складній попередній підготовці проб, що виливається у великі затрати часу та коштів. Тому постає актуальне питання створення більш зручного, точного, селективного, швидкого та дешевого методу визначення аніонних ПАР в реальних зразках довкілля. Розробка та створення ферментних біосенсорів для визначення ПАР може сьогодні найкраще вирішити проблеми, пов'язані з перерахованими вище недоліками, та задовольнити усім вищезгаданим вимогам. На даний момент існує кілька варіантів біосенсорів для визначення поверхнево-активних речовин [1, 11-13]. В одному з цих біосенсорів в якості біоселективного матеріалу використовували іммобілізовані на поверхню амперометричного перетворювача клітини Trichosporon cutaneum [12]. В інших варіантах біосенсорів в складі чутливого елементу були присутні вже клітини інших видів Pseudomonas rathonis [13] та Cornamonas testosteroni [2]. Але всі вже відомі біосенсори для визначення ПАР, розроблені на основі мікроорганізмів. Відповідно, порівняно з біосенсорами на 55939 4 основі ферментів, вони мають ряд недоліків, таких як недостатня чутливість та селективність. Крім того, біосенсори на основі бактерій складно стандартизувати. Відомий кондуктометричний ферментний біосенсор для визначення концентрації катіонних поверхнево-активних речовин у водних розчинах, який має дві пари кондуктометричних електродів, на одну з яких нанесено фермент ацетилхолінестераза [14]. В описаному пристрої застосовують кондуктометричний метод вимірювання, який часто є більш чутливим за інші методи, але менш селективним за рахунок того, що до зміни фонової провідності водних розчинів може призводити велика кількість неспецифічних сторонніх факторів (зміна температури, щільності, концентрації солей та інших речовин в розчині). Це призводить до відносного зменшення корисного сигналу. Потенціометричний метод реєстрації менш чутливий до фонової провідності розчинів, відповідно, більш селективний до специфічних змін. Авторами під час проведення патентноінформаційних досліджень і підготовки цієї заявки не виявлені конструкції ферментних біосенсорів на основі рН-чутливих польових транзисторів для визначення концентрації аніонних поверхнево активних речовин у водних розчинах. В основу пропонованої корисної моделі поставлено задачу створення ферментного біосенсору на основі рН-чутливих польових транзисторів для більш селективної оцінки вмісту аніонних поверхнево-активних речовин у досліджуваному зразку. Поставлена задача вирішується пропонованим ферментним біосенсором для визначення концентрації аніонних поверхнево-активних речовин у водних розчинах, який складається з потенціометричного датчика на основі двох рН-чутливих польових транзисторів, на один з яких нанесена робоча ферментна мембрана на основі ацетилхолінестерази, що є чутливою до аніонних поверхнево-активних речовин, на другий нанесена референтна мембрана, вказаний біосенсор розташований у вимірювальній кюветі для досліджуваного розчину, де встановлений і електрод порівняння, виходи датчиків призначені для підключення до відповідних входів приладу для вимірювання сигналів потенціометричних датчиків на основі іонселективних польових транзисторів, а виходи згаданого приладу призначені для підключення до відповідних входів комп'ютера. Суть пропонованої корисної моделі пояснюється графічними матеріалами, де на Фіг.1 схематично представлено пропонований ферментний біосенсор на основі рН-ПТ для визначення концентрації аніонних поверхнево активних речовин у водних розчинах; на Фіг.2 показана блок-схема портативного приладу для роботи з потенціометричними датчиками на основі іон-селективних польових транзисторів; на Фіг.3 продемонстровано принцип роботи ферментного біосенсора на основі рН-ПТ для визначення концентрації аніонних поверхневоактивних речовин на реальному прикладі проведення експерименту; 5 на Фіг.4 наведено калібрувальний графік залежності швидкості зменшення відгуку біосенсора від концентрації додецилсульфат натрію (C12H25О4NaS - аніонна поверхнево-активна речовина). Потенціометричний ферментний біосенсор для визначення концентрації аніонних поверхневоактивних речовин у водних розчинах складається з двох рН-чутливих р-канальних польових транзисторів 1 та 2 в якості перетворювачів (Фіг.1). На поверхню (затвор) транзистору 1 нанесена робоча мембрана 3, яка містить у собі фермент ацетилхолінестеразу, селективний до аніонних поверхневоактивних речовин, на поверхню (затвор) транзистору 2 нанесена референтна мембрана 4. Також він складається з зовнішніх контактів до виходів датчиків - 5, вимірювальної комірки з досліджуваним розчином - 6, блоку реєстрації вимірювального приладу - 7, блоку керування та інтерфейсу - 8, інформаційних входів блоку реєстрації - 9, загальної шини пристрою - 10, електроду порівняння -11, виходів блоку керування та інтерфейсу - 12, комп'ютеру - 13. Поверхні обох вказаних транзисторів безпосередньо контактують з досліджуваною рідиною, що міститься у вимірювальній комірці 6 (Фіг.2). Датчики 1 та 2 підключаються за допомогою зовнішніх контактів 5 до інформаційних входів 9 блоку реєстрації 7 вимірювального приладу для роботи з потенціометричними датчиками. Виходи блоку реєстрації підключені до входів блоку керування та інтерфейсу 8, виходи якого 12 підключається через послідовний порт до комп'ютера 13. Електрод порівняння 11 є підключений до вимірювальної комірки 6 по рідинному з'єднанню та до загальної шини пристрою 10 по електричному з'єднанню. Застосування потенціометричного методу вимірювання з використанням пари диференційних рН-чутливих польових транзисторів та створення оптимальних умов для визначення аніонних ПАР за рахунок використання ферменту ацетилхолінестерази в складі біосенсора дозволить проводити більш селективну оцінку вмісту аніонних поверхнево-активних речовин у досліджуваному зразку. Серед поверхнево-активних речовин 70% займають саме аніонні поверхнево-активні речовини, які є токсичними. Тому було поставлено задачу створити ферментний біосенсор на основі рН-ПТ для визначення аніонних поверхнево-активних речовин з більш високою порівняно з прототипом селективністю та незалежністю від впливу на результати аналізу факторів середовища. Необхідну селективність роботи пристрою автори отримали завдяки використанню у складі чутливої мембрани ферменту ацетилхолінестераза, яка є чутлива до аніонних поверхнево-активних речовин. Застосування потенціометричного методу дозволяє отримати селективний біосенсор, який можна використовувати для роботи з реальними зразками, і результати вимірювань не залежать від зміни провідності розчинів. В основі роботи ферментного біосенсора на основі рН-ПТ для визначення аніонних поверхнево активних речовин лежить ефект інгібування фермента ацетилхолінестерази аніонними поверхне 55939 6 во-активними речовинами. Реакція розщеплення субстрату під каталітичною дією ферменту має наступний вигляд: АХЕ + Ацетилхолін+Н2О→Холін+СН3СОО +Н В процесі ферментативної реакції ацетилхолінестераза розщеплює ацетилхолін при цьому збільшується концентрація протонів в робочій мембрані, відповідно, відбувається зміна рН, яку і можна реєструвати за допомогою рН-ПТ [15]. Далі перевіряли реакцію ферментного біосенсора на досліджуваний розчин з можливим вмістом в ньому аніонних поверхнево-активних речовин. В ході цього впливу поверхнево активні речовини інгібують роботу фермента. Відповідно, в процесі ферментативної реакції при наявності інгібіторів генерувалося менше протонів, що також призводить до зміни рН в мембрані, але у меншій мірі ніж без інгібіторів. В залежності від цієї різниці і визначали наявність аніонних поверхневоактивних речовин в досліджуваному зразку. Ферментативна система вибиралась авторами експериментально за умов отримання покращених аналітичних характеристик біосенсора таких як селективність, операційна стабільність, та відтворюваність сигналу, а також мінімальної собівартості. Пропонований ферментний біосенсор на основі рН-чутливих польових транзисторів та інгібіторного аналізу для визначення концентрації аніонних поверхнево-активних речовин у водних розчинах працює наступним чином. На робочу поверхню рН-ПТ 1 потенціометричного біосенсора наносили вихідну суміш для створення робочої мембрани 3 (об'єм 50нл), яку вносили в насичені пари глутарового альдегіду (ГА) на 20-30 хвилин. Цю робочу мембрану готували із 20мМ фосфатного буфера, рН 6.5, і наступних інгредієнтів у такому їх співвідношенні (у мас. %): ацетилхолінестерази (АцХЕ), 5 сироватковий альбумін бика (БСА), 5 гліцерин 10 На інший рН-ПТ 2 наносили вихідну суміш для створення референтної мембрани 4 (50нл), яку вносили в ГА на 20-30 хвилин, цю мембрану формували з 20мМ фосфатного буфера, рН 6,5, і наступних інгредієнтів у такому їх співвідношенні (у мас %): БСА 10 гліцерин 10 Вимірювання проводили за допомогою портативного вимірювального приладу, розробленого та виготовленого в Інституті фізики напівпровідників ім. В. Є. Лашкарьова НАН України [16], що працює по схемі прямого вимірювання струму в каналі польового транзистора з активним навантаженням. Чутливість приладу становила близько 25мкА/рН. До входу приладу підключається двохелементний потенціометричний ферментний біосенсор, а також електрод порівняння. Вихід приладу підключається до комп'ютера через послідовний СОМ або USB порт. Пропоновану систему використовували таким чином. 7 Попередньо виготовляли біоселективні мембрани. Створення ферментного біосенсору: виготовляли робочу мембрану 3. Для цього готували розчин з вмістом 5% Ацетилхолінестерази (АцХЕ), 5% БСА та 10% гліцерину у 20мМ фосфатному буфері, рН 6,5. Референтну мембрану 4 виготовляли таким же чином, але замість наважки ферменту брали лише 10% БСА. Гліцерин у складі мембран 3, 4 використовувався для стабілізації ферменту при іммобілізації та запобігання передчасного підсихання розчину, нанесеного на поверхню перетворювача до його внесення в ексикатор для ковалентної зшивки. В свою чергу, БСА в складі робочої мембрани 3 відігравав роль стабілізуючого агенту для ферменту. Для створення мембран біосенсору, відповідно, 3 та 4, краплю суміші АцХЕ-БСА (50нл) наносили на затворну область поверхні перетворювача 1, а на іншу 2 - розчин БСА без ферменту (це був датчик порівняння). Для іммобілізації мембран датчики розміщували в атмосфері насичених парів глутарового альдегіду (ГА) на 20-30хв. і потім підсушували на повітрі й відмивали від надлишку ГА у буферному розчині протягом 10-20хв. Протокол аналізу аніонних поверхневоактивних речовин представлено на прикладі додецилсульфат натрію (ДСН) в модельних розчинах (Фіг.3). Спочатку в комірку додавали 4мМ ацетил холін хлориду, а після отримання сигналу, додавали ДСН і отримували зменшення сигналу. Швидкість цього зменшення була пропорційна концентрації поверхнево-активних речовин. Після цього отримували залежність швидкості зменшення величин відгуків біосенсора на ацетилхолінхлорид після додавання в розчин різних концентрацій додецилсульфат натрію - одержували калібрувальний графік (Фіг.4). Для перевірки роботи пропонованого ферментного біосенсора на основі рН-ПТ з реальними зразками, готували розчин з умовно невідомою концентрацією ДСН. За допомогою біосенсору отримували сигнал на внесення до вимірювальної комірки 4мМ ацитилхолінхлориду. Потім до вимірювальної комірки додавали розчин з умовно невідомою концентрацією ДСН. Починав зменшуватись відгук біосенсору на субстрат з відповідною швидкістю. В залежності від цієї швидкості, по калібрувальному графіку отримували концентрацію ДСН, яка співпадала з умовно невідомою концентрацією додецилсульфат натрію у розчині. Таким чином, отримана калібрувальна крива демонструє, що пропонований ферментний біосенсор на основі рН-чутливих польових транзисторів є функціонально придатним і дозволяє проводити експрес-аналізи рідин з можливістю визначення концентрації аніонних поверхнево-активних речовин в реальних водних розчинах. Література: 1. L. Taranova, I. Semenchuk, T. Manolov, P. Iliasov, A. Reshetilov. Bacteria-degraders as the base of an amperometric biosensor for detection of anionic surfactants // Biosensors and Bioelectronics. - 2002. 17. - P. 635-640. 55939 8 2. L. Taranova, A. Fesay, G. Ivashchenko, A. Reshetilov, M Wmther-Nielsen, J. Emneus. Comamonas testosteroni strain ТІ as a potential base for a microbal sensor detecting surfactants. // Applied Biochemistry and Microbiology. - 2004. - 40. - P. 404408. 3. A.E. Greenberg, L.S. Clesceri, A.D. Eaton, Standard Methods for the Examination of Water and Wastewater, 18th ed., American Public Health Association, Washington, DC, 1992, pp. 5-36. 4. Y. Hirai, K. Tomokuni. Extractionspectrophotometric determination of anionic surfactants with a flow-injection system // Anal. Chim. Acta. - 1985. - 167. - P. 409-412. 5. T. Sakai, H. Harada, X. Liu, N. Ura, K. Takeyoshi, K. Sugimoto. New phase separator for extraction-spectrophotometric determination of anionic surfactants with Malachite Green by flow injection analysis // Talanta. - 1998. - 45. - P. 543548. 6. Q. He, H. Chen. Flow injection spectrophotometric determination of anionic surfactants using methyl orange as chromogenic reagent // Fresenius J. Anal. Chem. - 2000. - 367. - P. 270-274. 7. Y. Shimoishi, H. Miyata. Spectrophotometric determination of anionic surfactants in tap and river waters with l-(10-bromodecyl)-4-(4aminonaphthylazo)pyrimidinium bromide // Fresenius J. Anal. Chem. - 1990. - 338. - P. 46-49. 8. H. Kubota, M. Katsuki, S. Motomizu. Batchwise and Flow-Injection Methods for the Spectrophotometric Determination of Anionic Surfactants with 4-(4-N, N-Dimethylaminophenylazo)-2-methylquinoline // Anal. Sci. 1990. - 6. - P. 705-709. 9. Y. Shimoishi, H. Miyata. Some N-alkylnaphthylazo pyridinium salts as new reagents for the spectrophotometric determination of anionic surfactants // Fresenius J. Anal. Chem. - 1993.-345.P. 456-461. 10. І. Kasahara, K. Hashimoto, T. Kawabe, A. Kunita, K. Magawa, N. Hata, S. Taguchi, K. Goto. Spectrophotometric determination of anionic surfactants in sea-water based on ion-pair extraction with bis[2-(5-trifluoromethyl-2-pyridylazo)-5diethylaminophenolato]cobalt(III) as counter ion // Analyst. - 1995. - 120. - P. 1803-1807. 11. A. Seki, K. Tokita. Surfactant cytotoxicity assay based on a silicon transducer // Chemosphere 2009. - 76. - P. 341-344. 12. Y. Nomura, К. Ikebukuro, К. Yokoyama, Т. Takeuchi, Y. Arikawa, S. Ohno, I. Karube. Application of a linear alkylbenzene sulfonate biosensor to river water monitoring // Biosensors and Bioelectronics. 1998. - 13. - P. 1047-1053. 13. A. Reshetilov, I. Semenchuk, P. lliasov, L. Taranova. The amperometric biosensor for detection of sodium dodecyl sulfate // Analytica Chimica Acta. 1997. - 347. - P. 19-26. 14. О.О. Солдаткін, І.С. Кучеренко, В.М. Архипова, С.В. Дзядевич, О.П. Солдаткін. Кондуктометричний ферментний біосенсор для визначення поверхнево-активних речовин у водних розчинах. 9 // Рішення про видачу патенту на корисну модель за заявкою № u201002509, МПК G01N 33/02. 15. S.V. Dzyadevych, A.P. Soldatkin, A.V. El'skaya, C. Martelet, N. Jaffrezic-Renault. Enzyme biosensors based on ion-selective field-effect transistors // Analytica Chimica Acta. - 2006, 568. - P. 248-258. 55939 10 16. Кукла О.Л., Павлюченко О.С, Бушма О.В., Голтвянський Ю.В., Дзядевич СВ., Солдаткін О.П. Патент України на корисну модель "Аналогоцифровий іонно-сенсорний вимірювач параметрів рідких середовищ", UA № 48359, МПК G01N 27/26, 27/27, заявл. 26.10.2009, опубл. 10.03.2010, Бюл. № 5. 11 Комп’ютерна верстка А. Крижанівський 55939 Підписне 12 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюFerment bio-sensor for determinatio of anion surface-active substances i water solutions
Автори англійськоюArkhypova Valentyna Mykolaivna, Sheliakina Marharyta Kostiantynivna, Soldatkin Oleksandr Oleksiiovych, Dziadevych Serhii Viktorovych, Soldatkin Oleksii Petrovych, Pavliuchenko Oleksii Serhiiovych, Kukla Oleksandr Leonidovych
Назва патенту російськоюФерментный биосенсор для определения анионных поверхностно-активных веществ в водных растворах
Автори російськоюАрхипова Валентина Николаевна, Шелякина Маргарита Константиновна, Солдаткин Александр Алексеевич, Дзядевич Сергей Викторович, Солдаткин Алексей Петрович, Павлюченко Алексей Сергеевич, Кукла Александр Леонидович
МПК / Мітки
МПК: G01N 33/18
Мітки: розчинах, аніонних, ферментний, водних, речовин, біосенсор, визначення, поверхнево-активних
Код посилання
<a href="https://ua.patents.su/6-55939-fermentnijj-biosensor-dlya-viznachennya-anionnikh-poverkhnevo-aktivnikh-rechovin-u-vodnikh-rozchinakh.html" target="_blank" rel="follow" title="База патентів України">Ферментний біосенсор для визначення аніонних поверхнево-активних речовин у водних розчинах</a>
Попередній патент: Спосіб комплексного очищення фільтратів звалищ твердих побутових відходів
Випадковий патент: Спосіб отримання кардіоліпіну