Спосіб фотометричного визначення пероксимоносульфатної кислоти та пероксидисульфату за їх сумісної присутності
Формула / Реферат
Спосіб фотометричного визначення пероксимоносульфатної кислоти та пероксидисульфату за їх сумісної присутності, за яким вимірюють оптичну густину розчину J3-, що утворюється в результаті окиснення J- за його надлишку, який відрізняється тим, що до розчину суміші пероксидів при рН=4,0 доливають 2,0±0,1 мл 10 %-го розчину KJ, фіксують початок реакції і вимірюють оптичну густину розчину А щохвилини упродовж 5-ти хвилин, будують залежність величини А від часу t, за якою знаходять вміст компонентів суміші.
Текст
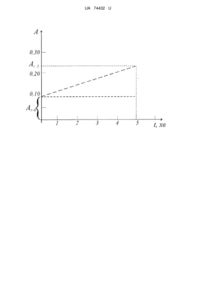
Реферат: UA 74432 U UA 74432 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель належить до галузі аналітичної хімії і може використовуватись для дослідження властивостей пероксидів. Відомий хемілюмінесцентний спосіб визначення пероксимоносульфатної кислоти (Зинчук В.К., Стадничук Е.Н. Хемилюминесцентное определение пероксимоносерной кислоты // Журн. аналит. химии. 2001. Т. 56, № 10. С. 1050-1051), який ґрунтується на вимірюванні інтенсивності хемілюмінесценції в реакції окиснення люмінолу пероксимоносульфатною кислотою у лужному середовищі. Недоліком способу є мала селективність визначення пероксикислоти у присутності інших пероксидів - Н2О2, пероксидисульфату, а система пероксимоносульфатна кислота + пероксидисульфат відзначається специфічною дією на процес окиснення люмінолу, що вимагає окремого дослідження. Крім того, спосіб обмежений суттєвим впливом величини фонового сигналу, який важко контролювати в умовах лужного середовища, що відображається на чутливості і точності визначення пероксимоносульфатної кислоти. Відомий хемілюмінесцентний спосіб визначення пероксимоносульфатної кислоти у присутності пероксидисульфату [Пилипчук Е.А., Зинчук В.К., Василечко В.О. Хемилюминесцентное определение пероксимоносульфата и пероксидисульфата при их совместном присутствии // Заводская лаборатория. Диагностика материалов. 1996. Т. 62. № 11. С. 31-32], який ґрунтується на реакції окиснення метилсульфату-9,10-диметилакридинію пероксимоно- та пероксидисульфатом і вимірюванні інтенсивності хемілюмінесценції. Недоліком способу є необхідність використання дефіцитних реагентів та спеціальної апаратури. Найближчим за технічною суттю - найближчим аналогом - є спосіб фотометричного визначення пероксимоносульфатної кислоти у присутності 50-кратного надлишку Н2О2 та 200-кратного пероксидисульфату [Зінчук В., Могитич С. Фотометричне визначення пероксимоносульфатної кислоти у присутності інших пероксидів // Праці НТШ. 2005. Т. 15. С. 3539], який ґрунтується на реакції окиснення іонів J пероксидами і фотометруванні розчину J3 . Недоліком способу є необхідність контролю і врахування побічної реакції окиснення J розчиненим киснем, швидкість якої у значній мірі залежить від кислотності середовища. Крім того, проведення реакції у кислому середовищі згідно способу не дає можливості визначати пероксидисульфат за малою різницею у швидкостях окиснення J пероксимоно- та пероксидисульфатом. В основу корисної моделі поставлено задачу удосконалити спосіб фотометричного визначення пероксимоносульфатної кислоти шляхом вибору її концентраційних меж і рН середовища, при якому суттєво зменшується вплив побічної реакції окиснення J розчиненим киснем, що дасть змогу оптимізувати умови аналізу. При вибраному оптимальному рН середовища відсутня взаємодія між пероксимоно- та пероксидисульфатом, спостерігається найбільша різниця у швидкості окиснення ними іону J , що сприяє їх визначенню за сумісної присутності в розчині. Поставлена задача вирішується тим, що у способі фотометричного визначення пероксимоносульфатної кислоти і пероксидисульфату за їх сумісної присутності, за яким вимірюють оптичну густину розчину J3 , що утворюється внаслідок реакції окиснення J за його надлишку, згідно з корисною моделлю, до розчину суміші пероксидів з відповідним рН доливають 2,0 мл 10 %-го розчину KJ, фіксують початок реакції і вимірюють оптичну густину розчину А щохвилини упродовж 5-ти хвилин, будують залежність цієї величини від часу t, за якою визначають вміст сполук. З літературних джерел відомо [Зінчук В., Могитич С. Фотометричне визначення пероксимоносульфатної кислоти у присутності інших пероксидів // Праці НТШ. 2005. Т. 15. С. 3539], що при визначенні пероксимоносульфатної кислоти важливу роль відіграє кислотність середовища. Для визначення концентрації пероксикислоти використовують фотометричний спосіб, який проводять у кислому середовищі, де пероксимоносульфатна кислота миттєво витискує J2 з KJ згідно реакції H2SO5+2KJ J2+K2SO4 + Н2О. Вільний J2 реагує з надлишком KJ, утворюючи нелеткий KJ 3, розчин якого характеризується смугою світлопоглинання з макс=350 нм. Детальніше вивчення умов перебігу цієї реакції показало, що швидке і повне витіснення J 2 з KJ має місце і у слабкокислому та нейтральному середовищі з рН 4,0-7,0. У слабколужному середовищі стає помітною реакція самочинного розкладання пероксикислоти 222HSО5 + SO5 2S2O4 + 3О2 + Н2О та реакція диспропорціонування J2+2ОН JO + J + Н2О. 1 UA 74432 U 5 На відміну від пероксимоносульфатної кислоти пероксидисульфат у зазначених межах рН дуже повільно реагує J . Автором вперше вивчена взаємодія пероксидисульфату з J в умовах слабкокислого і слабколужного середовища і встановлено, що швидкість реакції мало змінюється, про що свідчать дані табл. 1, отримані експериментально. Таблиця 1 -4 Швидкість реакції окиснення J пероксидисульфатом (2,1·10 М) при різних рН. рН 2,0 4,0 6,3 7,4 8,0 10 15 20 25 30 35 40 45 50 tg5 0,018 0,022 0,020 0,024 0,020 Мірою швидкості реакції вибрано тангенс кута нахилу (tg 5) лінійної залежності А - txв, отриманої за перші 5 хв. спостереження. Різниця у швидкості окиснення J пероксимоно- та пероксидисульфатом поставлена в основу розроблення фотометричного способу визначення їх за сумісної присутності. За оптимальне значення вибрано рН=4,0 (0,02 Μ біфталатний буферний розчин), при якому мінімальний вплив конкуруючої реакції окиснення J розчиненим киснем, яка є причиною зростання оптичної густини холостої проби, а остання, в свою чергу, зростає зі "старінням" розчину KJ. У зв'язку з цим необхідно використовувати свіжовиготовлений водний розчин KJ та старанно підходити до виготовлення розчину холостої проби, контролю значення його оптичної густини. При рН=4,0 практично відсутня за час експерименту взаємодія між визначуваними пероксидами. Мірою концентрації пероксимоносульфатної кислоти є оптична густина розчину J 3 (At=0), а концентрації пероксидисульфату - значення оптичної густини розчину J3 за 5 хв реакції з врахуванням At=0 (At=5-At=0) (див. креслення). Обов'язковим, як при визначенні пероксимоносульфатної кислоти, так і пероксидисульфату, є контроль і врахування значення оптичної густини холостої проби. Пероксикислоту синтезували за способом [Перекись водорода и перекисные соединения / Под ред. М.Е. Позина. М.: ГХИ, 1951], звертаючи особливу увагу на стадію нейтралізації розчину та наступного руйнування Н2О2 при нагріванні з контролем на присутність останнього -2 реакцією з Ti(IV). Вихідна концентрація розчину ~10 М з рН=3-4, який розводять водою до -4 -5 робочих 10 -10 М. Концентрацію вихідного розчину пероксикислоти контролюють титриметричним йодометричним способом, а робочих розчинів йодометричним способом у фотометричному варіанті: вимірюванням оптичної густини розчинів J3 на фотоелектроколориметрі ФЭК-56 Μ зі світлофільтром № 3 (максимум пропускання =400 нм) та кюветах з товщиною поглинаючого шару l=30 мм. Розчин K2S2O8 з Τ=1,0 мг/мл готують з перекристалізованого препарату солі марки "хч" розчиненням наважки у дистильованій воді. В роботі користуються свіжовиготовленими розчинами. Для вивчення впливу рН середовища на швидкість реакції окиснення J вибирають серію ~0,1 Μ буферних розчинів - тетраоксалатного, біфталатного, ацетатного, пірофосфатного, боратного в межах рН 2,0-9,2. Нижче подаються способи та результати фотометричного визначення пероксимоносульфатної кислоти і пероксидисульфату окремо та за їх сумісної присутності. Визначення пероксимоносульфатної кислоти. У мірну колбу місткістю 25,0 мл вносять 5 мл 0,1 Μ біфталатного буферного розчину з рН=4,0, при перемішуванні досліджуваний на пероксикислоту розчин з вмістом 1,0 мкМ, 2,0 мл 10 %-го розчину KJ, воду до позначки, добре перемішують і фотометрують на ФЭК-56 Μ зі світлофільтром № 3 у кюветі з l=30 мм навпроти води. Окремо готують і фотометрують розчин холостої проби, враховуючи у подальшому значення А для цього розчину. Вміст пероксикислоти у мкМ/25,0 мл знаходять за градуювальним графіком, побудованим в аналогічних умовах у межах концентрацій пероксикислоти 0,05-1,0 мкМ/25,0 мл. 2 UA 74432 U Рівняння прямої графіка А=0,003+0,334mi де mi - вміст пероксикислоти, мкМ/25,0 мл. Для перевірки правильності отриманих результатів використовують спосіб "введено-знайдено" (табл. 2). Таблиця 2 Результати визначення пероксимоносульфатної кислоти, мкМ/25,0 мл (n=4, Р=0,95) Введено пероксикислоти, m 0,260 0,750 Знайдено пероксикислоти, m 0,258 0,733 SX 0,021 0,022 Sr 0,081 0,031 5 10 15 Визначення пероксидисульфату. У мірну колбу місткістю 25,0 мл вносять 5 мл 0,1 Μ біфталатного буферного розчину з рН=4,0, при перемішуванні доливають досліджуваний на пероксидисульфат розчин з вмістом 1,0-10,5 мкМ/25,0 мл, 2,0 мл 10 %-го розчину KJ, фіксуючи час початку реакції, воду до позначки, і фотометрують щохвилини упродовж 5 хв. на ФЭК-56 Μ зі світлофільтром № 3 у кюветах з l=30 мм по відношенню до води. Окремо готують і фотометрують розчин холостої проби (розчин без пероксидисульфату), оптична густина якого за 5 хв. практично не змінюється. За даними вимірювання А будують кінетичну залежність A-tхв., що є прямою. Мірою вмісту пероксидисульфату є значення оптичної густини за 5 хв. перебігу реакції (A t=5) з врахуванням значення At=5 для холостої проби. Вміст пероксидисульфату знаходять за градуювальним графіком, побудованим у координатах At=5-m, де m - вміст пероксидисульфату, мкМ/25,0 мл. Рівняння прямої графіка має вигляд А5=0,003+0,01 lm. Для перевірки правильності визначення пероксидисульфату застосовують спосіб "введено знайдено". У табл. 3 подані результати аналізу та їх статистична обробка. 20 Таблиця 3 Результати фотометричного визначення пероксидисульфату, мкМ/25,0 мл (n=4, Р=0,95). Введено, m 1,04 2,08 2,60 4,17 5,20 25 30 35 40 Знайдено, m 1,13 2,08 2,55 4,11 5,46 SX 0,018 0,026 0,023 0,035 0,031 Sr 0,018 0,012 0,009 0,008 0,006 Визначення пероксимоносульфатної кислоти та пероксидисульфату за їх сумісної присутності. Розчин, що містить суміш пероксидів повинен мати рН у межах 4,0-6,5; інтервал вмістів пероксикислоти 0,05-1,00 мкМ, пероксидисульфату 1,0-10,5 мкМ у 25,0 мл відповідно. Спосіб аналізу та отримані результати стосуються визначення пероксидів при рН=4,0 (0,02 Μ біфталатний буферний розчин). У мірну колбу місткістю 25,0 мл вносять розчин суміші пероксидів, при перемішуванні додають 5 мл 0,1 Μ біфталатного буферного розчину, 2,0 мл 10 %-го розчину KJ, фіксуючи початок реакції; доливають воду до позначки, добре перемішують і фотометрують на ФЭК-56 Μ зі світлофільтром № 3 у кюветі з l=30 мм, вимірюючи щохвилини оптичну густину розчину А навпроти води упродовж 5 хв. В аналогічних умовах визначають оптичну густину холостої проби (розчин без пероксидів), значення якої практично не змінюється за час фотометрування. Будують залежність A-tхв. (фіг. 1). Екстраполяція прямої на t=0 дає значення Аt=0, що відповідає вмісту пероксимоносульфатної кислоти після врахування А для холостої проби. За значенням At=0 знаходять вміст пероксимоносульфатної кислоти за градуювальним графіком у межах 0,051,00 мкМ пероксикислоти у 25,0 мл (див. визначення пероксикислоти). Вміст пероксидисульфату знаходять за значенням At=5-At=0 і розрахунком за градуювальним графіком (див. визначення пероксидисульфату) з вмістом 1,0-10,5 мкМ у 25,0 мл. Результати визначення пероксидів у суміші подано у табл. 4. 3 UA 74432 U Таблиця 4 Результати визначення пероксимоносульфатної кислоти і пероксидисульфату за їх сумісної присутності, мкМ/25,0 мл (n=4, Р=0,95). Bведено, m Знайдено, m пероксикислоти пероксидисульфату пероксикислоти пероксидисульфату 0,100 1,04 0,106 1,02 0,100 1,00 0,103 0,94 0,500 5,20 0,490 4,95 0,750 4,00 0,73 4,04 5 10 15 Пероксикислота Пероксидисульфат SX 4,4·10-3 6,0·10-3 2,6·10-2 5,1·10-2 SX 9,3·10-2 7,2·10-2 0,2·10-2 4,4·10-2 Sr 0,041 0,060 0,053 0,070 Sr 0,092 0,077 0,038 0,019 Вміст пероксидів у суміші знаходять і порівнянням відповідних значень A t=0 і At=5-At=0 для досліджуваного розчину суміші і At=0, At=5 для близьких за вмістом компонентів у стандартних розчинах пероксикислоти і пероксидисульфату. Наведені у табл. 4 результати визначення пероксимоносульфатної кислоти і пероксидисульфату за їх сумісної присутності підтверджують передбачуваний технічний результат. ФОРМУЛА КОРИСНОЇ МОДЕЛІ Спосіб фотометричного визначення пероксимоносульфатної кислоти та пероксидисульфату за їх сумісної присутності, за яким вимірюють оптичну густину розчину J3 , що утворюється в результаті окиснення J за його надлишку, який відрізняється тим, що до розчину суміші пероксидів при рН=4,0 доливають 2,00,1 мл 10 %-го розчину KJ, фіксують початок реакції і вимірюють оптичну густину розчину А щохвилини упродовж 5-ти хвилин, будують залежність величини А від часу t, за якою знаходять вміст компонентів суміші. Комп’ютерна верстка Л. Купенко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for photometric determination of peroximonosulfate acid and peroxidisulfate at joint presence of those
Автори англійськоюZinchuk Vasyl Kostiantynovych
Назва патенту російськоюСпособ фотометрического определения пероксимоносульфатной кислоты и пероксидисульфата при их совместном присутствии
Автори російськоюЗинчук Василий Константинович
МПК / Мітки
МПК: G01N 21/00, G01N 21/31
Мітки: кислоти, пероксимоносульфатної, сумісної, пероксидисульфату, присутності, спосіб, визначення, фотометричного
Код посилання
<a href="https://ua.patents.su/6-74432-sposib-fotometrichnogo-viznachennya-peroksimonosulfatno-kisloti-ta-peroksidisulfatu-za-kh-sumisno-prisutnosti.html" target="_blank" rel="follow" title="База патентів України">Спосіб фотометричного визначення пероксимоносульфатної кислоти та пероксидисульфату за їх сумісної присутності</a>