7(6)-дифторметокси-3-метил-2н-1,2,4-бензотіадіазин-1,1-діоксид
Номер патенту: 77344
Опубліковано: 15.11.2006
Автори: Тарасова Катерина Вікторівна, Шевчук Віктор Григорович, Малєтіна Ірина Ісааківна, Пивовар Світлана Миколаївна, Петко Кирило Ігоревич, Ягупольський Лев Мусійович, Карвацький Ігор Миколайович, Мойбенко Олексій Олексійович, Струтинський Руслан Борисович
Формула / Реферат
7(6)-Дифторметокси-3-метил-2Н-1,2,4-бензотіадіазин-1,1-діоксид загальної формули (І)
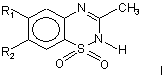 ,
,
де Іа: R1 = Н, R2 = OCHF2;
Іб: R1 = ОСНF2, R2 = Н.
Текст
7(6)-Дифторметокси-3-метил-2Н-1,2,4бензотіадіазин-1,1-діоксид загальної формули (І) R1 R2 S CH3 N O N O H I , де Іа: R1 = Н, R2 = OCHF2; Іб: R1 = ОСНF2, R2 = Н. (13) C2 (21) a200503296 (22) 11.04.2005 (24) 15.11.2006 (46) 15.11.2006, Бюл. № 11, 2006 р. (72) Ягупольський Лев Мусійович, Малєтіна Ірина Ісааківна, Петко Кирило Ігоревич, Мойбенко Олексій Олексійович, Струтинський Руслан Борисович, Пивовар Світлана Миколаївна, Шевчук Віктор Григорович, Карвацький Ігор Миколайович, Тарасова Катерина Вікторівна (73) ІНСТИТУТ ОРГАНІЧНОЇ ХІМІЇ НАЦІОНАЛЬНОЇ АКАДЕМІЇ НАУК УКРАЇНИ (56) Машковский М.Д. Лекарственные средства. -М ООО" Издательство Новая Волна". 2000 г. T.I, стр.395. Zivcovich I., Thomson D., Bertoimo М. // J. Pharm. Exp. Ther. - 1995. -Vol. 272.-P. 300-309 2 (11) UA Діазоксид в сучасній медицині розглядається, як один з основних периферичних вазодилататорів, який до того ж проявляє і кардіопротекторні властивості. В останній час з'явилась велика кількість публікацій, в яких окреслені перспективи використання аналогів діазоксиду, зокрема для лікування діабету [3, 4], психічних порушень [5], ВІЛ-інфекції [6]. Фармакологічна дія похідних 1,2,4-бензотіадіазинів пов'язана з їх здатністю активувати АТФ-залежні калієві канали клітин [7]. Відомо, що введення фторовмісних замісників в молекули потенційно біологічно-активних сполук сприяє проявленню фармакологічної дії, підвищує стійкість речовин, знижує їх токсичність [8]. Раніше [9, 10]. було показано, що фторовмісні активатори (19) Сполуки, що заявляються, є новими і в літературі не описані. Цінність речовин подібного типу 7(6)дифторметокси-3-метил-2Н-1,2,4бензотіадіазин-1,1-діоксидів полягає в тому, що вони є фторовмісними аналогами відомого антигіпертензивного засобу «Діазоксид» (II) [1, 2]. 77344 Винахід належить до органічної хімії, конкретно до нових дифторметокси-похідних бензотіадіазина загальної формули (І) 3 77344 4 калієвих каналів, якими є аналоги препарату піна(VII) та 4-нітро-5-дифторометоксианіліну (VIII) у цидил, мають більш виражені кардіопротекторні молярному співвідношенні 2:1. Отримані аміно властивості та значно меншу токсичність за нефпродукти розділяють колоночною хроматографією торовані аналоги цього препарату. на силікагелі марки MN-Kiesel-gel-60. Елюент Задача винаходу - створення нових фторовміхлористий метилен. Необхідний для подальших сних аналогів діазоксиду - потенційно біологічноперетворень фторовмісний о-нітроанілін (VII) був активних речовин з покращеними властивостями. отриманий, виходячи зі сполуки (IV) з виходом Задача вирішується шляхом синтезу нових хібіля 45%. мічних сполук - 7(6)дифторметокси-3-метил-2ННітроанілін (VII) діазотували розчином нітриту 1,2,4-бензотіадіазин-1,1-діоксидів (І) - аналогів натрію в соляній кислоті з масовою часткою оснодіазоксиду, які містять в положенні 7 або 6 конденвної речовини 20% при температурі (0±2)°С, потім сованого гетероциклу фармакоформну дифтормеутворену діазонієву сіль вводили у взаємодію з токси-групу замість атому хлора. сірчистим газом в оцтовій кислоті в присутності Синтез 7-дифторметокси-3-метил-2Н-1,2,4хлориду міді (II) при тій же температурі. бензотіадіазин-1,1-діоксида (Іа) здійснюється виТаким чином одержували 2-нітро-5ходячи з 3-дифторметоксианіліну (III) за схемою: дифторометоксибензолсульфохлорид (IX), який розчиняли в безводному етері та насичували його розчин при температурі (20±2)°С амоніаком, суміш витримували 1год і після випаровування розчинника одержували сульфамід (X). Відновлення нітросульфаміда (X) залізом у водно-спиртовому розчині хлористого амонію приводить до аміно сульфамід а (XI), який ацетилюють оцтовим ангідридом in situ до диацетильного похідного, замикання якого в присутності ацетату натрію приводить до бажаного аналогу діазоксида (Іа). Синтез 6-дифторметокси-3-метил-2Н-1,2,4бензотіадіазин-1,1-діоксида (16) здійснюється аналогічно виходячи з доступного 4дифторметоксианіліну (XII) за схемою: Взаємодія 3-дифторметоксианіяіну (III) з оцтовим ангідридом приводить до утворення ацетильного похідного (IV). Потім сполуку (IV) нітрують сумішшю азотної (густина 1.41) та сірчаної (густина 1.84) кислот у об'ємному співвідношенні 1:1. При цьому утворюється суміш продуктів нітрування (V та VI) у молярному співвідношенні 2:1. Після омилення цієї суміші розчином гідроксиду натрію з масовою часткою основної речовини 10% була отримана суміш 2-нітро-5-дифторометоксианіліну Слід підкреслити лише, що в данному випадку нітрування сполуки (XIII) приводить тільки до одного можливого нітропродукту (XIV), і таким чином синтез дещо спрощується. Склад та будова усіх нових сполук, що заявляються, підтверджені даними елементного аналізу та спектрами ПМР. Далі наведені конкретні приклади одержання сполук, що заявляються. Приклади 1. 7-Дифторметокси-3-метил-2Н-1,2,4бензотіадіазин-1,1-діоксид (Іа) Суміш 7,15г (0,03моль) 2-аміно-5дифторометоксибензолсульфаміду (XI) та 30мл 5 77344 6 оцтового ангідриду кип'ятять 2 години. Відганяють (IV) 45%. Т.пл. 83-84°С. Знайдено, %: С 41,40; Η 15-20мл суміші оцтової кислоти та ангідріду, до 3,28; F 18,46. C7H6F2N2O3. Розраховано, %: С залишка додають 15мл диметилацетаміду та 2,5г 41,15; Η 2,94; F 18,61. ΠΜΡ (CDCl3) , м.ч.: 6,13 с (0,03моль) безводного ацетата натрію. Реакційну (2Н, ΝΗ2); 6,37 д.д (1Н, Н4); 6,42 д (1Н, Н6); 6,51 т суміш кип'ятять 6 годин, відганяють від неї розчин(1Η, OCHF2); 8,11 д (1Н, Н2). ники до об'єму 10мл. Після охолодження залишок 5. 2-Нітро-5-дифторометокси бензолсульфохрозмішують з 150мл води і створений кристалічний лорид (IX) осад відділяють фільтруванням та кристалізують з Розчиняють 8,16г (0,04моль) 2-нітро-5водного метанолу. Вихід: 7,08г (90%). Т.пл.=230дифторометоксианіліну (VII) при температурі 238°С. Знайдено. %: С 40,97; Η 2,85; Ν 10,64. (70±2)°С у 150мл соляної кислоти з масовою частC9H8F2N2O3S. Розраховано, %: С 41,42; Η 3,08; Ν кою основної речовини 20%. Утворений розчин 10,68. Спектр ПМР (ДМСО-d6) , м.ч.: 2,30 с (3Н, при перемішуванні охолоджують до температури СН3); 7,34-7,59 (1H,OCHF2; 1H,H5; 1H, Η6; 1Η, Н8); мінус (3±2)°С. При цьому випадає осад гідрохло12,18 с (1Н, Н4). риду 2-нітро-5-дифторометоксианіліну. До утворе2. 6-Дифторметокси-3-метил-2Н-1,2,4ної суспензії додають при перемішуванні розчин бензотіадіазин-1,1-діоксид (la) 2,76г (0,04моль) нітриту натрію у 20мл води з таОдержаний аналогічним способом виходячи з кою швидкістю, щоб температура реакційної маси 2-аміно-4-дифторометоксибензолсульфаміду не була вище 0°С. При цьому утворюється майже (XVIII), Вихід: (91%). Т.пл.=227°С, Знайдено, %: С прозорий розчин солі діазонію. 41,05; Η 3,11; Ν 10,59. C9H8F2N2O3S. Розраховано, У тригорлий реактор з механічною мішалкою, %: С 41,42; Η 3,08; Ν 10,68. Спектр ΠΜΡ (ДМСОкрапельною воронкою та барботером вносять 100мл льодяної оцтової кислоти та розчин 0,5г d6) , м.ч.: 2,30 с (3Н, СН3); 6,99 д (1Н, Н5); 7,24 д.д хлориду міді (II) в 10мл води. Суміш насичують при (1Н, Н7); 7,38 т (1Н, OCHF2); 7,89 д (1Н, Н8); 12,12 с температурі (0±2)°С сірчистим газом, а потім при (1Н, Н4). цій температурі пропускають струмень сірчистого 3. 3-Дифторометоксиацетанілід (IV). газу і поступово додають раніше одержаний розЗмішують 15,9г (0,1моль) 3чин солі діазонію з такою швидкістю, щоб темпедифторометоксиацетаніліну та 12,5г (0,12мол) ратура суміші в реакторі не перевищувала 3°С. оцтового ангідриду. Суміш перемішують при темПісля закінчення додавання солі перемішують при пературі (60±2)°С протягом 1год. Оцтову кислоту температурі (7±2)°С до припинення виділення газу відганяють в вакуумі (20мм рт.ст.) при температурі (біля 40хв). Продукт екстрагують бензолом, су(60±2)°С. Залишок кристалізують із суміші беншать MgSO4. Після того, як бензол відганяють та зол/гексан (1:3). Вихід сполуки (IV) 97%. Т.пл. 73сушать в вакуумі 0,1мм рт.ст. при температурі 74°С. (30±2)°С протягом 3год, вихід важкої олії - сульфо4. 2-Нітро-5-дифторометоксианілін (VII) хлориду (IX) кількісний. Охолоджують до температури мінус (10±2)°С 6. 2-Нітро-5-дифторометоксибензолсульфа10мл концентрованої сірчаної кислоти з масовою мід (X). часткою основної речовини 96% (густина 1,84). Сульфохлорид (IX), 11,5г (0,04моль) розчиняПри перемішуванні присипають до неї 10г ють у 100мл безводного етеру та пропускають (0,05моль) 3-дифторометоксиацетаніліду (IV). До струмень амоніаку при кімнатній температурі утвореної суспензії, яку інтенсивно перемішують, (18±2)°С до завершення його поглинання (біля прикапують суміш 10мл концентрованої азотної 1год). Перемішування продовжують ще 2год, потім кислоти з масовою долею основної речовини 80% випаровують розчинник у вакуумі, а залишок крис(питома вага 1,41) та 5мл концентрованої сірчаної талізують із суміші бензол/гексан (1:2). Вихід 8,37г кислоти з масовою долею основної речовини 96% (78%). Т.пл. 95-98°С. Знайдено, %: N 10,50. (питома вага 1,84). Реакційну суміш охолоджують C7H6F2N2O5S Розраховано, %: N 10,45. ПМР так, щоб її температура не підвищувалася вище за мінус 7°С. Після додавання всієї кількості нітрую(CDCl3) , м.ч.: 5,58 с (2Н, SO2NH2); 6,67 т (1Н, чої суміші продовжують перемішування утвореної OCHF2); 7,46 д. д. (1Н, Η4); 7,94 д. (1Н, Η2); 8,03 д. маси при температурі (0±2)°С протягом 1год та (1Η, Η5). виливають на льод. При цьому випадає осад, який 7. 2-Аміно-5-дифторометоксибензолсульфавідфільтровують, потім промивають водою так, мід (XI), щоб промивні води мали рН 7. Продукт, який є До розчину 8г (0,03моль) нітросульфаміду (Х) сумішшю ізомерних нітроацетанілідів (V та VI), та 10г (0,187моль) NH4CI в 80мл метанолу та 45мл змішують з розчином 5г (0,125моль) гідроксиду води при кипінні та розмішуванні додають невелинатрію в 25мл води та 25мл метанолу. Суміш інтечкими порціями 10г (0,178моль) залізного порошнсивно перемішують при температурі 70-80°С ка. Кип’ятять 1-1,5 години. Реакційну суміш фільт1год, а потім охолоджують при температурі рують у гарячому стані через складчастий фільтр, (20±2)°С. Утворені кристали відфільтровують, крипромивають гарячим метанолом (3 20мл). До фісталізують із водного метанолу з додаванням акльтрату додають 200мл води, при цьому коагулютивованого вугілля. Продукт є сумішшю 2-нітро-5ють залишки заліза. Суміш фільтрують через дифторометоксианіліну (VII) та 4-нітро-5складчастий фільтр. Якщо розчин забарвлений, дифторометоксианіліну (VIII) у молярному співвідкип’ятять зі жменькою активованого вугілля і знов ношенні 2:1. Аміно продукти розділяють колоночфільтрують. Розчин випаровують до об’єму 150ною хроматографією на силікагелі марки MN200мл та залишають на ніч у холодильнику. ОдеKiesel-gel-60. Елюент - хлористий метилен. Вихід ржаний осад відфільтровують та сушать. Вихід 2-нітро-5-дифторометоксианіліну (VII) з сполуки 6,36г (89%). Т. т.. 105-107°С. Знайдено, %: N 7 77344 8 11,94 C7H8F2N2O3S. Розраховано, %: Ν 11,76. Т. т.. 94-97°С. Знайдено, %: N 11,85 C7H8F2N2O3S. Спектр ΠΜΡ (CDCl3) , м.ч.: 4,83 с (2Η, ΝΗ2); 4,97 с Розраховано, %: Ν 11,76. Спектр ПМР (CDCl3) , (2Н, SO2NH2); 6,42 т (1H,OCHF2); 6,79 д (1H, Η3); м.ч.: 4,84 с (2Η, ΝΗ2); 4,95 с (2Η, SO2NH2); 6,507,17 д.д (1Н, Н4); 7,58 д (1H, Н6). 6,55 м (1H, OCHF2; 1H, Η3; 1Η, Η5); 7,75 д (1H, Η6). 8. 4-Дифторометоксиацетанілід (ХIIІ). Спектри ПМР записані на спектрометрі Varian Одержаний аналогічно 3VXP-300, робоча частота 299,95МГц. дифторометоксиацетаніліду (IV) виходячи з 4Дослідження фармакологічної дії нових сполук дифторометоксианіліну (XII), Вихід 87%. Т. т.. (Іа) та (Іб). 115-116°С Експериментальне вивчення впливу досліджу9. 2-Нітро-4-дифторометоксиацетанілід (XIV) ваних сполук на серцево-судинну систему провоАцетанілід (XIII) нітрують в тих же умовах, як дили на наркотизованих тіопенталом натрію сполуку (IV). Після виливання на льод випадає т. слих щурах лінії Вістар вагою 250-300г і моросад, який відфільтровують, промивають водою ських свинках вагою 580-780г. Визначали показни(рН 7), сушать на повітрі та кристалізують із суміші ки гемодинаміки: артеріальний тиск – систолічний і бензол/гексан (1:2). Вихід 78%. Т. т.. 69-71°С. діастолічний (Атсист. І Атдіаст.) – прямим методом 10. 2-Нітро-4-дифторометоксианілін (XV) в сонній артерії за допомогою елєктроманометра, Омилюють ацетанілід (XIV) розчином гідрокчастоту серцевих скорочень (ЧСС) – за ЕКГ, заресиду натрію в тих же умовах, як суміш єстрованою у другому стандартному відведенні, т. инамікдів (V) та (VI). Кристалізують із суміші ударний об’єм крові (УОК) – т. инаміки метот.зол/гексан (1:2) з додаванням силікагелю. Продом. Показники реєстрували у вихідному стані і дукт має вигляд т. инаміки кристалів. Вихід протягом 60 хвилин після введення речовин, запи78%. Т. т.. 68-69°С. сували на приладі Polygraph System 600, Nihon 11. 2-Нітро-4-дифторометокси бензолсульфоKohden, Японія. Речовини розчиняли в ДМСО і хлорид (XVI) вводили в підключичну вену в дозі 5мг/кг ваги тваАнілін (XV) діазотують та сульфохлорують в рини. Вплив речовин на судинний тонус щурів витих же умовах, як анілін (VII). Утворюється криставчали за допомогою методу тензометричного вилічний продукт, який промивають льодяною вомірювання ізольованих судинних препаратів, а дою. Сушать в вакуумі, кристалізують з бензолу. дослідження впливу на перфузійний тиск коронарВихід 80%. Т. т.. 79-80°С. Знайдено, %: N 5,25, S них судин та протекторні властивості проводили 10.69. C7H4CIF2NO5S. Розраховано, %: N 4,87, S на ізольованому серці, яке перфузували по Ланге10,64 ндорфу. Визначення достовірності отриманих ре12. 2-Нітро-4-дифторометокси бензолсульфазультатів проводили за методом Стьюдента. Досмід (XVII) товірним вважали рівень значимості р
ДивитисяДодаткова інформація
Назва патенту англійською7(6)- difluoromethoxy -3-methyl-2н-1,2,4-benzothiadiazine-1,1-dioxide
Автори англійськоюYahupolskyi Lev Musiiovych, Malietina Iryna Isaakivna, Petko Kyrylo Ihorevych, Moibenko Oleksii Oleksiiovych, Strutynskyi Ruslan Borysovych
Назва патенту російською7(6)-дифторметокси-3-метил-2н-1,2,4-бензотиадиазин-1,1-диоксид
Автори російськоюЯгупольский Лев Мусийович, Малетина Ирина Исааковна, Петко Кирилл Игоревич, Мойбенко Алексей Алексеевич, Струтинский Руслан Борисович
МПК / Мітки
МПК: C07D 285/24, A61K 31/54
Мітки: 7(6)-дифторметокси-3-метил-2н-1,2,4-бензотіадіазин-1,1-діоксид
Код посилання
<a href="https://ua.patents.su/6-77344-76-diftormetoksi-3-metil-2n-124-benzotiadiazin-11-dioksid.html" target="_blank" rel="follow" title="База патентів України">7(6)-дифторметокси-3-метил-2н-1,2,4-бензотіадіазин-1,1-діоксид</a>
Попередній патент: Спосіб рафінування алюмінієвих сплавів
Наступний патент: Штам бактерій rhodococcus erythropolis ek-1 – продуцент поверхнево-активних речовин
Випадковий патент: Вихровий повітроохолоджувач з очищенням інею










