Мічені радіоактивним галогеном похідні фенілоксіаніліну
Номер патенту: 93870
Опубліковано: 25.03.2011
Автори: Чжан Мін-Рон, Крістар Халдін, Судзукі Кадзутосі, Накадзато Ацуро, Сухара Тецуя
Формула / Реферат
1. Мічене радіоактивним галогеном похідне фенілоксіаніліну, представлене формулою (1)
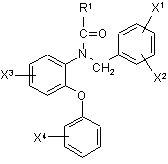 , Формула 1
, Формула 1
де R1 представляє атом водню, заміщену або незаміщену алкільну групу, що має 1-10 атомів вуглецю, а X1, X2, X3 та X4 однакові або різні і кожен представляє кожний атом водню, алкоксигрупу, що має 1-5 атомів вуглецю, атом галогену, радіоактивний атом галогену, вибраний з-поміж 121І, 123І,124І, 125І, 131І, 75Вr, 76Вr, 77Вr та 34mСl, за умови, що принаймні один з X1, X2, X3 та X4 представляє радіоактивний атом галогену, вибраний з-поміж 121I, 123І, 124І, 125І, 131I, 75Вr, 76Вr, 77Вr та 34mСl.
2. Мічене радіоактивним галогеном похідне фенілоксіаніліну, як заявлено в п. 1, де
R1 представляє алкільну групу, що має 1-10 атомів вуглецю,
X1 та X2 представляють кожний алкоксигрупу, що має 1-5 атомів вуглецю,
X3 представляє радіоактивний атом галогену, вибраний з-поміж 121І, 123І, 124І, 125І, 131І,75Вr, 76Вr, 77Вr та 34mСl, а
X4 представляє атом водню.
3. Мічене радіоактивним галогеном похідне фенілоксіаніліну за п. 1, де
R1 представляє алкільну групу, що має 1-10 атомів вуглецю,
X1 та X2 є однакові або різні й представляють кожний алкоксигрупу, що має 1-5 атомів вуглецю, або радіоактивний атом галогену, вибраний з-поміж 121І, 123І, 124І, 125І, 131І, 75Вr, 76Вr, 77Вr та 34mСl, за умови, що один з X1 або X2 представляє радіоактивний атом галогену, вибраний з-поміж 121І, 123І, 124І, 125І, 131I, 75Вr, 76Вr, 77Вr та 34mСl,
X3 представляє атом галогену, а
X4 представляє атом водню.
Текст
1. Мічене радіоактивним галогеном похідне фенілоксіаніліну, представлене формулою (1) X1 R1 C2 2 UA 1 , Формула 1 Цей винахід стосується мічених радіоактивним галогеном похідних фенілоксіаніліну, які мають високу спорідненість до периферійних рецепторів бензодіазепину. 3 Передумови створення винаходу Рецептори бензодіазепину (БЗ) поділяються на центральні та периферійні. Периферійні рецептори бензодіазепину (ПРБ) були спочатку відкриті у периферійних органах, але вони також зустрічаються у центральній нервовій системі. Більш того, встановлено, що щільність ПРБ у центральній нервовій системі досить висока, така сама, або навіть більша, ніж центральних рецепторів бензодіазепину (ЦРБ) у такій самій області. Виконані дослідження пов'язують ПРБ з такими захворюваннями, як хвороба Альцгеймера, передньоскроневе слабоумство, розсіяна корпускулярна хвороба Леві, пошкодження судин, стани, пов'язані із хворобою Паркінсона, кортікобазилярне виродження, хвороба Паркінсона, хорея Гантінгтона, множинна системна атрофія, множинний склероз, епілепсія, менінгіт, енцефаліт, травми периферійних нервів, рак гортані, рак молочної залози, пухлини яєчника, рак печінки, рак великого кишковика, рак шлунку, пухлини надниркової залози, гліома, гліобластома, фібробластома, нейросаркома, рак легенів, рак матки, лімфома, рак простати, меланома, пухлини яєчок, астроцитома, пухлини, що виробляють ектопічні гормони тощо. Для діагностики церебральної гліоми та хвороби Альцгеймера шляхом відображення внутрішньомозкового розподілу ПРБ на позитронному емісійному томографі (ПЕТ) використовують загальновідомий ліганд ПРБ - мічений 11С N-метил-N(1-метилпропил)-1-(2-хлорфеніл)-ізохінолін-3карбоксамід (надалі РК 11195). Однак, оскільки ця сполука дуже погано накопичується у мозку і важко піддається кількісному аналізу, бажано створити такий ліганд ПРБ, який давав би кращий сигнал. Зараз встановлено, що N-(2,5діметилоксібензил)-N-(5-фтор-2феноксіфеніл)ацетамід (надалі DAA1106) та N-(2фторметил-5-метоксібензил)-N-(5-фтор-2феноксіфеніл)ацетамід (надалі FMDAA1106) (патентний документ 2) та N-[2-(2-фтор)етил-5метоксібензил]-N-(5-фтор-2феноксіфеніл)ацетамід (надалі FEDAA1106) (патентний документ 2) посідають високу спорідненість та високу селективність і тому є придатні для цієї цілі. Отже, [11C]DAA1106, мічений 11С, [18F]FMDAA1106 та [18F]FEDAA1106, мічені 18F, дають сильний сигнал у якості ізотопних індикаторів на ПЕТ при зовнішньому підрахунку внутрішньомозкових ПРБ, уможливлюючи високоточний кількісний аналіз. Патентний документ 1: JP 11-171844 А Патентний документ 2: JP 2004-231647 А Розкриття винаходу Задача винаходу В основу винаходу покладене завдання створити сполуки, які можуть діяти як ліганди ПРБ з високою спорідненістю та високою селективністю й дозволяють вимірювати ПРБ з використанням не лише ПЕТ, але також і SPECT, причому ліганди ПРБ з високою спорідненістю та високою селективністю мітять при зовнішньому підрахунку ПРБ радіоактивними нуклідами галогенів. 93870 4 Засоби вирішення задачі Автори цього винаходу провели широкі дослідження з метою вирішення зазначеного завдання і встановили, що високої спорідненості до ПРБ можна досягти заміною алкільної групи у сполуках згідно з JP 11-171844 А на галогенізовану алкільну групу, чим і вирішується завдання винаходу. Отже, предметом цього винаходу є мічене радіоактивним галогеном похідне фенілоксіаніліну формули (1) Формула 1 де R1 представляє атом водню, заміщену або незаміщену алкільну групу, що має 1-10 атомів вуглецю, заміщену або незаміщену алкоксігрупу, що має 1-10 атомів вуглецю, заміщену або незаміщену фенільну групу, групу формули –NR2(R3), де R2 та R3 однакові або різні та представляють атом водню, заміщену або незаміщену алкільну групу, що має 1-10 атомів вуглецю, або разом із сусіднім атомом азоту утворюють 4-10-членну циклічну аміногрупу, а X1, X2, X3 та X4 однакові або різні й представляють кожний атом водню, алкільну групу, що має 1-5 атомів вуглецю, алкоксігрупу, що має 1-5 атомів вуглецю, феноксігрупу, трифторметильну групу, карбамоїльну групу, аміносульфонільну групу, атом галогену або радіоактивний атом галогену, обрані з-поміж 121l, 123l, 124l, 125l, 131l, 75 Вr, 76Вr, 77Вr та 34mСl, за умови, що принаймні один з X1, X2, X3 та X4 представляє радіоактивний атом галогену, обраний з-поміж 121l, 123l, 124l, 125І, 131 75 l, Вr, 76Вr, 77Вr та 34mCl. Переважно предметом цього винаходу є мічене радіоактивним галогеном похідне фенілоксіаніліну за п. 1, де R1 представляє атом водню, заміщену або незаміщену алкільну групу, що має 1-10 атомів вуглецю, а X1, X2, X3 та X4 однакові або різні й представляють кожний атом водню, алкоксігрупу, що має 1-5 атомів вуглецю, атом галогену або радіоактивний атом галогену, обрані з-поміж 121l, 123 124 125 131 75 l, l, l, І, Вr, 76Вr, 77Вr та 34mСl, за умови, що принаймні один з X1, X2, X3 та X4 представляє радіоактивний атом галогену, обраний з-поміж 121l, 123 124 125 131 75 l, l, l, l, Вr, 76Вr, 77Вr та 34mСl. Більш переважно предметом цього винаходу є мічене радіоактивним галогеном похідне фенілоксіаніліну за п.1, де R1 представляє алкільну групу, що має 1-10 атомів вуглецю, X1 та X2 представляють кожний алкоксігрупу, що має 1-5 атомів вуглецю, X3 представляє радіоактивний атом галогену, обраний з-поміж 121l, 123l, 124l, 125І, 131l, 75Вr, 76Вr, 77Вr та 34mCl, a X4 представляє атом водню. В оптимальному варіанті предметом цього винаходу є мічене радіоактивним галогеном похідне 5 фенілоксіаніліну за п.1, де R1 представляє алкільну групу, що має 1-10 атомів вуглецю, X1 та X2 є однакові або різні й представляють кожний алкоксігрупу, що має 1-5 атомів вуглецю, або радіоакти121 123 124 вний атом галогену, обраний з-поміж l, l, І, 125 131 75 76 77 34m l, l, Вr, Вr, Вr та Сl, за умови, що один з X1 або X2 представляє радіоактивний атом галогену, обраний з-поміж 121l, 123l, 124l, 125l, 131l, 75Вr, 76Вr, 77 Вr та 34mСl, X3 представляє атом галогену, а X4 представляє атом водню. Крім того, предметом цього винаходу є діагностичний засіб для виявлення таких захворювань, як хвороба Альцгеймера, передньоскроневе слабоумство, розсіяна корпускулярна хвороба Леві, пошкодження судин, стани, пов'язані із хворобою Паркінсона, кортікобазилярне виродження, хвороба Паркінсона, хорея Гантінгтона, множинна системна атрофія, множинний склероз, епілепсія, менінгіт, енцефаліт, травми периферійних нервів, рак гортані, рак грудей, пухлини яєчника, рак печінки, рак великого кишковика, рак шлунку, пухлини надниркової залози, гліома, гліобластома, фібробластома, нейросаркома, рак легенів, рак матки, лімфома, рак простати, меланома, пухлини яєчок, астроцитома, пухлини, що виробляють ектопічні гормони, який містить у ролі діючої речовини мічене радіоактивним галогеном похідне фенілоксіаніліну за п. 1. Переваги даного винаходу Згідно з винаходом створені сполуки, які є лігандами ПРБ з високою спорідненістю та високою селективністю. Крім того, стає можливим вимірювання ПРБ у живому організмі з застосуванням на лише ПЕТ, а й SPECT, завдяки тому, що ліганди ПРБ з високою спорідненістю та високою селективністю мітять при зовнішньому підрахунку ПРБ радіоактивними нуклідами галогенів. Це уможливлює ранню діагностику таких захворювань, як хвороба Альцгеймера, передньоскроневе слабоумство, розсіяна корпускулярна хвороба Леві, пошкодження судин, стани, пов'язані із хворобою Паркінсона, кортікобазилярне виродження, хвороба Паркінсона, хорея Гантінгтона, множинна системна атрофія, множинний склероз, епілепсія, менінгіт, енцефаліт, травми периферійних нервів, рак гортані, рак грудей, пухлини яєчника, рак печінки, рак великого кишковика, рак шлунку, пухлини надниркової залози, гліома, гліобластома, фібробластома, нейросаркома, рак легенів, рак матки, лімфома, рак простати, меланома, пухлини яєчок, астроцитома, пухлини, що виробляють ектопічні гормони тощо. Крім того, сполуки за винаходом є придатні для профілактики та лікування зазначених захворювань. Короткий опис креслень Фіг.1 - авторадіограма ex vivo мозку щура за 30 хвилин після введення [131I]2IDAA1106; Фіг.2 - авторадіограма ех vivo мозку щура за 30 хвилин після введення [131I]2IDAA1106. Опис переважних варіантів здійснення винаходу У цьому винаході атомом галогену є атом фтору, атом хлору, атом брому або атом йоду, переважно атом фтору, атом брому або атом йоду, оптимально атом фтору або атом йоду. 93870 6 У цьому винаході алкільною групою, що має 110 атомів вуглецю, є пряма, розгалужена або циклічна алкільна група, наприклад, метильна, етильна, пропильна, ізопропильна, циклопропильна, бутильна, ізобутильна, циклобутильна, циклопропилметильна, пентильна, ізопентильна, циклопентильна, циклобутилметильна, 1-етилпропильна, гексильна, ізогексильна, циклогексильна, циклопентилметильна, 1-етилбутильна, гептильна, ізогептильна, циклогексилметильна, октильна, нонильна та децильна група. У цьому винаході заміщеною алкільною групою, що має 1-10 атомів вуглецю, є алкільна група, заміщена гідроксильною групою, алканоїлоксігрупа, алканоїльна група, алкокісгрупа, атом галогену, азидогрупа, аміногрупа, карбонільна група; як приклади можна навести гідроксіметильну, ацетилоксіметильну, метоксіметильну, хлорметильну, трифторметильну, азидометильну, амінометильну, діметиламінометильну, піролідинметильну групу. У цьому винаході алкоксігрупою, що має 1-10 атомів вуглецю, є пряма, розгалужена або циклічна алкоксігрупа, наприклад, метоксігрупа, етоксігрупа, пропоксігрупа, ізопропоксігрупа, бутоксігрупа, ізобутоксігрупа, циклопропилметоксігрупа, пентилоксігрупа, ізопентилоксігрупа, гексилоксігрупа, гептилоксігрупа, октилоксігрупа, нонилоксігрупа, децилоксігрупа. У цьому винаході заміщена фенільна група може бути заміщена однією-трьома групами, обраними з-поміж алкільної групи, що має 1-10 атомів вуглецю, алкільної групи, що має 1-10 атомів вуглецю, заміщеної атомом галогену, гідроксильною групою, алканоїлоксігрупою, що має 1-10 атомів вуглецю, карбоксильною групою або алкоксікарбонільною групою, алкенільної групи, що має 210 атомів вуглецю, алкоксігрупи, що має 1-10 атомів вуглецю, алкілтіогрупи, що має 1-10 атомів вуглецю, групи, представленої формулою O-Z-R4 (де Z представляє пряму або розгалужену алкіленову групу, що має 1-10 атомів вуглецю, a R4 представляє аміногрупу, аміногрупу, заміщену однією або двома алкільними групами, що мають 1-7 атомів вуглецю, циклічну аміногрупу, що має 27 атомів вуглецю, гідроксильну групу, карбоксильну групу або алкоксікарбонільну групу), алканоїльної групи, що має 2-10 атомів вуглецю, або її кеталю, формильної групи або її ацеталю, карбоксильної групи, алкоксікарбонільної групи, що має 2-10 атомів вуглецю, карбамоїльної групи, карбамоїльної групи, у якій атом азоту заміщений однією або двома алкільними групами, що мають 1-10 атомів вуглецю, аміносульфонільної групи, аміносульфонільної групи, у якій атом азоту заміщений однією або двома алкільними групами, що мають 1-10 атомів вуглецю, атома галогену та нітрогрупи; сюди входять, наприклад, 2метилфенільна група, 2-пропилфенільна група, 2ізопропилфенільна група, 2-циклопентилфенільна група, 2-(1-гідроксіетил)фенільна група, 2карбоксіметилфенільна група, 2метоксікарбонілфенільна група, 2-вінілфенільна група, 2-метоксіфенільна група, 3-метоксіфенільна група, 4-метоксіфенільна група, 2-етоксіфенільна 7 група, 2-гексилоксіфенільна група, 2ізопропоксіфенільна група, 2циклопентоксіфенільна група, 2,5діметоксіфенільна група, 2,4,6-триметоксіфенільна група, 4-метилтіофенільна група, 2ізопропилтіофенільна група, 4циклогексилтіофенільна група, 2-(2діметиламінетоксі)фенільна група, 2-(2гідроксіетоксі)фенільна група, 2карбоксіметоксіфенільна група, 2метоксікарбонілметоксіфенільна група, 2ацетилфенільна група, 2-(2-метил-1,3-діоксолан-2іл)фенільна група, 2-формилфенільна група, 2(1,3-діоксолан-2-іл)фенільна група, 2карбоксіфенільна група, 2-(Nметиламінкарбоніл)фенільна група, 2-(N,Nдіметиламінкарбоніл)фенільна група, 2амінокарбонілфенільна група, 2аміносульфонілфенільна група, 4аміносульфонілфенільна група, 2метиламіносульфонілфенільна група, 2діметиламіносульфонілфенільна група, 2фторфенільна група, 3-фторфенільна група, 4фторфенільна група, 3-хлорфенільна група, 4хлорфенільна група, 2-бромфенільна група, 3бромфенільна група, 4-бромфенільна група, 2,4діфторфенільна група, 2-нітрофенільна група, 2амінофенільна група, 2-піролідинфенільна група та 4-діметиламінфенільна група. У цьому винаході 4-10-членна циклічна аміногрупа, представлена формулою - NR2(R3), яка може містити атом азоту або атом кисню, являє собою, наприклад, піролідинову групу, піперидинову групу, піперазинову групу, Nметилпіперазинову групу, морфолінову групу. Сполуки за винаходом можна одержати із сполук, приготованих за способом, що описаний у JP 11-171844 А, як показано нижче (у формулах реакцій X1, X2 та R1 мають ті самі значення, як зазначено вище). Формула 2 Отже, сполуки N-(2-бензилоксі-5алкоксібензил)-N-(феноксіфеніл)ациламіду, які містять різні нерадіоактивні атоми галогенів, представлені вищенаведеною формулою, можуть реагувати з паладієвим комплексом та оловоорганічною сполукою з метою заміни нерадіоактивного атома галогену на оловоорганічний замінник, а потім реагувати з різними радіоактивними галогенними сполуками з одержанням похідних фенілоксіаніліну, мічених атомом галогену. Тут принаймні один з X1, X2, X3 та X4 представляє радіоактивний атом галогену, обраний з-поміж 121І, 123 124 І25 131 75 І, І, І, l, Вr, 76Вr, 77Вr та 34mСl. Далі винахід докладніше описується на прикладах одержання та випробувальних прикладах. 93870 8 Приклади Приклад 1 Одержання [131І]-N-(2,5-діметоксібензил)-N-(5йод-2-феноксіфеніл)ацетаміду (надалі [131I]11 DAA1106) 1-1)510 мг (1,12 ммоля) N-(2,5діметоксібензил)-N-(5-бром-2феноксіфеніл)ацетаміду розчиняють у толуолі та піддають циркуляції з гексабутилдіоловом (IV) та діхлорбіс(трифенілфосфін)паладієм (0) протягом 4 діб. Після видалення толуолу продукт реакції очищують колонковою хроматографією з силікагелем (елюент гексан : етилацетат = 1:4), одержуючи 320 мг N-(2,5-діметоксібензил)-N-(5трибутилстаннил-2-феноксіфеніл)ацетаміду. FABMS C36H48FNO3Sn (m/z) 680,5 (m++1) До розчину 55 мг (0,083 ммоля) N-(2,5діметоксібензил)-N-(5-трибутилстаннил-2феноксіфеніл)ацетаміду у хлороформі додають 100 мг твердого йоду, рідку реакційну суміш перемішують при кімнатній температурі 1 годину, після чого додають насичений водний розчин тіосульфату натрію, доки суміш не стане безбарвною. Органічну фазу відокремлюють, промивають насиченим розсолом та сушать над безводним сульфатом магнію. Сирий продукт, одержаний випарюванням розчинника під зниженим тиском, очищують колонковою хроматографією з силікагелем (елюент гексан : етилацетат =1:4), одержуючи 32 мг (вихід 77%) цільової сполуки. 1-2)100 мкл суміші 3:1 оцтової кислоти з 30% перекисом водню додають до 100 мкл етилацетатефіру 0,1 мг N-(2,5-діметоксібензил)-N-(5трибутилстаннил-2-феноксіфеніл)ацетаміду й перемішують. До суміші додають [131I]NaI (0,1 мКі) і дають відстоятися 1 хвилину. Після закінчення реакції суміш піддають напівпрепаративній високоточній рідинній хроматографії із зверненою фазою (колонка YMC J'sphere ODS-Н80, внутрішній діаметр 10250 мм). Частину [131І]11 DAA1106 одержують з CH3CN/H2O (9:1) у якості рухомої фази при витраті 4 мл/хв. З цієї частини розчинник видаляють під зниженим тиском, осад розчиняють в 1 мл нормального розсолу, а потім пропускають крізь фільтр Millipore 0,22 мкм, одержуючи [131І]11 DAA1106 (0,091 мКі). Приклад 2 Одержання N-(2-[131І]йод-5-метоксібензил)-N(5-фтор-2-феноксіфеніл)ацетаміду (надалі [131І]21DАА1106) 100 мкл суміші 3:1 оцтової кислоти з 30% перекисом водню додають до 100 мкл етилацетатефіру 0,1 мг N-(2-трибутилстаннил-5метоксібензил)-И-(5-фтор-2феноксіфеніл)ацетаміду й перемішують. Додають [131I]NaI (0,1 мКі) і дають відстоятися 1 хвилину. Після закінчення реакції суміш піддають напівпрепаративній високоточній рідинній хроматографії із зверненою фазою (колонка YMC J'sphere ODSH80, внутрішній діаметр 10250 мм). Частину [131І]11 DAA1106 одержують з CH3CN/H2O (9:1) у якості рухомої фази при витраті 4 мл/хв. З цієї частини розчинник видаляють під зниженим тиском, осад розчиняють в 1 мл нормального розсолу, а 9 потім пропускають крізь фільтр Millipore 0,22 мкм, одержуючи [131І]2lDАА1106 (0,095 мКі). Випробувальний приклад Авторадіографія ex vivo На фіг.1 та 2 наведені авторадіограми ex vivo мозку щура, зроблені за 30 хвилин після введення [131I]2IDAA1106. [131I]2IDAA1106 відносно активно приникає до мозку, як видно на фіг.1, й відповідає основним вимогам до радіоліганду. Радіоактивність досить рівномірно розподіляється у нюховій головці, хороїдному сплетінні та мозочку, і ця картина розподілу збігається з внутрішньомозковим розподілом периферійних рецепторів бензодіазепину. Крім того, радіоактивність зменшується в усьому мозку, як показано на фіг.2, коли одночасно вводять DAA1106 та [131I]2IDAA1106. Зокрема, рівні радіоактивності у нюховій головці, хороїдному сплетінні та мозочку помітно зменшуються і становлять 20% значення за фіг.1 або й менше. Це свідчить про те, що [131I]2IDAA1106 є радіолігандом, специфічним до периферійних рецепторів бензодіазепину. Крім того, можна вважати, що [131I]2IDAA1106 здатний відтворювати зображення периферійних рецепторів бензодіазепину. Далі описується синтез сполук за винаходом, які містять алкоксігрупу з введеним до неї 11С. Приклад 3 N-(4-хлор-2-феноксіфеніл))-N-(2-[211 С]ізопропоксібензил)ацетамід ([11С]3) Надчистий газоподібний азот під 1,5 МПа з вмістом 0,01% газоподібного кисню опромінюють протонами 18,5 МеВ від циклотрона й одержують вільний від носіїв [11С]СО2 шляхом ядерної реакції 14 N (р, ) 11С. Після опромінювання [11С]СО2 відокремлюють від опромінюваного газу за допомогою 500 мл/хв N2 та концентрують, поки радіоактивність в усьому змійовику з нержавіючої сталі, який охолоджується рідким N2 при -150°С, не стабілізується. Концентрований [11С]СО2 підігрівають і дають витекти до контуру, який містить CH3MgBr з сухим N2 (2 мл/хв) при -5°С. Коли перехід радіоактивності закінчується, подачу N2 припиняють і підтримують у контурі 93870 10 Формула 3 DAA1106 (2): R=CH3 DAA1097 (3): [11C]DAA1106 ([11С] (2): R=CH(CH3)2 R=11СН3 [11С] 3: R=11CH(CH3)2 [11C] 3: R=11CH2CH3 [11С] 8: R=11СН3 Формула 4 DAA1097 (3): R=CH(CH3)2 [11C] 3: R=11CH(CH3)2 [11C] 3: R=11CH2CH3 [11C] 8: R=11CH3 температуру 25°С протягом 5 хвилин, щоб пройшла реакція Гріньяра. Після того через контур пропускають 500 мкл розчину 0,2 М LiAlH4 у ТГФ і подають реакційну суміш до реактора-нагрівача при 180°С на 1 хвилину. Далі реактор охолоджують до 50-60°М, після чого додають 800 мл 57%-ого водного розчину НІ. Суміш у реакторі нагрівають до 180°С і одержану радіоактивну фракцію продувають 50 мл/хв N2 та подають на вхід колонки Porapak при кімнатній температурі. N2 прокачують 3 хвилини, доки не стабілізується рівень радіоактивності на вході колонки. При нагріванні колонки із швидкістю 15°С/30 сек. починається витік [11С]lO з виходу колонки протягом 6 хвилин, і його збирають до вмістини з 1 мл безводного ДМФ. Далі цей [11С]СО2 реагує з реагентом Гріньяра MeMgBr, після чого його відокремлюють газовою хроматог 11 93870 рафією, одержуючи [11С]lO (3,7-4,4 ГБк, n=3) з радіохімічною чистотою >95%. Суспензію 1,0 мг 9, [11С]10 (3,0-3,2 ГБк) та NaH у ДМФ (7 мкл, 0,5 г / 20 мл ДМФ) нагрівають до 130°С та витримують при цій температурі 10 хвилин. Реакційну суміш з вмістом [11С]3 гасять доданням CH3CN/H2O (90:10, 0,5 мл) та розділяють у напівфракціонуючій колонці (внутрішній діаметр 10 мм250 мм, CAPSELL РАК C18, фірми Сісейдо), оснащеній системою високоточної рідинної хроматографії JASCO. Елюентом у колонці слугує CH3CN/H2O із швидкістю 5,0 мл/хв, цільову фракцію (tR=8,8 хвилин) збирають до колби. Розчинник видаляють із колби під зниженим тиском при 90°С, а осад збирають до 10 мл стерилізованого розсолу. Розсіл із [11С]3 пропускають крізь стерилізований фільтр 0,22 мкм до стерилізованої пляшки. Наприкінці синтезу одержують [11С]3 (180-310 МБк, n=3) з радіохімічною чистотою >98%. Приклад 4 N-(4-хлор-2-феноксіфеніл))-N-(2-[211 С]етоксібензил)ацетамід ([11С]7) Наприкінці синтезу одержують [11С]11 (3,95,3 ГБк, n=3) з радіохімічною чистотою >95% шляхом реакції CH3MgBr з [11С]СО2. Суспензію 1,0 мг 9, [11С]11 (3,0-3,2 ГБк) та NaH у ДМФ (7 мкл, 0,5 г / 20 мл ДМФ) в 1 мл ДМФ нагрівають до 50°С та витримують при цій температурі 5 хвилин. Реакційну суміш очищують у такій самій колонці, як у попередньому прикладі, тільки для одержання цільової радіоактивної фракції використовують CH3CN/H2O (80:20) (tR=8,1 хвилин). Після обробки таким само чином, як [11С]3, наприкінці синтезу одержують [11С]7 (300-350 МБк, n=3) з радіохімічною чистотою >98%. Приклад 5 N-(4-хлор-2-феноксіфеніл))-N-(2-[211 С]метоксібензил)ацетамід ([11С]8) Комп’ютерна верстка М. Ломалова 12 Одержання [11C]12 та наступне метилювання [11С]9 у [11С]8 виконують в автоматичному синтезаторі. Одержаний [11С]12 дистилюють, пропускають через колонку з аскаритом та Р2О5 і вміщують до колби, яка містить 1,0 мг 9, NaH у ДМФ (7 мкл, 0,5 г / 20 мл ДМФ) та 1 мл ДМФ, на 1,5 хвилини при температурі від -15 до -20°С. Далі колбу нагрівають до 30°С й витримують при цій температурі 5 хвилин. Реакційну суміш очищують у такій само колонці, як у попередньому прикладі, тільки для одержання цільової радіоактивної фракції використовують CH3CN/H2O (70:30) (tR=9,5 хвилин). Після обробки таким само чином, як [11С]3, наприкінці синтезу одержують [11С]8 (1,0-1,3 ГБк, n=3) з радіохімічною чистотою >98%. Приклад 6 N-(5-фтор-2-феноксіфеніл))-N-(2-[211 С]метоксі-5-метоксібензил)ацетамід ([11С]2) Зазначену сполуку одержують аналогічно способу, наведеному у прикладі 5. Промислова придатність Сполуки за винаходом можуть використовуватися для діагностики на ранній стадії таких хвороб, як хвороба Альцгеймера, передньоскроневе слабоумство, розсіяна корпускулярна хвороба Леві, пошкодження судин, стани, пов'язані із хворобою Паркінсона, кортікобазилярне виродження, хвороба Паркінсона, хорея Гантінгтона, множинна системна атрофія, множинний склероз, епілепсія, менінгіт, енцефаліт, травми периферійних нервів, рак гортані, рак грудей, пухлини яєчника, рак печінки, рак великого кишковика, рак шлунку, пухлини надниркової залози, гліома, гліобластома, фібробластома, нейросаркома, рак легенів, рак матки, лімфома, рак простати, меланома, пухлини яєчок, астроцитома, пухлини, що виробляють ектопічні гормони, а також для профілактики та лікування зазначених хвороб. Підписне Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюRadioactive halogen-labeled phenyloxyaniline derivatives
Автори англійськоюSuzuki Kazutoshi, Suhara Tetsuya, Christar Halldin, Zhang Ming-Rong, Nakazato Atsuro
Назва патенту російськоюМеченные радиоактивным галогеном производные фенилоксианилина
Автори російськоюСудзуки Кадзутоси, Cyxapa Тецуя, Кристар Халдин, Чжан Мин-Рон, Накадзато Ацуро
МПК / Мітки
МПК: C07C 233/25, A61K 51/00, C07B 59/00
Мітки: фенілоксіаніліну, мічені, радіоактивним, похідні, галогеном
Код посилання
<a href="https://ua.patents.su/6-93870-micheni-radioaktivnim-galogenom-pokhidni-feniloksianilinu.html" target="_blank" rel="follow" title="База патентів України">Мічені радіоактивним галогеном похідні фенілоксіаніліну</a>
Попередній патент: Спосіб одержання піразолів
Наступний патент: Електронний ендоскоп
Випадковий патент: Пристрій для спуску людей по пожежному рукаву










