Спосіб одержання сертиндолу
Формула / Реферат
1. Спосіб одержання N-(4-фторфеніл)-N-(2-карбокси-4-хлорфеніл)гліцину, при якому здійснюють каталізоване міддю арилування 2,5-дихлорбензойної кислоти за допомогою N-(4-фторфеніл)гліцину, в якому використовують солі лужних металів 2,5-дихлорбензойної кислоти та N-(4-фторфеніл)гліцину у водно-лужному реакційному середовищі в присутності мідного каталізатора у відповідності зі схемою реакції:
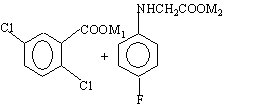
1)Основа/Cu/H2O
![]()
2)Водний розчин
кислоти
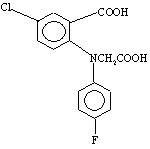 ,
,
де М1 і М2 - іони лужних металів.
2. Спосіб за п.1, який відрізняється тим, що реакцію здійснюють при підвищеній температурі, переважно при температурі між 80°С і температурою флегми середовища, зокрема близької до температури флегми.
3. Спосіб за п.1 або п.2, який відрізняється тим, що реакційне середовище є водою або водою, до якої додано співрозчинник.
4. Спосіб за п.3, який відрізняється тим, що як реакційне середовище використовують воду.
5. Спосіб за п.3 або п.4, який відрізняється тим, що кількість води становить менш ніж 10 мл/г 2,5-дихлорбензойної кислоти, переважно менш ніж 5 мл/г.
6. Спосіб за п.5, який відрізняється тим, що кількість води менш ніж 3,5 мл/г, переважно менш ніж 2,5 мл/г 2,5-дихлорбензойної кислоти.
7. Спосіб за будь-яким з пп.1-6, який відрізняється тим, що солі лужних металів реагентів є солями літію, натрію або калію.
8. Спосіб за п.7, який відрізняється тим, що використовують однакові солі лужних металів реагентів, переважно солі калію.
9. Спосіб за будь-яким з пп.1-8, який відрізняється тим, що основа є карбонатом лужного металу, переважно Li2СО3, Na2CO3 або К2СО3.
10. Спосіб за п.9, який відрізняється тим, що лужний метал карбонату лужного металу є тим же, що і лужний метал солей лужного металу реагентів.
11. Спосіб за будь-яким з пп.1 - 8, який відрізняється тим, що основа є карбонатом калію.
12. Спосіб за будь-яким з пп.1-11, який відрізняється тим, що кількість основи більше ніж стехіометрична кількість 2,5-дихлорбензойної кислоти.
13. Спосіб за будь-яким з пп.1-12, який відрізняється тим, що каталізатором є мідь-бронза.
14. Спосіб за будь-яким з пп.1-13, який відрізняється тим, що співвідношення кількостей солі лужного металу N-(4-фторфеніл)гліцину і солі лужного металу 2,5-дихлорбензойної кислоти складає від 0,5 до 3,0, переважно від 1,0 до 2,5, зокрема від 2,0 до 2,3 мол/мол.
15. Спосіб одержання 5-хлор-1-(4-фторфеніл)-3-(1,2,3,6-тетрагідропіридин-4-іл)індолу, при якому здійснюють реакцію 5-хлор-1-(4-фторфеніл)індолу з 4-піперидоном у суміші мінеральної кислоти і оцтової кислоти.
16. Спосіб за п.15, який відрізняється тим, що 4-піперидон використовують у формі гідрохлориду 4-піперидонгідрату.
17. Спосіб за п.15 або п.16, який відрізняється тим, що як мінеральну кислоту використовують фосфорну кислоту, азотну кислоту, сірчану кислоту або соляну кислоту.
18. Спосіб за п.17, який відрізняється тим, що як мінеральну кислоту використовують концентровану соляну кислоту.
19. Спосіб за п.15 або п.16, який відрізняється тим, що використовують принаймні 1,5 еквівалента 4-піперидону на еквівалент 5-хлор-1-(4-фторфеніл)індолу.
20. Спосіб за п.19, який відрізняється тим, що використовують принаймні 1,75 еквівалента 4-піперидону на еквівалент 5-хлор-1-(4-фторфеніл)індолу.
21. Спосіб за п.20, який відрізняється тим, що використовують принаймні 2,0 еквівалента 4-піперидону на еквівалент 5-хлор-1-(4-фторфеніл)індолу.
22. Спосіб за п.18, який відрізняється тим, що соляну кислоту використовують в кількості принаймні 2,5 мл концентрованої НСl на грам 5-хлор-1-(4-фторфеніл)індолу.
23. Спосіб за п.15 або п.16, який відрізняється тим, що використовують принаймні 8 мл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)індолу.
24. Спосіб за п.23, який відрізняється тим, що використовують принаймні 10 мл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)індолу.
25. Спосіб за п.24, який відрізняється тим, що використовують 10 -14 мл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)індолу.
26. Спосіб за п.22, який відрізняється тим, що співвідношення концентрованої НСl на грам 5-хлор-1-(4-фторфеніл)індолу складає 3,5 - 5 мл.
27. Спосіб за п.18, який відрізняється тим, що співвідношення між оцтовою кислотою та концентрованою НСl складає від 2:1 до 4:1 (об'єм/об'єм).
28. Спосіб одержання сертиндолу, при якому здійснюють етапи, в яких:
a) одержують N-(4-фторфеніл)-N-(2-карбокси-4-хлорфеніл)гліцин за будь-яким з пп.1-14 шляхом взаємодії солі лужного металу 2,5-дихлорбензойної кислоти з сіллю лужного металу N-(4-фторфеніл)гліцину у водно-лужному реакційному середовищі в присутності мідного каталізатора,
б) проводять циклізацію N-(4-фторфеніл)-N-(2-карбокси-4-хлорфеніл)гліцину до відповідного 3-ацетоксііндолу з використанням оцтового ангідриду/ацетату лужного металу, переважно ацетату натрію,
в) відновлюють 3-ацетоксііндол і після цього,
г) вилучають Н2O з одержанням таким чином 5-хлор-1-(4-фторфеніл)індолу,
д) здійснюють взаємодію 5-хлор-1-(4-фторфеніл)індолу з 4-піперидоном за будь-яким з пп.15-27 в суміші оцтової кислоти та концентрованої НСl,
е) відновлюють одержаний 5-хлор-1-(4-фторфеніл)-3-(1,2,3,6-тетрагідропіридин-4-іл)індол для одержання 5-хлор-1-(4-фторфеніл)-3-(піперидин-4-іл)індолу,
є) здійснюють взаємодію продукту стадії е) з 1-(2-хлоретил)-2-імідазолідиноном, або
ж) здійснюють взаємодію 5-хлор-1-(4-фторфеніл)-3-(1,2,3,6-тетрагідропіридин-4-іл)індолу з 1-(2-хлоретил)-2-імідазолідиноном з подальшим відновленням продукту.
Текст
1 Спосіб одержання І\І-(4-фторфеніл)-І\І-(2карбокси-4-хлорфеніл)гліцину, при якому здійснюють каталізоване міддю арилування 2,5дихлорбензойної кислоти за допомогою N-(4фторфеніл)гліцину, в якому використовують солі лужних металів 2,5-дихлорбензойноі кислоти та N(4-фторфеніл)гліцину у водно-лужному реакційному середовищі в присутності мідного каталізатора (31)60/046,011 (32)09 05 1997 (33) US (46) 17 11 2003, Бюл № 1 1 , 2003 р (72) Бек Соммер Мікаел, DK (73) X ЛУННБЕКА/С, DK NHCH 2 CC у ВІДПОВІДНОСТІ зі схемою реакції соон СООМ. 1)Основа/Си/Н2О сн,соон 2)Водний розчин кислоти де М-і і Мг - іони лужних металів 2 Спосіб за п 1, який відрізняється тим, що реакцію здійснюють при підвищеній температурі, переважно при температурі між 80°С і температурою флегми середовища, зокрема близької до температури флегми 3 Спосіб за п 1 або п 2, який відрізняється тим, що реакційне середовище є водою або водою, до якої додано співрозчинник 4 Спосіб за п 3, який відрізняється тим, що як реакційне середовище використовують воду 5 Спосіб за п 3 або п 4, який відрізняється тим, що КІЛЬКІСТЬ води становить менш ніж 10 мл/г 2,5дихлорбензойної кислоти, переважно менш ніж 5 мл/г 6 Спосіб за п 5, який відрізняється тим, що КІЛЬКІСТЬ води менш ніж 3,5 мл/г, переважно менш ніж 2,5 мл/г 2,5-дихлорбензойноі кислоти 7 Спосіб за будь-яким з пп 1-6, який відрізняється тим, що солі лужних металів реагентів є солями ЛІТІЮ, натрію або калію 8 Спосіб за п 7, який відрізняється тим, що використовують однакові солі лужних металів реагентів, переважно солі калію 9 Спосіб за будь-яким з пп 1-8, який відрізняється тим, що основа є карбонатом лужного металу, переважно L12CO3, ІЧагСОз або К2СО3 10 Спосіб за п 9, який відрізняється тим, що лужний метал карбонату лужного металу є тим же, що і лужний метал солей лужного металу реагентів 11 Спосіб за будь-яким з пп 1 - 8, який відрізняється тим, що основа є карбонатом калію 12 Спосіб за будь-яким з пп 1-11, який відрізняється тим, що КІЛЬКІСТЬ основи більше ніж стехіометрична КІЛЬКІСТЬ 2,5-дихлорбензойноі кислоти 13 Спосіб за будь-яким з пп 1-12, який відрізняється тим, що каталізатором є мідь-бронза 14 Спосіб за будь-яким з пп 1-13, який відрізняється тим, що співвідношення кількостей солі лужного металу І\І-(4-фторфеніл)гліцину і солі лужного металу 2,5-дихлорбензойноі кислоти складає від 0,5 до 3,0, переважно від 1,0 до 2,5, зокрема від 2,0 до 2,3 мол/мол 15 Спосіб одержання 5-хлор-1 -(4-фторфеніл)-3(1,2,3,6-тетрапдропіридин-4-іл)індолу, при якому здійснюють реакцію 5-хлор-1-(4-фторфеніл)шдолу з 4-піперидоном у суміші мінеральної кислоти і О Ю О (О 61105 оцтової кислоти 16 Спосіб за п 15, який відрізняється тим, що 4піперидон використовують у формі пдрохлориду 4піперидонпдрату 17 Спосіб за п 15 або п 16, який відрізняється тим, що як мінеральну кислоту використовують фосфорну кислоту, азотну кислоту, сірчану кислоту або соляну кислоту 18 Спосіб за п 17, який відрізняється тим, що як мінеральну кислоту використовують концентровану соляну кислоту 19 Спосіб за п 15 або п 16, який відрізняється тим, що використовують принаймні 1,5 еквівалента 4-піперидону на еквівалент 5-хлор-1-(4фторфеніл)шдолу 20 Спосіб за п 19, який відрізняється тим, що використовують принаймні 1,75 еквівалента 4піперидону на еквівалент 5-хлор-1 -(4фторфеніл)шдолу 21 Спосіб за п 20, який відрізняється тим, що використовують принаймні 2,0 еквівалента 4піперидону на еквівалент 5-хлор-1 -(4фторфеніл)шдолу 22 Спосіб за п 18, який відрізняється тим, що соляну кислоту використовують в КІЛЬКОСТІ принаймні 2,5 мл концентрованої НСІ на грам 5-хлор1-(4-фторфеніл)шдолу 23 Спосіб за п 15 або п 16, який відрізняється тим, що використовують принаймні 8 мл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)шдолу 24 Спосіб за п 23, який відрізняється тим, що використовують принаймні 10 мл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)шдолу 25 Спосіб за п 24, який відрізняється тим, що використовують 10 -14 мл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)шдолу 26 Спосіб за п 22, який відрізняється тим, що співвідношення концентрованої НСІ на грам 5хлор-1-(4-фторфеніл)шдолу складає 3,5 - 5 мл 27 Спосіб за п 18, який відрізняється тим, що співвідношення між оцтовою кислотою та концентрованою НСІ складає від 2 1 до 4 1 (об'єм/об'єм) 28 Спосіб одержання сертиндолу, при якому здійснюють етапи, в яких а) одержують г\І-(4-фторфеніл)-г\І-(2-карбокси-4хлорфеніл)гліцин за будь-яким з пп1-14 шляхом взаємодії солі лужного металу 2,5дихлорбензойної кислоти з сіллю лужного металу І\І-(4-фторфеніл)гліцину у водно-лужному реакційному середовищі в присутності мідного каталізатора, б) проводять циклізацію г\І-(4-фторфеніл)-г\І-(2 Цей винахід відноситься до нового способу одержання сполуки 1 -[2-[4-[5-хлор-1 -(4фторфеніл)-1 -Н-ІНДОЛ-3-ІЛ]-1 -піперидиніл]етил]-2імідазолідинону, яка має рекомендоване INN найменування "сертиндол", і до нового способу одержання проміжних сполук ^(4-фторфеніл)-^(2карбокси-4-хлорфеніл)гліцину та 5-хлор-1-(4фторфеніл)-3-(1,2,3,6-тетрапдропіридин-4іл)шдолу, що використовуються в даному способі Сертиндол є добре відомим антипсихотичним лікарським засобом, що має формулу його активність на моделях, що показує дію цього лікарського засобу при лікуванні неспокою, гіпертензії, зловживання лікарськими засобами і розладів пізнавальної спроможності Нещодавно повідомлялося про те, що цей препарат показав антипсихотичну дію в КЛІНІЧНИХ дослідженнях, Psychopharmacology (1996) 124 168-175 Патент США №4710500 охоплює клас 1-арил3-(піперазиніл-, тетрапдропіридил або піперидил)шдолових сполук, який містить сертиндол Були розкриті деякі загальні способи одержання цих сполук, деякі з яких можна використовувати для одержання сертиндолу Цими способами були a) взаємодія підхожим образом заміщеного 1ариліндолу з підхожим 1 -заміщеним 4піперидоном, і наступне відновлення отриманої тетрапдропіридилової сполуки, b) арилування відповідної сполуки 1заміщеного індолу, c) відновлення ВІДПОВІДНОГО сполуки, що має оксо групу в положенні 2 індольного кільця Сертиндол був підтверджений конкретними прикладами, однак, не були наведені приклади експериментального одержання цієї сполуки Perregaard та ІНШІ, J Med Chem , 1992, NH U . J Y О Сполуку розкрито в патенті США №4710500, а його антипсихотична дія описана в патенті США №5112838 Сертиндол є сильнодіючим антагоністом 5НЇ2 рецептора, що оказує дію на центральну нервову систему in vivo, і крім того була розкрита карбокси-4-хлорфеніл)гліцину до ВІДПОВІДНОГО 3 ацетокемндолу з використанням оцтового ангідриду/ацетату лужного металу, переважно ацетату натрію, в) відновлюють 3-ацетоксмндол і після цього, г) вилучають НгО з одержанням таким чином 5хлор-1-(4-фторфеніл)шдолу, д) здійснюють взаємодію 5-хлор-1-(4фторфеніл)шдолу з 4-піперидоном за будь-яким з пп 15-27 в суміші оцтової кислоти та концентрованої НСІ, є) відновлюють одержаний 5-хлор-1-(4фторфеніл)-3-(1,2,3,6-тетрапдропіридин-4-іл)шдол для одержання 5-хлор-1-(4-фторфеніл)-3(піперидин-4-іл)індолу, є) здійснюють взаємодію продукту стадії є) з 1-(2хлоретил)-2-імідазолідиноном, або ж) здійснюють взаємодію 5-хлор-1-(4-фторфеніл)3-(1,2,3,6-тетрапдропіридин-4-іл)шдолу з 1-(2хлоретил)-2-імідазолідиноном з подальшим відновленням продукту 61105 35,1092-1101 розкрили новий спосіб одержання Однак, було виявлено, що вищенаведені спосертиндолу Цей спосіб включає взаємодію промісоби не можна використати в промисловому вирожної сполуки 5-хлор-1 -(4-фторфеніл)шдолу з 4бництві Загальний вихід продукту в цих способах піперидоном в суміші трифтороцтової кислоти та занадто низький і в них також використовують реаоцтової кислоти, відновлення отриманого 5-хлоргенти або розчинники, що не є підхожими, а в де1-(4-фторфеніл)-3-(1,2,3 6-тетрапдропіридин-4яких випадках заборонені по екологічним причиіл)шдолу для одержання 5-хлор-1-(4-фторфеніл)нам і причинам безпеки Крім того, із-за того, що 3-(піперидин-4-іл)шдолу, що в свою чергу взаємоNMP є водорозчинними, реакція проходить мляво, діє з 1-(2-хлоретил)-2-імідазолідиноном в присута відновлення NMP є тривалим і дорогим ності КагСОз та КІ в метилізобутилкетоні (МІВК) 5Таким чином, цей винахід відноситься до нохлор-1-(4-фторфеніл)шдол одержували з ВІДПОВІДвого способу, який можна використати для промиНОГО 3-ацетокси-індолу шляхом відновлення з вислового одержання сертиндолу користанням NaBbU в метанолі та наступним виБуло виявлено, що основними обмежувальлученням НгО в кислотних умовах 3-ацетоксиними стадіями способу є одержання N-(4індол одержували з г\І-(4-фторфеніл)-І\І-(2фторфеніл)-І\І-(2-карбокси-4-хлорфеніл)гліцину та карбокси-4-хлорфеніл)гліцину, слідуючи процедуреакція 5-хлор-1-(4-фторфеніл)шдолу з 4рам, що описані в літературі піперидоном Процедура одержання г\І-(4-фторфеніл)-І\І-(2Цей винахід відноситься до способу одержанкарбокси-4-хлорфеніл)гліцину описана в ня г\І-(4-фторфеніл)-І\І-(2-карбокси-4Perregaard та ІНШІ, Dansk Кеті, 95, 3, р 6-9 Згідно хлорфеніл)гліцину, який містить взаємодію солі з цим способом гліцин одержують реакцією 2,5лужного металу 2,5-дихлорбензойноі кислоти з дихлорбензойної кислоти та N-(4сіллю лужного металу І\І-(4-фторфеніл)гліцину у фторфеніл)гліцину з використанням мідного катаводно-лужному реакційному середовищі в присутлізатора Солі калію цих двох кислот використовуності мідного каталізатора, з наступною обробкою ють в присутності К2СО3 в розчинникові Nводним розчином кислоти, як показано на наведеметилпірролідоні (NMP) ній нижче схемі реакції NHCM5COOM5 СООМІ де М-і і ІУІ2 - іони лужних металів Як вказано в Perregaard та ІНШІ, Dansk Кеті, 95, реакцію з використанням солей калію вищезазначених реагентів здійснюють в NMP Однак, при використанні NMP необхідна екстракційна обробка, яка займає багато часу, і в результаті реакції утворюється значна КІЛЬКІСТЬ СМОЛИСТИХ побічних продуктів Температура реакції 120-130°С При заміні середовища NMP водним реакційним середовищем при здійсненні реакції одержують більш високий вихід і незначну КІЛЬКІСТЬ СМОЛИСТИХ побічних продуктів Крім того, процедура здійснення способу проста і використання водного 1)Основа/Си/Н2О ^ 2} Водний розчин кислоти NCHjCOOH реакційного середовища дає значні переваги з точки зору захисту навколишньої середовища І, нарешті, температуру реакції знижують до температури флегми водного реакційного середовища або нижче Об'єктом винаходу є також спосіб одержання 5-хлор-1 -(4-фторфеніл)-3-(1,2,3,6тетрапдропіридин-4-іл)індолу, який містить взаємодію 5-хлор-1-(4-фторфеніл)шдолу з 4піперидоном в суміші мінеральної кислоти та оцтової кислоти, як показано на наступній схемі реакції NH.HCI Використання суміші оцтової кислоти і мінеральної кислоти замість суміші трифтороцтова кислота-оцтова кислота, забезпечує значні переваги з точки зору захисту навколишнього середовища Крім того, трифтороцтова кислота є сильно лету чою і агресивною сполукою і, отже, вона небажана для використання в промисловому виробництві При цьому також не утворяться небажані бісзаміщені піперидини 8 61105 вати поступово в ході реакції Каталізатор може бути будь-яким Си(0)каталізатором, переважно це мідно-бронзовий каталізатор Його додають в каталітичних кількостях Конкретна КІЛЬКІСТЬ не має критичного значення і легко визначається фахівцем в даній області Співвідношення між кількостями солі лужного металу І\І-(4-фторфеніл)гліцину і солі лужного металу 2,5-дихлорбензойноі кислоти звичайно складає від 0,5 до 3,0, переважно 1,0-2,5 і найбільш переважно 2,0-2 3 мол/мол Надлишок N-(4фторфеніл)гліцину регенерують Звичайно реакцію здійснюють в мінімально можливій КІЛЬКОСТІ водного реакційного середовища, наскільки це технічно може бути досягнуто Так, поліпшений вихід одержують шляхом знижен Формула І Згідно З ще одним аспеїсгом, об'єісгом винаходу є спосіб одержання сертиндолу, який містить одержання г\І-(4-фторфеніл)-г\І-(2-карбокси-4хлорфеніл)гліцину шляхом взаємодії, яка містить каталітичну реакцію на МІДІ СОЛІ лужного металу 2,5-дихлорбензойноі кислоти з сіллю лужного металу І\І-(4-фторфеніл)гліцину в водно-лужному середовищі в присутності мідного каталізатора та/або в якій 5-хлор-1-(4-фторфеніл)-3-(1,2,3,6тетрапдропіридин-4-іл)індол одержують шляхом взаємодії, що містить реакцію 5-хлор-1-(4фторфеніл)-шдолу з 4-піперидоном в суміші мінеральної кислоти та оцтової кислоти Реакцію солі лужного металу 2,5дихлорбензойної кислоти з сіллю лужного металу І\І-(4-фторфеніл)гліцину здійснюють в умовах підвищеної температури, звичайно в інтервалі від 80°С до температури флегми реакційного середовища, що використовується, переважно при температурі флегми В даному описі та в формулі винаходу термін "водне реакційне середовище" включає воду і воду, в яку додано сорозчинник, такий як етиленгліколь, для використання в якості реакційного середовища Переважно використовують демшералізовану, деюнізовану або дистильовану воду Переважно солі лужних металів реагентів є солями ЛІТІЮ, натрію або калію, і звичайно використовують такі ж солі речовин, які беруть участь в реакції Найбільш переважно використовують солі калію Важливо для запобігання небажаних побічних реакцій, щоб утворена в ході реакції НСІ була нейтралізована Реакційне середовище підлужують шляхом додавання основи, такої як гідроксид лужного металу, ацетат лужного металу, карбонат лужного металу, гідрокарбонат лужного металу, фосфат лужного металу або цитрат лужного металу Переважно використовують карбонат лужного металу, такий як L12CO3, ІЧагСОз або К2СО3 Зручно, коли такий же лужний метал входить до складу речовин, що беруть участь в реакції Переважною основою є карбонат калію КІЛЬКІСТЬ ОСНОВИ переважно більше, ніж стехіометрична КІЛЬКІСТЬ 2,5-дихлорбензойноі кислоти 3 іншого боку, підвищення [ОН ] може викликати гідроліз 2,5дихлорбензойної кислоти, при цьому знижується вихід продукту Таким чином, основу зручно дода ня КІЛЬКОСТІ реакційного середовища КІЛЬКІСТЬ води переважно складає менш ніж 10мл/г 2,5дихлорбензойної кислоти, більш переважно менш ніж 5мл/г, зокрема менш ніж 3,5мл/г, і найбільш переважно менш ніж 2,5мл/г Час реакції не є критичним і його легко визначить фахівець в даній області техніки Обробку продукту розбавленим водним розчином кислоти здійснюють просто додаванням відфільтрованої реакційної суміші до розбавленої кислоти, при цьому продукт осаджується Потім продукт наражають на подальшу очистку гарячим толуолом або шляхом перекристалізації з водного розчину етанолу Розбавленою у воді кислотою переважно є соляна кислота Мінеральною кислотою, що використовується в реакції 5-хлор-1-(4-фторфеніл)шдолу з 4піперидоном, переважно є фосфорна кислота, азотна кислота, сірчана кислота або соляна кислота, наприклад, більш ніж 30% вага/вага водний розчин соляної кислоти, зокрема концентрованої соляної кислоти Під концентрованою соляною кислотою мають на увазі 37% вага/вага розчин НСІ 4-піперидон переважно використовують у вигляді пдрохлориду 4-піперидонпдрату Реакцію переважно проводять в надлишковій КІЛЬКОСТІ пдрохлориду піперидонпдрату Більш переважно використовують більше ніж 1,5 еквіваленту 4-піперидону на еквівалент 5-хлор-1-(4фторфеніл)шдолу, більш переважно використовують більше ніж 1,75 еквіваленту Звичайно використовують 2,0 еквіваленту Для одержання значного виходу продукту важливою умовою є присутність достатньої КІЛЬКОСТІ кислоти Коли в якості мінеральної кислоти використовують соляну кислоту, переважна КІЛЬКІСТЬ складає 2,5мл концентрованої НСІ на грам 5-хлор1-(4-фторфеніл)шдолу Більш переважною є КІЛЬКІСТЬ 3,5-5мл концентрованої НСІ на грам 5-хлор-1(4-фторфеніл)індолу Необхідно, щоб КІЛЬКІСТЬ оцтової кислоти була достатньою, щоб реакція була технічно здійснюваною Звичайно використовують по меншій мірі 8мл оцтової кислоти на грам 5-хлор-1 -(4фторфеніл)шдолу Переважна КІЛЬКІСТЬ оцтової кислоти більше ніж Юмл оцтової кислоти на грам 5-хлор-1-(4-фторфеніл)шдолу, більш переважно 10-14мл Співвідношення оцтової кислоти та концентрованої НСІ переважно складає від 2 1 до 4 1 61105 10 об'єм/об'єм дукту у вигляді дрібнокристалічної речовини жовто-коричневого кольору Суспензію перемішуРеакцію звичайно здійснюють шляхом додавали протягом ЗО хвилин при температурі 75-80°С, вання по каплям розчину 5-хлор-1 -(4охолоджували до 15-20°С і фільтрували, фільтруфторфеніл)шдолу в гарячій оцтовій кислоті до пдвальний осад промивали 500мл води та сушили в рохлориду піперидонпдрату або шляхом змішуструмі повітря при температурі 50°С протягом ночі вання цих двох реагентів у суміші оцтової кислоти і Фільтрат збирали для регенерації N-(4мінеральної кислоти з наступним нагріванням зі фторфеніл)гліцинату зворотним холодильником Час реакції легко визначається фахівцем в даній області техніки Вихід неочищеного продукту 113г (80,3%), Т пл 170-86°С Дані ВЕЖХ 84,2% вага/вага продукПроміжний продукт можна легко обробляти ту, 10,5% вага/вага 3-хлорсаліциловоі кислоти звичайним способом Подальший процес, що приводить до утворення сертиндолу, включає циклі20г зазначеного вище неочищеного сухого зацію г\І-(4-фторфеніл)-І\І-(2-карбокси-4продукту наражали на подальшу очистку шляхом хлорфеніл)гліцину до ВІДПОВІДНОГО 3-ацетоксисуспендування в 200мл толуолу і кип'ятіння зі звоіндолу з використанням, наприклад, оцтового ангіротним холодильником протягом ЗО хвилин Судриду в присутності ацетату лужного металу, такоспензії давали охолонути до кімнатної температуго як ацетат натрію 5-хлор-1-(4-фтор)шдол після ри при перемішуванні та після цього цього одержують із 3-ацетокси-індолу шляхом відфільтрувальний осад промивали толуолом (20мл) новлення з наступним вилученням Ь^О Отримаі сушили у вакуумі протягом ночі при температурі ний 5-хлор-1-(4-фторфеніл)шдол наражають на 50°С взаємодію з 4-піперидоном у ВІДПОВІДНОСТІ З вищеВихід 17,0Г, Т ПЛ 190-92°С Чистота продукту, зазначеною процедурою, отриманий 5-хлор-1-(4яка визначена ЯМР-аналізом, >98% фторфеніл)-3-(1,2,3,6-тетрапдропіридин-4-іл)шдол Приклад 2 відновлюють для одержання 5-хлор-1-(4Одержання г\І-(4-фторфеніл)-г\І-(2фторфеніл)-3-(піперидин-4-іл)шдолу, що, в свою карбоксифеніл)гліцину чергу, взаємодіє з 1 -(2-хлоретил)-2В реактор ємністю 180л додавали 21,0кг 2,5імідазолідиноном з одержанням сертиндолу Альдихлорбензоату калію, після цього додавали 36,0л тернативно, 5-хлор-1 -(4-фторфеніл)-3-(1,2,3 6води Цю суміш нагрівали при перемішуванні до тетрапдропіридин-4-іл)індол спочатку наражають практичних повного розчинення всіх твердих речона взаємодію з 1-(2-хлоретил)-2-імідазолідиноном вин (темп 60-70°С) і поволі додавали 25,0кг N-(4з наступним відновленням, одержуючи при цьому фторфеніл)гліцинату калію Суміш нагрівали до сертиндол, який можна виділити у вигляді кислотповного розчинення всіх речовин, тобто до близьно-адитивної солі, наприклад тартрату, або у вико 80°С і додавали до суміші 7,67кг К2СО3, 582г гляді вільної основи Си-бронза і 7л води Об'єднану суміш КИП'ЯТИЛИ ЗІ Сіль лужного металу 2,5-дихлорбензойноі кислоти та сіль лужного металу N-(4фторфеніл)гліцину, які використовуються в якості вихідних матеріалів, можна легко отримати з комерційно доступних 2,5-дихлорбензойноі кислоти та І\І-(4-фторфеніл)гліцину, ВІДПОВІДНО, З використанням стандартних процедур Отриманий таким способом сертиндол зручно формулюють в композицію, як описано в патенті США №5112838 Експериментальна частина Приклад 1 Одержання г\І-(4-фторфеніл)-І\І-(2карбоксифеніл)гліцину Суспензію, яка містить 2,5-дихлорбензоат калію (100г, 0,44 мол, 1 екв), N-(4фторфеніл)гліцинат калію (190г, 0,92 мол, 2,1 екв ), карбонат калію (36,2г, 0,26 мол, 0,6 екв СОз ), мідно-бронзовий каталізатор (2,8г, 0,04 мол Си, 0,1 екв) і 250мл демінералізованої води, нагрівали до температури кипіння зі зворотним холодильником в атмосфері азоту протягом 20,5 годин і після цього охолоджували до 50°С До реакційної суміші додавали 2,5мл води і 5г активованого вугілля, при цьому реакційна суміш, за винятком Cu-бронзи, була гомогенною Суміші давали охолодитися при перемішуванні протягом 1 години, потім суміш фільтрували Фільтрувальний осад промивали водою 2х125мл Фільтрат виливали на суміш льоду (2л) та 37% водного розчину НСІ (3-400мл) при інтенсивному перемішуванні, що сприяє кристалізації неочищеного про зворотним холодильником протягом ночі (біля 15 годин) і охолоджували до 50°С Додавали 1кг активованого вугілля, суспендованого в 5л води, потім додавали 40л води Суміш перемішували при охолоджуванні протягом 1 години і фільтрували на жолобі, покритому допоміжним фільтруючим матеріалом Фільтрувальний осад промивали 10л води та сирий фільтрат поволі протягом 2 годин виливали на суміш 22,5л 37% НСІ і 30л води при обережному нагріванні (45-50°С) і перемішуванні Суміш нагрівали до 72°С, охолоджували до 25°С і фільтрували Фільтрувальний осад промивали водою (2x10л) і сушили на піддонах протягом ночі при 60°С Вихід неочищеного кристалічного продукту блідо-жовтого кольору складав 26,7кг Неочищений продукт (26,7кг) переносили в реактор ємністю 200л та додавали 150л толуолу і суміш нагрівали до температури флегми (90°С) під шаром азоту Після цього суміш наражали на перегонку до досягнення температури 110°С (5л дистиляту) Додавали 5л толуолу і суміш кип'ятили зі зворотним холодильником при 110°С протягом 2 годин, охолоджували до близько 60°С і залишали на ніч при 27°С Суміш фільтрували і фільтрувальний осад промивали толуолом (3x15л) та сушили, при цьому одержували 21,0кг чистого означеного в заголовку продукту Приклад З 1-(4-фторфеніл)-3-ацетокси-5-хлориндол В тригорлу колбу ємністю 4л, яку обладнано механічним змішувальним приладом і зворотним холодильником, поміщали г\І-(4-фторфеніл)-г\І-(2 12 11 61105 карбоксифеніл)гліцин (717,1г, 2,22 мол), ацетат залишали на ніч для кристалізації Продукт ВІДДІнатрію (36,4г, 0,44 мол, 0,2 екв) і оцтовий ангідЛЯЛИ на жолобі, промивали 7,5л н-гептану і суширид ли у вакуумі протягом ночі при 60°С Суспензію нагрівали при перемішуванні до теВихід 5,39КГ (74,3%), Т ПЛ 146,4°С мператури флегми Суміш кип'ятили зі зворотним Приклад 7 холодильником протягом 1 години і охолоджували Тартрат 1 -[2-[4-[5-хлор-1 -(4-фторфеніл)-1 -Ндо кімнатної температури на бані лід/вода ГомоІНДОЛ-3-ІЛ]-1 -піперидиніл]етил]-2-імідазолідинону генну суспензію при перемішуванні виливали на 1 -[2-[4-[5-хлор-1 -(4-фторфеніл)-1 Н-шдол-3-іл]лід (2л) і нейтралізували концентрованою NaOH 1,2,3,6-тетрапдро-1-піридил]етил]-2-імідазолідинон (приблизно 6л) до досягнення рН 6-7 В процесі (3,5кг) розчинили в оцтовій кислоті (98-100%, 29л) нейтралізації температуру підтримували біля припри нагріванні до 40°С Додавали активоване вублизно 30°С, що вимагало додавання додаткових гілля і суспензію перемішували протягом 1 години, 5-6л льоду При цьому отримували осадження залишали на ніч і відфільтрували Фільтрувальний продукту і продукт виділяли фільтруванням Проосад промивали 6л оцтової кислоти Об'єднані дукт ретельно промивали Зл води та 2л н-гептану фільтрати додавали в реактор гідрогенізації (ємніта сушили у вакуумі протягом ночі при 60°С стю 50л) під шаром азоту Додавали 70г РЮг, реактор закрили та продували азотом протягом 5 хвиВихід 600,5Г (89,1%), Т пл 109-12°С лин Гідрогенізацію здійснювали в потоці Нг (2,5л Приклад 4 за хвилину) протягом 8,25 годин 1 -(4-фторфеніл)-5-хлориндол 1-(4-фторфеніл)-3-ацетокси-5-хлориндол Реакційну суміш продували азотом, додавали (100,0г, 0,33 мол) розчиняли в 1000мл ЕЮН Проактивоване вугілля і суміш фільтрували на закритягом наступної години при КИП'ЯТІННІ ЗІ зворотним тому жолобі Отриманий фільтрат об'єднували з холодильником порціями додавали гранули бороВІДПОВІДНИМИ фільтратами трьох інших циклів гідпдриду натрію (18,7г, 1,5 екв) Реакційну суміш рогенізації (всього 14,53кг вихідного матеріалу) і перемішували протягом ночі при КИП'ЯТІННІ ЗІ звовипарювали у вакуумі при близько 50°С Фільтрат ротним холодильником і охолоджували до кімнатВІДДІЛЯЛИ промиванням 3x10л толуолу при 50ної температури Додавали концентровану НСІ 60°С Речовину, яка залишалася, розчиняли в (приблизно 50мл до досягнення рН 1) і реакційну 146л етанолу і до цієї суспензії при перемішуванні суміш перемішували протягом 1 години при кімнадодавали нагріту до 40°С суспензію І_-(+) винної тній температурі Додавали 200мл демшералізокислоти (5,22кг) в демшералізованій воді (16л) ваної води та отриману суспензію фільтрували Суспензію залишали на ніч без охолоджування Фільтрувальний осад промивали додатковими або перемішування Кристалізований тартрат від50мл води і Юмл ЕЮН Продукт сушили у вакуумі фільтрували на жолобі та промивали 15л етанолу протягом ночі при 50°С Неочищений тартрат перекристалізували з Вихід 68,4Г (84,7%), Т ПЛ 91-93°С Приклад 5 Одержання 5-хлор-1-(4-фторфеніл)-3-(1,2,3,6тетрапдропіридин-4-іл)індолу В реактор ємністю 200л під шаром азоту перенесли 6,70кг 5-хлор-1-(4-фторфеніл)шдолу та 8,38кг пдрохлориду 4-піперидон-монопдрату Додавали оцтову кислоту (67л) і реакційну суміш нагрівали до 60°С Протягом 1/2 години додавали концентровану НСІ (37%, 33,5л) і потім суміш нагрівали до температури флегми (85°С) і кип'ятили зі зворотним холодильником протягом 1 години (кінцева температура 95°С) Після охолоджування до 30°С додавали 33,5л ацетону і потім продовжували охолоджування до 25°С Після фільтрування, промивання (ацетон, 20л) і сушки у вакуумі при 60°С одержували означений в заголовку продукт у вигляді порошку білого кольору з виходом 8,94кг 190л етанолу та 30л демшералізованої води при нагріванні до кипіння (близько 78°С) Суспензію залишали на ніч для кристалізації без охолоджування або перемішування На наступний день суспензію охолоджували до приблизно 18°С і тартрат відфільтровували, промивали 60л етанолу і сушили протягом ночі в потоці повітря при 60°С Приклад 8 1 -[2-[4-[5-хлор-1 -(4-фторфеніл)-1 Н-шдол-3-іл]1-піперидиніл]етил]-2-імідазолідинон 7,96кг тартрату 1-[2-[4-[5-хлор-1-(4фторфеніл)-1Н-шдол-3-іл]-1,2,3,6-тетрапдро-1піридил]етил]-2-імідазолодинона суспендували в 25л демшералізованої води та додавали 30л дихлорметану До суспензії при перемішуванні додавали 27% розчин NaOH, рН = 9 (загальна КІЛЬКІСТЬ Зл) Суміш перемішували протягом 1 години (при збереженні рН=9), після цього дихлорметанову Приклад 6 1 -[2-[4-[5-хлор-1 -(4-фторфеніл)-1 Н-шдол-3-іл]1,2,3,6-тетрапдро-1-піридил]етил]-2-імідазолідинон Змішували 5-хлор-1-(4-фторфеніл)-3-(1,2,3,6тетрапдропіридин-4-іл)індол (6,0кг, 16,5 мол), 1-(2хлоретил)імідазолон (3,19кг, 1,3 екв), карбонат натрію (безводний) та метилізобутилкетон (60л) Реакційну суміш нагрівали до 90-95°С при перемішуванні під шаром азоту і перемішували при цій температурі протягом ночі На наступний день ще гарячу реакційну суміш фільтрували Реактор і фільтрувальний осад промивали додатковими 2,5л метилізобутилкетону Об'єднані фільтрати фазу ВІДДІЛЯЛИ Водну фазу екстрагували додатковими 15л дихлорметану Об'єднані дихлорметанові фази сушили NaSO4 і випарювали Продукт виділяли промиванням 5л ацетону, додавали 35л ацетону і суспензію нагрівали до температури флегми Кристалізований продукт не розчинявся повністю Нагрівання припиняли і суміш залишали на ніч при обережному охолоджуванні Кристалізований продукт ВІДДІЛЯЛИ на жолобі, промивали додатковими 5л ацетону та сушили в потоці повітря протягом ночі при 60°С Вихід 4,90КГ (83,2%), Т ПЛ 154,7°С 13 Комп'ютерна верстка А Крулевський 61105 14 Підписне Тираж 39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюA process of manufacturing sertindole
Назва патенту російськоюСпособ производства сертиндола
МПК / Мітки
МПК: C07D 401/04, C07C 229/58, C07B 61/00, C07D 401/14, C07C 227/00
Мітки: одержання, спосіб, сертіндолу
Код посилання
<a href="https://ua.patents.su/7-61105-sposib-oderzhannya-sertindolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сертиндолу</a>
Попередній патент: Розподільчий матеріал для виробів особистої гігієни, жіноча гігієнічна прокладка, система для виробів особистої гігієни та жіночий гігієнічний виріб (варіанти)
Наступний патент: Шарнірне рейкове з’єднання для рейкових стиків профільних ходових рейок монорейкової підвісної дороги
Випадковий патент: Спосіб і пристрій для отримання електричної енергії на основі використання розсіювання енергії гарматного пострілу











