Застосування тризаміщених бензопіранонів
Номер патенту: 88165
Опубліковано: 25.09.2009
Автори: Гауер Германн, Шец Карл, Кох Еґон, ермер Штефан
Формула / Реферат
1. Застосування сполук загальної формули І
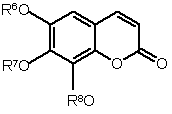 , (I)
, (I)
де радикали R6, R7 та R8 незалежно представляють Н або SO3Н, та їх фізіологічно прийнятних солей для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями.
2. Застосування за п. 1, де радикали R6, R7 та R8 - атоми гідрогену.
3. Застосування за п. 1, де радикали R6 та R8 представляють SO3Н, а радикал R7 - гідроген.
4. Застосування за будь-яким із пп. 1-3, де одна або більше сполук загальної формули І міститься у рослинному екстракті.
5. Застосування за п. 4, де рослинний екстракт є екстрактом із видів пеларгонії.
6. Застосування за п. 5, де рослинний екстракт є екстрактом з Pelargonium sidoides.
7. Застосування за будь-яким із пп. 4-6, де концентрація принаймні одної сполуки загальної формули І у сухому вмісті рослинного екстракту складає 0,1 % - 10 %.
8. Застосування за будь-яким із пп. 4-6, де концентрація принаймні одної сполуки загальної формули І у сухому вмісті рослинного екстракту складає 0,5 % - 5 %.
9. Застосування за будь-яким із пп. 1-8, де патологічний стан вибрано із групи:
цукровий діабет типу І та/або II,
запальні хвороби, що охоплюють ревматоїдний артрит, астму, виразковий коліт, хворобу Крона, псоріаз, нейродерматит,
інфікування бактеріями, вірусами, що охоплюють грип, СНІД, вірусний гепатит, та іншими патогенами, що охоплюють паразитів, грибки та пріони,
атеросклероз та ендотеліальна дисфункція,
ішемія,
неврологічні хвороби, що охоплюють хворобу Альцгеймера, хворобу Паркінсона та інші нейродегенеративні хвороби, або
катаракта та пухлинні хвороби.
10. Сполука загальної формули І
 , (I)
, (I)
де радикали R6, R7 та R8 незалежно представляють Н або SO3Н, та
її фізіологічно прийнятна сіль,
за умови, що R6, R7 та R8 не представляють одночасно Н.
11. Сполуки за п. 10, де
R6 та R8 представляють SO3Н, а R7 - гідроген, або
R6 - SO3Н, а R7 та R8 - гідроген, або
R8 - SO3Н, а R6 та R7 - гідроген.
12. Рослинний екстракт, що містить одну або більше сполук за п. 10 або 11.
13. Рослинний екстракт за п. 12, де рослинний екстракт є екстрактом із видів пеларгонії.
14. Рослинний екстракт за п. 13, де рослинний екстракт е екстрактом з Рelargonium sidoides.
15. Рослинний екстракт за будь-яким із пп. 12-14, де концентрація принаймні одної сполуки(сполук) за пп. 10 або 11 у сухому вмісті рослинного екстракту складає 0,1 % - 10 %.
16. Рослинний екстракт за п. 15, де концентрація принаймні одної сполуки(сполук) за п. 10 або 11 у сухому вмісті рослинного екстракту складає 0,5 % - 5 %.
17. Продукт для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями, який містить принаймні одну сполуку загальної формули І, яку визначено в пп. 1, 2 або 3.
18. Продукт за п. 17, яким є медикамент.
19. Продукт за п. 17, яким є дієтичний харчувальний продукт.
20. Фармацевтичний препарат, що складається принаймні з одної сполуки загальної формули І, яку визначено в пп. 1, 2 або 3, та придатних ад'ювантів, як форма для перорального застосування.
21. Фармацевтичний препарат, що містить рослинний екстракт за будь-яким із пп. 12-16 та придатні ад'юванти, як форма для перорального застосування.
Текст
1. Застосування сполук загальної формули І 2 3 88165 4 19. Продукт за п.17, яким є дієтичний харчувальний продукт. 20. Фармацевтичний препарат, що складається принаймні з одної сполуки загальної формули І, яку визначено в пп.1, 2 або 3, та придатних ад'ювантів, як форма для перорального застосування. 21. Фармацевтичний препарат, що містить рослинний екстракт за будь-яким із пп.12-16 та придатні ад'юванти, як форма для перорального застосування. Заявлений винахід стосується застосування тризаміщених бензопіранонів для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями, та нових тризаміщених бензопіранонів та їхніх фізіологічно прийнятних солей. Заявлений винахід, крім того, стосується рослинних екстрактів, медикаментів, продуктів дієтичного харчування та фармацевтичних препаратів. Вільні радикали - атоми або молекули, які мають неспарений електрон на їх зовнішній орбіталі. Для біологічних процесів найважливішими вільними радикалами є молекулярний кисень, здатний при відновленні утворювати різноманітні метаболіти. Ці метаболіти, звичайно, узагальнюють під сукупним терміном "активні види кисню" (АВК). Приклади АВК охоплюють супероксид-аніон, гідроксильний радикал, гідроген пероксид, пероксид-аніон, синглетний кисень, гіпохлорид, оксид нітрогену та пероксонітрит. АВК спонтанно утворюються в різних біологічних процесах. Особливо важливим є так званий "респіраторний розрив" лейкоцитів, де після стимулювання клітин мікроорганізмами, ксенобіотиками або ендогенними субстанціями утворюються супероксид-радикал та інші АВК як продукти реакції активування молекулярного кисню мембранною NADPH-оксидазою. Респіраторний розрив є одним із найважливіших механізмів раннього неспецифічного імунного захисту та переважно служить для знищення інфекційних збудників та новоутворених клітин. Крім того, АВК переважно генеруються втратою електронів у результаті недостатньо спряжених реакцій. Це відбувається, наприклад, у синтезі простагландинів та лейкотриєнів з арахідонової кислоти, протягом мітохондріального дихання, каталізованим ксантиноксидазою окисненням гіпоксантину в ішемічних станах або у процесі опосередкованої цитохромом Р450 метаболізації ксенобіотиків. Оскільки респіраторний розрив по суті є реакцією, потрібною для захисту від інфекцій, збільшене та безперервне утворення АВК, звичайно, є шкідливим тому, що окислювальна атака не є обмеженою щодо вторгнення мікроорганізмів, але також власна тканина організму піддається їх токсичному потенціалу. Це, зокрема, призводить до неінфекційних хвороб, як-то збільшення утворення АВК у процесі автоімунної хвороби, при дегенеративних хворобах, протягом ішемії або при метаболізації фармацевтичних засобів. Небажана дія вільних радикалів та АВК базується на їхній взаємодії з нуклеїновими кислотами (наприклад, індукуванні розривів молекулярного ланцюгу ДНК), білками (наприклад, денатурації, інактивації системи ферментів), вуглеводами (наприклад, деполімеризації гіалуронових кислот) та, зокрема, ліпідів (наприклад, перокисненні ліпіду, пошкодженні мембран, утворенні прозапальних простагландинів та лейкотриєнів). Після припущення приблизно 50 років тому, що активні види кисню (АВК) залучені у патогенез різних хвороб, тепер упевнено вважають, що ці молекули грають важливу роль у патогенезі численних хвороб, як-то цукрового діабету типу І та II, запальних хвороб (наприклад, ревматоїдного артриту, астми, виразкового коліту, псоріазу), бактеріальних та вірусних інфекцій (наприклад, грипу, СНІД'у, вірусного гепатиту), атеросклерозу, ішемії, неврологічних хвороб (наприклад, хвороби Альцгеймера, хвороби Паркінсона та інших нейродегенеративних хвороб), катаракти, серпоподібної клітинної анемії та пухлинних хвороб, крім того, вони також є несуть спільну відповідність за процеси старіння (A. Bendich (1994) у: В. Frei (ed.) "Natural Antioxidants in Human Health and Disease", Academic Press, San Diego, p. 447; E. Peterhans (1997) J. Nutr. 127, 962 S; D. V. Parke (1999) y: T. K. Basu et al. (ed.) "Natural Antioxidants in Human Health ", CAB International, p. 1). Організм має різні системи захисту проти шкідливої дії вільних радикалів та АВК. Вони охоплюють вітаміни (наприклад, вітаміни Е та С) та інші низькомолекулярні сполуки (наприклад, глутатіони, сечову кислоту), антиокиснювальні ферменти (наприклад, супероксиддисмутазу, каталазу та глутатіонпероксидазу), а також метал-зв'язувальні білки (наприклад, трансферин, церулоплазмін). Однак, власні антиокиснювальні системи організму часто є активними тільки протягом вихідної фази патологічного процесу тому, що збільшення концентрації АВК, яку утворено при розвитку патологічного процесу, набагато перевершує здатність механізмів ендогенного захисту. Тому вважають, що окиснювальний стрес створює диспропорцію між концентрацією АВК та системами антиокиснювального захисту. Таким чином, завдяки особливій важливості АВК відносно численних хвороб існує надзвичайна зацікавленість у субстанціях, що мають антиокиснювальні властивості, які можна застосовувати в профілактиці та лікуванні таких патологічних станів. Оскільки АВК є особливо важливими для запальних реакцій, а окиснювальний стрес часто супроводжується збільшеним синтезом прозапальних ейкозаноїдів (наприклад, прстагландинів, лейкотриєнів) та цитокінів (наприклад, IL-1, TNF-α, IL-6), зокрема, існує потреба в субстанціях, які ви 5 являють антиокиснювальні властивості та, крім того, також попереджують утворення цих медіаторів запалення. Заявлений винахід стосується сполук для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями. Ця проблема вирішується застосуванням сполук загальної формули І, де радикали R6, R7 та R8 незалежно представляють Н або SO3H, та їх фізіологічно прийнятних солей для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями. Несподівано виявлено, що 6,7,8-тригідрокси2Н-1-бензопіран-2-он (сполука II), зокрема, виявляє переважні фармакологічні властивості. На додаток до потужної антиокиснювальної дії ця сполука також інгібує синтез лейкотриєнів та прстагландинів, а також синтез прозапальних цитокінів IL-ip, TNF-α та IL-6. Таким чином, сполука II є по суті придатною для лікування або профілактики хвороб, супроводжуваних окиснювальним стресом, як-то цукрового діабету типу І та/або II, атеросклерозу та ендотеліальної дисфункції, ішемії, неврологічних хвороб (наприклад, хвороби Альцгеймера, хвороби Паркінсона та інших нейродегенеративних хвороб), катаракти та пухлинних хвороб. Однак, сполука II, зокрема, є переважною для патологічних хвороб, що мають запальну компоненту, як-то ревматоїдного артриту, астми, виразкового коліту, хвороби Крона, псоріазу, нейродерматиту та інфікування бактеріями, вірусами (наприклад, грипу, СНІД'у, вірусного гепатиту) та іншими патогенами (наприклад, паразитами, грибком та пріонами). Сполуку II вже описано у літературі (О.Kayser та Н.Kolodziej, Phytochemistry 39, 1181-1185 (1995); S.Kumar, А.В.Ray, С.Konno, Y.Oshima та H.Hikino, Phytochemistry 27, 636-638 (1988); K.P.Latte, O.Kayser, N.Tan, M.Kaloga та H.Kolodziej, Z.Naturforsch. 55c, 528-533 (2000)), однак, фармакологічна дія сполуки II дотепер невідома. Сполука II міститься у Pelargonium sidoides тільки у концентрації 0,0004 % (Kayser et al.; Latte et al., зістав з вищезазначеним) та у Pelargonium reniforme тільки у концентрації 0,02% (Latte et al., зістав з вищезазначеним). З того можна зробити висновок, що сполука II, відповідно, у цих низьких концентраціях не забезпечує значний внесок у біологічну ефективність Pelargonium sidoides та reniforme. Тому заявлений винахід полягає в застосуванні сполуки II для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями. Також можна застосовувати сполуку II у формі етерів сульфатної кислоти загальної формули І внаслідок виділення сполуки II із цієї сполуки після 88165 6 перорального застосування. Тому сполуки загальної формули І також є придатними для лікування або профілактики вищезгаданих патологічних станів. Переважними сполуками загальної формули І є 6,7-дигідрокси-8-сульфокси-2Н-1-бензопіран-2-он (R6=R7=Н; R8=SO3H) та 7,8-дигідрокси-6сульфокси-2Н-1-бензопіран-2-он (R7=R8 Н; = 6 R =SO3H). Особливо переважним є 6,8біс(сульфокси)-7-гідрокси-2Н-1-бензопіран-2-он (R6=R8=SO3H; R7=Н ; сполука III). Сполуки загальної формули І, де принаймні один із радикалів R6, R7 або R8 представляє SO3H, є новими. Тому, ці сполуки, та, зокрема, сполука III, a також їх застосування для лікування або профілактики патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями, також є частиною заявленого винаходу. У загальній формулі І радикали R6, R7 та R8 незалежно представляють атом гідрогену або SO3H. Сполуки загальної формули І, а також сполуки II та III також можуть бути у формі їх фізіологічно прийнятних солей лужного металу, лужноземельного металу та інших, наприклад, солей калію. Ці солі також є предметом заявленого винаходу. Крім того, рослинні екстракти, зокрема, з видів пеларгонії, що містять одну або більше сполук загальної формули І, де принаймні один із залишків R6, R7 та R8 є SO3H, та отримані з них фармацевтичні препарати, складають частину заявленого винаходу. Таким чином, ці екстракти, що мають концентрацію принаймні одної сполуки загальної формули І у складі сухої речовини рослинного екстракту 0,1%-10%, є переважними разом із тими, що мають концентрацію 0,5%-5%, які є особливо переважними. Склад сухої речовини відповідає сухому залишку згідно з Ph. Eur. (рідинних екстрактів), де аналіз також можна робити безпосередньо, наприклад, у рідинному екстракті та сухому залишку може бути визначеним розрахунком. Отримання сполуки II можна здійснювати гідролізом та/або розщепленням етеру, наприклад, комерційно доступного фраксину або сполуки загальної формули І, де принаймні один із радикалів R6, R7 та R8 представляє SO3H. Отримання сполуки загальної формули І де принаймні один із радикалів R6, R7 та R8 представляє SO3H, можна здійснювати реакцією сполуки II із комплексом сульфур триоксид-триметиламін, або у разі сполуки III - виділенням із придатного 7 рослинного матеріалу, наприклад, із сухих корінців Pelargonium sidoides. Сполуки 6,7-дигідрокси-8сульфокси-2Н-1-бензопіран-2-он (загальна формула І; R6=R7=Н; R8=SO3H) та 7,8-дигідрокси-6сульфокси-2Н-1-бензопіран-2-он (загальна формула І; R7=R8=Н; R6=SO3H) можна також отримувати частковим гідролізом сполуки III. Згідно із заявленим винаходом екстракти можна отримувати зі змінним складом із рослин пеларгонії або їхніх частин відомими способами отримання, застосовуючи розчинники як-то воду, метанол, етанол, ацетон, тощо, та їх суміші при температурах від кімнатної температури до 60°С при перемішуванні від слабкого до енергійного, або перколяцією від 10 хвилин до 24 годин. Переважними екстракційними розчинниками є вода або суміші етанолу та води з відсотком води принаймні 50мас.%, особливо переважно - у співвідношенні етанол/вода 10/90-15/85 (масова частка). Згідно із заявленим винаходом подальші концентрати сполуки загальної формули І можна отримувати, як-то розподіленням у шарах рідина-рідина, застосовуючи, наприклад, 1-бутанол/воду або етилацетат/воду, адсорбцію-десорбцію, застосовуючи іонообмінники LH20, НР20 та інші смоли, або хроматографічне розділення, застосовуючи RP18, силікагель тощо. Якщо потрібно, подальшу обробку для отримання сухих екстрактів по суті роблять відомими способами видалення розчиннику при збільшеній температурі та/або зменшеному тиску, або сушкою сублімацією. Згідно з Європейською Фармакопеєю сухі екстракти, звичайно, мають сухий залишок принаймні 95мас.%. Згідно із заявленим винаходом сполуки загальної формули І та екстракти, що містять принаймні одну із цих сполук, відповідно, переважно можна застосувати перорально у формі порошків, гранул, таблеток, драже, капсул, або як розчин. Дозування є ефективним при застосуванні 0,1мг-250мг на добу, переважно 0,3мг-50мг на добу одної або більше сполук загальної формули І. Для отримання таблеток принаймні одну сполуку загальної формули І або відповідний екстракт змішують із придатними фармацевтично прийнятними ад'ювантами, як-то лактозою, целюлозою, діоксидом силіцію, кроскармелозою та магній стеаратом та пресують у таблетки, котрі, як варіант, забезпечені придатним покриттям, наприклад, зробленим із гідроксиметилпропілцелюлози, поліетиленгліколю, барвниками (наприклад, титан оксидом, ферум оксидом) та тальком. У випадку патологічних станів, асоційованих з окиснювальним стресом та/або запальними реакціями, ефективність сполуки II підтверджується наступними описаними експериментами. Антиокиснювальні властивості: Автоокиснення ліпідів асоційовано з випромінюванням світла. Визначення цієї надзвичайно слабкої хемілюмінесценції можна застосовувати для визначення пероксидів та розрахунку ефективності оксидантів. У цих дослідженнях використовували тканину мозку самців мишей (NMRI; 20-30г; Centre d'Elevage Janvier, Le Genest-Saint Isle, France) як багату ліпідами тканину. Після видалення мозок промивали холодним льодяним бу 88165 8 ферованим фосфатом фізіологічним розчином (БФФР, рН=7,4) та звільняли від мозкових оболонок та залишкової крові. Зразки тканин гомогенізували 4-кратним об'ємом (об'єм до маси) БФФР, та центрифугували при 1000´g, 4°С протягом 10 хвилин. Надосадкові рідини одразу розбавляли тим самим буфером до 3-кратного об'єму та зберігали на льоду. 250мкл розбавленого надосадкової рідини переносили в тест-пробірку та інкубували протягом 10 хвилин при 37°С у 6-канальному люменометрі (Multi-Biolumat LB 9505 С, Berthold, Bad Wildbad). Після додавання 25мкл сполуки II у БФФР із 2,5% ДМСО інкубацію продовжували протягом подальших 10 хвилин Тоді визначали інтенсивність хемілюмінесценції (CL) протягом 60 хвилин. Відсоток інгібування автоокиснення розраховували у порівнянні з виміряним одночасно контрольним розчинником (БФФР з 2,5% ДМСО). Сполука II інгібує автоокиснення ліпідів із чудовою потужністю при концентрації напівмаксимального інгібування 53нг/мл (Фіг.1). На відміну від тролоксу, часто застосовуваного як еталонна речовина у визначеннях антиокиснювальної властивості, котрий показував концентрацію напівмаксимального інгібування тільки 1665нг/мл. На Фіг. показано вплив сполуки II та тролоксу на автоокиснення ліпідів. Для трьох незалежних тестів установлено відсоток інгібування пероксидування ліпіду порівняно з контролем розчинником (середнє значення ± СВ). Інгібування синтезу прозапальних цитокінів: Вплив сполуки II на синтез прозапальних цитокінів IL-β, TNF-α та IL-6 визначали застосуванням активованих перитонеальних макрофагів мишей. Для отримання активованих макрофагів інтраперитонеально вводили в самців мишей NMRI (Centre d'Elevage Janvier, Le Genest-Saint Isle, France) 3´109 вбитих бактерій coryn bacterium parvum (Changzhou Yanshen Co. Ltd., Changzhou, China) у 0,5мл БФФР. Через 6 діб черевну порожнину промивали 2,5мл збалансованого фізіологічного розчину Хенкса (ЗФРХ), вільного від кальцію та магнію, що додавали з 10 одиниця/мл гепарину. Клітини ресуспендували при концентрації 2´106 клітин/мл у повному середовищі RPMI, доповненому 10% сироваткою зародка теляти. У комірки 96-коміркових мікротитрувальних планшетів уводили відповідно 200мкмоль суспензії клітин. Після 2 годинного періоду інкубації видаляли клітини, що не прилипли, та клітинний газон, що залишився, промивали двічі культиваційним середовищем (37°С). Макрофаги преінкубували протягом 30 хвилин зі сполукою II, а тоді індукували синтез прозапальних цитокінів додаванням 1мкг/мл ліпополісахариду Е. соli (серотип 0127:В8, Sigma, Deisenhofen). Після інкубації протягом 24 годин (37°С, 5% СО2 у повітрі) клітини руйнували заморожуванням та таненням протягом 3 разів, клітини надосадкових шарів виділяли та заморожували при -80°С до аналізу. Визначення концентрації цитокіну у надосадковому шарі клітин виконували за допомогою комерційних тест-комплектів (Duosets IL-1b, TNF-α та IL-6, R&D, Wiesbaden) у відповідності із інструкціями виробника. Усі дослідження проводили 3 рази. Вплив сполуки II на си 9 88165 нтез цитокінів оцінювали у порівнянні з контролем розчинником (0,1% ДМСО у повному середовищі RPMI), що тестували одночасно. Як можна бачити нижче з таблиці 1, сполука II при концентрації 10 100мкг/мл давала значне інгібування синтезу всіх трьох вимірюваних цитокінів із дією на продукування IL-6, що відзначалася як найміцніша. Таблиця 1 Вплив сполуки II на синтез прозапальних цитокінів у активованих перитонеальних макрофагах миші. Показано середнє значення ±СВ трьох паралельних тестів. Дію сполуки II розраховували як відсоток зміни у порівнянні з контролем розчинником Тест Контроль Сполука II 100 мкг/мл Сполука II 30мкг/мл Сполука II 10 м кг/мл IL-β пг/мл 3553±293 430±65 3356±87 3789±72 Дія(%) -88* -6 +7 TNF-a пг/мл Дія (%) 8393±923 6251±7 -26* 10189±1018 +21 10050±462 +19 IL-6 пг/мл 31449±2201 976±244 22519±3153 23078±3461 Дія(%) -97* -28* -27* *можлива похибка Р
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of trisubstituted benzopyranones
Автори англійськоюGermer Stefan, Hauer Hermann, Koch Egon, Schoetz Karl
Назва патенту російськоюПрименение трехзамещенных бензопиранонов
Автори російськоюГермер Штефан, Гауэр Германн, Кох Эгон, Шец Карл
МПК / Мітки
МПК: C07D 311/10
Мітки: застосування, тризаміщених, бензопіранонів
Код посилання
<a href="https://ua.patents.su/7-88165-zastosuvannya-trizamishhenikh-benzopiranoniv.html" target="_blank" rel="follow" title="База патентів України">Застосування тризаміщених бензопіранонів</a>
Попередній патент: Спосіб обробки поверхні скла металевим алюмінієм, його застосування та скло, отримане цим способом
Наступний патент: Застосування пептидних сполук для лікування есенційного тремтіння та інших синдромів тремтіння
Випадковий патент: Автомобільний газогенератор поперечного процесу газифікації з регульованою потужністю











