Спосіб комбінованої терапії для лікування проліферативних захворювань
Формула / Реферат
1. Спосіб лікування проліферативного захворювання у індивідуума, який включає в себе введення індивідууму композиції, що містить наночастинки, які містять паклітаксел і альбумін, причому композиція повинна вводитися з ефективною кількістю щонайменше одного іншого засобу, вибраного з децитабіну і азацитидину, причому азацитидин придатний для орального введення.
2. Спосіб за п. 1, в якому іншим засобом є азацитидин.
3. Спосіб за п. 1, в якому іншим засобом є децитабін.
4. Спосіб за будь-яким з пп. 1-3, в якому проліферативним захворюванням є злоякісна пухлина.
5. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак молочної залози.
6. Спосіб за п. 5, в якому індивідуум є негативним відносно ER, PR або HER2.
7. Спосіб за п. 4, в якому індивідуум є негативним відносно ER, PR і HER2.
8. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак яєчника.
9. Спосіб за п. 4, в якому злоякісна пухлина являє собою недрібноклітинний рак легень.
10. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак ендометрія.
11. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак шийки матки.
12. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак підшлункової залози.
13. Спосіб за п. 4, в якому злоякісна пухлина являє собою меланому.
14. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак сечового міхура.
15. Спосіб за п. 4, в якому злоякісна пухлина являє собою рак голови та шиї.
16. Спосіб за будь-яким з пп. 1-3, в якому композицію, що містить наночастинки, які містять паклітаксел і альбумін, і інший засіб вводять спільно.
17. Спосіб за будь-яким з пп. 1-3, в якому композицію, що містить наночастинки, які містять паклітаксел і альбумін, і інший засіб вводять послідовно.
18. Спосіб за будь-яким з пп. 1-3, в якому композицію, що містить наночастинки, що містять паклітаксел і альбумін, і інший засіб вводять одночасно.
19. Спосіб за будь-яким з пп. 1-3, в якому середній діаметр наночастинок в композиції складає не більше ніж приблизно 200 нм.
20. Спосіб за п. 19, в якому альбумін являє собою сироватковий альбумін людини.
21. Спосіб за п. 19, в якому альбумін являє собою альбумін людини.
22. Спосіб за п. 19, в якому співвідношення по масі альбуміну і паклітакселу в композиції на основі наночастинок менше ніж приблизно від 1:1 до приблизно18:1.
23. Спосіб за п. 19, в якому співвідношення по масі альбуміну і паклітакселу в композиції на основі наночастинок менше ніж приблизно від 1:1 до приблизно 9:1.
24. Спосіб за будь-яким з пп. 1-3, в якому індивідуумом є людина.
25. Спосіб за будь-яким з пп. 1-3, в якому наночастинки в композиції вводять внутрішньовенно.
26. Спосіб за п. 25, в якому кількість паклітакселу в композиції становить від 80 мг/м2 до близько 150 мг/м2.
27. Спосіб за п. 26, в якому кількість паклітакселу в композиції становить від 100 мг/м2 до близько 125 мг/м2.
28. Спосіб за будь-яким з пп. 1-3, в якому інший засіб у композиції вводять перорально.
29. Спосіб за п. 28, в якому ефективна кількість іншого засобу в композиції становить від близько 80 мг до близько 1000 мг.
30. Спосіб за п. 29, в якому ефективна кількість іншого засобу в композиції становить від близько 100 мг до близько 200 мг.
31. Набір для лікування проліферативного захворювання у індивідуума, що включає в себе:
a) композицію, що містить наночастинки, які містять паклітаксел і альбумін, і
b) ефективну кількість щонайменше одного іншого засобу, що вибраний з децитабину і азацитидину, причому азацитидин придатний для орального введення.
32. Набір за п. 31, в якому іншим засобом є азацитидин.
33. Набір за п. 31, в якому іншим засобом є децитабін.
34. Набір за будь-яким з пп. 31-33, в якому середній діаметр наночастинок в композиції становить не більше ніж приблизно 200 нм.
35. Набір за п. 34, в якому альбумін являє собою людський сироватковий альбумін.
36. Набір за п. 34, в якому альбумін являє собою людський альбумін.
37. Набір за будь-яким з пп. 31-33, в якому інший засіб в композиції придатний для перорального введення.
Текст
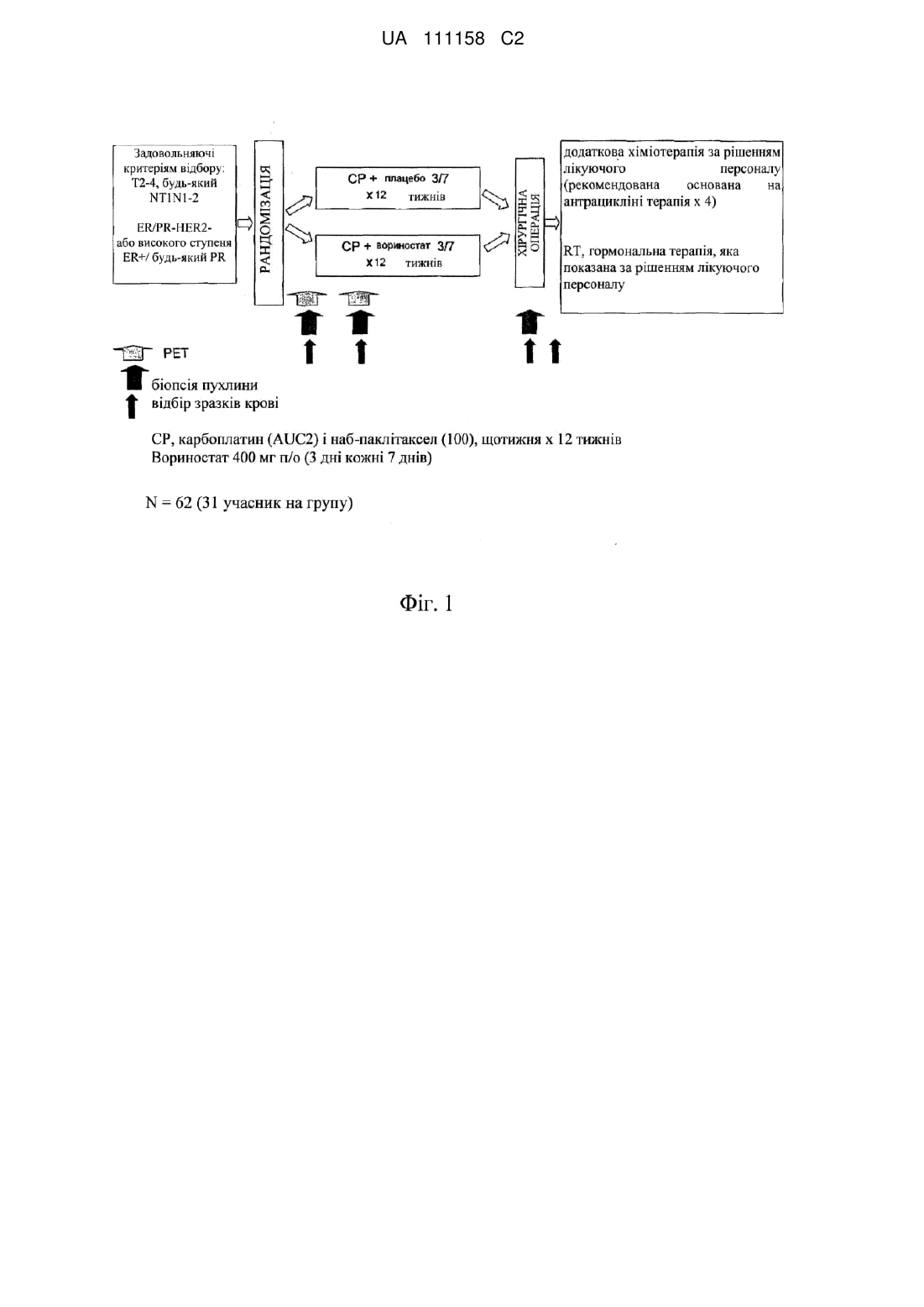
Реферат: Винахід стосується способу комбінованої терапії для лікування проліферативного захворювання, що включає введення індивідууму композиції, що містить наночастинки, які містять паклітаксел і альбумін, та ефективної кількості щонайменше одного іншого засобу, вибраного з децитабіну і азацитидину, причому азацитидин придатний для орального введення. UA 111158 C2 (12) UA 111158 C2 UA 111158 C2 5 10 15 20 25 30 35 40 45 50 55 60 ПЕРЕХРЕСНЕ ПОСИЛАННЯ НА СПОРІДНЕНІ ЗАЯВКИ Дана заявка заявляє перевагу пріоритету на основі попередніх заявок на видачу патенту № 61/352333, поданої 7 червня 2010 р., і № 61/446909, поданої 25 лютого 2011 р., зміст кожної з яких включений в даний опис у вигляді посилання в повному об'ємі. ГАЛУЗЬ ТЕХНІКИ, ДО ЯКОЇ НАЛЕЖИТЬ ВИНАХІД Даний винахід стосується способів і композицій для лікування проліферативних захворювань, які включають в себе введення комбінації таксану і щонайменше одного іншого терапевтичного засобу, застосовного для лікування проліферативних захворювань. РІВЕНЬ ТЕХНІКИ Злоякісна пухлина є лідируючою причиною смертності у всьому світі. Незважаючи на значні успіхи в галузі хіміотерапії, багато які з найбільш поширених форм злоякісної пухлини все ще резистентні до хіміотерапевтичного втручання. Рак молочної залози є найбільш поширеною формою злоякісної пухлини у жінок. Судячи за оцінками, в 2009 році очікується діагностування 192370 нових випадків інвазивного раку молочної залози у жінок в США, нарівні з 62280 новими випадками неінвазивного (in situ) раку молочної залози. Передбачається, що приблизно 40170 жінок помруть в 2009 році від раку молочної залози. Тричі негативний рак молочної залози є підтипом раку молочної залози, який є клінічно негативним відносно експресії рецептора естрогену (ER), рецепторів прогестерону (PR) і білка HER2. Оскільки тричі негативні злоякісні клітини молочної залози не експресують жоден з вказаних рецепторів, вони звичайно не реагують на стандартні опосередковані рецепторами обробки. У цей час хіміотерапія є найбільш ефективним лікуванням пацієнтів з тричі негативним раком молочної залози. Однак багато які пацієнти продовжать страждати від рецидивів і вмирають, незважаючи на інвазивну терапію, що підкреслює необхідність в нових терапевтичних методиках. Епігенетичні зміни в геномі вносять внесок в ініціацію і прогресування злоякісної пухлини. Наприклад, гіпоацетилування гістонів і аномальне метилування ДНК в промоторних областях важливих генів може приводити до сайленсингу генів. Множина генів є метилованими і, отже такими, що мовчать в злоякісній пухлині молочної залози. Pu RT. Mod. Path., 2003. Були досліджені функції епігенетичних модифікаторів при лікуванні різних злоякісних пухлин. Cooper et al., Gynecol. Oncol. 2007, 104(3):596-601;Ramalingam et al., J. Clin. Oncology, 2006 ASCO Annual Meeting Proceedings, Part I., Vol. 24 (18S); і Kim MS, Cancer Res 2003. Було показано, що таксани (такі як паклітаксел і доцетаксел) надають значну антинеопластичну і протиракову дію на широке коло злоякісних пухлин. Наприклад, паклітаксел діє, перешкоджаючи нормальній функції руйнування мікротрубочок. Паклітаксел зв'язується з бета-субодиницею тубуліну, будівельними блоками мікротрубочок, викликаючи гіперстабілізацію структур мікротрубочок. Отримана в результаті структура паклітаксел/мікротрубочки нездатна до розбирання, приводячи тим самим до затримки мітозу і інгібуючи ангіогенез. Однак погана розчинність таксанів у воді являє собою значну проблему для розробки ефективних, основаних на таксанах, терапевтичних засобів проти злоякісних пухлин. Крім того, взаємодія різних препаратів таксанів з іншими терапевтичними засобами в контексті комбінованої терапії ще необхідно дослідити. Композиції, що містять наночастинки на основі альбуміну, були розроблені як система доставки для того, щоб доставляти по суті не розчинні у воді лікарські засоби, такі як таксани. Див., наприклад, патенти США № 5916596, 6506405, 6749868 і 6537579 і 7820788, а також публікації патентів США № 2007/0082838. У методиці застосування наночастинок на основі альбуміну використовують природні властивості білка альбуміну транспортувати і доставляти по суті не розчинні у воді лікарські засоби в місце, уражене захворюванням. Такі наночастинки легко включаються у власні процеси транспорту в організмі, і здатні використовувати залучення пухлинами альбуміну, забезпечуючи можливість доставки більш високих концентрацій активного лікарського засобу, інкапсульованого в наночастинках, до ділянки-мішені. Крім того, методика використання основаних на альбуміні наночастинок надає можливість підвищити розчинність лікарського засобу, уникаючи необхідності в застосуванні токсичних хімічних речовин, таких як розчинники, в процесі введення, таким чином потенційно підвищуючи безпеку за рахунок виключення пов'язаних з розчинниками побічних ефектів. Інші публікації включають заявки PCT № WO08/057562, WO2009126938A1, WO2009126401A1, WO2009126175A1. Описи всіх публікацій, патентів, заявок на видачу патенту і опублікованих заявок на видачу патенту, що згадуються в даному описі, включені при цьому в дану публікацію шляхом посилання в повному об'ємі. 1 UA 111158 C2 5 10 15 20 25 30 35 40 45 50 55 60 СУТЬ ВИНАХОДУ Винахід стосується способів комбінованої терапії для лікування проліферативного захворювання (такого як злоякісна пухлина), що включають в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять таксан (такий як паклітаксел) і білок-носій (такий як альбумін), і b) ефективної кількості щонайменше одного іншого засобу, який модифікує епігенетику в клітині (який також називається в даному описі «епігенетичним модифікатором» або «іншим засобом»). У деяких варіантах винахід стосується способу лікування проліферативного захворювання (такого як злоякісна пухлина) у індивідуума, що включає в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять паклітаксел, покритий альбуміном (такий як абраксан® або «набпаклітаксел»), і b) ефективної кількості щонайменше одного іншого засобу, який модифікує епігенетику в клітині. У деяких варіантах інший засіб модифікує (наприклад, інгібує) метилування ДНК. У деяких варіантах інший засіб модифікує модифікацію гістонів, яка включає без обмеження ацетилування гістонів, метилування гістонів, сумоїлування гістонів і фосфорилування гістонів. У деяких варіантах інший засіб є інгібітором ДНК-метилтрансферази (таким як азацитидин). У деяких варіантах інший засіб є інгібітором ДНК-метилтрансферази (таким як децитабін). У деяких варіантах іншим засобом є інгібітор деацетилази гістонів (такий як вориностат). У деяких варіантах проліферативне захворювання є резистентним або рефрактерним до лікування таксаном при його введенні окремо або в сполученні з іншим засобом, відмінним від епігенетичного модифікатора. У деяких варіантах проліферативне захворювання є резистентним або рефрактерним до лікування, коли епігенетичний модифікатор вводять окремо або в сполученні з іншим засобом, відмінним від композиції, що містить наночастинки (такої як композиція таксану, яка не містить наночастинок, включаючи паклітаксел). У деяких варіантах композицію, що містить наночастинки (яка також називається «композицією на основі наночастинок») і інший засіб вводять одночасно, або в одній і тій же композиції, або у вигляді окремих композицій. У деяких варіантах композиція на основі наночастинок і інший засіб вводять послідовно, тобто, композицію на основі наночастинок вводять або до, або після введення іншого засобу. У деяких варіантах введення композиції на основі наночастинок і іншого засобу здійснюють одночасно, тобто, період введення композиції на основі наночастинок і період введення іншого засобу перекриваються один з одним. У деяких варіантах композицію на основі наночастинок вводять протягом щонайменше одного циклу (наприклад щонайменше протягом будь-якої кількості 2, 3 або 4 циклів) перед введенням іншого засобу. У деяких варіантах інший засіб вводять протягом щонайменше одного, двох, трьох або чотирьох тижнів після припинення введення композиції на основі наночастинок. У деяких варіантах композицію на основі наночастинок і епігенетичний модифікатор вводять протягом одних і тих же циклів лікування. У деяких варіантах введення композиції на основі наночастинок і іншого засобу здійснюють не одночасно. Наприклад, в деяких варіантах введення композиції на основі наночастинок припиняють перед введенням іншого засобу. У деяких варіантах введення іншого засобу припиняють перед введенням композиції на основі наночастинок. У деяких варіантах інший засіб являє собою інгібітор деацетилази гістонів, включаючи без обмеження вориностат, ромідепсин, панобіностат, беліностат і ентиностат. У деяких варіантах інший засіб являє собою інгібітор ДНК-метилтрансферази, включаючи без обмеження 5азацитидин (азацитидин або відаза), 5-аза-2'-дезоксицитидин (децитабін або дакоген), 1-β-Dарабінофуранозил-5-азацитозин, дигідро-5-азацитидин, антисмисловий олігонуклеотид MG98 і зебуларин. Таким чином, наприклад, в деяких варіантах пропонується спосіб лікування проліферативного захворювання (такого як злоякісна пухлина), що включає в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять таксан (такий як паклітаксел), і білок-носій (такий як альбумін), і b) ефективної кількості вориностату. У деяких варіантах пропонується спосіб лікування проліферативного захворювання (такого як злоякісна пухлина), що включає в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять таксан (такий як паклітаксел), і білок-носій (такий як альбумін), і b) ефективної кількості азацитидину. У деяких варіантах пропонується спосіб лікування проліферативного захворювання (такого як злоякісна пухлина), що включає в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять таксан (такий як паклітаксел), і білок-носій (такий як альбумін), і b) ефективної кількості децитабіну. У деяких варіантах пропонується спосіб лікування раку молочної залози у індивідуума, що 2 UA 111158 C2 5 10 15 20 25 30 35 40 45 50 55 60 включає в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять таксан (такий як паклітаксел), і білок-носій (такий як альбумін), і b) ефективної кількості щонайменше одного іншого засобу, який модифікує епігенетику в клітині. У деяких варіантах пропонується спосіб лікування раку молочної залози у індивідуума, при цьому індивідуум є негативним відносно ER, PR і HER2, що включає в себе введення індивідууму a) ефективної кількості композиції, що містить наночастинки, які містять таксан (такий як паклітаксел), і білок-носій (такий як альбумін), і b) ефективної кількості щонайменше одного іншого засобу, який модифікує епігенетику в клітині. У деяких варіантах спосіб додатково включає в себе проведення остаточної операції в межах приблизно 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10 після передопераційної терапії. Способи згідно з винаходом звичайно включають в себе введення композиції, що містить наночастинки, які містять таксан (такий як паклітаксел) і білок-носій. У деяких варіантах композиція на основі наночастинок містить наночастинки, які містять паклітаксел і альбумін. У деяких варіантах наночастинки в композиції, описаній в даній публікації, мають середній діаметр не більший ніж приблизно 200 нм, включаючи, наприклад, не більше ніж приблизно 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 90, 80, 70 або 60 нм. У деяких варіантах щонайменше приблизно 50% (наприклад щонайменше приблизно 60%, 70%, 80%, 90%, 95% або 99%) всіх наночастинок в композиції мають діаметр не більше ніж приблизно 200 нм, включаючи, наприклад, не більше ніж приблизно 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 90, 80, 70 або 60 нм. У деяких варіантах щонайменше приблизно 50% (наприклад щонайменше 60%, 70%, 80%, 90%, 95% або 99%) всіх наночастинок в композиції знаходяться в межах діапазону приблизно від 20 до приблизно 400, включаючи, наприклад, приблизно від 20 до приблизно 200 нм, приблизно від 30 до приблизно 180 нм, і в межах будь-якого з діапазонів приблизно від 40 до приблизно 150, приблизно від 50 до приблизно 120, і приблизно від 60 до приблизно 100 нм. У деяких варіантах білок-носій має сульфгідрильні групи, які можуть утворювати дисульфідні зв'язки. У деяких варіантах щонайменше приблизно 5% (включаючи, наприклад щонайменше приблизно 10%, 15%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80% або 90%) білканосії в частині композиції, що складається з наночастинок, поперечно пов'язані (наприклад, поперечно зв'язані одним або декількома дисульфідними зв'язками). У деяких варіантах наночастинки містять таксан (такий як паклітаксел), покритий білкомносієм, таким як альбумін (наприклад, сироватковий альбумін людини). У деяких варіантах композиція містить таксан як в формі наночастинок, так і не в формі наночастинок, при цьому щонайменше приблизно 50%, 60%, 70%, 80%, 90%, 95% або 99% таксану в композиції знаходиться в формі наночастинок. У деяких варіантах таксан в наночастинках складає більше ніж приблизно 50%, 60%, 70%, 80%, 90%, 95% або 99% наночастинок по масі. У деяких варіантах наночастинки містять серцевину з таксану, яка по суті не містить полімерних матеріалів (таких як полімерний матрикс). У деяких варіантах композиція на основі наночастинок по суті не містить (наприклад, не містить) поверхнево-активних речовин (таких як кремофор®, твін 80 або інших органічних розчинників, що використовуються для введення таксанів). У деяких варіантах композиція на основі наночастинок містить менше ніж приблизно 20%, 15%, 10%, 7,5%, 5%, 2,5%, або 1% органічних розчинників. У деяких варіантах масове відношення білка-носія (такого як альбумін) до таксану в композиції на основі наночастинок становить приблизно 18:1 або менше, наприклад, приблизно 15:1 або менше, наприклад, приблизно 9:1 або менше. У деяких варіантах масове відношення білка-носія (такого як альбумін) до таксану в композиції знаходиться в діапазоні приблизно від 1:1 до приблизно 18:1, приблизно від 2:1 до приблизно 15:1, приблизно від 3:1 до приблизно 13:1, приблизно від 4:1 до приблизно 12:1, приблизно від 5:1 до приблизно 10:1, приблизно 9:1. У деяких варіантах масове відношення білка-носія до таксану в частині композиції, що складається з наночастинок, становить приблизно 1:2, 1:3, 1:4, 1:5, 1:9, 1:10, 1:15 або менше. У деяких варіантах композиція, що складається з частинок має одну або декілька з перерахованих вище характеристик. У деяких варіантах композицією наночастинок є абраксан®. Композиції на основі наночастинок, які містять інші таксани (такі як доцетаксел і ортатаксел) також мають одну або декілька з перерахованих вище характеристик. Таким чином, наприклад, в деяких варіантах пропонується спосіб лікування раку молочної залози (такий як тричі негативний рак молочної залози), що включає в себе введення вказаному індивідууму a) ефективної кількості абраксану®, і b) ефективної кількості інгібітору деацетилази гістонів. У деяких варіантах пропонується спосіб лікування раку молочної залози (такого як тричі 3 UA 111158 C2 5 10 15 20 25 30 35 40 45 50 55 60 негативний рак молочної залози), що включає в себе введення вказаному індивідууму a) ефективної кількості абраксану® і b) ефективної кількості інгібітору ДНК-метилтрансферази. У деяких варіантах пропонується спосіб лікування раку молочної залози (такого як тричі негативний рак молочної залози), що включає в себе введення вказаному індивідууму a) ефективної кількості абраксану®, і b) ефективної кількості вориностату. У деяких варіантах спосіб додатково включає в себе введення індивідууму ефективної кількості основаного на платині засобу. У деяких варіантах пропонується спосіб лікування раку молочної залози (такий як тричі негативний рак молочної залози), що включає в себе: a) внутрішньовенне введення індивідууму ефективної кількості абраксану®, і b) пероральне введення індивідууму ефективної кількості вориностату. У деяких варіантах спосіб додатково включає в себе внутрішньовенне введення індивідууму ефективної кількості основаного на платині засобу (такого як карбоплатин). У деяких варіантах пропонується спосіб лікування раку молочної залози (такого як тричі негативний рак молочної залози), що включає в себе: a) внутрішньовенне введення індивідууму 2 2 приблизно від 80 до приблизно 200 мг/м (наприклад, приблизно 100 мг/м ) абраксану®, і b) пероральне введення індивідууму приблизно від 200 до приблизно 500 мг (наприклад, приблизно 400 мг) вориностату. У деяких варіантах спосіб додатково включає в себе внутрішньовенне введення індивідууму ефективної кількості основаного на платині засобу (такого як карбоплатин) в дозі AUC2. У деяких варіантах пропонується спосіб лікування раку молочної залози (такого як тричі негативний рак молочної залози), що включає в себе: a) внутрішньовенне введення індивідууму 2 2 приблизно від 80 до приблизно 200 мг/м (наприклад, приблизно 100 мг/м ) абраксану® щотижня, і b) пероральне введення індивідууму приблизно від 200 до приблизно 500 мг (наприклад, приблизно 400 мг) вориностату три дні з кожних семи днів. У деяких варіантах спосіб додатково включає в себе внутрішньовенне введення індивідууму ефективної кількості карбоплатину в дозі AUC2 щотижня. У деяких варіантах композицію на основі наночастинок (і карбоплатин) вводять в перший день кожного тижня, а вориностат вводять в 1-3 дні кожного тижня. У деяких варіантах пропонується спосіб лікування раку легень (такого як недрібноклітинний рак легень (NSCLC)), що включають в себе введення вказаному індивідууму a) ефективної кількості абраксану®, і b) ефективної кількості інгібітору ДНК-метилтрансферази. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе введення вказаному індивідууму a) ефективної кількості абраксану® і b) ефективної кількості децитабіну. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе: a) внутрішньовенне введення індивідууму ефективної кількості абраксану® і b) внутрішньовенне введення індивідууму ефективної кількості децитабіну. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе: a) 2 внутрішньовенне введення індивідууму приблизно від 80 до приблизно 200 мг/м (наприклад, 2 приблизно 90 або 100 мг/м ) абраксану®, і b) внутрішньовенне введення індивідууму приблизно 2 2 2 від 1 мг/м до приблизно 15 мг/м (наприклад, 4,5 мг/м ) децитабіну. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе: a) внутрішньовенне введення індивідууму приблизно від 80 до приблизно 2 2 200 мг/м (наприклад, приблизно 100 мг/м ) абраксану®, і b) внутрішньовенне введення 2 2 2 індивідууму приблизно від 5 мг/м до приблизно 100 мг/м (наприклад, 15 мг/м ) децитабіну. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе: a) внутрішньовенне введення індивідууму приблизно від 80 до приблизно 2 2 200 мг/м (наприклад, приблизно 90 або 100 мг/м ) абраксану® протягом п'яти днів, які йдуть 2 один за одним, і b) внутрішньоочеревинне введення індивідууму приблизно від 1 мг/м /доба до 2 2 приблизно 15 мг/м /доба (наприклад, 4,5 мг/м /доба) децитабіну два рази на добу протягом п'яти днів, які йдуть один за одним. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе: a) внутрішньовенне введення індивідууму приблизно від 80 до приблизно 2 2 200 мг/м (наприклад, приблизно 100 мг/м ) абраксану® на тиждень, і b) внутрішньовенне 2 2 2 введення індивідууму приблизно від 5 мг/м до приблизно 100 мг/м (наприклад, 15 мг/м ) децитабіну кожні вісім годин протягом трьох днів, які йдуть один за одним. У деяких варіантах лікування децитабіном повторюють кожні шість тижнів, проводячи чотири або більше циклів. У деяких варіантах пропонується спосіб лікування раку легень (такого як NSCLC), що включають в себе: a) внутрішньовенне введення індивідууму приблизно від 80 до приблизно 2 2 200 мг/м (наприклад, приблизно 100 мг/м ) абраксану® на тиждень, і b) внутрішньовенне 4 UA 111158 C2 2 5 10 15 20 25 30 35 40 45 50 55 60 2 2 введення індивідууму приблизно від 5 мг/м до приблизно 100 мг/м (наприклад, 20 мг/м ) децитабіну щодня протягом п'яти днів, які йдуть один за одним. У деяких варіантах лікування децитабіном повторюють кожні чотири тижні, проводячи чотири або більше циклів. Також пропонуються набори і композиції, застосовні в способах, описаних в даній публікації. Способи, які пропонуються в даній заявці, застосовні для лікування різних захворювань, включаючи, наприклад, рак молочної залози, рак легень (такий як дрібноклітинний рак легень і недрібноклітинний рак легень), рак нирок, рак сечового міхура, рак підшлункової залози, рак яєчника, рак простати, раку головного мозку, рак прямої і ободової кишки, лейкоз, лімфому і множинну мієлому. У деяких варіантах проліферативним захворюванням є солідна пухлина. У деяких варіантах проліферативним захворюванням є несолідна пухлина. Вказані і інші аспекти і переваги даного винаходу стануть очевидними з подальшого докладного опису і прикладеної формули винаходу. Потрібно розуміти, що один, декілька або всі властивості різних варіантів, описаних в даній публікації, можна поєднувати, отримуючи інші варіанти здійснення даного винаходу. КОРОТКИЙ ОПИС ФІГУР На фігурі 1 показаний дизайн дослідження лікування карбоплатином і наб-паклітакселом, що проводиться з вориностатом або без нього, у пацієнтів з HER2-негативним первинним операбельним раком молочної залози. На фігурі 2 показані результати ФДГ-ПЕТ перед неоад’ювантною терапією і на 7 день після неоад’ювантної терапії у 2 пацієнтів. Для пацієнта 1 (вгорі) показані результати ФДГ-ПЕТ перед неоад’ювантною терапією (зліва), документально підтверджуючі правостороннє об'ємне утворення в молочній залозі (SUV 12,4), і на 7 день після неоад’ювантної терапії (праворуч), що показують зменшення SUV до 6,7. У пацієнта 1 спостерігали часткову відповідь на терапію. Для пацієнта 2 (внизу) показані результати ФДГ-ПЕТ перед неоад’ювантною терапією (зліва), які документально підтверджують лівостороннє об'ємне утворення в молочній залозі (SUV 31) і на 7 день після неоад’ювантної терапії (праворуч), що показують зменшення SUV до 9,9. У пацієнта 2 спостерігали повну відповідь на терапію. На фігурі 3 показані типові приклади аналізу специфічної для метилування ПЛР для SPARC в лініях клітин NSCLC і ксенотрансплантатах NSCLC. Клітини H460 обробляли децитабіном (5 мкМ) in vitro протягом 3 днів (H460 w/DEC). Продукти ПЛР візуалізували в 1,5% агарозних гелях. Me означає метилований і UM означає неметилований. На фігурі 4 показаний Вестерн-блот-аналіз, який демонструє, що експресія SPARC в ксенотрансплантатах і лініях клітин NSCLC піддається підвищуючій регуляції при лікуванні децитабіном. На панелі А показаний Вестерн-блот ліній клітин NSCLC A549, H460 і H157, оброблених 5 мкМ децитабіну протягом 3 днів in vitro і потім зібраних для ПЛР-РВ. На панелі В показані отримані від пацієнтів (PD) ксенотрансплантати NSCLC і ксенотрансплантати H460, оброблених децитабіном в дозі 1,5 мг/кг/доба або без децитабіну. Ксенотрансплантати збирали для аналізу експресії SPARC. GAPDH використовували як ендогенний контроль. GAPDH означає гліцеральдегід-3-фосфатдегідрогеназу. На фігурі 5 показана ефективність абраксану® в порівнянні з таксолом в ксенотрансплантатах PD NSCLC. Миші SCID, які несуть SPARC-позитивні ксенотрансплантати (NSCLC_16372) (панель А), SPARC-проміжні ксенотрансплантати (NSCLC_15946) (панель В), або SPARC-негативні ксенотрансплантати, NSCLC_16465 (панель С) і NSCLC_16591 (панель D). Клітини обробляли наповнювачем, токсолом в дозі з еквівалентною токсичністю (13,4 мг/кг) або абраксаном® (30 мг/кг) (ABX). Загальну протипухлинну ефективність лікарських засобів вимірювали на основі об'єму пухлин кожні 2-3 дні. Планки погрішностей представляли стандартну помилку середнього. На фігурі 6 показана підвищена протипухлинна ефективність таксолу і абраксану® при попередній обробці децитабіном в SPARC-негативних ксенотрансплантатах. Панелі A-C, мишам SCID, які несуть SPARC-негативні ксенотрансплантати, NSCLC_16325 (панель А), NSCLC_16384 (панель В) або H460 (панель С), вводили децитабін (1,5 мг/кг) (DEC), таксол (13,4 мг/кг) або абраксан® (30 мг/кг) (ABX) окремо або комбінацію децитабіну і таксолу або децитабіну і абраксану®. Загальну протипухлинну ефективність лікарських засобів вимірювали на основі об'єму пухлин кожні 2-3 дні. Планки погрішностей представляли стандартну помилку середнього. На фігурі 7 показаний аналіз показника загибелі клітин у випадку ліній NSCLC-клітин A549 і H460 in vitro, що показує адитивну протипухлинну активність абраксану® (ABX) або таксолу при попередній обробці децитабіном. Панелі А і С показують результати, отримані на клітинах H460, оброблених зростаючими концентраціями абраксану® або таксолу після попередньої обробки децитабіном в концентрації 5 мкМ. Панелі В і D показують результати, отримані на клітинах 5 UA 111158 C2 5 10 15 20 25 30 35 40 45 50 55 60 A549, оброблених зростаючими концентраціями абраксану® від 0 до 50 нМ або таксолу, від 0 до 50 нМ, після попередньої обробки децитабіном в концентрації 5 мкМ. Оброблені клітини збирали для аналізу показника загибелі клітин (*р
ДивитисяДодаткова інформація
Назва патенту англійськоюCombination therapy for treating proliferative disease
Автори англійськоюDesai, Neil, P., Soon-Shiong, Patrick
Назва патенту російськоюСпособ комбинированной терапии для лечения пролиферативного заболевания
Автори російськоюДисей Нэйл П., Соон-Шионг Патрик
МПК / Мітки
МПК: A61P 35/00, A61K 9/14, A61K 31/7068, A61K 38/38, A61K 31/337
Мітки: захворювань, проліферативних, лікування, терапії, спосіб, комбінованої
Код посилання
<a href="https://ua.patents.su/79-111158-sposib-kombinovano-terapi-dlya-likuvannya-proliferativnikh-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">Спосіб комбінованої терапії для лікування проліферативних захворювань</a>
Попередній патент: Нові форми рифаксиміну і їх застосування
Наступний патент: Протез для часткової заміни трубчастої кістки
Випадковий патент: Пристрій для очистки рідини