Спосіб виготовлення індикатора для відкриття та напівкількісного визначення марганцю у воді
Номер патенту: 10382
Опубліковано: 25.12.1996
Автори: Бланк Абрам Борисович, Панталер Револьд Петрович, Гудзенко Людмила Василівна, Авраменко Людмила Йосипівна
Формула / Реферат
Способ изготовления индикатора для обнаружения и полуколичественного определения марганца в воде, предусматривающий обработку бумажной или картонной подложки раствором 1, сушку ее, обработку подложки раствором 2, сушку, отличающийся тем, что перед обработкой раствором 1 на подложку наносят сухую смесь периодата калия и сульфата бирия в соотношении 2:1, в качестве раствора 1 используют буферный раствор с рН 3,6-3,8, содержащий (мас.%):
нитрилотрпуксусную кислоту 0,002-0,02
1-10 фенантролин 0,002-0,02
дигидрофосфат калия 2,8-3,6
ортофосфорную кислоту 5´10-4 - 1´10-3
тритон X-100 1´10-4 - 3´10-4
0,4-0,8% раствор желатина остальное,
а в качестве раствора 2 используют индикаторный раствор, содержащий 0,055% малахитового зеленого, 0,023-0,032% родамина 6Ж и 0,5 % диметилглиоксима в ацетоне.
Текст
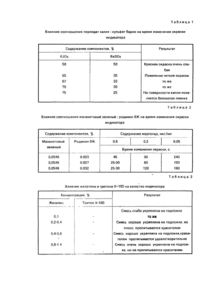
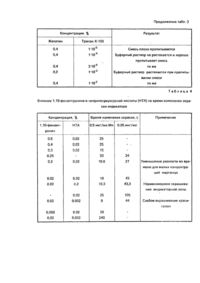
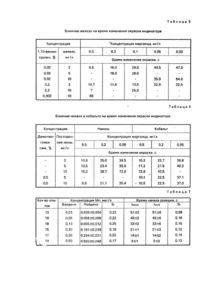
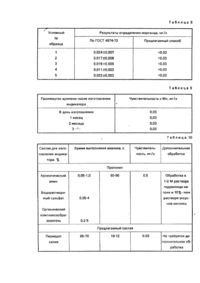
Предполагаемое изобретение относится к области анализа материалов путем определения их химических свойств, в частности, к качественному и полуколичественному определению содержания марганца в воде. В качестве прототипа к предлагаемому изобретению нами выбран способ изготовления индикатора тест-палочки с нанесенной индикаторной зоной. Индикатор изготавливают по следующей методике. На подложку последовательно наносят раствор I, содержащий 0,05 - 1% ароматического амина в 100 мл метанола, высушивают и наносят раствор II, содержащий в 100 мл воды 0,05 - 4% водорастворимых сульфатов щелочных и/или щелочно-земельных металлов, 0,2-5% органического комплексообразователя для связывания в комплекс ионов Fe (III) и снова высушивают. При взаимодействии амина с сульфатами на носителе осаждается труднораствоимый сульфат амина. В качестве ароматического амина применяют отолидин, бензидин, о-дианизидин или 2,7-диаминофлуорен. В качестве органического комплексообразователя используют винную, лимонную кислоту или их соли. В качестве подложки используют пластмассу, бумагу, хлопчатобумажное волокно. Сущность определения марганца заключается в следующем. Реакционную (индикаторную) зону тестпалочки погружают на 1 с в испытуемый раствор до полного смачивания, затем на 15 с в 1 ~ 2 Μ раствор гидроксида натрия. В случае наличия Μη (Η) после такой обработки на реакционной зоне появляется коричневое пятно (полоска), Затем выдерживают тест-палочку в течение 45 с в 10%-ной уксусной кислоте, так как область рН испытуемого раствора должна находиться в интервале рН 1 - 7, Коричневое пятно в присутствии ароматического амина превращается в окисленный продукт голубого цвета. Тест-палочку вынимают, стряхивают капельки жидкости и сравнивают окраску реакционной зоны с цветной шкалой. Чувствительность определения марганца этим методом составляет 5 мг/л. Достоинством такого определения является то, что выполнение реакции не требует точного контроля температуры, кислотность среды может изменяться в широком интервале значений рН, нет необходимости в сложной аппаратуре для контроля реакции. Недостатком этого способа является поэтапное применение двух отдельно приготовленных реактивов: 1 - 2 Μ раствора гидроксида натрия и 10%-ной уксусной кислоты, что вызывает трудности при определении марганца в воде в полевых условиях, низкая чувствительность определения (5 мг/л), а также невозможность определения в присутствии катионов или анионов со свойствами восстановителей и окислителей. Задачей изобретения является разработка способа изготовления индикатора для обнаружения и полуколичественного определения марганца в воде, в котором за счет изменения состава индикаторной зоны, нанесенной на подложку, получают индикатор с более высокой чувствительностью, экспрессностью определения марганца в воде, большей избирательностью, а также достигается упрощение выполнения анализа. Решение указанной задачи достигается тем, что в способе изготовления индикатора для обнаружения и полуколичественного определения марганца в воде, предусматривающем обработку бумажной или картонной подложки раствором 1, сушку ее, обработку подложки раствором 2, сушку, согласно изобретению, перед обработкой раствором 1 на подложку наносят сухую смесь периодата калия и сульфата бария в соотношении 2:1. в качестве раствора 1 используют буферный раствор с рН 3,6 - 3,8, содержащий нитролоуксусную кислоту, дигидрофосфат калия, 1,10-фенантролин, ортофосфорную кислоту, тритон Х-100 и 0,4 - 0,8% раствор желатина, а в качестве раствора 2 используют индикаторный раствор, содержащий малахитовый зеленый, родамин 6Ж и диметилглиоксим в ацетоне. Периодат калия применили в качестве окислителя, сульфат бария играет роль балластного вещества (в носителе). Впервые нами применена смесь двух красителей: малахитового зеленого и родамина 6Ж. В реакции каталитического окисления красителя участвует только малахитовый зеленый, сине-зеленая окраска которого при этом обесцвечивается и появляется хорошо различаемая розовая окраска родамина 6Ж. Применение такого сочетания красителей позволило повысить чувствительность определения марганца с помощью предлагаемого индикатора и определять до 0,03 мг/л марганца в воде или до 1нг в капле объемом 0,03 мл. Каталитическая активность марганца резко увеличивается в присутствии активаторов. Применение в качестве активаторов 1,10-фенантро-лина и нитрилотриуксусной кислоты привело к сокращению времени проведения анализа, что способствовало повышению чувствительности реакции определения марганца. Основное назначение желатина и тритона Х-100 - улучшение качества индикаторной зоны. Использование буферного раствора, приготовленного на желатине, способствовало лучшей адгезии реакционной зоны с подложкой, а добавка незначительных количеств неионного поверхностно-активного вещества тритона Х-100 -хорошему пропитыванию реакционных зон красителем и испытуемым раствором. Избирательность определения марганца снижается в присутствии ряда посторонних ионов. Сильное мешающее влияние оказывают ионы Fe (III), которые катализируют реакцию аналогично марганцу. Ионы Fe (III) маскировали 1,10-фенантролином. Для маскирования ионов никеля и кобальта применили диметилглиоксим. С целью выбора оптимальных условий кинетического определения марганца с помощью предлагаемого индикатора изучено влияние на скорость реакции соотношения BaSO4 : KJO4, природы буферного раствора, концентрации реагентов-красителей малахитового зеленого (восстановитель) и родамина 6Ж, активаторов 1,10-фенантролина и нитролотриуксусной кислоты, тритона X-100, диметилглиоксима, желатина, а также посторонних ионов. При разработке состава индикатора использован фосфатный буферный раствор, так как фосфаты способствуют растворению ионов Μn (III) и Μn (IV), которые являются промежуточными окисленными формами катализатора. Изучено влияние состава смеси периодата калия и сульфата бария на скорость изменения окраски индикатора. Результаты приведены в табл. 1. Максимальная скорость реакции и чувствительность наблюдаются для соотношения BaSO4 : KJO4 = 1 : 2. При увеличении доли сульфата бария,.как и при его уменьшении, чувствительность реакции уменьшалась. Максимум активности ионов марганца в реакции окисления малахитового зеленого наблюдается при рН 3,6 - 3,8, создаваемом 3,4% дигидрофосфатом калия с добавлением небольших количеств фосфорной кислоты. При увеличении его концентрации более 6,8% на периферии индикаторной зоны скапливаются кристаллы КН2РО4 и красителя, что приводит к снижению чувствительности реакции. При уменьшении концентрации дигидрофосфата калия ниже 3,4% не достигается оптимальное значение кислотности и уменьшается буферная емкость, создаваемая в растворе. В случае использования других буферных растворов каталитическая реакция либо сильно замедляется (бифталат калия, янтарная кислота с бурой), либо идет только на влажной индикаторной бумаге. При использовании буферного раствора, содержащего дигидрофосфат калия и фосфорную кислоту и имеющего рН в интервале 3,54 - 4,0, различие в окраске при отсутствии активаторов для 0,05 и 0,5 мкг/мл марганца отмечается только через 5-10 мин. Данные табл. 2 показывают влияние изменения концентрации родамина 6Ж на скорость окисления малахитового зеленого с концентрацией 0,055%. При рН 3,6 - 3,8 малахитовый зеленый окрашен в голубовато-зеленый цвет, родамин 6Ж - в красный. В случае окисления малахитового зеленого окраска ослабляется, и проявляется красная окраска родамина 6Ж. При концентрации малахитового зеленого меньше 0,055% его окисление, а значит и обесцвечивание происходит так быстро, что трудно визуально фиксировать время начала реакции. При более высоких концентрациях красителя окраска индикаторной зоны очень интенсивная, что также затрудняет установление времени протекания реакции. Как следует из табл. 2 чувствительность обнаружения изменения окраски максимальна при соотношении концентраций красителей малахитовый зеленый : родамин 6Ж, равном 2:1 В табл. 3 показано, что при приготовлении буферного раствора без желатина смесь BaSO4 : KJO4 плохо прикрепляется к подложке, легко осыпается с нее. В случае приготовления буфера из раствора, содержащего 0,2% и более желатина, смесь прочно укреплена на подложке, но плохо или вовсе не пропитывается красителем. Для улучшения пропитывания реакционных зон красителем вводили 3 10-4 - 1 10-4% тритона Х100. Введение больших количеств тритона Х-100 вызывало растекание капли, в его отсутствие смесь BaSO4 + KJO4 плохо пропитывалась красителем. Из данных табл. 4 видно, что введение в реакционную среду активаторов нитрилотриуксусной кислоты (0,02%) и 1,10-фенентро-лина (0,02%) значительно ускоряет окисление малахитового зеленого периодатом калия. При других соотношениях активаторов, например, содержании 0,02% 1,10-фенонтро-лина и изменении концентрации нитрилотриуксусной кислоты от 0,2 до 0,002% скорость реакции для 0,05 и 0,5 мкг/мл марганца высокая, но снижается чувствительность реакции, реакционная зона окрашивается неравномерно. Если концентрация нитрилотриуксусной кислоты постоянна (0,02%), а изменяется концентрация 1,10фенантролина от 0,2 до 0,002%, то наблюдается снижение чувствительности по отношению к ионам марганца (II) и уменьшение разности во времени для малых концентраций марганца. Изучено влияние ионов железа, свинца, кобальта и никеля на реакцию окисления малахитового зеленого периодатом калия 1,10-фенантролин, используемый в качестве активатора, одновременно является маскирующим агентом для ионов железа, присутствие которого допустимо до 10 мг/л (табл. 5). Как видно из табл. 6, наличие в воде 200-кратного избытка никеля или 100-кратного количества кобальта замедляет окисление малахитового зеленого периодатом калия. Установлено, что для маскирования такого количества никеля и кобальта достаточно наличия в растворе красителя 0,5% диметилглиоксима. Добавка меньшего количества комплексообразователя недостаточна для полного связывания никеля и кобальта, присутствующих в воде. Введение большего, чем 0,5% диметилглиоксима, приводит к тому, что кристаллы реагента оттесняют краситель на периферию индикаторной зоны. Это приводит к снижению чувствительности. Присутствие в воде до 100 мг/л свинца не оказывает влияния на скорость реакции окисления малахитового зеленого. Пример приготовления индикатора описан ниже. В качестве подложки может быть использована писчая бумага, картон и другие аналогичные материалы. Готовят сухую смесь периодата калия и сульфата бария в соотношении 2 : 1. На бумагу наносят отдельные порции массой 20 - 25 мг сухой смеси, смачивают их буферным раствором, приготовленным на 0,4%-ном растворе желатина, содержащем реагенты: 3,4% дигид-рофосфата калия и ортофосфоную кислоту до рН 3,63,8, по 0,02% 1,10-фенантролина и нитрилоуксусной кислоты, 10"4 % тритона Х-100 и высушивают. Затем выдерживают полоски бумаги в течение 5 минут в растворе, содержащем 0,035% малахитового зеленого, 0,027% родамина 6Ж и 0,5% диметилглиоксима в ацетоне, снова высушивают. Полученные индикаторные бумаги хранят в сухом, темном месте. Подложка может быть предварительно обработана 2-4%-ным раствором метилметакрилата в дихлорэтане. Другие варианты изготовления индикатора выполняют аналогично приведенному примеру с использованием данных табл. 1-4. Определение марганца. На индикаторную зону наносят каплю (0,03 мл) раствора, содержащего марганец, включают секундомер и определяют время появления розовой окраски. Для определения марганца сравнивают время начала изменения окраски с таблицей, в которой приведена зависимость времени изменения окраски индикатора от концентрации марганца. С целью получения указанной зависимости на индикаторные зоны наносят по одной капле раствора, содержащего 0,03; 0,05; 0,10; 0,20; 0,30; 0,50 мкг/л Μn и определяют по секундомеру время появления розовой окраски. Данные о метрологической оценке результатов полуколичественного определения марганца в искусственно приготовленных растворах, содержащих марганец, приведены в табл. 7. Для получения этих результатов наносили на индикаторные зоны по одной капле раствора ("введено") и для оценки концентрации марганца ("найдено") с помощью таблицы предлагали наблюдателям. Из табл. 7 видно, что предлагаемая индикаторная бумага позволяет с надежностью, достаточной для полу количественного метода, определять 0,03 - 0,50 мг/л марганца в воде. Правильность результатов полуколичественного определения марганца в водопроводной воде с помощью предлагаемой индикаторной бумаги проверена спектрофотометрическим методом в соответствии с ГОСТ 4974-72. Вода питьевая. Методы определения марганца с удалением хлориона выпариванием с серной кислотой. Данные исследований приведены в табл. 8, из которой видно, что содержание в водопроводной воде марганца ниже чувствительности индикаторной бумаги при определении прямым методом. Результаты определения марганца в воде с помощью предлагаемого индикаторного теста и стандартного персульфатного спектрофотометрического метода по ГОСТ 4974-72 удовлетворительно совпадают. Проверена устойчивость индикаторной бумаги во времени. Результаты приведены в табл. 9. Как видно из этой таблицы, индикатор не теряет чувствительности к ионам марганца (II) по меньшей мере в течение 3 месяцев со дня изготовления. Полученный индикатор устойчив при хранении "в защищенном от света месте. В табл. 10 приведены сравнительные данные, характеризующие возможности индикаторов, изготовленных согласно предлагаемому техническому решению и по прототипу. Из таблицы следует, что предлагаемое техническое решение позволяет повысить чувствительность определения в 150 - 200 раз, избирательность, сократить время анализа, а также существенно упростить процедуру определения. Данная разработка найдет широкое применение при определении марганца в подпочвенных и питьевых водах в быту, полевых условиях, а также в пунктах водоподготовки, в санитарно-эпидемиологических станциях.
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for making indicator for reveal and semi-quantitative determination of manganese in water
Автори англійськоюHudzenko Liudmyla Vasylivna, Pantaler Revold Petrovych, Avramenko Liudmyla Yosypivna, Blank Abram Borysovych
Назва патенту російськоюСпособ изготовления индикатора для открывания и полуколичественного определения марганца в воде
Автори російськоюГудзенко Людмила Васильевна, Панталер Револьд Петрович, Авраменко Людмила Иосифовна, Бланк Абрам Борисович
МПК / Мітки
МПК: G01N 31/00
Мітки: визначення, відкриття, спосіб, індикатора, води, марганцю, виготовлення, напівкількісного
Код посилання
<a href="https://ua.patents.su/8-10382-sposib-vigotovlennya-indikatora-dlya-vidkrittya-ta-napivkilkisnogo-viznachennya-margancyu-u-vodi.html" target="_blank" rel="follow" title="База патентів України">Спосіб виготовлення індикатора для відкриття та напівкількісного визначення марганцю у воді</a>
Попередній патент: Двигун внутрішнього згорання зі струйним охолодженням поршнів
Наступний патент: Спосіб зниження вмісту екологічно небезпечних речовин в організмі людини
Випадковий патент: Використання полімерних матеріалів, що змінюють в'язкість, у кислотних композиціях, призначених для орального застосування, та спосіб зниження ерозії зубів (варіанти)