Спосіб одержання цирконійсилікатного каталізатора крекінгу вакуумного газойлю
Номер патенту: 112153
Опубліковано: 12.12.2016
Автори: Хоменко Костянтин Миколайович, Прудіус Світлана Володимирівна, Іньшина Олена Ігорівна, Брей Володимир Вікторович
Формула / Реферат
Спосіб одержання цирконійсилікатного каталізатора крекінгу вакуумного газойлю на основі змішаних ZrO2-SiO2 оксидів, що включає приготування водного розчину сполуки цирконію і водно-спиртового розчину похідного кремнієвої кислоти, їх змішування з утворенням реакційної суміші, гідроліз цієї суміші з наступним співосадженням гідроксиду цирконію та сполук кремнію в присутності карбаміду з утворенням гелю та термічну обробку гелю, який відрізняється тим, що як вихідну речовину беруть цирконовий концентрат ZrSiO4, який спікають з карбонатом натрію і утворений пек вилуговують азотною кислотою, а в одержану реакційну суміш, що містить сполуки кремнію і цирконію, додають розчин аміаку у кількості, достатній для нейтралізації надлишку азотної кислоти та кислоти, що утворюється при гідролізі сполуки цирконію.
Текст
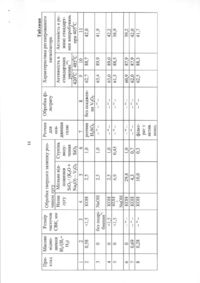
Реферат: Спосіб одержання цирконійсилікатного каталізатора крекінгу вакуумного газойлю на основі змішаних ZrO2-SiO2 оксидів, що включає приготування водного розчину сполуки цирконію і водно-спиртового розчину похідного кремнієвої кислоти, їх змішування з утворенням реакційної суміші, гідроліз цієї суміші з наступним співосадженням гідроксиду цирконію та сполук кремнію в присутності карбаміду з утворенням гелю та термічну обробку гелю, причому як вихідну речовину беруть цирконовий концентрат ZrSiO4, який спікають з карбонатом натрію і утворений пек вилуговують азотною кислотою, а в одержану реакційну суміш, що містить сполуки кремнію і цирконію, додають розчин аміаку у кількості, достатній для нейтралізації надлишку азотної кислоти та кислоти, що утворюється при гідролізі сполуки цирконію. UA 112153 U (12) UA 112153 U UA 112153 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель відноситься до способів одержання каталізаторів для процесів переробки нафти, а саме - до способів синтезу каталізаторів крекінгу вакуумного газойлю на основі змішаних оксидів цирконію та кремнію. Процес каталітичного крекінгу вакуумного газойлю є одним з найбільш багатотоннажних процесів переробки нафти. Цільовим призначенням процесу є підвищення виходу бензинової фракції. В промисловості використовують алюмосилікатні (в основному цеолітвмісні) мікросферичні лантаноідвмісні (~2 мас. %) каталізатори на основі Y фожазиту [1, 2]. Але в зв'язку з дефіцитом на рідкоземельні елементи, як замінники Ln-вмісних алюмосилікатних каталізаторів крекінгу пропонують каталізатори на основі діоксиду цирконію [3-5]. Так, в роботі [5] проведено порівняльне тестування висококислотних ZrO2-SiO2 оксидів і промислового цеолітного каталізатора крекінгу вакуумного газойлю при 480-550 °C. Показано, що цирконійсилікатні каталізатори є більш ефективними в крекінгу вакуумного газойлю, ніж алюмосилікатні завдяки їх вищій кислотності. Також цирконійсилікат продукує більше ізоалканів і менше ароматики у порівнянні з алюмосилікатом. Однак такі цирконосилікати не знайшли поки що широкого застосування через їх високу собівартість, оскільки при синтезі використовували тетраетоксисилан та нітрат цирконілу [5]. В 1942 році компанією Universal Oil Production (Чикаго, США) запропоновано спосіб виробництва каталізатора конверсії вуглеводнів, який включає співосадження гідратованого оксиду цирконію та кремнію розчином хлориду амонію з силікату натрію та солі цирконію, мольне співвідношення Zr:Si=1:6 [6]. Змішаний ZrO2-SiO2 оксид був запропонований Standard Oil як каталізатор крекінгу в 1944 році [7]. В патенті описаний спосіб одержання каталізатора імпрегнуванням гідратованого оксиду кремнію розчином солі цирконію. Вміст діоксиду цирконію в кінцевому продукті складає 20 %, тобто мольне співвідношення Zr:Si=1:8. Причинами, які перешкоджають досягненню потрібного технічного результату при синтезі каталізаторів [6, 7], є те, що, внаслідок використання силікату натрію, який містить іони натрію, необхідна тривала промивка гелю водою до повного видалення іонів натрію. В разі неповної відмивки вміст іонів натрію у кінцевому продукті значно знижує концентрацію каталітично активних кислотних центрів. Метод імпрегнування не дозволяє отримувати зразки з рівномірним розподілом іонів цирконію на поверхні оксиду кремнію. Також відомі такі способи синтезу змішаних оксидів ZrO2-SiO2 як осадження силікатів на діоксиді цирконію, імпрегнування, співосадження і золь-гель синтез. Останнім часом увага дослідників в основному зосереджена на золь-гель методах одержання ZrO2-SiO2 [8-10]. Всі вони відрізняються природою використовуваних алкоксидів, розчинників та добавок, які регулюють ті чи інші властивості цільового продукту. Наприклад, як алкоксиди використовують етилати, пропілати, ізопропілати, бутилати, та похідні інших спиртів. Ці ж спирти застосовують і як розчинники. Як каталізатор прискорення гідролізу алкоксидів кремнію застосовують різні органічні основи або мінеральні кислоти. У деяких варіантах гель витримують у надкритичних умовах, що дає можливість одержати змішаний оксид цирконію та кремнію з високими структурними параметрами. Незважаючи на різноманітність технологічних режимів та добавок допоміжних компонентів, усі відомі варіанти мають загальні ознаки - витримку при певній температурі розчину алкоксидів кремнію та цирконію протягом часу, за який протікає гідроліз суміші з утворенням золю, а потім гелю, та наступну термічну обробку гелю. Основна причина, що перешкоджає практичному застосуванню цирконій силікатних каталізаторів полягає в використанні досить дорогих алкоксидів кремнію та хлориду (нітрату) цирконілу як вихідних речовин. Також технологія одержання таких каталізаторів передбачає використання органічних розчинників, які на наступних стадіях потрібно видаляти, що створює екологічні проблеми. В роботі [11] для синтезу цирконійсилікату запропоновано використовувати як вихідну речовину природний мінерал циркон ZrSiO4, який в своєму складі містить одночасно і цирконій і кремній (теоретичний склад 67,1 % ZrO2 та 32,9 % SiO2). Недоліком способу є, по-перше, використання автоклаву, а по-друге, великий вміст іонів натрію, що не дає можливості одержати висококислотний оксид. Цирконовий концентрат має високу хімічну стійкість до більшості реагентів за нормальних умов, тому для промисловості вибір технічно можливих та економічно обґрунтованих способів його переробки часто обмежений такими методами: сплавлення з лугами, спікання з карбонатами лужних і лужноземельних металів та з гексафторосилікатом калію. Розкладання цирконових концентратів ведуть за високих температур у межах 500-1300 °C. Відомий спосіб розкладання цирконового концентрату спіканням з фторосилікатом калію K2SiF6 [12], який є побічним продуктом у виробництві суперфосфатів з апатитів, в присутності 1 UA 112153 U 5 10 15 20 25 30 35 40 45 50 55 60 промоутора - хлористого калію при 650-700 °C в муфельній барабанній печі, в результаті чого одержують K2ZrF6: K2SiF6+ZrSiO4=K2ZrF6+2SiO2 Недоліком даного способу є використання у великих кількостях дорогого фторсилікату калію, що зумовлює велику собівартість одержаного продукту, а також утворення важкорозчинного оксиду кремнію, що унеможливлює його подальше використання. Крім того, K2ZrF6 є токсичною і корозійно-активною речовиною, що ускладнює обладнання для роботи з нею. До того ж, фториди у промивних водах є екологічно шкідливими. Відомий також спосіб розкладання цирконового концентрату ZrSiO4, що включає змішування його із сполукою кальцію і розчином гідроксиду натрію, нагрівання суміші в автоклаві, відмивання утвореного продукту від лугу і обробку його кислотою [13]. Недоліками такого способу є використання автоклаву в досить високому температурному інтервалі, що є небезпечним для робітників. Кінцевим продуктом цього способу є цирконат кальцію, який після вилуговування кислотою дає побічні продукти кальцію, які шкодять навколишньому середовищу. Відомі також способи розкладання цирконового концентрату, які включають спікання його з кальцинованою содою при високих температурах [14, 15]. Для розкладання використовують високотемпературні печі розплаву безперервної дії, які захищені цирконієвою керамікою. Нагрів реакційних мас проводиться за рахунок тепла, яке виділяється електродами. Процес ведеться при механічному перемішуванні від 2 до 4 год. Температура, необхідна для завершення реакції, досягає 1100 °C. Склад одержуваних продуктів залежить від мольного співвідношення циркону та соди: ZrSiO4+2Na2CO3=Na2ZrO3+Na2SiO3+2СО2 ZrSiO4+Na2CO3=Na2ZrSiO5+CO2 Ці реакції можуть йти одночасно, оскільки температура достатньо висока, можуть йти і побічні реакції з утворенням, наприклад, ZrO2. Розкладання циркону складає 95-97 %. Одержану масу розмелюють і багатократно відмивають водою методом протиточної репульпації. Одержаний в результаті відмивання розчин соди використовують у виробництві мінеральних добрив. Відмитий осад розкладають концентрованою азотною кислотою при підвищеній температурі з утворенням розчину нітрату цирконію та сполук кремнію. Сполуки кремнію далі осаджуються кремнійорганічними коагулянтами і відділяються методами фільтрації. Недоліком таких технологій є застосування занадто високих температур реакції розкладання, а отже, велика енергоємність процесу. Найбільш близьким за технічною суттю до способу, що заявляється, є золь-гель спосіб одержання цирконійсилікатного каталізатора на основі змішаних ZrO2-SiO2 оксидів [16]. Спосіб включає приготування водних розчинів сполуки цирконію і похідного кремнієвої кислоти, змішування цих розчинів з утворенням реакційної суміші, її витримку до утворення гелю та термічну обробку гелю. Як речовину - похідне кремнієвої кислоти беруть мономер, олігомер, полімер та/або золь кремнієвої кислоти, а як сполуку цирконію - сіль цирконію, цирконілу, та/або розчинні продукти їх гідролізу. При цьому в реакційну суміш додатково вводять карбамід у кількості, достатній для нейтралізації кислоти, що утворюється при гідролізі сполуки цирконію, продуктами гідролізу карбаміду. Недоліками такої технології є її складність та використання досить дорогих солей цирконілу. Задачею, на вирішення якої спрямована корисна модель, є розробка ефективної і менш енерговитратної технології одержання цирконійсилікатного каталізатора крекінгу вакуумного газойлю. Розроблений для вирішення поставленої задачі спосіб одержання цирконійсилікатного каталізатора дає можливість одержати технічний результат, що полягає в спрощенні технології і здешевленні каталізатора крекінгу, а отже, і пального. Суть запропонованого способу полягає в тому, що у відомому золь-гель способі одержання цирконійсилікатного каталізатора крекінгу на основі змішаного ZrO2-SiO2 оксиду, що включає приготування водного розчину сполуки цирконію і водно-спиртового розчину похідного кремнієвої кислоти, їх змішування з утворенням реакційної суміші, гідроліз цієї суміші з наступним співосадженням гідроксиду цирконію та сполук кремнію в присутності карбаміду і утворенням гелю та термічну обробку гелю відповідно заявленій корисній моделі, як вихідну речовину беруть цирконовий концентрат ZrSiO4, який спікають з карбонатом натрію і утворений пек вилуговують азотною кислотою, а в одержану реакційну суміш, що містить сполуки кремнію і цирконію, додають розчин аміаку у кількості, достатній для нейтралізації надлишку азотної кислоти та кислоти, що утворюється при гідролізі сполуки цирконію. Аналіз відомих технічних рішень в даній області, опублікованих в доступних джерелах інформації, дозволяє зробити висновок про відсутність в них сукупності ознак, схожих на суттєві 2 UA 112153 U 5 10 15 20 25 30 35 40 45 50 55 відрізняючі ознаки запропонованого способу і признати заявлене рішення таким, що відповідає критерію "новизна". Спосіб, що заявляється, здійснюється таким чином. Для переводу іонів цирконію та кремнію, які містить циркон, в розчин використовують метод спікання з карбонатом натрію по реакції: ZrSiO4+Na2CO3 Na2ZrSiO5+СО2 Подрібнені порошки цирконового концентрату та карбонату натрію ретельно перемішують в мольному співвідношенні 1:1, розкладання ведуть при температурі 1050 °C 2 год. Вихід цирконосилікату натрію, Na2ZrSiO5, при таких умовах становить 100 %. На кресл. зображені дифрактограми циркону та зразка цирконосилікату натрію, одержаного після спікання циркону та карбонату натрію, що підтверджує одержання за способом, що заявляється, цирконосилікату натрію. Нижче наведені приклади, які підтверджують можливість здійснення заявленого способу. Наважку Na2ZrSiO5, попередньо розтерту в фарфоровій ступці, висипають в стакан (600 мл) і додають розчин 6М HNO3 з розрахунку Na2ZrSiO5:HNO3=1:12 (мольне співвідношення). Суміш нагрівають до кипіння при перемішуванні і витримують при цій температурі до повного розчинення осаду. Під час вилуговування відбувається наступна реакція: Na2ZrSiO5+4HNO3 2NaNO3+ZrO(NO3)2+H2SiO3+H2O Якщо потрібно одержати змішаний оксид із більшим вмістом кремнію, наприклад складу Zr:Si=1:2, тоді до одержаного розчину додають водний розчин олігомерів кремнієвої кислоти, одержаний гідролізом ТЕОС в водно-спиртовому розчині в присутності нітратної кислоти. Одержаний розчин обробляють NH3 (1:1) для нейтралізації залишку нітратної кислоти та кислоти, що утворюється при гідролізі сполуки цирконію, і витримують при певній температурі до утворення опалесцентного гелю. Гель промивають водою, і проводять відповідну термічну обробку. Приклад 1. Наважку подрібненого цирконового концентрату масою 18,3 г (0,1 моль) змішують з 10,6 г (0,1 моль) карбонату натрію, переносять в алундовий тигель і нагрівають до 1050 °C зі швидкістю 10 °C/хв. та витримують при цій температурі протягом 2 год. Одержаний пек охолоджують в тиглі, потім переносять до фарфорової ступки, де ретельно розтирають. Пек Na2ZrSiO5 масою 24,5 г (0,1 моль), висипають в стакан (600 мл) і додають 200 мл розчину азотної кислоти з масовою концентрацією 380 г/л. Суміш нагрівають до кипіння при перемішуванні магнітною мішалкою і кип'ятять до повного розчинення пеку. Одержаний розчин, який містить нітрат цирконію та олігомери кремнієвої кислоти, охолоджують і до нього краплями, при перемішуванні, додають розчин аміаку з масовою концентрацією 115 г/л до рН~8 (контролюють за допомогою лакмусового паперового індикатора). Суміш нагрівають до 60 °C і витримують при цій температурі 2 год. до утворення гелю, який промивають 5 л дистильованої води, фільтрують і прожарюють при 700 °C 2 год. Одержують білий змішаний оксид цирконію та кремнію з співвідношенням Zr:Si=1:1, маса якого становить 17,5 г, що, з врахуванням можливих втрат при різних операціях, близько до теоретичного виходу. Розрахований теоретично вихід для 0,1 моля ZrO2-SiO2 (формульна маса 181,3) становить 18,1 г. Далі цей зразок буде позначатися у тексті як ZrSi 1-1. Приклад 2. У цьому прикладі синтез проводили так само, як описано у прикладі 1, але після додавання аміаку одержаний осад додатково витримали протягом 24 год. при 95 °C для "старіння". Наступну відмивку та термообробку проводили так само, як у прикладі 1. Далі цей зразок буде позначатися у тексті як ZrSi 1-2. Приклад 3. Для одержання зразків з мольним співвідношенням Zr:Si=1:2 до розчину, одержаного після вилуговування нітратною кислотою, як додаткове джерело іонів кремнію, додають водний розчин олігомерів кремнієвої кислоти, який одержують гідролізом 20,8 г (0,1 моль) ТЕОС в водно-спиртовому розчині в присутності нітратної кислоти (6 мл 94 % етилового спирту та 5 мл 2М нітратної кислоти і 250 мл води). Далі цей зразок буде позначатися у тексті як ZrSi 2-3. Приклад 4. Зразок синтезовано за способом-прототипом з використанням як вихідних сполук нітрату цирконілу та ТЕОС зі співвідношенням Zr:Si=1:1 [16]. Далі цей зразок буде позначатися у тексті як ZrSi 1-4. Дані про структурні та кислотні характеристики одержаних зразків приведено в табл. 1. 3 UA 112153 U Таблиця 1 Текстурні та кислотні властивості зразків змішаного оксиду цирконію та кремнію, одержаних за прикладами 1-4 Зразок ZrSi 1-1 ZrSi 1-2 ZrSi 2-3 ZrSi 1-4 (прототип) 5 10 15 20 25 Питома поверхня 2 (БЕТ), м /г 202 240 386 Загальний об'єм пор по Середній Загальна ізотермі діаметр пор за концентрація Сила кислотних десорбції азоту методом BJH, кислотних центрів, Н0mах за методом нм центрів, ммоль/г 3 BJH, см /г 0,12 2,4 0,68 -8,2 0,15 2,4 0,83 -8,2 0,25 2,6 1,4 -11,35 240 0,14 4,8 1,0 -8,2 Каталітичні властивості зразків змішаного оксиду цирконію та кремнію тестували в процесі крекінгу вакуумного газойлю на лабораторній установці зі стаціонарним шаром каталізатора за наступною процедурою. Підігрітий до 50 °C вакуумний газойль шприцевим дозатором подавали 3 в потоці аргону (30 см /хв.) в сталевий реактор (d=12 мм, l=150 мм) із стаціонарним шаром 3 каталізатору (10 см ). Для попереднього розігріву газойлю до температури реакції, верхню 3 частину реакційної зони заповнювали кварцем (4 см ). Після реактора продукти крекінгу попередньо охолоджували в холодильнику (35 °C) і конденсували в приймальнику рідкої фракції, охолодженому до -20 °C. Об'єм газової фази визначали по об'єму витісненої води. Експерименти проводили при 500 °C при подачі 4 г рідкого газойлю на 1 г каталізатора за -1 годину (WHSV=4 год. ) протягом 10 хв. Після чого каталізатор регенерували при 600 °C 3 протягом 90 хв. в потоці повітря 200 см /хв. і повторювали експеримент. Кількість коксу, утвореного на каталізаторі, визначали як різницю ваги відпрацьованого і свіжого каталізатора після їх кальцинування при 600 °C. Дистиляцію рідких продуктів крекінгу (як правило 4 г) проводили в оригінальному скляному приладі для мікрооб'ємів, оснащеному 5 см холодильником. Приймач для дистиляту охолоджували до -20 °C. Розгонку проводили в два етапи. Першу фракцію з кінцевою температурою кипіння 100 °C відганяли при атмосферному тиску, після чого перегінний прилад з розчином охолоджували до кімнатної температури та відганяли другу фракцію під вакуумом (0,17 атм) до 146 °C згідно з ASTM-1160. Кінцева температура (146 °C) відгонки відповідає кінцевій температурі кипіння бензинової фракції 200 °C під нормальним тиском, як це було попередньо визначено для m-крезолу (Тк = 202 °C). Результати щодо порівняльного тестування досліджуваних зразків в процесі крекінгу вакуумного газойлю наведено в таблиці 2. В таблиці також для порівняння представлено результати тестування промислового алюмосилікатного каталізатора Petromax-50P крекінгу вакуумного газойлю. Таблиця 2 -1 Результати тестування каталізаторів в крекінгу вакуумного газойлю при 500 °C (WHSV=4 год. ) Каталізатор ZrSi 1-1 ZrSi 1-2 ZrSi 2-3 ZrSi 2-4 (прототип) Petromax-50P 30 Конверсія газойлю, % 56 65 66 Газ, С4, мас. % 10 12 12 6 6 8 Вихід бензину, мас. % 39 47 46 Залишок газойлю (>200 °C), мас. % 44 35 34 68 14 8 46 32 58 14 4 40 42 Кокс, мас. % Цирконійсилікатний каталізатор забезпечує вищий вихід бензинової фракції порівняно з цеолітним каталізатором Petromax-50P (Таблиця 2). Було знайдено, що при використанні цирконійсилікатних каталізаторів, одержаних за способом, що заявляється, конверсія вихідного 4 UA 112153 U 5 10 15 20 25 30 35 газойлю та вихід бензинової фракції при вказаних умовах зростає зі збільшенням кислотності каталізатора та його питомої поверхні. Слід відмітити, що цирконійсилікатні каталізатори крекінгу не містять дефіцитних лантаноїдів. Заявлений спосіб може знайти широке застосування для виробництва ефективних каталізаторів крекінгу вакуумного газойлю. Джерела інформації: 1. Патент РФ № 2473385, М. кл. B01J37/10; C10G11/05, опубл. 27.01.2013. 2. Патент РФ № 2473384, МПК B01J29/08, опубл. 27.01.2013. 3. Кузнецов П.Н., Твердохлебов В.П., Кузнецова Л.И., Казбанова А.В., Мельчаков Д.А., Довженко Н.Н. Новые катализаторы на основе диоксида циркония для изомеризации алканов нефтяных фракций //J. Sib. Fed. Univ. Engineering & Technologies. - 2011. - T.4. - С. 438-452. 4. Казаков М.О., Лавренов А.В., Михайлова М.С. и др. Гидроизомеризация 2бензолсодержащих бензиновых фракций на катализаторе Pt/SO4 -ZrO2-Аl2О3. I. Влияние 2химического состава на фазовое состояние и текстурные характеристики носителей SO4 -ZrO2Al2O3 // Кинетика и катализ. - 2010. - Т. 51, № 3. - С. 457-462. 5. Брей В.В., Іньшина О.І., Хоменко К.М. Каталізатори крекінгу. Цирконійсилікати як альтернатива алюмосилікатам // Хімічна промисловість України. - 2015. - Т. 128, № 3. - С. 33-37. 6. Pat. US № 2289918, Publ. 14.07.1942. 7. Pat. US № 2364949 A, Publ. 12.12.1944. 8. Aguilar D.H., Torres-Gonzalez L.C., Torres-Martinez L.M., Lopez Т., Quintana P. A study of the crystallization of ZrO2 in the sol-gel system: ZrO2-SiO2 // J. Solid State Chem. - 2001. - T. 158, № 2. P. 349-357. 9. Tarafdar A., Panda А.В., Pramanik P. Synthesis of ZrO2-SiO2 mesocomposite with high ZrO2 content via a novel sol-gel method // Microporous mesoporous materials. - 2005. - T. 84, № 1. - P. 223-228. 10. Han, Z., Li, X., Zhang, M., Liu, Z., Gao, M. Sol-gel synthesis of ZrO2-SiO2 catalysts for the transformation of bioethanol and acetaldehyde into 1,3-butadiene // RSC Advances. - 2015. - T. 5, № 126. - P. 103982-103988. 11. Pat. US № 3027230, Publ. 27.03.1962. 12. Патент РФ № 2263074 C2, опубл. 27.10.2005. 13. Патент на корисну модель UA 40810 U, Бюл. № 8 2009 p. 14. Большаков К.А. Химия и технология редких и рассеянных элементов. 4.2, 1976, "Высшая школа" Москва, с. 360. 15. Кулешов И.М., Шманенкова Г.И. О взаимодействии циркона с некоторыми карбонатами при нагревании // Журн. прикл. химии. - 1962. - Т. 35. - С. 1686-1690. 16. Прудиус С.В. Синтез мезопористого кислотного оксида ZrO2-SiO2 // Катализ и нефтехимия. - 2010. - № 18. - С. 1-5. (ПРОТОТИП). ФОРМУЛА КОРИСНОЇ МОДЕЛІ 40 45 50 Спосіб одержання цирконійсилікатного каталізатора крекінгу вакуумного газойлю на основі змішаних ZrO2-SiO2 оксидів, що включає приготування водного розчину сполуки цирконію і водно-спиртового розчину похідного кремнієвої кислоти, їх змішування з утворенням реакційної суміші, гідроліз цієї суміші з наступним співосадженням гідроксиду цирконію та сполук кремнію в присутності карбаміду з утворенням гелю та термічну обробку гелю, який відрізняється тим, що як вихідну речовину беруть цирконовий концентрат ZrSiO4, який спікають з карбонатом натрію і утворений пек вилуговують азотною кислотою, а в одержану реакційну суміш, що містить сполуки кремнію і цирконію, додають розчин аміаку у кількості, достатній для нейтралізації надлишку азотної кислоти та кислоти, що утворюється при гідролізі сполуки цирконію. 5 UA 112153 U Комп’ютерна верстка Л. Литвиненко Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 6
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C10G 11/00, B01J 37/00, B01J 29/08, C10G 11/05
Мітки: каталізатора, вакуумного, цирконійсилікатного, спосіб, одержання, крекінгу, газойлю
Код посилання
<a href="https://ua.patents.su/8-112153-sposib-oderzhannya-cirkonijjsilikatnogo-katalizatora-krekingu-vakuumnogo-gazojjlyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання цирконійсилікатного каталізатора крекінгу вакуумного газойлю</a>
Попередній патент: Спосіб кріотермодеструкції доброякісних новоутворень шкіри у дітей
Наступний патент: Нагрівальний регістр
Випадковий патент: Мікрохвильова інтегрована телерадіоінформаційна система "мітріс-н"