5,7-дипропіоніл-6-(41-циклогексилфеніл)-5н-[1,2,4]триазоло[3,4-b] [1,3,4]тіадіазин, що має протипухлинні властивості
Номер патенту: 118179
Опубліковано: 25.07.2017
Автори: Демченко Діана Анатоліївна, Демченко Анатолій Михайлович, Янченко Віктор Олексійович, Бобкова Людмила Станіславівна
Формула / Реферат
5,7-Дипропіоніл-6-(41-циклогексилфеніл)-5H-[1,2,4]триазоло[3,4-b][1,3,4]тіадіазин:
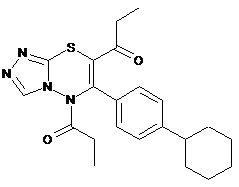 ,
,
що має протипухлинну активність.
Текст
Реферат: 1 5,7-Дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4-b][1,3,4]тіадіазин: S N N N O N O , що має протипухлинну активність. UA 118179 U (12) UA 118179 U UA 118179 U Корисна модель належить до органічної, фармацевтичної хімії та медицини, а саме до 1 одержання біологічно активного 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4b][1,3,4]тіадіазину формули: S N N N O N O , 5 10 15 20 25 30 35 що проявляє протипухлинну активність та може бути використаний при лікуванні пухлин молочної залози. Захворювання на пухлини молочної залози в світі становлять понад 20 % від загальної кількості онкологічних захворювань [1]. Рак молочної залози є найчастішою формою злоякісних пухлин у жінок. Найбільша смертність від нього зазвичай у віці 40-50 років. В 5-10 % може бути спадковим та проявляється внаслідок мутацій в генах BRCA1 та BRCA2, що призводить до виникнення раку молочної залози в 60-80 % випадків [2], що в деяких країнах Європи є показаннями до профілактичної мастектомії [3]. Вік та жіноча стать також підвищують ризик розвитку новоутворення [4]. Інші потенційні фактори ризику: відсутність пологів та вигодовування груддю [5], підвищений рівень естрогенів. [6]. У чоловіків рак грудної залози спостерігається дуже рідко. Попередні патологічні процеси в тканинах молочної залози відіграють не останню роль в розвитку раку. Причинами цих змін у тканині молочної залози служить ряд ендокринних порушень, нерідко обумовлених супутніми захворюваннями яєчників, повторними абортами, неправильним годуванням дитини і т.п. Ризик збільшується із збільшенням розміру залози, анатомо-ембріологічних відхиленнь, а також попередньої доброякісної пухлини - фіброаденоми молочної залози. На сучасному етапі для лікування пухлинної хвороби застосовують понад 40 протипухлинних препаратів, активних при різних формах злоякісних утворень, які призводять до зменшення пухлини і, відповідно, до клінічної ремісії. Протипухлинні препарати з різними механізмами дії застосовують в схемах лікування. Широке застосування в терапії набули циклофосфан, метатрексат, вінкристин, адріабластин. Зазначені лікарські засоби мають необхідні лікувальні властивості, але проявляють значні побічні ефекти на систему кровотворення (лейкопенія, анемія, тромбоцитопенія), ЦНС (почуття втоми, головокружіння, головна біль, афазія, сонливість, судоми), репродуктивної системи (порушення оогенезу та сперматогенезу, олігоспермія, порушення менструального циклу, зниження лібідо, імпотенція), сечовидільної системи (гематурія, цистит, виражені порушення функції нирок), алергічні та дерматологічні реакції, тощо. Відома також сполука - похідне 1,2,4-триазолу (лікарський засіб анастрозол) формули: N N N N N . 1 UA 118179 U 5 10 15 Анастрозол [7] проявляє активність проти естрогензалежних пухлин молочної залози у жінок. Він є селективним нестероїдмим інгібітором ферменту ароматази, який призводить до зниження рівня естрадіолу в периферичних тканинах. При застосуванні анастрозолу може розвиватися анемія, тромбофлебіт та лейкопенія, що є показаннями для відміни препарату. В основу корисної моделі поставлена задача пошуку нових речовин, що проявляють протипухлинну активність - здатність пригнічувати ріст ракових клітин молочної залози (MCF7, MDA-MB-231/ATCC, HS, 578T, ВТ-549, Т-47D), лейкемії, раку легень, раку товстого кишечнику, раку ЦНС, меланоми, раку яєчників, раку нирок та раку простати. Поставлена задача вирішується тим, що як нову хімічну речовину синтезовано 5,71 дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4] триазоло[3,4-b][1,3,4]тіадіазин(DАМ009143). Заявлену сполуку одержують з високим виходом при використанні відомих синтетичних підходів у декілька стадій (схема 1). 1 Схема 1. Синтез 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4b][1,3,4]тіадіазину (DAM009143). O N Br N N + N S N ТЕА SH N N NH2 1 2 3 (СH3СH2СO)2O S N N N O N O DAM009143 20 25 30 35 . Дослідження мітотичної активності проведено методом флуоресцентного зафарбування (барвник - сульфородамін Б) (табл.). Приклади конкретного виконання. 4-Аміно-4Н-[1,2,4]триазол-3-тіол 1 був одержаний взаємодією тіокарбогідразиду з мурашиною кислотою за методом [8]. -Бромо-4-циклогексилацетофенон 2 був одержаний за методом [9]. 1 Приклад 1. Синтез 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4b][1,3,4)тіадіазину (DAM009143): суміш 1,16 г 4-аміно-4Н-[1,2,4]триазол-3-тіолу 1 та 2.81 г бромо-4-циклогексилацетофенону 2 кип'ятили в 50 мл етанолу протягом 4 годин з оберненим холодильником. Після охолодження в реакційну суміш додавали 1 мл триетиламіну, а через 15 1 хв. виливали в 100 мл води. Отриманий осад 6-(4 -циклогексилфеніл)-7H-[1,2,4]триазоло[3,4b][1,3,4]тіадіазину 7 відфільтровували, висушували та використовували без додаткового 1 очищення та ідентифікації. 1,49 г (0,005 Моля) 6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4b][1,3,4]тіадіазину 3 кип'ятили в 10 мл ангідриду пропанової кислоти протягом 3 годин з оберненим холодильником. Реакційну суміш охолоджували і виливали в 200 мл води з льодом. Одержаний продукт відфільтровували та перекристалізовували із пропанолу-2. Вихід 1,66 г (81 1 %). Тпл.=138-140 °C. Спектр ЯМР Н, , м.ч. (ДМСО): 1,05 (т, 3Н, СН3), 1,13 (т, 3Н, СН3), 1,21-1,82 (м, 10H, (СН2)5), 2,51 (м, 1Н, СН), 2,65 (к, 2Н, СОСН2), 3,04 (к, 2Н, СОСН2), 7,34 та 7,61 (д-д, 4Н, 2 UA 118179 U 5 10 15 20 С6Н4), 9,411 (с, 1H, СН). Знайдено, %: N 13,8; S 7,63. C22H26N4O2S. Вирахувано, %: N 13,7; S 7,81. 1 Приклад 2. Для визначення протипухлинної активності 5,7-дипропіоніл-6-(4 циклогексилфеніл)-5H-[1,2,4]триазоло[3,4-b][1,3,4]тіадіазину (DAM009143) дослідження проведено in vitro на 60 лініях ракових клітин (лейкемії, легень, товстого кишечнику, ЦНС, -5 меланоми, яєчників, нирок, простати, молочної залози) при дії речовини в концентрації 10 моль/л за стандартною процедурою [10] оцінки мітотичної активності нових потенційних біологічно активних сполук методом флуоресцентного зафарбування (барвник - сульфородамін Б), виконаних у Національному інституті раку США (National Cancer Institute of Health, USA) в рамках Development Therapeutic Program. Результат проведених досліджень виражали у відсотках росту клітин раку у порівнянні з контролем - 5-флуорурацилом. Наведені у таблиці значення показують на скільки досліджувані сполуки є більш ефективними у пригніченні росту ракових клітин у порівнянні з контролем. Визначення проводили високочутливим флюорометричним методом, кількісно оцінюючи інтенсивність кольору флуоресцентного випромінювання (барвник - сульфородамін Б) через 48 год. опромінення клітини зі сполукою, що тестується. Результат проведених досліджень виражали у відсотках росту клітин раку до контролю. 1 В умовах експерименту заявлений 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H-5 [1,2,4]триазоло[3,4-b][1,3,4]тіадіазин (DAM009143 ) у концентрації 10 моль/л виявив здатність пригнічувати ріст ракових клітин молочної залози: MCF7, MDA-MB-231/ATCC, HS, 578T, ВТ-549, T-47D та MDA-MB-468. Крім цього було відмічено, що досліджувана сполука також в певній мірі пригнічують ріст клітин практично всього спектру онкологічних захворювань людини (табл.). Таблиця Протипухлинна активність 1 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4-b][1,3,4]тіадіазину in vitro на лініях -5 клітин раку при дії речовин в концентрації 10 моль/л (GP) та при концентрації -4 -8 10 -10 моль/л (Log10GI50, Log10TGI, Log10GI50). Лінії ракових клітин CCRF-CEM HL-60(TB) К-562 MOLT-4 RPMI-8226 SR А549/АТСС НОР-62 НОР-92 NCI-H226 NCI-H23 NCI-H322M NCI-H460 NCI-H522 COLO 205 HCC-2998 HCT-116 НСТ-15 НТ29 КМ12 SW-620 GP (%) Log10GI50 Лейкемія 8,55 -6,47 -22,49 -6,34 9,80 -6,48 0,86 -6,33 2.11 -6,52 -6,37 Дрібноклітинний рак легень 14,89 -6,42 41,64 -6,15 35,41 42,15 -6,36 20,64 -6,24 59,41 0,49 -6,55 5,31 -6,18 Рак товстого кишечнику 6,16 -6,17 29,48 -6,17 12,44 -6,37 8,01 -6,38 24,16 -6,18 11,63 -6,17 16,65 -6,26 25 3 Log10TGI Log10GI50 > -4,00 > -4,00 -4,40 -5,12 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 -5,53 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 UA 118179 U Лінії ракових клітин GP (%) SF-268 SF-295 SF-539 SNB-19 SNB-75 U251 33,73 18,05 16,26 51,32 47,67 25,71 LOX IMVI MALME-3M М14 MDA-MB-435 SK-MEL-2 SK-MEL-28 SK-MEL-5 UACC-257 UACC-62 8,59 40,05 29,88 16,47 9,14 48,46 -55,79 10,79 19,21 IGROV1 OVCAR-3 OVCAR-4 OVCAR-5 OVCAR-8 NCI/ADR-RES SK-OV-3 39,82 27,47 32,73 32,73 8,86 23,70 64,54 786-0 A498 AСHN CAKI-1 RFX 193 SN12C 27,35 52,07 18,43 41,41 72,75 30,80 TK-10 UO-31 40,06 17,82 РС-3 DU-145 7,82 46,59 MCF7 MDA-MB-231/ATCC HS 578T ВТ-549 T-47D MDA-MB-468 20,43 -10,48 52,89 10,47 13,67 39,55 Log10GI50 Рак головного мозку -5,94 -6,41 -6,11 -6,08 -5,70 -6,32 Меланома -6,42 -6,01 -5,98 -6,25 -5,47 -5,90 -6,87 -6,49 -6,44 Рак яєчників -6,27 -6,15 -6,61 -5,28 -6,35 -6,16 > -4,00 Рак нирок -6,12 -6,68 -6,30 -6,46 -6,06 -6,23 Log10TGI Log10GI50 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 -5,38 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 -5,76 -6,27 Рак простати -6,72 -5,94 Рак молочної залози -6,47 -5,80 -5,40 -5,89 -6,38 -7,48 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 -4,71 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 > -4,00 1 5 10 Відповідно до наведеної таблиці 1, 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H[1,2,4]триазоло[3,4-b][1,3,4]тіадіазин виявив більш високу протипухлинну активність відносно клітин лейкемії, меланоми, дрібноклітинного раку легенів, раку товстого кишечнику, пухлин головного мозку, яєчників, простати, молочної залози та нирок ніж препарат порівняння - 5флуороурацил. Так, щодо клітин дрібноклітинного раку легенів затримка росту пухлин вище стандарту на 40,59-99,51 %, клітин раку товстого кишечнику - на 71,52-93,84 %, клітин раку кори головного мозку - на 48,62-83,74 %, клітин меланоми на 32,51-63,98 %, клітин раку яєчників - на 35,46-91,14 %, клітин раку нирок - на 27,25-82,18 %, клітин раку простати РС-3 на 92,18 %, Відносно клітин раку молочної залози T-47D заявлена сполука зупиняє ріст і поділ клітин на 67,58 %. Крім цього відносно клітин раку молочної залози, меланоми та лейкемії досліджувана 4 UA 118179 U 5 10 15 20 25 сполука не тільки затримує ріст пухлин, але і знищує деякі лінії ракових клітин. Так відносно клітин лінії раку молочної залози MDA-MB-231/ATCC показник склав -10,48 % , клітин лейкемії HL-60(TB) - 22,49 %, а клітин меланоми SK-MEL - 55,79 %. 1 Приклад 3. На другому етапі досліджувану 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H[1,2,4]триазоло[3,4-b][1,3,4]тіадіазин тестували у п'яти концентраціях при 10-кратному розведенні (100 М, 10 М, 1 М, 0,1 М, та 0,01 М) на 60 лінія людських ракових клітин. У результаті експерименту було розраховано 3 дозазалежні параметри: 1) GI50 - концентрація сполуки, яка викликає пригнічення росту 50 % пухлинних клітин лінії; 2) TGI-концентрація, при якій відмічається повне пригнічення росту клітин; LC50 - концентрація, за якої гине 50 % пухлинних клітин. Якщо логарифмічні значення цих параметрів є меншими за -4,00 сполуки розглядають як активні [11-13]. 1 Встановлено, що 5,7-дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4b][1,3,4]тіадіазин при поглибленому скринінгу in vitro на лініях клітин раку при дії речовин в -4 -8 концентрації 10 -10 моль/л має ефективний рівень інгібування майже всіх ліній ракових клітин. Так для ліній раку лейкемії показник Log10GI50 знаходиться в межах від -6,52 до -6,33, для клітин дрібноклітинного раку легенів в межах від -6,55 до-6,15, для клітин раку товстого кишечнику в межах -6,38 - -6,17, для клітин раку кори головного мозку в інтервалі від -6,41 до -5,70, для клітин меланоми в інтервалі від -6,87 до -5,47, для клітин раку яєчників OVCAR-4 - -6,61, для клітин раку нирок від -6,68 до -5,76. Для клітин раку простати РС-3 показник складає -6,72. Відносно клітин раку молочної залози показник знаходиться в межах від -7,48 до -5,40. Повне пригнічення росту ракових клітин було відмічено для лінії клітин раку молочної залози MDA-MB-231/ATCC для якої показник Log10 TGI склав -4,71. Крім цього повне пригнічення відмічено для клітин дрібноклітинного раку легень NCI-H522 (-5,53), клітин меланоми SK-MEL-5 (-5,38) та лейкемії MOLT-4 і RPMI-8226 (-4,45 та -5,12 відповідно). Таким чином, запропонована нова біологічно активна сполука, яка може бути потенційним протипухлинним засобом з ефективним рівнем інгібування росту майже всього спектру ракових клітин, та може повністю пригнічувати ріст клітин щодо ліній раку молочної залози MDA-MB231/ATCC, клітин дрібноклітинного раку легень NCI-H522, клітин меланоми SK-MEL-5 та лейкемії MOLT-4 і RPMI-8226. 30 35 40 45 50 55 60 Джерела інформації: 1. World Cancer Report 2014. World Health Organization. 2014. 2. Gage, M; Wattendorf, D; Henry, LR. Translational advances regarding hereditary breast cancer syndromes // Journal of surgical oncology. 2012 - Vol.105, № 5. - P.444-451. 3. Unukovych, D; Sandelin K, Wickman M, Arver B, Johansson H, Brandberg Y, Liljegren A. Breast reconstruction in patients with personal and family history of breast cancer undergoing contralateral prophylactic mastectomy, a 10-year experience // Acta Oncologica. 2012. - Vol. 51. - P 934-941. 4. Reeder, JG; Vogel, VG. Breast cancer prevention // Cancer treatment and research. 2008. Vol.141. - P. 149-164. 5. Collaborative Group on Hormonal Factors in Breast Cancer. Breast cancer and breastfeeding: collaborative reanalysis of individual data from 47 epidemiological studies in 30 countries, including 50302 women with breast cancer and 96973 women without the disease // Lancet. 2002. - Vol.360, № 9328. - P. 187-195. 6. Yager JD. Estrogen carcinogenesis in breast cancer// New Engl J Med. 2006 - Vol.354, № 3. P. 270-82. 7. M. Baum, J. Cuzick, J. Forbes, J. Houghton, A. Howell (The ATAC Trialists Group): Anastrozole alone or in combination with tamoxifen versus tamoxifen alone for adjuvant treatment of postmenopausal women with early stage breast cancer. Results of the ATAC (Arimidex, Tamoxifen Alone or in Combination) trial efficacy and safety update analyses // Cancer. 2003. - Vol.98. - P. 18021810. 8. Bonafoux, Dominique; Nanthakumar, Suganthini; Bandarage, Upul K.; Memmott, Christine; Lowe, Derek; Aronov, Alex M.; Bhisetti, Govinda Rao; Bonanno, Kenneth C; Coll, Joyce; Leeman, Joshua; Lepre, Christopher A.; Lu, Fan; Perola, Emanuele; Rijnbrand, Rene; Taylor, William P.; Wilson, Dean; Zhou, Yi; Zwahlen, Jacque; Ter Haar, Ernst. Fragment-Based Discovery of Dual JC Virus and В К Virus Flelicase Inhibitors // Journal of Medicinal Chemistry. 2016. - Vol.59, № 15. - P. 7138-7151. 9. Ladopoulou, Eleni M.; Matralis, Alexios N.; Nikitakis, Anastasios; Kourounakis, Angeliki P. Antihyperlipidemic morpholine derivatives with antioxidant activity: An investigation of the aromatic substitution // Bioorganic and Medicinal Chemistry. 2015. - Vol. 23, № 21. - P. 7015-7023. 5 UA 118179 U 5 10 10. Beverly A. Teicher, Paul A. Andrews. Anticancer drug development guide: preclinical screening, clinical// Medical. 2004. - Vol. 1. - P. 450. 11. Alley M.C., Scudiero D.A., Monks P.A. et al., Feasibility of Drug Screening with Panels of Human Tumor Cell Lines Using a Microculture Tetrazolium Assay //Cancer Research. 1988. - Vol. 48. - P. 589-601. 12. Boyd M.R., Pauli K.D. Some practical considerations and applications of the national cancer institute in vitro anticancer drug discovery screen // Drug Development Research. 1995. - Vol. 34, № 2. - P. 91-109. 13. Monks A., Scudiero D., Skehan P., et al. Feasibility of a High-Flux Anticancer Drug Screen Using a Diverse Panel of Cultured Fluman Tumor Cell Lines //Journal of National Cancer Institute. 1991. - Vol. 83, № 11. - P. 757-766. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 15 1 5,7-Дипропіоніл-6-(4 -циклогексилфеніл)-5H-[1,2,4]триазоло[3,4-b][1,3,4]тіадіазин: S N N N O N O , що має протипухлинну активність. 20 Комп’ютерна верстка В. Мацело Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 6
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07D 417/00
Мітки: має, властивості, протипухлинні, 5,7-дипропіоніл-6-(41-циклогексилфеніл)-5н-[1,2,4]триазоло[3,4-b, 1,3,4]тіадіазин
Код посилання
<a href="https://ua.patents.su/8-118179-57-dipropionil-6-41-ciklogeksilfenil-5n-124triazolo34-b-134tiadiazin-shho-maeh-protipukhlinni-vlastivosti.html" target="_blank" rel="follow" title="База патентів України">5,7-дипропіоніл-6-(41-циклогексилфеніл)-5н-[1,2,4]триазоло[3,4-b] [1,3,4]тіадіазин, що має протипухлинні властивості</a>
Попередній патент: Спосіб виробництва борошна з цілого зерна
Наступний патент: Спосіб рукавної резекції шлунка
Випадковий патент: Спосіб освітлення біохімічно очищеної фенольної стічної води












