Спосіб одержання наночастинок міді в іонному каприлатному середовищі
Номер патенту: 121719
Опубліковано: 11.12.2017
Автори: Асаула Віталій Миколайович, Боровик Поліна Володимирівна, Яремчук Галина Григорівна, Мирна Тетяна Альфредівна
Формула / Реферат
Спосіб одержання наночастинок міді, рівномірно розподілених в об'ємі скловидної іонної рідкокристалічної каприлатної матриці, що включає їх синтез шляхом відновлення іонів міді, який відрізняється тим, що синтез відбувається в одну стадію в інертній атмосфері протягом 3 годин у іонному розплаві на основі каприлату кадмію (C8H15O2)2Cd при температурі 185-200 °C, яке одночасно виконує функцію відновника та стабілізатора.
Текст
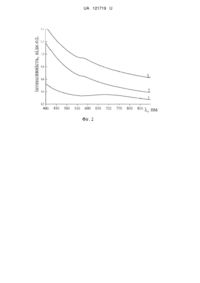
Реферат: Спосіб одержання наночастинок міді, рівномірно розподілених в об'ємі скловидної іонної рідкокристалічної каприлатної матриці, що включає їх синтез шляхом відновлення іонів міді, причому синтез відбувається в одну стадію в інертній атмосфері протягом 3 годин у іонному розплаві на основі каприлату кадмію (C8H15O2)2Cd при температурі 185-200 °C, яке одночасно виконує функцію відновника та стабілізатора. UA 121719 U (12) UA 121719 U UA 121719 U 5 10 15 20 25 30 35 40 45 50 55 60 Запропонована корисна модель належить до темплатного способу одержання наночастинок міді у скловидних прозорих матрицях на основі каприлату кадмію. Синтез відбувається у іонному неводному середовищі, яке відіграє роль відновника і сприяє рівномірному розподілу наночастинок міді та їх стабілізації. Одержані таким способом матеріали можуть застосовуватися в оптичних пристроях та нелінійно-оптичних матеріалах, в таких як оптичні перемикачі чи фотохромне скло [1]. Аналіз науково-технічної літератури показав, що на даний час розроблено велику кількість різноманітних методів синтезу наночастинок міді. Загалом проводяться такі синтетичні процеси як відновлення, гідроліз, конденсація та окиснення. Крім того, можна виділити такі основні категорії синтезу наночастинок міді: хімічний синтез, електрохімічний синтез, фотохімічні і сонохімічні методи та термічна обробка (термоліз). Хімічний синтез є одним з поширених доступних і зручних методів синтезу, що полягає в конденсації атомів або молекулярних угрупувань з газової фази або розчину для отримання наночастинок заданого розміру та морфології. Ці параметри задаються умовами синтезу, такими як температура, концентрація прекурсору, відновника, стабілізуючого агента та природа розчинника. Серед хімічних методів синтезу наночастинок міді заданого розміру та морфології найпростішими є реакції відновлення [2-4]. Хімічні реакції відновлення є чутливими до реакційного середовища та впливу повітря, оскільки поверхня наночастинок міді легко окиснюється, тому зазвичай необхідно використовувати інертні умови (атмосфера аргону або азоту) або поверхнево активні речовини для захисту поверхні наночастинок [5, 6]. Поширеним методом одержання наночастинок міді як в гомогенних, так і гетерогенних системах є відновлення солей міді боргідридом натрію. Так, в роботі [7] одержано наночастинки, розмір яких знаходиться в інтервалі 14-22 нм. В роботі [8] нанорозмірний порошок міді розміром 20-100 нм одержано, використовуючи в якості відновника натрій борогідрид та полівініпіролідон як стабілізатор. Метод мікроемульсійного відновлення передбачає застосування системи масло-вода або вода-масло, а також поверхнево активної речовини (ПАВ), що забезпечує утворення нанореакторів [9]. Міцелярні системи можна розглядати як сукупність нанорозмірних хімічних "реакторів", які формуються із молекул поверхнево-активних речовин. Метод синтезу наночастинок міді полягає в змішуванні двох зворотних мікроемульсій, одна з яких містить розчиненну в солюбілізованній воді сіль міді, а інша - відновник. При цьому можуть бути використані як мономерні, так і димерні ПАВ [10]. Загалом відновлення в мікроемульсіонному середовищі було вперше використано для синтезу наночастинок золота, але в подальшому було застосовано для інших металів, зокрема міді. Для цього використовувались солі міді (сульфати, нітрати, хлориди) та відновники (боргідрид натрію, ізопропіловий спирт, аскорбінова кислота та гідразин) і, в деяких випадках, стабілізуючі агенти (полівініл піролідон та поліетилен гліколь) [11, 12]. Також як відновник застосовуються різні фітоекстракти, які призводять до формування стабільних сферичних наночастинок міді розміром 15-20 нм [13]. Відомі також приклади [14] отримання наночастинок міді методом відновлення за допомогою поліакрилової кислоти. Таким чином були отримані композитні плівки поліакрилової кислоти, що містили наночастинки міді. В іншій статті для отримання наночастинок міді діаметром до 10 нм було використано відновлення в суміші поліакрилової кислоти та блоккополімерів [15]. Також було доведено можливість використовувати боргідрид натрію як відновник [16] та желатин як стабілізатор [17]. Електрохімічний синтез ґрунтується на пропусканні електричного струму між катодом та анодом, розділених розчином електроліту. Відновлення відбувається на поверхні катода. Наприклад, в [18] протягом 30 хв пропускали струм 4 V, 5 А через розчин сульфату міді і сірчаної кислоти, в результаті чого було отримано наночастинки діаметром 40-60 нм.Використання мікрохвиль є відносно новими методами отримання монодисперсних частинок міді з заданою морфологією [19, 20]. Даний метод, оснований на впливі електромагнітних хвиль частотою від 300 МГц до 300 ГГц, при цьому значна кількість енергії витрачається саме на формування наночастинок міді. Так, при дії мікрохвиль і використанні сульфату міді як прекурсора та гіпофосфіту натрію як відновника одержано наночастинки діаметром 10 нм [21]. Метод термічного розкладання полягає у проведенні хімічної реакції в автоклавах в умовах підвищенного тиску та температур, вищих, за температури кипіння розчинників. У випадку, коли як розчинник використовується вода, процес називається гідротермальним [22]. Так авторами статті [23] даний метод був використаний для синтезу наночастинок міді діаметром 3,5-40 нм. В 1 UA 121719 U 5 10 15 20 25 30 35 40 45 50 55 роботі [24] було використано гідротермальний метод з використанням додецилбензенсульфату як стабілізатора та для контролю форми наночастинок. Показано, що наявність стабілізатора та зміна температури значно впливають на процесе формування наночастинок. Термоліз солей органічних солей перехідних металів широко використовується на практиці як один із методів синтезу нанорозмірних частинок металів та їх оксидів. При цьому наночастинки металів одержують як в індивідувальному стані, так і іммобілізованими в композитах. При переході від термолізу солей насичених кислот (форміатів і оксалатів) до солей ненасичених кислот (акрилати і малеати) середні розміри наночастинок зменшуються. Крім того, в останньому випадку одержують нанорозмірні частинки, які стабілізовані полімерною матрицею. Так, при термолізі Сu(ІІ) форміату, середній розмір наночастинок Сu складає 30 нм [25], у випадку Сu(II) акрилату - 20-30 нм [26]. У всіх випадках одержуються наночастинки з великим розкидом розмірів (до 24 нм), одержуваний матеріал забруднений вкрапленнями оксидного матеріалу. Термоліз солей ароматичних кислот практично не досліджено. В основі нетрадиційних, так званих дисперсійних, методів отримання нанорозмірної міді лежить руйнування кристалічної решітки металічної міді під дією різних фізичних впливів. До таких методів належать, зокрема, методи лазерної абляції [27], механохімічний синтез [28-30] та конденсація парів металоорганічних реагентів [31]. Основним недоліком усіх фізичних методів є необхідність у дорогих вакуумних системах. Незважаючи на чималу різноманітність методів, наночастинки міді, в основному, отримують у вигляді колоїдних розчинів чи аморфних порошків. Такі методи мають ряд недоліків, серед яких: - обмежена часом стабільність наночастинок у розчині; - полідисперсність синтезованих наночастинок міді; - вплив багатьох параметрів синтезу на розмір та форму наночастинок; - вплив природи відновника на розмір та форму наночастинок; - використання додаткових методів фізичного впливу при формуванні наночастинок; - складність у подальшому використанні, наприклад, для створення композитних матеріалів на основі наночастинок міді. Найбільш близьким до запропонованого - є метод синтезу наночастинок міді з використанням блок-полімерного середовища [15]. У цьому методі блок-співполімер відіграє функцією стабілізатора. Формування наночастинок включає такі основні етапи: відновлення солі металу гідразин-бораном в розчині і формування металічних кластерів, адсорбція блок-співполімерів на кластерах металу та захист від окиснення і агрегацій цих наночастинок блок-співполімером. Цей метод також має певні недоліки, наприклад, він дозволяє отримувати наночастинки з розміром близько 20 нм та більше і, як правило, має обмежений вихід (концентрацію наночастинок), який не зростає із збільшенням концентрації солі металу в розчині, використання дорогих відновників та низька стабільність полімерного полікомплексу. В останні десятиліття інтенсивно розвивається наноплазмоніка - напрям дослідження, що вивчає взаємодію світла із поверхневими плазмонами в металодіелектричних структурах. При синтезі наночастинок міді слід пам'ятати, що велика увага до них зумовлена, в першу чергу, наявністю характерного для них ефекту поверхневого плазмонного резонансу (ППP), що має велике значення для нелінійної оптики та ін. Для отримання матеріалу з гарними оптичними характеристиками слід велику увагу приділяти як розміру наночастинок, так і їхній дисперсності, тобто, не слід допускати агрегації частинок, для запобігання цьому використовують стабілізатори. Крім того, найбільш вигідним методом буде досить простий та доступний спосіб отримання наночастинок, який не буде потребувати великих затрат матеріалів, обладнання та людських ресурсів, і у результаті використання якого будуть збереженими цінні оптичноструктурні характеристики наночастинок. Беручи до уваги наведені вище аргументи, нами був розроблений метод синтезу наночастинок міді у скловидних прозорих каприлатних матрицях. Для отримання матеріалу з хорошим розподілом наночастинок міді по всьому об'єму використовували іонні розплави алканоатів металів, так як така іонна матриця сприяє дезагрегації та стабілізації наночастинок міді, які розташовуються впоперек бішарів рідкокристалічного упорядкування скловидних нанокомпозитів. Наночастинки міді були синтезовані в одну стадію у іонному розплаві каприлату кадмію (C8H15O2)2Cd з використанням хлоридів міді CuCl та СuСl2 як джерела іонів міді. У цьому методі розплав каприлатів металів одночасно виступає і як відновник, і як стабілізуюче середовище. Синтез проводили при температурах 180-220 °C. При охолодженні розплавів отримували 2 UA 121719 U 5 10 15 20 25 30 35 40 45 50 55 рідкокристалічні нанокомпозитні стекла з наночастинками міді. Концентрацію міді в композиті варіювали від 1 до 8 мол. %. Отримані зразки досліджували методами електронної спектроскопії УФ та видимої області, малокутового рентгенівського розсіювання та політермічної поляризаційної мікроскопії (ППМ). Методом електронної спектроскопії досліджено оптичні властивості отриманих рідкокристалічних стекол з наночастинками міді. Показано, що в електронних спектрах поглинання присутня широка смуга в діапазоні від 570 нм до 610 нм, яка відповідає ППР наночастинок міді. При підвищенні концентрації наночастинок міді міді від 1 до 8 мол. % збільшується значення оптичної густини поглинання, але значного довгохвильового зсуву смуги поглинання не спостерігається (Фіг. 1). Використовуючи метод малокутового рентгенівського розсіювання, встановлено, що в іонному рідкокристалічному середовищі індивідуального каприлату кадмію формуються сферичні монодисперсні наночастинки міді з розміром від 3 до 15 нм залежно від концентрації наночастинок. Методом політермічної поляризаційної мікроскопії підтверджено формування і збереження структури засклованої мезофази. Таким чином, запропонований метод має ряд переваг порівняно з іншими методами синтезу наночастинок міді: 1) відносна простота проведення реакції синтезу; 2) відсутність необхідності застосування додаткових відновників та стабілізуючих агентів; 3) монодисперсність наночастинок в композиті; 4) досить висока концентрація наночастинок (до 8 мол. %); 5) можливість синтезу стабільних наночастинок певного розміру без наступного окиснення при тривалому зберіганні. Далі наведено приклади, що наглядніше і детальніше розкривають запропонований метод синтезу та розширюють його застосування. Приклад 1. Одержання наночастинок міді на основі індивідуального каприлату кадмію в залежності від концентрації іонів міді. Виходячи з того, скільки матеріалу необхідно отримати та яку концентрацію наночастинок міді він матиме, розраховуємо необхідні для синтезу кількості речовин. Так для синтезу 0,5 г кінцевого продукту з 2 мол. % наночастинок міді беремо 0,005 г СuСl2 × 2Н2О, що відповідає 2 мол. % Сu та розраховується за формулою: де m - маса зазначеного компонента; Mr - молярна маса відповідного компонента; х молярна концентрація наночастинок міді у матриці. Далі диспергуємо водний хлорид міді (ІІ)у 0,1 мл метанолу та додаємо до 0,5 г порошку каприлату кадмію (Сd(C8Н15О2)2). Ретельно перетираємо отриману суміш та поміщаємо її в скляний реактор, де в інертній атмосфері (Аr) нагріваємо до температури розплаву (180-200)°С і витримуємо протягом 3 годин. У процесі синтезу реакційна суміш поступово змінює колір з прозорого синьо-зеленого розплаву до насиченого коричневого кольору. При охолодженні розплаву отримуємо скловидний нанокомпозит, вміст наночастинок Сu в якому становить 2 мол. %. Отриманий зразок досліджуємо методом електронної спектроскопії на наявність смуги поглинання ППР та визначаємо розмір наночастинок міді, стабілізованих в РК-склі. Встановлено, що положення максимуму ППР знаходиться при λ=585 нм, що відповідає наночастинкам із розміром 7-10 нм, згідно з даними спектроскопії поглинання в працях [32-34]. Встановлено, що синтез практично повністю відбувається при температурі 200 °C. Для синтезу композитних матеріалів на основі каприлату кадмію з іншим вмістом наночастинок міді методика синтезу залишається незмінною, змінюються тільки кількості вихідних речовин згідно зі стехіометрією. Дослідження впливу вихідної концентрації іонів металу на розмір отриманих наночастинок проведено, використовуючи наступні концентрації прекурсору міді у реакційній суміші: 1 мол. %; 4 мол. %, і 8 мол. %. Аналіз оптичних спектрів поглинання нанокомпозицій показав, що зміна концентрації йонів міді суттєво не впливає на розмір частинок, але дозволяє отримувати нанокомпозити із досить значним вмістом металічних наночастинок Сu. Максимум смуги поглинання при А, - 585 нм спостерігається для всіх знятих зразків. На Фіг. 1 - Спектри поглинання нанокомпозитів на основі каприлату кадмію з наночастинками меді в залежності від концентрації прекурсору катіонів міді: 1-1 мол. %, 2-4 3 UA 121719 U 5 10 15 20 25 30 35 40 45 50 55 60 мол. %, 3-8 мол.; прекурсор - СuСl2. З Фіг. 1 видно, що оптимальною є концентрація в 4 мол. % прекурсора, оскільки при підвищенні концентрації катіонів міді (до 8 мол. %) при синтезі відбувається укрупнення або підвищується полідисперсність наночастинок міді, що проявляється в сильному уширенні при λ=590-680 нм смуги плазмонного резонансу на спектрах поглинання. При малій концентрації катіонів міді (1 мол. %) утворюється незначна кількість наночастинок міді. Приклад 2. Одержання наночастинок міді на основі каприлату кадмію залежно від тривалості синтезу. Диспергуємо 0,0085 г водного хлориду міді (II) у 0,1 мл метанолу та додаємо до 0,5 г порошку каприлату кадмію (Сd(C8Н15О2)2). Ретельно перетираємо отриману суміш та поміщаємо її в скляний реактор, де в інертній атмосфері (Аг) нагріваємо до температури розплаву ~ 200 °C і витримуємо протягом 3 годин. Експерименти проводилися протягом 1 год., 2 год. і 3 год. при температурі 200 °C. При охолодженні розплаву отримуємо скловидний нанокомпозит, вміст наночастинок Сu в якому становить 4 мол. %. Отриманий зразок досліджуємо методом електронної спектроскопії на наявність смуги поглинання ППР та визначаємо розмір наночастинок міді, стабілізованих в РК-склі. Фіг. 2 - Спектри поглинання нанокомпозитів на основі каприлату кадмію з наночастинками меді в залежності від тривалості синтезу; 1-1 год., 2-2 год., 3-3 год.; концентрації прекурсору катіонів міді: 4 мол. %; прекурсор - СuСl2. Аналіз оптичних спектрів поглинання одержаних нанокомпозитів (Фіг. 2) показав, що формування наночастинок відбувається повільно, протягом 2-3 год., проте, тривалість проведення реакції в термостаті не впливає на розмір частинок. Максимум смуги поглинання при 585 нм спостерігається для зразків, витриманих від 2 до 3 годин. Положення максимуму плазмонного поглинання при 680 нм на кривій 1 може відповідати формуванню нестійких комплексів іонів міді з каприлатними лігандами, які з часом руйнуються. Приклад 3. Одержання наночастинок міді на основі каприлату кадмію в при застосуванні одновалентного прекурсору міді. Диспергуємо 0,0052 г хлориду міді (І) у 0,1 мл метанолу та додаємо до 0,5 г порошку каприлату кадмію (Сd(C8Н15О2)2). Ретельно перетираємо отриману суміш та поміщаємо її в скляний реактор, де в інертній атмосфері (Аг) нагріваємо до температури розплаву (180-200)°С і витримуємо протягом 3 годин. У процесі синтезу реакційна суміш поступово змінює колір з прозорого синьо-зеленого розплаву до насиченого коричневого кольору. При охолодженні розплаву отримуємо скловидний нанокомпозит, вміст наночастинок Сu в якому становить 4 мол. %. Отриманий зразок досліджуємо методом електронної спектроскопії на наявність смуги поглинання ППР та визначаємо розмір наночастинок міді, стабілізованих в РК-склі. Встановлено, що положення максимуму ППР знаходиться при λ=575 нм, що відповідає наночастинками із середнім розміром 5-7 нм, згідно з даними спектроскопії поглинання в працях [32-34]. Встановлено, що синтез практично повністю відбувається при температурі 185 °C. Отже, як свідчить експеримент та Фіг. 1 і 2, збільшення концентрації до і більше 8 мол. % призводить до укрупнення наночастинок чи об'ємної фази, при цьому збільшення тривалості взаємодії алканоат-ланцюгів з наночастинками міді від 1 до 3 годин сприяє максимальному виходу продукту. Таким чином, для запропонованого способу оптимальними є концентраційний діапазон наночастинок 2-6 мол. %, тривалість синтезу 2,5-3 години, при температурі Т=185200 °C. Виявлено, що дешевий та доступний хлорид двовалентної міді повністю задовольняє умови синтезу наночастинок. Оцінено, що середній розмір отримуваних наночастинок міді 5-6 нм, при цьому розподіл розмірів наночастинок міді становить 4-15 нм. Джерела інформації: 1. Dang Т. М. et al. // Adv. Nat. Sci.: Nanosci. Nanotechnol. 2011. 2: 015009. 2. Song X. et al. // J. Colloid Interface Sci. 2004. 273, № 2: 463-469, 2004. 3. Kapoor S., Mukherjee T. // Chem.Phys. Lett. 2003. 370, № 1-2: 83. 4. Пат. RU 2426805. Способ получения нанодисперсного порошка меди / Сименюк Г. Ю., Образцова И. И., Еременко Н. К. Опубл. 20.08.2011. 5. Subhan A. et al. // J. Lumm.2014. 146: 123. 6. Charan S. et al. // J. Nanoscience Nanotechnology. 2006. 6, № 7: 2095. 7. Avchinnicova E. A., Vorob'eva S. A. // Vestnik Belorusskogo Gosudarstvennogo Universiteta. 2013. 3: 12 (in Russian). 8. Hashemipour H. et al. // Int. J. Phys. Sci. 2011. 6: 4331. 9. Ghorbani H. R. et al. // Oriental Journal of Chemistry. 2014. 30,№. 2: 15-18. 10. Pat. US 2008/0138643 Al. Method for manufacturing copper nanoparticles and copper nanoparticles manufactured using the same / Lee W.-J., Joung J.-W., Lee Y.-II, Jun B.-Ho. Pub. Date: Jun. 12, 2008 4 UA 121719 U 5 10 15 20 25 30 11. Pat. US 2008/0157029 Al. Method of producing copper nanoparticles and copper nanoparticles produced thereby / Lee Y.-II, Oh Y.-S., Juong J.-W. Pub. Date: Jul. 3, 2008. 12. Pat. US 2007/0180954 Al. Copper nanoparticles, method of preparing the same, and method of forming copper coating film using the same / Kim J. S., Moon J. Ho, JEONG Ho, Kim D. Jo, Park В. К. Pub. Date: Aug. 9, 2007. 13. Nasrollahzadeh M., Sajadi S.M. // J Colloid Interface Science. 2015. 457: 141. 14. Gotoh Y. et al. // J Mater. Chem. 2000. 10: 2548. 15. Ostaeva. G.Y. et al. // Polym. Set, Ser. B. 2008. 50: 147. 16. R. Prucek et al. // J. Mater. Chem. 2009. 19: 8463. 17. Chatterjee A. K. et al. // Nanotechnology. 2012. 23(8): 085103. 18. Raja M. et al. // Mater. Manuf. Process. 2008. 23, № 8: 782. 19. Quintana-Ramirez P. V. et al. II Beilstein J. Nanotechnology 2014. 5, №1: 1542. 20. Kanhed P. et al. // Materials Letters. 2014. 115:13. 21. Pat. US 2008/0072706 Al. Method for manufacturing copper nanoparticles using microwaves / Lee Y.-II, Joung J.-W. Pub. Date: Mar. 27, 2008. 22. Morones J. R. et al. // Nanotechnology. 16, № 10: 2346. 23. Baco-Carles V. et al. // International Scholarly Research Network ISRN Nanotechnology. 2011. ID 729594. 24. Chen H. et al. // J. Nanosci. Nanotechnol. 2010.10: 629. 25. Помогайло А.Д., Розенберг А.С., Уфлянд И.Е. Наночастицы металлов в полимерах. - М.: Химия, 2000. - с. 236-255. 26. Александрова Е.И. и др. // Изв. РАН, сер. Хим. 1993. № 2: 303. 27. Amendola V. et al. // J. Phys. Chem. B. 2006.110: 7232. 28. Shen T. D., С. С. Koch //Ada Mater. 1996. 44: 753. 29. Gaffet E. et al. // J. Alloys Compound. 1993. 194(1): 23. 30. Ding J. et al. // J. Alloys Compound. 1996. 234: 11. 31. Cioffi N. et al. // Metallic Nanomaterials. 2010. 1: 70. 32. Pileni M.P. // J.Phys. Chem.1993. 97.: 6961. 33. Singh M. et al. // Colloids Surf. A: Physicochem. Eng. Aspects. 2010. 359: 88. 34. Huang H.H. et al. // Langmuir. 1997. 13.: 172. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 35 Спосіб одержання наночастинок міді, рівномірно розподілених в об'ємі скловидної іонної рідкокристалічної каприлатної матриці, що включає їх синтез шляхом відновлення іонів міді, який відрізняється тим, що синтез відбувається в одну стадію в інертній атмосфері протягом 3 годин у іонному розплаві на основі каприлату кадмію (C8H15O2)2Cd при температурі 185-200 °C, яке одночасно виконує функцію відновника та стабілізатора. 5 UA 121719 U Комп’ютерна верстка Л. Бурлак Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 6
ДивитисяДодаткова інформація
МПК / Мітки
МПК: B82B 1/00, C01G 3/00, B22F 9/20
Мітки: іонному, середовищі, каприлатному, наночастинок, одержання, спосіб, міді
Код посилання
<a href="https://ua.patents.su/8-121719-sposib-oderzhannya-nanochastinok-midi-v-ionnomu-kaprilatnomu-seredovishhi.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання наночастинок міді в іонному каприлатному середовищі</a>
Попередній патент: Спосіб зниження забруднення ґрунтів сільськогосподарського призначення важкими металами
Наступний патент: Електричний генератор
Випадковий патент: Метаногідратна електростанція