Спосіб одержання тетраборату літію
Номер патенту: 32242
Опубліковано: 15.12.2000
Автори: Турок Іван Іванович, Пуга Павло Павлович, Головей Вадим Михайлович
Текст
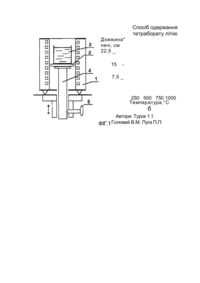
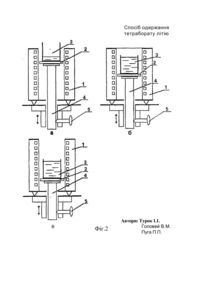
МПК С 01 В 35/12 Спосіб одержання тетраборату літію Винахід відноситься до хімічної технології і може бути використаний для одержання складних кисневих сполук, наприклад, вихідної шихти для вирощування монокристалів тетраборату літію Li2B4O7 (ТБЛ). Відомий спосіб одержання ТБЛ сплавленням оксиду бору В2О3 та карбонату літію Іл2СОз в контейнері, контроль стехіометрії якого проводять за допомогою диференціально-термічного аналізу (ДТА), а корекцію складу розплаву - шляхом введення потрібної кількості необхідного компоненту [1]. Однак відомий спосіб має слідуючий недолік. Карбонат літію на повітрі при атмосферному тиску розкладається при температурі 620-650 С, тобто в тих умовах, коли оксид бору вже цілком розплавлений, з виділенням значної кількості вуглекислого газу. При розкладі карбонату літію розплав вспінюється внаслідок його високої в'язкості, сильно збільшуючись в об'ємі, що може привести до викиду речовини з контейнера. Таким чином, в контейнері за один цикл сплавлення вихідних компонентів може бути синтезована мала по масі наважка ТБЛ, яка займає незначну частину об'єму контейнера. Для використання при синтезі і вирощуванні монокристалів ТБЛ одного контейнера (так як при перевантаженні вносяться додаткові забруднення) він мусить мати високу ступінь заповнення (80-90% об'єму) Найбільш близьким по технічній суті і ефекту, що досягається, є спосіб одержання ТБЛ сплавленням стехіометричних кількостей оксиду бору та карбонату літію [2], який обраний нами за прототип. Для підвищення продуктивності процесу синтезу за рахунок збільшення коефіцієнту використання об'єму контейнера оксид бору завантажують в попередньо нагрітий до 390 - 410 С контейнер, що знаходиться в печі і неперервно зважується, карбонат літію вводять в контейнер в інтервалі температур 930-950 С до досягнення попередньо розрахованої ваги, причому обидва компонента вводять в контейнер порціями. До недоліків приведеного способу слід віднести слідуючі. В процесі проведення синтезу по мірі введення до розплаву оксиду бору карбонату літію проходить постійна зміна хімічного складу розплаву. У відповідності із діаграмою стану [3] при цьому змінюються також температура плавлення і в'язкість для кожного конкретного складу, а, отже, змінюється і швидкість взаємодії компонентів. В результаті, не дивлячись на однакову масу порцій карбонату літію, які вносяться в розплав, об'єм вспіненої суміші в контейнері при кожному послідуючому циклі змінюється. Щоб уникнути викиду суміші з контейнера, доводиться регулювати швидкість взаємодії компонентів за допомогою зміни температури в об'ємі печі, так як контейнер з речовиною знаходиться у певному фіксованому положенні, причому початкова температура взаємодії розплаву з внесеною порцією карбонату літію більш низька, поскільки спочатку проходить його обезводжування, а також розклад карбонату літію з виділенням вуглекислого 2. газу і лише згодом їх хімічна взаємодія. Таким чином, температурні умови кожного циклу взаємодії відрізняються від попередніх і регулювати швидкість протікання хімічних процесів в контейнері доводиться за рахунок зміни температур у печі, що приводить до значних додаткових витрат часу і електроенергії, а також поганої керованості процесом. Отже, недоліком способу є низка продуктивність процесу синтезу внаслідок неоптимальної швидкості реакції взаємодії вихідних компонентів. Оптимальною швидкістю взаємодії можна вважати таку, при якій хімічна реакція відбувається за мінімальний проміжок часу без викиду речовини з контейнера. Викликає певні незручності і введення порцій вихідних компонентів в контейнер, який знаходиться у порожнині печі, поскільки це призводить до часткових втрат суміші і, як наслідок, при цьому порушується стехіометрія і забруднюються зовнішні стінки контейнера і внутрішні стінки печі. Наявність частини реагентів на зовнішніх стінках контейнера приводить до похибки при зважуванні і встановленні стехіометрії. Завданням винаходу є підвищення продуктивності процесу синтезу ТБЛ шляхом оптимізації швидкості взаємодії вихідних компонентів. Завдання досягається тим, що в способі одержання ТБЛ сплавленням вихідних компонентів в контейнері, що включає в себе їх порційне введення до попередньо нагрітого контейнеру, розміщеного в печі шахтного типу з наявністю градієнтної ділянки, контроль стехіометрії ваговим методом, гомогенізацію кінцевого продукту і його охолодження, причому щонайменше один з вихідних компонентів розкладається з виділенням газоподібної речовини швидкість реакції взаємодії регулюють за рахунок розміщення контейнера у різних температурних зонах печі з можливістю його фіксації у цих положеннях. Порівняльний аналіз з прототипом показує, що запропонований спосіб має ряд суттєвих переваг. Так, синтез проводять у печі шахтного типу з наявністю різних температурних зон (фіг. 1), а швидкість реакції взаємодії вихідних компонентів регулюють за рахунок розміщення контейнера у різних температурних зонах. Таким чином, при внесенні у розплав кожної чергової порції вихідного компонента, який розкладається з виділенням газоподібної речовини, швидкість реакції взаємодії може бути відрегульована до оптимальної шляхом розташування контейнера з реакційною сумішшю у відповідній температурній зоні печі. При цьому вдається запобігти викиду реакційної суміші з контейнера і в той же час зменшити витрати енергії і часу. Швидкість процесу контролюється візуально і може бути оперативно скоректована за рахунок переміщення контейнера у відповідну температурну зону печі. Швидкість реакції задають такою, щоб вспінена суміш не піднімалась вище за край контейнера. Запропонований спосіб може бути використаний для одержання ТБЛ. Спосіб реалізується слідуючим чином. Конструкція шахтної печі для синтезу показана на фіг. 1а. В порожнині печі 1 розміщена керамічна підставка 2 для контейнера 3, яка через шток 4 з'єднана з направляючими з можливістю вертикального переміщення підставки з контейнером і її фіксації в різних температурних зонах печі. Приблизний розподіл температур у печі синтезу 3. наведений на фіг.2б. Для проведення синтезу попередньо зважений контейнер розміщують на підставці, піч виводять на робочий режим (температура найбільш гарячої зони складає ~950°С). Для введення окремих порцій вихідних компонентів підставку з контейнером піднімають у положення, при якому верхній край контейнера виступає за верхній зріз печі (фіг.2а) і фіксують у ньому на час завантаження за допомогою фіксатора 5. Таким чином вдається уникнути втрат вихідних компонентів при їх введенні в контейнер. Далі контейнер з речовиною переміщують вглиб печі і встановлюють у відповідній температурній зоні в залежності від інтенсивності протікання процесів обезводжування, розкладу з виділенням газоподібного продукту і взаємодії. На початковому етапі синтезу проходить обезводжування (для В2 Оз) або розклад з виділенням води (для Н3ВО3), Що супроводжується вспінюванням В2О3. Оксид бору ( або борну кислоту) вводять до контейнера невеликими порціями, а швидкість протікання процесу обезводжування контролюють візуально і регулюють, змінюючи положення контейнера на градієнтному участку печі, що дозволяє запобігти викидам. Оксид бору (або борну кислоту) додають до контейнера до заповнення його об'єму розплавом на 80-90%. Після повного видалення вологи з розплаву, про що свідчить його прозорість і відсутність газових пухирців, контейнер з розплавом видаляють з печі, швидко зважують, знову розміщають у печі і витримують (підігрівають) до розплавлення оксиду бору. Виходячи з ваги одержаного безводного оксиду бору (яку вираховують по різниці ваги завантаженого і вільного контейнера), розраховують необхідну кількість літійвміщуюючого реактива (Li2CO3, LiNO3, Li2C2O4 тощо). На другій стадії процесу синтезу в розплав оксиду бору вводять порціями літійвміщуючий реактив, регулюючи швидкість протікання реакції його розкладу (з виділенням великої кількості газоподібних продуктів) шляхом зміни положення (а, відповідно, і температури) контейнера на градієнтному участку печі. Отриманий внаслідок термічного розкладу літійвміщуючого реактива з видаленням з розплава газоподібних продуктів оксид літію Li2O реагує з оксидом бору з утворенням ТБЛ. Швидкість протікання процесів розкладу літійвміщуючого реактива і взаємодії оксидів літію і бору регулюють переміщенням контейнера на градієнтній ділянці печі до досягнення оптимальної швидкості реакції, тобто такої, при якій процес протікає за мінімальний проміжок часу, але реакційна суміш не вихлюпується з контейнера. Після закінчення процесу синтезу контейнер з розплавом переміщують у найбільш гарячу зону печі, нагріту до ~950°С для проведення гомогенізації і після її завершення одержаний продукт охолоджують у режимі виключеної печі і зважують. Корекцію складу одержаного продукту до стехіометрії проводять додаючи необхідну кількість літійвміщуючого компонента. Запропонований спосіб дозволяє зменшити часові і енергетичні витрати на проведення синтезу ТБЛ за рахунок оптимізації швидкості протікання цього процесу, а також дозволяє коректувати його склад. Приводимо приклади реалізації. 4. Приклад 1 (прототип). Контейнер (платиновий тигель діаметром 50 мм і висотою 50 мм) встановлюють на керамічну підставку і розміщують у трубчатій печі шахтного типу. Підставка закріплена на штоці, який проходить через отвір у нижньому фланці печі і з'єднаний з вагами ВЛКТ-2-М. Тигель нагрівають до 400 С і порціями в 2-3 г вводять в нього оксид бору. Кожна послідуюча порція вводиться після встановлення постійної ваги речовини що знаходиться у тиглі. Після заповнення ~70% об'єму тигля збезводженим оксидом бору і досягнення його постійної ваги виходячи з цієї величини розраховують необхідну наважку карбонату літію, яка складає 0,5307 від ваги оксиду бору. Температуру розплаву збільшують до 935°С і порціями в 2-3 г вводять у тигель карбонат літію до досягнення розрахункової ваги. Розплав витримують при 940°С на протязі 10 годин до досягнення повної гомогенізації отриманого продукту, після чого проводять його охолодження до кімнатної температури. Коефіцієнт використання (заповнення) тигля складає 85%, час синтезу - 16 годин, енергозатрати - 19,2 кВт. Приклад 2. Контейнер 1 (платиновий тигель діаметром 50 мм і висотою 50 мм) встановлюють на керамічну підставку 2 (фіг. 1а) і розміщують у трубчатій печі шахтного типу. Підставка закріплена на штоці 3, який проходить через отвір у нижньому фланці печі і з'єднаний з направляючими з можливістю вертикального переміщення підставки з контейнером і її фіксації в різних температурних зонах печі (фіг. 2а,б,в). Приблизний розподіл температур у печі синтезу наведений на фіг. 16. Для проведення синтезу попередньо зважений контейнер розміщують на підставці 1, після чого піч виводять на робочий режим (температура найбільш гарячої зони складає ~950°С). Для введення окремих порцій вихідних компонентів підставку з контейнером кожний раз піднімають у положення, при якому верхній край контейнера виступає за верхній зріз печі (фіг.2а) і фіксують у ньому на час завантаження. Таким чином вдається уникнути втрат вихідних компонентів при їх введенні в контейнер. Далі контейнер з речовиною переміщують вглиб печі і встановлюють у низькотемпературній зоні (фіг.2в). На початковому етапі синтезу проходить обезводжування В2О3, що супроводжується його вспінюванням. Оксид бору вводять до контейнера невеликими порціями, а швидкість протікання процесу обезводжування контролюють візуально і регулюють, змінюючи положення контейнера на градієнтному участку печі, що дозволяє запобігти викидам. Оксид бору додають до контейнера до заповнення його об'єму розплавом на 85%. Після повного видалення вологи з розплаву, про що свідчить його прозорість і відсутність газових пухирців, контейнер з розплавом видаляють з печі, швидко зважують, знову розміщають у печі і витримують до розплавлення оксиду бору. Виходячи з ваги одержаного безводного оксиду бору (яку вираховують по різниці ваги завантаженого і вільного контейнера), розраховують необхідну кількість карбонату літію, який попередньо просушують до повного видалення вологи. На другій стадії процесу синтезу в розплав оксиду бору вводять порціями збезводжений карбонат літію, регулюючи швидкість протікання реакцій його розкладу (з виділенням великої кількості вуглекислого газу) шляхом зміни положення (а, відповідно, і температури) контейнера на градієнтному участку печі. Отриманий внаслідок 5. термічного розкладу карбонату літію з видаленням з розплава вуглекислого газу оксид літію Li2O реагує з оксидом бору з утворенням ТБЛ. Швидкість протікання процесів розкладу карбонату літію і взаємодії оксидів літію і бору регулюють переміщенням контейнера на градієнтній ділянці печі до досягнення оптимальної швидкості реакції, тобто такої, при якій процес протікає за мінімальний проміжок часу, але суміш не вихлюпується з контейнера. Після закінчення процесу синтезу контейнер з розплавом переміщують у найбільш гарячу зону печі, нагріту до ~950°С для проведення гомогенізації і після її завершення одержаний продукт охолоджують у режимі виключеної печі. Контейнер з одержаним продуктом зважують і при необхідності додають потрібну кількість літійвміщуючого компонента до досягнення стехіометричного співвідношення Li2O/2B2O3=0,2145955. Коефіцієнт використання (заповнення) тигля складає 85%, час синтезу - 12 годин, енергозатрати - 14,4 кВт. Приклад 3. Аналогічно прикладу 2, але замість В2Оз в якості борвміщуючого компонента використовують борну кислоту Н3ВОз- Коефіцієнт використання (заповнення) тигля складає 85%, час синтезу - 12 годин, енергозатрати - 14,4 кВт. Приклад 4. Аналогічно прикладу 2, але замість Li 2 CO 3 в якості літійвміщуючого компонента використовують нітрат літію ЬіІЧОз- Коефіцієнт використання (заповнення) тигля складає 85%, час синтезу - 12 годин, енергозатрати - 14,4 кВт. Приклад 5. Аналогічно прикладу 2, але замість Li 2 CO 3 в якості літійвміщуючого компонента використовують оксалат літію Li 2 C 2 O 4 . Коефіцієнт використання (заповнення) тигля складає 85%, час синтезу - 12 годин, енергозатрати - 14,4 кВт. Як видно з наведених прикладів, найбільш оптимальним є випадок, коли швидкість реакції взаємодії регулюють за рахунок розміщення контейнера у різних температурних зонах печі з можливістю його фіксації у цих положеннях. Таким чином, запропонований спосіб дозволяє підвищити продуктивність процесу синтезу ТБЛ шляхом оптимізації швидкості взаємодії вихідних компонентів. Час проведення процесу і енергозатрати в порівнянні з прототипом вдається зменшити на 33%. Намічається використання запропонованого пристрою в Інституті електронної фізики НАН України при синтезі шихти для вирощування монокристалів ТБЛ. Даний спосіб також може бути використаний при синтезі багатьох складних кисневих сполук, зокрема, боратів і силикатів. Директор ІЕФ Патентовід Шпеник О.Б. Роман І.Ю. Спосіб одержання тетраборату літію Довжина* печі, см 22,5 _ 15 7,5 _ 250 500 750 1000 Температура,°С б Автори: Турок 1.1. ФІГ.1 Головей В.М. Пуга П.П. Спосіб одержання тетраборату літію Автори: Турок 1.1. В Фіг.2 Головей В.М. Пуга П.П. ДЖЕРЕЛА ІНФОРМ АЦІЇ 1. Заявка Японії N60-5095, кл. С 30 В 15/00, С 30 В 29/22. 2. А.с. СРСР N1716724, кл. С 01 35/3512 - прототип. 3. B.S.R.Sastry, F.A.Hummel. Studies in the lithium oxide systems: I, Li2O В2Оз - B2O3. - J.Amer.Ceram.Soc.,1958, v.41, N1, p.7-17.
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of lithium tetraborate
Автори англійськоюTurok Ivan Ivanovych, Holovei Vadym Mykhailovych, Puha Pavlo Pavlovych
Назва патенту російськоюСпособ получения тетрабората лития
Автори російськоюТурок Иван Иванович, Головей Вадим Михайлович, Пуга Павел Павлович
МПК / Мітки
МПК: C01B 35/00
Мітки: одержання, літію, спосіб, тетраборату
Код посилання
<a href="https://ua.patents.su/8-32242-sposib-oderzhannya-tetraboratu-litiyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання тетраборату літію</a>
Попередній патент: Спосіб лікування запалювальних процесів у експериментальних тварин
Наступний патент: Суднова щогла, що завалюється
Випадковий патент: Ніж для знекровлення худоби і свиней