Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза
Номер патенту: 90410
Опубліковано: 26.04.2010
Автори: Кобза Тарас Ігорович, Федорів Данило Євгенович, Радиш Роман Васильович, Орел Юрій Глібович, Кобза Ігор Іванович, Жук Ростислав Андрійович
Формула / Реферат
Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза, що включає видалення інфікованого синтетичного біфуркаційного протеза із репротезуванням аутовенами in situ, який відрізняється тим, що формують центральну і одну із бічних бранш біфуркаційної неоаорто-клубово-стегнової конструкції шляхом введення одного аутовенозного сегмента в інший по всій його довжині з утворенням двошарового венозного сегмента.
Текст
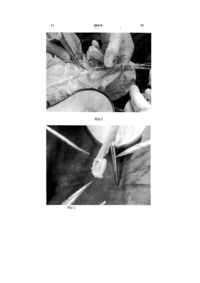
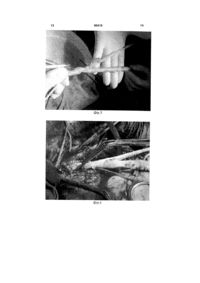
Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза, що включає видалення інфікованого синтетичного біфуркаційного протеза із репротезуванням аутовенами in situ, який відрізняється тим, що формують центральну і одну із бічних бранш біфуркаційної неоаорто-клубово-стегнової конструкції шляхом введення одного аутовенозного сегмента в інший по всій його довжині з утворенням двошарового венозного сегмента. UA (21) a200901229 (22) 16.02.2009 (24) 26.04.2010 (46) 26.04.2010, Бюл.№ 8, 2010 р. (72) КОБЗА ІГОР ІВАНОВИЧ, ОРЕЛ ЮРІЙ ГЛІБОВИЧ, ЖУК РОСТИСЛАВ АНДРІЙОВИЧ, РАДИШ РОМАН ВАСИЛЬОВИЧ, ФЕДОРІВ ДАНИЛО ЄВГЕНОВИЧ, КОБЗА ТАРАС ІГОРОВИЧ (73) КОБЗА ІГОР ІВАНОВИЧ, ОРЕЛ ЮРІЙ ГЛІБОВИЧ, ЖУК РОСТИСЛАВ АНДРІЙОВИЧ, РАДИШ РОМАН ВАСИЛЬОВИЧ, ФЕДОРІВ ДАНИЛО ЄВГЕНОВИЧ, КОБЗА ТАРАС ІГОРОВИЧ (56) Gustavo S. Oderich, Thomas С Bower, Kenneth J. Cherry Jr., Jean M. Panneton, Timothy M. Sullivan, Audra A. Noel, Michele Carmo, Stephen Cha, Manju Kalra, Peter Gloviczki. Evolution from axillofemoral to in situ prosthetic reconstruction for the treatment of aortic graft infections at a single center. J Vase Surg 2006; 43:1166-74. Audra A. Noel, Peter Gloviczki, Kenneth J. Cherry, Hazim Safi, Jerry Goldstone, Mark D. Morasch, Kaj H. Johansen, and Members of the United States Cryopreserved Aortic Allograft Registry. Abdominal aortic reconstruction in infected fields: Early results of the United States Cryopreserved Aortic Allograft Registry. J Vase Surg 2002;35:847-52. Paul D. Hayes, Akhtar Nasim, Nicholas J. ML, Robert D. Sayers, William W. Barrie, Peter R. F. Bell, A. Ross Naylor. In situ replacement of infected aortic grafts with rifampicin-bonded prostheses: the Leicester experience (1992 to 1998). J Vase Surg 1999;30:92-8. Paul R. Vogt, Hans-Peter Brunner-LaRocca, Mario Lachat, Christian Ruef, Marko I. Turina. Technical details with the use of cryopreserved arterial allografts for aortic infection: influence on early and midterm mortality. J Vase Surg 2002;35:80-6. Stephen O'Connor, Peter Andrew, Michel Batt, Jean Pierre Becquemin. A systematic review and metaanalysis of treatments for aortic graft infection. J Vase Surg 2006;44:38-45. 2 (19) 1 3 Винахід стосується медицини, зокрема судинної хірургії, і може бути використаний при лікуванні інфекції синтетичних протезів аорто-стегнової зони. Інфікування синтетичних протезів є одним із найважчих ускладнень в судинній хірургії, частота якого сягає від 0,6 до 6% [1]. Актуальність питань, пов'язаних із лікуванням пацієнтів з інфекцією судинних протезів, обумовлена високими показниками захворюваності, втрати кінцівок і смертності, навіть незважаючи на сучасний прогрес інтенсивної терапії, хірургічної техніки, анестезіологічного забезпечення та створення нових генерацій антибактеріальних середників. Прогноз стосовно ефективності лікування в більшості випадків залежить від локалізації і довжини інфікованого сегменту протеза, загального стану пацієнта і обраної лікувальної тактики. У зв'язку із поліетіологічністю інфікування протезів, різною локалізацією інфекційного вогнища і складною оперативною технікою єдиної погодженої стратегії лікування пацієнтів із інфікуванням аортальних судинних протезів немає. Лікування пацієнта із інфікуванням аортостегнового протеза переслідує дві основні мети: із мінімальним ризиком усунути вогнище інфекції і максимально повно реваскуляризувати анатомічні ділянки в басейні, який кровопостачався інфікованим протезом. Більшість спеціалістів вважають, що оптимальна схема лікування інфекції аортостегнового протеза повинна полягати у видаленні протеза (ліквідація вогнища інфекції) із подальшою реваскуляризацією органів тазу і нижніх кінцівок шляхом біфуркаційного репротезування in situ за допомогою синтетичного протеза (просоченого рифампіцином або посрібленого), кріопрезервованого аортального алошунта або аутовенозного матеріалу (глибоких вен стегново-підколінного сегменту або підшкірних вен). Відомий стандартний радикальний спосіб лікування інфекції протеза, який полягає в повному або частковому видаленні інфікованого протеза, вшиванні кукси аорти, санації і хірургічній обробці ложа протеза та екстраанатомічому шунтуванні (переважно аксілярно-стегновому) у неінфікованих зонах. Цей спосіб прийнятний як складова комплексного лікування (перший етап - видалення протеза, вшивання кукси аорти і екстраанатомічне шунтування, другий етап - репротезування in situ просоченим рифампіцином протезом після ліквідації інфекційного процесу) та є методом вибору у випадку масивного нагнійного процесу в позаочеревинному просторі із формуванням парааортальних абсцесів, коли інші способи лікування (репротезування in situ посрібленими або просоченими рифампіцином протезами, аутовенами) демонструють незадовільні результати, як і у випадку виявлення в якості етіологічного чинника інфікування метицилін-резистентного Staphylococcus aureus [2]. Незважаючи на досягнення хірургічної техніки, анестезіологічного забезпечення та інтенсивної терапії, результати використання цього способу (смертність від 24 до 70%) не дозволяють вважати його золотим стандартом лікування. Недоліками 90410 4 цього способу є також високий ризик порушення прохідності екстраанатомічних шунтів і великої ампутації (20-29%), високий ризик неспроможності кукси аорти, що переважно призводить до смерті (10-20%), високий ризик повторного інфікування аксілярно-стегнового протеза, особливо у випадках тотального інфікування протеза (10-40%), можливість розвитку ішемії тазу, органів малого тазу, висхідного тромбозу аорти та ниркової недостатності, неприйнятність у випадку розширення аорти або юкстаренального розташування проксимального анастомозу інфікованого протеза, коли немає умов для якісного вшивання кукси аорти, висока вартість армованого аксілярно-бістегнового протеза. Існують способи видалення інфікованого протеза із репротезуванням in situ, розроблені у зв'язку із незадовільними результатами тактики лікування, що включає тотальне видалення інфікованого протеза із вшиванням кукси аорти і екстраанатомічним шунтуванням. Реконструкції in situ забезпечують анатомічне відновлення кровопостачання в басейні інфікованого протеза (вища швидкість кровотоку, суттєво кращі показники прохідності шунтів, можливість зберегти кровотік по клубових артеріях з реваскуляризацією органів малого тазу)[3]. Відомий спосіб видалення інфікованого протеза із встановленням in situ просоченого рифампіцином протеза, запропонований Strachan та ін. в 1991 р. Використання способу забезпечує прийнятні результати (смертність - до 36%) [4]. Перевагами цього способу є анатомічність реконструкції in situ (показники прохідності шунтів - до 89% при 5-річному спостереженні, можливість зберегти кровотік по клубових артеріях з реваскуляризацією органів малого тазу), порівняно менший об'єм і тривалість оперативного втручання у зв'язку із наявністю готового просоченого рифампіцином протеза, можливість застосування у випадку розширення аорти або юкстаренального розташування проксимального анастомозу інфікованого протеза, прийнятність при виконанні оперативного втручання в ургентних умовах. Недоліками цього способу є ризик повторного інфікування (до 11%), необхідність окутування протеза сальником з метою зменшення ризику реінфікування, що збільшує тривалість і об'єм оперативного втручання, необхідність проводити бранші біфуркаційного протеза в нових тунелях з метою зменшення ризику реінфікування, що збільшує травматичність втручання, висока вартість просоченого рифампіцином біфуркаційного протеза, потреба у дуже тривалій або пожиттєвій агресивній супресивній антибіотикотерапії, погані результати у випадку масивного нагнійного процесу в позаочеревинному просторі із формуванням парааортальних абсцесів, дуже погані результати, якщо етіологічним чинником інфікування є метицилін-резистентний Staphylococcus aureus. Відомий також спосіб видалення інфікованого протеза із репротезуванням in situ кріопрезервованим аортальним алошунтом, запропонований як альтернатива до видалення інфікованого протеза із встановленням in situ просоченого рифампіцином протеза. Використання способу забезпечує 5 90410 6 прийнятні результати (смертність до 30%, втрата ваного винаходу є спосіб видалення інфікованого кінцівки - 0-5%, реінфікування - 0-9%) [5, 6]. Пересинтетичного протезу із аорто-клубово-стегновою вагами цього способу є анатомічність реконструкреконструкцією in situ аутовенами стегновоції in situ алогенним матеріалом (зокрема, висока підколінного сегменту, запропонований Clagett та швидкість кровотоку, низька ймовірність гіперплазії ін. 1993 р. як альтернативний метод лікування іннеоінтіми, сприятливіші адгезивні властивості стінфекції судинних протезів аорто-стегнової зони, ки, відповідно, суттєво кращі показники прохідності який базується на тому, що аутовенозний матеріал шунтів, кращі показники інкорпорації та реінфікудемонструє найкращу резистентність до реінфікування природного для організму реципієнта аловання, даючи одночасно можливість здійснити матеріалу із зниженими в процесі кріообробки анповноцінну реваскуляризацію шляхом створення тигенними властивостями). неоаорто-клубово-стегнової аутовенозної конструНедоліками цього способу є відсутність закокції, яка демонструє хороші показники прохідності нодавчої бази для виготовлення кріопрезервовапри тривалому спостереженні, проте потребує них алопротезів власного виробництва, необхіддодаткових затрат часу на забір аутовени і ствоність додаткових кріопрезервованих сегментів для рення неоконструкції. Виходячи із прийнятних пореконструкції, ризик кровотечі внаслідок розриву казників смертності (7-24%), порушення прохідноскріопрезервованого алошунта і неспроможності ті шунта (3,8-6%) та частоти реінфікування (2,4%), анастомозу із формуванням псевдоаневризм, що більшість спеціалістів вважають спосіб оптимальчасто призводить до смерті пацієнта (4-9%), ризик ним для лікування пацієнтів із інфікуванням протеповторного інфікування (до 9%), необхідність окузів аорто-стегнової зони [8]. тування протеза сальником з метою зменшення Суть способу - прототипу полягає у видаленні ризику реінфікування, що збільшує тривалість і інфікованого біфуркаційного алопротеза, і формуоб'єм оперативного втручання, погані результати, ванні із забраних поверхневих стегнових або веякщо етіологічним чинником інфікування є метиликих підшкірних вен біфуркаційної неоаортоцилін-резистентний Staphylococcus aureus, дуже клубово-стегнової аутовенозної конструкції, за висока вартість комерційних кріопрезервованих допомогою якої після санації ложа старого протеза алошунтів, ризик пізньої дилятації, розвитку оклюпроводять біфуркаційне аутовенозне аортозійних уражень і тромбозів кріопрезервованого бістегнове репротезування. Перевагами найближалошунта внаслідок дегенеративних змін в медії, чого аналога є анатомічність реконструкції in situ ризик передачі латентних інфекцій (віруси гепатита можливість реваскуляризації органів малого ту, ВІЛ, тощо), ризик ускладнень, пов'язаних із антазу, найкращі показники прохідності шунтів (до тигенними властивостями алошунта (Т-клітинна 100% при 5-річному спостереженні), найнижчі пореакція відторгнення). казники повторного інфікування (2-4%), можлиВідомий також спосіб видалення інфікованого вість застосування у випадку розширення аорти протеза із репротезуванням in situ посрібленим або юкстаренального розташування проксимальсинтетичним біфуркаційним шунтом. Спосіб заного анастомозу інфікованого протеза, відсутність пропонований як альтернатива до видалення інфівитрат на комерційні протези, прийнятні результакованого протеза із встановленням in situ просоти при інфікуванні метицилін-резистентним ченого рифампіцином протеза або Staphylococcus aureus та при наявності абсцесів в кріопрезервованого аортального алошунта. Викопарапротезному просторі. ристання способу забезпечує прийнятні результаНедоліками прототипу є неможливість його зати (смертність до 26%), втрата кінцівки - 0-4%, реістосування при малому діаметрі поверхневих стенфікування до 15%) [7]. Перевагами цього способу гнових вен, стоншенні стінок глибоких і підшкірних є анатомічна реконструкція in situ, можливість збевен, неможливість застосування при наявності регти кровотік по клубових артеріях з реваскуляварикозно змінених ділянок або значне збільшенризацією органів малого тазу, порівняно менший ня часу втручання для оптимізації таких вен (вшиоб'єм і тривалість оперативного втручання у зв'язвання варикозно змінених ділянок, резекція варику із наявністю готового посрібленого комерційного козно змінених ділянок із накладанням протеза, можливість застосування у випадку розанастомозів кінець в кінець, тощо), високий ризик ширення аорти або юкстаренального розташуванрозриву шунта і неспроможності місць вшивання ня проксимального анастомозу інфікованого провариксів, що призводить до кровотечі, яка, у свою теза, та при виконанні оперативного втручання в чергу, часто призводить до смерті пацієнта, особургентних умовах, тривалий антибактерійний ливо при розриві центральної бранші аутовенозної ефект внаслідок повільного вимивання іонів срібконструкції, неможливість застосування при перела. несеному раніше тромбозі глибоких вен стегновоНедоліками способу є ризик повторного інфіпідколінного сегменту, збільшення тривалості опекування, необхідність окутування протеза сальниративного втручання у зв'язку із необхідністю заком на ніжці з метою зменшення ризику реінфікубору стегнових вен і формування аутовенозної вання, що збільшує тривалість і об'єм неоконструкції. оперативного втручання, дуже висока вартість В основу винаходу поставлено завдання попосрібленого біфуркаційного протеза, потреба у ліпшити спосіб аорто-стегнової реконструкції аутотривалій антибіотикотерапії, погані результати у венами при інфікуванні синтетичного біфуркаційвипадку масивного нагнійного процесу в позаоченого протеза шляхом зміцнення бранш, що ревинному просторі із формуванням парааортальдозволить зменшити кількість інтра- та післяопених абсцесів. раційних ускладнень, зокрема, попередити розрив Найбільш близьким аналогом до запропоноаутовенозної конструкції, що, в свою чергу, змен 7 90410 8 шить ризик смерті і втрати кінцівок при інфікуванні ушивання може призвести до стенозування просинтетичного протеза аорто-стегнової зони. світу і прорізування швів, що збільшує ймовірність Поставлене завдання вирішується тим, що у розриву реконструкції. Водночас, якщо недостатспособі аорто-стегнової реконструкції аутовенами ньо ретельно вшити варикси, існує ризик дилятації при інфікуванні синтетичного біфуркаційного прошунта із подальшим розривом. Якщо наявні великі теза, що включає видалення інфікованого синтеварикси, непридатні до ушивання, їх залишають. тичного біфуркаційного протеза із репротезуванПісля підготовки двох венозних сегментів (баням аутовенами in situ, згідно з винаходом, жано однакової довжини і діаметру) їх максимальцентральну та одну із бічних бранш неоаортоно атравматично вводять один в один по всій довклубово-стегнової конструкції формують шляхом жині шляхом натягування одного венозного введення одного аутовенозного сегмента в інший сегменту на інший, дбаючи про відсутність перекпо всій його довжині з утворенням двошарового рутів по осі, після чого розправляють, ліквідують венозного сегмента. складки і адаптують краї (Фіг.1). Завдяки подвійній стінці біфуркаційна неоаорНаступним етапом проводять лапаротомію то-клубово-стегнова конструкція стійкіша до збі(поздовжню або поперечну), новокаїнову блокаду льшення внутрішньопросвітного тиску, що поперекореня брижі, розтинають задній листок очеревиджує його розрив. Особливе значення це має в ни, і проводять ревізію позаочеревинного простору аортальній позиції, де підвищення артеріального з метою виявлення гнійно-геморагічних затьоків, тиску найчастіше призводить до розривів аутовепсевдоаневризм, аорто-ентеральних або аортонозних реконструкцій, що закінчуються летально. уретральних фістул, джерел кровотечі. Після ревіЗапропонований спосіб дозволяє використозії виділяють аорту і місце проксимального анасвувати варикозно змінені вени, які часто розцінютомозу (при умові, якщо це можливо). Аорту беються як непридатні до реконструкції при застосуруть на контроль проксимальніше центрального ванні традиційної методики, що суттєво погіршує анастомозу і відсікають протез. Якщо аорта прокпрогноз при відсутності комерційних, резистентних симальніше центрального анастомозу тромбовадо інфекції, протезів, або як такі, що можуть призна, проводять тромбектомію, після чого центральвести до кровотеч з причини розриву вариксів (чаний кінець готують до накладання нового сто такі кровотечі, особливо з центральної аортаанастомозу. Інфікований протез видаляють, ложе льної бранші, призводять до летальних наслідків). протеза санують розчином повідон-йоду. Запропонований винахід ілюструється фотогПісля видалення інфікованого протеза пристурафічними зображеннями, де на Фіг. 1 відображепають до створення неоаорто-клубової аутовенозно введення однієї вени в іншу з утворенням веноної реконструкції. Краї попередньо створеного, зного сегмента з двома стінками, на Фіг.2 адаптованого по довжині, двошарового венозного фіксацію вузловими швами двох стінок вен для сегмента фіксують одне до одного шляхом наклапопередження зміщення, на Фіг.3 - вшивання бічдання поодиноких вузлових швів поліпропіленом ної аутовенозної бранші методом кінець в бік після 6/0 для попередження зміщення двох стінок двофіксації країв двошарової конструкції одиночними шарової венозної конструкції одна відносно одної вузловими швами в ділянці бічного отвору, на Фіг.4 по довжині і по осі (Фіг.2). - формування проксимального анастомозу метоПісля фіксації країв вен на боковій стінці стводом кінець в кінець між центральним кінцем аорти реного венозного сегмента скальпелем роблять і двошаровою центральною браншою аутовенозотвір наскрізь через обидві стінки. Отвір в боковій ної неоаорто-клубово-стегнової конструкції, на Фіг. стінці призначений для вшивання венозного сег5 - остаточний вигляд аутовенозної неоаортомента, який служитиме однією із стегнових бранш клубово-стегнової конструкції в позаочеревинному біфуркаційного аутовенозного шунта. Відповідно, просторі після репротезування in situ. цей отвір повинен бути достатнього діаметра для Спосіб аорто-стегнової реконструкції аутовезабезпечення нормальних гемодинамічних умов. нами при інфікуванні синтетичного біфуркаційного Для попередження зміщення, відшарування і попротеза здійснюють таким чином. легшення вшивання бічної бранші краї утвореного Пацієнта вкладають на операційний стіл в поотвору фіксують за допомогою вузлових швів із ложення на спині і обробляють операційне поле поліпропілену 6/0, після чого одиночними вузловід рівня сосків, каудально, включно із обома новими швами в отвір методом кінець в бік вшивагами на всьому протязі. Операційні доступи - повють бічну аутовенозну браншу. Анастомоз наклана поздовжня лапаротомія, поздовжні доступи на дають дуже уважно, щоб в нього попадали обидві стегнах від пупарта до коліна в проекції судинностінки двошарового венозного сегмента (Фіг.3). нервового пучка стегна. З доступів на стегнах проЦентральна і одна із бічних бранш створена із водять виділення поверхневих стегнових вен на двошарового венозного сегмента, інша бічна бравсьому протязі - від місця злиття із глибокою стегнша - одношарова, створена із великої підшкірної новою веною до переходу в підколінну. Бокові гілвени. Для виявлення затьоків між стінки двошароки ретельно перев'язують або прошивають атраввої аутовенозної біфуркаційної конструкції її перематичним поліпропіленом 6/0 або 5/0. Поверхневу віряють на герметичність гідравлічною пробою. стегнову вену відсікають, проксимальну і дистальПри наявності затьоків анастомоз додатково герну кукси двічі перев'язують або прошивають. метизують одиночними вузловими швами. Проводять повторну ревізію, гідравлічну підгоСтворену аутовенозну неоаорто-клубовотовку, остаточну герметизацію і реверсію вен. Дістегнову конструкцію вшивають в попередньо підлянки із вариксами, особливо мішкоподібними, готований кінець аорти. Анастомоз накладають ретельно ушивають, зважаючи на те, що надмірне методом кінець в кінець, особливу увагу звертаю 9 90410 10 чи на те, щоб обидва шари центральної аутовеноне виявлено. У відносно задовільному стані зної бранші потрапили в анастомоз для попере18.11.08 р. пацієнта виписано під спостереження дження затьоків і розшарування стінок неоаортохірурга за місцем проживання. клубово-стегновї конструкції. Після накладання Джерела інформації: анастомозу перевіряють його герметичність і, в 1. Stephen O'Connor, Peter Andrew, Michel Batt, разі потреби, додатково герметизують (Фіг.4). Jean Pierre Becquemin. A systematic review and Бранші біфуркаційного аутовенозного протеза meta-analysis of treatments for aortic graft infection. J виводять на стегна (бажано через нові канали для Vase Surg 2006;44:38-45. зменшення ймовірності реінфікування) і анастомо2. Gustavo S. Oderich, Thomas C. Bower, зують зі стегновими артеріями (кінець в кінець або Kenneth J. Cherry Jr., Jean M. Panneton, Timothy M. кінець в бік). При накладанні анастомозу із двошаSullivan, Audra A. Noel, Michele Carmo, Stephen ровою браншою слід проявляти уважність, щоб в Cha, Manju Kalra, Peter Gloviczki. Evolution from анастомоз попали обидві стінки бранші. Після наaxillofemoral to in situ prosthetic reconstruction for the кладання анастомозів здійснюють запуск кровотоtreatment of aortic graft infections at a single center. J ку, а при потребі - додатковий гемостаз. Після заVase Surg 2006; 43:1166-74. вершення репротезування перитонізують 3. Paul D. Hayes, Akhtar Nasim, Nicholas J. M., неоаорто-клубово-стегнову аутовенозну конструкRobert D. Sayers, William W. Barrie, Peter R.F. Bell, цію, виконують остаточний гемостаз та накладаA. Ross Naylor. In situ replacement of infected aortic ють пошарові шви на рани. grafts with rifampicin-bonded prostheses: the Клінічний приклад. Leicester experience (1992 to 1998). J Vase Surg Пацієнт Г.І.В., 54 р. (№14220), поступив у від1999;30:92-8. ділення судинної хірургії Львівської обласної ліка4. Giovanni Torsello, Wilhelm Sandmann, рні 29.10.08 р. в терміновому порядку із скаргами Andreas Gehrt, Reiner M. Jungblut. In situ на біль в лівій нозі (м'язах гомілки, стопі) в стані replacement of infected vascular prostheses with спокою та під час ходи, інтенсивного характеру, rifampin-soaked vascular grafts: early results. J Vase що погано проходив після прийому анальгетиків, Surg 1993;17:768-73. похолодіння лівої ноги, мерзлякуватість, порушен5. Audra A. Noel, Peter Gloviczki, Kenneth J. ня ходи через біль; в 2004 році виконано біфуркаCherry, Hazim San, Jerry Goldstone, Mark D. ційне алошунтування з приводу синдрому Леріша. Morasch, Kaj H. Johansen, and Members of the Ангіологічний статус: пульсація на лівій стегновій United States Cryopreserved Aortic Allograft Registry. артерії і дистальніше відсутня; справа на стеновій і Abdominal aortic reconstruction in infected fields: дистальніше відсутня. На руках пульсація задовіEarly results of the United States Cryopreserved льна, ритмічна, симетрична. Стопа і гомілка зліва Aortic Allograft Registry. J Vase Surg 2002;35:847прохолодні на дотик, блідо-мармурового кольору, 52. активні рухи збережені. Згідно з даними ультраз6. Paul R. Vogt, Hans-Peter Brunner-LaRocca, вуку біфуркаційний протез тромбований, ознаки Mario Lachat, Christian Ruef, Marko I. Turina. нагноєння, умови для оперативного лікування відTechnical details with the use of cryopreserved носно задовільні. Після дообстеження встановлеarterial allografts for aortic infection: influence on но діагноз: атеросклероз, нагноєння та тромбозearly and midterm mortality. J Vase Surg 2002;35:80біфуркаційного аорто-стегнового алошунта, оклю6. зія стегново-підколінно-гомілкового сегменту зліва, 7. M. Batt E. Jean-Baptiste, S. O'Connor, P.-J. ГІ ІА-ІБст., 06.11.08р пацієнт прооперований - виBouillanne, P. Haudebourg, R. Hassen-Khodja, S. далено нагноєний протез, виконано біфуркаційне Declemy, R. Farhad. In-situ Revascularisation for репротезування неоаорто-клубово-стегновою ауPatients with Aortic Graft Infection: A Single Centre товенозною конструкцією, центральна і одна із Experience with Silver Coated Polyester Grafts. Eur J бічних бранш якої двошарові, інша бічна бранша Vase Endovasc Surg (2008) 36, 182-188. одношарова (створені із стегнових вен і лівої ве8. Clagett GP, Bowers BL, Lopez-Viego MA, et ликої підшкірної вени відповідно). У післяопераal. Creation of a neo-aortoiliac system from lower ційному періоді реконструкція функціонує, регрес extremity deep and superficial veins. Ann Surg. ішемії, клініко-лабораторних даних про персисту1993;218:239-249. вання інфекційного процесу в позаочеревинному 11 90410 12 13 90410 14 15 Комп’ютерна верстка А. Крулевський 90410 Підписне 16 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for aorto-femoral reconstruction at infection of synthetic bifurcation prosthesis
Автори англійськоюKobza Ihor Viktorovych, Orel Yurii Hlibovych, Zhuk Rostyslav Andriiovych, Radysh Roman Vasyliovych, Fedoriv Danylo Yevhenovych, Kobza Taras Ihorovych
Назва патенту російськоюСпособ аорто-бедренной реконструкции аутовенами при инфицировании синтетического бифуркационного протеза
Автори російськоюКобза Игорь Иванович, Орел Юрий Глебович, Жук Ростислав Андреевич, Радыш Роман Васильевич, Федорив Данил Евгеньевич, Кобза Тарас Игоревич
МПК / Мітки
МПК: A61B 17/00
Мітки: синтетичного, спосіб, інфікуванні, реконструкції, аутовенами, аорто-стегнової, біфуркаційного, протеза
Код посилання
<a href="https://ua.patents.su/8-90410-sposib-aorto-stegnovo-rekonstrukci-autovenami-pri-infikuvanni-sintetichnogo-bifurkacijjnogo-proteza.html" target="_blank" rel="follow" title="База патентів України">Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза</a>
Попередній патент: Спосіб експрес-визначення віку технічної стиглості еталонних культур сосни у господарстві помірного приросту при відтворенні крупної і середньої деревини
Наступний патент: Пакер
Випадковий патент: Портативна метеорологічна станція