Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза
Номер патенту: 44591
Опубліковано: 12.10.2009
Автори: Кобза Ігор Іванович, Кобза Тарас Ігорович, Орел Юрій Глібович, Федорів Данило Євгенович, Жук Ростислав Андрійович, Радиш Роман Васильович
Формула / Реферат
Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза, що включає видалення інфікованого синтетичного біфуркаційного протеза із репротезуванням аутовенами in situ, який відрізняється тим, що центральну і одну із бічних бранш біфуркаційної неоаорто-клубово-стегнової конструкції формують шляхом введення одного аутовенозного сегмента в інший по всій його довжині з утворенням двошарового венозного сегмента.
Текст
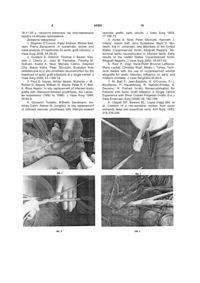
Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза, що включає видалення інфікованого синтетичного біфуркаційного протеза із репротезуванням аутовенами in situ, який відрізняється тим, що центральну і одну із бічних бранш біфуркаційної неоаорто-клубово-стегнової конструкції формують шляхом введення одного аутовенозного сегмента в інший по всій його довжині з утворенням двошарового венозного сегмента. (19) (21) u200903859 (22) 21.04.2009 (24) 12.10.2009 (46) 12.10.2009, Бюл.№ 19, 2009 р. (72) КОБЗА ІГОР ІВАНОВИЧ, ОРЕЛ ЮРІЙ ГЛІБОВИЧ, ЖУК РОСТИСЛАВ АНДРІЙОВИЧ, РАДИШ РОМАН ВАСИЛЬОВИЧ, ФЕДОРІВ ДАНИЛО ЄВГЕНОВИЧ, КОБЗА ТАРАС ІГОРОВИЧ (73) КОБЗА ІГОР ІВАНОВИЧ, ОРЕЛ ЮРІЙ ГЛІБОВИЧ, ЖУК РОСТИСЛАВ АНДРІЙОВИЧ, РАДИШ РОМАН ВАСИЛЬОВИЧ, ФЕДОРІВ ДАНИЛО ЄВГЕНОВИЧ, КОБЗА ТАРАС ІГОРОВИЧ 3 Незважаючи на досягнення хірургічної техніки, анестезіологічного забезпечення та інтенсивної терапії, результати використання цього способу (смертність від 24 до 70%) не дозволяють вважати його золотим стандартом лікування. Недоліками цього способу є також високий ризик порушення прохідності екстраанатомічних шунтів і великої ампутації (20-29%), високий ризик неспроможності кукси аорти, що переважно призводить до смерті (10-20%), високий ризик повторного інфікування аксілярно-стегнового протеза, особливо у випадках тотального інфікування протеза (10-40%), можливість розвитку ішемії тазу, органів малого тазу, висхідного тромбозу аорти та ниркової недостатності, неприйнятність у випадку розширення аорти або юкстаренального розташування проксимального анастомозу інфікованого протеза, коли немає умов для якісного вшивання кукси аорти, висока вартість армованого аксілярно-бістегнового протеза. Існують способи видалення інфікованого протеза із репротезуванням in situ, розроблені у зв'язку із незадовільними результатами тактики лікування, що включає тотальне видалення інфікованого протеза із вшиванням кукси аорти і екстраанатомічним шунтуванням. Реконструкції in situ забезпечують анатомічне відновлення кровопостачання в басейні інфікованого протеза (вища швидкість кровотоку, суттєво кращі показники прохідності шунтів, можливість зберегти кровотік по клубових артеріях з реваскуляризацією органів малого тазу) [3]. Відомий спосіб видалення інфікованого протеза із встановленням in situ просоченого рифампіцином протеза, запропонований Strachan та ін. в 1991 р. Використання способу забезпечує прийнятні результати (смертність - до 36%) [4]. Перевагами цього способу є анатомічність реконструкції in situ (показники прохідності шунтів - до 89% при 5-річному спостереженні, можливість зберегти кровотік по клубових артеріях з реваскуляризацією органів малого тазу), порівняно менший об'єм і тривалість оперативного втручання у зв'язку із наявністю готового просоченого рифампіцином протеза, можливість застосування у випадку розширення аорти або юкстаренального розташування проксимального анастомозу інфікованого протеза, прийнятність при виконанні оперативного втручання в ургентних умовах. Недоліками цього способу є ризик повторного інфікування (до 11%), необхідність окутування протеза сальником з метою зменшення ризику реінфікування, що збільшує тривалість і об'єм оперативного втручання, необхідність проводити бранші біфуркаційного протеза в нових тунелях з метою зменшення ризику реінфікування, що збільшує травматичність втручання, висока вартість просоченого рифампіцином біфуркаційного протеза, потреба у дуже тривалій або пожиттєвій агресивній супресивній антибіотикотерапії, погані результати у випадку масивного нагнійного процесу в позаочеревинному просторі із формуванням парааортальних абсцесів, дуже погані результати, якщо етіологічним чинником інфікування є метицилін-резистентний Staphylococcus aureus. 44591 4 Відомий також спосіб видалення інфікованого протеза із репротезуванням in situ кріопрезервованим аортальним алошунтом, запропонований як альтернатива до видалення інфікованого протеза із встановленням in situ просоченого рифампіцином протеза. Використання способу забезпечує прийнятні результати (смертність до 30%, втрата кінцівки - 0-5%, реінфікування - 0-9%) [5, 6]. Перевагами цього способу є анатомічність реконструкції in situ алогенним матеріалом (зокрема, висока швидкість кровотоку, низька ймовірність гіперплазії неоінтіми, сприятливіші адгезивні властивості стінки, відповідно, суттєво кращі показники прохідності шунтів, кращі показники інкорпорації та реінфікування природного для організму реципієнта аломатеріалу із зниженими в процесі кріообробки антигенними властивостями). Недоліками цього способу є відсутність законодавчої бази для виготовлення кріопрезервованих алопротезів власного виробництва, необхідність додаткових кріопрезервованих сегментів для реконструкції, ризик кровотечі внаслідок розриву кріопрезервованого алошунта і неспроможності анастомозу із формуванням псевдоаневризм, що часто призводить до смерті пацієнта (4-9%), ризик повторного інфікування (до 9%), необхідність окутування протеза сальником з метою зменшення ризику реінфікування, що збільшує тривалість і об'єм оперативного втручання, погані результати, якщо етіологічним чинником інфікування є метицилін-резистентний Staphylococcus aureus, дуже висока вартість комерційних кріопрезервованих алошунтів, ризик пізньої дилятації, розвитку оклюзійних уражень і тромбозів кріопрезервованого алошунта внаслідок дегенеративних змін в медії, ризик передачі латентних інфекцій (віруси гепатиту, ВІЛ, тощо), ризик ускладнень, пов'язаних із антигенними властивостями алошунта (Т-клітинна реакція відторгнення). Відомий також спосіб видалення інфікованого протеза із репротезуванням in situ посрібленим синтетичним біфуркаційним шунтом. Спосіб запропонований як альтернатива до видалення інфікованого протеза із встановленням in situ просоченого рифампіцином протеза або кріопрезервованого аортального алошунта. Використання способу забезпечує прийнятні результати (смертність до 26%, втрата кінцівки - 0-4%, реінфікування до 15%) [7]. Перевагами цього способу є анатомічна реконструкція in situ, можливість зберегти кровотік по клубових артеріях з реваскуляризацією органів малого тазу, порівняно менший об'єм і тривалість оперативного втручання у зв'язку із наявністю готового посрібленого комерційного протеза, можливість застосування у випадку розширення аорти або юкстаренального розташування проксимального анастомозу інфікованого протеза, та при виконанні оперативного втручання в ургентних умовах, тривалий антибактерійний ефект внаслідок повільного вимивання іонів срібла. Недоліками способу є ризик повторного інфікування, необхідність окутування протеза сальником на ніжці з метою зменшення ризику реінфікування, що збільшує тривалість і об'єм 5 оперативного втручання, дуже висока вартість посрібленого біфуркаційного протеза, потреба у тривалій антибіотикотерапії, погані результати у випадку масивного нагнійного процесу в позаочеревинному просторі із формуванням парааортальних абсцесів. Найбільш близьким аналогом до запропонованої корисної моделі є спосіб видалення інфікованого синтетичного протезу із аорто-клубовостегновою реконструкцією in situ аутовенами стегново-підколінного сегменту, запропонований Clagett та ін. 1993 р. як альтернативний метод лікування інфекції судинних протезів аортостегнової зони, який базується на тому, що аутовенозний матеріал демонструє найкращу резистентність до реінфікування, даючи одночасно можливість здійснити повноцінну реваскуляризацію шляхом створення неоаорто-клубово-стегнової аутовенозної конструкції, яка демонструє хороші показники прохідності при тривалому спостереженні, проте потребує додаткових затрат часу на забір аутовени і створення неоконструкції. Виходячи із прийнятних показників смертності (7-24%), порушення прохідності шунта (3,8-6%) та частоти реінфікування (2,4%), більшість спеціалістів вважають спосіб оптимальним для лікування пацієнтів із інфікуванням протезів аорто-стегнової зони [8]. Суть способу - прототипу полягає у видаленні інфікованого біфуркаційного алопротеза, і формуванні із забраних поверхневих стегнових або великих підшкірних вен біфуркаційної неоаортоклубово-стегнової аутовенозної конструкції, за допомогою якої після санації ложа старого протеза проводять біфуркаційне аутовенозне аортобістегнове репротезування. Перевагами найближчого аналога є анатомічність реконструкції in situ та можливість реваскуляризації органів малого тазу, найкращі показники прохідності шунтів (до 100% при 5-річному спостереженні), найнижчі показники повторного інфікування (2-4%), можливість застосування у випадку розширення аорти або юкстаренального розташування проксимального анастомозу інфікованого протеза, відсутність витрат на комерційні протези, прийнятні результати при інфікуванні метицилін-резистентним Staphylococcus aureus та при наявності абсцесів в парапротезному просторі. Недоліками прототипу є неможливість його застосування при малому діаметрі поверхневих стегнових вен, стоншенні стінок глибоких і підшкірних вен, неможливість застосування при наявності варикозно змінених ділянок або значне збільшення часу втручання для оптимізації таких вен (вшивання варикозно змінених ділянок, резекція варикозно змінених ділянок із накладанням анастомозів кінець в кінець, тощо), високий ризик розриву шунта і неспроможності місць вшивання вариксів, що призводить до кровотечі, яка, у свою чергу, часто призводить до смерті пацієнта, особливо при розриві центральної бранші аутовенозної конструкції, неможливість застосування при перенесеному раніше тромбозі глибоких вен стегновопідколіного сегменту, збільшення тривалості оперативного втручання у зв'язку із необхідністю за 44591 6 бору стегнових вен і формування аутовенозної неоконструкції. В основу корисної моделі поставлено завдання поліпшити спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза шляхом зміцнення бранш, що дозволить зменшити кількість інтра- та післяопераційних ускладнень, зокрема, попередити розрив аутовенозної конструкції, що, в свою чергу, зменшить ризик смерті і втрати кінцівок при інфікуванні синтетичного протеза аорто-стегнової зони. Поставлене завдання вирішується тим, що у способі аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза, що включає видалення інфікованого синтетичного біфуркаційного протеза із репротезуванням аутовенами in situ, згідно з корисною моделлю, центральну та одну із бічних бранш неоаорто-клубово-стегнової конструкції формують шляхом введення одного аутовенозного сегмента в інший по всій його довжині з утворенням двошарового венозного сегмента. Завдяки подвійній стінці біфуркаційна неоаорто-клубово-стегнова конструкція стійкіша до збільшення внутрішньопросвітного тиску, що попереджує його розрив. Особливе значення це має в аортальній позиції, де підвищення артеріального тиску найчастіше призводить до розривів аутовенозних реконструкцій, що закінчуються летально. Запропонований спосіб дозволяє використовувати варикозно змінені вени, які часто розцінюються як непридатні до реконструкції при застосуванні традиційної методики, що суттєво погіршує прогноз при відсутності комерційних, резистентних до інфекції, протезів, або як такі, що можуть призвести до кровотеч з причини розриву вариксів (часто такі кровотечі, особливо з центральної аортальної бранші, призводять до летальних наслідків). Запропонована корисна модель ілюструється фотографічними зображеннями, де на Фіг.1 відображено введення однієї вени в іншу з утворенням венозного сегмента з двома стінками, на Фіг.2 фіксацію вузловими швами двох стінок вен для попередження зміщення, на Фіг.3 - вшивання бічної аутовенозної бранші методом кінець в бік після фіксації країв двошарової конструкції одиночними вузловими швами в ділянці бічного отвору, на Фіг.4 - формування проксимального анастомозу методом кінець в кінець між центральним кінцем аорти і двошаровою центральною браншою аутовенозної неоаорто-клубово-стегнової конструкції, на Фіг.5 - остаточний вигляд аутовенозної неоаортоклубово-стегнової конструкції в позаочеревинному просторі після репротезування in situ. Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза здійснюють таким чином. Пацієнта вкладають на операційний стіл в положення на спині і обробляють операційне поле від рівня сосків, каудально, включно із обома ногами на всьому протязі. Операційні доступи - повна поздовжня лапаротомія, поздовжні доступи на стегнах від пупарта до коліна в проекції судиннонервового пучка стегна. З доступів на стегнах про 7 водять виділення поверхневих стегнових вен на всьому протязі - від місця злиття із глибокою стегновою веною до переходу в підколінну. Бокові гілки ретельно перев'язують або прошивають атравматичним поліпропіленом 6/0 або 5/0. Поверхневу стегнову вену відсікають, проксимальну і дистальну кукси двічі перев'язують або прошивають. Проводять повторну ревізію, гідравлічну підготовку, остаточну герметизацію і реверсію вен. Ділянки із вариксами, особливо мішкоподібними, ретельно ушивають, зважаючи на те, що надмірне ушивання може призвести до стенозування просвіту і прорізування швів, що збільшує ймовірність розриву реконструкції. Водночас, якщо недостатньо ретельно вшити варикси, існує ризик дилятації шунта із подальшим розривом. Якщо наявні великі варикси, непридатні до ушивання, їх залишають. Після підготовки двох венозних сегментів (бажано однакової довжини і діаметру) їх максимально атравматично вводять один в один по всій довжині шляхом натягування одного венозного сегменту на інший, дбаючи про відсутність перекрутів по осі, після чого розправляють, ліквідують складки і адаптують краї (Фіг.1). Наступним етапом проводять лапаротомію (поздовжню або поперечну), новокаїнову блокаду кореня брижі, розтинають задній листок очеревини, і проводять ревізію позаочеревинного простору з метою виявлення гнійно-геморагічних затьоків, псевдоаневризм, аорто-ентеральних або аортоуретральних фістул, джерел кровотечі. Після ревізії виділяють аорту і місце проксимального анастомозу (при умові, якщо це можливо). Аорту беруть на контроль проксимальніше центрального анастомозу і відсікають протез. Якщо аорта проксимальніше центрального анастомозу тромбована, проводять тромбектомію, після чого центральний кінець готують до накладання нового анастомозу. Інфікований протез видаляють, ложе протеза санують розчином повідон-йоду. Після видалення інфікованого протеза приступають до створення неоаорто-клубової аутовенозної реконструкції. Краї попередньо створеного, адаптованого по довжині, двошарового венозного сегмента фіксують одне до одного шляхом накладання поодиноких вузлових швів поліпропіленом 6/0 для попередження зміщення двох стінок двошарової венозної конструкції одна відносно одної по довжині і по осі (Фіг.2). Після фіксації країв вен на боковій стінці створеного венозного сегмента скальпелем роблять отвір наскрізь через обидві стінки. Отвір в боковій стінці призначений для вшивання венозного сегмента, який служитиме однією із стегнових бранш біфуркаційного аутовенозного шунта. Відповідно, цей отвір повинен бути достатнього діаметра для забезпечення нормальних гемодинамічних умов. Для попередження зміщення, відшарування і полегшення вшивання бічної бранші краї утвореного отвору фіксують за допомогою вузлових швів із поліпропілену 6/0, після чого одиночними вузловими швами в отвір методом кінець в бік вшивають бічну аутовенозну браншу. Анастомоз накладають дуже уважно, щоб в нього попадали обидві стінки двошарового венозного сегмента (Фіг.3). 44591 8 Центральна і одна із бічних бранш створена із двошарового венозного сегмента, інша бічна бранша - одношарова, створена із великої підшкірної вени. Для виявлення затьоків між стінки двошарової аутовенозної біфуркаційної конструкції її перевіряють на герметичність гідравлічною пробою. При наявності затьоків анастомоз додатково герметизують одиночними вузловими швами. Створену аутовенозну неоаорто-клубовостегнову конструкцію вшивають в попередньо підготований кінець аорти. Анастомоз накладають методом кінець в кінець, особливу увагу звертаючи на те, щоб обидва шари центральної аутовенозної бранші потрапили в анастомоз для попередження затьоків і розшарування стінок неоаортоклубово-стегновї конструкції. Після накладання анастомозу перевіряють його герметичність і, в разі потреби, додатково герметизують (Фіг.4). Бранші біфуркаційного аутовенозного протеза виводять на стегна (бажано через нові канали для зменшення ймовірності реінфікування) і анастомозують зі стегновими артеріями (кінець в кінець або кінець в бік). При накладанні анастомозу із двошаровою браншою слід проявляти уважність, щоб в анастомоз попали обидві стінки бранші. Після накладання анастомозів здійснюють запуск кровотоку, а при потребі - додатковий гемостаз. Після завершення репротезування перитонізують неоаорто-клубово-стегнову аутовенозну конструкцію, виконують остаточний гемостаз та накладають пошарові шви на рани. Клінічний приклад. Пацієнт Г. І. В., 54 р. (№14220), поступив у відділення судинної хірургії Львівської обласної лікарні 29.10.08 р. в терміновому порядку із скаргами на біль в лівій нозі (м'язах гомілки, стопі) в стані спокою та під час ходи, інтенсивного характеру, що погано проходив після прийому анальгетиків, похолодіння лівої ноги, мерзлякуватість, порушення ходи через біль; в 2004 році виконано біфуркаційне алошунтування з приводу синдрому Леріша. Ангіологічний статус: пульсація на лівій стегновій артерії і дистальніше відсутня; справа на стеновій і дистальніше відсутня. На руках пульсація задовільна, ритмічна, симетрична. Стопа і гомілка зліва прохолодні на дотик, блідо-мармурового кольору, активні рухи збережені. Згідно з даними ультразвуку біфуркаційний протез тромбований, ознаки нагноєння, умови для оперативного лікування відносно задовільні. Після дообстеження встановлено діагноз: атеросклероз, нагноєння та тромбоз біфуркаційного аорто-стегнового алошунта, оклюзія стегново-підколінно-гомілкового сегменту зліва, ГІ ІА-ІБст., 06.11.08 р пацієнт прооперований - видалено нагноєний протез, виконано біфуркаційне репротезування неоаорто-клубово-стегновою аутовенозною конструкцією, центральна і одна із бічних бранш якої двошарові, інша бічна бранша одношарова (створені із стегнових вен і лівої великої підшкірної вени відповідно). У післяопераційному періоді реконструкція функціонує, регрес ішемії, клініко-лабораторних даних про персистування інфекційного процесу в позаочеревинному не виявлено. У відносно задовільному стані 9 18.11.08 р. пацієнта виписано під спостереження хірурга за місцем проживання. Джерела інформації: 1. Stephen O'Connor, Peter Andrew, Michel Batt, Jean Pierre Becquemin. A systematic review and meta-analysis of treatments for aortic graft infection. J Vase Surg 2006; 44:38-45. 2. Gustavo S. Oderich, Thomas С Bower, Kenneth J. Cherry Jr., Jean M. Panneton, Timothy M. Sullivan, Audra A. Noel, Michele Carmo, Stephen Cha, Manju Kalra, Peter Gloviczki. Evolution from axillofemoral to in situ prosthetic reconstruction for the treatment of aortic graft infections at a single center. J Vase Surg 2006; 43:1166-74. 3. Paul D. Hayes, Akhtar Nasim, Nicholas J. M., Robert D. Sayers, William W. Barrie, Peter R. F. Bell, A. Ross Naylor. In situ replacement of infected aortic grafts with rifampicin-bonded prostheses: the Leicester experience (1992 to 1998). J Vase Surg 1999; 30:92-8. 4. Giovanni Torsello, Wilhelm Sandmann, Andreas Gehrt, Reiner M. Jungblut. In situ replacement of infected vascular prostheses with rifampin-soaked 44591 10 vascular grafts: early results. J Vase Surg 1993; 17:768-73. 5. Audra A. Noel, Peter Gloviczki, Kenneth J. Cherry, Hazim Safl, Jerry Goldstone, Mark D. Morasch, Kaj H. Johansen, and Members of the United States Cryopreserved Aortic Allograft Registry. Abdominal aortic reconstruction in infected fields: Early results of the United States Cryopreserved Aortic Allograft Registry. J Vase Surg 2002; 35:847-52. 6. Paul R. Vogt, Hans-Peter Brunner-LaRocca, Mario Lachat, Christian Ruef, Marko I. Turina. Technical details with the use of cryopreserved arterial allografts for aortic infection: influence on early and midterm mortality. J Vase Surg2002;35:80-6. 7. M. Batt E. Jean-Baptiste, S. O'Connor, P.-J. Bouillanne, P. Haudebourg, R. Hassen-Khodja, S. Declemy, R. Farhad. In-situ Revascularisation for Patients with Aortic Graft Infection: A Single Centre Experience with Silver Coated Polyester Grafts. Eur J Vase Endovasc Surg (2008) 36, 182-188. 8. Clagett GP, Bowers BL, Lopez-Viego MA, et al. Creation of a neo-aortoiliac system from lower extremity deep and superficial veins. Ann Surg. 1993; 218:239-249. 11 Комп’ютерна верстка А. Крижанівський 44591 Підписне 12 Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for aorto-femoral reconstruction of autologous vein in case of infection of synthetic bifurcation prosthesis
Автори англійськоюKobza Ihor Viktorovych, Orel Yurii Hlibovych, Zhuk Rostyslav Andriiovych, Radysh Roman Vasyliovych, Fedoriv Danylo Yevhenovych, Kobza Taras Ihorovych
Назва патенту російськоюСпособ аорто-бедренной реконструкции аутовенами при инфицировании синтетического бифуркационного протеза
Автори російськоюКобза Игорь Иванович, Орел Юрий Глебович, Жук Ростислав Андреевич, Радыш Роман Васильевич, Федорив Данил Евгеньевич, Кобза Тарас Игоревич
МПК / Мітки
МПК: A61B 17/00
Мітки: аутовенами, спосіб, синтетичного, реконструкції, інфікуванні, протеза, аорто-стегнової, біфуркаційного
Код посилання
<a href="https://ua.patents.su/6-44591-sposib-aorto-stegnovo-rekonstrukci-autovenami-pri-infikuvanni-sintetichnogo-bifurkacijjnogo-proteza.html" target="_blank" rel="follow" title="База патентів України">Спосіб аорто-стегнової реконструкції аутовенами при інфікуванні синтетичного біфуркаційного протеза</a>
Попередній патент: Робочий орган відвала бульдозера
Наступний патент: Спосіб приготування гранульованої насичуючої суміші
Випадковий патент: Спосіб визначення міри дефектності приповерхневих шарів монокристалів германію або кремнію