4-[етил(диметил)амоній]бутаноат та його застосування в лікуванні серцево-судинної хвороби
Номер патенту: 107201
Опубліковано: 10.12.2014
Автори: Лоза Ейнарс, Дамброва Майя, Грінберга Сольвєйга, Лієпіньш Едгарс, Кука Яніс, Калвіньш Іварс, Вілскерстс Рейніс, Пуговічс Освальдс
Формула / Реферат
1. 4-[Етил(диметил)амоній]бутаноат
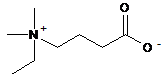 .
.
2. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють:
а) додавання етилброміду до 4-(диметиламоній)бутаноату в ацетоні з одержанням N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду;
б) обробку N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду розчином гідрооксиду калію в етиловому спирті з одержанням бажаної сполуки 4-[етил(диметил)амоній]бутаноату.
3. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють:
а) додавання калію карбонату і брометану до 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду в ацетоні з одержанням N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду;
б) пропускання N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду в присутності етилового спирту через колонку з іонообмінною смолою з одержанням 4-[етил(диметил)амоній]бутаноату.
4. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють:
а) додавання калію карбонату і дихлорметану до 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду з одержанням метил-4-(диметиламіно)бутаноату;
б) перемішування метил-4-(диметиламіно)бутаноату з брометаном в дихлорметані з одержанням N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду;
в) обробку N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду розчином калію гідроксиду в етиловому спирті з одержанням бажаної сполуки 4-[етил(диметил)амоній]бутаноату.
5. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють:
а) додавання N,N-диметилетиламіну до етил-4-бромбутаноату в дихлорметані з одержанням 4-етокси-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду;
б) пропускання 4-етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду, розчиненого у воді, через колонку з іонообмінною смолою з одержанням 4-[етил(диметил)амоній]бутаноату.
6. 4-[Етил(диметил)амоній]бутаноат для застосування як медикаменту.
7. 4-[Етил(диметил)амоній]бутаноат для застосування в лікуванні серцево-судинних хвороб.
8. Застосування 4-[етил(диметил)амоній]бутаноату для виготовлення медикаменту для лікування серцево-судинних хвороб.
9. Застосування 4-[етил(диметил)амоній]бутаноату за пунктом 8 для виготовлення медикаменту для лікування ішемічної хвороби серця.
10. Застосування за пунктом 9, де ішемічною хворобою серця є інфаркт міокарда.
Текст
Реферат: Надана сполука 4-[етил(диметил)амоній]бутаноат, спосіб її отримання і застосування в лікуванні серцево-судинної хвороби. UA 107201 C2 (12) UA 107201 C2 UA 107201 C2 Галузь техніки Даний винахід стосується нової сполуки 4-[етил(диметил)амоній]бутаноат і способу її приготування (сполуки формули 5) 5 10 15 20 25 30 35 40 45 50 55 Даний винахід стосується також застосування 4-[етил(диметил)амоній]бутаноату в лікуванні серцево-судинної хвороби. Рівень техніки Серцево-судинні хвороби (ССХ) - це група розладів серця і кровоносних судин. За оцінкою 16,7 мільйону або 29,2 % від загальної кількості смертей на нашій планеті є результатом різних форм серцево-судинної хвороби (ССХ). Інфаркт міокарду (серцевий напад) є серйозним результатом хвороби коронарних артерій. Інфаркт міокарду (ІМ) - це незворотний некроз серцевого м'язу, вторинний до тривалої ішемії. Серцевий напад або інфаркт міокарду є невідкладним медичним станом, при якому постачання крові до серця раптово і сильно зменшується або припиняється, призводячи до змертвіння м'язу через нестачу кисню. Понад 1,1 мільйону людей зазнають серцевого нападу (інфаркту міокарду) щороку, і для багатьох з них цей серцевий напад є їх першим симптомом хвороби коронарних артерій. Серцевий напад може бути достатньо тяжким, щоб викликати смерть, або він може бути мовчазним. Один з кожних п'яти людей має тільки слабкі симптоми або не має їх зовсім, і серцевий напад можна виявити тільки при рутинній електрокардіографії, виконаній через певний час. Серцевий напад (інфаркт міокарду) звичайно викликається згустком крові, який блокує артерію серця. Ця артерія часто вже є звуженою жировими відкладеннями на її стінках. Такі відкладення можуть відриватись або розриватись, зменшуючи потік крові і вивільнюючи речовини, які роблять тромбоцити крові клейкими і посилюють їх схильність утворювати згустки. Деколи згусток утворюється всередині самого серця; тоді він може відриватись і застрявати в артерії, яка постачає серце. Спазм в одній з цих артерій призводить до зупинки кровотоку. γ-Бутиробетаїн, з якого організм ссавця синтезує карнітин, спершу був охарактеризований як токсична речовина, що прискорює дихання, викликає слинотечу і сльозотечу, розширення зіниці, вазоконстрикцію і зупинку серця в діастолі LINNEWEH, W. Gamma-Butyrobetain, Crotonbetain und Carnitin im tierischen Stoffwechsel. Hoppe-Seylers Zeitschrift für physiologische Chemie. 1929, vol.181, p. 42-53. В той самий час, в більш пізніх статтях інші автори з'ясували, що токсичність γ-бутиробетаїну є дуже низькою (LD50>7000 мг/кг при підшкірному введенні) ROTZSCH, W. Iber die Toxizitat des Carnitins und einiger verwandter Stoffe. Acta biol. med. germ. 1959, vol. 3, p. 28-36. В літературі, присвяченій незаміщеному γ-бутиробетаїну, відсутні дані щодо його серцевосудинних ефектів, хоча повідомлялось (HOSEIN, Е.А. Pharmacological actions of γ-butyrobetaine. Nature. 1959, vol.183, p.328-329), що γ-бутиробетаїн є речовиною, подібною до ацетил холіну з пролонгованою дією. Однак пізніше ті самі автори повідомили, що в експерименті сталася помилка і що в дійсності холінергічними властивостями володіє не γ-бутиробетаїн, а його метиловий ефір. На противагу попередньому, γ-бутиробетаїн був охарактеризований як речовина інертна з фармакологічної точки зору (HOSEIN, E.A. Isolation and probable functions of betaine esters in brain metabolism. Nature. 1960, vol.187, p. 321-322). Сполуки, структурно споріднені з 4-[етил(диметил)амоній]бутаноатом, є описаними в: • публікації GB 1238868 А 14.07.1971, в якій йдеться про бетаїни, такі як 4триметиламоніобутаноат, використовувані для полімерів. Однак жодних фармакологічних властивостей цих бетаїнів не представлено; • патенті US 5973026 A (XEROX CORP) 26.10.1999, де йдеться про 4триметиламоніобутаноат і 3-[диетил(метил)амоніо]пропіонат для використання в композиціях чорнила; • LLOYD ANDREW, et al. A comparison of glycine, sarcosine, N, N-dimethylglycine, glycinebetaine and N-modified betaines as liposome cryoprotectants. Journal of pharmacy and pharmacology. 1992, vol. 44, no. 6, p. 507-511, де згадується 2-[етил(диметил)амоніо]ацетат, використовуваний для кріозахисту ліпосомів; 1 UA 107201 C2 5 10 15 20 25 30 35 40 45 50 55 • DAVID В., THOMAS, et al. Synthesis, Characterization, and Aqueous Solution Behavior of Electrolyte-and pH-Responsive Carboxybetaine-Containing Cyclocopolymers. Macromolecules. 2003, vol. 36, no. 26, p. 9710-9715, де йдеться про 4-[диаліл(метил)амоніо]бутаноат і його синтез, виходячи з N,N-диаліл-N-метиламонію і етил 4-бромбутаноату. Ці вільні кислоти одержуються з ефіру на другому етапі за допомогою іонообмінної смоли Амберліт. Даний продукт використовується як проміжний продукт для синтезу полімерів; • Prelog V. 1930, vol.2, p.712-722, де описано синтез 4-триметиламоніобутаноату, виходячи з 4-диметиламоніобутаноату і метилйодиду; • JP 2009096766 A (KONAN GAKUEN) 07.05.2009, де йдеться про 4-триметиламоніобутаноат і його синтез, починаючи з триметиламіну і етил 4-бромбутаноату. Вільні кислоти одержуються з ефіру на другому етапі за допомогою іонообмінної смоли Амберліт; • WO 2008/055843 A (KALVINSH IVARS; CHERNOBROVIJS ALEKSANDRS; VARACHEVA LARISA; PUGOVICHS OSVALDS) 15.05.2008, де викладені дані про 4-триметиламоніобутаноат і його синтез, який починається з відповідного ефіру і використання розчину KОН; • СА 2508094 A (VIVIER CANADA INC) 20.11.2006, де розглядаються бетаїни, такі як 4триметиламоніобутаноат, для застосування в якості медикаменту для прискорення синтезу колагену; • US 5965615 А (ТАІНО PHARMACEUTICAL CO LTD; VALSTS ZINATNISKA IESTADE BEZP) 12.10.1999, де йдеться про 4-триметиламоніобутаноат як медикамент для лікування розладу метаболізму міокарду; ту ж сполуку було описано в US 2007191381 A (CONCERT PHARMACEUTICALS INC) 16.08.2007 для лікування інфаркту міокарду. 3-(2,2,2-триметилгідразиній)пропіонат дигідрат є відомим як сполука з кардіопротекторними властивостями (ця речовина є відомою під своєю міжнародною невласною назвою Мелдоній). 3-(2,2,2-триметилгідразиній)пропіонат є описаним в патенті US 4481218 (INST ORGANICHESKOGO SINTEZA) 06.11.1984, а також в патенті US 4451485 A (INSTITU ORCH SINTEZA AKADEMII) 29.05.1984. Добре відомо, що 3-(2,2,2-триметилгідразиній)пропіонат у вигляді дигідрату широко використовується для контролю співвідношення концентрацій карнітину і гамма-бутиробетаїну і, як наслідок, швидкості бета-окислення жирних кислот в організмі (DAMBROVA М., LIEPINSH Е., KALVINSH I. I. Mildronate: cardioprotective action through camitine-lowering effect. Trends in Cardiovascular Medicine, 2002, vol. 12, no. 6, p. 275-279). Завдяки цим властивостям Мелдоній широко застосовується в медицині як антиішемічний, захищаючий від стресу і кардіопротекторний препарат в лікуванні різноманітних серцевосудинних хвороб та інших патологій, пов'язаних з ішемією тканин (KARPOV R.S., KOSHELSKAYA O.A., VRUBLEVSKY A.V., SOKOLOV A.A., TEPLYAKOV AT., SKARDA І., DZERVE V., KLINTSARE D., VITOLS Α., KALNINS U., KALVINSH I., MATVEYA L, URBANE D. Clinical Efficacy and Safety of Mildronate in Patients With Ischemic Heart Disease and Chronic Heart Failure. Kardiologiya, 2000, no. 6, p. 69-74). В лікуванні серцево-судинних хвороб механізм дії 3-(2,2,2триметилгідразиній)пропіонату базується на обмеженні швидкості біосинтезу карнітину і пов'язаному з цим обмеженні транспорту жирних кислот з довгим ланцюгом через мембрани мітохондрій (SIMKHOVICH B.Z., SHUTENKO Z.V., MEIRENA D.V., KHAGI K.B., MEZHAPUKE R.J., MOLODCHINA T.N., KALVINS I.J., LUKEVICS Е. 3-(2,2,2,-триметилгідразиній)пропіонат (ТГП) - новий інгібітор гамма-бутиробетаїну гідроксилази з кардіопротекторними властивостями. Biochemical Pharmacology. 1988, vol. 37, p. 195-202; KIRIMOTO Т., ASAKA Ν., ΝΑΚΑΝΟ Μ., TAJIMA Κ., ΜΙΥΑΚΕ Η., MATSUURA N. Сприятливі впливи МЕТ-88, інгібітору γ-бутиробетаїну гідроксилази у щурів із серцевою недостатністю після інфаркту міокарду. European Journal of Pharmacology, 2000, vol. 395, no. 3, p. 217-224). Сутність винаходу Хоча відомо, що Мелдонію дигідрат має кардіопротекторний ефект, немає жодних даних про те, що γ-бутиробетаїн сам володіє вираженим кардіопротекторним ефектом. В патенті ЕР 0845986 В (KALVINSH IVARS, VEVERIS MARIS) від 02.04.2003 року описана фармацевтична композиція з Мелдонію дигідрату і γ-бутиробетаїну для застосування в лікуванні серцевосудинних хвороб. Метою даного винаходу було запропонувати сполуку, що володіє вираженим кардіопротекторним ефектом. Поставлена мета досягається тим, що запропоновано нову сполуку 4[етил(диметил)амоній]бутаноат (сполуку формули 5), яка має структуру, подібну до Мелдонію або γ-бутиробетаїну. 60 2 UA 107201 C2 5 10 15 20 25 30 35 Неочікувано нами було виявлено, що 4-[етил(диметил)амоній]бутаноат володіє вираженим кардіопротекторним ефектом і є більш ефективним, ніж Мелдонію дигідрат, в моделях інфаркту міокарду in vivo; завдяки своїм властивостям 4-[етил(диметил)амоній]бутаноат може застосовуватись в медицині. 4-[Етил(диметил)амоній]бутаноат може використовуватись як розчин для ін'єкцій і як таблетки. Наступною метою даного винаходу є спосіб приготування вказаної сполуки формули 5. Тут описуються чотири процеси, які можуть бути використані для приготування цільової сполуки 4-[етил(диметил)амоній]бутаноат формули 5, дивись схему далі. Перший процес (Шлях А) передбачає наступні етапи: а) додавання етил броміду до 4-(диметиламоній)бутаноату для одержання N-етил-4метокси-N,N-диметил-4-оксо-1-бутанамінію броміду; б) обробка N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду гідрооксидом калію для одержання бажаної сполуки 4-[етил(диметил) амоній]бутаноату. Другий процес (Шлях В) передбачає наступні етапи: а) додавання калію карбонату і брометану до 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду для одержання N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду; б) пропускання N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду через колонку з іонообмінною смолою для одержання 4-[етил(диметил)амоній] бутаноату. Третій процес (Шлях С) передбачає наступні етапи: а) додавання калію карбонату і дихлорметану до 4-метокси-N,N-диметил-4-оксо-1бутанамінію хлориду для одержання метил-4-(диметиламіно) бутаноату; б) перемішування метил-4-(диметиламіно) бутаноату з брометаном в дихлорметані для одержання N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду; в) обробка N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду калію гідроксидом для одержання бажаної сполуки 4-[етил(диметил)амоній] бутаноату. Четвертий процес (Шлях D) передбачає наступні етапи: а) додавання N,N-диметилетиламіну до етил 4-бромбутаноату в дихлорметані для одержання 4-етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду; б) пропускання 4-етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду через колонку з іонообмінною смолою для одержання 4-[етил(диметил)амоній] бутаноату. Опис варіантів здійснення винаходу 3 UA 107201 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід буде описаний докладніше з посиланням на наступні приклади, що не є обмежуючими. СИНТЕЗ 4-[ЕТИЛ(ДИМЕТИЛ)АМОНІЙ]БУТАНОАТУ (5) Одержання 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду (3) До розчину 3-карбокси-N,N-диметил-1-пропанамінію хлориду (2) (45,93 г; 0,27 моль) в безводному метиловому спирті (300 мл) при (-10)-0 °C повільно додали тіонілу хлорид (55 мл; 0,76 моль), і одержану реакційну суміш перемішували впродовж години при температурі оточуючого середовища. Після цього реакційну суміш перемішували вже при 40-50 °C впродовж 3 годин і випарили. Залишок розчинили в ацетоні (110 мл) і виділили осад додаванням ефіру (400 мл). Тверду речовину відфільтрували, промили ефіром і ще раз розчинили в ацетоні (110 мл) з наступною преципітацією ефіром (400 мл). Преципітат відфільтрували, промили ефіром і висушили, щоб одержати 38,4 г (77 %) of 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду. 1 Н ЯМР (DMSO-d6, HMDSO) δ: 1,91 (qui, J=7,7 Гц, 2Н); 2,43 (t, J=7,74 Гц, 2Н); 2,71 (d, J=4,9 Гц, 6H); 2,98-3,06 (m, 2Н), 3,61 (s, 3Н); 10,76 (b s, 1H). Шлях А Одержання 4-[етил(диметил)амоній]бутаноат (5) Суміш 4-(диметиламоній)бутаноату (4) (7,87 г; 0,06 моль) і етил броміду (13,08 г; 0,12 моль) в безводному ацетоні (20 мл) нагрівали зі зворотним холодильником до зникнення вихідного матеріалу 4-(диметиламоній)бутаноату (ТШХ контроль, метанольний-водний гідроксид амонію, 3:1)). Реакційну суміш доповнили ізопропиловим спиртом (100 мл), і розчин випарили до сухості. До залишку додали розчин KОН (7,28 г; 0,13 моль) в 96 % етиловому спирті (70 мл) при 0 °C, і впродовж 4 годин перемішували реакційну суміш. Преципітат відфільтрували, а фільтрат обробляли 2N НСІ в метиловому спирті, доки рН середовища не становив 7-8. Реакційну суміш тримали при -18 °C впродовж 12 годин і профільтрували. Фільтрат випарили до сухості, а залишок азеотропно висушили ізопропиловим спиртом (3 × 100 мл). одержану маслянисту тверду речовину (13,4 г) розчинили в ізопропиловому спирті (100 мл) і витримали при -18 °C впродовж 12 годин. Преципітат відфільтрували, а фільтрат випарили до сухості і кристалізували з ацетону (30 мл) при -18 °C, щоб одержати 4,14 г (43 %) 4-[етил(диметил)аміак]бутаноату. 1 Н ЯМР (DMSO-d6, HMDSO) δ: 1,24 (t, J=7,3 Гц, 3H); 1,68-1,78 (m, 2H); 1,87 (t, J=6,5 Гц, 2H); + 2,96 (s, 6Н); 3,16-3,23 (m, 2Н); 3,29 (q, J=7,3 Гц, 2H). РХ IEP-MC (m/z): 160 [М+Н] . Аналітичний розрахунок для C8H17NO2·1,3 Н2О: С 52,61; Η 10,82; Ν 7,67. Знайшлось: С 52,64; Η 11,00; Ν 7,58 Шлях В Приготування N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду (6а) Суміш 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду (3) (7,27 г; 0,04 моль), безводного K2СО3 (5,52 г; 0,04 моль) і брометану (4,48 мл; 0,06 моль) в ацетоні (40 мл) енергійно перемішували при температурі оточуючого середовища впродовж 2 днів. Осад відфільтрували, промили ацетоном, суспендували в ізопропиловому спирті (100 мл) і енергійно перемішували при температурі оточуючого середовища впродовж 2 годин. Суміш профільтрували, фільтрат випарили до сухості і азеотропно висушили кілька разів ізопропиловим спиртом. Залишок кристалізували з ацетону (10 мл) додаванням етилацетату (35 мл) і висушили над Р2О5 in vacuo, щоб одержати 6,51 г (64 %) N-етил-4-метокси-N,Nдиметил-4-оксо-1-бутанамінію броміду. 1 Н ЯМР (CDCI3, HMDSO) δ: 1,44 (t, J=7,2 Гц, 3Н); 2,01-2,12 (m, 2H); 2,55 (t, J=6,6 Гц, 2H); 3,40 (s, 6H); 3,66-3,73 (m, 4H); 3,69 (s, 3Н). + PX IEP-MC (m/z): 174 [M+H] . Аналітичний розрахунок для C9H20BrNO2·0,09 Н2О: С 42,26; Η 7,95; Ν 5,48. Знайшлось: С 42,26; Η 8,28; Ν 5,35. Приготування 4-[етил(диметил)амоній]бутаноату (5) Розчин N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду (6а) (6,51 г; 0,025 моль) в етиловому спирті (20 мл) пропустили через колонку з іонообмінною смолою Amberlite® IRA410 (ОН) (190 мл), повільно вимиваючи його етиловим спиртом (100 мл). Елюат випарили до сухості, а залишок кілька разів азеотропно висушили ізопропиловим спиртом, після чого розчинили в ізопропиловому спирті (50 мл) і витримали при 0 °C впродовж 12 годин. Суміш профільтрували і фільтрат випарили. Залишок (7,35 г) змішали зхолодним етилацетатом і витримали при 0 °C впродовж 12 годин. Суміш профільтрували, а осад висушили над Р2О5 in vacuo, щоб одержати 3,54 г (86 %) 4-[етил(диметил)амоній]бутаноату. Чистоту матеріалу було підвищено шляхом пропускання водного розчину 4-[етил(диметил)амоній] бутаноату через іонообмінну смолу DOWEX® 50WX8. Розчин випарили до сухості; залишок азеотропно 4 UA 107201 C2 5 10 15 20 25 30 35 40 45 50 55 60 висушили ізопропиловим спиртом з наступною сушкою in vacuo над Ρ2Ο5, щоб одержати 1,27 г (31 %) 4-[етил(диметил)амоній]бутаноату. Шлях С Приготування метил 4-(диметиламіно)бутаноату (7) Суспензію 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду (3) (5,44 г; 0,03 моль) і безводного K2СО3 (5,52 г; 0,04 моль) в дихлорметані (70 мл) енергійно перемішували при температурі оточуючого середовища впродовж 24 годин. Осад відфільтрували, промили дихлорметаном, а фільтрат випарили. Залишок перегнали при 32-35 °C / 3-4 мм Hg, щоб одержати 2,88 г (66 %) 4-(диметиламіно)бутаноату. 1 Н ЯМР (DMSO-d6, HMDSO) δ: 1,64 (qui, J=7,2 Гц, 2Н); 2,09 (s, 6H); 2,17 (t, J=7,1 Гц, 2H); 2,30 (t, J=7,4 Гц, 2H); 3,57 (s, 3H). Приготування N-етил-4-метокси-N,N-диметил-4-оксо-1 -бутанамінію броміду (6а) Суміш метил 4-(диметиламіно)бутаноату (7) (1,45 г; 10 ммоль) і брометану (1,2 мл; 16 ммоль) в дихлорметані (15 мл) перемішували при температурі оточуючого середовища. Реакційну суміш випарили до сухості, білу тверду речовину (2,438 г) розтерли з ацетоном, відфільтрували і висушили in vacuo над Р2О5, щоб одержати 2,397 г (94 %) N-етил-4-метоксиN,N-диметил-4-оксо-1-бутанамінію броміду. Шлях D Приготування 4-етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду (6b) До розчину етил 4-бромбутаноату (8) (19,5 г; 0,1 моль) в дихлорметані при температурі льодяної ванни додали N,N-диметилетиламін (10,8 мл; 0,1 моль) і перемішували впродовж ночі при температурі оточуючого середовища. Реакційну суміш випарили до сухості, залишок розтерли з ацетоном (50 мл) і витримали при 0 °C 0,5 години. Осад відфільтрували і висушили in vacuo над Р2О5, щоб одержати 22,274 г (94 %) 4-етоксі-N-етил-N,N-диметил-4-оксо-1бутанамінію броміду. 1 Н ЯМР (CDCI3, HMDSO) δ: 1,26 (t, J=7,2 Гц, 3H); 1,44 (t, J=7,4 Гц, 3H); 2,00-2,11 (m, 2H); 2,52 (t, J=6,6 Гц, 2H); 3,40 (s, 6H); 3,64-3,73 (m, 2H); 3,69 (q, J=7,4 Гц, 2Н); 4,14 (q, J=7,2 Гц, 2Н). Приготування 4-[етил(диметил)амоній]бутаноату (5) Розчин 4-етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду (6b) (12,00 г; 44,7 ммоль) у воді (10 мл) пропустили через колонку з іонообмінною смолою Amberlite® IRA-410 (ОН) (250 мл), повільно вимиваючи (са. 10 крапель/хв.) етиловим спиртом (ТШХ контроль). Елюат випарили, а залишок (12 г) розчинили у воді (50 мл). До цього розчину додали іонообмінну смолу DOWEX® 50WX8 (5 г) was added і перемішували при температурі оточуючого середовища 0,5 години. Реакційну суміш профільтрували через целіт (1 см), і елюат випарили до сухості. Залишок азеотропно висушили ізопропиловим спиртом, ацетонітрилом і ацетоном, одержану тверду речовину розтерли з ацетоном (10 мл), і витримали суміш при 0 °C впродовж 2 годин. Осад відфільтрували і висушили in vacuo над Р2О5, щоб одержати 4,65 г (65 %) 4[етил(диметил)аміак]бутаноату. 1 Н ЯМР (DMSO-d6, HMDSO) δ: 1,24 (t, J=7,3 Гц, 3H); 1,66-1,76 (m, 2H); 1,81 (t, J=6,4 Гц, 2H); + 2,95 (s, 6Н); 3,16-3,23 (m, 2Н); 3,29 (q, J=7,3 Гц, 2H). РХ IEP-MC (m/z): 160 [М+Н] . Аналітичний розрахунок для C8Hi7NO2·1,55 Н2О: С 51,34; Η 10,82; Ν 7,48. Знайшлось: С 51,36; Η 11,40; Ν 7.34. Кардіопротекторна активність П'ятдесят самців, 10-тижневих щурів Wistar вагою 200-250 г утримувались в стандартних умовах (21-23 °C, 12-годинний цикл світла-темряви) з необмеженим доступом до корму (раціон R3, Lactamin AB, Швеція) і води. Щурі адаптувались до місцевих умов впродовж двох тижнів до початку обробки. Мелдонію дигідрат в дозі 5 мг/кг або 100 мг/кг, гамма-бутиробетаїн в дозі 5 мг/кг і EG в дозі 20 мг/кг вводились р.о. щоденно впродовж 8 тижнів. Контрольні щурі одержували воду. Дослідження інфаркту на ізольованому серці щура Експеримент на ізольованому серці щура здійснювався суттєво так, як описувалось раніше (Liepinsh et al., J. Cardiovasc. Pharmacol. 2006; 48(6):314-9). Через 24 години після останнього введення препарату серця висікались і підтримувались в умовах ретроградної перфузії через аорту при постійному тиску оксигенованим буфером Krebs-Henseleit при 37 °C. Частота скорочень серця, тиск в лівому шлуночку в кінці діастоли і тиск, розвинутий в лівому шлуночку, постійно реєструвались. Коронарний кровоток оцінювався за допомогою ультразвукового потокового детектору (HSE) і системи PowerLab 8 /ЗО від ADInstruments. Серця знаходились в стані перфузії 20 хвилин, щоб стабілізувати гемодинамічні функції, після чого стисненням пластикової трубки нитками здійснювали оклюзію на 60 хвилин. Достатність оклюзії підтверджувалась зменшенням коронарного кровотоку приблизно на 40 відсотків. Реперфузія 5 UA 107201 C2 5 10 15 20 досягалась відпусканням ниток. В кінці 150-хвилинного періоду реперфузії 0,1 % метиленовим синім виділяли зону ризику. Потім серця розтинали в поперечному напрямку від верхівки до основи на п'ять зрізів 2-мм товщини і інкубували в 1 % трифенілтетразолію хлориді в фосфатному буфері (рН 7,4; 37 °C) 10 хвилин, щоб зафарбувати життєздатну тканину червоним, а некротичну - білим. Комп'ютеризований планіметричний аналіз фотографій Sony A900 був здійснений з використанням програмного забезпечення Image-Pro Plus 6.3 для визначення площі ризику і площі некрозу, виражених як % площі лівого шлуночка, одержані цифри були потім використані для обчислення розміру інфаркту (РІ) як % від площі ризику за наступною формулою: Розмір інфаркту = Площа некрозу/Площа ризику × 100 %. Результати дослідження інфаркту на ізольованому серці щура Анти-інфарктний ефект досліджуваних речовин аналізувався на моделі інфаркту на ізольованому серці щура. Під час оклюзії лівої коронарної артерії коронарний потік у всіх експериментальних групах зменшувався на 40 % (з 11 мл/хв. до 7 мл/хв.). Більше того, спостерігалось падіння тиску, розвинутого в лівому шлуночку, на 50 %. Частота серцевих скорочень під час періоду оклюзії суттєво не змінювалась. На етапі реперфузії коронарний потік, розвинутий в лівому шлуночку тиск, величини ±dp/dt відновлювались приблизно до 80 % контрольного рівня. Достовірної різниці між контрольною і експериментальними групами не спостерігалось. Ефекти Мелдонію дигідрату (5 мг/кг і 100 мг/кг), гамма-бутиробетаїну (5 мг/кг) і 4[етил(диметил)амоній]бутаноату (EG) (5 мг/кг) після 2 обробки на розмір інфаркту на моделі інфаркту на ізольованому серці щура представлені в Таблиці 1. Таблиця 1 Вплив Мелдонію дигідрату, гамма-бутиробетаїну і EG на розмір інфаркту Розмір інфаркту, % від контролю 100,0±5 95±9 76±10* 90±5 59±6* Контроль Мелдонію дигідрат 5 мг/кг Мелдонію дигідрат 100 мг/кг Гамма-бутиробетаїн 5 мг/кг EG 5 мг/кг Кожне значення представляє собою середню величину ± стандартна похибка середньої величини для 9-10 тварин. *Достовірно відрізняється від контрольної групи (t-тест Ρ < 0,05). 25 Як видно з Таблиці 1, обробка Мелдонію дигідратом в дозі 5 мг/кг зменшила розмір інфаркту на 5 %, терапевтична активність Мелдонію дигідрату спостерігалась тільки при 100 мг/кг, коли розмір інфаркту зменшився на 24 %. Гамма-бутиробетаїн в дозі 5 мг/кг не мав жодного терапевтичного ефекту. 4-[Етил(диметил)амоній]бутаноат в дозі 5 мг/кг продемонстрував найкращий терапевтичний ефект, зменшивши розмір інфаркту на 41 %. 30 ФОРМУЛА ВИНАХОДУ 1. 4-[Етил(диметил)амоній]бутаноат O N+ 35 40 O . 2. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють: а) додавання етилброміду до 4-(диметиламоній)бутаноату в ацетоні з одержанням N-етил-4метокси-N,N-диметил-4-оксо-1-бутанамінію броміду; б) обробку N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду розчином гідрооксиду калію в етиловому спирті з одержанням бажаної сполуки 4-[етил(диметил)амоній]бутаноату. 3. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють: а) додавання калію карбонату і брометану до 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду в ацетоні з одержанням N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду; 6 UA 107201 C2 5 10 15 20 б) пропускання N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду в присутності етилового спирту через колонку з іонообмінною смолою з одержанням 4[етил(диметил)амоній]бутаноату. 4. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють: а) додавання калію карбонату і дихлорметану до 4-метокси-N,N-диметил-4-оксо-1-бутанамінію хлориду з одержанням метил-4-(диметиламіно)бутаноату; б) перемішування метил-4-(диметиламіно)бутаноату з брометаном в дихлорметані з одержанням N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду; в) обробку N-етил-4-метокси-N,N-диметил-4-оксо-1-бутанамінію броміду розчином калію гідроксиду в етиловому спирті з одержанням бажаної сполуки 4[етил(диметил)амоній]бутаноату. 5. Процес одержання 4-[етил(диметил)амоній]бутаноату, в якому здійснюють: а) додавання N,N-диметилетиламіну до етил-4-бромбутаноату в дихлорметані з одержанням 4етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду; б) пропускання 4-етоксі-N-етил-N,N-диметил-4-оксо-1-бутанамінію броміду, розчиненого у воді, через колонку з іонообмінною смолою з одержанням 4-[етил(диметил)амоній]бутаноату. 6. 4-[Етил(диметил)амоній]бутаноат для застосування як медикаменту. 7. 4-[Етил(диметил)амоній]бутаноат для застосування в лікуванні серцево-судинних хвороб. 8. Застосування 4-[етил(диметил)амоній]бутаноату для виготовлення медикаменту для лікування серцево-судинних хвороб. 9. Застосування 4-[етил(диметил)амоній]бутаноату за пунктом 8 для виготовлення медикаменту для лікування ішемічної хвороби серця. 10. Застосування за пунктом 9, де ішемічною хворобою серця є інфаркт міокарда. Комп’ютерна верстка Л. Ціхановська Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 7
ДивитисяДодаткова інформація
Автори англійськоюKalvins, Ivars, Dambrova, Maija, Liepins, Edgars, Pugovics, Osvalds, Vilskersts, Reinis, Kuka, Janis, Grinberga, Solveiga, Loza, Einars
Автори російськоюКальвиньш Иварс, Дамброва Майя, Лиепиньш Едгарс, Пуговичс Освальдс, Вилскерстс Рейнис, Кука Янис, Гринберга Сольвейга, Лоза Ейнарс
МПК / Мітки
МПК: A61P 9/10, A61K 31/14, C07C 229/12
Мітки: хвороби, серцево-судинної, 4-[етил(диметил)амоній]бутаноат, застосування, лікуванні
Код посилання
<a href="https://ua.patents.su/9-107201-4-etildimetilamonijjbutanoat-ta-jjogo-zastosuvannya-v-likuvanni-sercevo-sudinno-khvorobi.html" target="_blank" rel="follow" title="База патентів України">4-[етил(диметил)амоній]бутаноат та його застосування в лікуванні серцево-судинної хвороби</a>












