Нікелевмісний каталізатор для три-риформінгу метану
Номер патенту: 108461
Опубліковано: 25.07.2016
Автори: Курилець Ярослава Петрівна, Губарені Євген Віталійович, Соловйов Сергій Олександрович, Орлик Світлана Микитівна
Формула / Реферат
1. Нікелевмісний каталізатор для три-риформінгу метану, нанесений на носій, який відрізняється тим, що як носій використовується кордієрит та каталізатор додатково містить оксид алюмінію та оксид лантану або оксид церію, при наступному співвідношенні компонентів у мас.%:
NiO
4-6
Аl2О3
4-6
Lа2О3(СеО2)
0,5-1,5
кордієрит
решта.
2. Нікелевмісний каталізатор за п. 1, який відрізняється тим, що кордієрит має коміркову структуру.
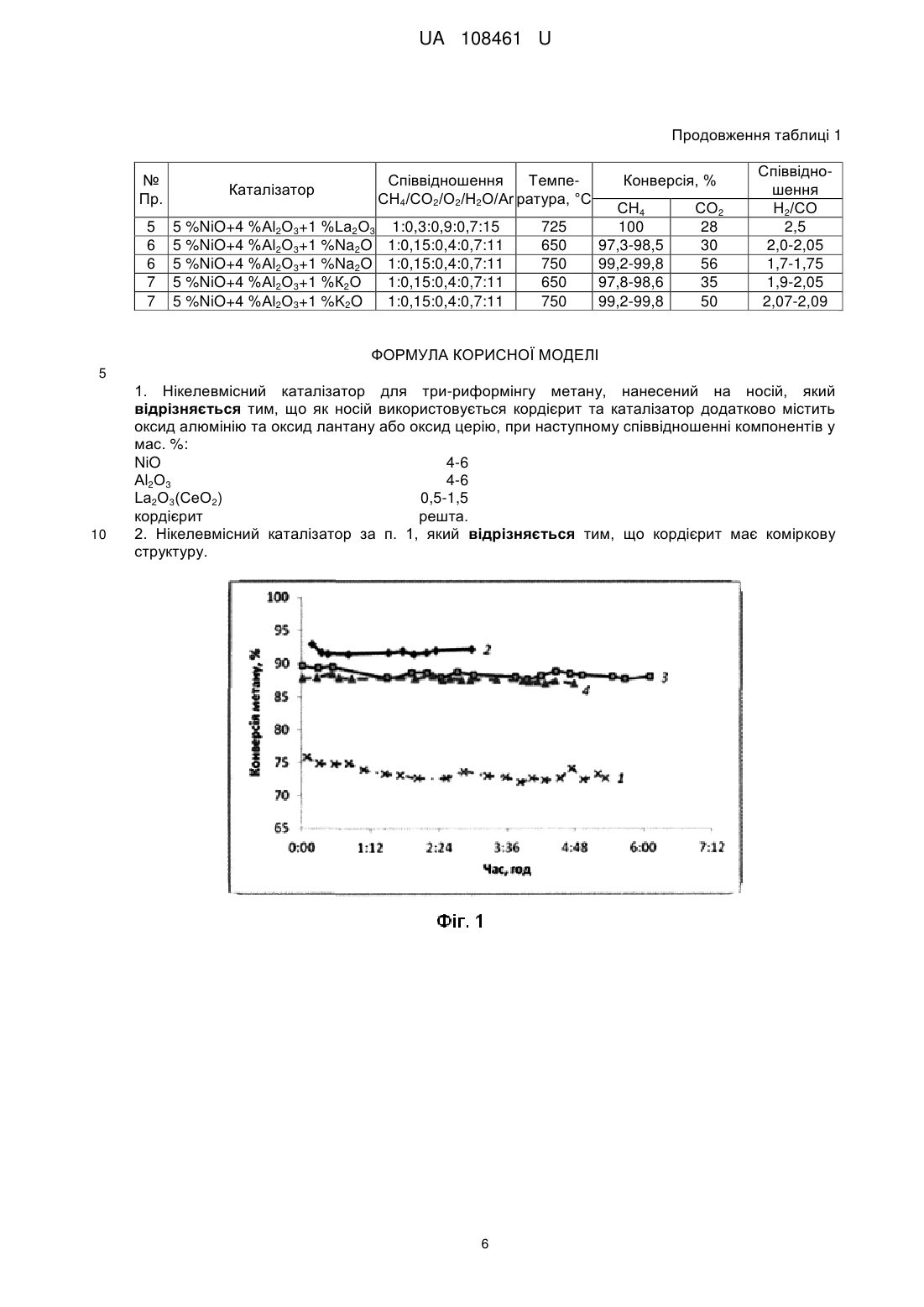
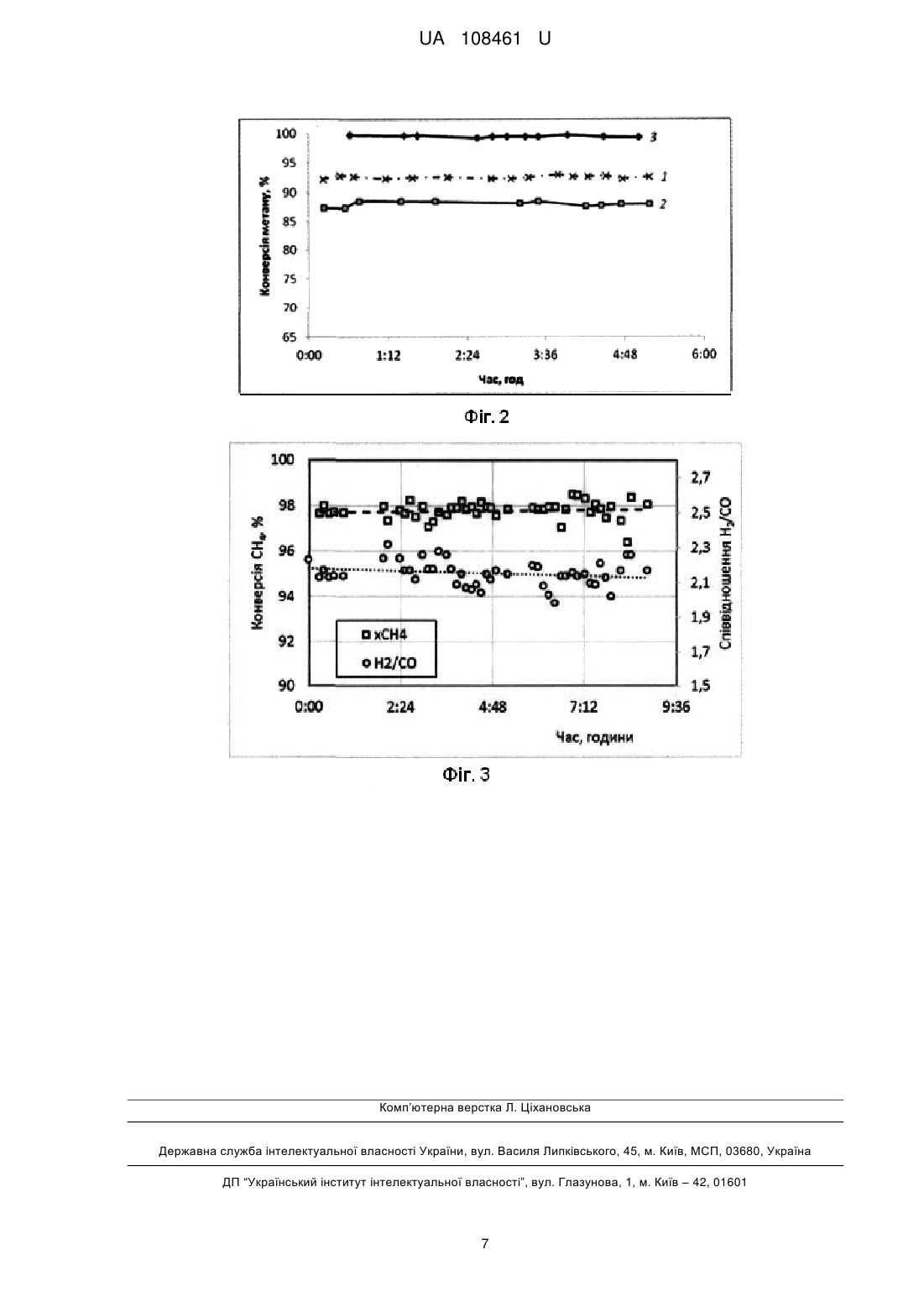
Текст
Реферат: Описується нікелевмісний каталізатор для три-риформінгу метану, нанесений на носій, в якому як носій використовується кордієрит та каталізатор додатково містить оксид алюмінію та оксид лантану або оксид церію. UA 108461 U (54) НІКЕЛЕВМІСНИЙ КАТАЛІЗАТОР ДЛЯ ТРИ-РИФОРМІНГУ МЕТАНУ UA 108461 U UA 108461 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель належить до нікелевмісних каталізаторів конверсії легких вуглеводнів (зокрема метану) у монооксид вуглецю та водень за участі різних окисників: діоксиду вуглецю, водяної пари та кисню. Рівень техніки Зазвичай для отримання синтез-газу та водню з вуглеводнів використовують водяну пару, діоксид вуглецю або їхню суміш. При цьому для кожного окисника розроблені свої каталітичні системи. Типовими процесами отримання синтез-газу з метану є паровий риформінг, вуглекислотний, парціальне окиснення та автотермічний риформінг з використанням декількох окисників. Паровий риформінг метану проходить за Схемою 1, в якості каталізаторів зазвичай використовують нікелевмісні каталітичні системи. Схема 1. СН4 + Н2О = CO+3H2, dH°298 = +206 кДж/моль. Дезактивація каталізатора, яка відбувається через завуглецювання каталізатора, є суттєвою проблемою парового риформінгу. В промисловості її вирішують за рахунок великого надлишку водяної пари над метаном (2,5-3 рази), що ускладнює технологічний процес та збільшує собівартість продукту та не дозволяє варіювати співвідношенням Н 2:СО, що значно обмежує можливості використання синтез-газу. Вирішити проблему завуглецювання намагаються варіюванням складу каталізатора. Підвищену стійкість до завуглецювання, в порівнянні з традиційним нікелевим каталізатором, задекларовано у патенті US4026823 для нікелевмісного каталізатора, нанесеного на оксид цирконію з додаванням кобальту. Автори пов'язують підвищену стійкість до утворення вуглецю синергічним ефектом нікелю і кобальту, нанесених на оксид цирконію, який не утворює шпінель з оксидами перехідних металів. В патентах US4297205 та US4240934 описані каталізатори для риформінгу вуглеводнів на основі іридію, нанесеного на оксиди цирконію та алюмінію. Вуглекислотна конверсія метану відбувається за Схемою 2. Зазвичай реалізують на нікелевмісних каталізаторах та каталізаторах на основі благородних металів. Схема 2. СН4 + СО2=2СО + 2Н2, dH°298 = +247,3 кДж/моль Синтез-газ з високим вмістом монооксиду вуглецю можна отримати у процесі вуглекислотного риформінгу метану. Отриманий синтез-газ може бути використаний для синтезу диметилового ефіру. Проте через суттєве завуглецювання каталізатора для стабільної роботи у процесі вуглекислотного риформінгу використовують каталізатори на основі дорогих благородних металів. Наприклад, в патенті US5068057 описано каталізатори Pt/Аl 2О3 та Pd/Аl2О3. В заявці WO 92/11199 зазначено, що каталізатори на основі таких благородних металів як іридій, родій та рутеній, нанесені на оксид алюмінію мають дуже високу активність та стабільність роботи. Проте, поряд зі своєю високою активністю та стійкістю до відкладення вуглецю, каталізатори на основі благородних металів є надто дорогими для використання у промислових масштабах, порівнюючи з нікелевмісними каталізаторами. Численні дослідження були присвячені пошуку більш дешевих нікелевмісних каталізаторів з достатньою активністю та стабільністю роботу у процесі вуглекислотної конверсії вуглеводнів. В японській патентній заявці №11-276893 описується процес вуглекислотного риформінгу алканів в присутності каталізатора на основі гідротальциту з нанесеними благородними металами (Rh, Pd, Ru) та перехідними металами (Ni) як співактивного компонента. Проте, незважаючи на вищу ніж 90 % при 800 °C конверсію метану, активність каталізатора помітно падає при зниженні температури і складає менше 30 % при 600 °C і лише каталізатор, що містить 5 % Rh показує конверсію метану 50 % при 600 °C. Парціальне окислення метану відбувається за Схемою 3. Цей процес, що дозволяє отримувати синтез-газ, збагачений воднем, важко реалізувати через швидке окислення каталізатора, що призводить до перебігу глибокого окислення метану за Схемою 4. Схема 3. СН4+1/2О2 = СО + 2Н2, dH°298 = - 35,6 кДж/моль Схема 4. СН4 + О2 = СО2+2Н2О, dH°298 = - 880 кДж/моль Три-риформінг метану (комбінація парового, вуглекислотного риформінгу та парціального окислення в одному реакторі на одному каталізаторі) проводиться за Схемою 5. Цей процес дозволяє отримувати синтез-газ зі співвідношенням Н2/СО у межах від 1 до 2, використовуючи як окислювач суміш діоксиду вуглецю, кисню та водяної пари. Це реакція може бути 1 UA 108461 U 5 10 15 20 25 30 35 40 45 50 55 використана у промисловості для отримання дешевого синтез-газу, утворення вуглецю при цьому інгібується присутністю окисників з високою реакційною здатністю - молекулярного кисню. Схема 5. 4СН4 + СO2 + Н2O+O2=5СO+5Н2. Раніше в літературі запропоновано процес три-риформінгу метану [С. Song, W. Pan, Catal. Today 98 (2004) 46] як технології утилізації діоксиду вуглецю та зменшення його викидів. Нажаль при реалізації три-риформінгу на промислових каталізаторах ІСІ, хоча при цьому і досягалася 65 % конверсія СО2 та 90 % конверсія метану, молярне співвідношення Н2/СО складало 1,5-2,2. В роботі роботі [S. Н. Lee, W. С. Cho, W. S. Ju, B. H. Cho, Y. С Lee, Y. S. Baek, Catal. Today 84 (2003) 133] в присутності Ni/CeiZrO 2 в процесі три-риформінгу досягались конверсії 85 % та 95 % для СО2 та метану, відповідно; молярне співвідношення Н2/СО складало 1-1,8. В заявці US2008/0260628 описані нікелевмісні каталізатори для отримання синтез-газу шляхом три-риформінгу метану в присутності нікель-цирконієвих каталізаторів, доповнених оксидом ітрію, лантану та/або лужноземельними елементами. В заявці вказано, що додавання ітрію у склад нікель-цирконієвих каталізаторів спотворює кристалічну ґратку оксиду цирконію, підвищуючи кількість рухомого кисню кристалічної ґратки та підвищує його рухливість, за рахунок чого зменшується накопичення вуглецю на кристалітах нікелю, підвищуючи активність та селективність каталізатора. Нанесені нікелеві каталізатори є досить важливими у промисловості, оскільки широко використовуються в процесах риформінгу, гідрування, метанування завдяки високій активності нікелю у їх складі. Зокрема, нанесені нікелеві каталізатори використовуються у паровому риформінгу природного газу, нафти та рідких палив з отриманням синтез-газу, що є основною початковою ланкою у С1-синтезах. З синтез-газу отримують метанол, діетиловий етер та інші кисеньвмісні продукти; також використовують для синтезу аміаку. Типовими способами приготування нанесених каталізаторів є співосадження, нанесення, іонний обмін, золь-гель, аерогель. Нікелеві каталізатори, отримані різними способами, мають відмінні властивості. Прототипом нашої розробки є описаний в заявці US2008/0260628 каталізатор Ni/(8Y, ZrO2,CeO2), в присутності якого реалізовано процес три-риформінгу метану при температурах -1 650-850° С, тиску 0,5-10 атмосфер та об'ємній швидкості 1000-300000 год. . Молярне співвідношення діоксиду вуглецю, кисню та водяної пари до метану складало 0,5-2,0 моль, 0,051,0 моль та 0,5-2,0 моль, відповідно. Падіння активності каталізатора не відбувалось після 430 -1 годин при роботі з об'ємною швидкістю 10000 год. температурі 800 °C та складі реакційної суміші СH4:O2:CO2:H2O=1:0,1:1:1. Проте на даному каталізаторі отримано синтез-газ зі співвідношенням Н2/СО в діапазоні 0,5-2,0. Також дослідження стабільності роботи проведене за умов, що зменшують ймовірність накопичення вуглецю: суттєвого надлишку окисників та невеликого вмісту кисню. З попереднього опису випливає, що існуючі каталізатори не дають можливості отримувати синтез-газ з необхідним співвідношенням H2/СО у процесі три-риформінгу. Також неможливо оцінити їх стійкість до накопичення вуглецю або окислення киснем за вмісту кисню вище, ніж за співвідношення СH4:O2:CO2:H2O=1:0,1:1:1. Нами неочікувано було встановлено, що в присутності нікель-алюмінієвих структурованих каталізаторів, нанесених на кордієрит, модифікованих оксидами рідкісноземельних або лужних елементів, у процесі три-риформінгу метану можливо отримувати синтез-газ зі співвідношенням -1 H2/СО в діапазоні 0,5-2,5 з об'ємною швидкістю 12000 год. без втрати активності каталізатора через завуглецювання, або окислення металевого нікелю під дією кисню в температурному діапазоні 650-800 °C. Задачею корисної моделі є нікелевмісний каталізатор для три-риформінгу метану, нанесений на носій, в якому як носій використовується кордієрит та каталізатор додатково містить оксид алюмінію та оксид лантану або оксид церію, при наступному співвідношення компонентів у мас. %: NiO 4-6 Аl2О3 4-6 La2O3(CeO2) 0,5-1,5 кордієрит решта. Варіантом реалізації корисної моделі є кордієрит, що має коміркову структуру. Корисна модель описується далі докладно з посиланням на численні варіанти здійснення тільки для цілей пояснення на прикладах і ілюстрації, а також з посиланням на наступні креслення, де 2 UA 108461 U 5 10 15 20 на Фіг. 1 показана зміна конверсії метану в процесі ТРМ з часом в присутності каталізатора 4,7 %NiO+3,8 %Al2O3+0,8 %K2O при складі початкової газової суміші (в об'ємних відсотках) СH4:O2:CO2:H2O: (1) 6,2:1,3:4,5:4,2; (2) 6,2:1,5:4,4:4,2; (3) 6,3:1,5:3,1:3,1; (4) 6,6:1,2:3,4:3,1, та температурах (1) 550°, (2-4) 610 °C; на Фіг. 2 показана зміна конверсії метану в процесі ТРМ з часом в присутності каталізаторів (1) 4,7 %NiО+3,8 %АІ2О3+0,8 %К2О, (2) 5,1 %NiO+4,1 %Al2O3+0,9 %CeO2, (3) 5,2 %NiO+4 %Al2O3+2,1 %CeO2 при температурах 610 °C (1, 2) та 705 °C (3) та складі початкової газової суміші (в об'ємних концентраціях) СH4:O2:CO2:H2O: (1) 6,5:2,6:4,3:4,2; (2) 6,2:2,2:2,5:3,1; (3) 5,9:2,8:3,5:3,1; на Фіг. 3 показана зміна показників процесу три-риформінгу метану в часі в присутності каталізатора 5,8 %NiO+4,65 %Al2O3+1,15 %La2O3. Температура 625 °C, Реакційна суміш: 5,6 % -1 СН4, 1,7 %О2. 2,0 % СО2, 2,8 % Н2О. Об'ємна швидкість 1200 год. . Модифікації конкретних варіантів здійснення, які визначаються формулою, будуть очевидними для спеціалістів в цій галузі. Якщо далі не буде визначатись більш конкретно, використовувана тут термінологія має своє звичайне значення. Мольний відсоток (моль % або %) і подібні терміни стосуються саме мольного відсотку, коли інше не вказується. Масовий відсоток (мас. % або %) і подібні терміни стосуються саме масового відсотку, коли інше не вказується. "Перетворення" виражається як відсоток початкового компонента, що прореагував. Перетворення СЩ обчислюється за даними газової хроматографії (ГХ) з використанням наступного рівняння: перетворення СН 4 (%) 100 ммоль СН 4 на вході (потік сировини) ммоль СН 4 на виході () ммоль СН 4 на вході (потік сировини) . 25 30 35 40 45 50 55 Масовий відсоток каталітичного металу визначається за масою металу і загальною сухою масою металу і підкладки. Три-риформінг метану досліджували з використанням проточної установки. Для дослідження каталітичної активності з каталітичного блока, приготованого в Прикладах приготування А-Е, вирізали фрагмент у вигляді циліндра діаметром 7 мм і висотою 12 мм, вага якого складала 0,5 г. Каталітичний фрагмент розташовували в кварцовому реакторі проточного типу таким чином, щоб уникнути байпасу газового потоку поза каталізатором. Перед початком каталізатор відновлювали в реакторі газовою сумішшю, яка містила 4 % молярних Н2 та 96 % молярних Аr при температурі 750 °C протягом 2 год., після чого охолоджували у до температури досліду. Швидкість газового потоку відновлювальної суміші складала 50 мл/хв. Приклади Нижче описані приклади, які більш точно описують корисну модель. Приклади наведені лише для ілюстрації та не обмежують границі дії корисної моделі. Приклад А Приготування 5 мас. % NiO і 4 мас. % Аl2О3 на кордієриті Каталізатори готували способом просочення блокових матриць із кордієриту азотнокислими солями нікелю й алюмінію по вологоємності з наступним сушінням і прожарюванням у муфельній печі протягом 3 годин при температурі 550-600 °C на повітрі. Співвідношення солей у розчині забезпечувало необхідний склад компонентів у каталізаторі 4 % Аl2О3, 5 %NiO. Приклад В Приготування 5 мас. % NiO, 4 мас. % Аl2О3 і 1 мас. % СеО2 на кордієриті Метод приготування аналогічний описаному у Прикладі А за відмінністю, що до розчину додають Ce(NH4)2(NO3)6 у кількості, необхідній для утворення у складі каталізатора після прожарювання 1 % СеО2. Приклад С Метод приготування аналогічний описаному у Прикладі А за відмінністю, що до розчину додають Lа(NaО3)3 у кількості, необхідній для утворення у складі каталізатора після прожарювання 1 % Nа2О3. Приклад D Метод приготування аналогічний описаному у Прикладі А за відмінністю, що до розчину додають NaNO3 у кількості, необхідній для утворення у складі каталізатора після прожарювання 1 %Na2O. Приклад Е 3 UA 108461 U 5 10 15 20 25 30 35 40 45 50 55 60 Метод приготування аналогічний описаному у Прикладі А за відмінністю, що до розчину додають KNО3 у кількості, необхідній для утворення у складі каталізатора після прожарювання 1 % K2О. Приклад 1 Використаний каталізатор містив 5 % мас. NiO і 4 % мас. Аl2О3 на кордієриті і був приготовлений за методикою, наведеною в Прикладі А -1 Реакційна газова суміш, що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2:Н2О:Аr зі співвідношенням, рівним 1:0,15:0,4:0,7:11. При температурі 650 °C показники процесу складали: конверсія метану приблизно 90 %, конверсія вуглекислого газу 36-38 %, співвідношення Н2/СО становило 1,7. При температурі 750 °C показники процесу складали: конверсія метану 98,8-99,9 %, конверсія вуглекислого газу 52-64 %, співвідношення H2/СО становило 1,67-1,76. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 2 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. СеО2 на кордієриті і був приготовлений за методикою, наведеною в Прикладі В, а також тим, що реакційна газова суміш, -1 що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2:Н2О:Аr зі співвідношенням, рівним 1:0,15:0,4:0,7:11. При температурі 650 °C показники процесу складали: конверсія метану приблизно 90 %, конверсія вуглекислого газу 58-65 %, співвідношення Н2/СО становило приблизно 1,65. При температурі 750 °C показники процесу складали: конверсія метану 96-98 %, конверсія вуглекислого газу 65-75 %, співвідношення Н2/СО становило 1,61-1,77. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 3 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. СеО2 на кордієриті і був приготовлений за методикою, наведеною в Прикладі В, а також тим, що реакційна газова суміш, -1 що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2. Н2О:Аr зі співвідношенням, рівним 1:0,2:0,6:0,9:15. При температурі 560 °C показники процесу складали: конверсія метану приблизно 80 %, конверсія вуглекислого газу 16 %, співвідношення Н2/СО становило 1,96. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 4 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. Lа2О3 на кордієриті і був приготовлений за методикою, наведеною в Прикладі С, а також тим, що реакційна газова суміш, -1 що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2:Н2О:Аr зі співвідношенням, рівним 1:0,15:0,4:0,7:11. При температурі 650 °C показники процесу складали: конверсія метану приблизно 97 %, конверсія вуглекислого газу 19-23 %, співвідношення Н2/СО становило 1,8-1,85. При температурі 755 °C показники процесу складали: конверсія метану 96-98 %, конверсія вуглекислого газу приблизно 50 %, співвідношення Н2/СО становило 1,7-1,9. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 5 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. АlО3 1 % мас. Lа2О3 на кордієриті і був приготовлений за методикою, наведеною в Прикладі С, а також тим, що реакційна газова суміш, -1 що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2:Н2О:Аr зі співвідношенням, рівним 1:0,3:0,9:0,7:15. При температурі 725 °C показники процесу складали: конверсія метану 100 %, конверсія вуглекислого газу приблизно 28 %, співвідношення H2/CO становило 2,5. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 6 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. Na2O на кордієриті і був приготовлений за методикою, наведеною в Прикладі D, а також тим, що реакційна газова суміш, -1 що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2:Н2О:Аr зі співвідношенням, рівним 1:0,15:0,4:0,7:11. 4 UA 108461 U 5 10 15 20 25 30 35 40 45 При температурі 650 °C показники процесу складали: конверсія метану 97,3-98,5 %, конверсія вуглекислого газу приблизно 30 %, співвідношення H2/СО становило 2,0-2,05. При температурі 750 °C показники процесу складали: конверсія метану 99,2-99,8 %, конверсія вуглекислого газу приблизно 56 %, співвідношення Н2/СО становило 1,7-1,75. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 7 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. К2О на кордієриті і був приготовлений за методикою, наведеною в Прикладі D, а також тим, що реакційна газова суміш, -1 що подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа, містила компоненти СН4:О2:СО2:Н2О:Аr зі співвідношенням, рівним 1:0,15:0,4:0,7:11. При температурі 650 °C показники процесу складали: конверсія метану 97,8-98,6 %, конверсія вуглекислого газу приблизно 35 %, співвідношення Н2/СО становило 1,9-2,05. При температурі 750 °C показники процесу складали: конверсія метану 99,2-99,8 %, конверсія вуглекислого газу приблизно 50 %, співвідношення Н2/СО становило 2,07-2,09. Результати описаної вище реакції три-риформінгу приведено в Таблиці 1 нижче. Приклад 8 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. K2О на кордієриті і був приготовлений за методикою, наведеною в Прикладі D, а також тим, що реакційна газова суміш -1 подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа; співвідношення компонентів реакційної газової суміші CH4:O2:CO2:H2O:Ar варіювалось у межах 1:0,180,24:0,5-0,75:0,5-0,7:13; процес проводили при визначених умовах протягом декількох годин при постійній температурі з інтервалу 550-610 °C. Результати дослідження приведені на Фіг. 1. Незначна втрата каталітичної активності спостерігається лише при 550 °C, а і за 705 °C каталізатор працює стабільно. Приклад 9 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. СеО2 на кордієриті і був приготовлений за методикою, наведеною в Прикладі В, а також тим, що реакційна газова суміш -1 подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа; співвідношення компонентів реакційної газової суміші CH4:O2:CO2:H2O:Ar варіювалось у межах 1:(0,180,24):(0,5-0,75):(0,5-0,7):13; процес проводили при визначених умовах протягом декількох годин при постійній температурі з інтервалу 610-705 °C. Результати дослідження приведені на Фіг. 2. Втрати каталітичної активності не спостерігалось. Приклад 10 Методику, викладену в Прикладі 1, було повторено. Приклад відрізняється тим, що використаний каталізатор містив 5 % мас. NiO, 4 % мас. Аl2О3 1 % мас. Lа2О3 на кордієриті і був приготовлений за методикою, наведеною в Прикладі С, а також тим, що реакційна газова суміш -1 подавалась на каталізатор з об'ємною швидкістю 12000 год. при тиску 0,1-0,15 мПа; співвідношення компонентів реакційної газової суміші СН4:О2:СО2:Н2О:Аr складало 1:0,3:0,35:0,5:13; процес проводили при визначених умовах протягом декількох годин при постійній температурі 625 °C. Результати дослідження приведені на Фіг. 3. Втрати каталітичної активності не спостерігалось. Таблиця 1 № Пр. Каталізатор 1 1 2 2 3 4 4 5 %NiO+4 %Аl2О3 5 %NiO+4 %Аl2О3 5 %NiO+4 %Al2O3+1 %СеО2 5 %NiO+4 %Аl2О3+1 %СеО2 5 %NiO+4 %Аl2О3+1 %СеО2 5 %NiO+4 %Аl2О3+1 %La2O3 5 %NiO+4 %Аl2О3+1 %La2O3 Співвідношення ТемпеСН4/СО2/О2/Н2О/Аr ратура, °C 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 1:0,2:0,6:0,9:15 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 5 650 750 650 750 560 650 755 Конверсія, % СН4 90 98,8-99,9 90 96-98 80 97 96-98 СО2 36-37 52-64 58-65 65-75 16 19-23 50 Співвідношення H2/СО 1,7 1,67-1,76 1,65 1,61-1,77 1,96 1,8-1,85 1,7-1,9 UA 108461 U Продовження таблиці 1 № Пр. Каталізатор Співвідношення ТемпеСН4/СО2/О2/Н2О/Аr ратура, °C 5 6 6 7 7 5 %NiO+4 %Аl2О3+1 %Lа2О3 5 %NiO+4 %Аl2О3+1 %Na2O 5 %NiO+4 %Аl2О3+1 %Na2O 5 %NiO+4 %Аl2О3+1 %К2О 5 %NiO+4 %Аl2О3+1 %K2O 1:0,3:0,9:0,7:15 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 1:0,15:0,4:0,7:11 725 650 750 650 750 Конверсія, % СН4 100 97,3-98,5 99,2-99,8 97,8-98,6 99,2-99,8 СО2 28 30 56 35 50 Співвідношення H2/СО 2,5 2,0-2,05 1,7-1,75 1,9-2,05 2,07-2,09 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 5 10 1. Нікелевмісний каталізатор для три-риформінгу метану, нанесений на носій, який відрізняється тим, що як носій використовується кордієрит та каталізатор додатково містить оксид алюмінію та оксид лантану або оксид церію, при наступному співвідношенні компонентів у мас. %: NiO 4-6 Аl2О3 4-6 Lа2О3(СеО2) 0,5-1,5 кордієрит решта. 2. Нікелевмісний каталізатор за п. 1, який відрізняється тим, що кордієрит має коміркову структуру. 6 UA 108461 U Комп’ютерна верстка Л. Ціхановська Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 7
ДивитисяДодаткова інформація
МПК / Мітки
МПК: B01J 35/04, B01J 23/755
Мітки: метану, каталізатор, три-риформінгу, нікелевмісній
Код посилання
<a href="https://ua.patents.su/9-108461-nikelevmisnijj-katalizator-dlya-tri-riformingu-metanu.html" target="_blank" rel="follow" title="База патентів України">Нікелевмісний каталізатор для три-риформінгу метану</a>
Попередній патент: Спосіб визначення активності очищеного (ппд) туберкуліну для ссавців на тваринах, сенсибілізованих авірулентними культурами m.bovis
Наступний патент: Гвинтовий класифікатор коренеплодів
Випадковий патент: Пристрій ударної дії для утворення свердловин у ґрунті