Спосіб синтезу івабрадину і його адитивних солей з фармацевтично прийнятною кислотою
Формула / Реферат
1. Спосіб синтезу івабрадину формули (І):
 , (I)
, (I)
який відрізняється тим, що сполуку формули (VI):
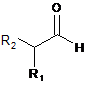 , (VI)
, (VI)
де R1 та R2, які є однаковими або різними, представляють нерозгалужені або розгалужені (С1-С6)алкоксигрупи або разом з атомом вуглецю, до якого вони приєднані, утворюють 1,3-діоксанове, 1,3-діоксоланове або 1,3-діоксепанове кільце,
вводять в реакцію відновлювального амінування зі сполукою формули (VII):
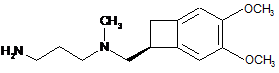 (VII)
(VII)
у присутності відновлювального реагента,
в органічному розчиннику, суміші органічних розчинників або суміші органічного розчинника(ів) та води,
з одержанням сполуки формули (VIII):
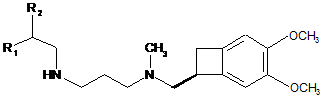 , (VIII)
, (VIII)
де R1 та R2 є такими, як визначено вище,
яку вводять в реакцію конденсації із сполукою формули (IX):
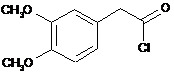 (IX)
(IX)
у присутності основи в органічному розчиннику,
з одержанням сполуки формули (X):
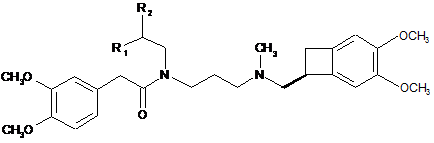 , (Х)
, (Х)
де R1 та R2 є такими, як визначено вище,
яку піддають реакції циклізації в кислому середовищі з одержанням сполуки формули (V):
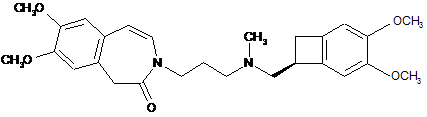 , (V)
, (V)
яку піддають реакції гідрогенізації з одержанням івабрадину формули (І), який необов'язково може бути перетворений на його адитивні солі з фармацевтично прийнятною кислотою, вибраною з хлористоводневої кислоти, бромистоводневої кислоти, сірчаної кислоти, фосфорної кислоти, оцтової кислоти, трифтороцтової кислоти, молочної кислоти, піровиноградної кислоти, малонової кислоти, бурштинової кислоти, глутарової кислоти, фумарової кислоти, винної кислоти, малеїнової кислоти, лимонної кислоти, аскорбінової кислоти, щавлевої кислоти, метансульфонової кислоти, бензолсульфонової кислоти і камфорної кислоти та їх гідратів.
2. Спосіб синтезу за п. 1, який відрізняється тим, що як відновлювальний реагент, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII), вибирають з натрію триацетоксиборгідриду, натрію ціаноборгідриду та диводню у присутності каталізатора, такого як паладій, платина, нікель, рутеній, родій та їх сполуки, зокрема, на основі або у формі оксидів.
3. Спосіб синтезу за п. 2, який відрізняється тим, що як відновлювальний реагент, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII), використовують диводень у присутності паладію на вуглеці.
4. Спосіб синтезу за п. 3, який відрізняється тим, що реакцію відновлювального амінування між сполукою формули (VI) та сполукою формули (VII) здійснюють при тиску диводню від 0,5 до 1,5 бар.
5. Спосіб синтезу за будь-яким з пп. 1-4, який відрізняється тим, що розчинник, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) із сполукою формули (VII), вибирають з тетрагідрофурану, дихлорметану, 1,2-дихлоретану, ацетатів та спиртів, переважно етанолу, метанолу або ізопропанолу, толуолу та ксилолу.
6. Спосіб синтезу за п. 5, який відрізняється тим, що розчинник, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) із сполукою формули (VII), включає суміш етанолу та води.
7. Спосіб синтезу за будь-яким з пп. 1-6, який відрізняється тим, що реакцію відновлювального амінування між сполукою формули (VI) та сполукою формули (VII) здійснюють при температурі від 0 до 40 °C.
8. Спосіб синтезу за будь-яким з пп. 1-7, який відрізняється тим, що органічний розчинник, використаний в реакції між сполуками формул (VIII) та (IX), вибирають з толуолу, дихлорметану, 2-метилтетрагідрофурану, хлорбензолу, 1,2-дихлоретану, хлороформу та діоксану.
9. Спосіб синтезу за п. 8, який відрізняється тим, що органічний розчинник, який використовують в реакції між сполуками формул (VIII) та (IX), являє собою дихлорметан.
10. Спосіб синтезу за будь-яким з пп. 1-9, який відрізняється тим, що реакцію між сполуками формул (VIII) та (IX) здійснюють при температурі від 0 до 40 °C.
11. Спосіб синтезу за будь-яким з пп. 1-10, який відрізняється тим, що основу, яку використовують в реакції між сполуками формул (VIII) та (IX), вибирають з піридину, 4-диметиламінопіридину (ДМАП) і третинного аміну.
12. Спосіб синтезу за п. 11, який відрізняється тим, що основа, яку використовують в реакції між сполуками формул (VIII) та (IX), являє собою триетиламін.
13. Спосіб синтезу за будь-яким з пп. 1-12, який відрізняється тим, що кислоту, яку використовують для здійснення циклізації сполуки формули (X) з утворенням сполуки формули (V), вибирають з концентрованої сірчаної кислоти, поліфосфорної кислоти, концентрованої хлористоводневої кислоти у водному розчині, концентрованої хлористоводневої кислоти в розчині в оцтовій кислоті, концентрованої бромистоводневої кислоти в розчині в оцтовій кислоті та метансульфоновій кислоті.
14. Спосіб синтезу за п. 13, який відрізняється тим, що кислота, яку використовують для здійснення циклізації сполуки формули (X) з утворенням сполуки формули (V), являє собою концентровану хлористоводневу кислоту в розчині в оцтовій кислоті.
15. Спосіб синтезу за будь-яким з пп. 1-14, який відрізняється тим, що циклізацію сполуки формули (X) з утворенням сполуки формули (V) здійснюють при температурі від 0 до 40 °C.
16. Сполука формули (VIII):
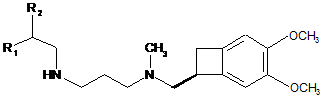 , (VIII)
, (VIII)
де R1 та R2, які є однаковими або різними, представляють нерозгалужені або розгалужені (С1-С6)алкоксигрупи або разом з атомом вуглецю, до якого вони приєднані, утворюють 1,3-діоксанове, 1,3-діоксоланове або 1,3-діоксепанове кільце.
17. Сполука формули (X):
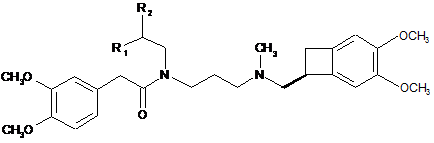 , (Х)
, (Х)
де R1 та R2 є такими, як визначено в п. 16.
Текст
Реферат: Спосіб синтезу івабрадину формули (І) CH3O CH3 CH3O N N OCH3 OCH3 O або його адитивних солей з фармацевтично прийнятною кислотою. (I) З ФАРМАЦЕВТИЧНО UA 110326 C2 (12) UA 110326 C2 UA 110326 C2 Даний винахід стосується способу синтезу івабрадину формули (І): CH3O OCH3 CH3 CH3O N N OCH3 O 5 10 15 , (I) або 3-{3-[{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл]метил}-(метил)аміно]пропіл}7,8-диметокси-1,3,4,5-тетрагідро-2Н-3-бензазепін-2-ону, його адитивних солей з фармацевтично прийнятною кислотою та його гідратів. Івабрадин та його адитивні солі з фармацевтично прийнятною кислотою, і, зокрема, його гідрохлорид, мають дуже цінні фармакологічні і терапевтичні властивості, зокрема, брадикардичні властивості, що робить такі сполуки придатними для лікування або профілактики в різноманітних клінічних ситуаціях ішемії міокарду, таких як стенокардія, інфаркт міокарду та супровідні порушення ритму, а також при різноманітних патологіях, що включають порушення ритму, зокрема, суправентрикулярні порушення ритму, та при серцевій недостатності. Спосіб одержання і терапевтичне застосування івабрадину та його адитивних солей з фармацевтично прийнятною кислотою, і, зокрема, його гідрохлориду, викладено в описі Європейського патенту ЕР 0 534 859. В описі зазначеного патенту охарактеризовано синтез івабрадину гідрохлориду, починаючи зі сполуки формули (II): OCH3 CH3HN OCH3 , (II) яку розділяють для одержання сполуки формули (III): OCH3 CH3HN 20 OCH3 , (III) яка реагує зі сполукою формули (IV): CH3O N CH3O I O , (IV) з утворенням сполуки формули (V): CH3O OCH3 CH3 CH3O N N OCH3 O 25 , (V) каталітична гідрогенізація якої дає івабрадин, який далі перетворюють на його гідрохлорид. Недоліком даного шляху синтезу є те, що івабрадин утворюється з виходом тільки 1 %. З точки зору фармацевтичної цінності даної сполуки, важливою була можливість одержувати її за допомогою ефективного способу синтезу, в ході якого івабрадин утворювався б із високим виходом. Даний винахід стосується способу синтезу івабрадину формули (І): 1 UA 110326 C2 CH3O OCH3 CH3 CH3O N N OCH3 O , (I) де спосіб відрізняється тим, що сполуку формули (VI): O R2 H R1 5 , (VI) де R1 та R2, які є однаковими або різними, представляють нерозгалужені або розгалужені (С1-С6)алкоксигрупи або разом з атомом вуглецю, до якого вони приєднані, утворюють 1,3діоксанове, 1,3-діоксоланове або 1,3-діоксепанове кільце, вводять в реакцію відновлювального амінування зі сполукою формули (VII): OCH3 CH3 N H2N 10 OCH3 (VII) у присутності відновлювального реагенту, в органічному розчиннику, суміші органічних розчинника(ів) та води, з одержанням сполуки формули (VIII): розчинників або суміші органічного R2 R1 N HN 15 OCH3 CH3 OCH3 , (VIII) де R1 та R2 є такими, як визначено в даному описі вище, яку вводять в реакцію конденсації із сполукою формули (IX): O CH3O Cl CH3O , (IX) у присутності основи в органічному розчиннику, з одержанням сполуки формули (X): R2 R1 CH3 N CH3O N OCH3 OCH3 O CH3O 20 , (Х) де R1 та R2 є такими, як визначено в даному описі вище, для якої здійснюють реакцію циклізації в кислому середовищі з одержанням сполуки формули (V): 2 UA 110326 C2 CH3O OCH3 CH3 CH3O N N OCH3 O 5 10 15 20 25 30 35 40 45 50 , (V) який необов'язково може бути перетворений на його адитивні солі з фармацевтично прийнятною кислотою, вибраною з хлористоводневої кислоти, бромистоводневої кислоти, сірчаної кислоти, фосфорної кислоти, оцтової кислоти, трифтороцтової кислоти, молочної кислоти, піровиноградної кислоти, малонової кислоти, бурштинової кислоти, глутарової кислоти, фумарової кислоти, винної кислоти, малеїнової кислоти, лимонної кислоти, аскорбінової кислоти, щавлевої кислоти, метансульфонової кислоти, бензолсульфонової кислоти і камфорної кислоти та їх гідратів. Перелік відновлювальних реагентів, які можуть бути використані для здійснення відновлювального амінування, наведений в довідкових роботах Comprehensive Organic Transformations (Richard C. Larock, VCH Publishers 1989, pp 421-425) та Advanced Organic Chemistry Fourth Edition (Jerry March, Wiley Interscience 1992, pp 898-900). Серед відновлювальних реагентів, які можуть бути використані для здійснення реакції відновлювального амінування сполуки формули (VI) із сполукою формули (VII), можна згадати, не обмежуючись ними, натрію триацетоксиборгідрид, натрію ціаноборгідрид та диводень у присутності каталізатора, такого як паладій, платина, нікель, рутеній, родій та їх сполуки, зокрема на основі або у формі оксидів. Переважним відновлювальним реагентом для використання з метою здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII) є диводень у присутності паладію на вуглеці. Переважно, реакцію відновлювального амінування сполуки формули (VI) зі сполукою формули (VII) здійснюють при тиску диводню від 0,5 до 1,5 бар. Серед розчинників, які можуть бути використані для здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII), можна згадати, не обмежуючись ними, тетрагідрофуран, дихлорметан, 1,2-дихлоретан, ацетати, спирти, переважно етанол, метанол або ізопропанол, толуол та ксилол. Переважний розчинник, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII) включає суміш етанолу та води. Реакцію відновлювального амінування сполуки формули (VI) зі сполукою формули (VII) переважно здійснюють при температурі від 0 °С до 40 °С. Серед органічних розчинників, які можуть бути використані в реакції між сполуками формул (VIII) та (IX), можна згадати, не обмежуючись ними, толуол, дихлорметан, 2метилтетрагідрофуран, хлорбензол, 1,2-дихлоретан, хлороформ та діоксан. Переважним органічним розчинником, який може бути використаний в реакції між сполуками формул (VIII) та (IX), є дихлорметан. Реакцію між сполуками формул (VIII) та (IX) переважно здійснюють при температурі від 0 до 40 °С. Серед основ, які можуть бути використані в реакції між сполуками формул (VIII) та (IX), можна згадати, не обмежуючись ними, піридин, ДМАП і третинні аміни, наприклад, триетиламін, ДІЕА, N-метилпіперидин, ДБУ, ДАБКО, ДБН та N-метилморфолін. Переважно, основа, яку використовують в реакції між сполуками формул (VIII) та (IX), являє собою триетиламін. Серед кислот, які можуть бути використані для реакції циклізації сполуки формули (X) з утворенням сполуки формули (V), можна згадати, не обмежуючись ними, концентровану сірчану кислоту, поліфосфорну кислоту, концентровану хлористоводневу кислоту у водному розчині, концентровану хлористоводневу кислоту у розчині в оцтовій кислоті, концентровану бромистоводневу кислоту у розчині в оцтовій кислоті та метансульфонову кислоту. Переважно, кислота, яку використовують для здійснення циклізації сполуки формули (X) з утворенням сполуки формули (V), являє собою концентровану хлористоводневу кислоту у розчині в оцтовій кислоті. Реакцію циклізації сполуки формули (X) з утворенням сполуки формули (V) в кислому середовищі переважно здійснюють при температурі від 0 до 40 °С. Сполуки формули (VIII) та (X) являють собою нові продукти, які є придатними як проміжні продукти для синтезу в хімічній або фармацевтичній промисловості, зокрема для синтезу 3 UA 110326 C2 5 10 15 20 25 30 35 40 45 50 55 івабрадину, його адитивних солей з фармацевтично прийнятною кислотою та його гідратів, і, таким чином, вони є невід'ємною частиною даного винаходу. Перелік використаних скорочень: ДАБКО: 1,4-діазабіцикло[2.2.2]октан. ДБН: 1,5-діазабіцикло[4.3.0]нон-5-ен. ДБУ: 1,8-діазабіцикло[5.4.0]ундец-7-ен. ДІЕА: N,N-діізопропілетиламін. ДМАП: 4-диметиламінопіридин. ІЧ: інфрачервоний. Наведені нижче Приклади ілюструють винахід. Спектри в інфрачервоній області зареєстровані на ІЧ-спектрометрі Bruker Tensor 27 з використанням пристрою Golden Gate ATR. Речовини вміщували на пластину в чистій формі. Приклад 1: 2-{3-[{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл]метил}(метил)аміно]пропіл}-1Н-ізоіндол-1,3(2Н)-діон 5,3 г (25,5 ммоль) 1-[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл]-Nметилметанаміну та 6,8 г (25,5 ммоль) 2-(3-бромпропіл)-1Н-ізоіндол-1,3(2H)-діону розчиняють в 230 мл ацетону. 13 г (95 ммоль, 3,7 екв.) калію карбонату додають до одержаного розчину. Далі суміш кип'ятять зі зворотним холодильником протягом 24 год. Після охолодження до кімнатної температури, калію карбонат відфільтровують, а фільтрат упарюють до сухого стану. Залишок переносять у воду та екстрагують дихлорметаном. Органічну фазу сушать над MgSO 4, фільтрують та упарюють до сухого стану. 9,7 г цільового продукту одержують у формі блідожовтого масла. Вихід = 97 %. -1 ІЧ: n = 2782, 1770, 1704, 1206, 836, 718 см . Приклад 2: N-{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл]метил}-N-метилпропан1,3-діамін 9,7 г (24,58 ммоль) фталімідної сполуки з попередньої стадії розчиняють в 100 мл етанолу. Додають 2,7 мл (36,87 ммоль, 1,5 екв.) гідразингідрату та кип'ятять зі зворотним холодильником протягом 4 год. Після охолодження до кімнатної температури, додають 100 мл водного розчину хлористоводневої кислоти (4 N); суміш перемішують протягом 1 год при кімнатній температурі та фільтрують крізь скляний фільтр. Далі фільтрат упарюють (для видалення етанолу). Після цього водну фазу двічі промивають ефіром та доводять рН до 9 додаванням холодного концентрованого розчину натрію гідроксиду. Екстракцію дихлорметаном здійснюють тричі, після чого об'єднані органічні фази промивають водою, сушать над MgSO 4, фільтрують та упарюють до сухого стану. Одержують 4,9 г цільового продукту у формі блідо-жовтого масла. Вихід = 75 %. -1 ІЧ: n = 3366, 3302, 1591 см . Приклад 3: N-{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл]метил}-N'-(2,2диметоксіетил)-N-метилпропан-1,3-діамін 1 г (3,7 ммоль) N-{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл]метил}-Nметилпропан-1,3-діаміну розчиняють в 20 мл етанолу. Додають 520 мг (0,45 мл) 60 % розчину гліоксалю 1,1-диметилацеталю у воді, і потім 100 мг 10 % Pd/C. Реакційну суміш гідрогенізують при атмосферному тиску та кімнатній температурі протягом 12 год. Каталізатор відфільтровують, а фільтрат упарюють до сухого стану. 1,2 г цільового продукту одержують у формі масла. Вихід = 90 %. -1 ІЧ: n = 1207, 1508, 834 см . Приклад 4: N-{3-[{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7іл]метил}(метил)аміно]пропіл}-N-(2,2-диметоксіетил)-2-(3,4-диметоксифеніл)ацетамід Готують розчин 6,3 г (17,9 ммоль) ацеталю з попередньої Стадії в 80 мл СН 2Сl2. 5 мл триетиламіну (35,8 ммоль, 2 екв.) додають до одержаного розчину, який далі охолоджують до 0 °С. Після цього краплями додають розчин 3,8 г (17,9 ммоль) гомовератрилхлориду в 40 мл дихлорметану. Далі здійснюють перемішування протягом 3 год при кімнатній температурі. Суміш розбавляють водою та екстрагують дихлорметаном. Органічну фазу сушать над MgSO 4, фільтрують та упарюють до сухого стану. Одержують 10 г масла, яке очищують на 500 г силікагелю (елюент = СН2Сl2/ЕtOН, 90:10). 8,5 г цільового продукту одержують у формі коричневого масла. Вихід = 90 %. -1 ІЧ: n = 1627, 1207, 1124, 1071, 1049, 1027 см . 4 UA 110326 C2 5 10 15 Приклад 5: 3-{3-[{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7іл]метил}(метил)аміно]пропіл}-7,8-диметокси-1,3-дигідро-2Н-3-бензазепін-2-он До суміші 10 мл оцтової кислоти та 10 мл концентрованої хлористоводневої кислоти додають 1 г (1,9 ммоль) ацеталю з попередньої стадії при кімнатній температурі. Далі перемішують при температурі 25 °С протягом 1 год. Доводять рН розчину до 9 додаванням льоду та водного розчину натрію гідроксиду (20 %). Після цього суміш екстрагують дихлорметаном. Органічну фазу промивають водою, сушать над MgSO4, фільтрують та упарюють до сухого стану. Одержують 1 г масла, яке очищують флеш-хроматографією на 40 г кремнію діоксиду (колонка Merck™, елюент = СН2Сl2/ЕtOН, 95:5). Одержують 270 мг цільового продукту у формі масла з оптичною чистотою більше 99 %. Вихід = 31 %. -1 ІЧ: n = 1656, 836, 760 см . Приклад 6: 3-{3-[{[(7S)-3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7іл]метил}(метил)аміно]пропіл}-7,8-диметокси-1,3,4,5-тетрагідро-2Н-3-бензазепін-2-он Названу в заголовку сполуку одержують за методикою зі Стадії D Прикладу 1 патентної заявки ЕР 0 534 859, розпочинаючи зі сполуки за Прикладом 5 вище. ФОРМУЛА ВИНАХОДУ 20 1. Спосіб синтезу івабрадину формули (І): CH3O OCH3 CH3 CH3O N N OCH3 O , (I) який відрізняється тим, що сполуку формули (VI): O R2 H R1 25 , (VI) де R1 та R2, які є однаковими або різними, представляють нерозгалужені або розгалужені (С 1С6)алкоксигрупи або разом з атомом вуглецю, до якого вони приєднані, утворюють 1,3діоксанове, 1,3-діоксоланове або 1,3-діоксепанове кільце, вводять в реакцію відновлювального амінування зі сполукою формули (VII): OCH3 CH3 N H2N 30 OCH3 (VII) у присутності відновлювального реагента, в органічному розчиннику, суміші органічних розчинників або суміші органічного розчинника(ів) та води, з одержанням сполуки формули (VIII): R2 R1 CH3 HN 35 N OCH3 OCH3 , (VIII) де R1 та R2 є такими, як визначено вище, яку вводять в реакцію конденсації із сполукою формули (IX): 5 UA 110326 C2 O CH3O Cl CH3O (IX) у присутності основи в органічному розчиннику, з одержанням сполуки формули (X): R2 R1 OCH3 CH3 N N CH3O OCH3 O CH3O 5 , (Х) де R1 та R2 є такими, як визначено вище, яку піддають реакції циклізації в кислому середовищі з одержанням сполуки формули (V): CH3O OCH3 CH3 CH3O N N OCH3 O 10 15 20 25 30 35 40 , (V) яку піддають реакції гідрогенізації з одержанням івабрадину формули (І), який необов'язково може бути перетворений на його адитивні солі з фармацевтично прийнятною кислотою, вибраною з хлористоводневої кислоти, бромистоводневої кислоти, сірчаної кислоти, фосфорної кислоти, оцтової кислоти, трифтороцтової кислоти, молочної кислоти, піровиноградної кислоти, малонової кислоти, бурштинової кислоти, глутарової кислоти, фумарової кислоти, винної кислоти, малеїнової кислоти, лимонної кислоти, аскорбінової кислоти, щавлевої кислоти, метансульфонової кислоти, бензолсульфонової кислоти і камфорної кислоти та їх гідратів. 2. Спосіб синтезу за п. 1, який відрізняється тим, що як відновлювальний реагент, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII), вибирають з натрію триацетоксиборгідриду, натрію ціаноборгідриду та диводню у присутності каталізатора, такого як паладій, платина, нікель, рутеній, родій та їх сполуки, зокрема, на основі або у формі оксидів. 3. Спосіб синтезу за п. 2, який відрізняється тим, що як відновлювальний реагент, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) зі сполукою формули (VII), використовують диводень у присутності паладію на вуглеці. 4. Спосіб синтезу за п. 3, який відрізняється тим, що реакцію відновлювального амінування між сполукою формули (VI) та сполукою формули (VII) здійснюють при тиску диводню від 0,5 до 1,5 бар. 5. Спосіб синтезу за будь-яким з пп. 1-4, який відрізняється тим, що розчинник, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) із сполукою формули (VII), вибирають з тетрагідрофурану, дихлорметану, 1,2-дихлоретану, ацетатів та спиртів, переважно етанолу, метанолу або ізопропанолу, толуолу та ксилолу. 6. Спосіб синтезу за п. 5, який відрізняється тим, що розчинник, який використовують для здійснення реакції відновлювального амінування сполуки формули (VI) із сполукою формули (VII), включає суміш етанолу та води. 7. Спосіб синтезу за будь-яким з пп. 1-6, який відрізняється тим, що реакцію відновлювального амінування між сполукою формули (VI) та сполукою формули (VII) здійснюють при температурі від 0 до 40 °C. 8. Спосіб синтезу за будь-яким з пп. 1-7, який відрізняється тим, що органічний розчинник, використаний в реакції між сполуками формул (VIII) та (IX), вибирають з толуолу, дихлорметану, 2-метилтетрагідрофурану, хлорбензолу, 1,2-дихлоретану, хлороформу та діоксану. 9. Спосіб синтезу за п. 8, який відрізняється тим, що органічний розчинник, який використовують в реакції між сполуками формул (VIII) та (IX), являє собою дихлорметан. 6 UA 110326 C2 5 10 15 10. Спосіб синтезу за будь-яким з пп. 1-9, який відрізняється тим, що реакцію між сполуками формул (VIII) та (IX) здійснюють при температурі від 0 до 40 °C. 11. Спосіб синтезу за будь-яким з пп. 1-10, який відрізняється тим, що основу, яку використовують в реакції між сполуками формул (VIII) та (IX), вибирають з піридину, 4диметиламінопіридину (ДМАП) і третинного аміну. 12. Спосіб синтезу за п. 11, який відрізняється тим, що основа, яку використовують в реакції між сполуками формул (VIII) та (IX), являє собою триетиламін. 13. Спосіб синтезу за будь-яким з пп. 1-12, який відрізняється тим, що кислоту, яку використовують для здійснення циклізації сполуки формули (X) з утворенням сполуки формули (V), вибирають з концентрованої сірчаної кислоти, поліфосфорної кислоти, концентрованої хлористоводневої кислоти у водному розчині, концентрованої хлористоводневої кислоти в розчині в оцтовій кислоті, концентрованої бромистоводневої кислоти в розчині в оцтовій кислоті та метансульфоновій кислоті. 14. Спосіб синтезу за п. 13, який відрізняється тим, що кислота, яку використовують для здійснення циклізації сполуки формули (X) з утворенням сполуки формули (V), являє собою концентровану хлористоводневу кислоту в розчині в оцтовій кислоті. 15. Спосіб синтезу за будь-яким з пп. 1-14, який відрізняється тим, що циклізацію сполуки формули (X) з утворенням сполуки формули (V) здійснюють при температурі від 0 до 40 °C. 16. Сполука формули (VIII): R2 R1 N HN 20 OCH3 CH3 OCH3 , (VIII) де R1 та R2, які є однаковими або різними, представляють нерозгалужені або розгалужені (С 1С6)алкоксигрупи або разом з атомом вуглецю, до якого вони приєднані, утворюють 1,3діоксанове, 1,3-діоксоланове або 1,3-діоксепанове кільце. 17. Сполука формули (X): R2 R1 OCH3 CH3 N CH3O N OCH3 O 25 CH3O , (Х) де R1 та R2 є такими, як визначено в п. 16. Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 7
ДивитисяДодаткова інформація
Автори російськоюJean-Louis Peglion, Aimee Dessinges
МПК / Мітки
МПК: C07D 223/16
Мітки: солей, спосіб, кислотою, фармацевтично, синтезу, прийнятною, адитивних, івабрадину
Код посилання
<a href="https://ua.patents.su/9-110326-sposib-sintezu-ivabradinu-i-jjogo-aditivnikh-solejj-z-farmacevtichno-prijjnyatnoyu-kislotoyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб синтезу івабрадину і його адитивних солей з фармацевтично прийнятною кислотою</a>
Попередній патент: Лікарські вуглеводи для лікування респіраторних розладів
Наступний патент: Смако-ароматична активна композиція
Випадковий патент: Спосіб рекламно-інформаційного освітлення балюстрад ескалаторних тунелів












