Тверді форми мезопрогестину-11b-[4е-(гідроксіімінометил)-феніл]-17a-метоксиметил-17b-метоксіестра-4,9-дієн-3-ону
Номер патенту: 73988
Опубліковано: 17.10.2005
Автори: Мюллер Уве, Хьосель Петер, Вінтер Габріеле, Граве Детлеф
Формула / Реферат
1. Аморфний ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он (J 867).
-метоксіестра-4,9-дієн-3-он (J 867).
2. Аморфний ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он за п. 1, який відрізняється тим, що його застосовують як лікувальний засіб.
-метоксіестра-4,9-дієн-3-он за п. 1, який відрізняється тим, що його застосовують як лікувальний засіб.
3. Аморфний ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он, одержаний шляхом сушіння кристалічного сольвату
-метоксіестра-4,9-дієн-3-он, одержаний шляхом сушіння кристалічного сольвату ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону при температурі нижче температури склування речовини, при цьому сушіння сольвату в процесі десольватації проводять зі швидкістю нагрівання продукту принаймні 0,5°С/хв., або з розчину сольвату шляхом розпилювального сушіння.
-метоксіестра-4,9-дієн-3-ону при температурі нижче температури склування речовини, при цьому сушіння сольвату в процесі десольватації проводять зі швидкістю нагрівання продукту принаймні 0,5°С/хв., або з розчину сольвату шляхом розпилювального сушіння.
4. Аморфний ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он за п. 3, який відрізняється тим, що його застосовують як лікувальний засіб.
-метоксіестра-4,9-дієн-3-он за п. 3, який відрізняється тим, що його застосовують як лікувальний засіб.
5. Кристалічний ансольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону.
-метоксіестра-4,9-дієн-3-ону.
6. Кристалічний ансольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону за п. 5, який відрізняється тим, що його застосовують як лікувальний засіб.
-метоксіестра-4,9-дієн-3-ону за п. 5, який відрізняється тим, що його застосовують як лікувальний засіб.
7. Кристалічний ансольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
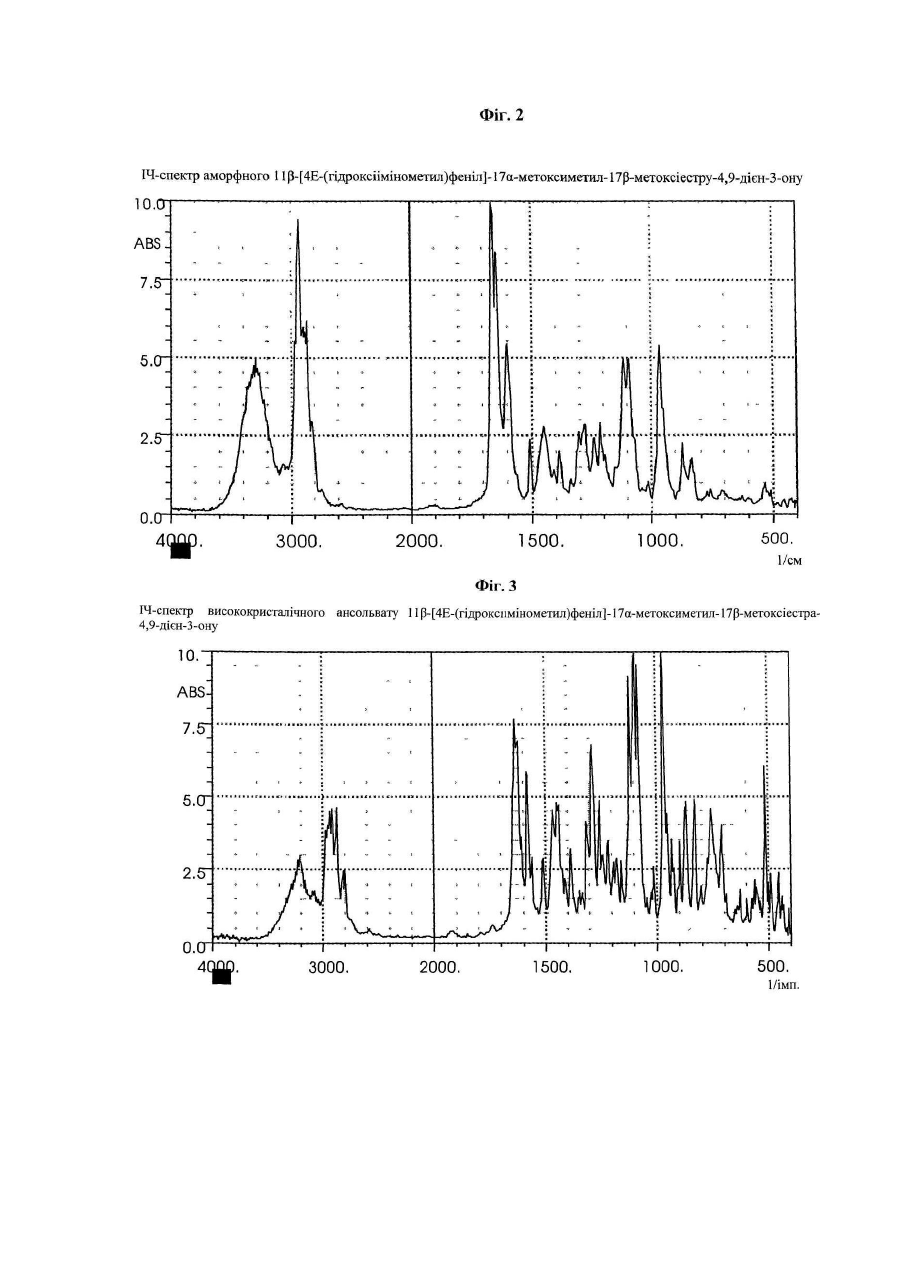
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону за п. 5 або 6, при цьому кристалічна форма характеризується представленим на фіг. 3 ІЧ-спектром.
-метоксіестра-4,9-дієн-3-ону за п. 5 або 6, при цьому кристалічна форма характеризується представленим на фіг. 3 ІЧ-спектром.
8. Кристалічний ансольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону за п. 5 або 6, при цьому кристалічна форма характеризується представленою на фіг. 1в (таблиця 1) рентгенівською порошковою дифрактограмою.
-метоксіестра-4,9-дієн-3-ону за п. 5 або 6, при цьому кристалічна форма характеризується представленою на фіг. 1в (таблиця 1) рентгенівською порошковою дифрактограмою.
9. Кристалічний сольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
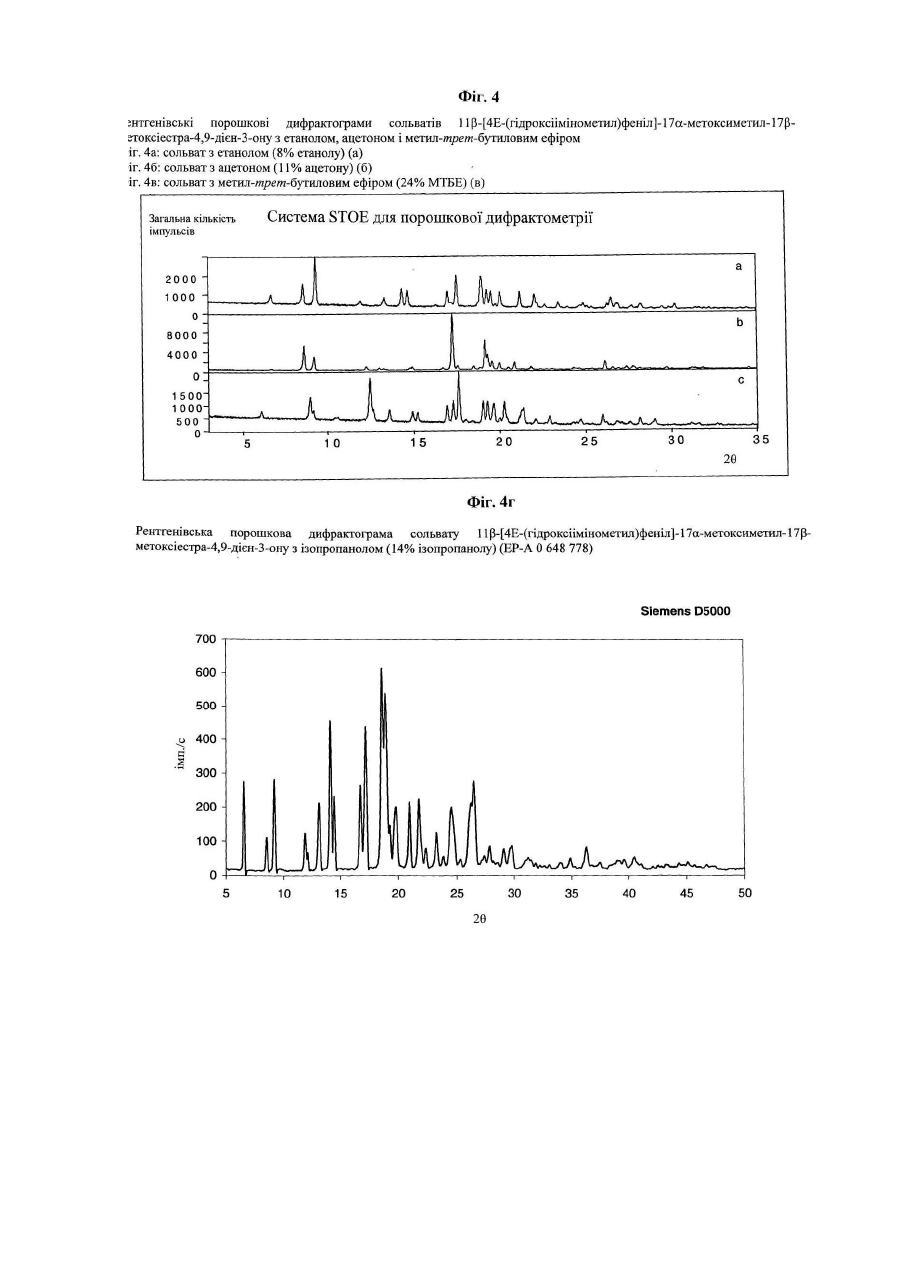
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону, вибраний з ряду: сольват з метил-трет-бутиловим ефіром, при цьому кристалічна форма характеризується представленою на фіг. 4в (таблиця 2) рентгенівською порошковою дифрактограмою, сольват з ацетоном, при цьому кристалічна форма характеризується представленою на фіг. 4б (таблиця 2) рентгенівською порошковою дифрактограмою, і сольват з етанолом, при цьому кристалічна форма характеризується представленою на фіг. 4а (таблиця 2) рентгенівською порошковою дифрактограмою.
-метоксіестра-4,9-дієн-3-ону, вибраний з ряду: сольват з метил-трет-бутиловим ефіром, при цьому кристалічна форма характеризується представленою на фіг. 4в (таблиця 2) рентгенівською порошковою дифрактограмою, сольват з ацетоном, при цьому кристалічна форма характеризується представленою на фіг. 4б (таблиця 2) рентгенівською порошковою дифрактограмою, і сольват з етанолом, при цьому кристалічна форма характеризується представленою на фіг. 4а (таблиця 2) рентгенівською порошковою дифрактограмою.
10. Спосіб одержання кристалічного сольвату ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону за п. 9, який полягає у тому, що
-метоксіестра-4,9-дієн-3-ону за п. 9, який полягає у тому, що
а) одержують сольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону з наступним розчиненням цього сольвату понад граничну розчинність у розчиннику, який відмінний від розчинника, який утворює сольват, та у якому кристалічна структура сольвату є нестабільною,
-метоксіестра-4,9-дієн-3-ону з наступним розчиненням цього сольвату понад граничну розчинність у розчиннику, який відмінний від розчинника, який утворює сольват, та у якому кристалічна структура сольвату є нестабільною,
б) додають розчинник, який утворює сольват, з наступною кристалізацією сольвату.
11. Спосіб одержання кристалічного сольвату ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону за п. 10, в якому додають додатковий розчинник як інгібітор рекристалізації.
-метоксіестра-4,9-дієн-3-ону за п. 10, в якому додають додатковий розчинник як інгібітор рекристалізації.
12. Спосіб одержання аморфного ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону, який полягає у тому, що отриманий способом за п. 10 кристалічний сольват
-метоксіестра-4,9-дієн-3-ону, який полягає у тому, що отриманий способом за п. 10 кристалічний сольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону піддають сушінню при температурі нижче температури склування аморфної речовини, при цьому сушіння сольвату в процесі десольватації проводять зі швидкістю нагрівання продукту принаймні 0,5°С/хв., чи з розчину сольвату шляхом розпилювального сушіння.
-метоксіестра-4,9-дієн-3-ону піддають сушінню при температурі нижче температури склування аморфної речовини, при цьому сушіння сольвату в процесі десольватації проводять зі швидкістю нагрівання продукту принаймні 0,5°С/хв., чи з розчину сольвату шляхом розпилювального сушіння.
13. Спосіб одержання кристалічного ансольвату ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону, вказаного в будь-якому з пп. 5-8, який відрізняється тим, що одну з вказаних у п. 9 сольватних форм суспендують у воді при температурі від 50 до 100°С.
-метоксіестра-4,9-дієн-3-ону, вказаного в будь-якому з пп. 5-8, який відрізняється тим, що одну з вказаних у п. 9 сольватних форм суспендують у воді при температурі від 50 до 100°С.
14. Фармацевтична композиція, яка відрізняється тим, що містить аморфний ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он та/або висококристалічний ансольват
-метоксіестра-4,9-дієн-3-он та/або висококристалічний ансольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-ону за будь-яким з пп. 1-8 у сполученні з фармацевтично прийнятним носієм та/або розріджувачем.
-метоксіестра-4,9-дієн-3-ону за будь-яким з пп. 1-8 у сполученні з фармацевтично прийнятним носієм та/або розріджувачем.
15. Лікувальний засіб, призначений для контролю репродуктивної здатності у жінок, для лікування гормонозалежних гінекологічних розладів і для гормонзамісної терапії, який містить аморфний ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он та/або кристалічний ансольват
-метоксіестра-4,9-дієн-3-он та/або кристалічний ансольват ![]() -[4Е-(гідроксіімінометил)феніл]-
-[4Е-(гідроксіімінометил)феніл]-![]() -метоксиметил-
-метоксиметил-![]() -метоксіестра-4,9-дієн-3-он за будь-яким з пп. 1-8.
-метоксіестра-4,9-дієн-3-он за будь-яким з пп. 1-8.
Текст
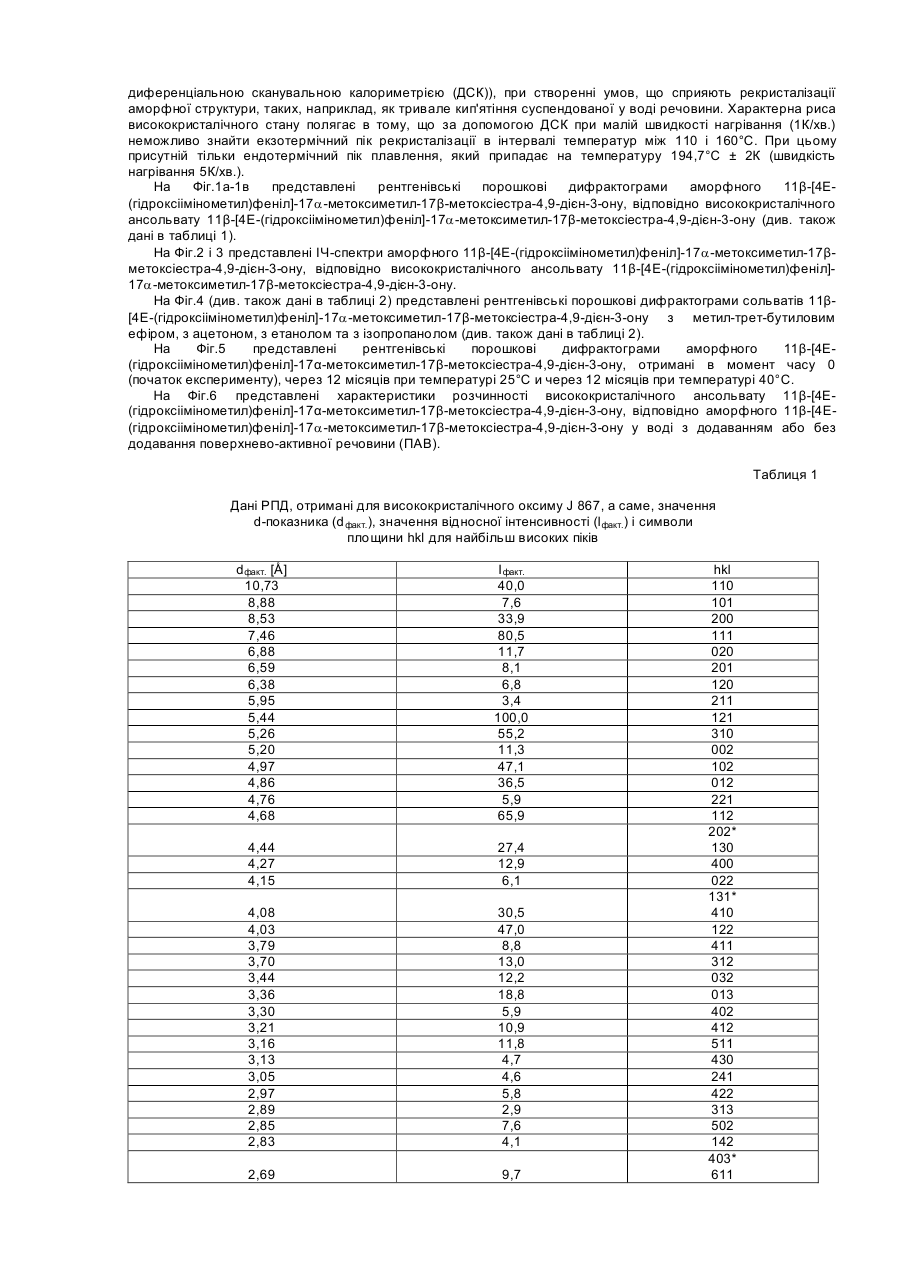
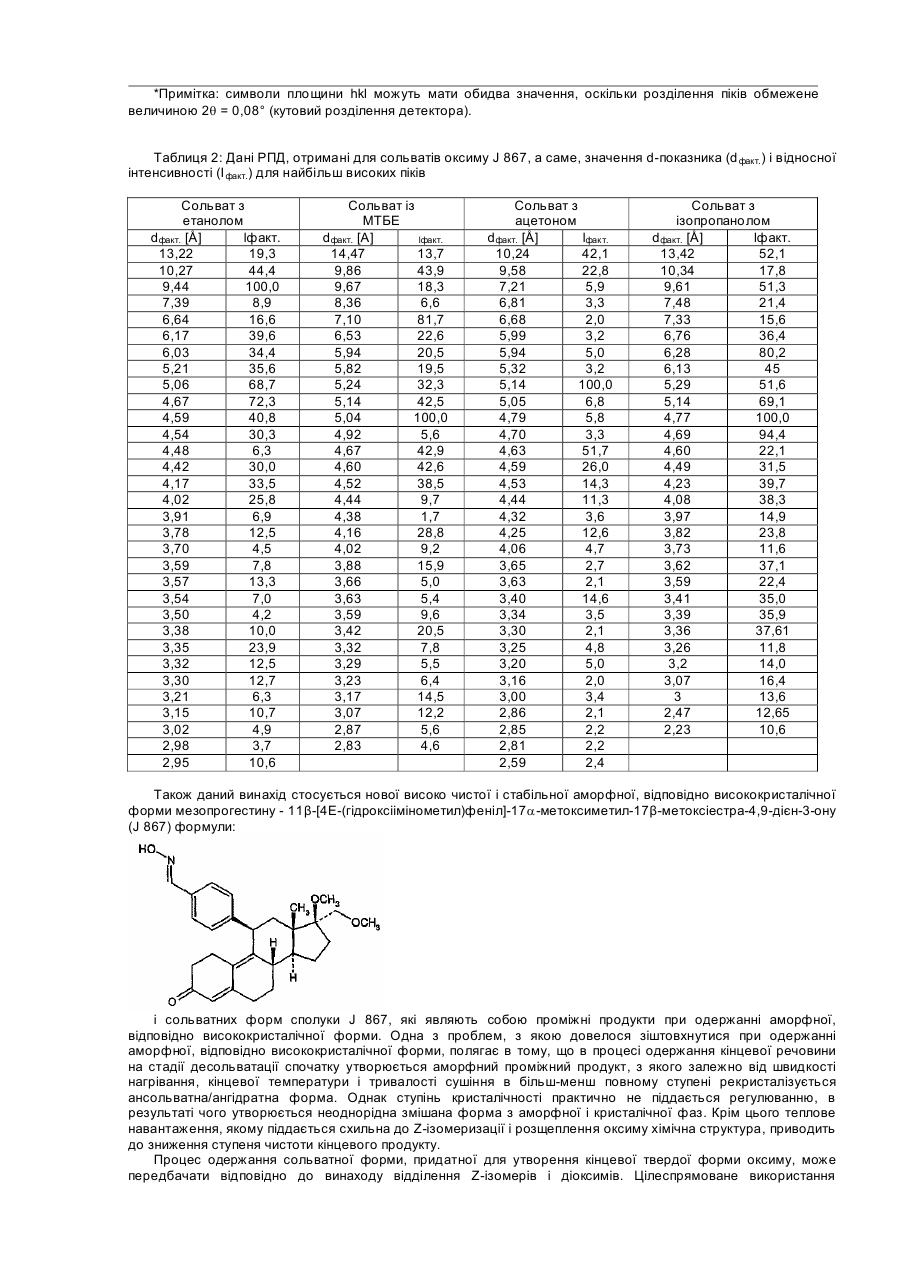
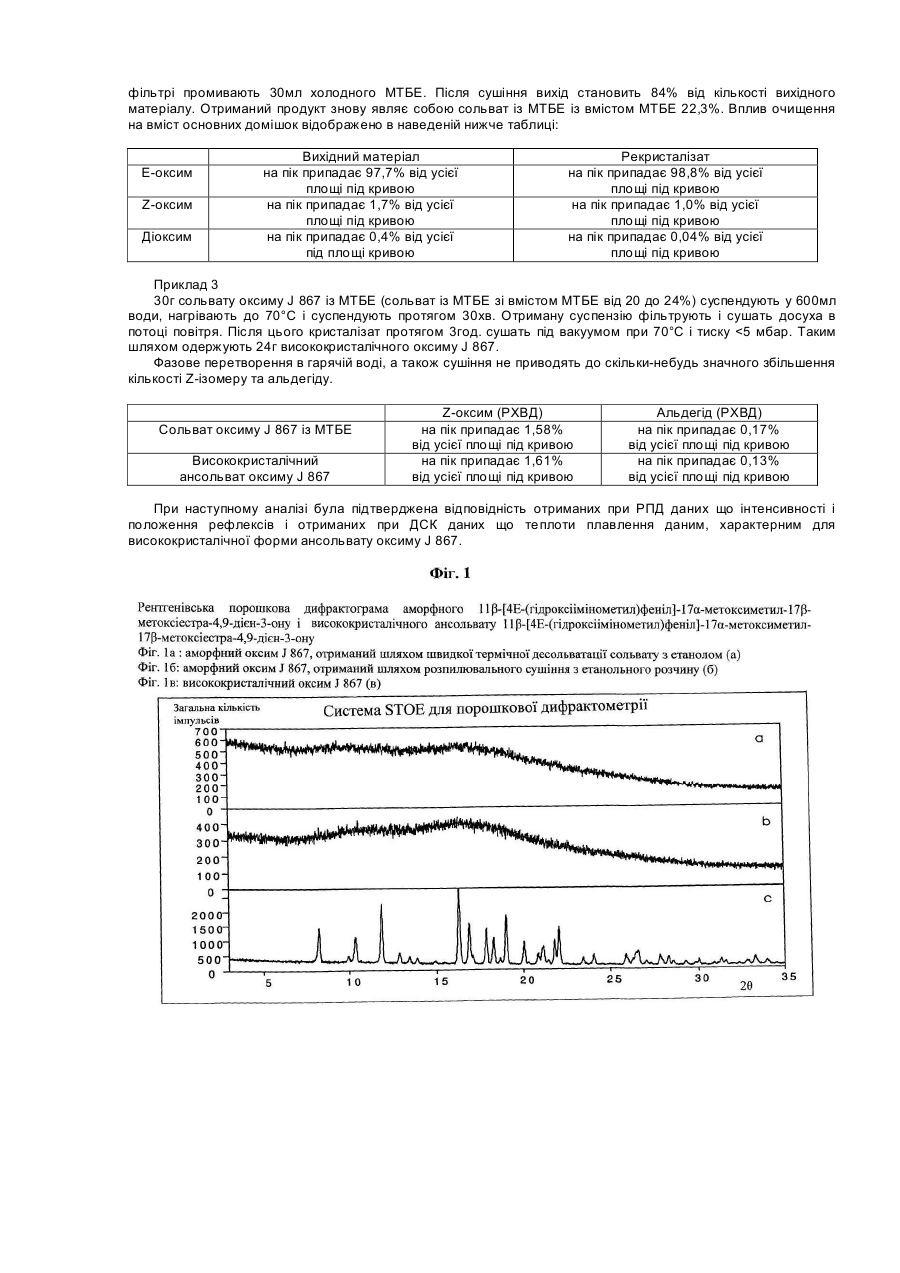
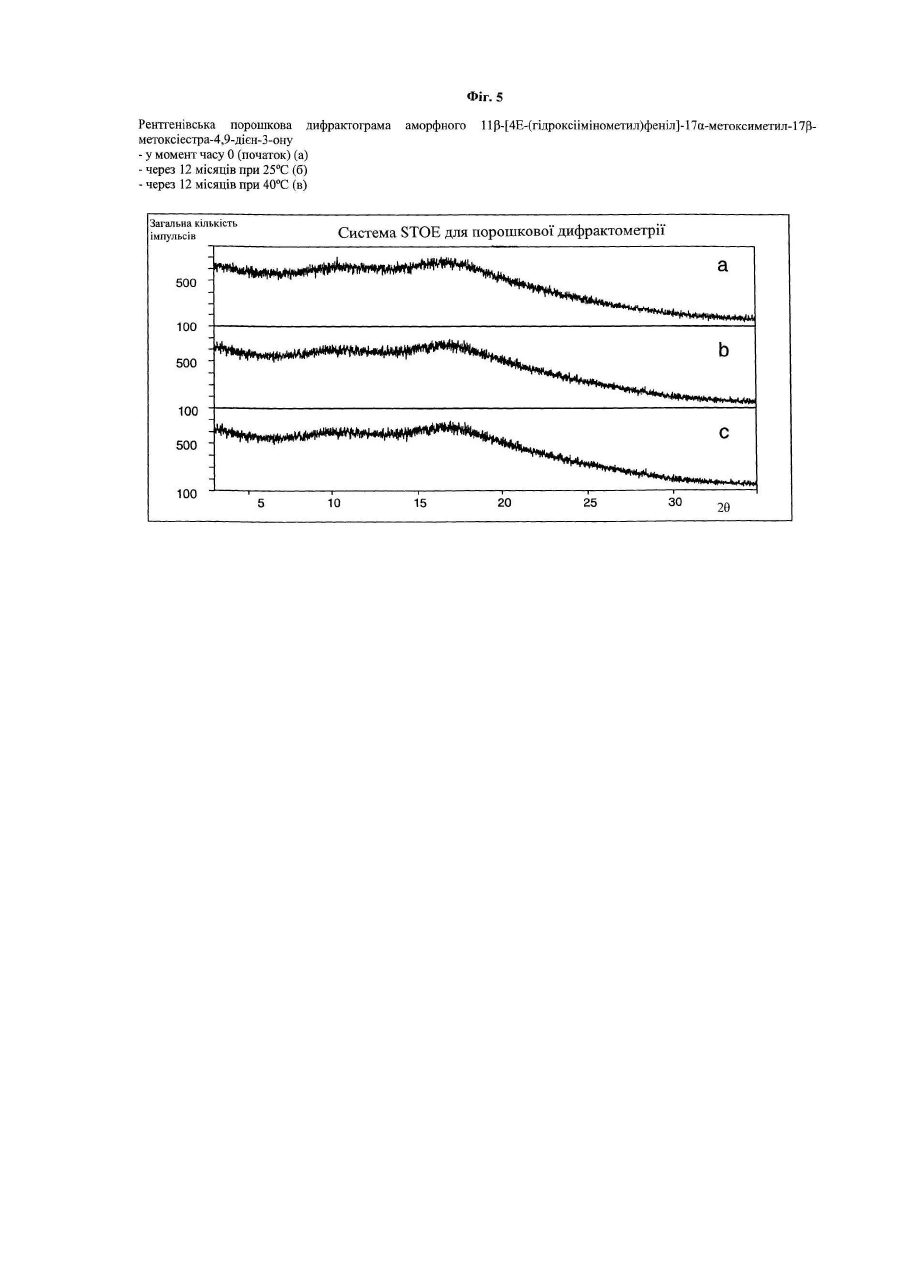
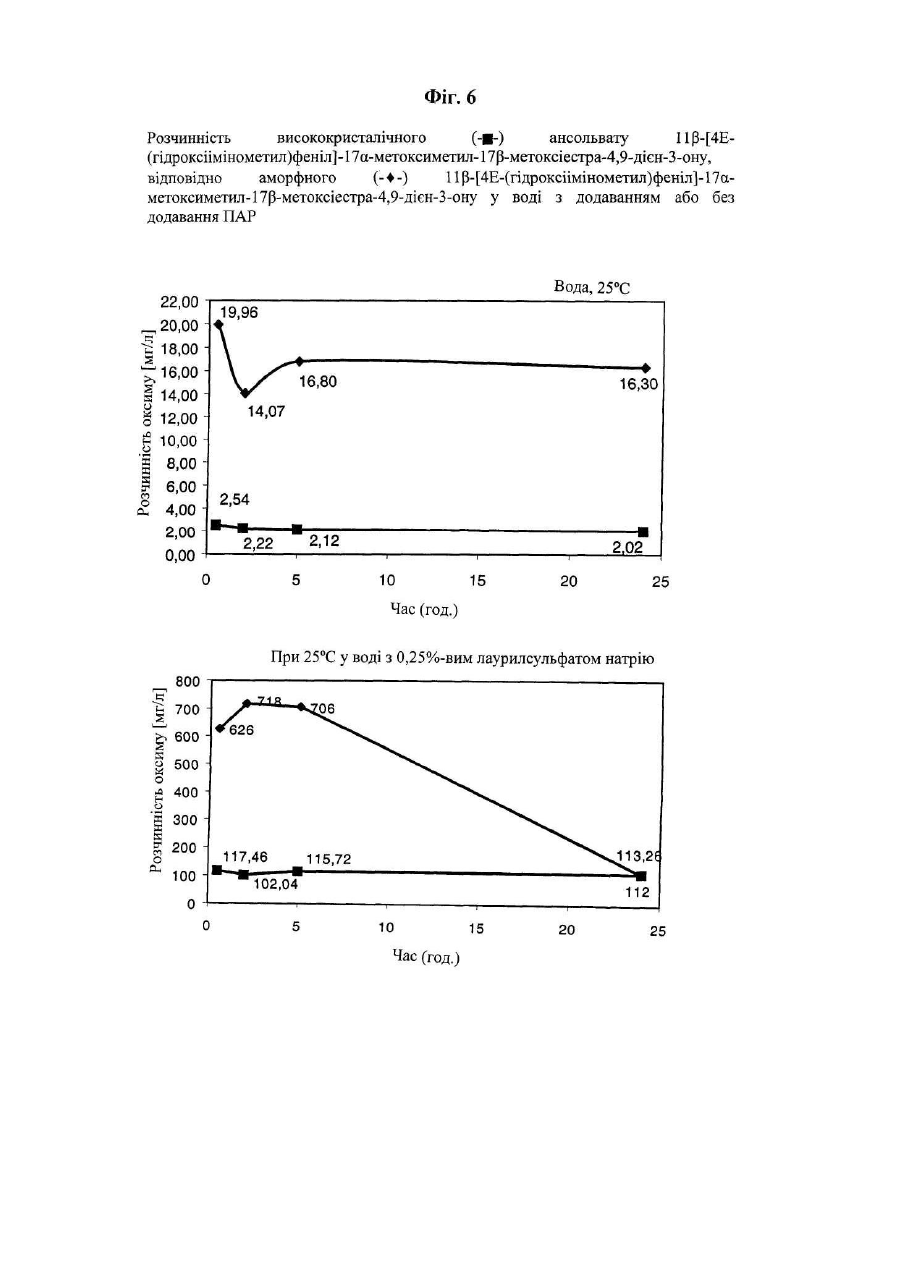
Даний винахід стосується нових твердих форм мезопрогестину - 11β-[4Е-(гідроксіімінометил)феніл]-17aметоксиметил-17a-метоксіестра-4,9-дієн-3-ону (який далі позначають як оксим J 867), насамперед високо чистої і стабільної аморфної, відповідно висококристалічної форми (у вигляді ансольвату/ангідрату) сполуки J 867, способу одержання таких форм, а також їх застосування у фармацевтичних композиціях. 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-он відомий, наприклад, із заявки ЕР-А 0648778, відповідно з заявки DE-A 4332283. Температура плавлення одержуваної відповідно до цих заявок шляхом перекристалізації із суміші метиленхлориду з ізопропанолом форми складає 113°С. Описана в вказаних заявках кристалічна форма являє собою утворений з ізопропанолом сольват, вміст ізопропанолу у якому складає 14% (див. дані рентгенівської порошкової дифрактометрії (РПД), які представлені нижче у таблиці 2 і на Фіг.4г). Характерною рисою оксиму є його яскраво виражена тенденція до викристалізовування з розчинників у вигляді сольвату. Однак сольватна форма власне кажучи не придатна для застосування у фармацевтиці. Це обумовлено винятково міцним зв'язком розчинника з речовиною, розрив якої можливий тільки при підвищених температурах. Повне відщеплення розчинника від сольватів оксиму звичайно відбувається тільки при температурі вище 100°С. При цьому в залежності від швидкості нагрівання утворюються неоднорідні змішані аморфно-кристалічні форми. Для очищення оксиму від побічних продуктів реакції оксимування (діоксимів, Z-оксиму) використовують трудомістку і складну в здійсненні колонкову хроматографію з градієнтним елююванням сумішшю толуолу з ацетоном. Очищення ж вказаного оксиму шляхом кристалізації ускладнено через його в цілому погану розчинність у розчинниках, що використовуються з цієї мети. Ще один фактор, який перешкоджає використанню кристалізації для очищення оксиму, полягає в тому, що при підвищених температурах у розчині відбувається ізомеризація Ε-ізомеру вказаної сполуки в його Z-ізомер. Виходячи з вищевикладеного, в основу даного винаходу була покладена задача замінити трудомістку і складну в здійсненні колонкову хроматографію іншим придатним для цих же цілей способом, а також одержати гомогенну і стабільну тверду форму, яка не містить розчинник, і властивості якої не обмежували б можливості її застосування у фармацевтиці. Вказана задача вирішується за допомогою аморфного 11β-[4Ε-(гідроксіімінометил)феніл]-17aметоксиметил-17β-метоксіестра-4,9-дієн-3-ону, який відрізняється тим, що на його рентгенівській порошковій дифрактограмі (РПД, Фіг.1а і 1б) відсутні характерні для кристалів рефлекси, і відповідно його модифікація характеризується представленим на Фіг.2 ІЧ-спектром. Поставлена у винаході задача вирішується також за допомогою висококристалічного ансольвату 11β-[4Е(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону. Така кристалічна форма ансольвату характеризується представленою на Фіг.1в рентгенівською порошковою дифрактограмою, відповідно представленим на Фіг.3 ІЧ-спектром. Кристалічні сольвати 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3ону можна одержувати способом, який полягає в тому, що а) одержують сольват 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3ону з наступним розчиненням цього сольвату понад граничну розчинність у розчиннику, насамперед у толуолі, який відмінний від утворюючого сольват розчинника та у якому кристалічна структура сольвату є нестабільною, б) необов'язково додають додатковий розчинник як інгібітор рекристалізації, насамперед метанол або етиловий ефір оцтової кислоти, і в) додають розчинник, який утворює сольват, насамперед етанол, ацетон і метил-трет-бутиловий ефір (МТБЕ), з наступною кристалізацією сольвату. Кристалічні сольвати 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3ону, а саме, сольват з метил-трет-бутиловим ефіром, сольват з ацетоном і сольват з етанолом, при цьому висококристалічні форми характеризуються представленими на Фіг.4а, 4б, 4в і у таблиці 2 рентгенівськими порошковими дифрактограмами, є новими сполуками і являють собою проміжні продукти в процесі одержання аморфного 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону, відповідно висококристалічного ансольвату 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9дієн-3-ону. В результаті висушування отриманих описаним вище способом кристалічних сольватів 11β-[4Е(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону, насамперед у результаті термічної десольватації переважно під вакуумом і зі швидкістю нагрівання продукту принаймні 0,5°С/хв. або з розчину сольвату шляхом розпилювального сушіння (РПД; Фіг.1) при температурі нижче температури склування аморфної структури, утворюється аморфна форма 11β-[4Ε-(гідроксіімінометил)феніл]-17aметоксиметил-17β-метоксіестра-4,9-дієн-3-ону. Висококристалічну форму 11β-[4Е-(гідроксіімінометил)феніл]17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону можна одержувати нагріванням сольватної, відповідної аморфної твердої форми, необов'язково у водній суспензії. Об'єктом даного винаходу є також фармацевтичні композиції, насамперед тверді фармацевтичні композиції, які містять описаний вище аморфний та/або висококристалічний 11β-[4Е(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-он у сполученні з фармацевтично прийнятним носієм та/або розріджувачем. Запропоновані у даному винаході фармацевтичні композиції одержують за відомою технологією шляхом переробки діючої речовини разом зі звичайними твердими чи рідкими носіями або розріджувачами і допоміжними речовинами, які звичайно використовують у фармацевтиці, з одержанням відповідних лікувальних форм, які містять діючу речовину в необхідному дозуванні, яке обумовлене методикою введення лікувального препарату. Під поняттям "висококристалічний" у контексті даного винаходу мається на увазі стан, після досягнення якого вже неможливо виявити подальше збільшення кристалічності, що піддається вимірюванню (РПД, диференціальною сканувальною калориметрією (ДСК)), при створенні умов, що сприяють рекристалізації аморфної структури, таких, наприклад, як тривале кип'ятіння суспендованої у воді речовини. Характерна риса висококристалічного стану полягає в тому, що за допомогою ДСК при малій швидкості нагрівання (1К/хв.) неможливо знайти екзотермічний пік рекристалізації в інтервалі температур між 110 і 160°С. При цьому присутній тільки ендотермічний пік плавлення, який припадає на температуру 194,7°С ± 2К (швидкість нагрівання 5К/хв.). На Фіг.1a-1в представлені рентгенівські порошкові дифрактограми аморфного 11β-[4Е(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону, відповідно висококристалічного ансольвату 11β-[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону (див. також дані в таблиці 1). На Фіг.2 і 3 представлені ІЧ-спектри аморфного 11β-[4Ε-(гідроксіімінометил)феніл]-17a-метоксиметил-17βметоксіестра-4,9-дієн-3-ону, відповідно висококристалічного ансольвату 11β-[4Ε-(гідроксіімінометил)феніл]17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону. На Фіг.4 (див. також дані в таблиці 2) представлені рентгенівські порошкові дифрактограми сольватів 11β[4Е-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-οну з метил-трет-бутиловим ефіром, з ацетоном, з етанолом та з ізопропанолом (див. також дані в таблиці 2). На Фіг.5 представлені рентгенівські порошкові дифрактограми аморфного 11β-[4Ε(гідроксіімінометил)феніл]-17α-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону, отримані в момент часу 0 (початок експерименту), через 12 місяців при температурі 25°С и через 12 місяців при температурі 40°С. На Фіг.6 представлені характеристики розчинності висококристалічного ансольвату 11β-[4Ε(гідроксіімінометил)феніл]-17α-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону, відповідно аморфного 11β-[4Ε(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону у воді з додаванням або без додавання поверхнево-активної речовини (ПАВ). Таблиця 1 Дані РПД, отримані для висококристалічного оксиму J 867, а саме, значення d-показника (d факт.), значення відносної інтенсивності (l факт.) і символи площини hkl для найбільш високих піків dфакт. [Å] 10,73 8,88 8,53 7,46 6,88 6,59 6,38 5,95 5,44 5,26 5,20 4,97 4,86 4,76 4,68 І факт. 40,0 7,6 33,9 80,5 11,7 8,1 6,8 3,4 100,0 55,2 11,3 47,1 36,5 5,9 65,9 4,44 4,27 4,15 27,4 12,9 6,1 4,08 4,03 3,79 3,70 3,44 3,36 3,30 3,21 3,16 3,13 3,05 2,97 2,89 2,85 2,83 30,5 47,0 8,8 13,0 12,2 18,8 5,9 10,9 11,8 4,7 4,6 5,8 2,9 7,6 4,1 2,69 9,7 hkl 110 101 200 111 020 201 120 211 121 310 002 102 012 221 112 202* 130 400 022 131* 410 122 411 312 032 013 402 412 511 430 241 422 313 502 142 403* 611 *Примітка: символи площини hkl можуть мати обидва значення, оскільки розділення піків обмежене величиною 2q = 0,08° (кутовий розділення детектора). Таблиця 2: Дані РПД, отримані для сольватів оксиму J 867, а саме, значення d-показника (d факт.) і відносної інтенсивності (І факт.) для найбільш високих піків Сольват з етанолом dфакт. [Å] lфакт. 13,22 19,3 10,27 44,4 9,44 100,0 7,39 8,9 6,64 16,6 6,17 39,6 6,03 34,4 5,21 35,6 5,06 68,7 4,67 72,3 4,59 40,8 4,54 30,3 4,48 6,3 4,42 30,0 4,17 33,5 4,02 25,8 3,91 6,9 3,78 12,5 3,70 4,5 3,59 7,8 3,57 13,3 3,54 7,0 3,50 4,2 3,38 10,0 3,35 23,9 3,32 12,5 3,30 12,7 3,21 6,3 3,15 10,7 3,02 4,9 2,98 3,7 2,95 10,6 Сольват із МТБЕ dфакт. [А] lфакт. 14,47 13,7 9,86 43,9 9,67 18,3 8,36 6,6 7,10 81,7 6,53 22,6 5,94 20,5 5,82 19,5 5,24 32,3 5,14 42,5 5,04 100,0 4,92 5,6 4,67 42,9 4,60 42,6 4,52 38,5 4,44 9,7 4,38 1,7 4,16 28,8 4,02 9,2 3,88 15,9 3,66 5,0 3,63 5,4 3,59 9,6 3,42 20,5 3,32 7,8 3,29 5,5 3,23 6,4 3,17 14,5 3,07 12,2 2,87 5,6 2,83 4,6 Сольват з ацетоном dфакт. [Å] lфакт. 10,24 42,1 9,58 22,8 7,21 5,9 6,81 3,3 6,68 2,0 5,99 3,2 5,94 5,0 5,32 3,2 5,14 100,0 5,05 6,8 4,79 5,8 4,70 3,3 4,63 51,7 4,59 26,0 4,53 14,3 4,44 11,3 4,32 3,6 4,25 12,6 4,06 4,7 3,65 2,7 3,63 2,1 3,40 14,6 3,34 3,5 3,30 2,1 3,25 4,8 3,20 5,0 3,16 2,0 3,00 3,4 2,86 2,1 2,85 2,2 2,81 2,2 2,59 2,4 Сольват з ізопропанолом dфакт. [Å] lфакт. 13,42 52,1 10,34 17,8 9,61 51,3 7,48 21,4 7,33 15,6 6,76 36,4 6,28 80,2 6,13 45 5,29 51,6 5,14 69,1 4,77 100,0 4,69 94,4 4,60 22,1 4,49 31,5 4,23 39,7 4,08 38,3 3,97 14,9 3,82 23,8 3,73 11,6 3,62 37,1 3,59 22,4 3,41 35,0 3,39 35,9 3,36 37,61 3,26 11,8 3,2 14,0 3,07 16,4 3 13,6 2,47 12,65 2,23 10,6 Також даний винахід стосується нової високо чистої і стабільної аморфної, відповідно висококристалічної форми мезопрогестину - 11β-[4Ε-(гідроксіімінометил)феніл]-17a-метоксиметил-17β-метоксіестра-4,9-дієн-3-ону (J 867) формули: і сольватних форм сполуки J 867, які являють собою проміжні продукти при одержанні аморфної, відповідно висококристалічної форми. Одна з проблем, з якою довелося зіштовхнутися при одержанні аморфної, відповідно висококристалічної форми, полягає в тому, що в процесі одержання кінцевої речовини на стадії десольватації спочатку утворюється аморфний проміжний продукт, з якого залежно від швидкості нагрівання, кінцевої температури і тривалості сушіння в більш-менш повному ступені рекристалізується ансольватна/ангідратна форма. Однак ступінь кристалічності практично не піддається регулюванню, в результаті чого утворюється неоднорідна змішана форма з аморфної і кристалічної фаз. Крім цього теплове навантаження, якому піддається схильна до Z-ізомеризації і розщеплення оксиму хімічна структура, приводить до зниження ступеня чистоти кінцевого продукту. Процес одержання сольватної форми, придатної для утворення кінцевої твердої форми оксиму, може передбачати відповідно до винаходу відділення Z-ізомерів і діоксимів. Цілеспрямоване використання термодинамічної нестабільності відповідних сольватів, переважно сольвату з метил-трет-бутиловим ефіром (МТБЕ), у середовищі придатному для цих цілей розчинника дозволяє повністю розчиняти сольватну решітку значно вище її граничної розчинності вже при температурах, близьких до кімнатної температури. Кристалічна форма сольвату з МТБЕ при її контакті з толуолом у масовому співвідношенні від 1:2 до 1:1 незважаючи на дуже низьку її розчинність у толуолі, що становить лише 3,3мас. %, швидко і повністю розчиняється вже при 20-50°С. При цьому відбувається так зване холодне плавлення. Подібний стан можна стабілізувати для наступного його технічного застосування шляхом додавання придатних для цієї мети розчинників як інгібіторів рекристалізації. Так, зокрема, перенасичений стан у толуоловому розчині можна стабілізувати на декілька годин додаванням метанолу в кількості лише 5об. %. Після цього в результаті додавання утворюючого сольват розчинника (МТБЕ) у прийнятній концентрації (наприклад 100-130об. % МТБЕ в перерахунку на кількість використовуваного толуолу) знову утворюється сольватна решітка, при цьому домішки здебільшого залишаються в розчині. Використання високошвидкісного методу сушіння, переважно розпилювального сушіння, проведеного при температурі нижче температури склування безпосередньо з розчину сольвату оксиму J 867 в органічному розчиннику, переважно етанолі, дозволяє одержувати стабільну повністю аморфну структуру, що не містить розчинника. З цією метою оксим, розчинений у етанолі в концентрації від 3 до 13мас. %, розпорошують через придатний для цієї мети розпилювальний пристрій (наприклад сопло для розпилення двокомпонентних матеріалів або відцентровий розпилювач) в атмосфері гарячого азоту і сушать протягом гранично короткого проміжку часу з одержанням аморфних дрібних частинок, розміри яких знаходяться у мікрометровому діапазоні. При цьому температура азоту на вході становить від 120 до 200°С, переважно від 150 до 180°С. Співвідношення між кількістю розчину оксиму і кількістю сушильного газу повинно становити при цьому від 0, 01 до 0,3кг розчину на м3 N2, переважно від 0,08 до 0,12кг розчину на м3 N2. Параметри процесу сушіння регулюють таким чином, щоб на виході із сушарки температура встановлювалася на рівні 55-95°С, переважно 75-85°С. Ця температура значно нижче температури склування аморфного оксиму (105°С), при якій речовина приймає гелеподібну/склоподібну консистенцію і вище якої може відбуватися більш-менш швидка, відповідно спонтанна рекристалізація. Використання розпилювального сушіння дозволяєодержувати за одну технологічну операцію гомогенну форму оксиму J 867 у вигляді дрібних твердих частинок, яка не містить розчинник. Перевага, пов'язана з застосуванням запропонованої у винаході аморфної форми оксиму J 867 для одержання лікувальних засобів, полягає в тому, що ця аморфна структура крім гарної розчинності має, як несподівано було встановлено, і винятково високу стабільність при зберіганні. Подібна аморфна структура навіть після закінчення 12 місяців її дослідженні в прискореному тесті на стабільність за методикою ІСН (40°С, 75%-ва відносна вологість) не виявляє ніяких ознак рекристалізації та/або хімічного розкладання (див. Фіг.5). Фізична структура оксиму залишається стабільною також у процесі його фармацевтичної переробки (вологе гранулювання, таблетування). Іншими словами, при цьому не відбувається перетворення аморфної форми у висококристалічну форму, відповідно E/Z-ізомеризації. Зберігання діючою речовиною стабільності протягом тривалого періоду часу дозволяє уникнути негативного впливу подібних перетворень на його біодоступність. Відносно стабільності при зберіганні все сказане вище справедливо й у відношенні застосування запропонованої у винаході висококристалічної форми оксиму J 867, при цьому, як і очікувалося, показники хімічної стабільності такої висококристалічної форми, насамперед у жорстких умовах (вплив високої температури і наявність високої вологості), перевищують показники стабільності аморфної форми. Аморфна форма має, крім того, винятково високі показники розчинності. Так, зокрема, гранична розчинність цієї форми у воді, а також у розчині ПАВ (0,25%-вий лаурилсульфат натрію) приблизно в 7-8 разів перевищує відповідний показник висококристалічної форми, при цьому настільки високий рівень перенасичення залишається стабільним протягом декількох годин, наприклад у випадку водного розчину зберігається більш 24год. (див. Фіг.6). Висококристалічну форму можна одержувати виходячи з однієї із сольватних форм оксиму J 867. З цією метою таку сольватну форму можна суспендувати у воді при температурі від 50 до 100°С, при цьому розчинник відщеплюється вже при температурі, що значно нижче температури десольватації сухої сольватної форми. У випадку сольвату з МТБЕ навіть короткочасна його обробка (порядку 10-30хв.) водою при температурі від 65 до 75°С призводить до повного його перетворення у висококристалічну форму. Запропонований у винаході спосіб і насамперед термічна десольватація в принципі дозволяє одержувати залежно від технологічних умов змішані аморфно-кристалічні форми, що, однак, не вдається одержувати з досить високим ступенем відтворювання, чим при підготовці технічного обґрунтування з промислового впровадження технологічного процесу може бути обумовлене виникнення значних проблем, пов'язаних з контролем якості продукції, з її наступною переробкою у фармацевтичних цілях і з одержанням дозволу на використання отриманих на її основі лікувальних засобів. Оксим J 867 являє собою відповідно до заявки ЕР-А 0648778, відповідно заявки DE-A 4332283 діючу речовину, яка має антигестагенну активність, і яка при однаковій зі сполукою RU 486 (міфепристон) активності у відношенні рецептора прогестерону має істотно більш низьку в порівнянні з цією сполукою RU 486 антиглюкокортикоїдну активність. У заявках на патент США 09/386141, 09/386140 і 09/386133 оксим J 867 позначений як мезопрогестин. При цьому такі мезопрогестини охарактеризовані як сполуки, які in vivo мають і агоністичну, і антагоністичну активність у відношенні рецептора прогестерону (PR). Гестаген і антигестаген не дозволяють досягти відповідних функціональних станів. Оксим J 867 придатний для застосування насамперед у наступних цілях: а) Відповідно до заявки на патент США 09/386133 оксим J 867, необов'язково разом з естрогеном, можна використовувати для одержання лікувального засобу, призначеного для жіночої контрацепції. б) Відповідно до заявки на патент США 09/386141 оксим J 867 може використовуватися для лікування і попередження доброякісних, гормонозалежних гінекологічних розладів, наприклад - для лікування таких гінекологічних розладів, як ендометріоз, фіброма матки, післяопераційні перитонеальні спайки, дисфункціональна кровотеча (метрорагія, менорагія) і дисменорея; - для попередження таких гінекологічних розладів, як утворення післяопераційних перитоніальних спайок, дисфункціональна маткова кровотеча (метрорагія, менорагія) і дисменорея. При цьому щоденна доза мезопрогестину становить від 0,5 до 100мг, переважно від 5,0 до 50мг, найбільш переважно від 10 до 25мг. в) Відповідно до заявки на патент США 09/386140 оксим J 867 також можна використовувати як фармацевтичний компонент при одержанні лікувального засобу, необов'язково разом з естрогеном, призначеного для гормонзамісної терапії (ГЗТ), а також для лікування гормональної недостатності і симптомів, пов'язаних з порушенням гормональної функції. Методи вимірювань Рентгенівська порошкова дифрактометрія (РПД) Дані одержували за допомогою порошкового дифрактометра типу STADIP фірми STOE з германієвим монохроматичним СuКa 1- випромінюванням (l =1,540598 Å) у діапазоні 3°£2q£35°, відповідно за допомогою дифрактометра типу D5000 фірми Siemens із Cu-анодом (5°£2θ£50°). ІЧ-спектроскопія Для спектроскопії використовували прилад типу 20 SXB фірми NICOLET з фотоакустичним детектором типу МТЕС (KBr, 8t, 90с). Дослідження розчинності 200мг речовини додавали при 25°С в 50мл води (без або з 0,25%-ним додецилсульфатом натрію (лауритсульфатом натрію). Проби відбирали через 0,5год., 2год., 5год. і 24год. Відбір проб: фільтрувальна насадка з розміром пор 0,45мкм, розведення МеОН у співвідношенні 1:1, РХВД. Рідинна хроматографія високого дозволу (РХВД) Чистоту продукту визначали з використанням наступного устаткування й у наступних умовах: Колонка: Superspher Si 60 розміром 250x4мм, 4мкм. Елюент: хлороформ (3%-вий етанол)/вода в співвідношенні 96,9:0,1. Швидкість потоку: 1мл/хв. Виявлення: УФ (з довжиною хвилі 299нм). Обробка результатів вимірювань: 100%-ва нормалізація за площею поверхні. Газова хроматографія в паровій фазі для визначення залишкового розчинника Автоматизована система для ГХ, оснащена приладом типу HS40 фірми Perkin Elmer, колонка типу DBWax розміром 30м x 0,23мм, FID. Гранулометричний аналіз Прилад типу HELOS (H0445) фірми Sympatec, система для сухого диспергування (диспергатор типу RODOS), тиск 2 бари. Диференціальна сканувальна калориметрія (ДСК) Прилади типу DSC 7 фірми Perkin Elmer і DSC 200/1/F фірми NETZSCH в алюмінієвому піддоні, перфорована кришка, азот. Нижче винахід проілюстрований на прикладах. Приклади Приклад 1 2кг оксиму J 867 (сольват із МТБЕ зі вмістом МТБЕ від 20 до 24%; дані про відсотковий вміст розчинника в сольватах відповідають, якщо не вказане інше, масовим відсоткам (мас. %)) при 50°С розчиняють при перемішуванні в 20л етанолу. Далі розчин піддають у прямотоці розпилювальному сушінню в розпилювальній сушарці, що працює в інертних умовах (атмосфера азоту). Через сушильну камеру розпилювальної сушарки пропускають попередньо нагрітий до 175°С азот з витратою 60м3/год. Після цього в сушильній камері за допомогою сопла для розпилення двокомпонентних матеріалів, у якому як робочий (ежектуючий) газ використовується азот під тиском 3 бари, розпорошують приготовлений розчин, подаючи його шланговим насосом з витратою 6,4л/год. Температура сушильного газу на виході становить 79-83°С. Оксим J 867, висушений до дрібних частинок, розміри яких знаходяться у мікрометровому діапазоні, повністю уловлюють на фільтрі для продукту. Оксим J 867 має наступні якісні характеристики: Залишковий розчинник Вода Величина частинок Чистота (вміст Z-оксиму) РПД 0,44% етанолу, 0,11% МТБЕ 0,5% 100%
ДивитисяДодаткова інформація
Назва патенту англійськоюSolid body forms of mesoprogestin -11b-[4е-(hydroxy iminomethyl)-phenyl]-17a-methoxy-17b-methoxy-estra-4,9-dien-3-one
Автори англійськоюMueller, Uwe, Winter, Gabriele
Назва патенту російськоюТвердые формы мезопрогестина-11b-[4е-(гидроксииминометил)-фенил]-17a-метоксиметил-17b-метоксиэстра-4,9-диен-3-она
Автори російськоюМюллер Уве
МПК / Мітки
МПК: C07J 41/00, A61K 31/569, A61P 15/08, A61P 5/36, A61P 15/18, A61P 15/12
Мітки: форми, тверді, мезопрогестину-11b-[4е-(гідроксіімінометил)-феніл]-17a-метоксиметил-17b-метоксіестра-4,9-дієн-3-ону
Код посилання
<a href="https://ua.patents.su/10-73988-tverdi-formi-mezoprogestinu-11b-4e-gidroksiiminometil-fenil-17a-metoksimetil-17b-metoksiestra-49-diehn-3-onu.html" target="_blank" rel="follow" title="База патентів України">Тверді форми мезопрогестину-11b-[4е-(гідроксіімінометил)-феніл]-17a-метоксиметил-17b-метоксіестра-4,9-дієн-3-ону</a>
Попередній патент: Колісний хід борони дискової важкої
Наступний патент: Високоміцний, корозійностійкий суперсплав на основі нікелю та спрямовано скристалізована деталь
Випадковий патент: Генераторне джерело електроенергії