Фармацевтична композиція антимікотиків і пребіотиків і спосіб лікування кандидозних вагінітів
Номер патенту: 96240
Опубліковано: 10.10.2011
Автори: Рудой Боріс Анатольєвіч, Дорожко Олєг Валентіновіч, Діковскій Алєксандр Владіміровіч
Формула / Реферат
1. Фармацевтична композиція для профілактики й лікування вагінозів, вагінітів і вульвовагінітів, виконана у формі, що є придатною для місцевої аплікації, яка містить щонайменше один антимікотик, а також пребіотик зі ступенем полімеризації від 2 до 30 або комбінацію пребіотиків, що змішані в наступних концентраціях (вага/об'єм), з розрахунку на масу композиції:
щонайменше один антимікотик
від 0,0001 до 5 %
пребіотик або комбінація пребіотиків
від 0,1 до 40 %
основа та/або допоміжні речовини
решта.
2. Фармацевтична композиція за п. 1, яка відрізняється тим, що як антимікотик використовують антибіотики й фунгіцидні препарати, вибрані із групи азолів: терконазол, тіоконазол, бутоконазол, кетоконазол, клотримазол, міконазол, омоконазол, фентиконазол, оксиконазол, біфоназол, еконазол, ізоконазол; аліламінів: нафтифін, тербінафін; полієнових антибіотиків: амфотерицин В, натаміцин, ністатин, леворин; нітрофуранів: ніфуратель, фуразолідон, а також їхні фармацевтично прийнятні комбінації.
3. Фармацевтична композиція за п. 1, яка відрізняється тим, що містить фармацевтично прийнятні концентрації пребіотиків, вибраних з груп природних або синтетичних сахаридів і олігосахаридів: лактулоза, фруктоолігоцукри, галактоолігоцукри, ксилоолігоцукри, мальтоолігоцукри, ізомальтоолігоцукри, або їхні комбінації.
4. Фармацевтична композиція за п. 1, яка відрізняється тим, що виробляється в лікарській формі супозиторіїв, песаріїв, глобул, м'яких капсул, тампонів, кремів, гелів, емульсій і інших форм для місцевої аплікації.
5. Спосіб лікування вагінозів, вагінітів і вульвовагінітів грибкової або бактеріальної етіології з використанням фармкомпозицій антимікотиків і пребіотиків за будь-яким з пп. 1-4 у лікарській формі для місцевої аплікації, заснований на інгібуванні росту патогенних грибів і дріжджів антимікотиками з одночасною стимуляцією росту нормальних представників мікрофлори піхви.
6. Спосіб за п. 5, який відрізняється тим, що фармкомпозиція антимікотиків і пребіотиків використовується для місцевої терапії в лікарській формі супозиторіїв, глобул, песаріїв, тампонів, м'яких желатинових капсул, таблеток, кремів, мазей, гелів, суспензій, розчинів і т. д.
Текст
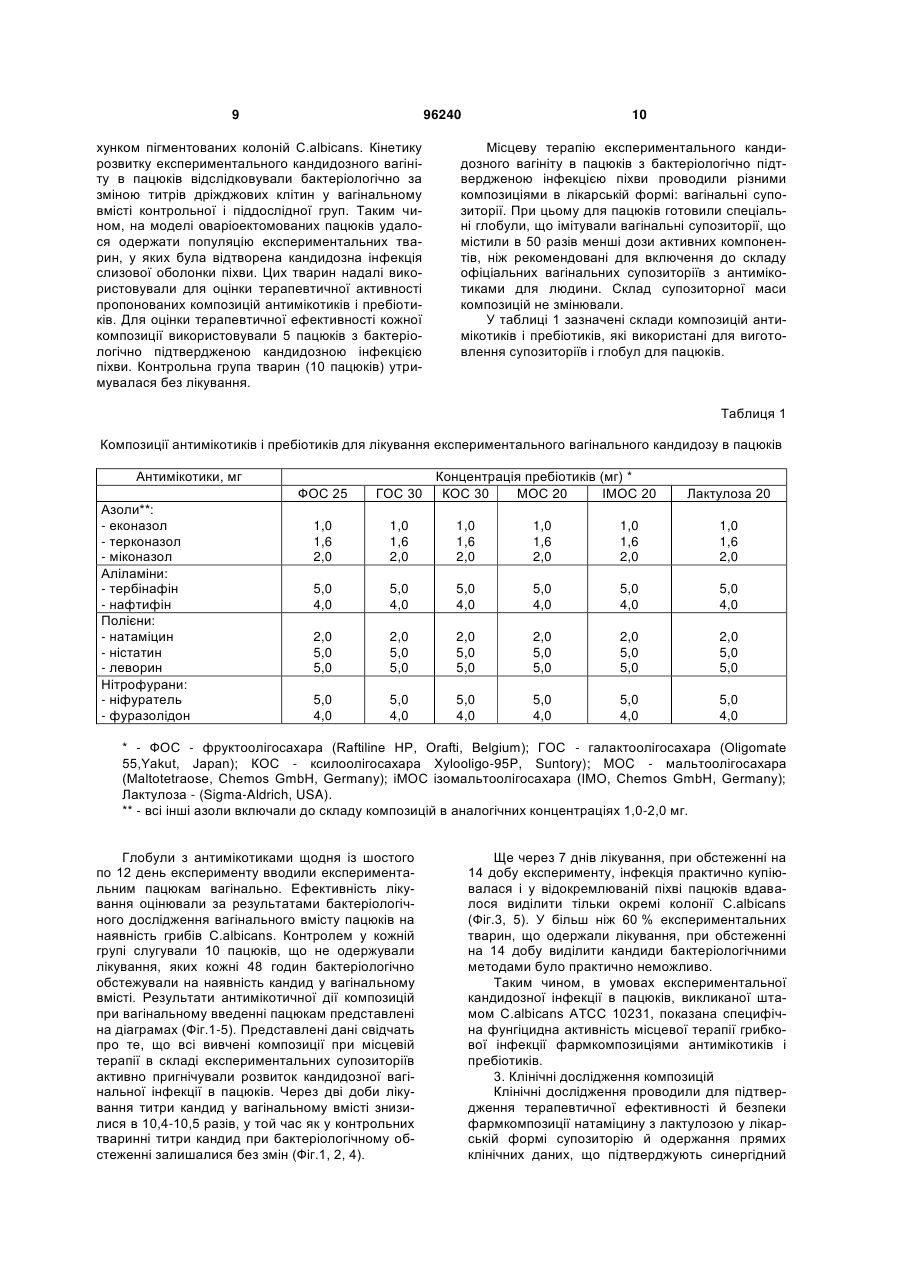
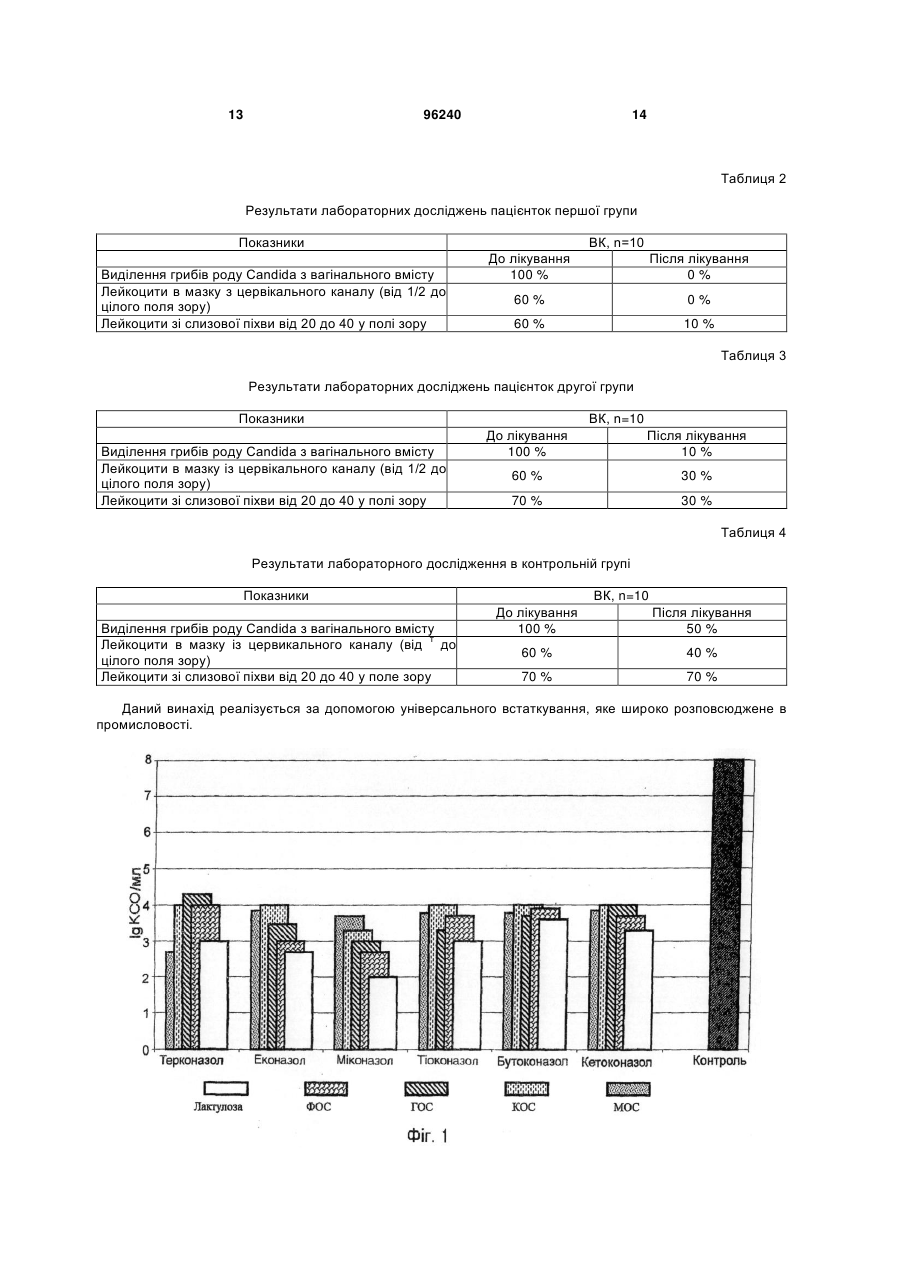
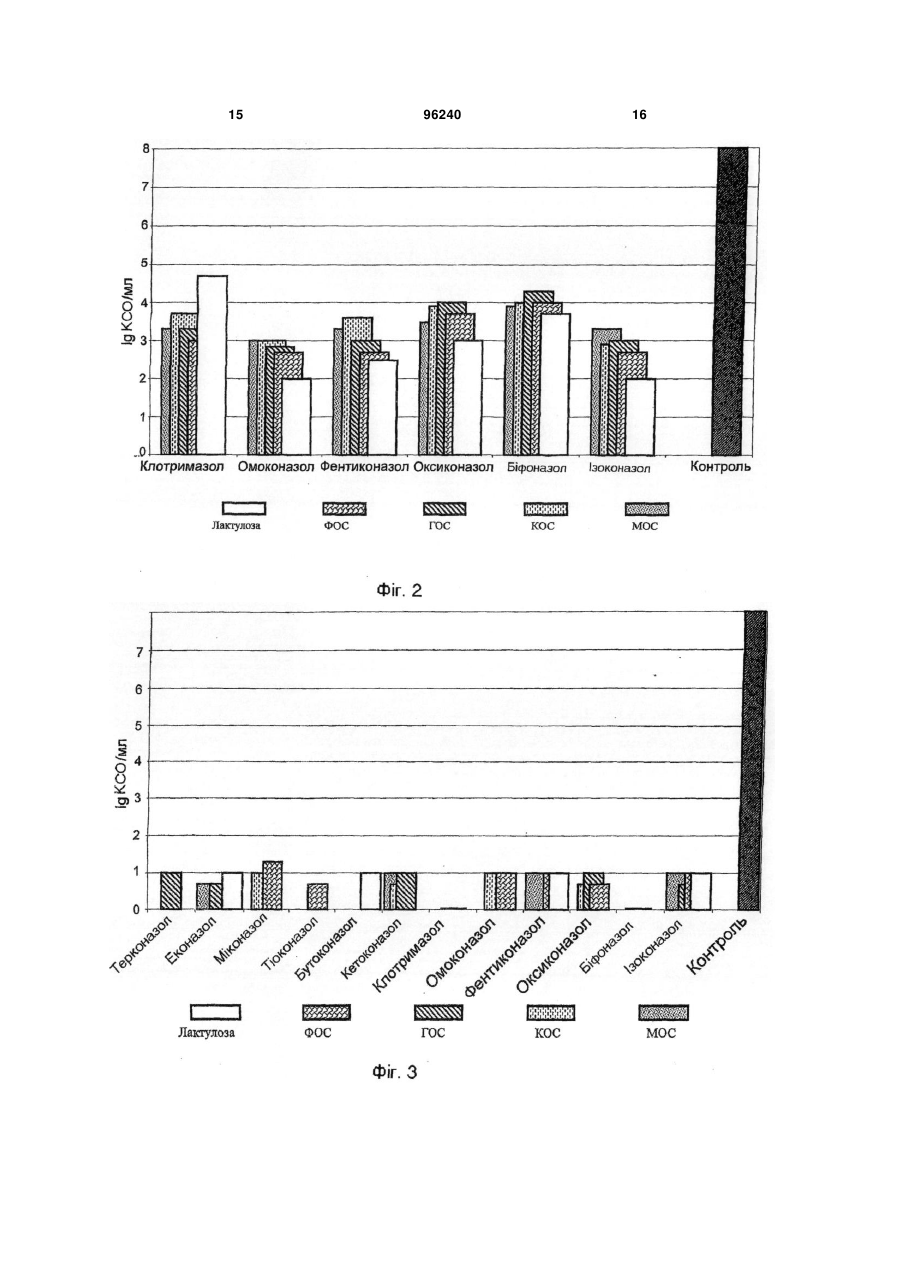
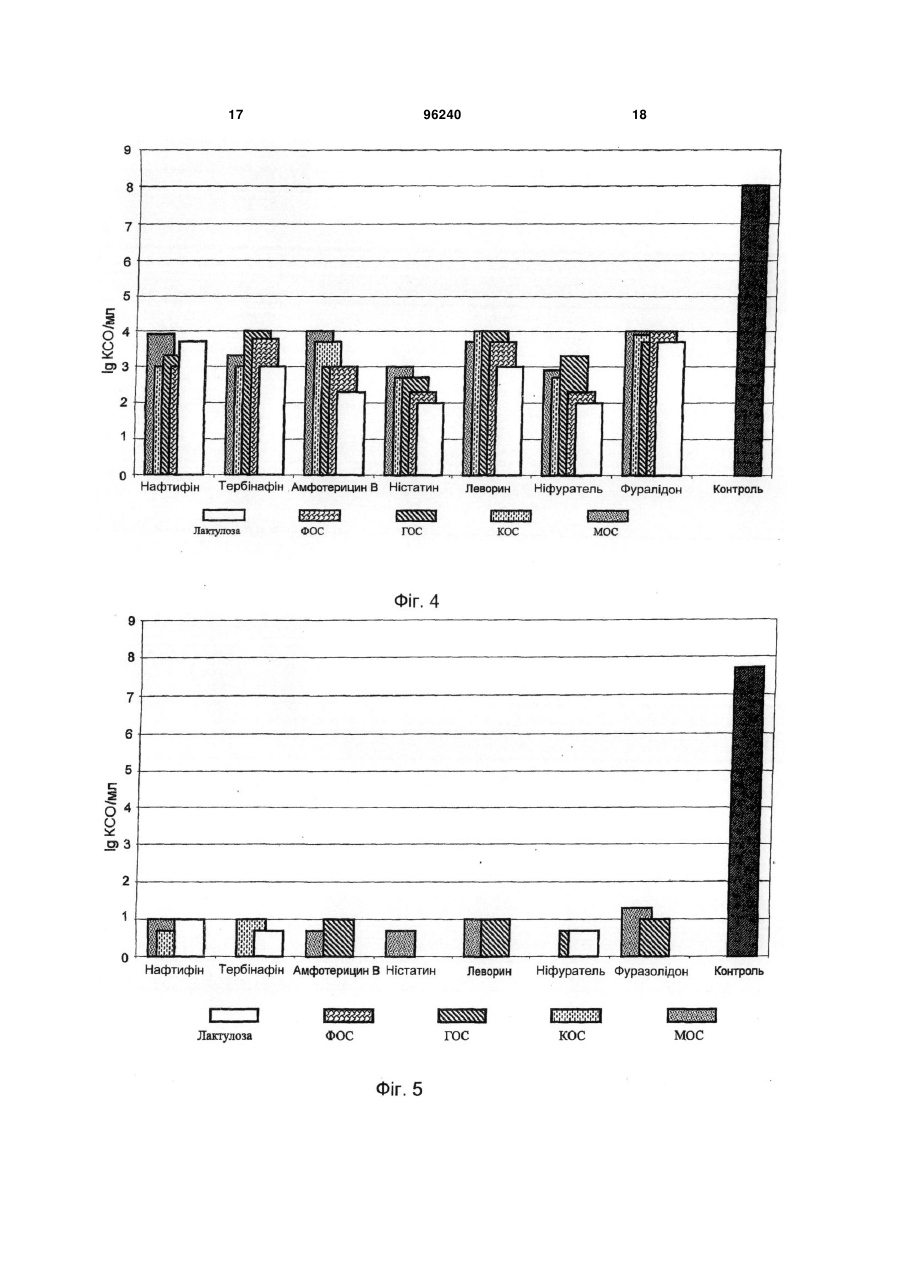
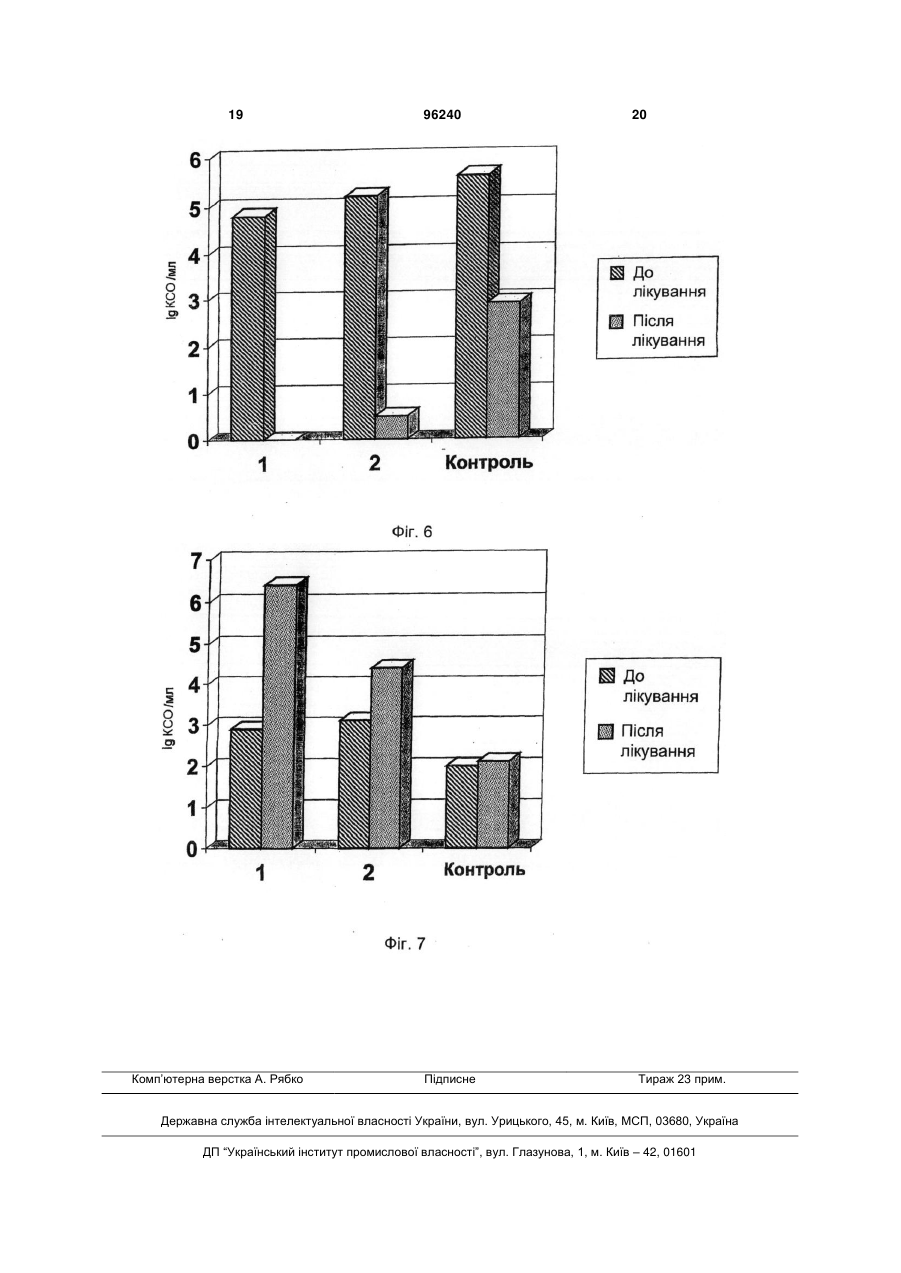
1. Фармацевтична композиція для профілактики й лікування вагінозів, вагінітів і вульвовагінітів, виконана у формі, що є придатною для місцевої аплікації, яка містить щонайменше один антимікотик, а також пребіотик зі ступенем полімеризації від 2 до 30 або комбінацію пребіотиків, що змішані в наступних концентраціях (вага/об'єм), з розрахунку на масу композиції: щонайменше один антимікотик від 0,0001 до 5 % пребіотик або комбінація пребіотиків від 0,1 до 40 % основа та/або допоміжні речовини решта. 2. Фармацевтична композиція за п. 1, яка відрізняється тим, що як антимікотик використовують антибіотики й фунгіцидні препарати, вибрані із групи азолів: терконазол, тіоконазол, бутоконазол, C2 2 (19) 1 3 зок вульви й піхви 30-45 %. Збудником кандидозного вульвовагініту є дріжджоподібні гриби роду Candida. У цей час описано понад 170 видів дріжджоподібних грибів. Найчастішими збудниками вульвовагінального кандидозу в 85-90 % пацієнток є C.albicans. Серед інших видів Candida клінічне значення мають C.glabrata (5-10 %), C.tropicalis (35 %), C.parapsilosis (3-5 %) і C.crusei (1-3 %). Значне підвищення захворюваності кандидозним вульвовагінітом обумовлено дією ряду сприяючих факторів, таких як тривалий і безконтрольний прийом антибіотиків, кортикостероїдів, цитостатиків, оральних контрацептивів, променева терапія, важкі інфекційні захворювання, ендокринні порушення, імунодефіцитні стани та ін. При призначенні антибіотиків широкого спектра не враховується, що вони пригнічують не тільки патогенні бактерії, але й сапрофіти, що перебувають на слизовій піхви: лактобацили й біфідобактерії. У результаті рН піхвового вмісту підвищується (зрушується в лужну сторону), а процеси самоочищення порушуються. Крім того, гриби роду Candida мають здатність використовувати деякі антибіотики як живильні субстрати. При цьому створюються сприятливі умови для активного розмноження Candida в полових органах жінки. Зміні рН піхвового секрету сприяють і гормональні препарати. Значне збільшення захворюваності кандидозним вагінітом пов'язано, головним чином, із застосуванням оральних контрацептивів. Виявлено, що при прийманні гормональних препаратів підвищується концентрація глікогену в клітинах вагінального епітелію, відбувається його розпушення, рН зрушується в лужну сторону й відбувається зниження неспецифічної резистентності. В 20 % жінок, що приймають оральні контрацептиви, змінюється толерантність до глюкози, що сприяє кандидозній інфекції. Вагітність, у зв'язку зі зміною гормонального фона, також сприяє розвитку кандидозів. Про зв'язок кандидозного вульвовагініту з вагітністю свідчить різке зменшення (на 60 %) частоти позитивних результатів виділення грибів у післяпологовому періоді. Розвитку кандидозного вульвовагініту сприяє використання білизни із синтетичних тканин, що щільно облягає тіло й створює мікроклімат з підвищеною вологістю й температурою. Гриби роду Candida можуть бути виділені з піхви практично здорових жінок при відсутності клінічних ознак кандидозного вульвовагініту (носіння). За певних умов під дією екзогенних і/або ендогенних факторів ці гриби стають патогенними. При наявності істотних факторів ризику, наприклад, при вагітності, усяке виявлення в піхві грибів роду Candida свідчить про наявність кандидозного вульвовагініту, а не про носіння. Це підтверджується результатами дослідження, у якому тільки в 2 % вагітних з висівами C.albicans з піхви була встановлена відсутність яких-небудь патологічних змін. Існують дані, що при рецидивному кандидозному вульвовагініті постійним резервуаром грибів і джерелом реінфекції піхви слугує шлунковокишковий тракт. У тих випадках, коли гриби висі 96240 4 вають із піхви, вони майже завжди виявляються й у фекаліях, причому в більшості випадків і піхвові, і інтестинальні штами ідентичні. Звичайно кандидоз виникає ендогенно, як наслідок дисбіозів, метаболічних розладів і дисфункцій імунної системи. З огляду на те, що штами C.albicans, що виділені у хворих кандидозним вульвовагінітом і в носіїв, істотно не розрізняються, можна зробити висновок про провідну роль імунної системи в розвитку кандидозного вульвовагініту. У цей час відомо кілька класів антимікотиків для лікування кандидозних вульвовагінітов. Це імідазоли: клотримазол, міконазол, оксиконазол, біфоназол, еконазол, омоконазол, фентиконазол, ізоконазол, терконазол, тіоконазол, кетоконазол; циклопірокс; аліламіни: нафтифін; полієнові антибіотики: амфотерицин, ністатин, леворин і натаміцин; триазоли: флуконазол, ітраконазол і інші фунгіцидні й фунгістатичні препарати. Зазначені антимікотики входять до складу лікарських форм, які використовують для місцевого й системного лікування кандидозних вагінітів і вульвовагінітів, а також у складі кремів, емульсій і гелів для нанесення на шкіру й слизові оболонки в місцях грибкових поразок. Відомі пребіотики - неперетравлювані елементи харчових продуктів, які в організмі людини стимулюють ріст і розвиток домінантних видів бактерій у мікробіоценозі товстого кишечника. Це лактобацили й біфідобактерії, які використовують пребіотики як джерела вуглеводів (US №6455068, 2002). У хімічному відношенні пребіотики представлені коротколанцюжковими оліго й дисахаридами (фруктоолігосахариди, галактоолігосахариди, мальтоолігосахариди, лактулоза й т.д.), які входять до складу багатьох харчових продуктів. При потраплянні в організм олігосахариди не розщеплюються у верхніх відділах шлунково-кишкового тракту й досягають товстого кишечника в незміненому вигляді. Тут вони утилізуються біфідобактеріями й лактобацилами, за що одержали найменування "біфідогенних факторів". Стимуляція росту індигенної мікрофлори кишечника пов'язана з інгібуванням росту патогенної мікрофлори, підвищенням бар'єрних функцій слизових оболонок кишечника й резистентністю до колонізації кишечника сторонньою мікрофлорою, включаючи патогенні гриби й дріжджі. У нормі вагінальна мікрофлора також включає грампозитивні й грамнегативні аеробні й анаеробні види мікроорганізмів. Домінуючим видом вагінальної мікрофлори є лактобацили. Для них оптимальними умовами культивування є анаеробні при низьких значеннях рН (5,5-6,5). У здорових жінок вагінальна мікрофлора повноцінно забезпечує механізм захисту від суперінфікування піхви патогенними бактеріями й грибами, підтримуючи низькі значення рН. При мікробіологічному обстеженні здорових жінок репродуктивного віку лактобацили в складі вагінальної мікрофлори визначаються в 97,8 %, з них Lactobacillus acidophilus в 86,7 %; біфідобактерії в 62,2 %, з них Bifidobacterium adolescentis в 5 20,0 % випадків. За різним даними лактобацили присутні у вмісті вапни в 70-100 % випадків. Зниження титру лактобацил у піхві є результатом зниження конкуренції за живильні субстрати й відбувається у зв'язку з підвищенням значень рН в умовах інтенсивного зростання й розмноження опортуністичної мікрофлори, що у нормальних умовах пригнічується продуцентами молочної кислоти. Захисні властивості нормофлори піхви проти екзогенних патогенів реалізуються різними способами: за рахунок антагоністичної активності, конкуренції за субстрати, здатності продукувати лізоцим, адгезивних властивостей, але головні механізми - це, безумовно, продукція молочної кислоти й перекису водню. Таким чином, головною терапевтичною проблемою в лікуванні кандидозних вульвовагінітів є відновлення нормальної мікрофлори піхви, коли фізіологічні механізми колонізації слизової оболонки сапрофітами сприяють пригніченню росту потенційних патогенів, у ролі яких найчастіше виступають гриби роду Candida. Антимікотики пригнічують ріст грибів і сприяють елімінації збудника, однак не створюють умов для відновлення нормальної мікрофлори піхви, що при постійній фізіологічній суперінфекції кандидами провокує рецидиви вагінальних кандидозів. Для відновлення нормальної мікрофлори в процесі лікування кандидозних вульвовагінітів пропонувалося використання пребіотику лактулози у формі вагінальних тампонів (US №377518, 1973). Однак недоліком даного винаходу є використання лактулози у формі сиропу, що має більше 40 % домішок інших сахаридів (лактоза, фруктоза, галактоза), які стимулюють ріст умовно-патогенних і патогенних видів мікроорганізмів. Пропонована лікарська форма тампонів, просочених рідким сиропом лактулози, незручна у використанні, тому що в момент аплікації частина лактулози видавлюється із тканини й бруднить білизну. Крім того, використання тампонів, просочених сиропом лактулози, небезпечно, тому що може викликати масове розмноження й лізис патогенних мікроорганізмів усередині тампона й усмоктування бактеріальних ендо й екзотоксинів слизовою оболонкою піхви. У тампонах, просочених сиропом лактулози, немає антисептичних компонентів, тому елімінація кандид відбувається повільно в процесі відновлення нормофлори піхви й конкурентного інгібування росту грибів, з огляду на конкуренцію за живильні субстрати в мікробній асоціації, що представлена бацилами, бактеріями й грибами. Технічним завданням даного винаходу є створення ефективної фармацевтичної композиції й способу лікування кандидозного вульвовагініту. Технічний результат, що забезпечує рішення поставленого завдання, полягає в тому, що пропонується фіксована фармацевтична композиція антимікотиків і пребіотиків для місцевої аплікації, наприклад, у лікарській формі вагінальних супозиторіїв. Склад композиції, при лікуванні кандидозних вульвовагінітов, дозволяє домогтися синергідного терапевтичного ефекту: стимуляції росту нормальної мікрофлори піхви пребіотиками при 96240 6 інгібуванні росту й елімінації патогенних грибів роду Candida сучасними антимікотиками. Сутність винаходу полягає у створенні фармацевтичної композиції антимікотиків і пребіотиків для профілактики й лікування вагінозів, вагінітів і вульвовагінітів у лікарській формі, що придатна для місцевої аплікації. У різних випадках реалізації фармацевтичної композиції антимікотиків і пребіотиків у якості антимікотиків використовують антибіотики й фунгіцидні препарати, обрані із групи азолів: терконазол, тіоконазол, бутоконазол, кетоконазол, клотримазол, міконазол, омоконазол, фентиконазол, оксиконазол, біфоназол, еконазол, ізоконазол; аліламінів: нафтифін, тербінафін; полієнових антибіотиків: амфотерицин В, натаміцин, ністатин, леворин; нітрофуранів: ніфуратель, фуразолідон. а також їх фармацевтично прийнятні комбінації. Переважно фармацевтична композиція містить не менш одного антимікотика в концентраціях від 0,0001 % до 5 % вага/об'єм у розрахунку на масу композиції. У різних випадках реалізації фармацевтичної композиції вона містить фармацевтично прийнятні концентрації пребіотиків, що обрані із груп природних або синтетичних сахаридів і олігосахаридів: лактулоза, фруктоолігосахара, галактоолігосахара, ксилоолігосахара, мальтоолігосахара, ізомальтоолігосахара, що мають ступінь полімеризації від 2 до 30, а також їхні комбінації. Переважно фармацевтична композиція містить пребіотики в концентраціях від 0,1 % до 40,0 % вага/об'єм у розрахунку на масу композиції. У різних випадках реалізації фармацевтична композиція антимікотиків і пребіотиків для профілактики й лікування вагінозів, вагінітів і вульвовагінітів виробляється в лікарській формі: супозиторіїв, песаріїв, глобул, м'яких капсул, тампонів, кремів, гелів, емульсій і інших форм для місцевої аплікації. Сутність винаходу в частині способу лікування вагінозів, вагінітів і вульвовагінітів грибкової або бактеріальної етіології полягає в використанні фармацевтичної композиції антимікотиків і пребіотиків у лікарській формі для місцевої аплікації, що базується на інгібуванні росту патогенних грибів і дріжджів антимікотиками з одночасною стимуляцією росту нормальних представників мікрофлори піхви. Переважно при реалізації способу лікування вагінозів, вагінітів і вульвовагінітів грибкової або бактеріальної етіології з використанням фармацевтичної композиції антимікотиків і пребіотиків, фармацевтична композиція антимікотиків і пребіотиків використовується для місцевої терапії в лікарській формі: супозиторіїв, глобул, песаріїв, тампонів, м'яких желатинових капсул, таблеток, кремів, мазей, гелів, суспензій, розчинів і т.д. При цьому передбачене використання антимікотиків, що не пригнічують ріст і розмноження лактобацил і біфідобактерій, які є домінантними видами в мікробіоценозах піхви. Процес готування заявленої фармкомпозиції в лікарській формі супозиторіїв передбачає підготовку заданих кількостей антимікотика й пребіотика, змішування компонентів, додавання до розплав 7 96240 леної основи супозиторію, що придатна для виготовлення вагінальних супозиторіїв, виливку супозиторіїв і пакування в блістери. У склад супозиторіїв можуть уводитися додаткові компоненти, що поліпшують фармацевтичні й споживчі властивості свіч (емульгатори, ароматизатори й т.д.). На кресленнях Фіг.1, Фіг.2 зображені діаграми терапевтичної ефективності азолів: терконазол, тіоконазол, бутоконазол, кетоконазол, клотримазол, міконазол, омоконазол, фентиконазол, оксиконазол, біфоназол, еконазол, ізоконазол (тут і далі зазначені нижче горизонтальної осі) з пребіотиками (тут і далі позначеними різним штрихуванням стовпців діаграм) на 7 день терапії експериментального вагініту в пацюків, на Фіг.3 - діаграми терапевтичної ефективності азолів: терконазол, тіоконазол, бутоконазол, кетоконазол, клотримазол, міконазол, омоконазол, фентиконазол, оксиконазол, біфоназол, еконазол, ізоконазол (зазначені нижче горизонтальної осі) з пребіотиками на 14 день терапії експериментального вагініту в пацюків, на Фіг.4 - діаграми терапевтичної ефективності композицій аліламінів, полієнів нітрофуранів із пребіотиками на 7 день терапії експериментального вагініту в пацюків, на Фіг.5 - діаграми терапевтичної ефективності композицій аліламінів, полієнів нітрофуранів із пребіотиками на 14 день терапії експериментального вагініту в пацюків, на Фіг.6 діаграми вмісту Candida spp. до й після терапії (тут і далі позначено різним штрихуванням) у пацієнток з вульвовагінальним кандиозом у трьох групах (одна група - контрольна), на Фіг.7 - діаграми вмісту вагінальних лактобацил до й після терапії у пацієнток з вульвовагінальним кандиозом у трьох групах (одна група - контрольна). На Фіг.1-5 прийняті скорочення: ФОС - фруктоолігосахара (Raftiline HP, Orafiti, Belgium); ГОСГалактоолігосахара (Oligomate 55, Yakut, Japan); КОС ксилоолігосахара Xylooligo-95P, Suntory); MOC - мальтоолігосахара (Maltotetraose, Chemos GmbH, Germany); iMOC - ізомальтоолігосахара (ІМО, Chemos GmbH, Germany); Лактулоза (Sigma-Aldrich, USA). По вертикальній осі на Фіг.1-7 відкладені значення вмісту відповідної мікрофлори в lg КСО/мл. Приклади 1. Відпрацьовування складів експериментальних супозиторіїв Як приклади представлені вагінальні супозиторії, у складі яких антимікотики натаміцин і ніфуратель комбінуються з пребіотиком лактулозою з використанням різних супозиторних основ і наступним співвідношенням компонентів. Склад супозиторіїв №1 Компоненти Натаміцин Лактулоза Кремофор RH40* Вітепсол РАЗОМ Склад супозиторіїв №2 Маса в мг 100 200 200 1500 2000 8 Компоненти Натаміцин Лактулоза Кремофор RH40* ПЕГ РАЗОМ Маса в мг 100 200 200 1500 2000 Склад супозиторіїв №3 Компоненти Ніфуратель Лактулоза Кремофор RH40* Вітепсол РАЗОМ Маса в мг 100 200 200 1500 2000 Склад супозиторіїв №4 Компоненти Ніфуратель Лактулоза Кремофор RH40* ПЕГ РАЗОМ Маса в мг 100 200 200 1500 2000 * Кремофор RH40 (поліоксил) - гідроване касторове масло (Polioxyl - 40 Hydrogenated Castor Oil) відповідно до вказівок європейської (EPh) і американської (USP) фармакопеї. Супозиторії №1 і №3 були приготовлені на супозиторній основі Вітепсол (Witepsol Н15,W35), супозиторії №2 і №4 - на основі поліетиленгліколя (PEG1500). 2. Дослідження терапевтичної ефективності композицій на експериментальних моделях Для моделювання в експерименті кандидозної вагінальної інфекції й вивчення питань, пов'язаних з лікуванням кандидозу, була використана раніше описана модель інфекції на пацюках (De Bernardis F., et al, 1999). Оваріоектомовані самки пацюків лінії Wistar (80-100 г) одержували щодня протягом п'яти днів 0,5 мг естрадіолу бензоату у вигляді підшкірної ін'єкції. На шостий день пацюки інтравагінально були інфіковані 0,1 мл суспензії клітин штаму С.albicans ATCC 10231, що містить 10,7 дріжджових клітин. Суспензію клітин уводили експериментальним тваринам інтравагінально за допомогою шприца зі спеціальною канюлею. Штам С.albicans ATCC 10231 перед введенням культивували на рідкому живильному середовищі, що містить 1 % дріжджового екстракту, 2 % пептону й 2 % глюкози, у качалці (200 об/хв) при температурі 30°С. Після 48 годин інкубації клітини збирали центрифугуванням, відмивали, ресуспендували в 0,9 % розчині NaCl, а потім використовували для вагінального інфікування пацюків. Бактеріологічне дослідження вагінального вмісту пацюків проводили кожні дві доби після інфікування тварин штамом C.albicans 10231 шляхом висіву 1 мкл вагінального секрету на агарові пластинки із середовищем Сабуро, що містить 50 мкг/мл хлорамфеніколу. Потім агарові пластинки культивували при 35°С протягом 48 годин з підра 9 96240 хунком пігментованих колоній C.albicans. Кінетику розвитку експериментального кандидозного вагініту в пацюків відслідковували бактеріологічно за зміною титрів дріжджових клітин у вагінальному вмісті контрольної і піддослідної груп. Таким чином, на моделі оваріоектомованих пацюків удалося одержати популяцію експериментальних тварин, у яких була відтворена кандидозна інфекція слизової оболонки піхви. Цих тварин надалі використовували для оцінки терапевтичної активності пропонованих композицій антимікотиків і пребіотиків. Для оцінки терапевтичної ефективності кожної композиції використовували 5 пацюків з бактеріологічно підтвердженою кандидозною інфекцією піхви. Контрольна група тварин (10 пацюків) утримувалася без лікування. 10 Місцеву терапію експериментального кандидозного вагініту в пацюків з бактеріологічно підтвердженою інфекцією піхви проводили різними композиціями в лікарській формі: вагінальні супозиторії. При цьому для пацюків готовили спеціальні глобули, що імітували вагінальні супозиторії, що містили в 50 разів менші дози активних компонентів, ніж рекомендовані для включення до складу офіціальних вагінальних супозиторіїв з антимікотиками для людини. Склад супозиторної маси композицій не змінювали. У таблиці 1 зазначені склади композицій антимікотиків і пребіотиків, які використані для виготовлення супозиторіїв і глобул для пацюків. Таблиця 1 Композиції антимікотиків і пребіотиків для лікування експериментального вагінального кандидозу в пацюків Антимікотики, мг Концентрація пребіотиків (мг) * КОС 30 МОС 20 ІМОС 20 ФОС 25 Азоли**: - еконазол - терконазол - міконазол Аліламіни: - тербінафін - нафтифін Полієни: - натаміцин - ністатин - леворин Нітрофурани: - ніфуратель - фуразолідон ГОС 30 Лактулоза 20 1,0 1,6 2,0 1,0 1,6 2,0 1,0 1,6 2,0 1,0 1,6 2,0 1,0 1,6 2,0 1,0 1,6 2,0 5,0 4,0 5,0 4,0 5,0 4,0 5,0 4,0 5,0 4,0 5,0 4,0 2,0 5,0 5,0 2,0 5,0 5,0 2,0 5,0 5,0 2,0 5,0 5,0 2,0 5,0 5,0 2,0 5,0 5,0 5,0 4,0 5,0 4,0 5,0 4,0 5,0 4,0 5,0 4,0 5,0 4,0 * - ФОС - фруктоолігосахара (Raftiline HP, Orafti, Belgium); ГОС - галактоолігосахара (Oligomate 55,Yakut, Japan); КОС - ксилоолігосахара Xylooligo-95P, Suntory); MOC - мальтоолігосахара (Maltotetraose, Chemos GmbH, Germany); iMOC ізомальтоолігосахара (IMO, Chemos GmbH, Germany); Лактулоза - (Sigma-Aldrich, USA). ** - всі інші азоли включали до складу композицій в аналогічних концентраціях 1,0-2,0 мг. Глобули з антимікотиками щодня із шостого по 12 день експерименту вводили експериментальним пацюкам вагінально. Ефективність лікування оцінювали за результатами бактеріологічного дослідження вагінального вмісту пацюків на наявність грибів С.albicans. Контролем у кожній групі слугували 10 пацюків, що не одержували лікування, яких кожні 48 годин бактеріологічно обстежували на наявність кандид у вагінальному вмісті. Результати антимікотичної дії композицій при вагінальному введенні пацюкам представлені на діаграмах (Фіг.1-5). Представлені дані свідчать про те, що всі вивчені композиції при місцевій терапії в складі експериментальних супозиторіїв активно пригнічували розвиток кандидозної вагінальної інфекції в пацюків. Через дві доби лікування титри кандид у вагінальному вмісті знизилися в 10,4-10,5 разів, у той час як у контрольних тваринні титри кандид при бактеріологічному обстеженні залишалися без змін (Фіг.1, 2, 4). Ще через 7 днів лікування, при обстеженні на 14 добу експерименту, інфекція практично купіювалася і у відокремлюваній піхві пацюків вдавалося виділити тільки окремі колонії C.albicans (Фіг.3, 5). У більш ніж 60 % експериментальних тварин, що одержали лікування, при обстеженні на 14 добу виділити кандиди бактеріологічними методами було практично неможливо. Таким чином, в умовах експериментальної кандидозної інфекції в пацюків, викликаної штамом С.albicans ATCC 10231, показана специфічна фунгіцидна активність місцевої терапії грибкової інфекції фармкомпозиціями антимікотиків і пребіотиків. 3. Клінічні дослідження композицій Клінічні дослідження проводили для підтвердження терапевтичної ефективності й безпеки фармкомпозиції натаміцину з лактулозою у лікарській формі супозиторію й одержання прямих клінічних даних, що підтверджують синергідний 11 ефект антимікотику натаміцину із пребіотиком, у хворих кандидозним вагінітом або вульво вагінітом. У дослідження було включено 30 пацієнток у віці від 20 до 45 років із уперше виявленим кандидозним вагінітом або вульвовагінітом. Діагностику кандидозу проводили на підставі об'єктивних клінічних даних (огляду слизової піхви в дзеркалах), скарг пацієнток на виділення, печіння, подразнення слизової піхви. Частина хворих пред'являла скарги на дизурію й диспаренурію. Діагноз підтверджували бактеріологічно: методом прямої мікроскопії мазків умісту піхви й виділення грибів роду Candida в чистій культурі. Для аналізу вагінального вмісту на хламідії, мікоплазми й уреаплазми використовували полімеразну ланцюгову реакцію (ПЛР). У всіх 30 пацієнток, включених у дані клінічні дослідження, перед початком і після закінчення курсу лікування експериментальними супозиторіями проводили мікробіологічне дослідження вагінального вмісту для визначення в складі мікрофлори піхви титрів біфідобактерій і лактобацил. Матеріал аналізували в мікробіологічній лабораторії інституту акушерства і гінекології ім. Д.О. Отта в м. Санкт-Петербурзі. Виділення з піхви досліджували прямим посівом матеріалу на тверді й рідкі живильні середовища: кров'яний агар, середовище МРС, бульйон і агар Сабуро. Проби культивували в аеробних і мікроаерофільних умовах (2-5 % кисню) при температурі 37 градусів. Ідентифікацію штамів проводили на підставі дослідження морфології колоній і клітин, культуральних, біохімічних і тинкторіальних властивостей мікроорганізмів. Виділені ізоляти лактобацил ідентифікували також по каталазної і оксидазної активності. Кількість бактерій у матеріалі оцінювали шляхом підрахунку колоній на щільних живильних середовищах, які представляли у вигляді lg КСО/мл. Всі, включені в дослідження пацієнтки із установленим діагнозом кандидозний вагініт, були рандомізовані в три групи по 10 пацієнток: - перша група одержувала місцеве лікування вагінальними супозиторіями з натаміцином і лактулозою один раз у день протягом 6 днів (склад №1) - друга група також одержувала місцеве лікування за допомогою вагінальних свіч із натаміцином і лактулозою один раз у день протягом 6 днів (склад №2). - контрольна група одержувала місцеве лікування антимікотиком натаміцин у супозиторіях 96240 12 "пімафуцин", виробництва компанії "Яманучи Юроп", по 100 мг вагінально один раз у день протягом 6 днів. У результаті клінічних досліджень було підтверджено, що фармкомпозиція натаміцину з лактулозою має високу терапевтичну ефективність відносно збудників кандидозних вагінітів (табл.2, 3) і відновлює нормальну мікрофлору піхви (Фіг.7), що є визначальним критерієм терапії кандидозу. При аналізі видового складу мікрофлори піхви в пацієнток першої групи після курсу лікування експериментальними супозиторіями з натаміцином і лактулозою встановлено, що елімінація грибів роду Candida мала місце в 100 % випадків (див. табл.2; Фіг.6), одночасно знижувалася виразність клінічних симптомів кандидозу. Титри лактобацил у вагінальному вмісті при бактеріологічному дослідженні збільшилися в 1000 і більше разів (Фіг.7). У другій групі успішна елімінації збудника зареєстрована в 90 % випадків (Фіг.2), у той же час у контрольній групі вилікування від кандид після курсу терапії відзначено тільки в 50 % пацієнток (табл.4; Фіг.6). Включення в комплексну терапію антимікотиками лактулози, дозволяє зберегти й істотно збільшити кількість лактобацил у піхвовому вмісті, що, безсумнівно, підвищує місцевий імунітет і перешкоджає розвитку грибкової інфекції. Представляється, що саме синергізм дії натаміцину й лактулози в адекватній супозиторній основі підвищує клінічну ефективність місцевої терапії кандидозу. Таким чином, клінічні дані об'єктивно підтверджують ефективність пропонованого способу лікування вагінальних кандидозів, виходячи з концепції синергідної дії антимікотиків і пребіотиків у складі фіксованої композиції й нормалізації мікробіоценозу за рахунок збільшення ступеня колонізації слизової піхви молочнокислими бацилами. Найбільш успішною в клінічному відношенні виявилася рецептура №1, приготовлена на супозиторній основі Вітепсол. Рецептура №2, виконана на ПЕГ 1500, була трохи менш ефективною, однак і в цьому випадку результати значно перевищували показники, зареєстровані в контрольній групі (див. табл.2-4). Клінічна ефективність, відсутність побічних ефектів, низька частота рецидивів і комплаентність місцевої терапії експериментальними супозиторіями роблять пропоновану фармкомпозицію новим перспективним засобом і методом лікування кандидозних поразок слизової піхви. 13 96240 14 Таблиця 2 Результати лабораторних досліджень пацієнток першої групи Показники Виділення грибів роду Candida з вагінального вмісту Лейкоцити в мазку з цервікального каналу (від 1/2 до цілого поля зору) Лейкоцити зі слизової піхви від 20 до 40 у полі зору ВК, n=10 До лікування 100 % Після лікування 0% 60 % 0% 60 % 10 % Таблиця 3 Результати лабораторних досліджень пацієнток другої групи Показники Виділення грибів роду Candida з вагінального вмісту Лейкоцити в мазку із цервікального каналу (від 1/2 до цілого поля зору) Лейкоцити зі слизової піхви від 20 до 40 у полі зору ВК, n=10 До лікування 100 % Після лікування 10 % 60 % 30 % 70 % 30 % Таблиця 4 Результати лабораторного дослідження в контрольній групі Показники Виділення грибів роду Candida з вагінального вмісту т Лейкоцити в мазку із цервикального каналу (від до цілого поля зору) Лейкоцити зі слизової піхви від 20 до 40 у поле зору ВК, n=10 До лікування 100 % Після лікування 50 % 60 % 40 % 70 % 70 % Даний винахід реалізується за допомогою універсального встаткування, яке широко розповсюджене в промисловості. 15 96240 16 17 96240 18 19 Комп’ютерна верстка А. Рябко 96240 Підписне 20 Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical composition comprising antimycotics and prebiotics and method for the treatment of candidal vaginitis
Автори англійськоюDikovskii Aleksander Vladimirovich, Dorozhko Oleg Valentinovich, Rudoy Boris Anatolievich
Назва патенту російськоюФармацевтическая композиция антимикотиков и пребиотиков и способ лечения кандидозных вагинитов
Автори російськоюДиковский Александр Владимирович, Дорожко Олег Валентинович, Рудой Борис Анатольевич
МПК / Мітки
МПК: A61K 45/06, A61K 31/4196, A61K 31/7016, A61P 15/02, A61K 9/02
Мітки: антимікотиків, композиція, пребіотиків, спосіб, кандидозних, лікування, фармацевтична, вагінітів
Код посилання
<a href="https://ua.patents.su/10-96240-farmacevtichna-kompoziciya-antimikotikiv-i-prebiotikiv-i-sposib-likuvannya-kandidoznikh-vaginitiv.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція антимікотиків і пребіотиків і спосіб лікування кандидозних вагінітів</a>
Попередній патент: Спосіб одержання ін’єкційної форми препарату на основі альфа-ліпоєвої кислоти
Наступний патент: Стробоскопічний спосіб реєстрації сигналів
Випадковий патент: Електронагрівач