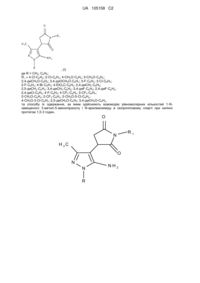
3-(5-аміно-3-метил-1-арил(метил)-1н-піразол-4-іл)-1-арилпіролідин-2,5-діони і спосіб їх одержання
Номер патенту: 105158
Опубліковано: 10.04.2014
Автори: Комихов Сергій Олександрович, Руденко Роман Володимирович, Десенко Сергій Михайлович, Афанасіаді Людмила Михайлівна, Муравйова Олена Олександрівна
Формула / Реферат
1. 3-(5-аміно-3-метил-1-арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5-діони загальної формули І
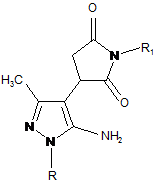 , (І)
, (І)
де R = СН3; С6Н5;
R1 = 4-Сl-С6Н4; 2-Сl-С6Н4; 4-СН3О-С6Н4; 3-СН3О-С6Н4;
2,4-диCH3O-C6H3; 3,4-диOCH2O-C6H4; 3-F-C6H4; 3-Cl-C6H4;
2-F-C6H4; 4-Br-C6H4; 4-EtO2C-C6H4; 2,4-диCH3-C6H3;
2,5-диCH3-C6H3; 3,4-диCH3-C6H3; 3,4-диF-C6H3; 2,4-диF-C6H3;
2,4-диCl-C6H3; 4-F-C6H4; 4-CF3-C6H4; 3-CF3-C6H4;
2-CH3O-C6H4; 2-CF3-C6H4; 2-CH3O-5-Cl-C6H3;
4-CH3O-3-Cl-C6H3; 2,5-диCH3O-C6H3; 3,4-диCH3O-C6H3.
2. Спосіб одержання 3-(5-аміно-3-метил-1-арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5-діонів формули І
 , (I)
, (I)
де R = СН3; С6Н5;
R1 = 4-Сl-С6Н4; 2-Сl-С6Н4; 4-СН3О-С6Н4; 3-СН3О-С6Н4;
2,4-диCH3O-C6H3; 3,4-диOCH2O-C6H4; 3-F-C6H4; 3-Cl-C6H4;
2-F-C6H4; 4-Br-C6H4; 4-EtO2C-C6H4; 2,4-диCH3-C6H3;
2,5-диCH3-C6H3; 3,4-диCH3-C6H3; 3,4-диF-C6H3; 2,4-диF-C6H3;
2,4-диCl-C6H3; 4-F-C6H4; 4-CF3-C6H4; 3-CF3-C6H4;
2-CH3O-C6H4; 2-CF3-C6H4; 2-CH3O-5-Cl-C6H3;
4-CH3O-3-Cl-C6H3; 2,5-диCH3O-C6H3; 3,4-диCH3O-C6H3,
за яким здійснюють конденсацію рівномолярних кількостей азотовмісної гетероциклічної сполуки і заміщеного малеіміду в органічному розчиннику при кипінні, який відрізняється тим, що як азотовмісну гетероциклічну сполуку використовують 1-N-заміщені 3-метил-5-амінопіразоли 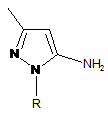 ,
,
як заміщений малеімід використовують N-арилмалеіміди 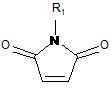 ,
,
як розчинник використовують ізопропіловий спирт, конденсацію проводять протягом 1,5-3 годин в одну стадію до утворення цільового продукту.
Текст
Реферат: Винахід стосується 3-(5-аміно-3-метил-1-арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5діонів загальної формули І UA 105158 C2 (12) UA 105158 C2 O R1 N H 3C O N N NH2 R , (І) де R = СН3; С6Н5; R1 = 4-Сl-С6Н4; 2-Сl-С6Н4; 4-СН3О-С6Н4; 3-СН3О-С6Н4; 2,4-диCH3O-C6H3; 3,4-диOCH2O-C6H4; 3-F-C6H4; 3-Cl-C6H4; 2-F-C6H4; 4-Br-C6H4; 4-EtO2C-C6H4; 2,4-диCH3-C6H3; 2,5-диCH3-C6H3; 3,4-диCH3-C6H3; 3,4-диF-C6H3; 2,4-диF-C6H3; 2,4-диCl-C6H3; 4-F-C6H4; 4-CF3-C6H4; 3-CF3-C6H4; 2-CH3O-C6H4; 2-CF3-C6H4; 2-CH3O-5-Cl-C6H3; 4-CH3O-3-Cl-C6H3; 2,5-диCH3O-C6H3; 3,4-диCH3O-C6H3, та способу їх одержання, за яким здійснюють взаємодію рівномолярних кількостей 1-Nзаміщеного 3-метил-5-амінопіразолу і N-арилмалеіміду в ізопропіловому спирті при кипінні протягом 1,5-3 годин. O R1 N H 3C O N N R NH2 UA 105158 C2 Винахід належить до області хімії, а саме до 3-(5-аміно-3-метил-1-арил-1Н-піразол-4-іл)-1арил(метил)піролідин-2,5-діонів загальної формули І і способу їх одержання. де R = СН3; С6Н5; R1=4Сl-С6Н4; 2-Сl-С6Н4; 4-СН3О-С6Н4; 3-СН3ОС6Н4; O 2,4-диCH3О-C6H3; 3,4диOCH2O-C6H4; 3-FC6H4; 3-Cl-C6H4; R1 N 2-F-C6H4; 4-Br-C6H4; 4EtO2C-C6H4; 2,4-диCH3H 3C C6H3; O 2,5-диCH3-C6H3; 3,4диCH3-C6H3; 3,4-диFN C6H3; 2,4-диF-C6H3; NH2 N 2,4-диCl-C6H3; 4-F-C6H4; 4-CF3-C6H4; 3-CF3-C6H4; R 2-CH3O-C6H4; 2-CF3, C6H4; 2-CH3O-5-Cl-C6H3; 4-CH3O-3-Cl-C6H3; 2,5диCH3O-C6H3; 3,4диCH3O-C6H3. (І) 5 10 15 Наявність фармакофорного піразольного фрагменту у молекулах сполук, що заявляються, припускає можливість використання таких речовин у якості лікарських препаратів [G. Yang et al., Chim. J. Chem., 18, 435 (2000)]; жарознижуючих речовин [М. Elnagdi, Tetrahedron, 30, 3791 (1971)]; снотворних засобів [Ger. Patent, 2131790 (1971)]. Вони використовуються як терапевтичні засоби при ішемічних процесах, при ревматоїдному артриті, астмі, запаленні кишечника [Пат. РФ 2266901, C07D 239/54; А61K 31/513], деякі з них мають високу біологічну активність як кардіопротектори, фібринолітики і т. ін. [S. Ghabrial et al., Egypt J. Pharm. Sci., 37, 375(1996)]. Ось чому зараз синтез сполук подібної структури з різними фармакофорними фрагментами є дуже актуальним, бо вони грають важливу роль у біологічних процесах живих організмів і людини. Відомий структурний аналог сполук, що заявляються, -3-(індол-3-іл)сукциніміди загальної формули II O R N де R = Η, CH3, CH2Ph; R1= Η, F, Br, OCH3, NO2, CN і т. ін., O R1 N H , (II) 20 25 і спосіб його одержання [J. Е. Macor, D. Н. Blank et al.,Synthesis, p.443-449 (1997)]. Сполуки формули II використовуються як проміжні у синтезі триптамінів, медичного препарату серотоніну, що є передавачем збудження в центральній нервовій системі і збільшує кількість тромбоцитів у крові. В структурі відомого аналога формули II як замісника R в молекулі N-малеіміду використано лише аліфатичні радикали і невідомо, як буде проходити реакція у випадках з ароматичними замісниками R. Спосіб одержання відомого аналога формули II складається з однієї стадії і реалізується за схемою: 1 UA 105158 C2 O R N O R 1 AH c , O R N + O R 1 N H N H 5 10 15 O . Розчин заміщеного індолу (10 ммол) і заміщеного малеіміду (30 ммол) нагрівають в оцтовій кислоті в атмосфері азоту протягом 24-144 годин (час встановлюють індивідуально в залежності від замісника в індолі). Суміш охолоджують. У випадку, якщо заміщені сукциніміди не випадають безпосередньо із реакційної маси, розчини випаровують під пониженим тиском, залишок розчиняють у етилацетаті і додають натрій карбонат Na2CO3- Водний шар екстрагують етилацетатом. Етилацетатні витяжки об'єднують, сушать над магнійсульфатом MgSO 4, концентрують під вакуумом, залишок кристалізують або хроматографують на силікагелі із відповідного розчинника. Одержують 3-(індол-3-іл)сукциніміди - жовті речовини з виходами 287 % (в залежності від замісника в індолі). До недоліків способу одержання відомого аналога формули II треба віднести значну тривалість технологічного процесу (30-150 годин з урахуванням виділення продукту концентрування під вакуумом, екстракція, і його очистка - перекристалізація або хроматографування), невисокі виходи в реакції (з переважною більшістю виходів до 60 %). Відомий аналог сполук, що заявляються, за хімічною структурою - 1-(2,5-діоксо-1фенілпіролідин-3-іл)бензотриазол формули III, описаний у [Фарион И.А., Халтаров З.М. и др. Изв. РАН, сер химическая, № 2, 399-401, (2008)]. N N N O N C6H5 O 20 . ІІІ Недоліком структури відомого аналога формули III є неможливість хімічної модифікації (що обмежує кількість потенційного одержання біологічно активних речовин). Спосіб одержання сполуки формули III здійснюється за схемою: N N O N N+ N H N c , O ,AH O N N C H 65 C H 65 O O 25 30 . Суміш бензотриазолу (0,01 моль) і N-фенілмалеіміду (0,01 моль) поміщають у фторопластову чашку, яка попередньо нагріта до 120 °C на сплаві Вуда. Температуру поступово підвищують до 220 °C, суміш витримують ще 5 хвилин при цій температурі. Охолоджують, склоподібний продукт видаляють із чашки виморожуванням рідким азотом. Вихід технічного продукту складає 90 %. Продукт розчиняють у суміші мурашиної кислоти і води, нагрівають 10 хвилин з активованим вугіллям, фільтрують. Додають водний розчин натрію гідроксиду NaOH до рН = 5. Осад фільтрують, розчиняють у киплячому етанолі і повільно охолоджують. Голки, що утворилися, сушать у вакуумі при 50-70 °C. Вихід складає 71 %. Т плавлення - 145-147 °C. Загальний час реакції становить 4,5-5 годин. До недоліків способу одержання аналога формули III слід віднести процес сплавлення, при якому в багатьох випадках утворюються продукти окислення, що можуть забруднювати основну 2 UA 105158 C2 5 речовину. Авторами у даному джерелі описано одержання лише одного продукту. Тривалість технологічного процесу, що потребує використання рідкого азоту і очистки основного продукту, також можна вважати недоліком відомого способу одержання аналога формули III. Відомий структурний аналог структури, що заявляються, 3-(2-метил-1H-індол-3-іл)піролідин2,5-діон формули IV, описаний у [Young Shin Cho, L. Whitehead et al., J. Med. Chem. 53, 29522963 (2010)]. O NH O CH3 N H . (IV) Спосіб одержання відомого аналога формули IV реалізується за схемою: O N H O O + C H 3 N H 10 15 20 25 N H A O H , ,c C H 3 N H O . Розчин малеіміду (56,9 ммоль) і 2-метил-1H-індолу (1,02 ммоль) у льодяній оцтовій кислоті кип'ятять 3 доби. Після охолодження розчинник випаровують у вакуумі і розбавляють етилацетатом. Органічний шар промивають водою, водним розчином натрій бікарбонату NaНСО3, сушать над магній сульфатом MgSO4, концентрують у вакуумі. Очищають на хроматографічній колонці (елюент суміш етилацетату і гексану). Вихід становить 31 %. Недоліками способу одержання аналога формули IV є тривалість технологічного процесу (приблизно 50-52 години), очистка продукту з використанням хроматографії, низький вихід реакції. Як прототип за хімічною будовою і технічною суттю вибрано останній із аналогів. В основу винаходу поставлено задачу пошуку нових сполук у низці похідних 3-(5-аміно-3метил-1-арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5-діонів з можливістю широкої варіації замісників у піразольному і піролідоновому фрагментах, а також розробки простого і доступного способу їх одержання, що дозволяє скоротити час синтезу, підвищити вихід реакції, використовувати нетоксичні розчинники як середовища для проведення реакції. Рішення поставленої задачі забезпечується розробкою похідних 3-(5-аміно-3-метил-1арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5-діонів формули І 3 UA 105158 C2 O N H 3C O N NH2 N R (І) де R = СН3; С6Н5; R1=4-Сl-С6Н4; 2-СlС6Н4; 4-СН3О-С6Н4; 3R1 СН3О-С6Н4; 2,4-диCH3O-C6H3; 3,4диOCH2O-C6H4; 3-FC6H4; 3-Cl-C6H4; 2-F-C6H4; 4-Br-C6H4; 4EtO2C-C6H4; 2,4-диCH3C6H3; 2,5-диCH3-C6H3; 3,4диCH3-C6H3; 3,4-диF, C6H3; 2,4-диF-C6H3; 2,4-диCl-C6H3; 4-FC6H4; 4-CF3-C6H4; 3CF3-C6H4; 2-CH3O-C6H4; 2-CF3C6H4; 2-CH3O-5-ClC6H3; 4-CH3O-3-Cl-C6H3; 2,5диCH3O-C6H3; 3,4диCH3O-C6H3. Рішення поставленої задачі забезпечується також тим, що у способі одержання сполук загальної формули І 5 O R1 N H 3C O N N R NH2 , де R = СН3; С6Н5; R1=4-Сl-С6Н4; 2-СlС6Н4; 4-СН3О-С6Н4; 3СН3О-С6Н4; 2,4-диCH3O-C6H3; 3,4диOCH2O-C6H4; 3-FC6H4; 3-Cl-C6H4; 2-F-C6H4; 4-Br-C6H4; 4EtO2C-C6H4; 2,4диCH3-C6H3; 2,5-диCH3-C6H3; 3,4диCH3-C6H3; 3,4-диFC6H3; 2,4-диF-C6H3; 2,4-диCl-C6H3; 4-FC6H4; 4-CF3-C6H4; 3CF3-C6H4; 2-CH3O-C6H4; 2-CF3C6H4; 2-CH3O-5-ClC6H3; 4-CH3O-3-Cl-C6H3; 2,5диCH3O-C6H3; 3,4диCH3O-C6H3, (I) що включає взаємодію рівномолярних кількостей азотовмісної гетероциклічної сполуки і малеіміду в органічному розчиннику при кипінні, згідно з винаходом, як азотовмісну N N гетероциклічну сполуку використовують 3-метил-1-арил(метил)-5-амінопіразоли 4 R NH2 , як UA 105158 C2 R1 N O 5 10 15 20 25 O малеімід використовують N-арилмалеіміди , як розчинник - ізопропіловий спирт, реакцію проводять протягом 1,5-3 години в одну стадію до утворення цільового продукту. Сполуки, що заявляються, являють собою безкольорові, кристалічні, складні азотовмісні гетероциклічні речовини. Можливість видозміни хімічної структури сполук формули І варіюванням замісників у піразольному і піролідиновому фрагментах відкриває перспективи синтезу великого набору корисних речовин з новими властивостями і застосуванням. Високореакційні центри в NH- і 4-СН-положеннях 5-амінопіразолу - вихідної речовини для одержання сполук, що заявляються, дозволяють одержувати великий асортимент піразолілпіролідин-2,5-діонів з різними потенційними біологічними активностями. Вибір реагентів, їх доступність, проведення реакції їх взаємодії в ізопропіловому спирті дозволяє значно зменшити тривалість технологічного процесу завдяки високій швидкості протікання реакції, а також зменшити енергозатрати. Реакцію проводять в спиртовому середовищі (у способі-прототипі - у кислому середовищі), що сприяє підвищенню якості і виходу цільового продукту (не потрібна перекристалізація і хроматографування). Крім того, спосіб, що заявляється, дозволяє уникнути застосування агресивної льодяної оцтової кислоти (т. кип. 118 °C). Вибір розчинника для реакції - ізопропілового спирту (Т кип. 82 °C) забезпечує не тільки необхідну пожежобезпечність проведення синтезу, а також запобігає утворенню смолистих побічних продуктів, що відбивається на якості і чистоті сполук, що заявляються. Тривалість технологічного процесу 1,5-3 години (у способі прототипі 50-52 години). Збільшення або зменшення часу реакції є недоцільним, адже за вказаний час реакція проходить повністю з високими виходами 59-81 % (у способі-прототипі вихід становить 31 %). У таблиці 1 наведено порівняльні характеристики способу, що заявляється, та способіваналогів. У таблиці 2 наведено характеристики сполук, що заявляються. Спосіб, що заявляється, здійснюється за схемою: O H C 3 N N R 30 35 40 45 N O N H 2 + N R 1 H C 3 R 1 ,i PH -r O O N N O R N H 2 . Рівномолярні кількості 1-заміщеного 3-метил-5-амінопіразолу і N-заміщеного малеіміду в ізопропіловому спирті нагрівають 1,5-3 години. Охолоджують суміш, фільтрують, осад промивають ізопропіловим спиртом, сушать при кімнатній температурі. Спосіб одержання сполук, що заявляються, ілюструється наступними прикладами. Приклад 1. Одержання 3-(5-аміно-3-метил-1-феніл-1Н-піразол-4-іл)-1-(4хлорфеніл)піролідин-2,5-діону Суміш 0,35 г (0,002 моль) 3-метил-1-феніл-5-амінопіразолу та 0,41 г (0,002 моль) N-(4хлорфеніл)малеіміду в 10 мл пропанолу-2 кип'ятять впродовж 3 годин. Реакційну суміш охолоджують, осад, що випав, відфільтровують, промивають пропанолом-2 та сушать на повітрі. Вихід складає 0,52 г (69 %). Температура плавлення 123-125 °C. 1 2 Спектр Н ЯМР (ДМСО-d6), δ (м. ч.), КССВ J (Hz):2.02 (с, 3Н, СН3), 2.83 (д. д., JAB=18.1 Гц, 3 3 JAX=6.2 Гц, 1Н, Ha(pyrr)), 3.25 (д.д., JBX=9.7 Гц, 1Н, Hb), 4.34 (д.д., 1H, 4-Hx), 5.27 (зш. c, 2H, NH2). 7.30-7.63 (м., 9Наrом). Приклад 2. Одержання 3-(5-аміно-1,3-диметил-1H-піразол-4-іл)-1-(4-хлорфеніл)піролідин2,5-діону. Продукт одержують як зазначено в прикладі 1. Для реакції беруть 0,22 г (0,0022 моль) 1,3диметил-5-амінопіразолу і 0,41 г (0,0022 моль) N-(4хлорфеніл)малеіміду. Час нагрівання 1,5 години. Вихід продукту складає 0,41 г (59 %). Температура плавлення 139-140 °C. 5 UA 105158 C2 1 2 Спектр H ЯМР (ДМСО-d6), δ (м. ч.), КССВ J (Hz):1.91 (с, 3Н, СН3), 2.72 (д.д., JAB=17.9 Гц, 3 JAX=6.2 Гц, 1Н, Ha(pyrr)), 3.16 (д.д., JBX=9.9 Гц, 1H, Hb), 3,45 (3Н, с, СН3), 4.18 (д.д., 1Н, 4-Нх), 5.03 (зш. с, 2Н, NH2). 7.34-7.61 (м., 4Нагом). Решту прикладів наведено у таблиці 2. Як видно із опису матеріалів винаходу і даних таблиць 1, 2, структура сполук, що заявляються, забезпечує одержання значного набору похідних 3-(5-аміно-3-метил-1арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5-діонів з високим ступенем чистоти. Спосіб одержання сполук формули І забезпечує: - значне зменшення тривалості процесу; - підвищення якості сполук, що заявляються, збільшення їх виходу; - широке варіювання у молекулі цільового продукту замісників різної електронної природи. Всі ці переваги нових сполук і способу їх одержання дають можливість їх потенційного використання як біологічно активних речовин, лікарських препаратів в медицині і фармації. 3 5 10 Таблиця 1 Спосіб, що заявляється Спосібпрототип Спосіб за статтею [J. Е. Масог, D. Н. Blank et al., Synthesis, p. 443-449(1997)] Спосіб за статтею [Фарион И.А., Халтаров З.М. и др. Изв. РАН, сер. химическая, № 2, 399-401, (2008)] Кількість Розчинник для Тривалість Вихід цільових стадій реакції процесу, год. продуктів, % реакції ізопропіловий 1 1,5-3 59-82 спирт льодяна оцтова 1 50-52 31 кислота 1 1 оцтова кислота сплавлення 30-150 4,5-5 15 6 Чистота цільових продуктів не потребується Хроматографування 2-87 (переважна більшість виходів до 60) використовують екстракцію, кристалізацію або хроматографування 71 Перекристалізацію із суміші мурашиної кислоти і води; із етанолу UA 105158 C2 Таблиця 2 № п/п 1 Сполуки, одержані за способом, що заявляється Замісник R Замісник R1 2 3 1 Т топ.°С Вихід, % 4 5 1. С6Н5 2-СН3О-5СlС6Н3 183-184 82 2. С6Н5 2,4-диСН3-С6Н3 204-205 78 3. С6Н5 4-СlС6Н4 123-125 69 4. С6Н5 3,4-диF-С6Н3 152-153 64 5. СН3 2-СН3О-5СlС6Н3 172-173 67 6. СН3 4-СlС6Н4 139-140 59 7. СН3 3,4-диF-С6Н3 136-137 63 8. СН3 3-СlС6Н4 170-171 60 7 ЯМР Н хімічний зсув, δ (м. ч.), (КССВ, J (Гц)) 5 2.05 (с, 3Н, СН3), 2.78 (д.д., 2 3 JAB=18.1 Гц, JAX=5.9 Гц, 1H, 3 На(руrr)), 3.21 (д.д., JBX=9.9 Гц, 1Н, Нb), 3.76 (3Н, с, СН3О), 4.32 (д.д., 1H, 4-Нх), 5.22 (зш. с, 2Н, NH2). 7.21-7.58 (м., 8Нагом). 2.05 (с, 3Н, СН3), 2.08 (3Н, с, СН3), 2.33 (3Н, с, СН3) 2.85 (д.д., 2 3 JAB=15.6 Гц, JAX=6.2 Гц, 1H, 3 На(руrr)), 3.21 (д.д., JBX=9.6 Гц, 1H, Нb), 4.42 (д.д., 1Н, 4-НX), 5.20 (зш. с, 2Н, NH2). 7.02-7.59 (м., 8Нагом). 2.02 (с, 3Н, СН3), 2.83 (д.д., 2 3 JAB=18.1 Гц, JAX=6.2 Гц, 1H, 3 На(руrr)), 3.25 (д.д., JBX=9.9 Гц, 1H, Нb), 4.34 (д.д., 1H, 4-Нх), 5.27 (зш. с, 2Н, NH2). 7.30-7.63 (м., 9Нагом.). 2.03 (с, 3Н, СН3), 2.82 (д.д., 2 3 JAB=17.9 Гц, JAX=6.4 Гц, 1H, 3 На(руrr)), 3.21 (д.д., JBX=9.5 Гц, 1H, Нb), 4.31 (д.д., 1Н, 4-Нх), 5.25 (зш. с, 2Н, NH2). 7.22-7.67 (м., 8Нагом.). 2.03 (с, 3Н, СН3), 2.72 (д.д., 2 3 JAB=18.0 Гц, JAX=6.4 Гц, 1H, 3 На(руrr)), 3.21 (д.д., JBX=9.8 Гц, 1H, Нb), 3,45 (3Н, с, СН3), 3.77 (3Н, с, СН3О), 4.25 (д.д., 1Н, 4-Нх), 5.04 (зш. с, 2Н, NH2). 7.32-7.68 (м., 3Нагом.). 1.91 (с, 3Н, СН3), 2.72 (д.д., 2 3 JAB=17.9 Гц, JAX=6.2 Гц, 1H, 3 Ha(pyrr)), 3.16 (д.д., JBX=9.9 Гц, 1H, Hb), 3,45 (3Н, с, СН3), 4.18 (д.д., 1H, 4-Нх), 5.03 (зш. с, 2Н, NH2). 7.34-7.61 (м., 4Нагом). 1.91 (с, 3Н, СН3), 2.72 (д.д., 2 3 JAB=17.9 Гц, JAX=6.4 Гц, 1H, 3 На(руrr)), 3.15 (д.д., JBX=9.7 Гц, 1H, Нb), 3,45 (3Н, с, СН3), 4.17 (д.д., 1Н, 4-Нх), 5.02 (зш. с, 2Н, NH2). 7.20-7.67 (м., 3Нагом.). 1.91 (с, 3Н, СН3), 2.73 (д.д., 2 3 JAB=18.1 Гц, JAX=6.3 Гц, 1Н, На 3 (руrr)), 3.15 (д.д., JBX=9.8 Гц, 1H, Нb), 3,45 (3Н, с, СН3), 4.18 (д.д., 1H, 4-Нх), 5.04 (зш. с, 2Н, NH2). 7.30-7.60 (м., 4Нагом.). UA 105158 C2 ФОРМУЛА ВИНАХОДУ 1. 3-(5-Aміно-3-метил-1-арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5-діони формули І загальної O R1 N H 3C O N NH 2 N 5 10 15 R , (І) де R = СН3; С6Н5; R1 = 4-Сl-С6Н4; 2-Сl-С6Н4; 4-СН3О-С6Н4; 3-СН3О-С6Н4; 2,4-диCH3O-C6H3; 3,4-диOCH2O-C6H4; 3-F-C6H4; 3-Cl-C6H4; 2-F-C6H4; 4-Br-C6H4; 4-EtO2C-C6H4; 2,4-диCH3-C6H3; 2,5-диCH3-C6H3; 3,4-диCH3-C6H3; 3,4-диF-C6H3; 2,4-диF-C6H3; 2,4-диCl-C6H3; 4-F-C6H4; 4-CF3-C6H4; 3-CF3-C6H4; 2-CH3O-C6H4; 2-CF3-C6H4; 2-CH3O-5-Cl-C6H3; 4-CH3O-3-Cl-C6H3; 2,5-диCH3O-C6H3; 3,4-диCH3O-C6H3. 2. Спосіб одержання 3-(5-аміно-3-метил-1-арил(метил)-1Н-піразол-4-іл)-1-арилпіролідин-2,5діонів формули І O R1 N H 3C O N N NH 2 R 20 25 , (I) де R = СН3; С6Н5; R1 = 4-Сl-С6Н4; 2-Сl-С6Н4; 4-СН3О-С6Н4; 3-СН3О-С6Н4; 2,4-диCH3O-C6H3; 3,4-диOCH2O-C6H4; 3-F-C6H4; 3-Cl-C6H4; 2-F-C6H4; 4-Br-C6H4; 4-EtO2C-C6H4; 2,4-диCH3-C6H3; 2,5-диCH3-C6H3; 3,4-диCH3-C6H3; 3,4-диF-C6H3; 2,4-диF-C6H3; 2,4-диCl-C6H3; 4-F-C6H4; 4-CF3-C6H4; 3-CF3-C6H4; 2-CH3O-C6H4; 2-CF3-C6H4; 2-CH3O-5-Cl-C6H3; 4-CH3O-3-Cl-C6H3; 2,5-диCH3O-C6H3; 3,4-диCH3O-C6H3, за яким здійснюють конденсацію рівномолярних кількостей азотовмісної гетероциклічної сполуки і заміщеного малеіміду в органічному розчиннику при кипінні, який відрізняється тим, що як азотовмісну гетероциклічну сполуку використовують 1-N-заміщені 3-метил-5 N N амінопіразоли R NH2 , 8 UA 105158 C2 R1 O N O як заміщений малеімід використовують N-арилмалеіміди , як розчинник використовують ізопропіловий спирт, конденсацію проводять протягом 1,5-3 годин в одну стадію до утворення цільового продукту. Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 9
ДивитисяДодаткова інформація
Автори англійськоюRudenko Roman Volodymyrovych, Muraviova Olena Oleksandrivna, Komikhov Serhii Oleksandrovych, Desenko Serhii Mykhailovych, Afanasiadi Liudmyla Mykhailivna
Автори російськоюРуденко Роман Владимирович, Муравьева Алена Александровна, Комихов Сергей Александрович, Десенко Сергей Михайлович, Афанасиади Людмила Михайловна
МПК / Мітки
МПК: C07D 231/38, C07D 403/04, C07D 207/40
Мітки: одержання, спосіб, 3-(5-аміно-3-метил-1-арил(метил)-1н-піразол-4-іл)-1-арилпіролідин-2,5-діони
Код посилання
<a href="https://ua.patents.su/11-105158-3-5-amino-3-metil-1-arilmetil-1n-pirazol-4-il-1-arilpirolidin-25-dioni-i-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">3-(5-аміно-3-метил-1-арил(метил)-1н-піразол-4-іл)-1-арилпіролідин-2,5-діони і спосіб їх одержання</a>
Попередній патент: Пристрій для рафінування металевого розплаву в проміжному ковші
Наступний патент: Спосіб лікування рецидиву варикозної хвороби нижніх кінцівок
Випадковий патент: Лікарський засіб "рібіфлан" гепатопротекторної та антиоксидантної дії