Композиція з уповільненим вивільненням для перорального введення лікарських засобів
Формула / Реферат
1. Композиція з уповільненим вивільненням для перорального введення лікарського засобу, що містить лікарську речовину, носій для уповільненого вивільнення лікарської речовини і прискорювач гідратації гелю, в якій вагове співвідношення лікарської речовини, носія для тривалого вивільнення лікарської речовини і прискорювача гідратації гелю знаходиться в інтервалі 1:3-30:0,1-15; носій є сумішшю альгінату натрію і ксантанової камеді у ваговому співвідношенні 1:0,1-10 і прискорювач гідратації гелю є сумішшю гідроксипропілметилцелюлози і альгінату пропіленгліколю у ваговому співвідношенні 1:0,05-20.
2. Композиція за п.1, в якій носій додатково містить камедь ріжкового дерева як основу (носій) для уповільненого вивільнення лікарської речовини.
3. Композиція за п.2, в якій вагове співвідношення альгінату натрію, ксантанової камеді і камеді ріжкового дерева знаходиться в інтервалі 1:0,2-10:0,1-5.
4. Композиція за п.1, в якій лікарська речовина вибрана з групи, що складається з антигіпертензивного засобу, лікарських засобів для лікування серцево-судинних захворювань, лікарських засобів для лікування гіперліпідемії, нестероїдних протизапальних лікарських засобів, лікарських засобів для лікування астми, протидіабетичних лікарських засобів, заспокійливого засобу, антибіотика, протисудомного засобу, стероїдів та їх суміші.
5. Композиція за п.1, в якій лікарський засіб вибраний з групи, що складається з ніфедипіну, ісрадипіну, ловастатину і гліпізиду.
Текст
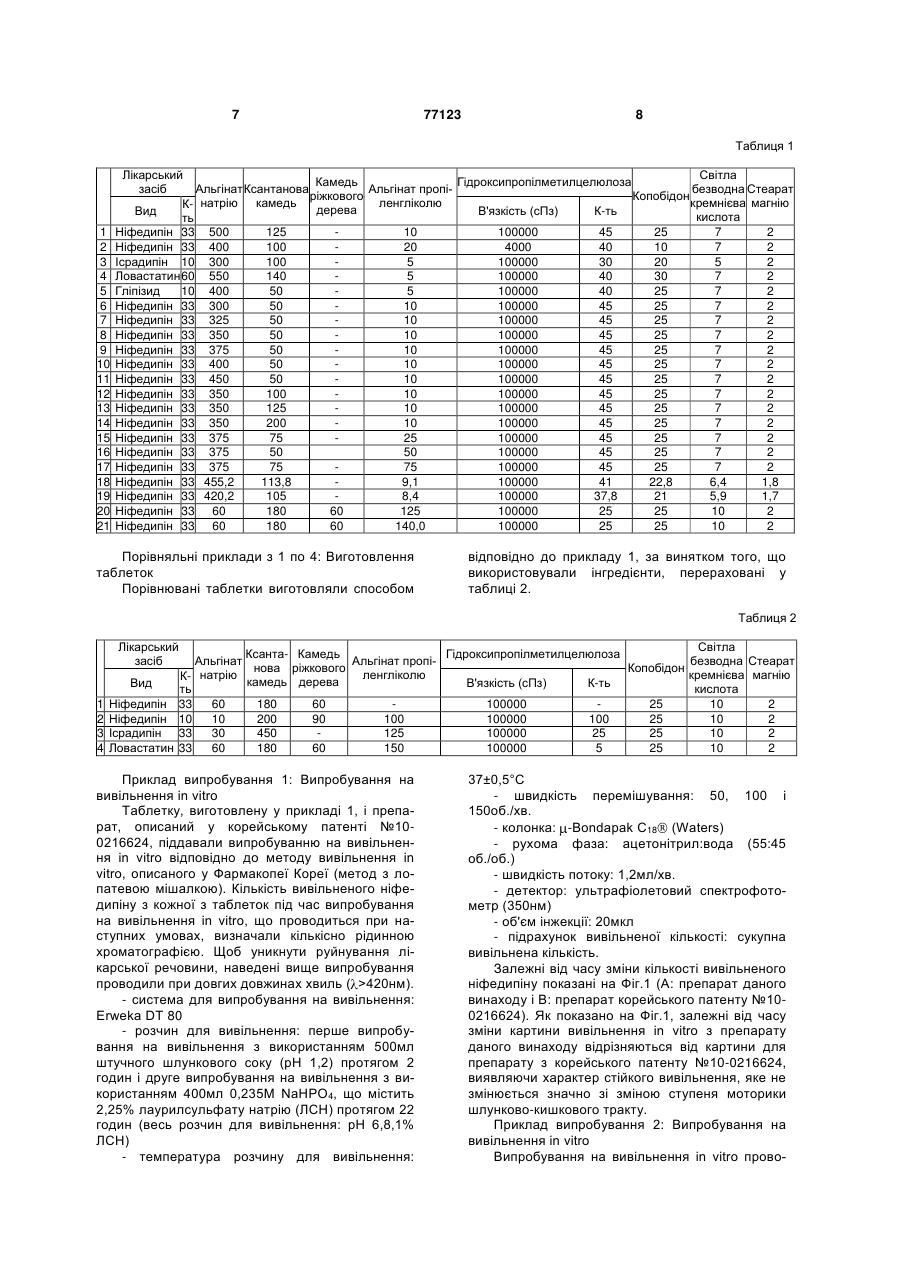
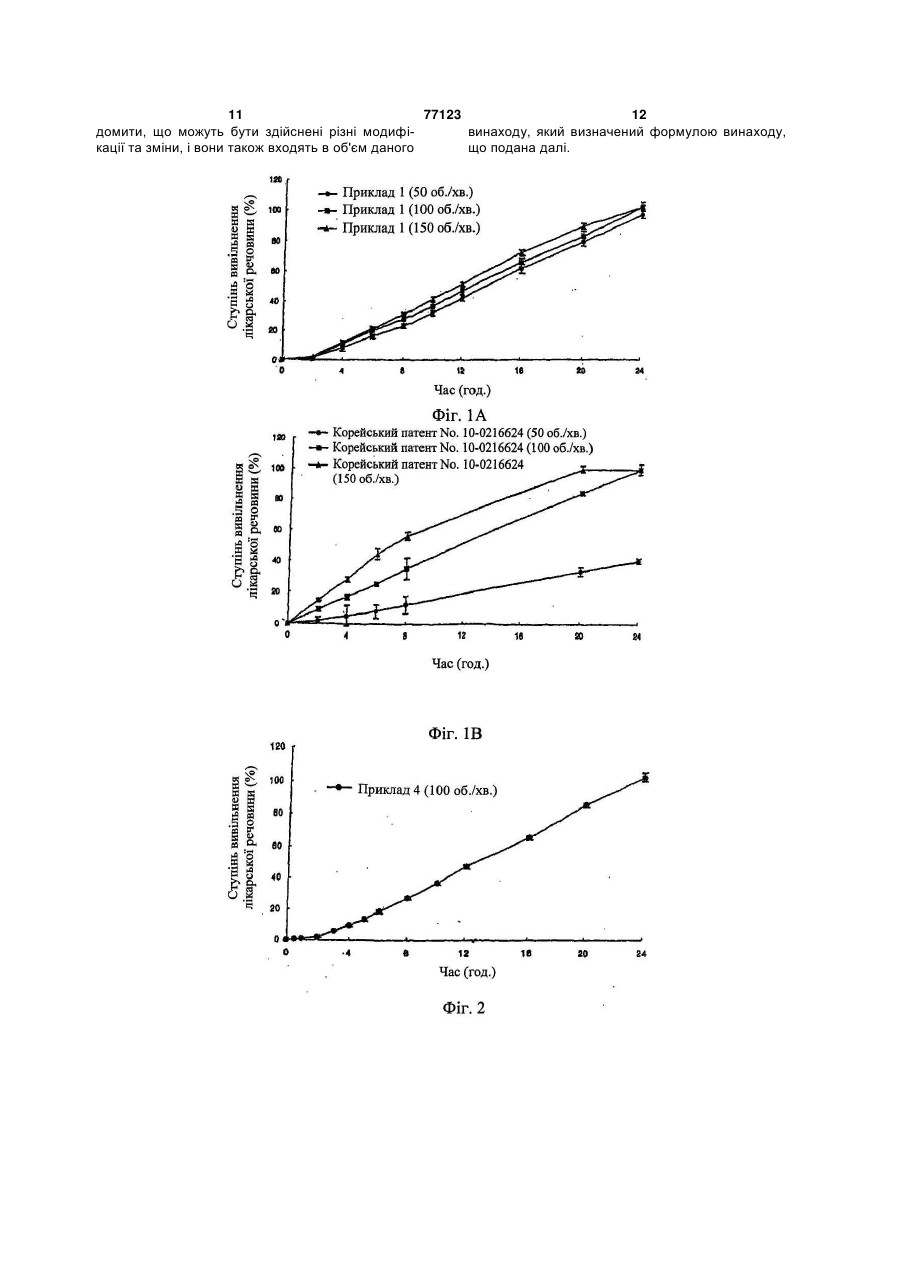
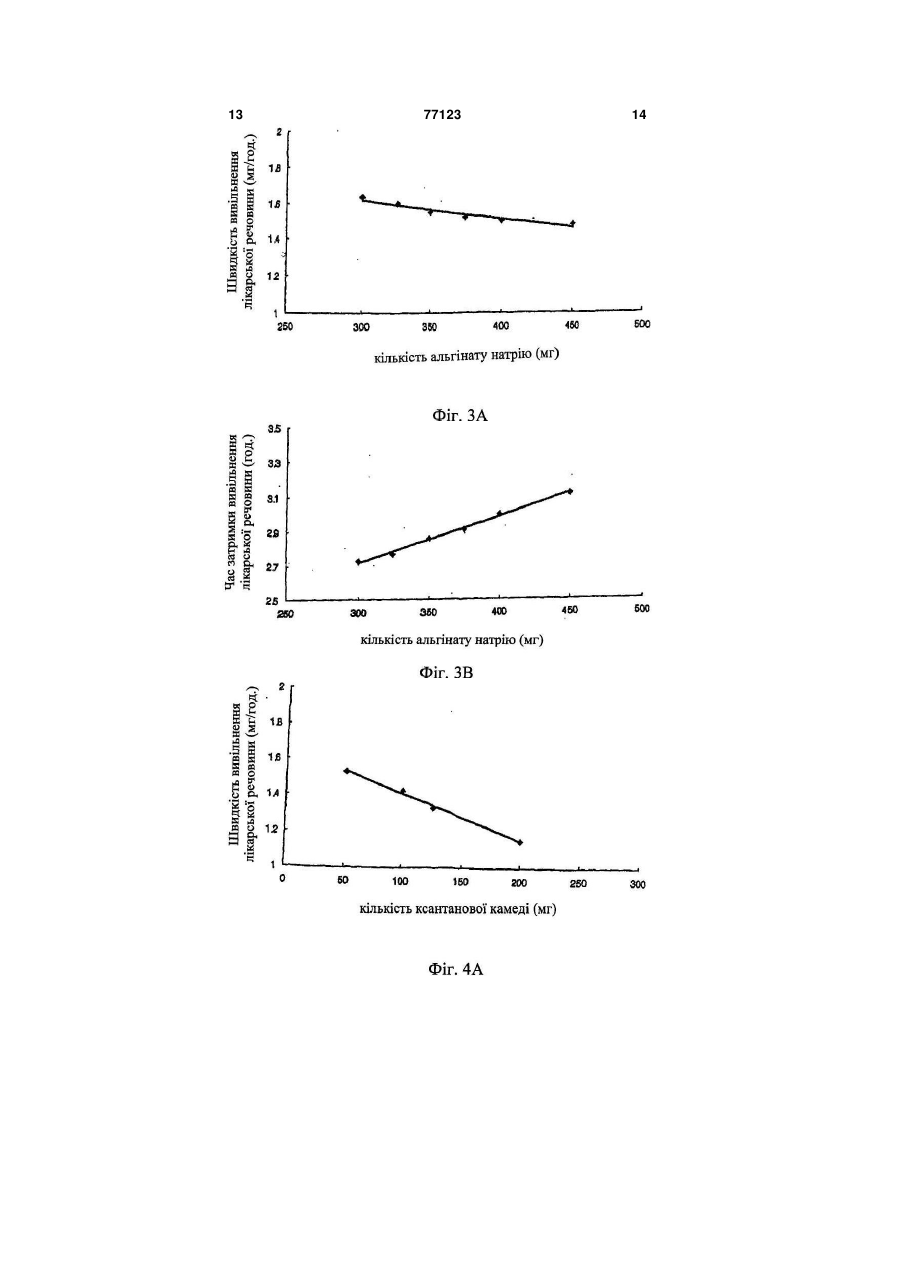
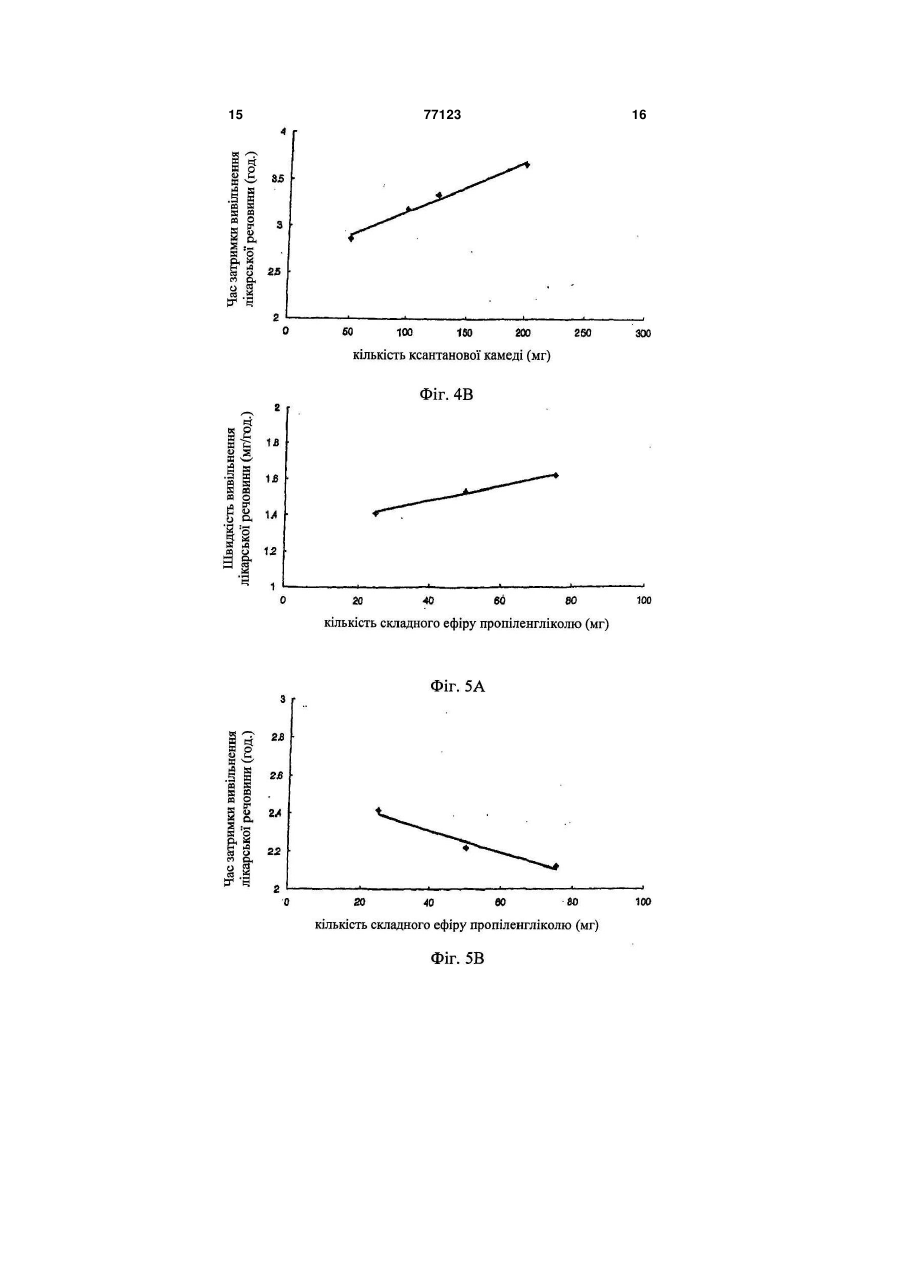
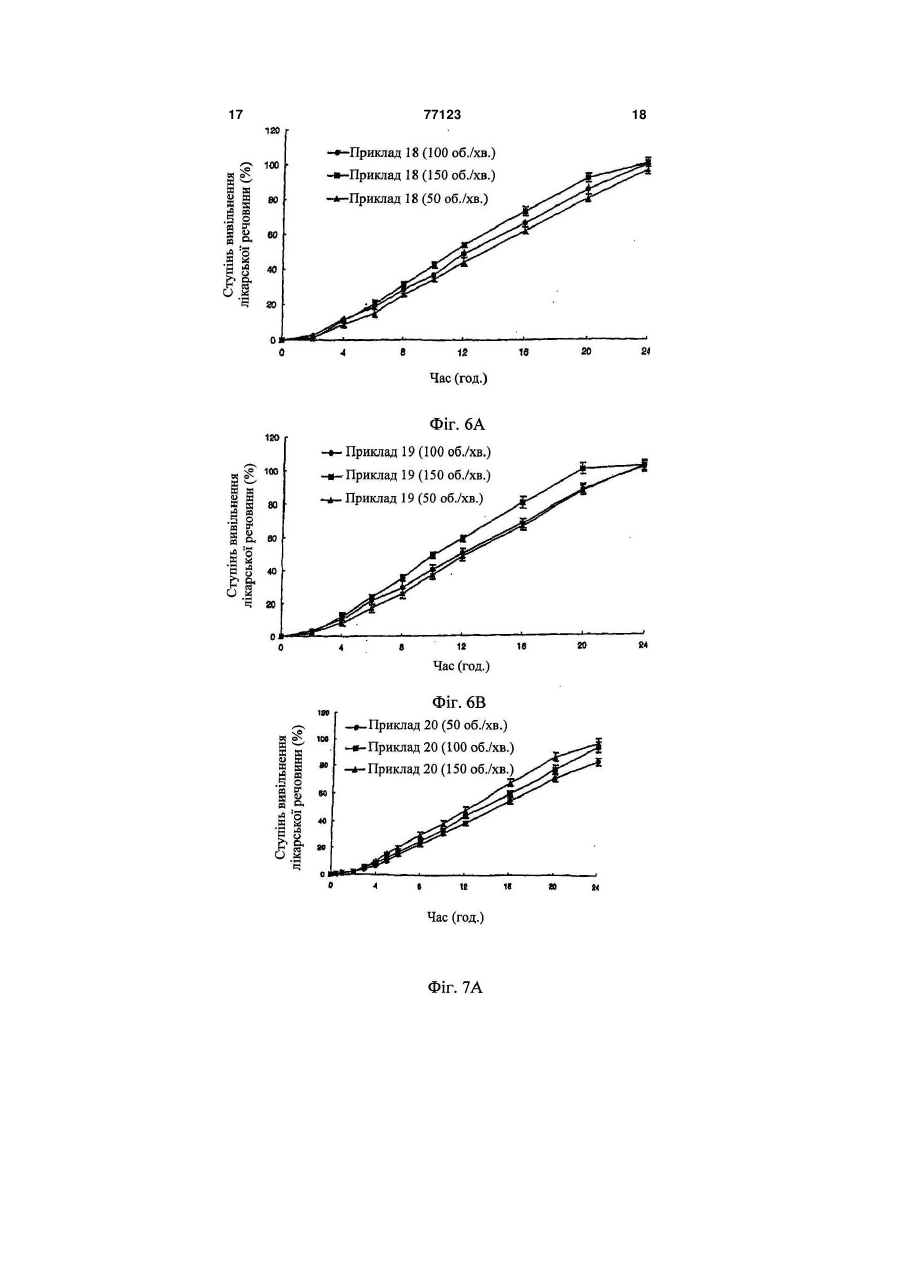
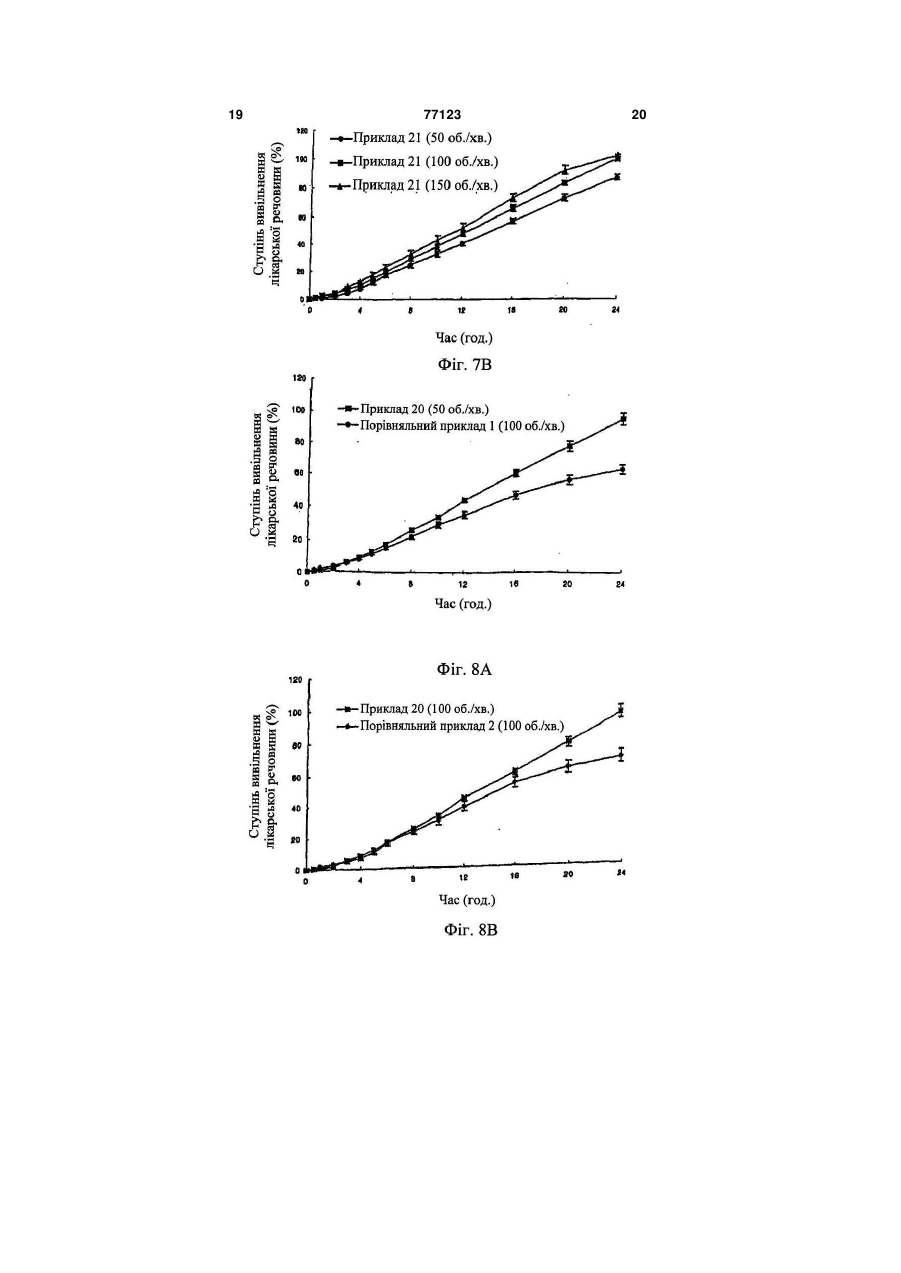
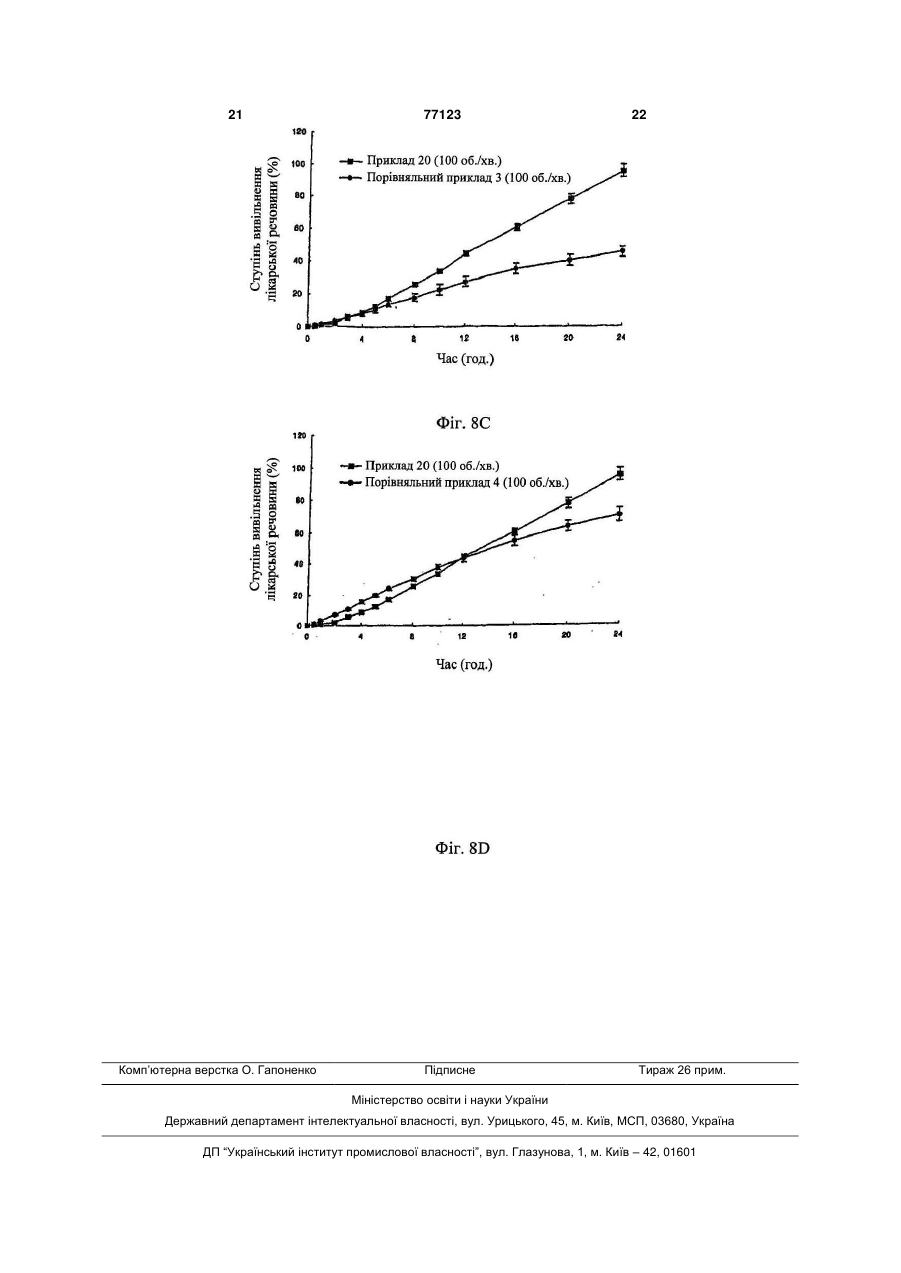
1. Композиція з уповільненим вивільненням для перорального введення лікарського засобу, що містить лікарську речовину, носій для уповільненого вивільнення лікарської речовини і прискорювач гідратації гелю, в якій вагове співвідношення лікарської речовини, носія для тривалого вивільнення лікарської речовини і прискорювача гідратації гелю знаходиться в інтервалі 1:3-30:0,1 C2 2 77123 1 3 77123 4 ська форма на основі суміші гідроксипропілцелюФіг.2: залежні від часу зміни кількості лікарсьлози і гідроксипропілметилцелюлози, яка є водокої речовини, вивільненої іn vіtrо препаратом дарозчинним полімерним гелетвірним засобом. ного винаходу; Крім того, в японській патентній публікації Фіг.3А і 3В: залежність швидкості вивільнення №62077335А (1987.4.9) описана гелеподібна лілікарської речовини і часу затримки вивільнення карська форма на основі карбоксивінілового полікарської речовини від кількості альгінату налімеру; в японській патентній публікації трію; №03169814А (1991.7.23) лікарська форма має в Фіг.4А і 4В: залежність швидкості вивільнення основі суміші водорозчинного полімеру, такого як лікарської речовини і часу затримки вивільнення гідроксипропілцелюлоза, гідроксипропілметилцелікарської речовини від кількості ксантанової калюлоза, полівінілпіролідон і метилцелюлоза, і меді; нерозчинний у воді полімер, такий як мікрокрисФіг.5А і 5В: залежність швидкості вивільнення талічна целюлоза; і в європейському патенті лікарської речовини і часу затримки вивільнення №274176В (1992.5.27) лікарська форма з уповілікарської речовини від кількості складного ефіру льненим вивільненням має в основі полівінілпіпропіленгліколю; ролідон. Однак недолік цих лікарських форм виФіг.6А і 6В: зміни швидкості вивільнення ліявляється у тому, що постійна швидкість карської речовини за допомогою визначеної кільвивільнення лікарської речовини не може зберікості носія для тривалого вивільнення (А: препагатися протягом більш ніж 24 годин через утворат, виготовлений у прикладі 18; і В: препарат, рення гслевої плівки на зовнішній стороні оболовиготовлений у прикладі 19); нки лікарської форми, залишаючи ядро Фіг.7А і 7В: зміни швидкості вивільнення лінежельованим. карської речовини, що спостерігаються, коли до Крім того, у патентах США №№ 4765989А, носія додають камедь ріжкового дерева (А: пре5208037А і 5019397А повідомляється про осмопарат, виготовлений у прикладі 20; і В: препарат, тичні лікарські форми з регульованим вивільненвиготовлений у прикладі 21); і ням, у яких виявляється постійна швидкість вивіФіг.8А-8D: залежні від часу зміни кількості лільнення лікарської речовини, дотримуючись карської речовини, вивільненої іn vіtrо препаракінетики нульового порядку. Однак, спосіб виробтом з тривалим вивільненням даного винаходу у ництва таких лікарських форм є дуже складним і порівнянні з показниками для препаратів, що подорогим, крім того, лікарська речовина, що місрівнюються (А: Порівняльний приклад 1; В: Порітиться у них, не повністю біодоступна [Jоnn S. вняльний приклад 2; С: Порівняльний приклад 3; і Grundaу аnd Robert Т. Fоster, Сlin. Fhаrmacokinet., D: Порівняльний приклад 4). 30(1): 28-51(1996)]. Композиція з уповільненим вивільненням для Раніше повідомлялося, що препарат лікарсьперорального введення лікарського засобу міскої речовини, виготовлений з використанням нотить лікарський засіб, носій для уповільненого сія з моногліцеридного гелю, вивільняє лікарську вивільнення лікарської речовини і прискорювач речовину з постійною швидкістю, яка дотримугідратації гелю. ється кінетики нульового порядку протягом 24 Носій, переважно, являє собою суміш альгігодин, коли приводиться у контакт з гідрофільною нату натрію і ксантанової камеді, а прискорювач матрицею або водорозчинною матрицею [корейгідратації гелю є сумішшю гідроксипропілметилський патент №10-0216624 (1999.5.31)]. Однак целюлози та альгінату пропіленгліколю. цей препарат відноситься до препаратів, що виКомпозиція з тривалим вивільненням даного кликають ерозію і легку деградацію скорочувальвинаходу може підтримувати постійний рівень них рухів в органах шлунково-кишкового тракту. лікарської речовини у крові протягом 24 годин Відповідно, об'єктом даного винаходу є наабо більше, завдяки тому факту, що швидкість дання композиції з уповільненим вивільненням вивільнення лікарської речовини дотримується для перорального введення лікарського засобу, кінетики нульового порядку і не змінюється значяка при введенні іn vіvо здатна до вивільнення ною мірою від ступеня моторики шлунковолікарської речовини з постійною швидкістю за кишкового тракту завдяки швидкій гідратації гелю кінетикою нульового порядку протягом 24 годин і без утворення нежельованого ядра. більше, причому на цю швидкість мало впливає Компоненти композиції даного винаходу деступінь моторики шлунково-кишкового тракту. тально описані нижче. Відповідно до одного з аспектів даного вина(1) Фармакологічно активний інгредієнт (ліходу представлена композиція з уповільненим карська речовина) вивільненням для перорального введення лікарФармакологічно активний інгредієнт композиської речовини, яка містить лікарську речовину, ції даного винаходу є будь-якою однією з тих ліносій з уповільненим вивільненням лікарської карських речовин, які придатні для використання речовини і прискорювач гідратації гелю. у препаратах з уповільненим вивільненням лікарНаведені вище та інші об'єкти і ознаки даного ської речовини. Приклади лікарських речовин винаходу стануть очевидними з подальшого опивключають антигіпертензивні засоби, такі як нісу винаходу у поєднанні з наступними супровідфедипін, доксазоцин, амосулралол, фелодипін, ними малюнками, які, відповідно, представляють: лекранідипін, лацидипін, нікардипін, фосиноприл, Фіг.1А і 1В: залежні від часу зміни кількості ліімідаприл, клізаприл, периндоприл, лізиноприл, карської речовини, вивільненої іn vіtrо (А: препалозартан, ірвесартан і кандесартан; лікарські рат даного винаходу; і В: препарат корейського засоби для лікування серцево-судинних захвопатенту №10-0216624); рювань, такі як ісрадипін; лікарські засоби для 5 77123 6 лікування гіперліпемії, такі як ловастатин і симванатрійкарбокси-метилцелюлозу і/або полівінілпістатин; нестероїдні протизапальні засоби; засоби ролідин, гідроксипропілцелюлозу і/або кофобідон для лікування астми; протидіабетичні засоби, такі (колідон VА64 , ВАSF, Німеччина) і, необов'язяк гліклазид, глімепірид і гліпізид; заспокійливі; ково, дезінтегрант (наприклад, крохмаль, агар і антибіотики; протисудомні та стероїди, переважальгінову кислоту або її натрієву сіль), газовану но, ніфедипін. воду і/або абсорбент, барвник, засіб, що поліп(2) Носій для тривалого вивільнення шує смак і запах, та підсолоджувач. Носій для тривалого вивільнення у композиції Композиції можуть додатково включати наподаного винаходу переважно є сумішшю альгінату внювачі, консерванти, антиоксиданти, стабілізанатрію і ксантанової камеді зі співвідношенням у тори, пігменти, протиаглютинувальні речовини, суміші (ваговим) в інтервалі 1:0,1~10, переважно, речовини, що поліпшують ковзання, речовини, 1:0,2~0,6, щоб знизити початкове залпове вивіщо поліпшують змочування, речовини, що поліпльнення і зміну у кількості, що вивільняється, шують смак і запах, емульгатори і тому подібне. лікарської речовини. Фармацевтичну композицію даного винаходу Крім того, щоб підвищити структурну цілісможна вводити щодня. Звичайна добова доза ність даної лікарської форми, носій даного винаактивного інгредієнта знаходиться в інтервалі від ходу додатково може містити камедь ріжкового приблизно 0,15 до 2мг/кг, переважно, від 0,5 до дерева, причому вагове співвідношення альгінату 1,5мг/кг, і її можна вводити у вигляді одиничної натрію:ксантанової камеді:камеді ріжкового дередози або у вигляді дробних доз. Однак, повинно ва знаходиться в інтервалі 1:0,2~10:0,1~5, перебути зрозуміло, що кількість активного інгредієнважно, 1:1~5:0,5~3. та, що дійсно вводиться, повинна бути визначена (3) Прискорювач гідратації гелю у світлі різних значимих факторів, включаючи Прискорювач гідратації гелю, що використопатологічний стан, який треба лікувати, вибраний вується у даному винаході, відіграє вирішальну шлях введення, вік і вагу конкретного пацієнта і роль у формуванні гомогенного жельованого ядтяжкість симптоматики у пацієнта; і тому дозура, не залишаючи нежельованої частини, коли вання, запропоноване вище, не повинне тлумалікарська форма приводиться у контакт з водним читися як таке, що обмежує об'єм даного винахосередовищем. Прискорювач гідратації гелю у ду яким-небудь чином. композиції даного винаходу, переважно, являє Наступні приклади і приклади випробування собою суміш гідроксипропілметилцелюлози та призначені для додаткової ілюстрації даного виальгінату пропіленгліколю зі співвідношенням у находу без обмеження його об'єму. суміші (ваговим) в інтервалі 1:0,05~20, переважКрім того, проценти, що наводяться нижче, но, 1:0,1~10. Гідроксипропілметилцелюлоза, яка для суміші твердих речовин, рідини у рідині, твевикористовується тут, переважно, має в'язкість, рдої речовини у рідині представлені у ваговому, що знаходиться в інтервалі від 4000 до об'ємному і вагооб'ємному вираженні, відповідно, 100000сПз. якщо особливо не вказано інакше. Відповідно до композиції даного винаходу ваПриклади 1-21: Виготовлення таблеток гове співвідношення лікарської речовини, носія Ніфедипін (Unique Chemicals, Індія), ісрадипін для тривалого вивільнення і прискорювача гідра(Sun Pharm., Індія), ловастатин (СКD Pharm., Котації гелю знаходиться в інтервалі 1:3~30:0,1~15, рея), гліпізид (Sun Pharm., Індія), альгінат натрію переважно, 1:5~25:0,5~10. (Keltonе НVСR, Kеltоеn LVF, Kеlсоsоl , Kеlset, Фармацевтична композиція даного винаходу ІSР США), ксантанову камедь (Kеltrоl F, Kеlсо, може бути виготовлена для перорального ввеСША), камедь ріжкового дерева (Сеsаgum LN1, дення. Композиції для перорального введення LR200, Сеsаlріnіа, Італія), альгінат пропіленгліконадають різних форм, таких як таблетки, пілюлі, лю (Kеlсоlоіd НVF, LVF, ІSР, США), гідроксипропіпорошок, саше, еліксир, суспензія, емульсія, розлметилцелюлозу (Меltоsе 90SН, 4000SR, чин, сироп, гранули, м'які і тверді желатинові кап100000SR, Shin-Etsu, Японія) і кофовідон сули і тому подібне, які можуть містити звичайні (Kоllіdon VА64, ВАSF, Німеччина) змішували, як домішки, такі як розріджувач (наприклад, лактоза, показано у таблиці 1, протягом 30 хвилин, туди ж декстроза, сахароза, маніт, сорбіт, целюлоза додавали стеарат магнію і світлу безводну кремі/або гліцин), речовина, що поліпшує ковзання нієву кислоту (порошок більш тонкий, ніж меш 30) (наприклад, двоокис кремнію, тальк, стеаринова і змішували протягом 5 хвилин. Потім одержану кислота або її цинкова, магнієва і кальцієва солі суміш таблетували з використанням звичайного і/або поліетиленгліколь). У таблетковій формі преса відповідно до методу виготовлення таблекомпозиція, крім того, може містити в'яжучу речоток для одержання таблеткового препарату. вину (наприклад, алюмосилікат магнію, крохмальну пасту, желатин, трагакант, метилцелюлозу, 7 77123 8 Таблиця 1 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 Лікарський Світла Гідроксипропілметилцелюлоза Камедь засіб Альгінат Ксантанова Альгінат пропібезводна Стеарат ріжкового Копобідон камедь ленгліколю кремнієва магнію К- натрію дерева Вид В'язкість (сПз) К-ть кислота ть Ніфедипін 33 500 125 10 100000 45 25 7 2 Ніфедипін 33 400 100 20 4000 40 10 7 2 Ісрадипін 10 300 100 5 100000 30 20 5 2 Ловастатин 60 550 140 5 100000 40 30 7 2 Гліпізид 10 400 50 5 100000 40 25 7 2 Ніфедипін 33 300 50 10 100000 45 25 7 2 Ніфедипін 33 325 50 10 100000 45 25 7 2 Ніфедипін 33 350 50 10 100000 45 25 7 2 Ніфедипін 33 375 50 10 100000 45 25 7 2 Ніфедипін 33 400 50 10 100000 45 25 7 2 Ніфедипін 33 450 50 10 100000 45 25 7 2 Ніфедипін 33 350 100 10 100000 45 25 7 2 Ніфедипін 33 350 125 10 100000 45 25 7 2 Ніфедипін 33 350 200 10 100000 45 25 7 2 Ніфедипін 33 375 75 25 100000 45 25 7 2 Ніфедипін 33 375 50 50 100000 45 25 7 2 Ніфедипін 33 375 75 75 100000 45 25 7 2 Ніфедипін 33 455,2 113,8 9,1 100000 41 22,8 6,4 1,8 Ніфедипін 33 420,2 105 8,4 100000 37,8 21 5,9 1,7 Ніфедипін 33 60 180 60 125 100000 25 25 10 2 Ніфедипін 33 60 180 60 140,0 100000 25 25 10 2 Порівняльні приклади з 1 по 4: Виготовлення таблеток Порівнювані таблетки виготовляли способом відповідно до прикладу 1, за винятком того, що використовували інгредієнти, перераховані у таблиці 2. Таблиця 2 Лікарський засіб 1 2 3 4 Світла Гідроксипропілметилцелюлоза Ксанта- Камедь Альгінат Альгінат пропібезводна Стеарат нова ріжкового Копобідон ленгліколю кремнієва магнію К- натрію камедь дерева Вид В'язкість (сПз) К-ть кислота ть Ніфедипін 33 60 180 60 100000 25 10 2 Ніфедипін 10 10 200 90 100 100000 100 25 10 2 Ісрадипін 33 30 450 125 100000 25 25 10 2 Ловастатин 33 60 180 60 150 100000 5 25 10 2 Приклад випробування 1: Випробування на вивільнення іn vіtrо Таблетку, виготовлену у прикладі 1, і препарат, описаний у корейському патенті №100216624, піддавали випробуванню на вивільнення іn vіtrо відповідно до методу вивільнення іn vіtrо, описаного у Фармакопеї Кореї (метод з лопатевою мішалкою). Кількість вивільненого ніфедипіну з кожної з таблеток під час випробування на вивільнення іn vіtrо, що проводиться при наступних умовах, визначали кількісно рідинною хроматографією. Щоб уникнути руйнування лікарської речовини, наведені вище випробування проводили при довгих довжинах хвиль ( >420нм). - система для випробування на вивільнення: Еrweka DТ 80 - розчин для вивільнення: перше випробування на вивільнення з використанням 500мл штучного шлункового соку (рН 1,2) протягом 2 годин і друге випробування на вивільнення з використанням 400мл 0,235М NаНРО4, що містить 2,25% лаурилсульфату натрію (ЛСН) протягом 22 годин (весь розчин для вивільнення: рН 6,8,1% ЛСН) - температура розчину для вивільнення: 37±0,5°С - швидкість перемішування: 50, 100 і 150об./хв. - колонка: -Воndараk С18 (Wаtеrs) - рухома фаза: ацетонітрил:вода (55:45 об./об.) - швидкість потоку: 1,2мл/хв. - детектор: ультрафіолетовий спектрофотометр (350нм) - об'єм інжекції: 20мкл - підрахунок вивільненої кількості: сукупна вивільнена кількість. Залежні від часу зміни кількості вивільненого ніфедипіну показані на Фіг.1 (А: препарат даного винаходу і В: препарат корейського патенту №100216624). Як показано на Фіг.1, залежні від часу зміни картини вивільнення іn vіtrо з препарату даного винаходу відрізняються від картини для препарату з корейського патенту №10-0216624, виявляючи характер стійкого вивільнення, яке не змінюється значно зі зміною ступеня моторики шлунково-кишкового тракту. Приклад випробування 2: Випробування на вивільнення іn vіtrо Випробування на вивільнення іn vіtrо прово 9 77123 10 дили, використовуючи препарат, виготовлений у нення лікарської речовини від кількості носія, прикладі 1 відповідно до методу з прикладу випроводили випробування на вивільнення іn vіtrо, пробування 1. Результат на Фіг.2 показує, що використовуючи препарати, виготовлені у прикпрепарат ловастатину вивільняє лікарську речоладах з 18 по 19 відповідно до способу з приклавину з постійною швидкістю вивільнення, дотриду випробування 1. Результат на Фіг.6А і 6В (А: муючись кінетики нульового порядку протягом 24 препарат з прикладу 18 і В: препарат з прикладу годин. 19) показує, що швидкість вивільнення лікарської Приклад випробування 3: Випробування на речовини дотримується кінетики нульового повивільнення іn vіtrо рядку, яка не залежить від кількості носія. Тобто Щоб оцінити, чи залежить швидкість вивільпрепарати вивільняють лікарську речовину з нення лікарської речовини від кількості альгінату більш або менш постійною швидкістю, коли співнатрію у носії, проводили випробування на вивівідношення сполук носія у суміші залишається льнення іп уііго, використовуючи препарати, вигонезмінним. товлені у прикладах з 6 по 11 відповідно до споПриклад випробування 7: Випробування на собу з прикладу випробування 1. Результат на вивільнення іn vіtrо Фіг.3 (А: швидкість вивільнення лікарської речоЩоб оцінити, чи змінюється швидкість вивівини і В: час затримки вивільнення лікарської льнення лікарської речовини, коли до носія доречовини) показує, що швидкість вивільнення дають камедь ріжкового дерева, проводили вилікарської речовини стає пропорційно повільніпробування на вивільнення іn vіtrо, шою, а час затримки вивільнення триваліший з використовуючи препарати, виготовлені у прикданою кількістю альгінату натрію. ладах з 20 по 21 відповідно до способу з приклаПриклад випробування 4: Випробування на ду випробування 1. Результат на Фіг.7А і 7В (А: вивільнення іn vіtrо препарат з прикладу 20 і В: препарат з прикладу Також, щоб оцінити, чи залежить швидкість 21) показує, що препарат з використанням суміші вивільнення лікарської речовини від кількості альгінату натрію, ксантанової камеді і камеді ріжксантанової камеді у носії, проводили випробукового дерева як носія дає чудове тривале вивівання на вивільнення іn vіtrо, використовуючи льнення. препарати, виготовлені у прикладах з 12 по 14 Приклад випробування 8: Випробування на відповідно до способу з прикладу випробування вивільнення іn vіtrо і кількісне визначення швид1. Результат на Фіг.4 (А: швидкість вивільнення кості утворення нежельованого ядра і жельованолікарської речовини і В: час затримки вивільненго ядра ня лікарської речовини) показує, що швидкість Щоб порівняти швидкість вивільнення препавивільнення лікарської речовини стає пропорційратами даного винаходу та іншими препаратами но повільнішою, а час затримки вивільнення трипроводили випробування на вивільнення іn vіtrо, валіший з даною кількістю ксантанової камеді. використовуючи препарати, виготовлені у прикПриклад випробування 5: Випробування на ладі 20 і порівняльних прикладах з 1 по 4, відповивільнення іn vіtrо відно до методу випробування з прикладу 1. РеЩоб оцінити, чи залежить швидкість вивільзультати на Фіг. з 8А по 8D (А: порівняльний нення лікарської речовини від кількості альгінату приклад 1; В: порівняльний приклад 2; С: порівпропіленгліколю, прискорювача гідратації гелю, няльний приклад 3; і D: порівняльний приклад 4) проводили випробування на вивільнення іn vіtrо, показують, що залежні від часу зміни у картині використовуючи препарати, виготовлені у приквивільнення іn vіtrо з препаратів, виготовлених у ладах з 15 по 17 відповідно до способу з приклапорівняльних прикладах з 1 по 4, відрізняються ду випробування 1. Результат на Фіг.5 (А: швидвід картини вивільнення з препарату даного викість вивільнення лікарської речовини і В: час находу. Тобто порівняльні препарати не виявлязатримки вивільнення лікарської речовини) покали кінетики нульового порядку. зує, що швидкість вивільнення лікарської речовиКрім того, на 4 день випробування досліджуни стає пропорційно вищою, а час затримки вивівали перерізи таблеток, щоб визначити величину льнення коротший з даною кількістю альгінату жельованого ядра і нежельованого ядра відповіпропіленгліколю. дно до методу K. N. Раrk еt аl. [Соntrolled Drug Приклад випробування 6: Випробування на Delivery, 18-23 (2000)]. Результати показані у вивільнення іn vіtrо таблиці 3. Щоб оцінити, чи залежить швидкість вивільТаблиця 3 Приклад 20 Порівняльний приклад 1 Порівняльний приклад 2 Порівняльний приклад 3 Порівняльний приклад 4 Нежельоване ядро 0,09±0,04см 0,39±0,03см 0,30±0,03см 0,32±0,02см 0,20±0,01см Як показано у таблиці 3, ступінь желювання ядра набагато інтенсивніший у препарату даного винаходу, ніж у препаратів, виготовлених у порів Жельоване ядро 0,73±0,03см 0,36±0,04см 0,54±0,02см 0,46±0,03см 0,54±0,03см Жельоване ядро/нежельоване ядро 8,11±0,45 0,92±0,13 1,85±0,14 1,44±0,05 2,72±0,14 няльних прикладах з 1 по 4. Хоча даний винахід був описаний відносно наведених вище конкретних втілень, треба усві 11 77123 12 домити, що можуть бути здійснені різні модифівинаходу, який визначений формулою винаходу, кації та зміни, і вони також входять в об'єм даного що подана далі. 13 77123 14 15 77123 16 17 77123 18 19 77123 20 21 Комп’ютерна верстка О. Гапоненко 77123 Підписне 22 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSustained-release composition for oral administration of drug
Автори англійськоюWoo Jong Soo, Chi Moon Hyuk
Назва патенту російськоюКомпозиция с замедленным высвобождением для перорального применения лекарственного средства
Автори російськоюВоо Дзонг-Соо, Чи Моон-Хиук
МПК / Мітки
МПК: A61K 9/34, A61P 9/00, A61K 47/36, A61P 31/00, A61P 3/10, A61K 47/38
Мітки: засобів, уповільненим, композиція, вивільненням, лікарських, введення, перорального
Код посилання
<a href="https://ua.patents.su/11-77123-kompoziciya-z-upovilnenim-vivilnennyam-dlya-peroralnogo-vvedennya-likarskikh-zasobiv.html" target="_blank" rel="follow" title="База патентів України">Композиція з уповільненим вивільненням для перорального введення лікарських засобів</a>
Попередній патент: Композиція інгредієнтів для настоянки “абсент голд”
Наступний патент: Спосіб промислового одержання субстанції флуренізид натрію
Випадковий патент: Похідні діарилпіридазинону, спосіб їх одержання та застосування для лікування людей