Спосіб одержання 2,3-дихлоропіридину
Формула / Реферат
1. Спосіб одержання 2,3-дихлоропіридину 1,
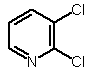 , 1
, 1
який відрізняється тим, що включає стадії:
(1) контактування 3-аміно-2-хлоропіридину 2 або розчину, який містить 3-аміно-2-хлоропіридин 2,
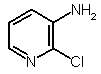 , 2
, 2
з хлористоводневою кислотою з утворенням 3-аміно-2-хлоропіридинової солі хлористоводневої кислоти;
(2) контактування 3-аміно-2-хлоропіридинової солі хлористоводневої кислоти з нітритною сіллю з утворенням відповідної діазоній хлоридної солі; та
(3) контактування відповідної діазоній хлоридної солі з хлористоводневою кислотою у присутності мідного каталізатора, де принаймні 50 % міді складає мідь у стані окиснення (II), з одержанням 2,3-дихлоропіридину 1.
2. Спосіб за п. 1, який відрізняється тим, що нітритна сіль являє собою нітрит натрію.
3. Спосіб за п. 1, який відрізняється тим, що принаймні 75 % міді являють собою мідь у стані окиснення (II).
4. Спосіб за п. 3, який відрізняється тим, що принаймні 90 % міді являють собою мідь у стані окиснення (II).
5. Спосіб за п. 4, який відрізняється тим, що принаймні 95 % міді являють собою мідь у стані окиснення (II).
6. Спосіб за п. 5, який відрізняється тим, що принаймні 99 % міді являють собою мідь у стані окиснення (II).
7. Спосіб за п. 6, який відрізняється тим, що 100 % міді являють собою мідь у стані окиснення (II).
8. Спосіб за п. 1, який відрізняється тим, що зазначений мідний каталізатор включає хлорид міді (II) або оксид міді (II).
9. Спосіб за п. 8, який відрізняється тим, що номінальне мольне відношення нітритної солі до 3-аміно-2-хлоропіридину 2 складає від 0,95 до 2,0; номінальне мольне відношення хлориду Сu (II) або оксиду міді (II) до 3-аміно-2-хлоропіридину 2 складає від 0,05 до 2,0, коли 100 % зазначеної міді являє собою хлорид міді (II) або оксид міді (II); номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2-хлоропіридину 2 на стадії (1) складає від 3 до 10; і номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2-хлоропіридину 2 на стадії (3) складає від більше 0 до 10.
10. Спосіб за п. 9, який відрізняється тим, що номінальне мольне відношення нітритної солі до 3-аміно-2-хлоропіридину 2 складає від 0,95 до 1,1; номінальне мольне відношення міді у мідному каталізаторі до 3-аміно-2-хлоропіридину 2 складає від 0,2 до 0,6; номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2-хлоропіридину 2 на стадії (1) складає від 3 до 6; і номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2-хлоропіридину 2 на стадії (3) складає від 1 до 5.
11. Спосіб за п. 1, який відрізняється тим, що стадії (1) та (2) проводять при температурі, що варіює від -15 до 20 °С; і стадію (3) проводять при температурі, що варіює від 30 до 90 °С.
12. Спосіб за п. 11, який відрізняється тим, що стадії (1) та (2) проводять при температурі, що варіює від -10 до 10 °С; і стадію (3) проводять при температурі, що варіює від 50 до 80 °С.
13. Спосіб за п. 1, який відрізняється тим, що 3-аміно-2-хлоропіридин 2 або розчин, який містить 3-аміно-2-хлоропіридин 2, одержують за способом, який включає стадії:
(a) контактування 3-амінопіридину 3 або розчину, який містить 3-амінопіридин 3
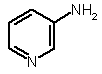 , 3
, 3
з хлористоводневою кислотою з утворенням 3-амінопіридинової хлористоводневої солі;
(b) контактування 3-амінопіридинової хлористоводневої солі з агентом хлорування з утворенням розчину, який містить 3-аміно-2-хлоропіридин 2; та
(c) при потребі, виділення зазначеного 3-аміно-2-хлоропіридину 2 із розчину стадії (b).
14. Спосіб за п. 13, який відрізняється тим, що агент хлорування являє собою хлор, гіпохлорит лужного металу або суміш хлористоводневої кислоти та пероксиду водню.
15. Спосіб за п. 14, який відрізняється тим, що агент хлорування являє собою хлор або суміш хлористоводневої кислоти та пероксиду водню.
16. Спосіб за п. 13, який відрізняється тим, що номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину 3 на стадії (а) складає від 3 до 20; і номінальне мольне відношення агента хлорування до 3-амінопіридину 3 на стадії (а) складає від 0,6 до 1,5.
17. Спосіб за п. 16, який відрізняється тим, що номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину 3 на стадії (а) складає від 5 до 15; і номінальне мольне відношення агента хлорування до 3-амінопіридину 3 на стадії (а) складає від 0,8 до 1,2.
18. Спосіб за п. 13, який відрізняється тим, що стадії (а) та (b) проводять при температурі, що варіює від 0 до 60 °С.
19. Спосіб за п. 18, який відрізняється тим, що стадії (а) та (b) проводять при температурі, що варіює від 10 до 35 °С.
20. Спосіб за п. 13, який відрізняється тим, що 3-амінопіридин 3 або розчин, який містить 3-амінопіридин 3, одержують за способом, який включає стадії:
(і) контактування нікотинаміду 4
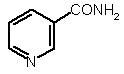 4
4
з сильною основою та агентом галогенування з утворенням суміші, яка містить N-галонікотинамідну сіль;
(іі) контактування зазначеної N-галонікотинамідної сольової суміші, утвореної на стадії (і), з нагрітою водою з утворенням водної суміші та витримки даної водної суміші при температурі, що варіює від 65 до 100 °С з утворенням розчину, який містить 3-амінопіридин 3;
(ііі) виділення 3-амінопіридину 3 із розчину стадії (іі), якщо агент галогенування є іншим, ніж агент хлорування; та
(iv) при потребі, виділення 3-амінопіридину 3 із розчину стадії (іі), якщо агент галогенування є агентом хлорування.
21. Спосіб за п. 20, який відрізняється тим, що сильна основа являє собою гідроксид лужного металу.
22. Спосіб за п. 21, який відрізняється тим, що гідроксид лужного металу являє собою гідроксид натрію.
23. Спосіб за п. 20, який відрізняється тим, що агент галогенування являє собою хлор, бром або гіпохлорит натрію.
24. Спосіб за п. 20, який відрізняється тим, що номінальне мольне відношення зазначеної сильної основи до нікотинаміду 4 складає від 1 до 5; і номінальне мольне відношення агента галогенування до нікотинаміду 4 складає від 0,8 до 2,0.
25. Спосіб за п. 24, який відрізняється тим, що номінальне мольне відношення сильної основи до нікотинаміду 4 складає від 2 до 4, якщо даним агентом галогенування є хлор або бром; номінальне мольне відношення даної сильної основи до нікотинаміду 4 складає від 1 до 2, якщо даним агентом галогенування є гіпохлорит натрію; і номінальне мольне відношення агента галогенування до нікотинаміду 4 складає від 0,9 до 1,1.
26. Спосіб за п. 20, який відрізняється тим, що стадію (і) проводять при температурі, що варіює від -5 до 20 °С.
27. Спосіб за п. 26, який відрізняється тим, що стадію (і) проводять при температурі, що варіює від 0 до 10 °С; і стадію (іі) проводять при температурі, що варіює від 70 до 95 °С.
28. Спосіб за п. 1, який відрізняється тим, що стадію (3) проводять в присутності органічного розчинника.
Текст
1. Спосіб одержання 2,3-дихлоропіридину 1, Cl 2 (19) 1 3 аміно-2-хлоропіридин 2, одержують за способом, який включає стадії: (a) контактування 3-амінопіридину 3 або розчину, який містить 3-амінопіридин 3 NH2 N ,3 з хлористоводневою кислотою з утворенням 3амінопіридинової хлористоводневої солі; (b) контактування 3-амінопіридинової хлористоводневої солі з агентом хлорування з утворенням розчину, який містить 3-аміно-2-хлоропіридин 2; та (c) при потребі, виділення зазначеного 3-аміно-2хлоропіридину 2 із розчину стадії (b). 14. Спосіб за п. 13, який відрізняється тим, що агент хлорування являє собою хлор, гіпохлорит лужного металу або суміш хлористоводневої кислоти та пероксиду водню. 15. Спосіб за п. 14, який відрізняється тим, що агент хлорування являє собою хлор або суміш хлористоводневої кислоти та пероксиду водню. 16. Спосіб за п. 13, який відрізняється тим, що номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину 3 на стадії (а) складає від 3 до 20; і номінальне мольне відношення агента хлорування до 3-амінопіридину 3 на стадії (а) складає від 0,6 до 1,5. 17. Спосіб за п. 16, який відрізняється тим, що номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину 3 на стадії (а) складає від 5 до 15; і номінальне мольне відношення агента хлорування до 3-амінопіридину 3 на стадії (а) складає від 0,8 до 1,2. 18. Спосіб за п. 13, який відрізняється тим, що стадії (а) та (b) проводять при температурі, що варіює від 0 до 60 °С. 19. Спосіб за п. 18, який відрізняється тим, що стадії (а) та (b) проводять при температурі, що варіює від 10 до 35 °С. 20. Спосіб за п. 13, який відрізняється тим, що 3амінопіридин 3 або розчин, який містить 3амінопіридин 3, одержують за способом, який включає стадії: (і) контактування нікотинаміду 4 CONH2 N 86604 4 з сильною основою та агентом галогенування з утворенням суміші, яка містить Nгалонікотинамідну сіль; (іі) контактування зазначеної N-галонікотинамідної сольової суміші, утвореної на стадії (і), з нагрітою водою з утворенням водної суміші та витримки даної водної суміші при температурі, що варіює від 65 до 100 °С з утворенням розчину, який містить 3амінопіридин 3; (ііі) виділення 3-амінопіридину 3 із розчину стадії (іі), якщо агент галогенування є іншим, ніж агент хлорування; та (iv) при потребі, виділення 3-амінопіридину 3 із розчину стадії (іі), якщо агент галогенування є агентом хлорування. 21. Спосіб за п. 20, який відрізняється тим, що сильна основа являє собою гідроксид лужного металу. 22. Спосіб за п. 21, який відрізняється тим, що гідроксид лужного металу являє собою гідроксид натрію. 23. Спосіб за п. 20, який відрізняється тим, що агент галогенування являє собою хлор, бром або гіпохлорит натрію. 24. Спосіб за п. 20, який відрізняється тим, що номінальне мольне відношення зазначеної сильної основи до нікотинаміду 4 складає від 1 до 5; і номінальне мольне відношення агента галогенування до нікотинаміду 4 складає від 0,8 до 2,0. 25. Спосіб за п. 24, який відрізняється тим, що номінальне мольне відношення сильної основи до нікотинаміду 4 складає від 2 до 4, якщо даним агентом галогенування є хлор або бром; номінальне мольне відношення даної сильної основи до нікотинаміду 4 складає від 1 до 2, якщо даним агентом галогенування є гіпохлорит натрію; і номінальне мольне відношення агента галогенування до нікотинаміду 4 складає від 0,9 до 1,1. 26. Спосіб за п. 20, який відрізняється тим, що стадію (і) проводять при температурі, що варіює від -5 до 20 °С. 27. Спосіб за п. 26, який відрізняється тим, що стадію (і) проводять при температурі, що варіює від 0 до 10 °С; і стадію (іі) проводять при температурі, що варіює від 70 до 95 °С. 28. Спосіб за п. 1, який відрізняється тим, що стадію (3) проводять в присутності органічного розчинника. 4 Є потреба в ефективних та практичних способах одержання 2,3-дихлоропіридину. 2,3дихлоропіридин є важливим сировинним матеріалом для приготування агентів захисту врожаю, фармацевтичних препаратів та інших чистих реактивів. H.J. den Hertog, et al., Reel. Trav. Chim. PaysBas, 1950, 69, 673, доповів про одержання 2,3дихлоропіридину із 3-аміно-2-хлоропіридину за реакцією Гаттермана, де як каталізатор використовувався порошок міді. Проте, придатність зазна ченого способу жорстко обмежена з плані низького виходу, про який повідомлялось (приблизно 45%), та обмеженого обсягу (приблизно 1 г). Даний винахід стосується способу одержання 2,3-дихлоропіридину 1, що включає стадії: 5 (1) контактування 3-аміно-2-хлоропіридину 2 або розчину, який містить 3-аміно-2 хлоропіридин 2, з хлористоводневою кислотою з утворенням 3аміно-2-хлоропіридинової солі хлористоводневої кислоти; (2) контактування 3-аміно-2-хлоропіридинової солі хлористоводневої кислоти з нітритною сіллю з утворенням відповідної діазонієвої хлоридної солі; та (3) контактування відповідної діазонієвої хлоридної солі з хлористоводневою кислотою у присутності мідного каталізатора, де принаймні приблизно 50% міді складає мідь у стані окиснення (II), при потребі, у присутності органічного розчинника, з одержанням 2,3-дихлоропіридину 1. Даний винахід також стосується вищезазначеного способу одержання 2,3-дихлопіридину 1, де 3-аміно-2-хлоропіридин 2 або розчин, який містить 3-аміно-2-хлоропіридин 2, одержується за способом, який включає стадії: (a) контактування 3-амінопіридину 3 або розчину, який містить 3-амінопіридин 3 з хлористоводневою кислотою з утворенням 3амінопіридинової хлористоводневої солі; (b) контактування 3-амінопіридинової хлористоводневої солі з агентом хлорування з утворенням розчину, який містить 3-аміно-2-хлоропіридин 2; та (c) при потребі, виділення зазначеного 3аміно-2-хлоропіридину 2 із розчину стадії (b). Даний винахід також стосується вищезазначених способів одержання 2,3-дихлоропіридину 1, де 3-амінопіридин 3 або розчин, який містить 3амінопіридин 3, одержується за способом, який включає стадії: (і) контактування нікотинаміду 4 з сильною основою та агентом галогенування з утворенням суміші, яка містить Nгалонікотинамідну сіль; (іі) контактування зазначеної Nгалонікотинамідної сольової суміші, утвореної на стадії (і), з нагрітою водою з утворенням водної 86604 6 суміші та витримки даної водної суміші при температурі, що варіює від приблизно 65 до приблизно 100 °С з утворенням розчину, який містить 3амінопіридин 3; (ііі) виділення 3-амінопіридину 3 із розчину стадії (іі), якщо агент галогенування є іншим, ніж агент хлорування; та (iv) при потребі, виділення 3-амінопіридину 3 із розчину стадії (іі), якщо агент галогенування є агентом хлорування. Як застосовується у даному тексті, терміни "охоплює", "що охоплює", "включає", "що включає", "має", "що має", "містить", "що містить", або будьякі інші їх варіанти, як мається на думці, покривають не ексклюзивне включення. Наприклад, композиція, суміш, процес, спосіб, виріб або апарат, що включає перелік елементів, не обов'язково обмежується лише цими елементами, але може включати й інші елементи, котрі навмисно не перелічені або притаманні таким композиціям, сумішам, процесам, способам, виробам або апаратам. Крім того, якщо спеціально не зазначено інше, "або" стосується інклюзивного або, а не ексклюзивного або. Наприклад, стан А або В задовольняється будь-яким із наступного: А є істина (або присутнє), і В є неправда(або не є присутнє), А є неправда (або не є присутнє), і В є істина (або присутнє), і як А, так і В є істиною (або присутні). Крім того, невизначені артиклі "а" та "an", що передують елементу або компоненту даного винаходу, як мається на думці, мають нерестриктивний характер стосовно числа прикладів (тобто появ) даного елемента чи компонента. Тому "а" та "an" мають прочитуватись як такі, що включають один або принаймні один, і окрема словесна форма елемента чи композиції також включає множинне число, якщо вона не є явно окремою. Варіанти даного винаходу включають: Варіант А. Спосіб (Спосіб А) одержання 2,3дихлоропіридину 1, що включає стадії: (1) контактування розчину, який містить 3аміно-2-хлоропіридин 2, з першим водним розчином, який містить хлористоводневу кислоту, з утворенням 3-аміно-2 хлоропіридинової солі хлористоводневої кислоти; (2) контактування 3-аміно-2-хлоропіридинової солі хлористоводневої кислоти з водним розчи 7 ном, який містить нітритну сіль, з утворенням діазонієвої солі; та (3) контактування зазначеної діазонієвої солі з водним розчином, який містить Сu (II) сіль, присутності другого водного розчину, який містить хлористоводневу кислоту, при потребі, присутності органічного розчинника, з одержанням 2,3дихлоропіридину 1. Варіант 1. Спосіб, згідно з Варіантом А, де зазначена нітритна сіль являє собою нітрит натрію. Варіант 2. Спосіб, згідно з Варіантом А, де зазначена Сu(ІІ) сіль являє собою хлорид міді (І або оксид міді (II), Варіант 3. Спосіб, згідно з Варіантом А, де номінальне мольне відношення нітритної солі до 3-аміно-2-хлоропіридину складає від приблизно 0,95 до приблизно 2,0; номінальне мольне відношення Сu(ІІ) солі до 3-аміно-2-хлоропіридину складає від приблизно 0,05 до приблизно 2,0; номінальне мольне відношення хлористоводневої кислоти у першому водному розчині до 3аміно-2-хлоропіридину складає від приблизно 3 до приблизно 10; та номінальне мольне відношення хлористоводневої кислоти у другому водному розчині до 3аміно-2-хлоропіридину складає від приблизно 0 до приблизно 10. Варіант 4. Спосіб, згідно з Варіантом 3, де номінальне мольне відношення нітритної солі до 3-аміно-2-хлоропіридину складає від приблизно 0,95 до приблизно 1,1; номінальне мольне відношення Cu(II) солі до 3-аміно-2-хлоропіридину складає від приблизно 0,2 до приблизно 0,6; номінальне мольне відношення хлористоводневої кислоти у першому водному розчині до 3аміно-2-хлоропіридину складає від приблизно 3 до приблизно 6; та номінальне мольне відношення хлористоводневої кислоти у другому водному розчині до 3аміно-2-хлоропіридину складає від приблизно 1 до приблизно 5. Варіант 5. Спосіб, згідно з Варіантом А, де стадії (1) та (2) проводяться при температурі, що варіює від приблизно -15 до приблизно 20 °С; і стадія (3) проводиться при температурі, що варіює від приблизно 30 до приблизно 90 °С. Варіант 6. Спосіб, згідно з Варіантом 5, де температура стадій (1) та (2) варіює від приблизно -10 до приблизно 10 °С; і температура стадії (3) варіює від приблизно 50 до приблизно 80 °С. Варіант В. Спосіб (Спосіб В) одержання 2,3дихлоропіридину 1, що включає стадії: (a) контактування розчину, який містить 3амінопіридин 3 86604 8 з водною хлористоводневою кислотою та агентом хлорування з утворенням суміші; (b) виділення розчину, який містить З-аміно-2хлоропіридинову хлористоводневу сіль, і зазначеної суміші; та (c) використання розчину, який містить 3аміно-2-хлоропіридинову хлористоводневу сіль способі Варіанту А, що описаний вище, для одержання 2,3-дихлоропіридину. Варіант а. Спосіб, згідно з Варіантом В, де зазначений агент хлорування являє собою хлор, гіпохлорит лужного металу або суміш хлористоводневої кислоти та пероксиду водню. Варіант b. Спосіб, згідно з Варіантом а, де зазначений агент хлорування являє собою хлор або суміш пероксиду водню та хлористоводневої кислоти. Варіант с Спосіб, згідно з Варіантом В, де номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину складає від приблизно 3 до приблизно 20; та номінальне мольне відношення агенту хлорування до 3-амінопіридину складає від приблизно 0,6 до приблизно 1,5. Варіант d. Спосіб, згідно з Варіантом с, де номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину складає від приблизно 5 до приблизно 15; та номінальне мольне відношення агенту хлорування до 3-амінопіридину складає від приблизно 0,8 до приблизно 1,2. Варіант є. Спосіб, згідно з Варіантом В, де стадія (а) проводиться при температурі, що варіює від приблизно 0 до приблизно 60 °С. Варіант f. Спосіб, згідно з Варіантом є, де температура на стадії (а) варіює від приблизно 10 до приблизно 35 °С. Варіант С Спосіб (Спосіб С) одержання 2,3дихлоропіридину 1, який включає стадії: (і) контактування нікотинаміду 4 з сильною основою та агентом галогенування у водному розчині при температурі, що варіює від приблизно -5 до приблизно 20 °С, з утворенням суміші, яка містить N-галонікотинамідну сіль; (іі) контактування зазначеної Nгалонікотинамідної сольової суміші, утвореної на стадії (і), з водою та витримки результуючої водної суміші при температурі, що варіює від приблизно 65 до приблизно 100 °С; (ііі) виділення розчину, який містить 3амінопіридинову хлористоводневу сіль, із водної суміш стадії (іі); та (iv) використання розчину, який містить 3амінопіридинову хлористоводневу сіль у Способі В що описаний вище, для одержання 2,3дихлоропіридину. 9 Варіант і. Спосіб, згідно з Варіантом С, де зазначена сильна основа являє собою гідроксид лужного металу. Варіант іі. Спосіб, згідно з Варіантом і, де зазначений гідроксид лужного металу являє собою гідроксид натрію. Варіант ііі. Спосіб, згідно з Варіантом С, де зазначений агент галогенування являє собою хлор, бром або гіпохлорит натрію. Варіант iv. Спосіб, згідно з Варіантом С, де номінальне мольне відношення сильної основи до нікотинаміду складає від приблизно 1 до приблизно 5; і номінальне мольне відношення агенту галогенування до нікотинаміду складає від приблизно 0,8 до приблизно 2,0. Варіант ν. Спосіб, згідно з Варіантом iv, де номінальне мольне відношення зазначеної сильної основи до нікотинаміду складає від приблизно 2 до приблизно 4, коли зазначеним агентом галогенування є хлор номінальне мольне відношення зазначеної сильної основи до нікотинаміду складає від приблизно 1 до приблизно 2, коли зазначеним агентом галогенування є гіпохлорит натрію; і номінальне мольне відношення зазначеного агенту галогенування до нікотинаміду складає від приблизно 0,9 до приблизно 1,1. Варіант vi. Спосіб, згідно з Варіантом vi, де температура стадії (і) варіює від приблизно 0 до приблизно 10 °С; і температура стадії (іі) варіює від приблизно 70 до приблизно 95 °С. Варіант В'. Спосіб (Спосіб В') одержання 2,3дихлоропіридину 1, який включає стадії: (а') контактування розчину, який містить 3-амінопіридин 3 з водною хлористоводневою кислотою та агентом хлорування з утворенням розчину, який містить 3-аміно-2-хлоропіридинову хлористоводневу сіль; (b') при потребі, виділення 3-аміно-2хлоропіридину 2 із розчину стадії (а'); та (с') використання розчину стадії (а') або 3аміно-2-хлоропіридину 2 стадії (b') у Варіанті А для одержання 2,3-дихлоропіридину 1. Варіанти a-f, що наведені вище для додаткового опису Варіанту В (Способу В), також Варіантами Варіанту В' (Способу В'). Варіант С’. Спосіб (Спосіб С’) одержання 2,3дихлоропіридину 1, який включає стадії: (і') контактування нікотинаміду 4 86604 10 з сильною основою та агентом галогенування у водному розчині при температурі, що варіює ві приблизно -5 до приблизно 20 °С, з утворенням суміші, яка містить N-галонікотинамідну сіль; (іі') контактування зазначеної Nгалонікотинамідної сольової суміші, утвореної на стад (і'), з нагрітою водою з утворенням водної суміші та витримки зазначеної водної суміші пр температурі, що варіює від приблизно 65 до приблизно 100 °С, з утворенням розчину, яки містить 3-амінопіридин 3; (ііі') при потребі, виділення 3-амінопіридину 3 із водної суміші стадії (іі'); та (iv') використання розчину стадії (іі'), якщо агент галогенування є агентом хлорування, або 3амінопіридину 3 стадії (ііі') у Варіанті В' для одержання 3-аміно-2-хлоропіридину 2 Варіанти i-vi, що наведені вище для додаткового опису Варіанту С (Способу С), також є Варіантами Варіанту С (Способу С). Варіант АА. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де зазначеною нітритною сіллю є нітрит натрію. Варіант ВВ Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де принаймні 75% міді являють собою мідь у стані окиснення (II). Варіант СС. Спосіб, згідно з Варіантом ВВ, де принаймні приблизно 90% міді являють собою мідь у стані окиснення (II). Варіант DD. Спосіб, згідно з Варіантом СС, де принаймні приблизно 95% міді являють собою мідь у стані окиснення (II). Варіант ЕЕ. Спосіб, згідно з Варіантом DD, де принаймні приблизно 99% міді являють собою мідь у стані окиснення (II). Варіант FF. Спосіб, згідно з Варіантом ЕЕ, де 100% міді являють собою мідь у стані окиснення (II). Варіант GG. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де зазначений мідний каталізатор включає хлорид міді (II) або оксид міді (II). Варіант НН. Спосіб, згідно з Варіантом GG, де номінальне мольне відношення нітритної солі до 3-аміно-2-хлоропіридину 2 складає від приблизно 0,95 до приблизно 2,0; номінальне мольне відношення хлориду міді (II) або оксиду міді (II) до 3аміно-2-хлоропіридину 2 складає від приблизно 0,05 до приблизно 2,0, коли 100% зазначеної міді являє собою хлорид міді (II) або оксид міді (II); номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2-хлоропіридину 2 на стадії (1) складає від приблизно 3 до приблизно 10; і номінальне мольне відношення хлористоводневої кис 11 лоти до 3-аміно-2-хлоропіридину 2 на стадії (3) складає від приблизно 0 до приблизно 10. Варіант ІІ. Спосіб, згідно з варіантом НН, де номінальне мольне відношення нітритної солі до 3-аміно-2-хлоропіридину 2 складає від приблизно 0,95 до приблизно 1,1; номінальне мольне відношення міді у мідному каталізаторі до 3-аміно-2хлоропіридину 2 складає від приблизно 0,2 до приблизно 0,6; номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2хлоропіридину 2 на стадії (1) складає від приблизно 3 до приблизно 6; і номінальне мольне відношення хлористоводневої кислоти до 3-аміно-2хлоропіридину 2 на стадії (3) складає від приблизно 1 до приблизно 5. Варіант JJ. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де стадії (1) та (2) проводяться пари температурі, що варіює від приблизно -15 до приблизно 20 °С; і стадія (3) проводиться при температурі, що варіює від приблизно 30 до приблизно 90 °С. Варіант КК. Спосіб, згідно з Варіантом JJ, де стадії (1) та (2) проводяться при температурі, що варіює від приблизно -10 до приблизно 10 °С; і стадія (3) проводиться при температурі, що варіює від приблизно 50 до приблизно 80 °С. Варіант LL. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де агент хлорування являє собою хлор, гіпохлорит лужного металу або суміш хлористоводневої кислоти та пероксиду водню. Варіант MM. Спосіб, згідно з Варіантом LL, де зазначеним агентом хлорування є хлор або суміш хлористоводневої кислоти та пероксиду водню. Варіант NN. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину 3 на стадії (а) складає від приблизно 3 до приблизно 20; і номінальне мольне відношення агенту хлорування до 3-амінопіридину 3 на стадії (а) складає від приблизно 0,6 до приблизно 1,5. Варіант ОО. Спосіб, згідно з Варіантом NN, де номінальне мольне відношення хлористоводневої кислоти до 3-амінопіридину 3 на стадії (а) складає від приблизно 5 до приблизно 15; і номінальне мольне відношення агенту хлорування до 3амінопіридину 3 на стадії (а) складає від приблизно 0,8 до приблизно 1,2. Варіант PP. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де стадії (а) та (b) проводяться пари температурі, що варіює від приблизно 0 до приблизно 60 °С. Варіант QQ. Спосіб, згідно з Варіантом РР, де стадії (а) та (b) проводяться пари температурі, що варіює від приблизно 10 до приблизно 35 °С. Варіант RR. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де зазначена сильна основа являє собою гідроксид лужного металу. Варіант SS. Спосіб, згідно з Варіантом RR, де зазначеним гідроксидом лужного металу є гідроксид натрію. 86604 12 Варіант ТТ. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де агент галогенування являє собою хлор, бром або гіпохлорит натрію. Варіант UU. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де номінальне мольне відношення зазначеної сильної основи до нікотинаміду 4 складає від приблизно 1 до приблизно 5; і номінальне мольне відношення агенту галогенування до нікотинаміду 4 складає від приблизно 0,8 до приблизно 2,0. Варіант VV. Спосіб, згідно з Варіантом UU, де номінальне мольне відношення зазначеної сильної основи до нікотинаміду 4 складає від приблизно 2 до приблизно 4, коли даним агентом галогенування є хлор або бром; номінальне мольне відношення даної сильної основи до нікотинаміду 4 складає від приблизно 1 до приблизно 2, коли даним агентом галогенування є гіпохлорит натрію; і номінальне мольне відношення агенту галогенування до нікотинаміду 4 складає від приблизно 0,9 до приблизно 1,1 Варіант WW. Спосіб одержання 2,3дихлоропіридину 1 як визначено у Стислому викладі винаходу, де стадія (і) проводиться при температурі, що варіює від приблизно -5 до приблизно 20 °С. Варіант XX. Спосіб, згідно з Варіантом WW, де стадія (і) проводиться при температурі, що варіює від приблизно 0 до приблизно 10 °С; і стадія (іі) проводиться при температурі, що варіює від приблизно 70 до приблизно 95 °С. Згідно з даним винаходом, наприклад, Спосіб А, як показано на Схемі 1, 2,3-дихлоропіридин 1 одержується шляхом діазотизації 2-хлоро-3амінопіридину 2 з наступним розкладом діазонієвої хлоридної солі у присутності солі Сu(ІІ), тобто у присутності мідного каталізатора, де принаймні приблизно 50% міді являють собою мідь у стані окиснення (II). Діазонієва хлоридна сіль може бути одержана за реакцією 3-аміно-2-хлоропіридину 2 з азотистою кислотою у водному розчині при придатній температурі. Азотиста кислота може бути одержана in situ із нітритної солі та хлористоводневої кислоти. Можуть використовуватись різні нітритні солі, такі як нітрит натрію, нітрит калію, нітрит кальцію або будь-який нітрит лужного або лужноземельного металу. У плані ціни та наявності придатною нітритною сіллю є нітрит натрію. Посилання щодо одержання діазонієвих солей дивись у роботах Н. Zollinger, Azo and Diazo Chemistry, Wiley-Interscience, New York, 1961; S Patai, The Chemistry of Diazonium and Diazo Groups, Wiley. New York, 1978, Chapters 8, 11 та 14; та Η. Saunders and R.L.M. Allen, Aromatic Diazo 13 Compounds, Third Edition, Edward Arnold, London, 1985. В одному із варіантів способу даного винаходу розчин, який містить 3-аміно-2-хлоропіридин 2, контактує з першим водним розчином, що містить хлористоводневу кислоту, з утворенням 3аміно-2-хлоропіридинової хлористоводневої солі. Потім дана 3-аміно-2-хлоропіридинова хлористоводнева сіль контактує з водним розчином, який містить нітритну сіль, з утворенням діазонієвої хлоридної солі. Діазотизація 3-аміно-2хлоропіридинової хлористоводневої солі здійснюється відповідним чином шляхом додавання водного нітриту натрію до суміші 3-аміно-2хлоропіридину 2 у приблизно від 10% до приблизно 37% водної хлористоводневої кислоти. Додаткові варіанти для цих стадій даного способу, наприклад, проте не обмежуючись цим, Способу А, описані вище. Діазонієва хлоридна сіль розкладається у присутності хлористоводневої кислоти та мідного каталізатора, де принаймні приблизно 50 % міді являють собою мідь у стані окиснення (II) з одержанням 2,3-дихлоропіридину 1. У додаткових варіантах принаймні приблизно 75%, принаймні приблизно 90%, принаймні приблизно 95%, принаймні приблизно 99% або 100% міді являють собою мідь у стані окиснення (II). Мідний каталізатор може включати, наприклад, проте не обмежуючись цим, ацетат міді (II), нітрат міді (II), сульфат міді (II), оксид (CuO) міді (II) або хлорид (СuСl2) міді (II). В одному варіанті зазначений мідний каталізатор включає оксид (CuO) міді (II), хлорид (CuCl2) міді (II) або хлорид міді (II), одержаний in situ із CuO та хлористоводневої кислоти (НСl). В інших варіантах принаймні 75% міді являють собою хлорид міді (II); принаймні 90% міді являють собою хлорид міді (II); принаймні 95% міді являють собою хлорид міді (II); принаймні 99% міді являють собою хлорид міді (II); 100% міді являють собою хлорид міді (II); принаймні 75% міді являють собою оксид міді (II); принаймні 90% міді являють собою оксид міді (II); принаймні 95% міді являють собою оксид міді (II), принаймні 99% міді являють собою оксид міді (II); і 100% міді являють собою оксид міді (II). Розклад може проводитись у водному розчині, тобто в однофазовій системі, що містить від приблизно 0 до приблизно 10, від приблизно 1 до приблизно 5 мольних еквівалентів (відносно 3аміно-2-хлоропіридину 2) від приблизно 10% до приблизно 37% водної НСl, та від приблизно 0,05 до приблизно 2, від приблизно 0,2 до приблизно 0,6 мольних еквівалентів (відносно 3-аміно-2хлоропіридину 2) мідного каталізатора при температурі, що варіює від приблизно 30 до приблизно 90 °С. В одному із варіантів температура розкладу складає від приблизно 50 до приблизно 80 °С. Продукт, 2,3-дихлоропіридин 1, в однофазовій системі, може бути виділений шляхом охолодження даної реакційної суміші до кімнатної температури, додавання, при потребі, основи для нейтралізації реакційної суміші з наступною фільтрацією. Розклад може також проводитись у двохфазовій системі, що містить придатний органічний розчинник та водний розчин зазначеної однофазової системи. Придатним органічним розчинником для 86604 14 даної двохфазової системи може бути, наприклад, проте не обмежуючись цим, тетрагідрофуран, циклогексан, етилацетат, n-хлоробутан, толуол або бензол. Об'ємне співвідношення органічної фази та водної фази у даній двохфазовій системі може варіювати від приблизно 1:10 до приблизно 10:1 Продукт, 2,3-дихлоропіридин 1, у даній двохфазовій системі, може бути виділений шляхом розведення реакційної маси водою або водною основою, розділення фаз та концентрування органічної фази до сухого стану. Даний продукт, 2,3дихлоропіридин 1, може також бути виділений із органічної фази розділенням фаз шляхом кристалізації. Кристалізація може проводитись шляхом парціального концентрування органічного розчину та додаванням, при потребі, "антирозчинника", такого як гептан або вода. Під "антирозчинником" мається на думці рідкий розріджувач, який при додаванні до розчину потрібного продукту знижує розчинність даного продукту у результуючій суміші. Так, якщо даний розчинник є полярним розчинником, таким як амід або нижчий спирт, такий як DMF або етанол, придатним антирозчинником може бути вода. З іншого боку, якщо даний розчинник є помірно неполярним розчинником, таким як етилацетат або дихлорометані, придатним антирозчинником може бути сильно неполярний або вуглеводневий розчинник, такий як циклогексан чи гептан. Вихід виділеного 2,3-дихлоропіридину 1 (приблизно 98% чистоти) може дорівнювати приблизно 90-95%, виходячи із чистого 3-аміно-2хлоропіридину 2. Водна фаза після розділення фаз може повертатись безпосередньо до наступної порції, що піддається розкладу, при потребі, з парціальним концентруванням, для повторного використання Сu(ІІ) сольового каталізатора та надлишку хлористоводневої кислоти. Згідно з даним винаходом, як показано на Схемі 2, наприклад, Спосіб В або Спосіб В', 2,3дихлоропіридин 1 може одержуватись шляхом хлорування 3-амінопіридину 3 з наступною діазотизацією результуючої проміжної сполуки 2-хлоро3-амінопіридину 2 та розкладом даної діазонієвої хлоридної солі, як описано вище, наприклад, у Способі А. В одному варіанті способу даного винаходу розчин, який містить 3-амінопіридин 3, контактує з водною хлористоводневою кислотою та агентом хлорування з утворенням суміші. Хлорування 3амінопіридину 3 може досягатись з допомогою різних придатних хлоруючих агентів, таких як хлор, гіпохлорит лужного металу (такого як літій, натрій або калій), або суміші хлористоводневої кислоти та пероксиду водню. Варіанти агентів хлорування також описані вище. Як відомо, 3-аміно-2хлоропіридин 2 одержується із 3-амінопіридину 3 шляхом реакції останнього з хлористоводневою кислотою та пероксидом водню при температурі 70-80 °С (О. von Schickh, A. Binz, та A. Schultz, Chem. Веr.,1936, 69, 2593). Проте, цей спосіб легко 15 дає надлишково хлоровані продукти (наприклад, 3-аміно-2,6-дихлоропіридин) через відносно високу реакційну температуру. Цей спосіб був оптимізований Yuan et al. (Zhongguo Yiyao Gongye Zazhi, 2000, 31, 420), для зниження реакційної температури до 20-30 °С та зменшення кількості надлишково хлорованого продукту до 8 ваг.% шляхом використання 1 мольн. еквівал. 15 ваг.% пероксиду водню та концентрованої водної НСl (приблизно 37 ваг.%). Як відомо, 3-аміно-2-хлоропіридин 2 може також бути одержаний із 3-амінопіридину 3 шляхом хлорування 3-амінопіридину 3, що каталізується перехідним металом (Blank, et al., US 3838136). Цей спосіб хоча й запроваджує кращі виходи у масштабах виробництва, ніж описаний вище спосіб фон Шика (von Schickh), але має обмеження у плані потреби застосування небезпечного матеріалу (хлору), у тому, що даний продукт виділяється у вигляді твердої речовини у відносно забрудненій формі (приблизно 87 ваг.%), і у тому, що металічний каталізатор погано рециркулюється, що може створювати проблеми, пов'язані з вилученням відходів. Очищення 3-аміно-2-хлоропіридину 2, одержаного за способом Blank et al, від побічного продукту, 3-аміно-2,6-дихлоропіридину, описано К. Іеnо у JP 09227522. В одному варіанті даного винаходу для одержання більш високоякісного 3-аміно-2хлоропіридину 2 із 3-амінопіридину 3 застосовується більш селективний спосіб хлорування шляхом використання висококонцентрованого пероксиду водню (від приблизно 20 до приблизно 50 ваг.%), концентрованої НСl та низької температури (від приблизно 10 до приблизно 35 °С). Цей селективний спосіб може мінімізувати утворення надлишково хлорованих продуктів (головним чином, 3-аміно-2,6-дихлоропіридину) навіть при високому відсотку перетворення 3-амінопіридину 3. Крім того, модифікація способу Іеnо дає можливість легко проводити очистку 3-аміно-2-хлоропіридину 2 і уводити його на стадію діазотизації без застосування рекристалізації та фільтрації. Описаний вище спосіб селективного хлорування може здійснюватись у присутності від приблизно 3 до приблизно 20, від приблизно 5 до приблизно 15 мольних еквівалентів концентрованої водної хлористоводневої кислоти відносно 3амінопіридину 3 і від приблизно 0,6 до приблизно 1,5, від приблизно 0,8 до приблизно 1,2 мольних еквівалентів пероксиду водню або хлору відносно 3-амінопіридину 3. Концентрація хлористоводневої кислоти може варіювати від приблизно 30 до приблизно 37 ваг.%. В одному із варіантів використовується максимальна концентрація НСl для досягнення оптимальної швидкості реакції та селективності на стадії хлорування. Зазначене хлорування може проводитись шляхом додавання від приблизно 30 до приблизно 50 ваг.% водного пероксиду водню при температурі, що варіює від приблизно 0 до приблизно 60 °С, протягом 1-8 годин до суміші 3-амінопіридину 3 та концентрованої хлористоводневої кислоти. Як альтернатива, хлорування може проводитись шляхом додавання газуватого хлору при температурі, що варіює від 86604 16 приблизно 0 до приблизно 35 °С, до досягнення >90 % перетворення 3-амінопіридину 3. В одному із варіантів температура хлорування варіює від приблизно 10 до приблизно 35 °С, що пов'язано з селективністю та швидкістю реакції. При >90% перетворенні 3-амінопіридину 3 може досягатись реакційний вихід від приблизно 70 до приблизно 80%. Для виділення неочищеного розчину 3-аміно2-хлоропіридинової хлористоводневої солі із даної суміші надлишково хлоровані побічні продукти можуть вилучатись з використанням модифікованого способу Іеnо, тобто шляхом селективної екстракції зазначених побічних продуктів органічним розчинником, що не змішується з водою, таким як діетиловий ефір, етилацетат, толуол, бензол або хлоробутан, після часткової нейтралізації даної реакційної суміші до рН від приблизно 0,3 до приблизно 1,0 неорганічною основою, такою як гідроксид натрію, гідроксид калію або карбонат натрію. Потім 3-аміно-2-хлоропіридин 2, що залишився у водному розчині, може бути екстрагований тим самим органічним розчинником або іншим придатним органічним розчинником після додаткової нейтралізації водного розчину до рН від приблизно 2 до приблизно 8. У результаті цієї процедури більшість неперетвореного 3-амінопіридину 3 може залишитись у водних відходах. Органічний екстракт, що містить 3-аміно-2-хлоропіридин 2, може екстрагуватись водною хлористоводневою кислотою, і водний екстракт може бути потім використаний у реакції діазотизації як описано вище. Як показано на Схемі 3, один варіант даного винаходу стосується ефективного та об'єднаного способу одержання 2,3-дихлоропіридину 1 без потреби виділення проміжних твердих речовин, наприклад, Спосіб С або Спосіб С Даний спосіб включає перегрупування Гофмана (Hofmann) нікотинаміду 4 з утворенням 3-амінопіридину 3, селективне хлорування 3-амінопіридину 3 з використанням придатного агенту хлорування, такого як описаний вище у Способі В або Способі В', діазотизацію 2-хлоро-3-амінопіридину 2, та розклад діазонієвої хлоридної солі з використанням мідного каталізатора, де принаймні 50% міді являють собою мідь у стані окислення (II), як описано вище у Способі А. Нікотинамід 4 є легкодоступним та ефективним у плані витрат попередником для одержання 3-аміно-2-хлоропіридину 2 та/або 2.3дихлоропіридину 1. Перегрупування Гофмана нікотинаміду 4 з утворенням 3-амінопіридину 3 може досягатись у присутності придатного галогенуючого агенту та сильної основи. Придатним агентом галогенування може бути, наприклад, але не обмежуючись цим, хлор, бром, гіпохлориста кислота, гіпобромиста кислота, гіпохлорит лужного металу (такого як літій, натрій або калій), гіпоброміт лужного металу або бензилтриметиламонійтрибромід. В одному із варіантів галогенуючим агентом даного винаходу є хлор, бром або гіпохлорит натрію. 17 Придатною сильною основою може бути гідроксид лужного металу, включаючи, проте не обмежуючись цим, гідроксид натрію, тобто каустичну соду. Щодо перегрупування Гофмана дивись Org. Synthesis, 1950, 30, 3; US 4082749; Chemistry Letters, 1989, 3, 463. Υ. Ahmad and D.H. Hey (J. Chem. Soc, 1954, 4516) описали процедуру перетворення нікотинаміду 4 у 3-аміно-2-хлоропіридину 2 без потреби виділення проміжної сполуки, 3амінопіридину 3. В одному варіанті способу даного винаходу використане модифіковане перегрупування Гофмана, що включає N-галонікотинамідну сіль, утворену за умов контрольованої подачі, де застосований мольний еквівалент сильної основи відносно нікотинаміду 4 може бути вищим, ніж той, що звичайно використовується у таких перегрупуваннях. Модифіковане перегрупування Гофмана може проводитись шляхом сумісної подачі від приблизно 0,8 до приблизно 2,0 еквівалентів приблизно від 5 до приблизно 15 ваг.% галогенуючого агенту у водному розчині і від приблизно 1,0 до приблизно 5,0 еквівалентів від приблизно 10 до приблизно 50% водної сильної основи відносно від 10 до 30 ваг.% нікотинамідної водної суміші при температурі, що варіює від приблизно -5 до приблизно 20 °С, і при підтримці величини рН реакційної суміші вище приблизно 10. В одному із варіантів температура варіює від приблизно 0 до приблизно 10 °С. Потім результуючий розчин Nгалонікотинамідної солі додається до приблизно від 1 до 10 об'ємів води у другому реакторі протягом від приблизно 0,5 до 3 годин, і результуюча водна суміш підтримується при температурі, що варіює від приблизно 65 до приблизно 100 °С. В одному із варіантів температура реакції складає від приблизно 70 до приблизно 95 °С, що пов'язано зі швидкістю реакції. В іншому варіанті використовується від приблизно 3 до приблизно 4 еквівалентів сильної основи відносно нікотинаміду 4 для мінімізації утворення побічного продукту, ди(3піридил)сечовини, коли агентом галогенування слугує хлор або бром. Ще в одному варіанті використовується від приблизно 1 до приблизно 2 еквівалентів сильної основи відносно нікотинаміду 4, коли галогенуючим агентом є гіпохлорит натрію. Ще в одному варіанті використовується від приблизно 0,9 до приблизно 1,1 еквівалентів галогенуючого агенту відносно нікотинаміду 4. Зазначене модифіковане перегрупування Гофмана може запровадити дуже високий реакційний вихід. Результуюча суміш, що містить неочищений 3амінопіридин 3, може бути спрямована на стадію хлорування як описано вище у Способі В або Способі В' після підкислення кислотою до рН від приблизно 1 до приблизно 5. Для досягнення оптимальної швидкості та селективності хлорування 3амінопіридину 3, що потребує максимальної концентрації НСl, дана підкислена суміш може бути сконцентрована до від приблизно 10 до приблизно 30 ваг.% 3-амінопіридину 3 і потім додана до від приблизно 7 до приблизно 15 еквівалентів газуватої НСl. В одному із варіантів 3-амінопіридин 3 може бути виділений із результуючої водної суміші шляхом екстракції органічними розчинниками та 86604 18 концентрування органічних екстрактів з одержанням неочищеного 3-амінопіридину 3, з подальшим очищенням шляхом кристалізації. Виділений 3амінопіридин 3 може бути використаний на стадії хлорування, як описано вище у Способі В або Способі В'. Можна сподіватись, що фахівець у даній галузі, використовуючи попередній опис, зможе застосувати даний винахід у повній мірі. Тому наступні Приклади мають на меті просто ілюстративний характер і не обмежують у будь-який спосіб даний винахід. Відсотки є ваговими відсотками, якщо не зазначене інше. Кількісну високоефективну рідинну хроматографію даного продукту проводили з використанням попередньо заповненої хроматографічної колонки типу Zorbax Eclipse XDB-C8® (колонка з оберненою фазою, що виготовляється фірмою Aglient Technologies, Palj Alto, CA 94303) (розмір частинок 3 мкм, 4,6 мм x 15 см, елюент 1595% ацетонітрил/0,05% TFА/вода). Приклад 1 Одержання 2,3-Дихлоропіридину 1 До 300-мл колби з боковим відгалуженням завантажували 12,8 г (0,10 моль) комерційного 3аміно-2-хлоропіридину 2, 30 мл води та 30 мл 37% водної НСl. Після охолодження даної суміші до -8 °С (утворилась суспензія) протягом 30 хвилин при температурі від -7 до -3 °С додавали розчин 7,0 г (0,10 ммоль) NaNO2 у 14 мл води. При введенні приблизно половини помаранчевий розчин перетворився у розріджену жовту суспензію. Після введення дану суміш, що містила діазонієву хлоридну сіль, переносили у крапельну лійку з оболонкою при 0 °С. Діазонієву хлоридну сольову суміш додавали по краплях у колбу, що містила 20 мл 37% водної НСl, 60 мл n-BuCl, та 4,5 г CuO при 5562 °С під азотом. Дану реакційну масу розводили 100 мл води, і n-BuCl шар відокремлювали, промивали водою та концентрували до сухого стану з одержанням 13,8 г неочищеного 2,3-дихлоропіридину 1 у вигляді блідо-жовтої твердої речовини (92% вихід) чистотою 98%. Приклад 2 Одержання 3-аміно-2-хлоропіридину 2 з використанням пероксиду водню 3-амінопіридин 3 (30,0 г, 0,32 моль) додавали до 300 мл 37% НСl у 1-л колбі Мортона з повітряним перемішуванням при температурі приблизно 30-35 °С. Після того, як дана суміш була охолоджена до приблизно 10 °С, протягом 20 хвилин при температурі приблизно 10-12 °С додавали 23 г (0,34 моль) 50% пероксиду водню. Дану суміш витримували приблизно при 10 °С протягом 2 годин і потім підігрівали до приблизно 19 °С протягом 2 годин та витримували при цій температурі ще 4 години. Аналіз за методом високоефективної рідинної хроматографії показав приблизно 90% перетворення 3-амінопіридину 3. Після охолодження даної реакційної суміші до 10 °С додавали розчин 6 г сульфіту натрію у 50 мл води. До даної суміші додавали 50 мл толуолу та 200 г (2,5 моль) 50% водного гідроксиду натрію при температурі приблизно 25-35 18 °С. Потім додавали воду для розчинення NaCl, що випав в осад, і шари розді 19 ляли. Органічну фазу піддавали зворотній екстракції 45 г 10% водної НСl для відновлення деякої кількості 3-аміно-2-хлоропіридину 2 в толуоловому екстракті, і повертали назад до вихідної водної фази. Об'єднані водні фази нейтралізували до рН 3 50% водним NaOH та екстрагували толуолом 3 рази. Толуолові екстракти об'єднували, промивали 30 мл насиченого водного NaCl та концентрували до сухого стану з одержанням 33 г неочищеного 3аміно-2-хлоропіридину 2 (76% вихід) чистотою 94%. Як показав аналіз, проведений за методом високоефективної рідинної хроматографії, даний продукт містив приблизно 3 ваг.% 3-аміно-2,6дихлоропіридину. Приклад 3 Одержання 3-аміно-2-хлоропіридину 2 з використанням хлору 3-амінопіридин 3 (21,0 г, 0,223 моль) додавали до 90 мл (приблизно 108 г, 1,08 моль) концентрованої водної НСl (приблизно 37%) у 300-мл колбі з боковим відгалуженням з магнітною мішалкою при 30-35 °С. Дану суміш охолоджували до 15 °С (густа суспензія), і протягом приблизно 1,5 години при 15-20 °С через поверхню барботували газуватий хлор. Аналіз, проведений за методом високоефективної рідинної хроматографії, показав приблизно 93% перетворення 3амінопіридину 3. Дану суміш охолоджували до 10 °С, і додавали розчин 6 г сульфіту натрію у 50 мл води. До даної суміші додавали 30 мл толуолу та 80 г (1,0 моль) 50% водного гідроксиду натрію при температурі приблизно 25-40 °С. Потім додавали воду для розчинення NaCl, що випав в осад, і шари розділяли. Водну фазу екстрагували ще раз 30 мл толуолу. До даної водної фази додавали 10 г 50% NaOH і екстрагували ще 50 мл толуолу для вилучення 3-аміно-2,6-дихлоропіридину. Об'єднану органічну фазу піддавали зворотній екстракції 40 мл 0,2 N водної НСl для відновлення деякої кількості 3-аміно-2-хлоропіридину 2 у толуолових екстрактах, і повертали назад до вихідної водної фази. Об'єднані водні фази розводили 100 мл толуолу та нейтралізували до рН 3 приблизно 20 г 50% водного NaOH при температурі близько 35 °С. Водну фазу екстрагували двома 50-мл порціями толуолу. Толуолові шари об'єднували та промивали 20 мл насиченого водного NaCl. Даний розчин концентрували до сухого стану з одержанням 21,4 г неочищеного 3-аміно-2-хлоропіридину 2 (74% вихід) чистотою 98,6%, котрий містив приблизно 1,4 ваг.% 3-аміно-2,6-дихлоропіридину. Приклад 4 Одержання 3-аміно-2-хлоропіридину 2 із нікотинаміду 4 У 200-мл колбу з боковим відгалуженням завантажували 12,2 г (0,100 моль) нікотинаміду 4 та 60 мл води, і дану суміш охолоджували до приблизно 5 °С. До даної суміші протягом 30 хвилин 19 при 0-5 °С додавали гіпохлорит натрію (63 г, 11,8 ваг.% водний розчин, 0,100 моль) сумісно з 14 г (0,175 моль) 50% водного NaOH з утворенням Nхлоронікотинамідного розчину. У той же час другу колбу (500-мл) завантажували 80 мл води, котру нагрівали до 80 °С. Розчин N-хлоронікотинаміду із першої колби потім переносили у другу колбу протягом 40 хвилин, підтримуючи температуру реакції 86604 20 у межах приблизно 75-81 °С. Залишок у першій колбі споліскували 20 мл води, і потім також переносили у другу колбу. Утворений в результаті розчин витримували при 80 °С протягом 15 хвилин після завершення переносу і потім охолоджували до 40 °С. До даного розчину при 40-50 °С обережно додавали концентровану водну НСl (30 г, 37%, 0,30 моль), і суміш концентрували під зниженим тиском (приблизно 50 мм Hg) доти, поки не було зібрано приблизно 160 мл води. Дану суміш охолоджували до 15 °С, і додавали безводну НСl (35,2 г, приблизно 1 моль). Дану суміш додатково охолоджували до 10 °С, і протягом 1,5 години додавали 10,5 г (приблизно 0,11 моль) 32% водного Н2О2. За 2 години при кімнатній температурі додавали ще 1 г Н2О2, і дану суміш витримували ще протягом 30 хвилин (перетворення близько 93%). До даної суміші при 15-25 °С послідовно додавали бісульфіт натрію (10 мл, 30% водний розчин), 100 мл води, 30 мл толуолу та 67 г 50% водного NaOH. Толуоловий шар відокремлювали, і водний шар промивали 30 мл толуолу. Водний шар підлуговували 4 г 50% водного NaOH до рН 3, і даний продукт частково екстрагували толуолом і потім дихлорометаном. Додатковий продукт екстрагували із водної фази після підлуговування до рН 7. Поєднані органічні екстракти концентрували. Залишок розчиняли у дихлорометані, і результуючий розчин промивали водним NaCl та концентрували до сухого стану з одержанням 10,4 г 3-аміно-2хлоропіридину 2 (загальний вихід 74%) чистотою 95%. Приклад 5 Одержання 2,3-дихлоропіридину 1 із нікотинаміду 4 До суміші 24.4 г (0,200 моль) нікотинаміду 4 та 120 мл води при температурі близько 0 °С додавали гіпохлорит натрію (237 г, 6,89 ваг.% водний розчин, 0,22 моль) протягом 30 хвилин. Після перемішування протягом 15 хвилин при 0 °С до даної суміші додавали водний NaOH (32 г, 0,40 моль, 50 ваг.%) протягом 30 хвилин при 0-5 °С. Цей результуючий розчин додавали до 280 мл води при 90 °С протягом 30 хвилин та додатково перемішували протягом 1 години при 90 °С. Протягом 45 хвилин при 40 °С додавали концентровану водну НСl (60 г, 37 ваг.%, 0,20 моль), і дану суміш перемішували протягом ночі та концентрували під зниженим тиском для вилучення більшої частини води. Потім дану суміш фільтрували для вилучення солі, котру промивали двома 80 мл порціями 9% водної НСl. Аналіз даного фільтрату показав, що він містить приблизно 16,1 г 3-амінопіридину 3 (вихід приблизно 86%). До розчину неочищеного 3амінопіридину 3 додавали безводну НСl (приблизно 80 г, 2,2 моля) при 0 °С. Протягом 2 годин при 0-5 °С додавали пероксид водню (17,6 г, 46% розчин, 0,24 моль), і дану суміш перемішували при 1520 °С ще протягом 3 годин. До даної суміші послідовно додавали водний розчин бісульфіту натрію (12 мл, 30%), воду (200 мл), толуол (50 мл) та водний NaOH (82 г, 1,03 моль, 50%) при температурі приблизно 0-20 °С. Шари розділяли. Водний шар промивали 10-ма 50 мл порціями толуолу для вилучення надлишково хлорованих побічних продук 21 86604 тів і потім підлуговували до рН 10 за допомогою 20 г 50% водного NaOH. Даний підлугований водний розчин екстрагували чотирма 100 мл порціями толуолу, і поєднані толуолові екстракти промивали двома 40 мл порціями 18 ваг.% водної НСl. Аналіз результуючих водних НСl екстрактів, проведений за методом високоефективної рідинної хроматографії, показав, що вони містять приблизно 15,3 г (0,119 моль) 3-аміно-2-хлоропіридину 2 (приблизно 69,7 % вихід відносно 3-амінопіридину 3, 60% відносно нікотинаміду 4). Зазначені екстракти охолоджували до приблизно -5 °С, і протягом 30 хвилин при температурі у межах -5 - 0 °С додавали розчин 8,3 г нітриту натрію (0,12 моль) у 16,6 мл Комп’ютерна верстка І.Скворцова 22 води. Результуючу суміш додавали протягом 1 години до суміші, що містила дигідрат хлориду міді (II) (10,14 г, 0,0595 моль), концентровану водну НСl (24,3 мл) та 1-хлоробутан (72 мл) при температурі приблизно 60 °С під атмосферою азоту Після додаткової витримки протягом 30 хвилин при 60 °С дану суміш охолоджували до кімнатної температури та розводили 120 мл води. Шари відокремлювали. Водний шар екстрагували двома 70 мл порціями 1-хлоробутану. Поєднані екстракти, як було знайдено, містили приблизно 14,7 г 2,3дихлоропіридину 1 (83,6% вихід відносно 3-аміно2-хлоропіридину 2 або 50% вихід відносно нікотинаміду 4). Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 2,3-dichloropyridine
Автори англійськоюShapiro Rafael
Назва патенту російськоюСпособ получения 2,3-дихлоропиридина
Автори російськоюШапиро Рафаэль
МПК / Мітки
МПК: C07D 213/82, C07D 213/73, C07D 213/61
Мітки: одержання, спосіб, 2,3-дихлоропіридину
Код посилання
<a href="https://ua.patents.su/11-86604-sposib-oderzhannya-23-dikhloropiridinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 2,3-дихлоропіридину</a>
Попередній патент: Сільськогосподарська машина для валкування і підбирання скошеної маси, що знаходиться на землі
Наступний патент: Антитіло, що містить варіант вихідної людської fс-ділянки
Випадковий патент: Спосіб закритого блокуючого металополімерного інтрамедулярного остеосинтезу












