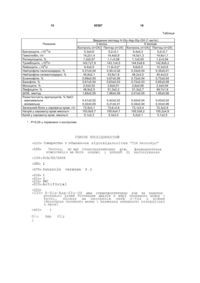
Пептид, що має стреспротекторну дію, фармацевтична композиція на його основі і спосіб її застосування
Номер патенту: 92387
Опубліковано: 25.10.2010
Автори: Грігорьєв Євгєній Іосіфовіч, Малінін Владімір Вікторовіч, Рижак Ґаліна Анатольєвна, Хавінсон Владімір Хацкєлєвіч
Формула / Реферат
1. Застосування пептиду глутаміл-аспартил-гліцин загальної формули: H-Glu-Asp-Gly-OH послідовності 1 [SEQ ID NO:1] як агента, що має стреспротекторну дію.
2. Фармацевтична композиція, що має стреспротекторну дію, яка відрізняється тим, що як активне начало містить ефективну кількість пептиду глутаміл-аспартил-гліцин загальної формули: H-Glu-Asp-Gly-OH послідовності 1 [SEQ ID NO:1] і фармацевтичнo прийнятний носій.
3. Фармацевтична композиція за п. 2, яка відрізняється тим, що вона знаходиться у формі, що підходить для парентерального або інтраназального введення.
4. Спосіб профілактики і/або лікування функціональних або стрес-індукованих порушень, що виникають при екстремальних впливах, який полягає у введенні пацієнту фармацевтичної композиції, що містить як активне начало ефективну кількість пептиду глутаміл-аспартил-гліцин загальної формули: H-Glu-Asp-Gly-OH послідовності 1 [SEQ ID NO:1] у дозі 0,01-100 мкг/кг маси тіла, принаймні один раз на день протягом періоду, необхідного для досягнення терапевтичного ефекту.
5. Спосіб за п. 4, який відрізняється тим, що введення здійснюють внутрішньом'язово або інтраназально крапельнo.
Текст
1. Застосування пептиду глутаміл-аспартилгліцин загальної формули: H-Glu-Asp-Gly-OH послідовності 1 [SEQ ID NO:1] як агента, що має стреспротекторну дію. C2 2 (19) 1 3 92387 4 Зазначені вище причини обумовлюють необПептид глутаміл-аспартил-гліцин загальної хідність розробки нових лікарських засобів. формули: H-Glu-Asp-Gly-OH одержують класичним З рівня техніки відомий пептид глутамілметодом пептидного синтезу в розчині. аспартил-гліцин загальної формули: H-Glu-AspВивчення біологічної активності проводили на Gly-OH (Реєстраційний номер RN-75007-24-8 згідінтактних тваринах, в експериментальних моделях но STN int. BD Registry Chemical abstract). стресу, з використанням сироватки крові здорових При експериментальному вивченні пептиду людей і на випробувачах - добровольцях, що підглутаміл-аспартил-гліцин загальної формули: Hдавалися екстремальному впливу зниженого парGlu-Asp-Gly-OH була виявлено його раніше невіціального тиску кисню. дома властивість, що проявляється в наданні Поняття «фармацевтична композиція», має на стреспротекторної дії. увазі різні лікарські форми, що містять новий пепДаним винаходом поставлена і вирішена затид, що можуть знайти лікувальне застосування в дача одержання засобу пептидної природи, що медицині як засіб, що має стреспротекторну дію. має стреспротекторну дію, фармацевтичної комДля одержання фармацевтичних композицій, що позиції на його основі і способу її застосування. відповідають винаходу, ефективну кількість пептиТехнічний результат винаходу полягає в проду H-Glu-Asp-Gly-OH як активного начала змішуяві пептидом глутаміл-аспартил-гліцин формули: ють з фармацевтично прийнятним носієм згідно з H-Glu-Asp-Gly-OH стреспротекторної дії, застосуприйнятими у фармацевтиці способами компаунвання його для виготовлення фармацевтичної дування. композиції, що містить цей пептид як активне наПоняття "ефективна кількість", має на увазі чало, використання якого дозволяє регулювати використання такої кількості активної речовини, рівень біогенних амінів у корі головного мозку і що відповідно до її кількісних показників активності крові, впливаючи на експресію гена c-fos у різних і токсичності, а також на підставі знань фахівця структурах головного мозку і знижуючи активність повинна бути ефективною у даній лікарській форенкефаліназ у крові, здійснюючи, таким чином, мі. стреспротекторну дію. Носій може мати різні форми, що залежать від Можливість об'єктивного прояву технічного релікарської форми препарату, бажаної для введензультату при використанні винаходу підтверджена ня в організм. достовірними даними, наведеними в прикладах, Для парентерального введення носій звичайно що містять відомості експериментального хараквключає фізіологічний розчин або стерильну воду, теру, отримані в процесі проведення досліджень хоча можуть бути включені інші інгредієнти, що по методиках, прийнятих у даній галузі, згідно з сприяють стабільності, або для збереження стеякими експериментальний стрес індукували у тварильності. рин. Для інтраназального введення носій звичайно Даний винахід стосується пептиду глутамілвключає фізіологічний розчин або стерильну воду, аспартил-гліцин загальної формули: H-Glu-Aspхоча можуть бути включені інші інгредієнти. Gly-OH послідовності 1 [SEQ ID NO:1], що має Сутність винаходу пояснюється фігурами і стреспротекторну дію. таблицею. Пропонується застосування пептиду глутамілНа Фіг. 1 показано (у % стосовно контролю) аспартил-гліцин загальної формули: H-Glu-Aspвплив пептиду H-Glu-Asp-Gly-ОН на рівень біогенGly-OH послідовності 1 [SEQ ID NO:1] для пригоних амінів у корі головного мозку щурів (1 - конттування фармацевтичної композиції, що має стрероль, 2 - пептид H-Glu-Asp-Gly-OH). спротекторний ефект. На Фіг. 2 (у % стосовно контролю) показаний Наступний аспект даного винаходу стосується вплив пептиду H-Glu-Asp-Gly-ОН на рівень біогенфармацевтичної композиції, що має стреспротекних амінів у сироватці крові щурів (1 - контроль, 2 торну дію, що характеризується тим, що вона міспептид Н-Glu-Asp-Gly-OH). тить як активне начало ефективну кількість пептиНа Фіг. 3 представлене імуногістохімічне виду глутаміл-аспартил-гліцин загальної формули: значення вмісту білка c-Fos у клітинах епіфіза пісH-Glu-Asp-Gly-OH [SEQ ID NO:1], а також фармаля осмотичного стресу (а - без пептиду H-Glu-Aspцевтично прийнятний носій. Gly-BIH; b - після інтраназального введення пепПри цьому фармацевтична композиція знахотиду H-Glu-Asp-Gly-OH (кластери клітин, що виродиться у формі, що підходить для парентеральнобляють білок c-Fos). го або інтраназального введення. На Фіг. 4 представлена паренхіма епіфіза пісНаступний аспект даного винаходу стосується ля осмотичного стресу (а - без пептиду H-Glu-Aspспособу профілактики і лікування функціональних Gly-OH; b - після інтраназального введення пептиабо стрес-індукованих порушень, що виникають ду H-Glu-Asp-Gly-OH). при екстремальних впливах, що полягає у введенНа Фіг. 5 показаний вплив пептиду H-Glu-Aspні пацієнту фармацевтичної композиції, що містить Gly-OH на енкефаліназну активність сироватки як активне начало ефективну кількість пептиду крові людей. глутаміл-аспартил-гліцин загальної формули: HУ Таблиці представлений вплив пептиду HGlu-Asp-Gly-OH послідовності 1 [SEQ ID NO:1] у Glu-Asp-Gly-OH на морфологічні і біохімічні показдозі 0,01-100 мкг/кг маси тіла, принаймні, один раз ники периферичної крові морських свинок при вина день протягом періоду, необхідного для досягвченні токсичності. нення терапевтичного ефекту. При цьому введенВинахід ілюструється прикладом синтезу пепня здійснюють парентерально або інтраназально. тиду глутаміл-аспартил-гліцин загальної формули: H-Glu-Asp-Gly-OH (приклад 1), прикладами, що 5 92387 6 підтверджують прояв біологічної активності пептиN-трет.бутилоксикарбоніл-( ду (приклади 2, 3, 4, 5), прикладом вивчення токбензил)глутамінову кислоту BOC-Glu(OBzl)-OH сичності (приклад 6), а також прикладом результа(33,7 г, 0,1 моль) розчиняли в 50 мл Ν,Ν'тів клінічного застосування пептиду, що диметилформаміду, охолоджували до температудемонструє його фармакологічні властивості і підри -10°С, додавали при перемішуванні охолоджені тверджує можливість досягнення профілактичного (4-6°С) розчини Ν,Ν'-дициклогексилкарбодііміду і/або лікувального ефекту (приклад 7). (23,0 г, 0,11 моль) у 30 мл Ν,Ν'-диметилформаміду Приклад 1. Синтез пептиду H-Glu-Asp-Gly-OH і Ν-гідроксисукциніміду (13,0 г, 0,11 моль) у 20 мл 1. Назва сполуки: глутаміл-аспартил-гліцин. Ν,Ν'-диметилформаміді. Реакційну суміш перемі2. Структурна формула: шували протягом 12 год. при охолодженні льодом і далі протягом 1 доби при кімнатній температурі. Ν,Ν'-дициклогексилсечовину, що випала, відфільтровували й отриманий розчин активованого ефіру використовували без виділення на наступній стадії. 2) BOC-Glu(OBzl)-Asp(OBzl)-OH, Nтрет.бутилоксикарбоніл-( -бензил)глутаміл-((3бензил)аспартат(ІІ). ( -Бензил) аспарагінову кислоту H-Asp(OBzl)OH (28,0 г, 0,12 моль) і 36 мл (0,12 моль) триетиламіну суспендували в 50 мл Ν,Ν'3. Брутто-формула без протиіона: С11Н17N3О8. диметилформаміду і перемішували протягом 1 4. Молекулярна вага без протиіона: 319,27. год. Потім додали порціями розчин активованого 5. Протиіон: ацетат. ефіру BOC-Glu(OBzl)-OSu (І), отриманий на попе6. Зовнішній вигляд: білий аморфний порошок редній стадії. Реакційну суміш перемішували при без запаху. кімнатній температурі протягом 2 діб. Потім підки7. Спосіб синтезу : пептид отриманий класичсляли 0,5 н сірчаною кислотою до рН 2-3 і екстраним методом синтезу в розчині за схемою: гували етилацетатом 4 50 мл. Витяжки поєднували і послідовно промивали 0,5 н H2SO4 3 50 мл, водою 2 50 мл, 5% розчином МаНСО3 2 50 мл, водою 2 50 мл, насиченим розчином NaCl 2 50 мл. Органічний шар сушили над Na2SO4, упарювали розчинник у вакуумі, залишок кристалізували під гексаном. Отримано 50 г продукту (92%). Rf=0,34 (бензол-ацетон 2:1). 3) BOC-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III), бензиловий ефір N-трет.бутилоксикарбоніл-( бензил)глутаміл-( -бензил)аспартил-гліцину (III). 2,7 г (5 ммоль) дипептиду і 0,95 г (7 ммоль) оксибензотриазолу розчиняли в тетрагідрофурані (10 мл) і охолоджували до температури -10°С. 1,44 г (7 ммоль) дициклогексилкарбодііміду розчиняли в 5 мл тетрагідрофурану і охолоджували до тієї ж температури. 3,4 г (10 ммоль) тозилату бензилового ефіру гліцину розчиняли в 10 мл тетрагідрофурану, додавали 1,4 мл (10 ммоль) триетиламіну і охолоджували до тієї ж температури. При охолоВОС - трет.бутилоксикарбонільна група, дженні на крижаній бані й інтенсивному перемішуOSu - N-оксисукцинімідний ефір, ванні поєднували розчини дипептиду з оксибензоDCC - Ν,Ν'-дициклогексилкарбодіімід, триазолом і карбодііміду, через 10 хв. додавали OBzl - бензиловий ефір, розчин тозилату бензилового ефіру гліцину. РеакTFA - трифтороцтова кислота, ційну суміш перемішували протягом 3 год. при HOBt - N-оксибензотриазол. охолодженні льодом і протягом 1 доби при кімнат6. Характеристики готового препарату: ній температурі. Дициклогексилсечовину, що ви- Вміст основної речовини: 97,93% (по ВЕРХ, пала, відфільтровували, фільтрат упарювали у 220 нм), вакуумі, залишок розчиняли в етилацетаті (100 - ТШХ - індивідуальний, Rf=0,45 (ацетонітрилмл). Розчин промивали послідовно 0,5 н сірчаною вода 1:2), кислотою, водою, 5% розчином бікарбонату на- Вміст вологи: 6%, трію, водою, сушили над безводним сульфатом - рН 0,01% розчину: 4,9, натрію. Етилацетат упарювали у вакуумі, кристалі22 - Питоме оптичне обертання: [ ]D : -31° (с=1, зація залишку в системі етилацетат/гексан. ПерекН2О), "Polamat A", Carl Zeiss Jena. ристалізація з ізопропанолу. Отримано після суПриклад синтезу: шіння у вакуумі 2,74 г продукту (85%). Rf=0,78 1) BOC-Glu(OBzI)-OSu, N-оксисукцинімідний (бензол-ацетон 1:1). ефір Ν-трет.бутилоксикарбоніл-( бензил)глутамінової кислоти (І). 7 92387 8 4) H-Glu-Asp-Gly-OH (IV), глутаміл-аспартилВстановлено, що введення пептиду тваринам гліцин. сприяло значним зрушенням у рівні біогенних аміЗахищений трипептид BOC-Glu(OBzl)нів у корі головного мозку і сироватці крові. Asp(OBzl)-Gly-OBzl (III) (2,7 г) розчиняли в суміші Так, після введення пептиду H-Glu-Asp-Gly-OH метиловий спирт-вода (4:1) (50 мл) і гідрували над щурам у корі головного мозку спостерігалося доскаталізатором Pd/C (5%) протягом 4 год. Каталізатовірне збільшення вмісту норадреналіну, дофатор відфільтровували, розчинник упарювали у міну і серотоніну (Фіг. 1). вакуумі, залишок сушили у вакуумі над KОН і Р2О5. При цьому в сироватці крові спостерігалося Далі продукт розчиняли в 15 мл суміші хлористий зниження вмісту дофаміну, серотоніну і гістаміну метилен-трифтороцтова кислота (5:1) і витриму(Фіг. 2). вали при кімнатній температурі протягом 2 год. Таким чином, у результаті проведеного досліПовноту проходження реакції деблокування контдження встановлено, що пептид H-Glu-Asp-Gly-OH ролювали по ТШХ у системі ацетонітрил-вода впливає на вміст біогенних амінів у корі головного (1:3). Розчинник упарювали у вакуумі, залишок мозку і сироватці крові, що свідчить про вплив цьосушили у вакуумі над KОН. го пептиду на центральні і периферичні механізми Для очищення 300 мг препарату розчиняли в 4 регуляції стресу. мл 0,01% трифтороцтової кислоти і піддавали виПриклад 3. Вплив пептиду H-Glu-Asp-Gly-OH сокоефективній рідинній хроматографії на колонці на експресію гена c-fos у нейронах паравентрикулярного ядра гіпоталамуса щурів при емоційному зі зверненою фазою 50 250 мм Diasorb-130-C16T, стресі 7mkm. Хроматограф Beckman System Gold, 126 Емоційний стрес підсилює експресію ранніх Solvent Module, 168 Diode Array Detector Module. генів у різних структурах мозку. Відомим маркером Умови хроматографування А: 0,1% TFA; B: активації нейрональних клітин є продукт гена неMeCN/0,1% TFA, градієнт B 0 50% за 100 хв. гайної відповіді - c-fos-білок, що виконує функцію Об'єм проби 5 мл, детекція при 215 нм, сканування посередника між зміною характеру транскрипції 190-600 нм, швидкість потоку 10 мл/хв. Відбирали під дією стимулу і реалізацією інформаційного фракцію основного піка. Розчинник упарювали у сигналу в довгострокові фенотипові зміни. Білки вакуумі при температурі не вище 40°С, розпарюсімейства Fos активуються в нейронах у різний час вання багаторазово (5 разів) повторювали з 10 мл після надходження стимулу. Так, експресія c-fos 10% розчину оцтової кислоти. мРНК починається вже через кілька хвилин і досяОстаточно залишок розчиняли в 20 мл деіонігає максимуму через 30-60 хв. після надходження зованої води і ліофілізували. Отримано 150 мг стимулу. Максимальний синтез c-Fos-білка споочищеного препарату у вигляді аморфного білого стерігається між 1-шою і 3-ою годиною, а через 4-6 порошку без запаху. год. після пред'явлення стимулу відбувається зни5) Аналіз готового препарату. ження його синтезу в нейронах. Експресія гена c- Вміст основної речовини визначали методом fos у головному мозку тварин, стійких і схильних ВЕРХ на колонці Phenomenex С 18 LUNA 4,6 150 до емоційного стресу, різна. Найбільш інтенсивна мм. A: 0,1% TFA, B: MeCN; grad.B 0-100% in 10 експресія гена c-fos виявлена в структурах мозку min. Швидкість потоку 1 мл/хв. Детекція при 220 (кора, мигдалина, гіпоталамус і стовбур мозку) у нм, сканування 190-600 нм, проба 20 1. Вміст оссхильних до емоційного стресу щурів. В особин, новної речовини 97,93%. стійких до емоційного стресу, в аналогічних умо- ТШХ: індивідуальний, Rf=0,45 (ацетонітрилвах експерименту експресія гена c-fos визначалавода 1:2, пластинки ПТШХ-П-В-УФ Sorbfil, силікася тільки в інфралімбічній корі і нюхових ядрах. гель СТХ-1ВЕ 8-12 мкм, проявлення В експерименті вивчали вплив пептиду H-Gluхлор/бензидин). Asp-Gly-OH на експресію гена c-fos у паравентри- Вміст вологи: 6% (гравіметрично по втраті кулярному ядрі гіпоталамуса (PVH) стійких і схимаси при сушінні 20 мг при 100°С). льних до емоційного стресу тварин, а також у щу- рН 0,01% розчину: 4,9 (потенціометрично). 22 рів, підданих емоційному стресу. - Питоме оптичне обертання: [ ]D : -31° (с=1, Експерименти були проведені на 28 щурах ліН2О), "Polamat A", Carl Zeiss Jena. нії Вістар. Приклад 2. Вплив пептиду H-Glu-Asp-Gly-OH Поведінку тварин попередньо (для прогнозуна рівень біогенних амінів у корі головного мозку і вання ступеня їхньої стійкості до емоційного стресироватці крові в щурів су) оцінювали в тесті "відкрите поле". ЕфективДослідження проведене на 27 білих щурах ність застосування пептиду H-Glu-Asp-Gly-OH обох статей масою 300-320 г. вивчали в стійких і схильних до емоційного стресу Пептид H-Glu-Asp-Gly-OH тваринам піддослідособин. Пептид H-Glu-Asp-Gly-OH вводили внутних груп вводили внутрішньоочеревинно в дозі 2,5 рішньоочеревинно в дозах 0,1 і 0,01 мкг на щура в мкг/кг маси тіла в 0,5 мл стерильного фізіологічно0,5 мл стерильного фізіологічного 0,9% розчину го 0,9% розчину NaCl щодня протягом 5 діб. NaCl через 7-10 днів після першого тесту. Через 1 Щурам контрольної групи за аналогічною схегод. після ін'єкції пептиду тварин піддавали 60мою вводили стерильний фізіологічний розчин у хвилинному емоційному стресу, що створювали, тому ж об'ємі. обмежуючи їхню рухливість. Після закінчення введення препаратів тварин Для ідентифікації клітин, що містять білок Fos декапітували, потім у корі головного мозку і сиропродукт ранньої експресії гена c-fos - провели імуватці крові визначали вміст норадреналіну, дофаногістохімічне дослідження зрізів мозку з автомаміну, 5-оксііндолоцтової кислоти (5-ОІОК), серотоніну і гістаміну. 9 92387 10 тизованим підрахунком Fos-позитивних клітин. ктора. Хронічний стрес пригнічує активність гена зОсобливості індукції гена c-fos вивчали в PVH. fos у PVH через підвищення в плазмі крові рівня Число Fos-позитивних клітин у PVH у щурів глюкокортикоїдів. прогностично стійких до емоційного стресу виявиНевелике, але достовірне підвищення вмісту лося вірогідно вищим, ніж у тварин, схильних до білка c-Fos у пінеалоцитах при стресі спостерігаемоційного стресу. Це відзначалося в щурів обох лося тільки після інтраназального введення пепконтрольних груп (не підданих стресу і після емотиду H-Glu-Asp-Gly-OH (Фіг. 3). ційного стресу). Даний ефект пептиду H-Glu-Asp-Gly-OH споВведення пептиду H-Glu-Asp-Gly-OH у дозі стерігався тільки при стресі. Це свідчить про те, 0,01 мкг приводило до збільшення кількості Fosщо пептид H-Glu-Asp-Gly-OH бере участь у пептипозитивних нервових клітин у щурів, стійких до дній саморегуляції діяльності епіфіза при екстрестресу, що не піддавалися стресорному впливу і мальних станах організму. на фоні стресу. Навпроти, пептид H-Glu-Asp-GlyБуло виявлено, що білок c-Fos нерівномірно OH у дозі 0,1 мкг сприяв зниженню числа Fosміститься в різних пінеалоцитах. При стресі виявпозитивних нервових клітин у PVH як у стійких, так ляються кластери (по 5-10 клітин), що містять cі в схильних до стресу тварин. На фоні стресу в Fos у цитоплазмі. Можливо, ці кластери пінеалостійких щурів пептид H-Glu-Asp-Gly-OH у дозі 0,1 цитів є групами клітин, що взаємодіють. мкг збільшував кількість Fos-позитивних нейронів. При оцінці стану паренхіми епіфіза було встаТаким чином, були виявлені дозозалежні стреновлено, розширення капілярів і перикапілярного спротекторні ефекти пептиду Н-Glu-Asp-Gly-OH, простору, що виникає при осмотичному стресі (Фіг. що проявляються в посиленні експресії гена c-fos і 4) частково усувалося інтраназальним введенням спрямовані на активацію нейронів і формування пептиду H-Glu-Asp-Gly-OH. адаптаційних реакцій. Таким чином, пептид H-Glu-Asp-Gly-OH вплиПриклад 4. Вплив пептиду H-Glu-Asp-Gly-OH ває на пінеальну залозу при впливі на організм на вміст білка c-Fos в епіфізі щурів при осмотичекстремальних факторів. Пептид H-Glu-Asp-Glyному стресі OH перешкоджає патологічним структурним зміЕпіфіз поряд з гіпоталамо-гіпофізарним комнам паренхіми епіфіза при осмотичному стресі, і плексом залучається у формування множинних його дія на епіфіз опосередкована активацією сисадаптаційних відповідей організму на стресорний теми певних генів. вплив. При стресі підсилюється продукція епіфізом Приклад 5. Вплив пептиду H-Glu-Asp-Gly-OH мелатоніну і речовин пептидної природи, що мана активність енкефаліназ у сироватці крові людей ють здатність послабляти негативний вплив на Метою даного дослідження було визначення організм окисного, осмотичного, психічного й інших опіоїдної активності пептиду Н-Glu-Asp-Gly-OH. видів стресу. Опіоїдна активність може бути обумовлена як взаЕпіфіз належить до нейрогемальних органів, ємодією пептидів з опіоїдними рецепторами різнопозбавлених гематоенцефалічного бар'єра, тому го типу, так і інгібуванням енкефаліназ, що привовін дуже чутливий до високомолекулярних біологідить до відповідного збільшення концентрації чно активних речовин, що циркулюють з мозковим нативних енкефалінів. кровотоком, особливо до пептидів. Унікальне поЗдатність пептиду H-Glu-Asp-Gly-OH впливати ложення нюхової системи, хімічний зв'язок однона активність ферментів деградації ендогенних часно з навколишнім середовищем і з ЦНС дозвоопіоїдних пептидів - енкефалінів оцінювали в кінеляє речовинам неінвазивно проникати в мозковий тичних дослідженнях з розщеплення малих концекровотік і в нейрогемальні органи. Існує постійна нтрацій (0,15 мкМ) [3Н]Лей-енкефаліну ферментадифузія ліквору через підпавутинний простір узми сироватки крові людини. Як препарати довж факторних нейронів до носової підслизової і порівняння використовували загальноприйняті носової лімфатичної системи. інгібітори енкефаліназ N-карбоксиметил-РhЕ-Lеu В експерименті вивчали вплив пептиду H-Glu(N-CMPL) і бацитрацин. Визначали сумарну енкеAsp-Gly-OH при інтраназальному застосуванні на фаліназну активність сироватки крові, отриманої вміст білка c-Fos в епіфізі щурів при стресі. Для від 5 здорових донорів, in vitro. Результати оцінюімуногістохімічного визначення вмісту білка c-Fos вали після проведення 4 досліджень. використовували інтактних і підданих 48На Фіг. 5 показаний вплив пептиду H-Glu-Aspгодинному осмотичному стресу щурів, яким інтраGly-OH на енкефаліназну активність сироватки назально вводили пептид H-Glu-Asp-Gly-OH у дозі крові людей. 0,5 мкг на тварину в 0,1 мл стерильного фізіологіУ результаті дослідження встановлено, що печного 0,9% розчину NaCl (остання інфузія провоптид H-Glu-Asp-Gly-OH, доданий до культуральнодилася за 2 год. до взяття матеріалу). У цей же го середовища в кінцевій концентрації 10 мкг/мл, час проводили світлооптичне дослідження стану інгібував активність енкефаліназ сироватки крові паренхіми епіфіза у тварин усіх груп. (Фіг. 5). Причому ступінь інгібування був порівнянБілок c-Fos є одним із тригерів, що запускають ний з таким для N-CMPL (10 мкг/мл) і бацитрацину синтетичні процеси в епіфізі при дії екстремальних (50 мкг/мл). факторів, зокрема, при стресі. У наших дослідах Відомо, що час ферментативної деградації енмайже повна відсутність білка c-Fos в епіфізі щурів кефалінів у крові вимірюється хвилинами, тому при осмотичному стресі, ймовірно, була пов'язана саме ці ферменти найбільшою мірою визначають з хронічним характером цього стресу, оскільки периферичні біологічні ефекти ендогенних опіоїднайбільший вміст продуктів гена c-fos спостеріганих пептидів. Застосування пептиду H-Glu-Aspється через 1-2 год. після впливу стресорного фаGly-OH, що інгібує активність енкефаліназ сирова 11 92387 12 тки крові спрямоване на збереження регуляторних що свідчить про велику терапевтичну широту превластивостей ендогенних опіоїдних пептидів, що є парату. підставою використання його для корекції стресВивчення підгострої і хронічної токсичності пеіндукованих порушень. птиду свідчить про відсутність побічних ефектів Приклад 6. Вивчення токсичності пептиду Hпри тривалому застосуванні препарату в дозах, що Glu-Asp-Gly-OH перевищують терапевтичну в 100-1000 разів. При Загальнотоксичну дію пептиду H-Glu-Asp-Glyдослідженні впливу пептиду на морфологічний OH досліджували відповідно до вимог «Посібника склад крові морських свинок встановлено збільз експериментального (доклінічного) вивчення шення кількості лейкоцитів через 3 місяці після нових фармакологічних речовин» (2000): гострої початку введення препарату, що нормалізувалося токсичності при однократному введенні препарату, до 6-го місяця спостереження (Таблиця). Інші поа також підгострої і хронічної токсичності при триказники морфологічної сполуки крові тварин праквалому введенні пептиду. тично не змінювалися. Не відзначено достовірного Дослідження з вивчення гострої токсичності впливу препарату на ШОЕ, резистентність еритропроведене на 66 білих безпородних мишах-самцях цитів і біохімічні показники сироватки крові. масою 20-22 г. Тварини були рандомізовано розПри оцінці загального стану тварин, морфолоділені на 6 рівних груп. Препарат вводили тваригічних і біохімічних показників периферичної крові, нам однократно внутрішньом'язово в дозах 1 мг/кг, морфологічного стану внутрішніх органів, стану 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг у 0,25 мл стерильносерцево-судинної і дихальної систем, функції печіго 0,9% розчину NaCl. Тваринам контрольної групи нки і нирок патологічні зміни в організмі не виявв тому ж об'ємі вводили 0,9% розчин NaCl. лені. Дослідження з вивчення підгострої токсичності Відсутність загальнотоксичної дії дозволяє репроведено на 64 білих безпородних щурах-самцях комендувати фармацевтичну композицію, що місмасою 180-220 г. Щодня однократно тваринам тить як активне начало пептид H-Glu-Asp-Gly-OH, піддослідних груп вводили препарат внутрішньодля проведення клінічних досліджень. м'язово протягом 90 днів у дозах 1 мкг/кг, 0,1 мг/кг, Приклад 7. Вплив пептиду H-Glu-Asp-Gly-OH 1 мг/кг у 0,5 мл стерильного 0,9% розчину NaCl. на функціональний стан людини при впливі зниТваринам контрольної групи вводили в тому ж женого парціального тиску кисню обсязі стерильний 0,9% розчин NaCl. До введення Для оцінки впливу пептиду H-Glu-Asp-Gly-OH препарату, на 30, 60 і 90 добу після початку ввена функціональний стан і працездатність людини в дення препарату у тварин досліджували морфолоекстремальних умовах впливу зниженого парціагічний склад і властивості периферичної крові. При льного тиску кисню було обстежено 80 практично завершенні експерименту досліджували біохімічні і здорових чоловіків у віці 20-22 років. Випробувачі коагулологічні показники крові. були розділені на 3 групи: у контрольну групу Дослідження з вивчення хронічної токсичності ввійшли 20 чоловік, у І і II основні - по 30 чоловік у проводили протягом 6 місяців, виходячи з тривакожній. У перший день дослідження проводилося лості клінічного призначення препарату, що рекофонове обстеження, що включало дослідження мендується, на 92 морських свинках-самцях мадихальної, серцево-судинної і центральної нервосою 310-350 г. Тварини піддослідних груп вої систем. одержували щодня однократно внутрішньом'язово Після закінчення фонового обстеження випропептид протягом 6 міс. у дозах 1 мкг/кг, 0,1 мг/кг, 1 бувачі І основної групи починали приймати фармг/кг у 0,5 мл стерильного 0,9% розчину NaCl. У мацевтичну композицію, що містить як активне контрольній групі тваринам вводили за аналогічначало пептид H-Glu-Asp-Gly-OH, інтраназально ною схемою стерильний 0,9% розчин NaCl у тому крапельно, у дозі 5,0 мг в 1 мл фізіологічного розж обсязі. У тварин у периферичній крові загальночину (І підгрупа), у дозі 100,0 мкг (II підгрупа) і в прийнятими методами визначали: кількість еритдозі 1,0 мкг у 1,0 мл фізіологічного розчину (III підроцитів, гемоглобіну, ретикулоцитів, тромбоцитів, група) 3 рази на день, протягом 2-х днів. Таким лейкоцитів, лейкоцитарну формулу, швидкість чином, випробувачі І основної групи одержували осідання еритроцитів (ШОЕ), резистентність еритпептид H-Glu-Asp-Gly-OH інтраназально в дозі 10 роцитів. Поряд з цим визначали вміст у сироватці мг (І підгрупа), 200 мкг (II підгрупа) і 2 мкг (III підгкрові загального білка по методу Лоурі, калію і рупа) на курс. натрію методом плазменної спектрофотометрії. Випробувачі II основної групи після закінчення Після завершення експерименту проводили патофонового обстеження починали приймати фармаморфологічне дослідження головного і спинного цевтичну композицію, що містить як активне начамозку, спинномозкових гангліїв, щитовидної залоло пептид H-Glu-Asp-Gly-OH, внутрішньом'язово в зи, паращитовидних залоз, наднирниких залоз, дозі 5,0 мг у 1 мл фізіологічного розчину (І підгрусім'яників, гіпофіза, серця, легень, аорти, печінки, па), у дозі 100,0 мкг (II підгрупа) і в дозі 1,0 мкг у нирки, сечового міхура, підшлункової залози, шлу1,0 мл фізіологічного розчину (III підгрупа) щодня нка, тонкої кишки, товстої кишки, тимусу, селезіноднократно протягом 2-х днів. ки, лімфатичних вузлів, кісткового мозку. Випробувачі контрольної групи одержували При вивченні гострої токсичності встановлено, плацебо у вигляді води для ін'єкцій. що однократне введення досліджуваного пептиду На четвертий день експерименту випробувачів тваринам в дозі, що перевищує терапевтичну, ретрьох груп піддавали впливу гіпоксичної гіпоксії комендовану для клінічного застосування, більш методом «підйому» у барокамері СБК-80 на висоту ніж у 5000 разів, не викликає токсичних реакцій, 5000 м з експозицією 60 хв. без додаткового кисневого забезпечення. До початку підйому, у про 13 92387 14 цесі і після закінчення підйому випробувачів обприймали фармацевтичну композицію, що містить стежували за скороченою схемою. На п'ятий день як активне начало пептид H-Glu-Asp-Gly-ОН, - на дослідження проводилося заключне підсумкове 10-20% в залежності від дози і способу введення, обстеження в повному обсязі. Реактивна тривожа в осіб, що приймали плацебо, - на 30-40%. Після ність протягом дослідження у всіх випробувачів закінчення гіпоксичної проби ЧСС у випробувачів, відповідала рівню помірної тривожності (31-45 бащо приймали фармацевтичну композицію, що міслів). Однак у межах цього рівня спостерігалася тить як активне начало пептид Н-Glu-Asp-Gly-OH, різнонаправлена динаміка цього показника у вивідповідала вихідним показникам, а у випробувапробувачів різних груп. Після дводенного застосучів, що приймали плацебо, на 6-7% перевищувала вання фармацевтичної композиції, що містить як їх. Систолічний артеріальний тиск повертався до активне начало пептид H-Glu-Asp-Gly-OH у різних вихідних даних у випробувачів, що приймали фадозуваннях, реактивна тривожність у випробувачів рмацевтичну композицію, що містить як активне знижувалася на 10-13% в залежності від дозуванначало пептид H-Glu-Asp-Gly-OH, до 10-15-ої хвиня і способу введення фармацевтичної композиції лини в різних підгрупах, а у випробувачів, що в порівнянні з випробувачами контрольної групи. приймали плацебо, тільки після закінчення гіпоксії. Наступного дня після впливу гіпоксії реактивна Динаміка зміни діастолічного артеріального тривожність у випробувачів контрольної групи, що тиску у випробувачів була подібною: приріст у пеприймали плацебо, була на 9-10% вище вихідних рші 10 хвилин дії гіпоксії і поступове зниження наданих, а на тлі застосування фармацевтичної комдалі. Фізична працездатність наприкінці досліпозиції, що містить як активне начало пептид Hдження зростала в порівнянні з фоновими даними Glu-Asp-Gly-ОН у різних дозуваннях незалежно від у всіх випробувачів, але в різному ступені. Так, способу введення, відповідала вихідним показниіндекс фізичної працездатності (PWC170) і максикам. Подібну динаміку змін мали показники тесту мальне споживання кисню у випробувачів, що "САН" (самопочуття, активність, настрій). приймали фармацевтичну композицію, що містить В умовах гіпоксичної гіпоксії суб'єктивний стан як активне начало пептид Н-Glu-Asp-Gly-OH, збіпогіршувався у випробувачів трьох груп, але в різльшувалися на 15-20% в залежності від дози і споному ступені. В осіб, що приймали фармацевтичну собу введення, а в групі плацебо - лише на 10композицію, що містить як активне начало пептид 11%. Особливістю дії пептиду H-Glu-Asp-Gly-OH H-Glu-Asp-Gly-OH, суб'єктивний стан залишався на виявилося зниження легеневої вентиляції при довихідному рівні при внутрішньом'язовому способі зованому фізичному навантаженні після впливу введення препарату в різних дозуваннях або погігіпоксії. ршувався на 4-5% у випробувачів при інтраназаЗ представленого матеріалу видно, що функльному способі введення, тоді як в осіб, що прийціональний стан у процесі проведення гіпоксичної мали плацебо, - на 10-15%. Наступного дня після проби у випробувачів, що приймали фармацевтигіпоксії суб'єктивний стан випробувачів, що прийчну композицію, що містить як активне начало пемали фармацевтичну композицію, що містить як птид H-Glu-Asp-Gly-OH у різних дозуваннях, був активне начало пептид Н-Glu-Asp-Gly-OH, був більш адекватним з фізіологічної точки зору, ніж у краще вихідних даних на 15% при внутрішньом'явипробувачів, що приймали плацебо. зовому способі введення або на 10% при інтранаТаким чином, вивчення ефективності застосульному способі введення, тоді як в осіб, що прийвання пептиду H-Glu-Asp-Gly-ОН, у дослідженнях мали плацебо, на 4-5% гірше. Слід зазначити, що за участю випробувачів добровольців, що були найбільш стабільні показники реєструвалися в піддані "підйому" у барокамері на висоту 5000 м осіб, що одержували досліджувану композицію в без додаткового кисневого забезпечення, показадозуванні 5,0 мг як при внутрішньом'язовому, так і ло, що випробувачі, що приймали фармацевтичну при інтраназальному способі введення. композицію, що містить як активне начало пептид Отримані дані свідчать про те, що пептид HH-Glu-Asp-Gly-OH, краще переносили гіпоксичний Glu-Asp-Gly-OH впливає на суб'єктивний стан вивплив, як по об'єктивних ознаках, так і суб'єктивно. пробувачів, знижуючи емоційні і поведінкові проВиявлений дозозалежний ефект дозволяє рекомеяви стресу, зменшуючи тривожність, підвищуючи ндувати застосування досліджуваної фармацевтиактивність, поліпшуючи самопочуття, настрій. чної композиції в дозах від 5 мг до 1 мкг у 1 мл Об'єктивно випробувачі, що приймали фармацевфізіологічного розчину як внутрішньом'язово, так і тичну композицію, що містить як активне начало інтраназально в залежності від ступеня порушень пептид H-Glu-Asp-Gly-OH, краще переносили гіпофункціонального стану випробувачів. ксичну гіпоксію. Гарна здатність переносити гіпокЗміни фізіологічних показників у групі випробусію відзначена у 80-90% випробувачів, що прийвачів, що приймали фармацевтичну композицію, мали пептид H-Glu-Asp-Gly-OH, і тільки у 60% що містить пептид H-Glu-Asp-Gly-OH, були більш випробувачів, що приймали плацебо. згладженими і характеризувалися швидким відноДинаміка частоти серцевих скорочень (ЧСС) вленням до фонових значень, що свідчить про була однаковою в обстежуваних усіх груп. Під дією стреспротекторні властивості пептиду H-Glu-Aspгіпоксії ЧСС вірогідно зростала: у випробувачів, що Gly-OH. 15 92387 16 Таблиця Показник Еритроцити, 1012/л Гемоглобін, г/л Ретикулоцити, % Тромбоцити, 109/л Лейкоцити, 109/л Нейтрофіли паличкоядерні, % Нейтрофіли сегментоядерні, % Еозинофіли, % Базофіли, % Моноцити, % Лімфоцити, % ШОЕ, мм/год. Резистентність еритроцитів, % NaCl - максимальна - мінімальна Загальний білок у сироватці крові, г/л Натрій у сироватці крові ммоль/л Калій у сироватці крові, ммоль/л * - Р
ДивитисяДодаткова інформація
Назва патенту англійськоюPeptide exhibiting stress protective action, pharmaceutical composition based thereon and use thereof
Автори англійськоюKhavinson Vladimir Khatskielievich, Hrihoriev Yevhienii Iosifovich, Malinin Vladimir Viktorovich, Ryzhak Galina Anatolievna
Назва патенту російськоюПептид, который имеет стресспротекторное действие, фармацевтическая композиция на его основе и способ ее применение
Автори російськоюХавинсон Владимир Хацкелевич, Григорьев Евгений Иосифович, Малинин Владимир Викторович, Рыжак Галина Анатольевна
МПК / Мітки
МПК: A61P 25/00, A61K 38/06
Мітки: застосування, спосіб, дію, стреспротекторну, композиція, має, фармацевтична, пептид, основі
Код посилання
<a href="https://ua.patents.su/11-92387-peptid-shho-maeh-stresprotektornu-diyu-farmacevtichna-kompoziciya-na-jjogo-osnovi-i-sposib-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Пептид, що має стреспротекторну дію, фармацевтична композиція на його основі і спосіб її застосування</a>