Спосіб лікування або полегшення симптомів атеросклерозу за допомогою анти-cd3 антитіла
Формула / Реферат
1. Спосіб лікування або полегшення симптомів атеросклерозу, який включає визначення суб'єкта, який страждає на атеросклероз або для якого існує небезпека розвитку такого розладу, і введення цьому суб'єкту анти-СD3 антитіла.
2. Спосіб за п. 1, який відрізняється тим, що згадане анти-СD3 антитіло вводять у кількості, достатній для пригнічення експресії запального цитокіну або підвищення експресії протизапального цитокіну.
3. Спосіб за п. 1, який відрізняється тим, що згадане анти-СD3 антитіло вводять у кількості, достатній для індукування імунологічної супресії.
4. Спосіб за п. 1, який відрізняється тим, що згадане анти-СD3 антитіло вводять у кількості, достатній для індукування імунологічної толерантності.
5. Спосіб за п. 1, який відрізняється тим, що згадане антитіло є моноклональним антитілом.
6. Спосіб за п. 5, який відрізняється тим, що згадане моноклональне антитіло є повністю людським моноклональним антитілом.
7. Спосіб за п. 1, який відрізняється тим, що згаданим суб'єктом є людина або кінь.
8. Спосіб за п. 1, який додатково включає введення згаданому суб'єкту протизапального засобу або імуносупресивного засобу.
9. Спосіб за п. 8, який відрізняється тим, що згаданим протизапальним засобом або імуносупресивним засобом є статин.
10. Спосіб пригнічення утворення атеросклеротичних бляшок на артеріях, який включає введення суб'єкту анти-CD3 антитіла.
11. Спосіб за п. 10, який відрізняється тим, що згадане анти-СD3 антитіло вводять у кількості, достатній для пригнічення експресії запального цитокіну або підвищення експресії протизапального цитокіну у артеріальній тканині.
12. Спосіб за п. 11, який відрізняється тим, що згадане антитіло є моноклональним антитілом.
13. Спосіб за п. 12, який відрізняється тим, що згадане моноклональне антитіло є повністю людським моноклональним антитілом.
Текст
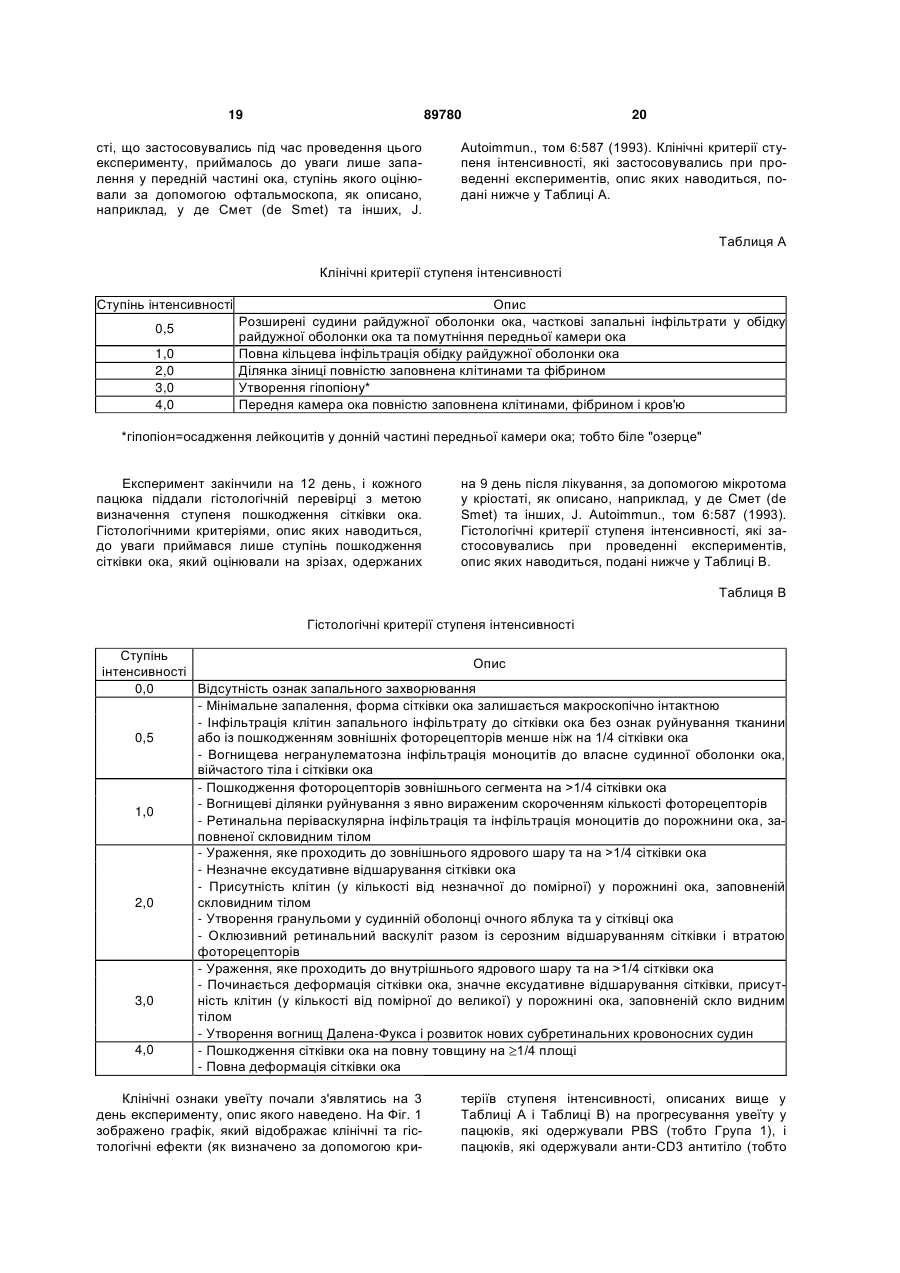
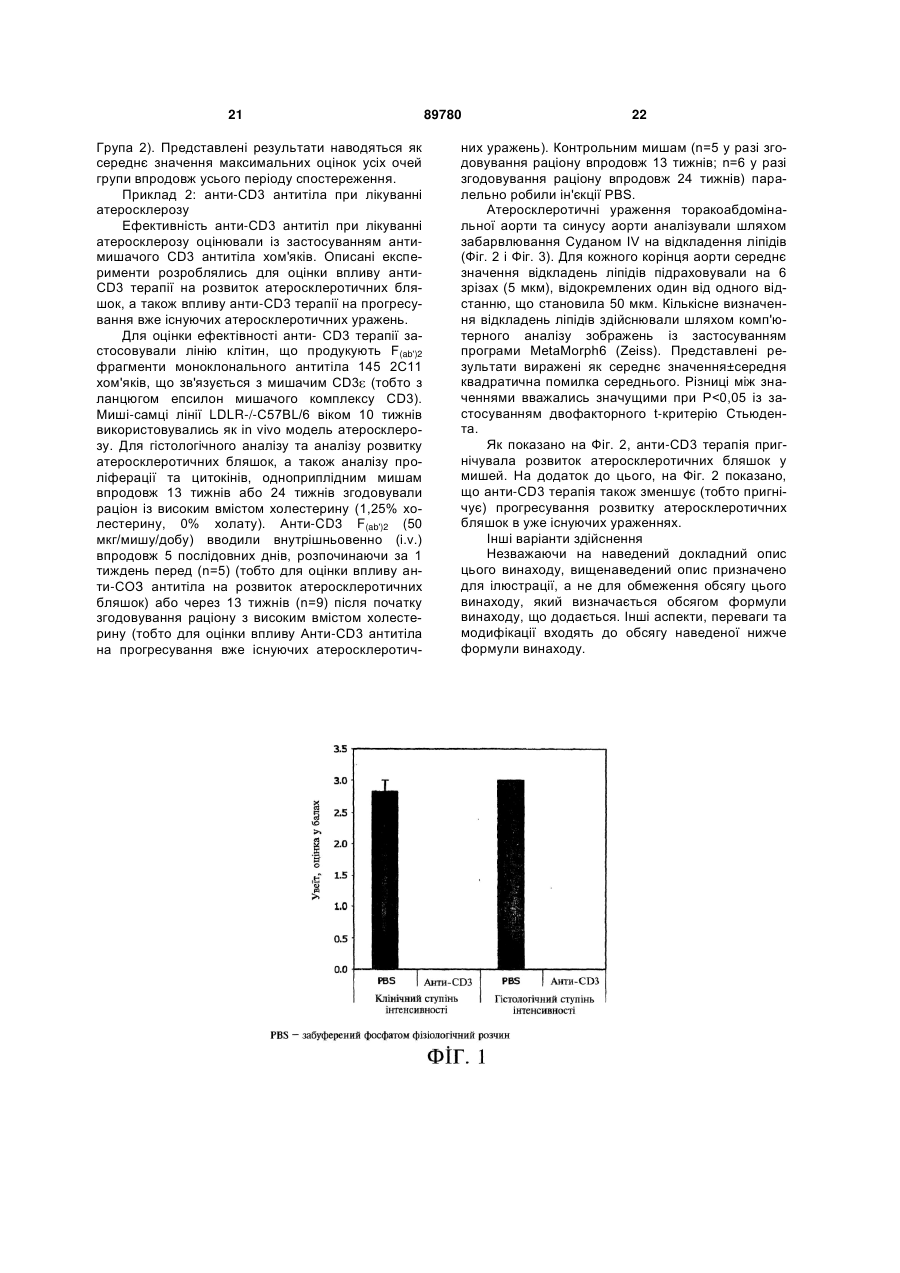
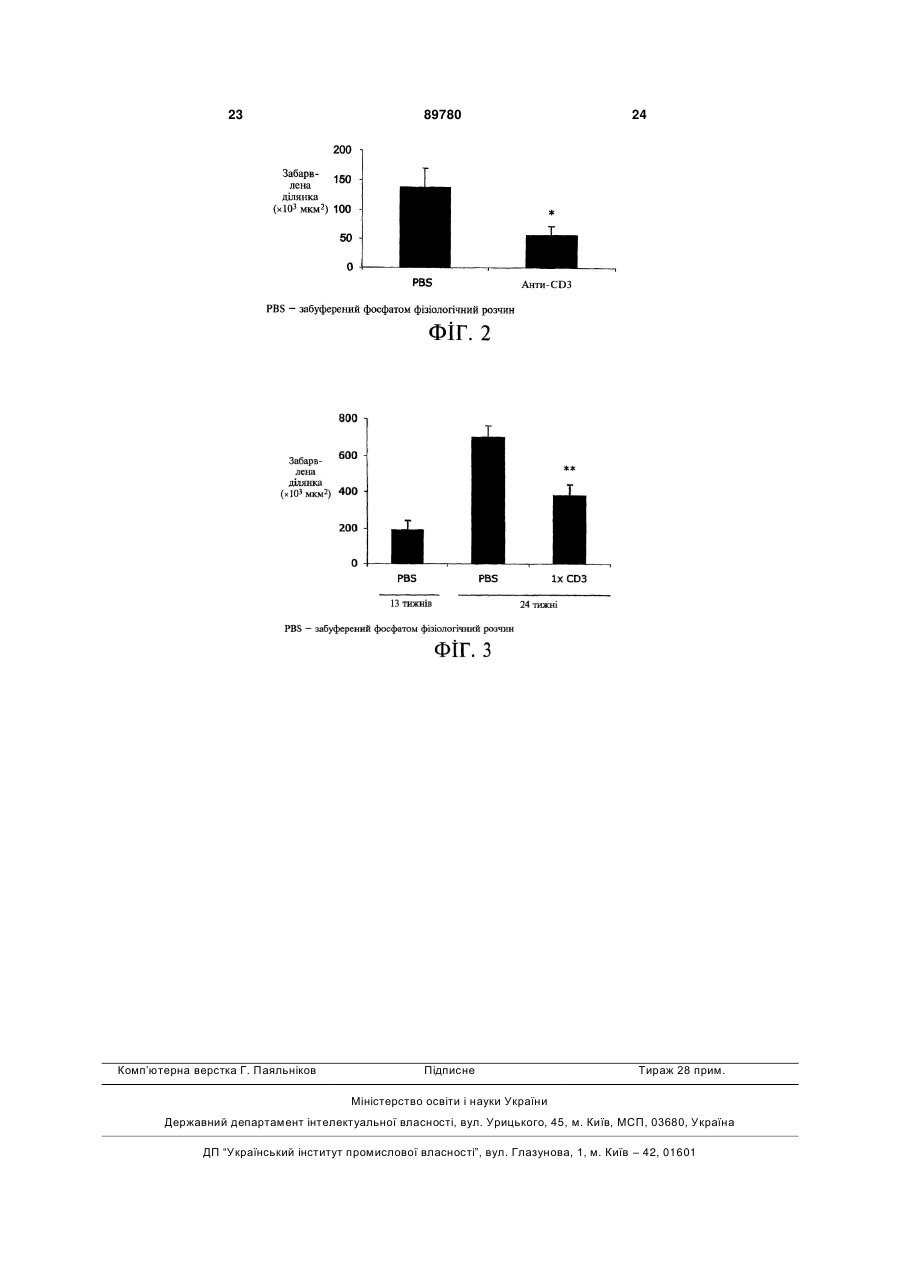
1. Спосіб лікування або полегшення симптомів атеросклерозу, який включає визначення суб'єкта, який страждає на атеросклероз або для якого іс 2 (19) 1 3 Галузь, до якої належить винахід Цей винахід, у цілому, має відношення до застосування модуляторів CD3, наприклад, антиCD3 антитіл, для індукування імунологічної толерантності і модуляції імунної реакції для лікування автоімунних захворювань та/або запальних розладів. Передумови створення винаходу Імунна система є дуже складною і суворо регульованою з багатьма альтернативними шляхами, здатними компенсувати недостатності у інших частинах системи. Існують, однак, випадки, коли імунна реакція, у разі активації, стає причиною захворювання або інших небажаних станів. Такими захворюваннями або небажаними станами є, наприклад, автоімунні захворювання, відторгнення трансплантата після трансплантації, алергія на нешкідливі алергени, псоріаз, хронічні запальні захворювання, наприклад, атеросклероз, і запалення у цілому. У подібних та інших випадках, що включають невідповідну та небажану імунну реакцію, існує клінічна потреба у імуносупресії. Відповідно, існує потреба у композиціях, які можуть застосовуватись для лікування імунопатологічних захворювань та/або розладів. Суть винаходу Цей винахід грунтується на відкритті того, що наслідком модуляції експресії або активності CD3 є пригнічення запалення на пацючій моделі клінічного увеїту і зниження інтенсивності розвитку атеросклеротичних бляшок на мишачій моделі клінічного атеросклерозу. Відповідно, відмітною ознакою цього винаходу є способи запобігання або пригнічення запалення тілесної тканини. Характерними ознаками запаленої тканини, взагалі, є почервоніння, біль і опухання згаданої тканини. Увеїт характеризується зниженою гостротою зору, присутністю клітин та помутнінням (фібрин, денатуровані білки) порожнини ока, заповненої скловидним тілом (задня частина ока) і передньої камери ока. Згаданою тканиною може бути очна тканина, наприклад, судинна оболонка очного яблука, або серцева тканина, наприклад, вена, артерія або капіляр. Запалення пригнічується шляхом піддання клітини або тканини впливу модулятора CD3 у кількості, наслідком застосування якої є зниження продукування прозапального цитокіну, підвищення рівня протизапального цитокіну або у кількості, наслідком застосування якої є виникнення імунологічної толерантності. Цей винахід пропонує способи пригнічення утворення атеросклеротичних бляшок шляхом піддання клітин, що експресують CD3, впливу модулятора CD3. Утворення атеросклеротичних бляшок пригнічується таким чином, що кількість згаданих бляшок, зв'язаних з артеріальними стінками, зменшується після піддання впливу модулятора CD3, порівняно з відповідними показниками перед підданням впливу інгібітора CD3. Згаданими клітинами можуть бути будь-які клітини, здатні до експресії CD3, наприклад, лімфоцити, наприклад, Т-клітини. Згаданими Т-клітинами є циркулюючі Т-клітини, тобто клітини, що знаходяться у крові або лімфі. За альтернативним варі 89780 4 антом, згадані Т-клітини знаходяться у тканині, наприклад, у лімфатичному вузлі, лімфатичних протоках, лімфатичних судинах і селезінці. Згаданою тканиною є запалена тканина (або тканина, для якої існує небезпека стати запаленою). Словосполучення "піддання впливу" означає, що клітина або тканина контактує з модулятором CD3. Клітина тканини контактує безпосередньо або опосередковано (тобто системно). Згадана клітина контактує in vivo, in vitro або ex vivo. Відмітною ознакою цього винаходу є також способи запобігання або полегшення симптомів запального захворювання шляхом розпізнавання суб'єкта, що страждає на або належить до групи ризику розвитку запального захворювання, і введення згаданому суб'єкту модулятора CD3. Модулятором CD3 є сполука, що зменшує експресію або активність CD3. Активності CD3 включають активацію Т-клітин. Способи визначення активації Т-клітин є добре відомими у цій галузі. До числа модуляторів CD3 належать, наприклад, анти-СБЗ антитіла. Модулятори CD3 вводять самостійно або у комбінації з іншим протизапальним засобом або імуносупресорними лікарськими засобами, що застосовуються для лікування запального розладу. Модулятор CD3, наприклад, вводять разом із кортикостероїдом, статином, інтерфероном бета, нестероїдними протизапальними лікарськими засобами (NSAIDs), метотрексатом, циклоспорином А або модифікуючими захворювання протиревматичними лікарськими засобами (DMARDs). Згаданим суб'єктом є ссавець, наприклад, людина, миша, пацюк, собака, кішка, корова, кінь і свиня. Згаданий суб'єкт страждає на запальний розлад або для нього існує небезпека розвитку такого розладу. До запальних розладів належить запалення серцево-судинної системи, запалення очей, запалення шлунково-кишкового тракту, запалення печінки, запалення легень, автоімунні розлади або запалення м'язів. Суб'єкта, що страждає на запальний розлад або для якого існує небезпека розвитку такого розладу, виявляють способами, відомими у цій галузі, наприклад, шляхом макроскопічного дослідження тканини або виявлення асоційованого запалення у тканині або крові. Симптоми запалення включають біль, почервоніння і опухання ураженої тканини. Якщо не визначено інше, усі технічні і наукові терміни, які вживають у цьому описі, мають таке саме значення, яке традиційно розуміється пересічним фахівцем у тій галузі, до якої належить цей винахід. Незважаючи на те, що у разі практичного застосування або випробування цього винаходу можуть застосовуватись способи і матеріали, подібні або еквівалентні тим, опис яких наведено, нижче наведено опис відповідних способів і матеріалів. Усі публікації, заявки на патенти, патенти та інші посилання, згадані у цьому описі, включено до цього опису у повному обсязі шляхом посилання. У разі виникнення протиріччя, для його вирішення може застосовуватись цей опис з включенням визначень. На додаток до цього, матеріали, способи і приклади наведені лише з ілюстративною метою і 5 не призначені для обмеження обсягу цього винаходу. Інші відмітні ознаки і переваги цього винаходу будуть очевидними з наведеного нижче докладного опису і формули винаходу. Короткий опис фігур На Фіг. 1 зображено графік, який відображає клінічні та гістологічні ефекти анти- CD3 терапії на пацючій моделі увеїту. На Фіг. 2 зображено графік, який відображає пригаічувальний ефект анти-CD3 терапії на розвиток атеросклеротичних бляшок у корінці аорти мишей. На Фіг. З зображено графік, який відображає пригнічувальний ефект анти-CD3 терапії на прогресування існуючих атеросклеротичних уражень у мишей. Докладний опис винаходу Цей винахід частково грунтується на відкритті того, що наслідком модуляції експресії або активності CD3 є ослаблена імунна реакція та протизапальний ефект. Конкретніше, наслідком введення анти-CD3 антитіл є зменшення інтенсивності ознак та симптомів, пов'язаних з увеїтом і зниження інтенсивності розвитку атеросклеротичних бляшок. CD3 являє собою комплекс щонайменше п'яти мембранних поліпептидів у зрілих Т-лімфоцитів, які є нековалентно зв'язаними один з одним та з рецептором Т-клітин. Комплекс CD3 включає гамма, дельта, епсилон, зета і ета ланцюги (які також називають субодиницями). Коли антиген зв'язується з рецептором Т-клітин, комплекс CD3 трансдукує сигнали активації до цитоплазми Т-клітини. Модулятори CD3 Модулятор CD3 означає засіб, що модулює експресію або активність CD3. Термін "модулює" означає, що згаданий засіб стимулює, підвищує, знижує або нейтралізує експресію або активність CD3. Активність CD3 включає, наприклад, трансдукцію сигналу активації Т-клітин. Активація Тклітин визначається підвищенням вмісту опосередкованого кальцієм внутрішньоклітинного циклічного гуанозин-3',5'-монофосфату (cGMP) або збільшенням кількості рецепторів IL-2 на поверхні клітин. Посилення активації Т-клітин, наприклад, характеризується зменшенням вмісту опосередкованого кальцієм внутрішньоклітинного циклічного гуанозин-3',5'-монофосфату та/або кількості рецепторів IL-2 у присутності згаданої сполуки, порівнянно з відсутністю згаданої сполуки. Вміст внутрішньоклітинного циклічного гуанозин-3',5'монофосфату визначають, наприклад, за допомогою конкурентного імуноаналізу або аналізу за ефектом близькості сцинтиляції із застосуванням комерційно доступних наборів для проведення випробувань. Кількість рецепторів IL-2 на поверхні клітин встановлюють, наприклад, шляхом визначення зв'язування з рецептором IL-2 антитіла, наприклад, антитіла РС61. Модулятором CD3 є, наприклад, анти-CD3 антитіла або їхні фрагменти. За факультативним варіантом, анти-CD3 антитілом є одноланцюгове анти-CD3 антитіло, біспецифічне анти-CD3 антитіло або гетерокон'югатне анти-CD3 антитіло. Згадане антитіло є активаційним анти-CD3 антитілом, 89780 6 яке, таким чином, індукує активність CD3. За альтернативним варіантом, згаданим антитілом є нейтралізуюче анти-CD3 антитіло, яке, таким чином, знижує рівень активності CD3. Анти-CD3 антитіла є добре відомими у цій галузі. Типовими анти-CD3 антитілами є (але ними не обмежуються) ОКТЗ, G4.18, 145-2С11, Leu4, НІТЗа, ВСЗ, SK7, SP34, RTV-9 та UCHT1. Відповідно до варіанта, якому віддається перевага, антиCD3 антитіло зв'язує ті самі антигенні детермінанти, що і ОКТЗ, G4.18, 145-2С11, Leu4, НІТЗа, ВСЗ, SK7, SP34, RIV-9 та UCHT1. Відповідно до варіанта, якому віддається перевага, згадане антитіло є гуманізованим або включає структурні елементи конячого антитіла для ослаблення імунної реакції хазяїна на згадане антитіло. Фахівцям у цій галузі буде зрозумілою можливість визначення, без зайвого експериментування, чи має антитіло ті самі антигенні детермінанти, що і анти-CD3 антитіло ОКТЗ, G4.18, 145-2С11, Leu4, НІТЗа, ВСЗ, SK7, SP34, RIV-9 та UCHT1, шляхом визначення того, чи перешкоджає перше згадане антитіло зв'язуванню другого згаданого антитіла з CD3 антигенним поліпептидом або іншим антигенним поліпептидом поверхні Т-клітин. Згаданим CD3 антигенним поліпептидом є, наприклад, поліпептид CD3 епсилон у комплексі з іншим субодиничним поліпептидом CD3 (наприклад, гамма, дельта, епсилон, зета або ета ланцюги). Якщо антитіло, яке піддають перевірці, конкурує з антитілом за цим винаходом, як показано зниженням ступеня зв'язування антитілом за цим винаходом, у такому разі два згадані антитіла зв'язуються з тією самою, або близько спорідненою, антигенною детермінантою. Інший спосіб визначення, чи має антитіло специфічність антитіла за цим винаходом, полягає у попередньому інкубуванні антитіла за цим винаходом із CD3 антигенним поліпептидом або поверхневим антигенним поліпептидом Тклітини, з яким воно за звичайних умов реагує, з подальшим доданням антитіла, що піддається перевірці, для визначення, чи пригнічується здатність антитіла, яке піддають перевірці, до зв'язування CD3 або поверхневого антигенного поліпептиду Т-клітини. У разі, якщо антитіло, яке піддають перевірці, пригнічується, тоді, з повною ймовірністю, воно має таку саму, або функціонально еквівалентну, специфічність антигенних детермінант, що і антитіло за цим винаходом. Термін "антитіло", який вживають у цьому описі, означає імуноглобулінові молекули та імунологічно активні частини імуноглобулінових (Ig) молекул, тобто молекул, що містять антигензв'язувальну ділянку, яка специфічно зв'язує антиген (вступає до імунної реакції з ним). До числа таких антитіл належать поліклональні, моноклональні, химерні, одноланцюгові, Fab, Fab , F(ab )2 фрагменти та бібліотека послідовностей Fab, що експресуються. Відповідно до варіанта, якому віддається перевага, згаданим антитілом є повністю людське антитіло. Словосполучення "специфічно зв'язується з" або "вступає в імунну реакцію" означає, що згадане антитіло реагує з однією або декількома антигенними детермінантами бажаного антигену і не реагує (тобто зв'язується) з іншими 7 поліпептидами або зв'язується з іншими поліпеп-6 тидами з набагато нижчою спорідненістю (Кd>10 ). Термін "антигенна детермінанта", який вживають у цьому описі, означає будь-яку білкову детермінанту, здатну до специфічного зв'язування з імуноглобуліном, scFv або рецептором Т-клітин. Термін "антигенна детермінанта" означає будь-яку білкову детермінанту, здатну до специфічного зв'язування з імуноглобуліном або рецептором Тклітин. Антигенні детермінанти, як правило, являють собою хімічно активні поверхневі угруповання молекул, наприклад, амінокислот або бічних ланцюгів цукрів і, як правило, мають специфічні об'ємні структурні характеристики, а також специфічні зарядні характеристики. Кажуть, що антитіло специфічно зв'язує антиген у разі, коли константа дисоціації є 1 мкМ; відповідно до варіанта, якому віддається перевага, є 100 нМ і відповідно до варіанта, якому віддається найбільша перевага, є 10 нМ. Словосполучення "імунологічне зв'язування" та "властивості імунологічного зв'язування", що вживаються у цьому описі, означають нековалентні взаємодії того типу, які відбуваються між імуноглобуліновою молекулою і антигеном, для якого згаданий імуноглобулін є специфічним. Сила або спорідненість імунологічних зв'язувальних взаємодій може виражатись за допомогою константи дисоціації (Кd) взаємодії, де менше значення Kd представляє більшу спорідненість. Кількісне визначення властивостей імунологічного зв'язування вибраних поліпептидів здійснюють за допомогою способів, добре відомих у цій галузі. Одним із таких способів є визначення швидкості утворення і дисоціації комплексів антигензв'язувальна ділянка/антиген, де згадана швидкість залежить від концентрації партнерів, що утворюють комплекс, спорідненості взаємодії та геометричних параметрів, які рівною мірою впливають на швидкість у обох напрямках. Таким чином, як "константа збільшення швидкості" (Коn), так і "константа зменшення швидкості" (Кoff) можуть бути визначені шляхом визначення концентрацій і фактичної швидкості асоціації та дисоціації. [Дивись Nature 361:186-187 (1993)]. Співвідношення Kon/Koff надає можливість відміни усіх параметрів, не пов'язаних зі спорідненістю і дорівнює константі дисоціації Кd. [Дивись, у цілому, Девіс (Davies) (1990) Annual. Rev. Biochem. 59:439-473]. Кажуть, що антитіло за цим винаходом специфічно зв'язується з антигенною детермінантою CD3 у тому разі, коли константа зв'язування у стані рівноваги (Kd) є 1 мкМ; відповідно до варіанта, якому віддається перевага, є 100 нМ, за варіантом, якому віддають більшу перевагу, є 10 нМ, і відповідно до варіанта, якому віддається найбільша перевага, знаходиться у межах від 100 нМ до приблизно 1 нМ, за даними аналізів, наприклад, аналізів зв'язування радіолігандів або подібних аналізів, відомих фахівцям у цій галузі. Антитіло за цим винаходом бажано модифікувати щодо його ефекторних функцій для підсилення ефективності згаданого антитіла при лікуванні імунопатологічних захворювань. Наприклад, до Fc ділянки може(-уть) бути введеним(-і) залишок(-ки) 89780 8 цистеїну, що забезпечить можливість утворення на цій ділянці дисульфідного зв'язку між ланцюгами. Одержане подібним чином гомодимерне антитіло може мати поліпшену інтерналізаційну здатність та/або підвищену здатність до комплементопосередкованого вбивання клітин і антитілозалежну клітинну цитотоксичність (ADCC) [Дивись Карон (Сагоп) та інші, J. Exp. Med., 176:1191-1195 (1992) та Шопс (Shopes), J. Immunol., 148:2918-2922 (1992)]. За альтернативним варіантом, засобами генної інженерії може бути сконструйованим антитіло, що має подвійні Fc ділянки і, завдяки цьому, посилену інтенсивність лізису комплементу та антитілозалежну клітинну цитотоксичність. [Дивись Стевенсон (Stevenson), Anty-Cancer Drag Design, 3:219-230 (1989)]. Антитіла очищають за добре відомими методами, наприклад, засобами афінної хроматографії із застосуванням білка А або білка G, які забезпечують, головним чином, IgG фракцію імунної сироватки. Після цього, або за альтернативним варіантом, специфічний антиген, що є мішенню необхідного імуноглобуліну, або його антигенна детермінанта, можуть іммобілізовуватись на колонці для очищення імуноспецифічного антитіла засобами імуноафінної хроматографії. Очищення імуноглобулінів обговорюється, наприклад, у роботі Д. Вілкінсон [D. Wilkinson) (The Scientist, опубліковано The Scientist, Inc., Philadelphia PA, том 14, № 8 (17 квітня 2000 року), crop. 25-28]. Терапевтичні методи Запалення пригнічується шляхом піддання, наприклад, контактування, тканини або клітини, що експресує CD3, впливу CD3 модулятора, наприклад, анти-CD3 антитіла. Клітиною, що експресує CD3, є, наприклад, лімфоцит, такий як Тклітина. Т-клітини включають цитотоксичні Тклітини, Т-клітини-хелпери (наприклад, Thl та Th2) та природні Т-клітини-кілери. Тканини, призначені для обробки, включають тканину шлунковокишкового тракту, наприклад, тканину кишечнику, серцеву тканину, наприклад, вену, артерію або капіляр, легеневу тканину, шкірну тканину, очну тканину, наприклад, райдужну оболонку ока, війчасте тіло, власне судинну оболонку ока або печінкову тканину. Пригнічення запалення може характеризуватись зменшенням почервоніння, болю та опухання тканини, яка зазнає обробки, порівняно із тканиною, яка не контактувала з CD3 модулятором. За альтернативним варіантом, щодо увеїту, пригнічення запалення характеризується підвищенням гостроти зору, зменшенням кількості клітин та помутніння (фібрин, денатуровані білки) порожнини ока, заповненої скловидним тілом (тобто задньої частини ока) і передньої камери ока. Тканини або клітини безпосередньо контактують із CD3 модулятором. За альтернативним варіантом, CD3 модулятор вводять системним шляхом. CD3 модулятори вводять у кількості, достатній для зниження (наприклад, пригнічення) продукування прозапальних цитокінів. Прозапальним цитокіном є цитокін, що індукує запальну реакцію. До числа прозапальних цитокінів належать, наприклад, інтерлейкін-1 (IL-1), фактор некрозу пухлин (TNF), 9 IL-17, IL-18 і макрофагальний медіатор алергічного запалення-1 альфа (МІР-1 альфа). За альтернативним варіантом, CD3 модулятори вводять у кількості, достатній для підвищення (наприклад, стимулювання) продукування протизапальних цитокінів. Протизапальним цитокіном є цитокін, що зменшує запальну реакцію. Конкретніше, протизапальний цитокін контролює реакцію прозапальних цитокінів для регулювання імунної реакції. Протизапальні цитокіни включають, наприклад, антагоніст рецепторів інтерлейкіну-1 (IL-1), TGFp (трансформуючий фактор росту β), IL-4, IL-6, IL-10, IL-11 та IL-13. Цитокіни виявляють, наприклад, у сироватці, плазмі або тканині. Продукування цитокінів визначають за допомогою способів, відомих у цій галузі. Продукування цитокінів визначають, наприклад, за допомогою імуноаналізу, специфічного для прозапального цитокіну або протизапального цитокіну. Морфологічну оцінку запальної реакції роблять шляхом спостереження пошкодження тканини, локалізованого почервоніння, опухання ураженої ділянки, клітин та помутніння порожнини ока, заповненої скловидним тілом та передньої камери ока. За альтернативним варіантом, запальну реакцію оцінюють шляхом визначення вмісту Среактивного білка або IL-1 у тканині, сироватці або плазмі. Повернення кількості лейкоцитів до вихідного рівня також вказує на зменшення запалення. За альтернативним варіантом, запалення знижують шляхом піддання тканини або клітини, що експресує CD3, впливу модулятора CD3 у кількості, яка забезпечує перерозподіл та/або видалення комплексу CD3-рецептора Т-клітини або комплексу CD3 на поверхні клітини, наприклад, лімфоциту. Наприклад, клітину, що експресує CD3, піддають впливу модулятора CD3 у кількості, достатній для модуляції, тобто зниження міжклітинного контакту клітин, що експресують CD3. Зниження рівня експресії на поверхні клітини або активності TcR (рецептор Т-клітин) на клітині означає, що кількість або функція TcR є зниженою. Модуляція рівня експресії на поверхні клітини або активності CD3 означає, що кількість CD3 на поверхні клітини або функція CD3 є зміненою, наприклад, зниженою. Кількість CD3 або TcR, експресованих на плазматичній мембрані клітини, знижується, наприклад, шляхом інтерналізації CD3 або TcR при контактуванні згаданої клітини з модулятором CD3. За альтернативним варіантом, при контактуванні клітини з модулятором CD3, CD3 маскується. Наслідком перерозподілу та/або видалення комплексу СОЗ-рецептора Т-клітин на поверхні клітини є імунологічна супресія або імунна толерантність. Імунологічна супресія означає нездатність до підвищення загальної імунної реакції на усі антигени, наслідком чого є зміна одного або декількох симптомів автоімунного розладу або зниження запальної реакції. Імунологічна супресія має зворотний характер після припинення лікування модулятором CD3. Таким чином, імунологічна супресія є особливо корисною у разі лікування або полегшення симптомів гострого запального розладу. У протилежність до цього, імунною толерантністю є нездатність до підвищення імунної реакції на 89780 10 специфічний антиген, наслідком чого є полегшення одного або декількох симптомів автоімунного розладу або зниження запальної реакції, причому згадана властивість зберігається впродовж тривалого часу після припинення лікування. Імунологічна толерантність зберігається щонайменше впродовж 1 тижня, 1 місяця, 3 місяців, 6 місяців, 1 року, 2 років або 5 чи більше років після припинення лікування. Таким чином, імунологічна толерантність є особливо корисною у разі лікування або полегшення симптомів хронічного запального розладу. Довгострокову імунологічну толерантність можна забезпечити або через розчинні механізми, наприклад, цитокіни, або через безпосередній міжклітинний контакт, що залучає (але без обмеження) гранзим А, гранзим В та/або перфорин. Утворення атеросклеротичних бляшок на артерії, тобто на артеріальній стінці, зменшується або запобігається шляхом введення суб'єкту модулятора CD3. Бляшка являє собою комбінацію холестерину, інших жирових матеріалів, кальцію і компонентів крові, які накопичуються у межах вистілки артеріальної стінки. Зменшення атеросклеротичних бляшок визначається за зменшенням звуження просвіту, тобто за розширенням просвіту. Ширина просвіту визначається за способами, відомими у цій галузі, наприклад, за допомогою контрастної ангіографії або доплер-аналізу швидкості і форми хвилі. Згадані способи є корисними для полегшення симптомів цілого ряду різноманітних запальних захворювань або автоімунних розладів. Запальний розлад є гострим або хронічним. Запальні розлади включають запалення серцево-судинної системи (наприклад, атеросклероз, інсульт), запалення шлунково-кишкового тракту, запальні розлади печінки, легеневі запалення (наприклад, астму, пошкодження легень, викликане апаратом штучної вентиляції), запалення нирок, запалення очей (наприклад, увеїт), запалення підшлункової залози, запалення сечостатевої системи, запальні розлади нервової системи (наприклад, розсіяний склероз, хвороба Альцгеймера), алергію (наприклад, алергічний риніт/синусит, шкірні алергії та розлади (наприклад, уртикарія/кропив'янка, набряк Квінке, дифузний нейродерміт, контактний дерматит, псоріаз), харчові алергії, лікарські алергії, алергії на комах, мастоцитоз), запалення скелетних м'язів (наприклад, артрит, остеоартрит, ревматоїдний артрит, спондилоартропатії), інфекцію (наприклад, бактеріальну або вірусну інфекції; запальні розлади ротової порожнини (тобто пародонтоз, гінгівіт або стоматит); і трансплантацію (наприклад, відторгнення алотрансплантата або ксенотрансплантата чи толерантність матері та плода). Автоімунні захворювання включають, наприклад, синдром набутого імунодефіциту (СНІД, який являє собою вірусне захворювання з автоімунною складовою), вогнищеву алопецію, анкілозивний спондилоартрит, антифосфоліпідний синдром, автоімунну хворобу Аддісона, автоімунну гемолітичну анемію, автоімунний гепатит, автоімунне захворювання внутрішнього вуха (AIED), автоімунний лімфопроліферативний синдром (ALPS), автоімунну тромбоцитопенічну пурпуру (АТР), хворобу 11 Бехчета, кардіоміопатію, синдром черевної мальабсорбції-герпетоформний дерматит; синдром хронічного перевтомлення з дисфункцією імунної системи (CFIDS), хронічну запальну демієлінізуючу поліневропатію (CIPD), рубцевий пемфігоїд, синдром холодової аглютинації, гребінцевий синдром, хворобу Крона, хворобу Дего, юнацький дерматоміозит, дискоїдний червоний вовчак, ідіопатичну кріоглобулінемію змішаного типу, фіброміалгію-фіброміозит, хворобу Грейвса, хворобу Гійєна-Барре, тиреоідит Хаишмото, ідіопатичний фіброз легень, ідіопатичну тромбоцитопенічну пурпуру (ІТР), нефропатію IgA-типу, інсулінозалежний цукровий діабет, юнацький інфекційний артрит (хвороба Стілла-Шоффара), юнацький ревматоїдний артрит, хворобу Меньєра, дифузну хворобу сполучної тканини змішаного типу, розсіяний склероз, важку псевдопаралітичну міастенію, злоякісну анемію, нодозний поліартеріїт, поліхондрит, плюригландулярний синдром, ревматичну поліміалгію, поліміозит і дерматоміозит, початкову агаммоглобулінемію, первинний біліарний цироз печінки, псоріаз, псоріазний артрит, феномен Рейно, синдром Рейтера, ревматизм, ревматоїдний артрит, саркоідоз, склеродермію (прогресуючий системний склероз (PSS), відомий також як системний склероз (SS)), синдром Шегрена, синдром ригідної людини, системний червоний вовчак, синдром Такаясу, темпоральний артеріїт/гігантоклітинний артеріїт, неспецифічний виразковий коліт, увеїт, вітиліго і гранулематоз Вегенера. Наслідком застосування способів, опис яких наведено, є зниження тяжкості або полегшення одного або декількох симптомів запального розладу або автоімунного захворювання, опис яких, наприклад, наведено у описі до цього винаходу. Ефективність лікування визначають у поєднанні з будь-яким відомим способом діагностування або лікування конкретного запального розладу. Полегшення одного або декількох симптомів запального розладу або автоімунного захворювання свідчить про те, що згадана сполука забезпечує клінічно сприятливий ефект. Запальні розлади та автоімунні розлади діагностуються та/або контролюються, як правило, лікарем або ветеринарним лікарем за допомогою стандартних методів. Увеїт Увеїт визначається як запалення судинної оболонки очного яблука. Судинна оболонка очного яблука складається з трьох структур: райдужна оболонка ока, війчасте тіло і власне судинна оболонка ока. Райдужна оболонка ока являє собою забарвлену структуру, що оточує зіницю, яку видно у передній частині ока. Війчасте тіло являє собою структуру, що містить м'яз, який знаходиться за райдужною оболонкою ока і фокусує кришталик ока. Власне судинна оболонка ока являє собою шар, що містить кровоносні судини, які вистилають задню частину ока, і знаходиться між сітківкою і склерою. Симптоми увеїту включають обмежену гостроту зору, клітини і помутніння (фібрин, денатуровані білки) порожнини ока, заповненої сюгавидним тілом, і передньої камери ока та васкуліт судин сітківки. Райдужна оболонка ока може при 89780 12 липати до капсули кришталика (задня синехія) або, рідше, до периферичної частини рогівки (передня синехія). На додаток до цього, у межах строми райдужної оболонки можуть спостерігатись гранулематозні вузлики. Внутрішньоочний тиск в ураженому оці початково знижується унаслідок секреторної гіпотонії війчастого тіла. Однак, оскільки реакція триває, у трабекулі можуть накопичуватись запальні побічні продукти. У разі значного накопичення цих залишків органічних речовин, і якщо війчасте тіло відновлює своє нормальне секретування, тиск може різко зрости, наслідком чого є вторинна увеїтна глаукома. Увеїт діагностується лікарем або ветеринарним лікарем під час офтальмологічного обстеження. Васкуліт Васкуліт являє собою запалення кровоносних судин. Запалення являє собою стан, під час якого тканина пошкоджується клітинами крові, які проникають до тканин. Це, головним чином, лейкоцити, які циркулюють і відіграють роль нашого головного захисту проти інфекції. Лейкоцити, як правило, знищують бактерії та віруси. Однак вони можуть пошкоджувати нормальну тканину, у разі проникнення до неї. Васкулітом можуть уражатись дуже малі кровоносні судини (капіляри), кровоносні судини середнього розміру (артеріоли або венули) або великі кровоносні судини (артерії та вени). Васкуліт може спричинювати багато різних симптомів у залежності від того, які тканини є залученими і тяжкості пошкодження тканин. Деякі хворі не відчувають хвороби і помічають випадкові плями на своїй шкірі. Інші сильно хворіють із системними симптомами і пошкодженням головних органів. Симптоми включають пропасницю, загальне нездужання ("дискомфорт"), біль у м'язах і суглобах, поганий апетит, втрату маси, втомлюваність, петехіальні висипи, пурпуру, ділянки мертвої шкіри можуть з'являтись як виразки (зокрема, довкола щиколоток), біль у суглобах і виражений артрит із болем, опуханням і жаром у суглобах, головний біль, розлади поведінки, сплутаність свідомості, припадки, інсульти, оніміння і поколювання. Діагноз васкуліту грунтується на історії хвороби особи, наявних симптомах, повному об'єктивному обстеженні і результатах спеціалізованих лабораторних аналізів. До числа відхилень від норми показників крові, які тасто спостерігаються у разі васкуліту, належить підвищена швидкість седиментації, анемія, велика кількість лейкоцитів і велика кількість тромбоцитів. Аналізи крові можуть також застосовуватись для виявлення імунних комплексів або антитіл, що спричинюють васкуліт, у системі кровообігу і визначення відхилень від норми рівнів комплементу. Атеросклероз Наслідком атеросклерозу є накопичення відкладень жирових речовин, холестерину, продуктів життєдіяльності клітин і кальцію у внутрішній вистілці артерії (тобто бляшок) і це захворювання має суттєву запальну складову. Зрештою, ця жирова тканини може роз'їсти стінку артерії, зменшити її еластичність (розтягуваність) і перешкоджати кровотоку. Бляшки можуть також розриватись, 13 унаслідок чого залишки органічних речовин переміщаються За течією крові у артерії. Це поширена причина серцевого нападу та інсульту. Довкола відкладень бляшок можуть утворюватись також згустки, які додатково перешкоджають кровотоку і становлять додаткову небезпеку у разі відривання і переміщення до серця, легень або головного мозку. Симптоми у разі атеросклерозу часто виникають лише після серйозного порушення кровотоку у судинах. Типовими симптомами атеросклерозу є біль у грудній клітині, коли до процесу залучається коронарна артерія, або біль у ногах, коли залучається ножна артерія. Подеколи симптоми з'являються лише у разі фізичного напруження. У деяких людей, однак, вони можуть з'являтись і у стані спокою. До факторів ризику належать паління, діабет, ожиріння, високий рівень холестерину у крові, раціон, багатий жирами, а також серцеве захворювання у особистому або родинному анамнезі. Розладами, які також можуть асоціюватись з атеросклерозом, є захворювання цереброваскулярної системи, захворювання периферичних кровоносних судин, високий кров'яний тиск і захворювання нирок із залученням діалізу. Терапевтичне введення Цей винахід включає введення суб'єкту, наприклад, людині або коню, композиції, що містить модулятор CD3 (який у цьому описі називають "терапевтичною сполукою"). Ефективна кількість терапевтичної сполуки, відповідно до варіанта, якому віддається перевага, становить від приблизно 0,1 мг/кг до приблизно 150мг/кг. Ефективна доза змінюється, що є зрозумілим для фахівців у цій галузі, у залежності від шляху введення, застосованого наповнювача та одночасного введення з іншими терапевтичними засобами, у тому числі у разі застосування інших протизапальних засобів або терапевтичних засобів для лікування, запобігання або полегшення симптомів конкретного запального розладу. Схему лікування здійснюють шляхом встановлення ссавця, наприклад, хворої людини або коня, що страждає на запальний розлад або автоімунні розлади (або для якого існує небезпека їх розвитку), за допомогою стандартних методів. Фармацевтичну сполуку вводять такому індивіду за допомогою способів, відомих у цій галузі. Відповідно до варіанта, якому віддається перевага, згадану сполуку вводять пероральним, ректальним, назальним, місцевим або парентеральним шляхом, наприклад, підшкірним, внутрішньоочеревинним, внутрішньом'язовим та внутрішньовенним. Згадану сполуку вводять із профілактичною метою або після виявлення запального явища, наприклад, нападу астми або алергічної реакції. Згадану сполуку факультативно вводять як складову частину суміші терапевтичних засобів для лікування запальних розладів. Прикладами лікарських форм, придатних для парентерального введення, є водні розчини активного агента у ізотонічному фізіологічному розчині, 5% розчині глюкози або іншому стандартному фармацевтично прийнятному наповнювачі. Стандартні солюбілізаційні 89780 14 агенти, наприклад, полівінілпіролідон або циклодекстрини, також застосовуються у ролі фармацевтичних наповнювачів для доставки терапевтичних сполук. Терапевтичні сполуки, опис яких наведено, вводяться до складу композицій для інших шляхів введення за допомогою традиційних способів. Наприклад, інгібітор терапевтичної сполуки вміщують у капсулу або вводять до складу таблетки для введення пероральним шляхом. Капсули можуть містити будь-які стандартні фармацевтично прийнятні матеріали, наприклад, желатин або целюлозу. Таблетки можуть виготовлятись за традиційними методиками шляхом пресування сумішей терапевтичної сполуки з твердим носієм і змащувальною речовиною. Прикладами твердих носіїв є крохмаль і бентоніт із цукром. Сполуку вводять у формі таблетки з твердою оболонкою або капсули, що містить зв'язувальний засіб, наприклад, лактозу або маніт, традиційний заповнювач і компонент, який сприяє таблетуванню. Іншими лікарськими формами є мазь, супозиторій, паста, спрей, пластир, крем, гель, розсмоктувальна губка або піна. Такі лікарські форми виготовляють за способами, добре відомими у цій галузі. Терапевтичні сполуки є ефективними у разі безпосереднього контакту згаданої сполуки з ураженою тканиною. Відповідним чином, згадану сполуку вводять місцевим шляхом. Наприклад, для лікування контактних дерматитів, сполуку наносять на уражену ділянку шкіри. За альтернативним варіантом, терапевтичну сполуку вводять системним шляхом. На додаток до цього, сполуки вводять шляхом імплантування (безпосередньо до органа, наприклад, кишечнику чи печінки, або підшкірно) твердої або розсмоктувальної матриці, яка повільно виділяє згадану сполуки до прилеглих і оточуючих тканин суб'єкта. Наприклад, для лікування запальних розладів шлунково-кишкового тракту, згадану сполуку вводять системно або місцево безпосередньо до тканини шлунка. Сполуку для системного введення вводять внутрішньовенним, ректальним або оральним шляхом. Для місцевого введення просякнуту сполукою облатку або розсмоктувальну губку розмішують для безпосереднього контакту з тканиною шлунка. Сполука або суміш сполук повільно виділяється in vivo шляхом дифузії лікарського засобу з облатки і унаслідок роз'їдання полімерної матриці. Запалення печінки (тобто гепатит) лікують, наприклад, шляхом вливання до судинної сітки печінки розчину, що містить згадану сполуку. Внутрішньоочеревинне вливання або лаваж є придатними для зниження генералізованого внутрішньоочеревинного запалення або запобігання запалення після хірургічного втручання. Для лікування неврологічного запалення, сполуку вводять внутрішньовенним або підоболонковим шляхом (тобто шляхом безпосереднього вливання до цереброспінальної рідини). Для місцевого введення просякнуту сполукою облатку або розсмоктувальну губку розміщують для безпосереднього контакту з тканиною центральної нервової системи. Сполука або суміш сполук повільно 15 виділяється in vivo шляхом дифузії лікарського засобу з облатки і унаслідок роз'їдання полімерної матриці. За альтернативним варіантом, згадану сполуку вливають до головного мозку або цереброспінальної рідини за допомогою відомих способів. Наприклад, кільце з отвором і катетером для застосування у ролі вхідного отвору для ін'єкцій розміщують на черепі на трепанаційному отворі, просвердленому у черепі. Доступ до рідинного резервуара, що сполучається з катетером, забезпечується за допомогою голки або тонкого зонда, який вставляють через перетинку, розміщену на верхній частині кільця з отвором. Катетер у зібраному вигляді (наприклад, збірна одиниця, описана у патенті США № 5,954,687) забезпечує шлях для перетікання рідини, придатний для проходження рідин до або з вибраного місця на, поблизу або у межах головного мозку, для уможливлення введення лікарського засобу впродовж періоду часу. Для лікування запалення серця, згадану сполуку доставляють, наприклад, до серцевої тканини шляхом безпосередньої внутрішньокоронарної ін'єкції через стінку грудної клітини або за допомогою стандартних способів із застосуванням черезшкірного катетера з рентгеноскопічним контролем для безпосередньої ін'єкції до тканини, наприклад, серцевого м'яза, або вливання інгібітора через стент або катетер, введений до просвіту тіла. Для введення згаданої сполуки застосовують коронарний катетер або катетер для вливання будь-якого типу. За альтернативним варіантом, згадану сполуку наносять або нею просякають стент, який вміщують до коронарної судини. Запалення легень лікують, наприклад, введенням сполуки інгаляційним шляхом. Сполуки доставляють у формі аерозольного спрею з контейнера під підвищеним тиском або пристрою, що містить відповідний пропелент, наприклад, газ, наприклад, діоксид вуглецю, або розпилювача. Запалення очей лікують, наприклад, шляхом введенням згаданої сполуки місцево до ока. Сполуки доставляють, наприклад, у формі гелю, рідини або мазі. Мазі, гелі або рідини для закапування можуть доставлятись за допомогою систем для доставки до ока, відомими у цій галузі, як інструменти для локального застосування лікарського засобу або очні піпетки. За альтернативним варіантом, сполуки доставляють у полімерному імплантаті, якій вмішують під сполучну оболонку ока. За факультативним варіантом, сполуки доставляють системним шляхом. Васкуліт лікують шляхом, специфічним для ураженої ділянки. Взагалі, васкуліт лікують системно шляхом внутрішньовенного введення модулятора CD3. Модулятори CD3 також вводять у поєднанні з одним або декількома додатковим терапевтичними сполуками, наприклад, протизапальним засобом або імуносупресивним засобом. Наприклад, модулятор CD3 вводять у комбінації з будь-яким із різноманітних відомих лікарських засобів для лікування автоімунних захворювань та/або запальних розладів. Відповідними відомими засобами для лікування автоімунних захворювань та/або запальних розладів для застосування за способами за 89780 16 цим винаходом є (але без обмеження) метотрексат, циклоспорин А (з включенням, наприклад, мікроемульсії циклоспорину та такролімусу), кортикостероїдні препарати, статини, інтерферон бета, нестероїдні протизапальні лікарські засоби (NSAIDs) та протиревматичні засоби, що модифікують захворювання, (DMARDs). Додаткові засоби вводять перед, після або одночасно з введенням модулятора CD3. Корисним ефектом згаданої комбінації є (але без обмеження) комбінована фармакокінетична або фармакодинамічна дія, що є результатом об'єднання терапевтичних засобів. Введення цих терапевтичних засобів у комбінації здійснюють, як правило, впродовж певного періоду часу (як правило, хвилин, годин, днів або тижнів, у залежності від вибраної комбінації). Словосполучення "комбінований спосіб лікувального впливу" може, однак як правило не означає, введення двох або декількох із цих терапевтичних засобів, як частини окремих схем лікування одним лікарським засобом, результатом чого, між іншим та довільно, є комбінації за цим винаходом. Словосполучення "комбінований спосіб лікувального впливу" означає введення цих терапевтичних засобів послідовно, тобто коли кожен терапевтичний засіб вводять у різний час, а також введення цих терапевтичних засобів (або щонайменше двох терапевтичних засобів) по суті одночасно. По суті одночасне введення може здійснюватись, наприклад, шляхом введення суб'єкту одноразової капсули, що має визначене співвідношення кожного терапевтичного засобу або декількох одноразових капсул для кожного з терапевтичних засобів. Терапевтичні засоби можуть вводитись тим самим або різними шляхами. Наприклад, перший терапевтичний засіб вибраної комбінації може вводитись шляхом внутрішньовенної ін'єкції, у той час як інші терапевтичні засоби комбінації можуть вводитись пероральним шляхом. За альтернативним варіантом, наприклад, усі терапевтичні засоби можуть вводитись пероральним шляхом або усі терапевтичні засоби можуть вводитись шляхом внутрішньовенної ін'єкції. Послідовність введення терапевтичних засобів не є суворо критичною. Словосполучення "комбінований спосіб лікувального впливу" може також означати введення терапевтичних засобів, як описано вище, у додатковій комбінації з іншими біологічно активними інгредієнтами та нефармацевтичними засобами (наприклад, хірургія або променева терапія). У разі, коли комбінований спосіб лікувального впливу додатково включає лікування нефармацевтичними засобами, згадане лікування нефармацевтичними засобами може здійснюватись у будь-який придатний час доти, доки не буде досягнуто корисного ефекту завдяки комбінованій дії об'єднання терапевтичних засобів і лікування нефармацевтичними засобами. Наприклад, у відповідних випадках, корисного ефекту все ж досягають навіть у тому разі, коли лікування нефармацевтичними засобами тимчасово видаляють зі схеми введення терапевтичних засобів, можливо, на дні або навіть тижні. 17 Для оцінки того, чи є корисним для хворого введення анти-CD3 антитіла, самостійно або у комбінації, слід провести кількісне дослідження симптомів та/або імунної реакції хворого, і порівняти симптоми та/або імунну реакцію хворого перед та після лікування згаданим антитілом. Симптоми хворого можна, наприклад, визначити шляхом визначення конкретного симптому або набору симптомів у хворого перед та після лікування анти-CD3 антитілом. Можна, наприклад, визначити і контролювати такі симптоми, як пропасниця, біль у суглобах, м'язова слабість, за допомогою будь-яких зі стандартних методів визначення, відомих у цій галузі. У разі успішного лікування, стан хворого буде поліпшуватись (тобто показники визначень будуть зменшуватись або буде збільшуватись час до тривалого прогресування). Наприклад, у разі лікування увеїту, анти-CD3 антитіла можуть вводитись, наприклад, у поєднанні з кортикостероїдами, метотрексатом, циклоспорином А, циклофосфамідом та/або статинами. Подібним чином, хворих, уражених такою хворобою, наприклад, як хвороба Крона або псоріаз, можна лікувати комбінацією анти-CD3 антитіла за цим винаходом і ремікейду (remicaid) (інфліксімабу (infliximab)) та/або гуміру (humira) (адалімумабу (adalimumab)). У разі лікування ревматоїдного артриту, антиCD3 антитіла вводять разом із кортикостероїдами, метотрексатом, циклоспорином А, статинами, ремікейдом (remicade) (інфліксімабом), енбрелом (enbrel) (етанерцептом (etanercept)) та/або гуміром (адалімумабом). Хворі на розсіяний склероз можуть одержувати комбінацію анти-CD3 з, наприклад, ацетатом глатирамеру (копаксоном (сорахопе)), інтерфероном бета-1а (авонексом (avonex)), інтерфероном бета-1а (ребіфом (rebif)), інтерфероном бета-1b (бетасероном (betaseron) або бетафероном (betaferon)), мітоксантроном (новантроном (novantrone)), дексаметазоном (декадроном (decadron)), метилпреднізолоном (депо-медролом (depo-medrol)) та/або преднізоном (делтазоном (deltasone)) та/або статинами. Хворим із діабетом типу І або латентним автоімунним діабетом дорослих (LADA) також вводять другий засіб, наприклад, GLP-1 (глюкагоноподібний пептид) або сполуку, що переводить бетаклітини у стан спокою (тобто сполуку, що зменшує або іншим чином пригнічує вивільнення інсуліну, наприклад, відкривачі калієвих каналів). На додаток до цього, модулятори CD3 вводять хворому профілактично (тобто перед початком автоімунного захворювання та/або запального розладу) або терапевтично (тобто впродовж перебігу автоімунного захворювання та/або запального розладу). За способами за цим винаходом, модулятори вводять у терапевтично ефективній кількості. Термін "терапевтично ефективна кількість" модулятора CD3 означає кількість, необхідну для досягнення терапевтичної цілі, наприклад, лікування автоімунного захворювання та/або запального розладу, або полегшення симптомів, пов'язаних з 89780 18 автоімунним захворюванням та/або запальним розладом. Усі публікації та патентні документи, згадані у цьому описі, включені до нього шляхом посилання таким чином, як нібито кожна окрема публікація або документ були б конкретно та індивідуально призначені до включення шляхом посилання. Згадування публікацій і патентних документів не призначене для визнання того, що будь-який з них належить до відомого рівня техніки і не становить жодного визнання щодо їх вмісту або дати публікації. Після наведення письмового опису цього винаходу, фахівцям у цій галузі буде зрозуміло, що цей винахід може бути практично втіленим цілим рядом варіантів здійснення і що вищенаведений опис і наведені нижче приклади мають ілюстративне призначення, а не обмеження формули винаходу, яка додається. Приклади Приклад 1: анти-CD3 антитіла при лікуванні увеїту Анти-CD3 антитіла за цим винаходом включають будь-яке з різноманітних моноклональних антитіл (mAb), що розпізнають CD3, наприклад, ОКТЗ, SP34, UCHTI або 64.1. [Дивись, наприклад, Джун (June) та інші, J. Immunol. 136:3945-3952 (1986); Янг (Yang) та інші, J. Immunol. 137:10971100 (1986); Хейуард (Hayward) та інші, Immunol. 64:87-92 (1988)]. Очищене мишаче анти-пацюче CD3 моноклональне антитіло (фірма BD Pharmingen); яке у цьому описі називають антитілом G4.18, перевіряли на індуцибельній пацючій моделі увеїту, як описано, наприклад, у Вілднер Г. (Wildner G.), ДідріхсМорінг М. (Diedrichs-Mohring Μ.), Туро С.Р. (Thurau S.R.), Eur. J. Immunol. 32(1):299-306 (2002); Вілднер Г. (Wildner G.), Дідріхс-Морінг Μ. (DiedrichsMohring Μ.), Int. Immunol. 15(8):927-935 (2003). Антитіло G4.18 реагує з поверхневим антигеном CD3, асоційованим із рецептором Т-клітин, який знаходиться на тимоцитах, периферичних Тлімфоцитах та дендритних епідермальних Тклітинах. (Дивись, наприклад, Ніколлз М.Р. (Nicolls M.R.) та інші, Transplantation 55:459-468 (1993); НелсонД.Дж. (Nelson D.J.) та інші, J. Exp. Med. 179:203-212 (1994); Морріс Д.Л. (Morris D.L.), В.Дж. Комоцар (WJ. Komocsar), J. Pharmacol. Toxicol. Methods 37:37-46 (1997)). Для оцінки ефектів анти-CD3 терапії на увеїт, у пацюків, шляхом процесу внутрішньоочеревинного (і.р.) перенесення Т-клітин, індукували експериментальний автоімунний увеїт (EAU). Зокрема, у День 0, пацюки-самиці лінії Lewis (маса кожної приблизно 140 г), n=3 пацюки/групу, одержали внутрішньоочеревинну ін'єкцію 2,4х106 клітин L37, трансфікованих PDSAg-2/З, який одержали з ретинального автоантигенного S-антигену (SAg). За 30 хв перед і у дні 1, 2 і 3 після перенесення трансгенних Т-клітин для індукування EAU, пацюки одержали внутрішньоочеревинні ін'єкції 300 мкл забуференого фосфатом фізіологічного розчину (PBS) (Група 1) або розчину антитіла G4.18 у 300 мкл PBS (Група 2). Кожну групу пацюків контролювали щоденно для виявлення клінічних ознак увеїту. Клінічними критеріями ступеня інтенсивно 19 89780 сті, що застосовувались під час проведення цього експерименту, приймалось до уваги лише запалення у передній частині ока, ступінь якого оцінювали за допомогою офтальмоскопа, як описано, наприклад, у де Смет (de Smet) та інших, J. 20 Autoimmun., том 6:587 (1993). Клінічні критерії ступеня інтенсивності, які застосовувались при проведенні експериментів, опис яких наводиться, подані нижче у Таблиці А. Таблиця А Клінічні критерії ступеня інтенсивності Ступінь інтенсивності 0,5 1,0 2,0 3,0 4,0 Опис Розширені судини райдужної оболонки ока, часткові запальні інфільтрати у обідку райдужної оболонки ока та помутніння передньої камери ока Повна кільцева інфільтрація обідку райдужної оболонки ока Ділянка зіниці повністю заповнена клітинами та фібрином Утворення гіпопіону* Передня камера ока повністю заповнена клітинами, фібрином і кров'ю *гіпопіон=осадження лейкоцитів у донній частині передньої камери ока; тобто біле "озерце" Експеримент закінчили на 12 день, і кожного пацюка піддали гістологічній перевірці з метою визначення ступеня пошкодження сітківки ока. Гістологічними критеріями, опис яких наводиться, до уваги приймався лише ступінь пошкодження сітківки ока, який оцінювали на зрізах, одержаних на 9 день після лікування, за допомогою мікротома у кріостаті, як описано, наприклад, у де Смет (de Smet) та інших, J. Autoimmun., том 6:587 (1993). Гістологічні критерії ступеня інтенсивності, які застосовувались при проведенні експериментів, опис яких наводиться, подані нижче у Таблиці В. Таблиця В Гістологічні критерії ступеня інтенсивності Ступінь Опис інтенсивності 0,0 Відсутність ознак запального захворювання - Мінімальне запалення, форма сітківки ока залишається макроскопічно інтактною - Інфільтрація клітин запального інфільтрату до сітківки ока без ознак руйнування тканини 0,5 або із пошкодженням зовнішніх фоторецепторів менше ніж на 1/4 сітківки ока - Вогнищева негранулематозна інфільтрація моноцитів до власне судинної оболонки ока, війчастого тіла і сітківки ока - Пошкодження фотороцепторів зовнішнього сегмента на >1/4 сітківки ока - Вогнищеві ділянки руйнування з явно вираженим скороченням кількості фоторецепторів 1,0 - Ретинальна періваскулярна інфільтрація та інфільтрація моноцитів до порожнини ока, заповненої скловидним тілом - Ураження, яке проходить до зовнішнього ядрового шару та на >1/4 сітківки ока - Незначне ексудативне відшарування сітківки ока - Присутність клітин (у кількості від незначної до помірної) у порожнині ока, заповненій 2,0 скловидним тілом - Утворення гранульоми у судинній оболонці очного яблука та у сітківці ока - Оклюзивний ретинальний васкуліт разом із серозним відшаруванням сітківки і втратою фоторецепторів - Ураження, яке проходить до внутрішнього ядрового шару та на >1/4 сітківки ока - Починається деформація сітківки ока, значне ексудативне відшарування сітківки, присут3,0 ність клітин (у кількості від помірної до великої) у порожнині ока, заповненій скло видним тілом - Утворення вогнищ Далена-Фукса і розвиток нових субретинальних кровоносних судин 4,0 - Пошкодження сітківки ока на повну товщину на 1/4 площі - Повна деформація сітківки ока Клінічні ознаки увеїту почали з'являтись на 3 день експерименту, опис якого наведено. На Фіг. 1 зображено графік, який відображає клінічні та гістологічні ефекти (як визначено за допомогою кри теріїв ступеня інтенсивності, описаних вище у Таблиці А і Таблиці В) на прогресування увеїту у пацюків, які одержували PBS (тобто Група 1), і пацюків, які одержували анти-CD3 антитіло (тобто 21 Група 2). Представлені результати наводяться як середнє значення максимальних оцінок усіх очей групи впродовж усього періоду спостереження. Приклад 2: анти-CD3 антитіла при лікуванні атеросклерозу Ефективність анти-CD3 антитіл при лікуванні атеросклерозу оцінювали із застосуванням антимишачого CD3 антитіла хом'яків. Описані експерименти розроблялись для оцінки впливу антиCD3 терапії на розвиток атеросклеротичних бляшок, а також впливу анти-CD3 терапії на прогресування вже існуючих атеросклеротичних уражень. Для оцінки ефектівності анти- CD3 терапії застосовували лінію клітин, що продукують F(ab')2 фрагменти моноклонального антитіла 145 2С11 хом'яків, що зв'язується з мишачим CD3 (тобто з ланцюгом епсилон мишачого комплексу CD3). Миші-самці лінії LDLR-/-C57BL/6 віком 10 тижнів використовувались як in vivo модель атеросклерозу. Для гістологічного аналізу та аналізу розвитку атеросклеротичних бляшок, а також аналізу проліферації та цитокінів, одноприплідним мишам впродовж 13 тижнів або 24 тижнів згодовували раціон із високим вмістом холестерину (1,25% холестерину, 0% холату). Анти-CD3 F(ab')2 (50 мкг/мишу/добу) вводили внутрішньовенно (i.v.) впродовж 5 послідовних днів, розпочинаючи за 1 тиждень перед (n=5) (тобто для оцінки впливу анти-СОЗ антитіла на розвиток атеросклеротичних бляшок) або через 13 тижнів (n=9) після початку згодовування раціону з високим вмістом холестерину (тобто для оцінки впливу Анти-CD3 антитіла на прогресування вже існуючих атеросклеротич 89780 22 них уражень). Контрольним мишам (n=5 у разі згодовування раціону впродовж 13 тижнів; n=6 у разі згодовування раціону впродовж 24 тижнів) паралельно робили ін'єкції PBS. Атеросклеротичні ураження торакоабдомінальної аорти та синусу аорти аналізували шляхом забарвлювання Суданом IV на відкладення ліпідів (Фіг. 2 і Фіг. 3). Для кожного корінця аорти середнє значення відкладень ліпідів підраховували на 6 зрізах (5 мкм), відокремлених один від одного відстанню, що становила 50 мкм. Кількісне визначення відкладень ліпідів здійснювали шляхом комп'ютерного аналізу зображень із застосуванням програми MetaMorph6 (Zeiss). Представлені результати виражені як середнє значення±середня квадратична помилка середнього. Різниці між значеннями вважались значущими при Р
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod of treating or alleviating symptoms of an atherosclerosis by means of anti-cd3 antibody
Автори англійськоюMach Bernard, Dean Yann, Kosco-Vilbois Marie
Назва патенту російськоюСпособ лечения или облегчения симптомов атеросклероза с помощью анти-cd3 антитела
Автори російськоюМах Бернар, Дин Ян, Коско-Вильбуа Мари
МПК / Мітки
МПК: A61P 9/10, A61K 39/395
Мітки: симптомів, допомогою, атеросклерозу, спосіб, антитіла, анти-cd3, лікування, полегшення
Код посилання
<a href="https://ua.patents.su/12-89780-sposib-likuvannya-abo-polegshennya-simptomiv-aterosklerozu-za-dopomogoyu-anti-cd3-antitila.html" target="_blank" rel="follow" title="База патентів України">Спосіб лікування або полегшення симптомів атеросклерозу за допомогою анти-cd3 антитіла</a>
Попередній патент: Спосіб приготування рідкого хлібопекарського поліпшувача
Наступний патент: Рідкий склад гормона росту
Випадковий патент: Універсальна руслова гес