Способи одержання амідів і складних ефірів піридинкарбонової кислоти
Номер патенту: 90767
Опубліковано: 25.05.2010
Автори: Веверс Ян Хендрік, Брінк Моніка, Кнелль Маркус
Формула / Реферат
1. Спосіб одержання амідів та складних ефірів піридинкарбонової кислоти І
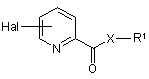 , I
, I
де
Hal означає атом галогену;
X означає О або NR2;
R1 означає C1-С6-алкільну або арильну групу, де обидві групи можуть бути заміщені одним або декількома атомами галогену, нітро, ціано, C1-С6-алкільними, C1-С6-галоалкільними або C1-С6-алкоксильними групами;
R2 означає атом водню або C1-С6-алкільну групу;
який включає наступні стадії:
(а) нагрівання суміші, яка складається по суті із трихлорметилпіридину II
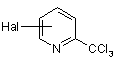 , ІІ
, ІІ
де Hal має наведені значення,
та 1,0-1,5 еквівалентів концентрованої сірчаної кислоти,
(б) введення у реакцію проміжного продукту, одержаного на стадії (а), з аміном або спиртом III
HXR1, ІІІ
де X і R1 мають наведені значення,
який відрізняється тим, що трихлорметилпіридин II у вигляді рідини додають до концентрованої сірчаної кислоти при температурі від 110 °С до 160 °С.
2. Спосіб за п. 1, де стадію (б) проводять в присутності розчинника і/або основи.
3. Спосіб за п. 1 або 2, де трихлорметилпіридин II являє собою трихлорметилпіридин ІІА
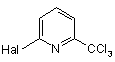 , ІІА
, ІІА
де Наl означає атом галогену.
4. Спосіб за будь-яким з пп. 1-3, де
X означає О; та
R1 означає C1-С6-алкільну групу.
5. Спосіб за будь-яким з пп. 1-4, де
X означає NR2;
R1 означає фенільну групу, яка заміщена одним або двома атомами галогену і/або C1-С6-галоалкільними групами; та
R2 означає атом водню.
6. Спосіб за будь-яким з пп. 1-5, де трихлорметилпіридин II додають до концентрованої сірчаної кислоти при температурі від 120 до 150 °С.
7. Спосіб за будь-яким з пп. 1-6, де суміш трихлорметилпіридину II і концентрованої сірчаної кислоти витримують при температурі від 120 до 150 °С протягом від 30 до 300 хвилин.
8. Спосіб за будь-яким з пп. 1-7, де застосовувана сірчана кислота містить менш ніж 3 мас. % води.
9. Спосіб за будь-яким з пп. 1-8, де проміжний продукт, утворений на стадії (а), включає сполуку формули VI і/або VII або її структурно-ізомерні форми:
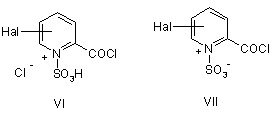 ,
,
де Hal означає атом галогену.
10. Спосіб за будь-яким з пп. 1-9, де проміжний продукт, утворений на стадії (а), додають до аміну або спирту III у вигляді рідини.
11. Спосіб за будь-яким з пп. 1-10, де проміжний продукт, одержаний на стадії (а), обробляють аміном III у присутності основи та ароматичного вуглеводню як розчинника.
12. Спосіб за будь-яким з пп. 1-11, де складний ефір піридинкарбонової кислоти І обробляють аміном III у присутності основи та ароматичного вуглеводню як розчинника.
13. Спосіб одержання амідів та складних ефірів (арилокси)піридинкарбонової кислоти IV
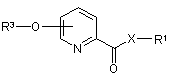 , IV
, IV
де
X означає О або NR2;
R1 означає C1-С6-алкільну або арильну групу, де обидві групи можуть бути заміщені одним або декількома атомами галогену, нітро, ціано, C1-С6-алкільними, C1-С6-галоалкільними або C1-С6-алкоксильними групами;
R2 означає атом водню або C1-С6-алкільну групу;
R3 означає арильну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, C1-С6-алкільними, C1-С6-алкокси або C1-С6-галоалкільними групами;
який включає наступні стадії:
(а) нагрівання суміші, яка складається по суті із трихлорметилпіридину II, визначеного вище, і від 1,0 до 1,5 еквівалентів концентрованої сірчаної кислоти;
(б) введення у реакцію проміжного продукту, одержаного на стадії (а), з аміном або спиртом III, визначеними вище; та
(в) введення у реакцію амідів і складних ефірів піридинкарбонової кислоти І або їх солі, одержаних на стадії (б), з ароматичним спиртом V
R3-OH, V
де R3 має наведенізначення,
який відрізняється тим, що трихлорметилпіридин II у вигляді рідини додають до концентрованої сірчаної кислоти при температурі від 110 до 160 °С.
14. Спосіб за п. 13, де стадію (б) проводять в присутності розчинника і/або основи та стадію (в) проводять в присутності основи.
15. Спосіб за п. 13 або 14, де на стадії (в) аміди та складні ефіри піридинкарбонової кислоти І або їх сіль вводять у реакцію з ароматичним спиртом V без додаткового очищення.
16. Спосіб за будь-яким з пп. 13-15, де на стадії (в) складний ефір піридинкарбонової кислоти ІА
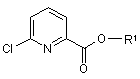 , IA
, IA
де R1 означає C1-С6-алкільну групу,
вводять у реакцію з ароматичним спиртом V у присутності основи.
17. Спосіб одержання амідів (арилокси)піридинкарбонової кислоти IV за будь-яким з пп. 13-16, який включає
(в) введення у реакцію складного ефіру піридинкарбонової кислоти І або його солі, одержаних на стадії (б), з ароматичним спиртом V у присутності основи, та
(г) обробку одержаного складного ефіру (арилокси)піридинкарбонової кислоти IV аміном III.
18. Спосіб одержання амідів (арилокси)піридинкарбонової кислоти IV за пунктом 13, де R2 означає водень, а стадія (в) включає
введення у реакцію складного ефіру піридинкарбонової кислоти І з аміном III,
де R2 означає водень, та обробку одержаних солей I.1
 I.1
I.1
ароматичним спиртом V.
Текст
1. Спосіб одержання амідів та складних ефірів піридинкарбонової кислоти І 2 3 90767 11. Спосіб за будь-яким з пп. 1-10, де проміжний продукт, одержаний на стадії (а), обробляють аміном III у присутності основи та ароматичного вуглеводню як розчинника. 12. Спосіб за будь-яким з пп. 1-11, де складний ефір піридинкарбонової кислоти І обробляють аміном III у присутності основи та ароматичного вуглеводню як розчинника. 13. Спосіб одержання амідів та складних ефірів (арилокси)піридинкарбонової кислоти IV R3 O X N O 4 14. Спосіб за п. 13, де стадію (б) проводять в присутності розчинника і/або основи та стадію (в) проводять в присутності основи. 15. Спосіб за п. 13 або 14, де на стадії (в) аміди та складні ефіри піридинкарбонової кислоти І або їх сіль вводять у реакцію з ароматичним спиртом V без додаткового очищення. 16. Спосіб за будь-яким з пп. 13-15, де на стадії (в) складний ефір піридинкарбонової кислоти ІА Cl R1 , IV де X означає О або NR2; R1 означає C1-С6-алкільну або арильну групу, де обидві групи можуть бути заміщені одним або декількома атомами галогену, нітро, ціано, C1-С6алкільними, C1-С6-галоалкільними або C1-С6алкоксильними групами; R2 означає атом водню або C1-С6-алкільну групу; R3 означає арильну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, C1-С6-алкільними, C1-С6-алкокси або C1-С6галоалкільними групами; який включає наступні стадії: (а) нагрівання суміші, яка складається по суті із трихлорметилпіридину II, визначеного вище, і від 1,0 до 1,5 еквівалентів концентрованої сірчаної кислоти; (б) введення у реакцію проміжного продукту, одержаного на стадії (а), з аміном або спиртом III, визначеними вище; та (в) введення у реакцію амідів і складних ефірів піридинкарбонової кислоти І або їх солі, одержаних на стадії (б), з ароматичним спиртом V R3-OH, V де R3 має наведені значення, який відрізняється тим, що трихлорметилпіридин II у вигляді рідини додають до концентрованої сірчаної кислоти при температурі від 110 до 160 °С. Даний винахід стосується способу одержання амідів і складних ефірів піридинкарбонової кислоти І де Hal означає атом галогену; X означає О або NR2; R1 означає С1-С6-алкільну або арильну групу, де обидві групи можуть бути заміщені одним або декількома атомами галогену, нітро, ціано, С1-С6алкільними, C1-С6-галоалкільними або С1-С6алкоксильними групами; O N R1 O , IA де R1 означає C1-С6-алкільну групу, вводять у реакцію з ароматичним спиртом V у присутності основи. 17. Спосіб одержання амідів (арилокси)піридинкарбонової кислоти IV за будь-яким з пп. 13-16, який включає (в) введення у реакцію складного ефіру піридинкарбонової кислоти І або його солі, одержаних на стадії (б), з ароматичним спиртом V у присутності основи, та (г) обробку одержаного складного ефіру (арилокси)піридинкарбонової кислоти IV аміном III. 18. Спосіб одержання амідів (арилокси)піридинкарбонової кислоти IV за пунктом 13, де R2 означає водень, а стадія (в) включає введення у реакцію складного ефіру піридинкарбонової кислоти І з аміном III, де R2 означає водень, та обробку одержаних солей I.1 H Hal + N N O R1 I.1 ароматичним спиртом V. R2 означає атом водню або С1-С6-алкільну групу; який включає наступні стадії: (а) нагрівання суміші, яка складається по суті із трихлорметилпіридину II де Hal має наведені значення, і від 1.0 до 1.5 еквівалентів концентрованої сірчаної кислоти, яке відрізняється тим, що трихлорметилпіридин II у вигляді рідини додають до концентрованої сірчаної кислоти при температурі від 110 до 160°С; та 5 (б) введення у реакцію проміжного продукту, одержаного на стадії (а), з аміном або спиртом III HXR1 III, де X і R1 мають наведені значення, необов'язково в присутності розчинника і/або основи. Іншим аспектом даного винаходу є спосіб одержання амідів і складних ефірів (арилокси)піридинкарбонової кислоти IV де R1 і X мають наведені значення, і R3 означає арильну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або С1-С6-алкоксильними групами; у якому приготовляють аміди та складні ефіри піридинкарбонової кислоти І або їх солі із трихлорметилпіридину II відповідно до даного винаходу та (в) потім їх вводять у реакцію з ароматичним спиртом V де R3 має наведені значення, необов'язково в присутності основи. Аміди та складні ефіри піридинкарбонової кислоти І є придатними проміжними сполуками для одержання великої кількості різних сполук, які є придатними для застосування як агрохімікати або фармацевтичні препарати. Зокрема, вони є ключовими проміжними сполуками для одержання гербіцид них феноксипіридинкарбоксамідів, які описані, наприклад, в ЕР 0 447 004. У заявці на європейський патент ЕР 0 646 566 пропонується гідролізувати трихлорметилгетероарени водою в присутності хлорованих вуглеводнів і кислоти Льюїса, і одержаний гетероарилкарбонілхлорид вводити у реакцію з аміном. Однак цей спосіб викликає труднощі відносно здійснення точного еквімолярного дозування води та швидкості такого дозування. Будь-який надлишок води приводить до гідролізу цільового хлорангідриду кислоти й, отже, знижує виходи. Крім того, у наші дні небажано застосування хлорованих вуглеводнів через проблеми захисту навколишнього середовища, а кількість розчинника, застосовуваного в способі рівня техніки, є високою. До того ж, час реакції, необхідний при використанні суміші вода/1,2-дихлоретан, є дуже великим (24год). Заявка на європейський патент ЕР 0 899 262 розкриває спосіб одержання амідів і складних ефірів піридинкарбонової кислоти, у якому сірчану кислоту додають до піридинтрихлорметанової сполуки. Однак цей спосіб викликає труднощі, тому що утворена проміжна сполука твердіє при температурах нижче 100°С, а повторне плавлення цієї затверділої проміжної сполуки відбувається важко 90767 6 внаслідок розкладання з виділенням соляної кислоти та триоксиду сірки. Отже, задача даного винаходу полягала в тому, щоб запропонувати новий ефективний спосіб одержання амідів та складних ефірів піридинкарбонової кислоти з високим виходом та чистотою. Новий поліпшений спосіб дозволяє уникнути труднощів способів, відомих з рівня техніки, і надає можливість здійснювати одержання піридинкарбоксамідів і відповідних складних ефірів у промисловому масштабі й з високим виходом, використовуючи готові, наявні у продажу вихідні продукти. Крім того, спосіб відповідно до даного винаходу має декілька переваг відносно технологічної безпеки в порівнянні зі способом, розкритим в ЕР 0 899 262 А: Суміш, одержана на стадії (а) є не такою чутливою до охолодження під час додавання трихлорметилпіридину II. Реакційна суміш, одержана під час додавання, є більш стабільною й послаблення нагрівання не приводить до труднощів, пов'язаних із застиганням. Крім того, коли до трихлорметилпіридину II додають сірчану кислоту, як розкрито в ЕР 0 899 262, трихлорметилпіридин II демонструє схильність до випаровування з реакційної суміші в систему повітряних ліній і там конденсується і/або застигає. Додатково до потенційного зниження виходу, це може привести до засмічення клапанів і витяжних трубопроводів, що являє загрозу безпеки. Таким чином, спосіб відповідно до даного винаходу, безсумнівно, знижує випаровування трихлорметилпіридину II. Інші задачі та переваги даного винаходу будуть очевидні спеціалісту в даній галузі техніки з наступного опису та прикладеної формули винаходу. Загалом, якщо тут не зазначено інше, термін "трихлорметилпіридин формули II у вигляді рідини" включає трихлорметилпіридини II, які є рідиною при кімнатній температурі; та трихлорметилпіридини II, які є твердою речовиною при кімнатній температурі, але використовуються або у вигляді розчину в інертному розчиннику, або при температурі вище їх температури плавлення, тобто, у розплавленому вигляді. Загалом, якщо тут не зазначено інше, термін "аміди піридинкарбонової кислоти І" означає "аміди та складні ефіри піридинкарбонової кислоти І, де X означає NR2". Загалом, якщо тут не зазначено інше, термін "складні ефіри піридин карбонової кислоти І" означає „аміди та складні ефіри піридинкарбонової кислоти І, де X означає О". Загалом, якщо тут не зазначено інше, термін "амін III" означає "амін або спирт III, де X означає NR2". Загалом, якщо тут не зазначено інше, термін "спирт III" означає „амін або спирт III, де X означає О". Загалом, якщо тут не зазначено інше, термін "аміди (арилокси)піридин карбонової кислоти IV" означає "аміди та складні ефіри (арилок 7 си)піридинкарбонової кислоти IV, де X означає NR2". Загалом, якщо тут не зазначено інше, термін "складні ефіри (арилокси)піридинкарбонової кислоти IV" означає "аміди та складні ефіри (арилокси)піридинкарбонової кислоти IV, де X означає О". Органічні залишки, наведені у визначеннях замісників R1, R2 і R3 або як замісники фенільного, нафтильного або антранілового кілець є-подібно терміну галоген-збірними термінами для індивідуальних переліків індивідуальних членів груп. Всі вуглеводневі ланцюги, тобто всі алкільні, галоалкільні та алкоксильні групи, можуть бути нерозгалуженими або розгалуженими, приставка Cn-Cm показує в кожному випадку можливе число атомів вуглецю в групі. Галогеновані замісники переважно несуть один, два, три, чотири або п'ять однакових або різних атомів галогену. Термін галоген означає в кожному випадку фтор, бром, хлор або йод. Прикладами інших значень є: - С1-С4-алкіл: СН3, С2Н5, н-пропіл, СН(СН3)2, нбутил, СН(СН3)-С2Н5, СН2-СН(СН3)2 та С(СН3)3; - С1-С6-алкіл: С1-С4-алкіл як визначено вище, і також, наприклад, н-пентил, 1-метилбутил, 2метилбутил, 3-метилбутил, 2,2-диметилпропіл, 1етилпропіл, н-гексил, 1,1-диметилпропіл, 1,2диметилпропіл, 1-метилпентил, 2-метилпентил, 3метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-іметилпропіл або 1-етил-2-метилпропіл, переважно метил, етил, н-пропіл, 1-метилетил, н-бутил, 1,1диметилетил, н-пентил або н-гексил; - С1-С4-галоалкіл: С1-С4-алкільний радикал, як визначено вище, який є частково або повністю заміщений фтором, хлором, бромом і/або йодом, тобто, наприклад, CH2F, CHF2, CF3, СН2СІ, дихлорметил, трихлорметил, хлорфторметил, дихлорфторметил, хлордифторметил, 2-фторетил, 2хлоретил, 2-брометил, 2-йодетил, 2,2-дифторетил, 2,2,2-трифторетил, 2-хлор-2-фторетил, 2-хлор-2,2дифторетил, 2,2-дихлор-2-фторетил, 2,2,2трихлоретил, C2F5, 2-фторпропіл, 3-фторпропіл, 2,2-дифторпропіл, 2,3-дифторпропіл, 2хлорпропіл, 3-хлорпропіл, 2,3-дихлорпропіл, 2бромпропіл, 3-бромпропіл, 3,3,3-трифторпропіл, 3,3,3-трихлорпропіл, 2,2,3,3,3-пентафторпропіл, гептафторпропіл, 1-(фторметил)-2-фторетил, 1(хлорметил)-2-хлоретил, 1-(бромметил)-2брометил, 4-фторбутил, 4-хлорбутил, 4-бромбутил або нонафторбутил; - С1-С6-галоалкіл: С1-С4-галоалкільний радикал, як визначено вище, а також, наприклад, 5фторпентил, 5-хлорпентил, 5-бромпентил, 5йодпентил, ундекафторпентил, 6-фторгексил, 6хлоргексил, 6-бромгексил, 6-йодгексил і додекафторгексил; - С1-С4-алкокси: наприклад ОСН3, ОС2Н5, нпропокси, ОСН(СН3)2, н-бутокси, ОСН(СН3)-С2Н5, ОСН2-СН(СН3)2 або ОС(СН3)3, переважно ОСН3, ОС2Н5 або ОСН(СН3)2; - С1-С6-алкокси: С1-С4-алкоксильний радикал, як визначено вище, і також, наприклад, пентокси, 90767 8 1-метилбутокси, 2-метилбутокси, 3метоксилбутокси, 1,1-диметилпропокси, 1,2диметилпропокси, 2,2-диметилпропокси, 1етилпропокси, гексокси, 1-метилпентокси, 2метилпентокси, 3-метилпентокси, 4метилпентокси, 1,1-диметилбутокси, 1,2диметилбутокси, 1,3-диметилбутокси, 2,2диметилбутокси, 2,3-диметилбутокси, 3,3диметилбутокси, 1-етилбутокси, 2-етилбутокси, 1,1,2-триметилпропокси, 1,2,2-триметилпропокси, 1-етил-1-метил пропокси та 1-етил-2метилпропокси; - арил: моно-, бі- або трициклічне ароматичне вуглецеве кільце, яке містить від 6 до 14 кільцевих членів, наприклад феніл, нафтил та антраценіл. Кращими ароматичними групами, як правило, є ті, які заміщені, принаймні, однією електроноакцепторною групою, зокрема одним або декількома атомами галогену, нітро, ціано або С1-С6галоалкільними групами. В окремому варіанті способу відповідно до даного винаходу, радикали сполук відповідно до даного винаходу приймають наведені нижче значення, ці визначення є як самі по собі, так і в комбінації один з одним, окремими варіантами здійснення даного винаходу: Перевагу віддають способу відповідно до даного винаходу, де Hal означає фтор, хлор або бром; краще хлор або бром; особливо краще хлор. Перевагу також віддають способу відповідно до даного винаходу, де X означає кисень. Перевагу також віддають способу відповідно до даного винаходу, де X означає NR2. Перевагу також віддають способу відповідно до даного винаходу, де R1 означає С1-С6-алкіл, який може бути заміщений одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або С1-С6-алкоксильними групами; краще С1-С6-алкіл, який може бути заміщений одним або декількома атомами галогену; особливо краще С1-С6-алкіл; найбільш краще С1-С4-алкіл. Перевагу також віддають способу відповідно до даного винаходу, де R1 означає арильну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або С1-С6-алкоксильними групами; переважно фенільну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або С1-С6-алкоксильними групами; особливо краще фенільну групу, яка може бути заміщена одним або двома атомами галогену, вибраними із фтору й хлору; найбільш краще фенільну групу, яка може бути заміщена одним атомом галогену; надзвичайно краще фенільну групу, яка може бути заміщена одним атомом фтору. 9 90767 10 Перевагу також віддають способу відповідно до даного винаходу, де R2 означає водень. Перевагу також віддають способу відповідно до даного винаходу, де R2 означає С1-С6-алкіл; краще С1-С4-алкіл. Перевагу також віддають способу відповідно до даного винаходу, де X означає О; і R1 означає С1-С6-алкіл, який може бути заміщений одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або С1-С6-алкоксильними групами; переважно С1-С6-алкіл, який може бути заміщений одним або декількома атомами галогену; особливо краще С1-С6-алкіл; надзвичайно краще С1-С4-алкіл; найбільш краще ізопропіл. Перевагу також віддають способу відповідно до даного винаходу, де X означає NR2; R1 означає арильну групу, яка заміщена одним або декількома атомами галогену, нітро, ціано, С1С6-алкільними, С1-С6-галоалкільними або С1-С6алкоксильними групами; переважно фенільну групу, яка заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6-галоалкільними або С1-С6-алкоксильними групами; особливо краще фенільну групу, яка заміщена одним або двома атомами галогену і/або С1-С6галоалкільними групами; найбільш краще фенільну групу, яка може бути заміщена одним або двома атомами галогену, вибраними із фтору та хлору; найбільш краще фенільну групу, яка може бути заміщена одним атомом галогену; особливо краще фенільну групу, яка може бути заміщена одним атомом фтору; та 2 R означає водень. Перевагу також віддають способу відповідно до даного винаходу, де R3 означає арильну групу, яка може бути заміщена одним або двома атомами галогену або С1-С6-галоалкільними групами; переважно арильну групу, яка може бути заміщена однією С1-С6-галоалкільною групою. Перевагу також віддають способу відповідно до даного винаходу, де 3 R означає фенільну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або С1-С6-алкоксильними групами; переважно фенільну групу, яка може бути заміщена одним або декількома атомами галогену або С1-С6-галоалкільними групами; особливо краще фенільну групу, яка може бути заміщена С1-С6-галоалкільною групою; найбільш краще фенільну групу, яка може бути заміщена С1-С6-галоалкільною групою в 3-му положенні фенільного фрагмента; особливо краще фенільну групу, яка може бути заміщена С1-С4-галоалкільною групою в 3-му положенні фенільного фрагмента. Перевагу також віддають способу відповідно до даного винаходу, де трихлорметилпіридини II заміщені одним атомом галогену, переважно атомом хлору. Особливу перевагу віддають способу відповідно до даного винаходу, де трихлорметилпіридини II являють собою трихлорметилпіридини ІІА Проміжний продукт, утворений на стадії (а), включає сполуку формули VI і/або формули VII, або їх структурно-ізомерні форми: Реакцію трихлорметилпіридину II із сірчаною кислотою проводять при температурі від 110°С до 160°С, краще від 120°С до 150°С, найбільш краще при 135°С. Перевагу віддають способу відповідно до даного винаходу, де на стадії (а) суміш трихлорметилпіридину II і концентрованої сірчаної кислоти витримують при температурі від 120 до 150°С протягом від 30 від 300 хвилин, більш краще від 30 до 240 хвилин. де Hal означає атом галогену; переважно фтор, хлор або бром; особливо краще хлор або бром; надзвичайно краще хлор. Найбільшу перевагу віддають способу відповідно до даного винаходу, де трихлорметилпіридини II являють собою нітрапірин (НП), сполуку llА, де Hal означає СІ. Стадія (а) способу відповідно до даного винаходу, включає нагрівання суміші, яка складається по суті із трихлорметилпіридину II і від 1.0 до 1.5 еквівалентів концентрованої сірчаної кислоти, яке відрізняється тим, що трихлорметилпіридин II у вигляді рідини додають до концентрованої сірчаної кислоти при температурі від 110 до 160°С: 11 90767 12 Стадію (а) можна здійснювати при зниженому або підвищеному тиску, переважно її проводять при тиску навколишнього середовища. Стадію (а) можна здійснювати в інертному органічному розчиннику із придатною температурою кипіння або при відсутності будь-якого розчинника. Придатними розчинниками є аліфатичні вуглеводні, такі як суміші С5-С8-алканів, ароматичні вуглеводні, такі як толуол, о-, м- та п-ксилол, і галогеновані вуглеводні, такі як хлорбензол. Також можливе застосування сумішей згаданих розчинників. Перевагу віддають способу відповідно до даного винаходу, де стадію (а) проводять при відсутності будь-якого розчинника. Перевагу віддають способу відповідно до даного винаходу, де на стадії (а) концентрована сірчана кислота містить менш ніж 3 мас.% води. Стадію (а) проводять у присутності від 1.0 до 1.5 еквівалентів, переважно від 1.1 до 1.4 еквіва лентів, особливо краще від 1.25 до 1.35 еквівалентів концентрованої сірчаної кислоти. Перевагу віддають способу відповідно до даного винаходу, де на стадії (а) трихлорметилпіридин II додають до концентрованої сірчаної кислоти повільно, більш краще, в інтервалі часу від 1 до 5 годин. При цих кращих умовах, реакція стадії (а), як правило, завершується протягом від 30 до 300 хвилин, переважно протягом від 45 до 240 хвилин, зокрема, протягом від 60 до 210 хвилин. Необхідні трихлорметилпіридини II доступні для придбання або можуть бути приготовлені шляхом галогенування 2-трихлорметилпіридину (наприклад, згідно A. R. Katritzky, С. D. Johnson, Angew. Chem. Int. Ed. 1967, 6, 608-615). Стадія (б) способу відповідно до даного винаходу включає введення у реакцію проміжного продукту, одержаного на стадії (а), з аміном або спиртом III необов'язково в присутності інертного розчинника або основи: Реакцію проміжного продукту, одержаного на стадії (а) з аміном або спиртом III звичайно проводять при температурі між температурою навколишнього середовища та температурою флегми реакційної суміші, переважно при температурі від 0°С до 140°С, особливо краще при температурі від 20°С до 120°С, найбільш краще від 40°С до 100°С у присутності інертного розчинника або основи. Як правило, стадію (б) можна здійснювати при зниженому або підвищеному тиску, переважно її проводять при тиску навколишнього середовища. Стадію (б) реакції відповідно до винаходу можна проводити при відсутності або в присутності розчинника, який сприяє реакції або, принаймні, не заважає її протіканню. Придатними розчинниками є неполярні розчинники, включаючи аліфатичні вуглеводні, такі як пентан, гексан, циклогексан і суміші С5-С8-алканів, ароматичні вуглеводні, такі як толуол, о-, м- і пксилол, галогеновані вуглеводні, такі як дихлорметан, хлороформ, 1,2-дихлоретан і хлорбензол, нітроалкани, такі як нітроетан. Також можливе застосування сумішей згаданих розчинників. Стадію (б) реакції відповідно до винаходу можна проводити при відсутності або в присутності основи. Придатними основами є, звичайно, органічні основи, наприклад третинні аміни, такі як три(С1С6-алкіл)аміни (наприклад триметиламін, триетиламін, діізопропілетиламін), N-метилпіперидин, піридин, заміщені піридини, такі як колідин, лутидин, N-метилморфолін і 4-диметиламінопіридин, а також біциклічні аміни. Основи звичайно використовують в еквімолярних кількостях, у надлишку або, при необхідності, як розчинник. Переважно основи застосовують в еквімолярних кількостях. Звичайно, проміжний продукт, одержаний на стадії (а), і амін або спирт III застосовують в еквімолярних кількостях. Може бути корисним використовувати надлишок III у перерахунку на проміжний продукт. Проміжний продукт, одержаний на стадії (а), переважно вводять у реакцію з аміном або спиртом III у вигляді рідини або після розведення інертним розчинником. У кращому варіанті проміжний продукт стадії (а) додають до аміну або спирту III переважно у вигляді рідини. Реакцію стадії (б) зі спиртом III переважно проводять при температурі від 40°С до 70°С, найбільш краще при 65°С. У тому випадку, якщо проміжний продукт, утворений на стадії (а), вводять у реакцію зі спиртом III, стадію (б) переважно проводять при надлишку зазначеного спирту. Переважно, проміжний продукт, утворений на стадії (а), вводять у реакцію зі спиртом III, який одночасно виконує функції розчинника. Альтернативно, проміжний продукт, одержаний на стадії (а), можна обробити спиртом III у присутності інертного розчинника, такого як толуол. Перевагу віддають способу відповідно до даного винаходу, де на стадії (б) проміжний продукт, одержаний на стадії (а), обробляють спиртом III, де 13 90767 14 R1 означає С1-С6-алкіл, який може бути заміщений одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6галоалкільними або Сі-Сб-алкоксильними групами; краще С1-С6-алкіл; більш краще етил або ізопропіл. Реакцію стадії (б) з аміном III переважно проводять при температурі від 50°С до 140°С, найбільш краще при 80°С. У тому випадку, якщо проміжний продукт, утворений на стадії (а), вводять у реакцію з аміном III, стадію (б) переважно проводять у присутності основи, зазначеної вище; особливо краще в присутності три(С1-С6алкіл)амінів (наприклад триметиламіну, триетиламіну, діізопропілетиламіну), N-метилпіперидину, піридину, заміщених піридинів, таких як колідин, лутидин, N-метилморфолін і 4диметиламінопіридин; найбільш краще три(С1-С6алкіл)амінів; особливо краще триетиламіну. Переважно проміжний продукт, утворений на стадії (а), вводять у реакцію з аміном III, який одночасно виконує функції розчинника. Альтернативно, проміжний продукт, одержаний на стадії (а), можна обробити аміном III у присутності інертного розчинника, переважно ароматичного вуглеводню, такого як толуол. Перевагу віддають способу відповідно до даного винаходу, де проміжний продукт, одержаний на стадії (а), обробляють аміном III у присутності основи та ароматичного вуглеводню як розчинника. Перевагу також віддають способу відповідно до даного винаходу, де проміжний продукт, одержаний на стадії (а), обробляють аміном III де R1 означає фенільну групу, яка заміщена одним або двома атомами галогену і/або С1-С6галоалкільними групами; переважно фенільну групу, яка може бути заміщена одним або двома атомами галогену, вибраними із фтору та хлору; особливо краще фенільну групу, яка може бути заміщена одним атомом галогену; особливо краще фенільну групу, яка може бути заміщена одним атомом фтору; і R2 означає водень. При цих кращих умовах реакції, стадія (б), як правило, завершується протягом від 0.5 до 5, зокрема від 1 до 4 годин. Необхідні аміни або спирти III доступні для придбання. Одержані аміди та складні ефіри піридинкарбонової кислоти І можуть бути очищені за допомогою стандартних методик, як, наприклад, шляхом кристалізації або хроматографії, зокрема, шляхом кристалізації. Однак, оскільки аміди та складні ефіри піридинкарбонової кислоти І у способі відповідно до винаходу одержують із високою чистотою, також можливо їх застосування для одержання амідів та складних ефірів (арилокси)піридинкарбонової кислоти IV без додаткового очищення. Аміди піридинкарбонової кислоти І можна також одержати зі складних ефірів піридинкарбонової кислоти І, які одержані на стадії (б) шляхом обробки проміжного продукту, одержаного на стадії (а), спиртом III, який визначений вище, шляхом обробки складних ефірів піридинкарбонової кислоти І аміном III, які визначені вище, у присутності основи: Реакцію складного ефіру піридинкарбонової кислоти І з аміном III звичайно проводять при температурі між температурою навколишнього середовища та температурою флегми реакційної суміші, переважно при температурі від 25°С до 140°С, особливо краще, від 50°С до 110°С, найбільш краще від 80°С до 100°С у присутності інертного розчинника та основи. Як правило, стадію (б) можна здійснювати при зниженому або підвищеному тиску, переважно її проводять при тиску навколишнього середовища. Цю реакцію відповідно до винаходу можна проводити при відсутності або в присутності розчинника, який сприяє реакції або, принаймні, не заважає її протіканню. Придатними розчинниками є неполярні розчинники, включаючи аліфатичні вуглеводні, такі як пентан, гексан, циклогексан і суміші С5-С8-алканів, ароматичні вуглеводні, такі як толуол, о-, м- та пксилол, галогеновані вуглеводні, такі як дихлорметан, хлороформ, 1,2-дихлоретан і хлорбензол. Особливу перевагу віддають аліфатичним вуглеводням, галогенованим вуглеводням і ароматичним вуглеводням. Також можливе застосування сумішей згаданих розчинників. Придатними основами є, звичайно неорганічні сполуки, такі як гідроксиди лужних і лужноземельних металів, такі як гідроксид літію, гідроксид натрію, гідроксид калію та гідроксид кальцію, оксиди лужних і лужноземельних металів, такі як оксид літію, оксид натрію, оксид кальцію та оксид магнію, так само як алкоголяти лужних і лужноземельних металів, такі як метилат натрію, етилат натрію, етилат калію, трет-бутоксид калію, трет-пентоксид калію та диметоксимагній, і, крім того, органічні 15 основи, такі як третинні аміни, такі як триметиламін, триетиламін, діізопропілетиламін і Nметилпіперидин, піридин, заміщені піридини, такі як колідин, лутидин, N-метилморфолін та 4диметиламінопіридин, а також біциклічні аміни. Кращими основами є алкоголяти металів, такі як метилат натрію або етилат натрію. Основи звичайно використовують у каталітичних кількостях, однак вони можуть також використовуватися в еквімолярних кількостях, у надлишку або, при необхідності, як розчинник. Звичайно, складний ефір піридинкарбонової кислоти І та амін III застосовують в еквімолярних кількостях. Може бути корисним використовувати надлишок III у перерахунку на складний ефір піридинкарбонової кислоти І. Перевагу віддають способу відповідно до даного винаходу, де складний ефір піридинкарбонової кислоти І обробляють аміном III у присутності основи, визначеної вище, і ароматичного вуглеводню як розчинник. У тому випадку, якщо аміди піридинкарбонової кислоти І приготовляють зі складних ефірів піридинкарбонової кислоти І шляхом обробки складних ефірів піридинкарбонової кислоти І аміном III, де R2 означає атом водню, у присутності основи, утворюютьсясолі формули 1.1: Перевагу віддають способу відповідно до даного винаходу, де складний ефір піридинкарбонової кислоти ІА де R1 означає С1-С6-алкільну групу; переважно ізопропільну групу, вводять у реакцію з аміном III, де R2 означає атом водню, з одержанням солей 1.1 А Реакцію амідів та складних ефірів піридинкарбонової кислоти І або їх солі з ароматичним спиртом V звичайно проводять при температурі від 0°С до температури кипіння реакційної суміші, переважно при температурі від 60°С до 200°С, особливо краще від 140°С до 180°С, в інертному органіч 90767 16 Іншим аспектом даного винаходу є спосіб одержання амідів та складних ефірів (арилокси)піридинкарбонової кислоти IV Де X означає О або NR2; R1 означає С1-С6-алкільну або арильну групу, де обидві групи можуть бути заміщені одним або декількома атомами галогену, нітро, ціано, С1-С6алкільними, С1-С6-галоалкільними або С1-С6алкоксильними групами; R2 означає атом водню або С1-С6-алкільну групу; R3 означає арильну групу, яка може бути заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6-алкокси або С1-С6-галоалкільними групами; який включає наступні стадії: (а) нагрівання суміші, яка складається по суті із трихлорметилпіридину II, визначеного вище, і від 1.0 до 1.5 еквівалентів концентрованої сірчаної кислоти, яке відрізняється тим, що трихлорметилпіридин II у вигляді рідини додають до концентрованої сірчаної кислоти при температурі від 110 до 160°С; (б) введення у реакцію проміжного продукту, одержаного на стадії (а), з аміном або спиртом III, визначеними вище, необов'язково в присутності розчинника і/або основи; та (в) введення у реакцію амідів та складних ефірів піридинкарбонової кислоти І або їх солі, одержаних на стадії (б), з ароматичним спиртом V, де R3 має наведені значення; необов'язково в присутності основи: ному розчиннику необов'язково в присутності основи. Придатними розчинниками є неполярні розчинники, включаючи аліфатичні вуглеводні, такі як пентан, гексан, циклогексан і суміші С5-С8-алканів, ароматичні вуглеводні, такі як толуол, о-, м- і п 17 90767 18 ксилол, галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і хлорбензол, так само як аміди, такі як диметилформамід, Ν,Νдиметилацетамід або N-метилпіролідон. Особливу перевагу віддають неполярним або полярним апротонним розчинникам, подібним аліфатичним вуглеводням, галогенованим вуглеводням, ароматичним вуглеводням або амідам, таким як диметилформамід, Ν,Ν-диметилацетамід або N-метилпіролідон або сумішам будь-яких із цих розчинників. Також можливе застосування сумішей згаданих розчинників. Придатними основами є, звичайно неорганічні сполуки, такі як гідроксиди лужних і лужноземельних металів, такі як гідроксид літію, гідроксид натрію, гідроксид калію та гідроксид кальцію, так само як алкоголяти лужних і лужноземельних металів, такі як метилат натрію, етилат натрію, етилат калію, трет-бутоксид калію, трет-пентоксид калію та диметоксимагній, і крім того, органічні основи, такі як третинні аміни, такі як триметиламін, триетиламін, діізопропілетиламін і N метилпіперидин, піридин, заміщені піридини, такі як колідин, лутидин, N-метилморфолін та 4диметиламінопіридин, а також біциклічні аміни. Особливу перевагу віддають алкоголятам металів або гідроксидам металів, таким як метилат натрію, етилат натрію, гідроксид натрію або гідроксид калію. Основи звичайно використовують в еквімолярних кількостях, однак вони можуть також використовуватися в надлишку або, при необхідності, як розчинник. Перевагу віддають способу відповідно до даного винаходу, де на стадії (в) аміди та складні ефіри піридинкарбонової кислоти І або їх сіль, одержані відповідно до даного винаходу, вводять у реакцію з ароматичним спиртом V без додаткового очищення. Перевагу також віддають способу відповідно до даного винаходу, де складний ефір піридинкарбонової кислоти ІА вводять у реакцію з ароматичним спиртом V у присутності основи з одержанням складних ефірів (арилокси)піридинкарбонової кислоти IVA: В особливо кращому варіанті відповідно до даного винаходу рідину, одержану на стадії (а) додають до від 5 до 15 еквівалентів спирту III, зокрема, ізопропанолу, при температурі між 20 і 85°С. Реакційну суміш, яку одержують, розбавляють ароматичним вуглеводнем і промивають водою. Одержаний розчин додають при температурі від 120 до 160°С до розчину солі ароматичного спирту V, який одержують шляхом взаємодії від 1.01 до 1.30 еквівалентів, зокрема, близько 1.22 еквівалентів, ароматичного спирту V, і розчину алкоголяту натрію, переважно від 1.01 до 1.30 еквівалентів алкоголяту натрію, зокрема 1.22 еквівалентів алкоголяту натрію, найбільш краще метилату натрію, у спирті; в ароматичному вуглеводні, зокрема, ксилолі, при 100-140°С. Переважно, надлишок спирту V, який залишився, відганяють до того, як складний ефір піридинкарбонової кислоти І додають до розчину солі ароматичного спирту V. Реакційну суміш, як правило, нагрівають до 140-160°С і залишають при цій температурі на 2-8 годин до завершення перетворення. У кращому варіанті даного винаходу складний ефір піридинкарбонової кислоти І або його сіль l.1, одержані відповідно до даного винаходу на стадії (б), вводять у реакцію з ароматичним спиртом V у присутності основи [стадія (в)], і одержаний складний ефір (арилокси)піридинкарбонової кислоти IV потім нагрівають із аміном III [стадія (г)] з одержанням амідів (арилокси)піридинкарбонової кислоти IV: Особливу перевагу віддають способу відповідно до даного винаходу, де на стадії (в) складний ефір піридинкарбонової кислоти ІА 19 90767 20 де R1 означає С1-С6-алкільну групу; переважно ізопропільну групу, вводять у реакцію з ароматичним спиртом V у присутності основи; і одержаний складний ефір (арилокси)піридинкарбонової кислоти IVA де R1 і R3 мають наведені значення, обробляють аміном III, визначеним вище, у присутності основи. У додатковому кращому варіанті даного винаходу складний ефір піридинкарбонової кислоти І вводять у реакцію з аміном III, де R2 означає водень, і одержані солі l.1 потім обробляють ароматичним спиртом V з одержанням амідів (арилокси)піридинкарбонової кислоти IV, де R2 означає водень: Особливу перевагу також віддають способу відповідно до даного винаходу, де складний ефір піридинкарбонової кислоти ІА без використання будь-якої додаткової основи. У додатковому особливо кращому варіанті відповідно до даного винаходу амін III, зокрема від 0.9 до 1.2 еквіваленти, переважно галогенований анілін, зокрема 4-фторанілін, додають до одержаної реакційної суміші при 120-150 С, зокрема, при 135°С; необов'язково з наступним додаванням розчину алкоголяту натрію, зокрема, розчину метилату натрію, переважно каталітичних кількостей, більш краще від 0.05 до 0.20 еквіваленти, головним чином переважно близько 0.13 еквіваленти, протягом від 10 до 60 хвилин з одночасною відгонкою застосовуваного спирту [стадія (г)]. Реакційну суміш перемішують протягом від 1 до 4 годин при температурі від 120 до 150°С, зокрема, близько 135°С, до завершення перетворення. У ще одному кращому варіанті даного винаходу, амід піридинкарбонової кислоти І або його сіль l.1, одержані відповідно до даного винаходу, обробляють ароматичним спиртом формули V: де R1 означає С1-С6-алкільну групу; переважно ізопропільну групу, вводять у реакцію з аміном III, де R2 означає атом водню, з одержанням солей l.1 А які потім обробляють ароматичним спиртом V з одержанням амідів (арилокси)піридинкарбонової кислоти IV.A, де R2 означає водень 21 Реакцію амідів піридинкарбонової кислоти І або l.1 з ароматичним спиртом V проводять при температурі від 0°С до 250°С, переважно при підвищеній температурі в діапазоні від 60 до 200°С, зокрема, від 140 до 180°С, найбільш краще, при 160°С. Особливу перевагу віддають способу відповідно до даного винаходу, де амід піридинкарбонової кислоти І або його сіль, одержані відповідно до даного винаходу, обробляють ароматичним спиртом формули V, де R3 означає фенільну групу, яка заміщена одним або декількома атомами галогену, нітро, ціано, С1-С6-алкільними, С1-С6-алкокси або С1-С6галоалкільними групами; зокрема, фенільну групу, яка є заміщеною С1С6-галоалкілом; переважно, фенільну групу, яка є заміщеною С1-С4-галоалкілом; найбільш краще, фенільну групу, яка є заміщеною 3-трифторметилом; необов'язково, у присутності основи та інертного розчинника. В особливо кращому варіанті відповідно до даного винаходу, розчин амідів піридинкарбонової кислоти І, зокрема N-(4-фторфеніл)-2-хлорпірид-6илінкарбоксаміду, в ароматичному вуглеводневому розчиннику, додають до суміші - основи, переважно гідроксиду лужного металу, зокрема, гідроксиду калію; - полярного апротонного розчинника, зокрема Ν,Ν-диметилацетаміду; та - ароматичного спирту формули VII, зокрема, 3-гідроксибензотрифториду; при температурі від 100 до 140°С. Одержану суміш нагрівають до температури від 140 до 200°С і ароматичний вуглеводень і воду, утворену протягом реакції, відганяють. Потім суміш перемішують при підвищеній температурі протягом від 1 до 4 годин. Розчинник відганяють при зниженому тиску. Залишок розбавляють неполярним розчинником, зокрема, сумішшю ароматичних і аліфатичних вуглеводнів і промивають водою або водним гідроксидом лужного металу. Водну фазу відокремлюють, а органічну фазу сушать. Кристали, які утворюються, збирають шляхом фільтрування, промивають і сушать при підвищеній температурі та зниженому тиску. Далі, з метою додатково полегшити розуміння суті винаходу, представлені ілюстративні приклади. Винахід не обмежується конкретними варіантами здійснення, описаними або проілюстрованими, але повною мірою обмежений прикладеною формулою винаходу. Приклад 1: N-(4-Фторфеніл)-2-хлорпірид-6илкарбоксамід В 98.1г (1 моль) концентрованої сірчаної кислоти (98 мас.%) протягом 3 годин при 135°С дозу 90767 22 ють 231г (1 моль) розплавленого 2-хлор-6трихлорметилпіридину (= нітрапірин = НП). Одержану суміш перемішують протягом 3 годин при 135°С. Утворюється грузла, розплавлена маса, яку додають до суміші 122.0г (1.1 моль) 4-фтораніліну, 202.0г (2 моль) триетиламіну та толуолу при температурі між 20 та 100°С протягом 45 хвилин. Одержану реакційну суміш нагрівають до температури між 80 і 120°С і перемішують протягом 1 години. Суміш обробляють 500мл соляної кислоти (7.5 мас.%) при 80°С і фази розділяють. Одержаний розчин N-(4-фторфеніл)-2-хлорпірид-6илінкарбоксаміду в толуолі використовують для одержання N-(4-фторфеніл)-2-(3-трифторметилфенокси)-пірид-6-илінкарбоксаміду (приклад 3) без додаткового очищення. Приклад 2: Ізопропіл-2-хлорпірид-6илкарбоксилат (СРАРЕ) В 510.2г (5.2 моль) концентрованої сірчаної кислоти (98 мас.%) протягом 3 годин при 135°С дозують 924г (4 моль) розплавленого НП. Одержану суміш перемішують протягом 3 годин при 135°С. Одержують грузлу розплавлену масу, яку дозують в 2145г (35.7 моль) ізопропанолу протягом 30 хвилин, починаючи з температури навколишнього середовища, яку далі піднімають до 60-65°С. Ізопропанол, який залишився, відганяють при зниженому тиску протягом 3 годин. Одержану суміш продуктів додають до суміші ксилолу та води. Після нагрівання до 50°С органічну фазу відокремлюють і промивають водою. Одержану органічну фазу висушують і концентрують шляхом відгонки ксилолу при зниженому тиску. Одержаний продукт (2070г) містить 34.1 мас.% ізопропіл-2-хлорпірид-6-илкарбоксилату в ксилолі, що відповідає виходу 88.4% у перерахунку на НП і використовують для одержання N-(4-фторфеніл)2-(3-трифторметилфенокси)-пірид-6илінкарбоксаміду без додаткового очищення (приклади 4 та 5). Приклад 3: N-(4-Фторфеніл)-2-(3трифторметилфенокси)-пірид-6-илінкарбоксамід До суміші 19.8г (0.300 моль) гідроксиду калію, 47.1г (0.291 моль) 3-гідрокси-бензотрифториду та 200мл Ν,Ν-диметилацетаміду при 120°С додають при перемішуванні розчин 13.5% (0.226 моль) N(4-фторфеніл)-2-хлорпірид-6-илінкарбоксаміду в толуолі, одержаний відповідно до прикладу 1. Одержану суміш нагрівають до 160°С і відганяють толуол та воду, яка утворилася протягом реакції. Потім суміш перемішують при 160°С протягом двох годин. Розчинник відганяють. Залишок розбавляють ксилолом і ізооктаном і промивають во 23 90767 дою при 80°С. Водну фазу відокремлюють, а органічну фазу сушать, розбавляють ізооктаном і охолоджують до 10°С протягом 4 годин. Кристали, які одержують, збирають шляхом фільтрування, промивають ізооктаном і сушать при 45°С і 100мбар. Одержують 73.2г (0.195 моль) N-(4фторфеніл)-2-(3-трифторметилфенокси)-пірид-6илінкарбоксаміду у вигляді білої твердої речовини із чистотою 97%, що відповідає загальному виходу 83.5% у перерахунку на амід, одержаний у прикладі 2. Приклад 4: Ізопропіл-2-(3трифторметилфенокси)-пірид-6-илінкарбонат Протягом 1 години на розчин 194.5г (1.24 еквіваленти) 3-гідроксибензотрифториду в 856г (8.31 еквівалентів) ксилолу при 120-110°С дозують 30мас.% розчин 212.5г метилату натрію в метанолі (1.22 еквіваленти NaOMe) при одночасній відгонці метанолу. Одержану суміш, яка містить фенолят, повільно нагрівають до 140°С, відганяючи метанол, що залишився. Розчин 194.5г (0.97 моль) ізопропіл-2хлорпірид-6-илкарбоксилату в ксилолі, одержаний у прикладі 2, дозують протягом 30 хвилин при 140°С у суміш, яка містить фенолят, з наступним додатковим нагріванням і відгонкою ксилолу при температурі реакційної суміші 150-155°С, яку утримують протягом 4-6 годин до завершення перетворення. Одержану реакційну суміш охоло Комп’ютерна верстка М. Ломалова 24 джують до 135°С і безпосередньо застосовують у прикладі 5. Приклад 5: N-(4-Фторфеніл)-2-(3трифторметилфенокси)-пірид-6-илінкарбоксамід До реакційної суміші із прикладу 4 при 135°С додають 111.1г (1.03 еквіваленти) 4-фтораніліну, з наступним дозуванням одержаної суміші в 30 мас.% розчин 24.3г (0.13 еквіваленти) метилату натрію протягом 30 хвилин з одночасною відгонкою метанолу. Реакційну суміш перемішують протягом 2 годин при 135°С до завершення перетворення. Реакційну суміш потім додають до суміші ізооктану та води при 70°С, що приводить до кінцевої температури 80°С. Водну фазу відокремлюють, органічну фазу промивають водою при 80°С. Одержаний розчин продукту висушують азеотропною відгонкою за Діном-Старком до кінцевої температури реакційної суміші 105-110°С. Розчин продукту охолоджують до 5°С протягом 5 годин, включаючи введення затравки при 68°С. Продукт, який закристалізувався, відфільтровують, промивають ізооктаном і сушать при 45°С і 100 мбар. Одержують 316.5г N-(4-фторфеніл)-2-(3трифторметилфенокси)-пірид-6-илінкарбоксамід у вигляді білої твердої речовини із чистотою 99.3%, що відповідає загальному виходу 75.8% у перерахунку на НП. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of pyridylcarboxylic amides and esters
Автори англійськоюBrink Monika, Knell Marcus, Wevers Jan Hendrik
Назва патенту російськоюСпособ получения амидов и сложных эфиров пиридинкарбоновой кислоты
Автори російськоюБринк Моника, Кнелль Маркус, Веверс Ян Хендрик
МПК / Мітки
МПК: C07D 213/81, C07D 213/79
Мітки: піридинкарбонової, способи, кислоти, ефірів, амідів, одержання, складних
Код посилання
<a href="https://ua.patents.su/12-90767-sposobi-oderzhannya-amidiv-i-skladnikh-efiriv-piridinkarbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Способи одержання амідів і складних ефірів піридинкарбонової кислоти</a>
Попередній патент: Програмно-апаратний контролер інтерфейсу
Наступний патент: Газовий пальник парогенератора
Випадковий патент: Двигун внутрішнього згоряння












