Лікарський засіб для лікування амілоїдозу, антрациклін та фармацевтична композиція
Номер патенту: 61875
Опубліковано: 15.12.2003
Автори: Барджотті Альберто, Суарато Антоніно, Лансен Жаклін, Карузо Мікеле, Баллінарі Даріо
Формула / Реферат
1. Применение антрациклина, выбранного из группы, включающей:
даунорубицин (A19);
доксорубицин (А20);
4-деметоксидаунорубицин (А21);
4-деметоксидоксорубицин (А22);
4'-эпидаунорубицин (А23);
4'-эпидоксорубицин (А24);
4'-деоксидаунорубицин (А25);
4'-деоксидоксорубицин (А26);
4'-йоддаунорубицин (А27);
4'-йоддоксорубицин (А28);
9-деоксидаунорубицин (А29);
9-деоксидоксорубицин (А30);
9-деацетилдаунорубицин (А31);
9-деацетил-9-деоксидаунорубицин (A32);
9-деацетил-9-гидроксиметилендаунорубицин (А33);
13 -дигидродаунорубицин (A34);
13-дигидродоксорубицин (A35);
13-дигидро-4-деметоксидаунорубицин (A36);
13-дигидро-4'-эпидаунорубицин (А37);
13-дигидро-4'-эпидоксорубицин (А38);
13-дигидро-4'-йоддоксорубицин (A39);
13-деоксодаунорубицин (А40);
N-трифторацетилдаунорубицин (A41);
N-трифторацетилдоксорубицин (А42);
N-трифторацетил-4-деметоксидаунорубицин (А43);
N-трифторацетил-4'-эпидаунорубицин (А44);
N-трифторацетил-4'-йоддаунорубицин (A45);
4'-деокси-4'-метансульфонатдаунорубицин (А46); и
4'-деокси-4'-метансульфонатдоксорубицин (А47),
или их фармацевтически приемлемых солей,
при лечении амилоидоза или для изготовления лекарственного средства для использования при лечении амилоидоза.
2. Применение по п.1, где указанное лекарственное средство представляет собой лекарственное средство для лечения AL амилоидоза, болезни Альцгеймера или синдрома Дауна.
3. Применение по любому из пп.1-2, где лекарственное средство представляет собой стандартную лекарственную форму, содержащую от 5 до 500 мг соединения или его фармацевтически приемлемой соли.
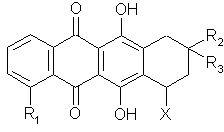
4. Антрациклин формулы А:
 , A
, A
где R1 обозначает
водород или гидрокси;
группу формулы OR4, где R4 представляет собой C1-С6-алкил, C5-C6-циклоалкил или CH2Ph с фенильным кольцом, необязательно замещенным 1, 2 или 3 заместителями, выбранными из F, Сl, Br, C1-С6-алкила, C1-С6-алкокси и СF3; или
группу формулы ОSО2R5, в которой R5 представляет собой C1-С6-алкил или Ph, необязательно замещенные 1, 2 или 3 заместителями, выбранными из галогена, такого как F, Сl или Br, и C1-С6-алкила;
R2 обозначает водород, гидрокси или OR4, как указано выше;
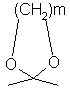
R3 обозначает водород, метил или группу формулы YСН2R6, в которой Υ обозначает СО, СН2, СНОН или группу формулы:
 ,
,
в которой m равно 2 или 3, и R6 обозначает
водород или гидрокси;
группу формулы ΝR7R8, в которой R7 и R8, каждый, независимо, выбран из:
а) водорода,
b) C1-С6-алкильной или C2-С6-алкенильной группы, необязательно замещенных гидрокси, CN, COR9, COOR9, CONR9R10, O(CH2)nNR9R10 (n равно 2-4) или NR9R10, в которых R9 и R10, каждый, независимо, выбран из водорода, C1-С12-алкила, C2-С12-алкенила и фенила, необязательно замещенных одним или несколькими заместителями, выбранными из C1-С6-алкила, C1-С6-алкокси, F, Br, Cl, СF3, ОН, NH2 и CN,
c) C3-С6-циклоалкила, необязательно замещенного COR9, COOR9 или ОН, где R9 имеет указанное выше значение,
d) фенил-C1-С4-алкила или фенил-C2-С4-алкенила, необязательно замещенных в фенильном кольце одним или несколькими заместителями, выбранными из C1-С6-алкила, C1-С6-алкокси, F, Br, Cl, СF3, ОН, NH2 и CN,
e) COR9, COOR9, CONR9R10, COCH2NR9R10, CONR9COOR10, SO2R9, в которых R9 и R10 имеют указанные выше значения, или R7 и R8 вместе с азотом образуют:
f) морфолиновое кольцо, необязательно замещенное C1-С4-алкилом или C1-С4-алкокси,
g) пиперазиновое кольцо, необязательно замещенное C1-С6-алкилом, C2-С6-алкенилом или фенилом, необязательно замещенными одним или несколькими заместителями, выбранными из C1-С6-алкила, C1-С6-алкокси, F, Br, Cl, СF3, ОН, NH2 и CN, и
h) пирролидиновое или пиперидиновое, или тетрагидропиридиновое кольцо, необязательно замещенные ОН, NH2, COOH, COOR9 или CONR9R10, где R9 и R10 имеют указанные выше значения, C1-С6-алкилом, C2-С6-алкенилом или фенилом, необязательно замещенными одним или несколькими заместителями, выбранными из C1-С6-алкила, C1-С6-алкокси, F, Br, Cl, СF3, ОН, NH2 и CN;
группу формулы OR4 или SR4, в которых R4 имеет указанное выше значение;
группу формулы O-Ph, где фенильное кольцо необязательно замещено нитро, амино или ΝR7R8, как указано выше; или
группу формулы В или С:
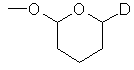 , B
, B
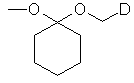 , C
, C
где
D представляет собой группу формулы COOR9 или CONR7R8, в которых R7, R8 и R9 имеют указанные выше значения; и
Χ представляет собой остаток сахара формулы X1 или Х2
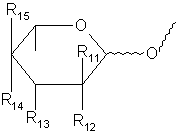 , X1
, X1
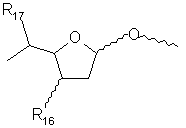 , X2
, X2
где
R11 и R12, оба, представляют собой водород, или один из R11 и R12 является водородом, а другой представляет собой F, Cl, Br или I;
R13 представляет собой водород, гидрокси, C1-С4-алкокси, амино, NHCOCF3, N=C(C6H5)2, NHCOR9, NHCONR7R8 или группу формулы Ε или F
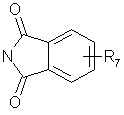 , E
, E
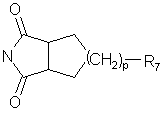 , F
, F
в которых R7, R8 и R9 имеют указанные выше значения; и
p равно 0 или 1;
R14 и R15 обозначают водород, или один из R14 или R15 обозначает водород, а другой обозначает ОН, F, Cl, Br, I или группу формулы OSO2R5, где R5 имеет указанное выше значение;
R16 обозначает СН2ОН или R13, как указано выше;
R17 обозначает F, Cl, Br, I или группу формулы OSO2R5, в которой R5 имеет указанное выше значение;
и его фармацевтически приемлемых солей;
при условии, что соединение формулы А не является 4'-йод-4'-деоксидоксорубицином, и при условии, что:
X1 не является остатком, в котором оба R14 и R15 являются атомами водорода или один из R14 и R15 представляет собой гидрокси, F, Br, Cl или CF3SO2O-, и R13 является водородом, гидрокси, амино, NHCOCF3 или NCPh2, когда R3 является водородом, группой формулы CH3, YCH3, CH2CH2OR’4, COCH2NR’7R’8, COCH2OR’4 или YCH2OH, где Y указан выше, R’4 обозначает фенил, бензил, С1-С6-алкил или С5-С6-циклоалкил, R’7 и R’8, каждый, независимо, обозначает водород, С1-С12-алканоил, или, взятые вместе, образуют морфолиновый, пиперазиновый или пиперидиновый остаток;
X1 не является остатком, в котором оба R11 и R12 являются атомами водорода, R13 обозначает амино, иR14 обозначает йод, когда R1 представляет собой водород или метокси, R2 представляет собой гидрокси и R3 представляет собой CОСH3, CH2CH3, CH2СНОH, СОСН2ОН или СНОНСН2ОН,
X не является X2, когда R3 представляет собой CОСH2ОН или CОCH3;
R13 не является NHCOCF3, когда R3 представляет собой CH2CH3, CОСH2ОН или CОCH3.
5. Антрациклин формулы А по п. 4 или его фармацевтически приемлемая соль для применения при лечении амилоидоза.
6. Фармацевтическая композиция для лечения амилоидоза, содержащая в качестве активного ингредиента эффективное количество антрациклина по любому из пп.1 или 4 или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем.
Текст
1 Применение антрациклина, выбранного из группы, включающей даунорубицин (А19), доксорубицин (А20), 4-деметоксидаунорубицин (А21), 4-деметоксидоксорубицин (А22), 4'-эпидаунорубицин (А23), 4'-эпидоксорубицин (А24), 4'-деоксидаунорубицин (А25), 4'-деоксидоксорубицин (А26), 4'-йоддаунорубицин (А27), 4'-йоддоксорубицин (А28), 9-деоксидаунорубицин (А29), 9-деоксидоксорубицин (АЗО), 9-деацетилдаунорубицин (А31), 9-деацетил-9-деоксидаунорубицин (А32), 9-деацетил-9-гидроксиметилендаунорубицин (АЗЗ), 13 -дигидродаунорубицин (А34), 13-дигидродоксорубицин (А35), 13-дигидро-4-деметоксидаунорубицин (А36), 13-дигидро-4'-эпидаунорубицин (А37), 13-дигидро-4'-эпидоксорубицин (А38), 13-дигидро-4'-йоддоксорубицин (А39), 13-деоксодаунорубицин (А40), N-трифторацетилдаунорубицин (А41), N-трифторацетилдоксорубицин (А42), М-трифторацетил-4-деметоксидаунорубицин (А43), |\|-трифторацетил-4'-эпидаунорубицин (А44), |\|-трифторацетил-4'-йоддаунорубицин (А45), 4'-деокси-4'-метансульфонатдаунорубицин (А46), и 4'-деокси-4'-метансульфонатдоксорубицин (А47), или их фармацевтически приемлемых солей, при лечении амилоидоза или для изготовления лекарственного средства для использования при лечении амилоидоза 2 Применение по п 1, где указанное лекарственное средство представляет собой лекарственное средство для лечения AL амилоидоза, болезни Альцгеймера или синдрома Дауна 3 Применение по любому из пп 1-2, где лекарственное средство представляет собой стандартную лекарственную форму, содержащую от 5 до 500 мг соединения или его фармацевтически приемлемой соли 4 Антрациклин формулы А О он где Ri обозначает водород или гидрокси, группу формулы OR4, где R4 представляет собой Сі-Сб-алкил, Сб-Сє-циклоалкил или СНгРп с фенильным кольцом, необязательно замещенным 1, 2 или 3 заместителями, выбранными из F, CI, Вг, Сі-Сб-алкила, Сі-Сє-алкокси и CF3, или группу формулы OSO2R5, в которой Rs представляет собой Сі-Сб-алкил или Рп, необязательно замещенные 1, 2 или 3 заместителями, выбранными из галогена, такого как F, CI или Вг, и Сі-Сєалкила, R2 обозначает водород, гидрокси или OR4, как указано выше, R3 обозначает водород, метил или группу формулы YCH2R6, в которой Y обозначает СО, СЬЬ, СНОН или группу формулы Ю 00 (О 61875 (CH2)m О. P в которой m равно 2 или 3, и F?6 обозначает водород или гидрокси, группу формулы NR7R8, в которой R7 и Rs, каждый, независимо, выбран из a) водорода, b) СгСб-алкильной или Сг-Сє-алкенильной группы, необязательно замещенных гидрокси, CN, CORg, COORg, CONR9R10, 0(CH 2 ) n NR 9 Rio (n равно 2-4) или NRgRio, в которых Rg и Rio, каждый, независимо, выбран из водорода, Сі-Сі2-алкила, С2-С12алкенила и фенила, необязательно замещенных одним или несколькими заместителями, выбранными из Сі-Сб-алкила, Сі-Сє-алкокси, F, Br, СІ, CF 3 , OH, NH2HCN, c) Сз-Сб-циклоалкила, необязательно замещенного CORg, COORg или ОН, где Rg имеет указанное выше значение, d) фенил-Сі-С4-алкила или фенил-С2-С4-алкенила, необязательно замещенных в фенильном кольце одним или несколькими заместителями, выбранными из Сі-Сб-алкила, Сі-Сє-алкокси, F, Br, СІ, CF 3 , OH, NH2HCN, Є) CORg, COORg, CONR9R10, COCH2NR9R10, CONRgCOORio, SO2Rg, в которых Rg и R-іо имеют указанные выше значения, или R7 и Rs вместе с азотом образуют f) морфолиновое кольцо, необязательно замещенное СгС4-алкилом или СгС4-алкокси, g) пиперазиновое кольцо, необязательно замещенное Сі-Сб-алкилом, Сг-Сє-алкенилом или фенилом, необязательно замещенными одним или несколькими заместителями, выбранными из СіСб-алкила, Сі-Сб-алкокси, F, Br, Cl, CF3, OH, NH2 и CN, и h) пирролидиновое или пиперидиновое, илитетрагидропиридиновое кольцо, необязательно замещенные ОН, NH 2 , COOH, COORg или CONRgRio, где Rg и Rio имеют указанные выше значения, d Сє-алкилом, Сг-Сб-алкенилом или фенилом, необязательно замещенными одним или несколькими заместителями, выбранными из Сі-Сє-алкила, Сі-Сб-алкокси, F, Br, Cl, CF 3 , OH, NH 2 и CN, группу формулы OR4 или SR4, в которых R4 имеет указанное выше значение, группу формулы O-Ph, где фенильное кольцо необязательно замещено нитро, амино или NR7R8, как указано выше, или группу формулы В или С где D представляет собой группу формулы COORg или CONR7R8, в которых R7, Rs и Rg имеют указанные выше значения, и X представляет собой остаток сахара формулы Х1 или Х2 где Rn и R12, оба, представляют собой водород, или или один из Rn и R12 является водородом, а другой представляет собой F, Cl, Br или I, Ri3 представляет собой водород, гидрокси, С1-С4алкокси, амино, NHCOCF3, N=C(C 6 H 5 )2, NHCORg, NHCONR7R8 или группу формулы Е или F О О ,Е ^ ,F в которых R7, Rs и Rg имеют указанные выше значения, и р равно 0 или 1, R H и R15 обозначают водород, или один из Rn или Ri5 обозначает водород, а другой обозначает ОН, F, СІ, Вг, І или группу формулы OSO2R5, где Rs имеет указанное выше значение, Ri6 обозначает СНгОН или R13, как указано выше, Ri7 обозначает F, СІ, Вг, І или группу формулы OSO2R5, в которой Rs имеет указанное выше значение, и его фармацевтически приемлемых солей, при условии, что соединение формулы А не является 4'-йод-4'-деоксидоксорубицином, и при условии, что Х1 не является остатком, в котором оба Rn и R15 являются атомами водорода или один из Rn и R15 представляет собой гидрокси, F, Br, CI или CF3SO2O-, и R13 является водородом, гидрокси, амино, NHCOCF3 или NCPh2, когда R3 является водородом, группой формулы СНз, УСНз, CH 2 CH 2 OR' 4 , COCH 2 NR' 7 R'8, COCH 2 OR' 4 или YCH2OH, где Y указан выше, RU обозначает фенил, бензил, СгСб-алкил или Сб-Сє-циклоалкил, RV и R's, каждый, независимо, обозначает водород, Сі-Сі2-алканоил, или, взятые вместе, образуют морфолиновый, пиперазиновый или пиперидиновый остаток, Х1 не является остатком, в котором оба Rn и R12 являются атомами водорода, R13 обозначает амино, и R H обозначает йод, когда Ri представляет собой водород или метокси, R2 представляет собой гидрокси и R3 представляет собой СОСНз, СН 2 СН 3 , СН 2 СНОН, СОСН 2 ОН или СНОНСН 2 ОН, X не является Х2, когда R3 представляет собой СОСН 2 ОН или СОСНз, Ri3 не является NHCOCF3, когда R3 представляет собой СН 2 СН 3 , СОСН 2 ОН или СОСНз 5 61875 5 Антрациклин формулы А по п 4 или его фармаингредиента эффективное количество антрацикцевтически приемлемая соль для применения при лина по любому из пп 1 или 4 или его фармацевлечении амилоидоза тически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем 6 Фармацевтическая композиция для лечения амилоидоза, содержащая в качестве активного Данное изобретение касается лечения амилоидоза, новых соединений для такого лечения, способов их получений и содержащих их фармацевтических композиций Связь между амилоидозом, смертью клеток и потерей функции ткани, по-видимому, имеет отношение к различным типам заболеваний, в том числе нейродегенеративных заболеваний Поэтому предотвращение образования амилоида и/или индуцирование деградации амилоида могут быть важными терапевтическими инструментами для всех патологических нарушений, связанных с амилоидозом, в том числе AL амилоидозом и нейродегенеративными заболеваниями типа болезни Альцгеймера Более конкретно, настоящее изобретение относится к использованию при изготовлении лекарственного средства для применения в лечении амилоидоза антрациклина формулы А О R, О где Ri обозначает водород или гидрокси, группу формулы OR4 в которой R4 представляет собой Сі-Сб-алкил, Cs-Сб-циклоалкил или CbbPh с фенильным (Рп) кольцом, необязательно замещенным 1, 2 или 3 заместителями, выбранными из F, СІ, Вг, Сі-Сб-алкила, Сі-Сє-алкокси и CF3 или группу формулы OSO2R5 в которой Rs обозначает Сі-Сб-алкил или Рп, необязательно замещенный 1, 2 или 3 заместителями, выбранными из галогена, такого как F, CI или Вг, и Сі-Сєалкила, R2 обозначает водород, гидрокси или OR4, где R4 имеет указанное выше значение, R3 обозначает водород, метил или группу формулы YCH2R6 в которой Y обозначает СО, СЬІ2, СНОН или группу формулы алкила или Сг-Сє-алкенила, необязательно замещенного гидрокси, CN, CORg, COORg, CONR9R10, 0(CH2)nNR9Rio (n обозначает 2-4) или NRgRio, в которой Rg и R-іо каждый независимо, выбран из водорода, Сі-Сі2-алкила С2-С12алкенила или фенила, необязательно замещенного одним или несколькими, например 1, 2 или 3, заместителями, выбранными из Сі-Сє-алкила d-Сб-алкокси, F, Br, CL, CF3, ОН, NH2 или CN, с) Сз-Сб-циклоалкила, необязательно замещенного CORg, COORg или ОН, где Rg имеет указанное выше значение, d) фенил-Сі-С4-алкила или фенил-С2-С4-алкенила, необязательно замещенных в фенильном кольце одним или более, например, 1, 2 или 3, заместителями, выбранными из Сі-Сб-алкила, Сі-Сє-алкокси, F, Br, CI, CF3 ОН, NH2 или CN, и е) CORg, COORg, CONRgRio, COCH2NR9Rio CONRgCOORio или SO2Rg, где Rg и R-іо имеют указанные выше значения, или R7 и Rs вместе с азотом образуют f) морфолиновое кольцо, необязательно замещенное dС4алкилом или СгС4-алкокси, g) пиперазиновое кольцо, необязательно замещенное С-і-Сєалкилом, Сг-Сб-алкенилом или фенилом, необязательно замещенным одним или более, например 1, 2 или 3, заместителями, выбранными из Сі-Сб-алкила, Сі-Сє-алкокси, F, Br, CI, CF3, ОН, NH2 или CN, и h) пирролидиновое, пиперидиновое или тетрагидропиридиновое кольцо, необязательно замещенное ОН, NH2, COOH, COORg или CONRgRio, где Rg и R-іо имеют указанные выше значения, Сі-Сє-алкилом, Сг-Сє-алкенилом или фенилом, необязательно замещенным одним или более, например 1, 2 или 3, заместителями, выбранными их Сі-Сє-алкила, С-і-Сєалкокси, F, Br, CI, CF3, ОН, NH2 или CN, группу формулы OR4 или R4 в которых R4 имеет указанное выше значение, группу формулы O-Ph где фенильное кольцо необязательно замещено нитро, амино или NR7R8, как указано выше, или группу формулы В или С О. ,D в которой m обозначает 2 или 3, а R6 обозначает водород или гидрокси, группу формулы NR7R8, в которой R7 и Rs, каждый независимо, выбраны из а) водорода, Ь) Сі-Сє где D обозначает группу формулы COORg или CONR7R8, в которых R7, Rs и Rg имеют указанные выше значения, и X обозначает сахарный остаток формулы Х1 или Х2 8 61875 Х2 где Rn и R12 оба представляют собой водород или один из Rn и R-I2 является водородом, а другой является F, CI, Вг или I, Ri3 обозначает водород, гидрокси, С1-С4алкокси, амино, NHCOCF3, N=C(C 6 H 5 )2, NHCORg, NHCONR7R8 или группу формулы Е или F в которых R7, Rs и Rg имеют значения, указанные выше, и р обозначает 0 или 1, R-I4 и R-I5 обозначают водород или один из Ri4 и R-I5 является водородом, а другой является ОН, F, СІ, Вг, І или группой формулы OSO2R5 где Rs имеет указанное выше значение, R-іб обозначает СНгОН или R13 как указано выше, Ri7 обозначает F, СІ, Вг, І или группу формулы OSO2R5 где имеет указанное выше значение, и их фармацевтически приемлемых солей, при условии, что соединение формулы А не является 4'-иод-4'дезоксидоксорубицином^1=ОСНз, R2=OH, R3=COCH2OH, X=Xi, Rii=Ri2=Ri5=H, Ri 3 =NH 2 и Ru= I) По следующему аспекту настоящего изобретения предложены новые антрациклины формулы А, как указано выше, где Х1 не является остатком, в котором оба Ru и R-I5 являются атомами водорода или один из Ru или R15 является гидрокси и R13 является аминогруппой, когда R3 является группой формулы YCH3, COCH2NR7R8, COCH2R4 или YCH2OH, где Y имеет указанное выше значение, R4 обозначает фенил, бензил, СгСб-алкил или Сб-Сєциклоалкил, R7 и Rs, каждый независимо, обозначают водород, Сі-Сі2-алканоил или, взятые вместе, образуют морфолиновый, пиперазиновый или пиперидиновый остаток, Х1 не является остатком, в котором Rn и R12 оба являются атомами водорода, R-із обозначает аминогруппу и Ru обозначает йод, когда Ri представляет собой метокси, R2 представляет собой гидрокси и R3 представляет собой СОСН2ОН Каждая алкильная, алкокси или алкенильная группа может быть группой с прямой или разветвленной цепью Сі-Сі2-алкильная группа, предпочтительно, является СгСб-алкильной группой С-і-Сєалкильная группа представляет собой предпочтительно СгС4алкильную группу С-і-Сє алкильная группа предпочтительно представляет собой метил, этил, н-пропил, изопропил, н-бутил, третбутил, вторбутил или н-пентил С1-С4алкильная группа представляет собой, предпочтительно метил, этил, н-пропил, изопропил, нбутил, третбутил или вторбутил Сз-Сб-циклоалкильная группа представляет собой предпоч-тительно Сб-Сб-циклоалкильную группу Сб-Сб-циклоалкильная группа представляет собой предпочтительно/ циклопентил или циклогексил Пептидильный остаток может содержать до 6, например от 1 до 4, аминокислотных остатков Подходящими остатками являются Glu, Ala, Phe, Leu, Glu-Phe, Leu-Glu, Val-Ala, Phe-Ala, Leu-Phe, Phe-Leu-Glu, Phe-Phe-Leu, Leu-Leu-Glu, Phe-TyrAla, Phe-Glu-Phe, Phe-Leu-Glu-Phe, Glu-Phe-LeuGlu, Glu-Phe-Leu-Glu В настоящем изобретении Ri предпочтительно представляет собой водород или метокси R2 предпочтительно является гидрокси R3 предпочтительно является группой формулы YCH2R6 в которой Y обозначает СО или группу формулы и R6 обозначает водород или гидрокси, группу формулы NR7R8, в которой R7 и Rs независимо выбраны из a) водорода, b) СгС4-алкила, c) фенил-С1-С2-алкила, необязательно замещенного в фенильном кольце одной или двумя метоксигруппами, и d) COCH2NR9R10 в которой Rg и R-іо представляют собой метильные группы, или R7 и Rs вместе образуют e) морфолиновое кольцо или f) пиперазиновое кольцо, д) тетрагидропиридиновое кольцо, группу формулы О-Рп, в которой фенильное (Рп) кольцо необязательно замещено NR7R8, как описано выше, или группу формулы О D где D обозначает группу формулы CONR?Rs где NR7R8 имеет указанное выше значение, и X обозначает сахарный остаток формулы XI где Rn и R-I2 обозначают водород, или один из Rn или R12 является водородом, а другой I, 61875 Ri3 обозначает амино, NHCOCF3, N=C(C6H5)2 или группу формулы 10 NHCOCH2 N(CH3)2], Rii=Ri2=Ri5=H, Ri3=HCOCF3, Ri4=l A5 13-деоксо-13-этилендиокси-14-N(морфолино)-3'-г\І-трифторацетил-4'иоддауномицин R2=OK, R3=C(OCH2CK2O}CH2'V где RM и R15 обозначают водород, или один из R H или R15 является водородом, а другой является ОН, I или OSO2CH3 Настоящее изобретение относится к солям тех соединений формулы А, которые имеют образующие соль группы, в частности соли соединений, имеющих карбоксильную группу, основную группу(например, аминогруппу) Эти соли являются, в частности, физиологически приемлемыми солями, например солями щелочных металлов или щелочноземельных металлов(например солями натрия, калия, лития, кальция и магния), солями аммония, солями с подходящими органическим амином или аминокислотой (например, солями аргинина, прокаина) и солями добавления кислот, образованными с подходящими органическими или неорганическими кислотами, например соляной кислотой, серной кислотой, карбоновой кислотой и сульфоорганическими кислотами(например, уксусной, трифторуксусной, п-толуолсульфоновой кислотой) Настоящее изобретение включает в себя все возможные стереоизомеры, а также их рацемические или оптически активные смеси Конкретные примеры предпочтительных соединений по настоящему изобретению перечислены ниже А1 14-г\1-(морфолино)-3'-г\1-трифторацетил4'-иоддауномицин А2 14-г\1-(3,4-диметоксибензиламино)-3'-г\1трифторацетил-4'-иоддауномицин Ri=OCH3, R2=OH, R3=COCH2NHCH2[C6H3(OCH3)2], Rn=Ri2=Ri5=H, Ri3=NHCOCF3 R14=l A3 14-O-[2-(1пиперазинил)карбонилтетрагидропиран-6-ил]-3'|\|-трифторацетил-4'-иоддауномицин О А6 13-деоксо-13-этилендиокси-14-[пдиметиламинокарбониламино)-фенилокси]-3'-І\Ітрифторацетил-4'-иоддауномицин Ri=OCH3, R2=OH, R3=C(OCH2CH2O)CH2OС6Н4[п NHCOCH2 N(CH3)2], Rn=Ri2=Ri5=H, Ri3=HCOCF3, R14=l A7 13-дигидро-14-М-(морфолино)-3'-Ытрифторацетил-4'-иоддауномицин А8 14-М-(морфолино)-3'-М-фталоил-4'иоддауномицин А9 14-г\І-(3,4-диметоксибензиламино)-3'-г\Іфталоил-4'-иоддауномицин Ri=OCH3, R2=OH R3=COCH2N НСН2[С6Н3(ОСН2)2,] R3=COCH2N Ri=OCH3, R2=OH HCH2(C6H3(OCH3)2 14-О-[2-(1 -пиперазинил)A10 карбонилтетрагидропиран-6-ил]-3'-М-фталоил-4'иоддауномицин R.-GCH,. B2-OH, Riі—Ri2~Ri5~H, Ri3— MHCOCF 3 , R14— I A4 14-[n (диметиламинокарбониламино)фенилокси]-3'-І\Ітрифторацетил-4'-иоддауномицин Ri=OCH3, R2=OH, R3=COCH2O-C6H4[n A11 14-М-(морфолино)-3'-М-трифторацетил4'-метансульфонатдауномицин 11 Б;3=СОСНЭ Л/ 6 1 8 7 5 О, R11=R.12=%5=H, А12 14-О-[2-(1 -пиперазинил)карбонилтетрагидропиран-6-ил]-3-І\Ітрифторацетил-4'-метансульфонатдауномицин 1 2 указанные выше значения, при условии, что R7 и Rs не являются группами CORg, CONRgRio, CONRgCOORio, или SO2R9 в которых Rg и Rm имеют указанные выше значения, заключается в следующем 1) превращение соединения формулы G R,-OCHJt Йг-ОН, Rn=Ri2=R15=H, Ri4=OSO 2 CH 3 Ri3=NHCOCF 3, А13 14-[п(диметиламинокарбониламино)фенилокси]-3'-І\Ітрифторацетил-4'-метансульфонатдауномицин Ri=OCH3, R2=OH, R3=COCH2O-C6H4[n NHCOCH2N(CH3)2], Rn—Ri2—R15—H, Ri3— HCOCF3, R14—Оо02СНз A14 14-М-(морфолино)-3'-г\І-фталоил-4'метансульфонатдауномицин где R6 обозначает водород, R-i, R2, X имеют указанные выше значения, при условии, что в G не присутствуют остатки алкенила, и в сахарном остатке X R-із не является гидрокси, когда один из остальных заместителей X является гидрокси, в соответствующее 14бромпроизводное, затем 2) взаимодействие полученного бромпроизводного формулы Н О А15 3'-І\І-дифенилметилен-4'эпидаунорубицин Ri=OCH3, R2=OH, R3=COCH3, Rii=Ri2=Ri4=H, Ri3=NC(C6H5)2, R15=OH A16 3'-І\І-дифенилметилен-4'иодоксорубицин Ri=OCH3, R2=OH, R3=COCH2OH, R11-R12-R15-H, Ri3-C(C6Hs)2, R H = I A17 14-М-(морфолино)-3'-І\Ідифенилметилен-4'-иоддауномииин N' A18 4-деметокси-2'-иоддаунорубицин Ri = H, R2—OH, R3—COCH3, R11—R15— H, Ri2—I, Ri3=NH2, Ri4=OH Соединения формулы А могут быть приготовлены, в зависимости от природы заместителей, исходя из известных антрациклинов, подходящими химическими модификациями агликоновой или сахарной части молекулы или обеих частей молекулы или соединением антрациклинонов с сахарами Способами получения соединений формулы А и их фармацевтически приемлемых солей являются следующие способы (і) Предпочтительный способ получения соединений формулы А, где R3 представляет собой группу формулы COCH2NR7R8 где R7 и Rs имеют ОН в которой R-i, R2 и X имеют данные выше значения, с подходящим амином формулы NHR7R8, R7 и Rs имеют данные выше значения, при условии, что R7 и Rs не являются группами COR9, CORgRio, CONRgCOORio или SO2R9 описанными выше, и, если желательно, превращение полученного соединения формулы А в его фармацевтически приемлемую соль (м) В другом примере соединения А, описанные в (і), могут далее быть преобразованы в другие антрациклины формулы А, в которых один Йди оба R7 и Rs обозначают группу формулы CORg или SO2Rg где Rg имеет данное выше значение, путем взаимодействия 14аминопроизводного формулы А, описанного в (і), при условии, что один или оба R7 и Rs обозначают атом водорода, с ацильным производным формулы HalCORg или HalSO2Rg где Hal представляет собой галоген, a Rg имеет указанное выше значение, и, если желательно, превращения полученного указанного соединения формулы А в его фармацевтически приемлемую соль (їм) В другом примере предпочтительный способ получения соединений формулы А, где R3 представляет собой группу формулы В или С, указанные выше, при условии, что Ri и заместители сахарного остатка X не являются первичными гидроксигруппами, заключается в следующем 1) взаимодействие соединения, представленного формулой G, в которой R6 обозначает 61875 13 гидрокси, a Ri и X указаны выше, с соединением формулы В1 или С1 ь\ где D имеет указанное выше значение, и, если желательно, удаление защиты у защищенных гидроксигрупп, и, если желательно, превращение полученного указанного соединения формулы А в его фармацевтически приемлемую соль (iv) В другом примере предпочтительный способ получения соединений формулы А, где R3 представляет собой CHOHCH2R5, заключается в восстановлении соединения формулы А, в которой R3 обозначает COCH2R6 где R6 имеет указанное выше значение, при условии, что в А не присутствуют дополнительные кетогруппы, и, если желательно, превращение полученного указанного соединения формулы А в его фармацевтически приемлемую соль (v) В другом примере предпочтительный способ получения соединений формулы А, где R3 является группой формулы CH2CH2R6, включает 1) преобразование соединения формулы А, в котором R3 является COCH2R6, при условии, что в А не присутствуют дополнительные кетогруппы, в 13-(замещенный)бензолсульфонилгидразон, предпочтительно, 13(п-фтор)бензолсульфонилгидразон, затем 2) восстановление его в условиях, способных сохранять гликозидную связь, и, если желательно, превращение полученного указанного соединения формулы А в его фармацевтически приемлемую соль (vi ) В другом примере способ получения соединений формулы А, в которой Rn и R12 являются атомами водорода, включает 1) конденсацию агликона формулы К где R-і, R2, R3 имеют указанные выше значения, при условии, что R-і, R2, R3 не являются группами, несущими первичные или вторичные гидроксигруппы, с производным сахара формулы L1 или L2 LI L2 14 где R-I8 обозначает подходящую отщепляемую группу, такую как атом галогена, например атом хлора, или активированный эфирный остаток, такой как OCOCF3 или OCO(n-NO2C6H5), R19, R20 обозначают атомы водорода, R21 обозначает водород, СгС4-алкокси, остаток эфира, такой как OCOCF3 или ОСО(пNO2C6H5) или группу NHCOCF3, R22, R23 оба обозначают водород или один из R22 или R23 является водородом, а другой является эфирным остатком, таким как OCOCF3 или OCO(n-NO2C6H5) или группой NHCOCF3, R24 обозначает CH2OCOCF3, или имеет то же значение, что и R21 и выше, и R25 обозначает OCOCF3 или ОСО(пNO2C6H5), затем (vi) удаление защиты амино- и гидроксигрупп, и, если желательно, превращение полученного соединения формулы А в его фармацевтически приемлемую соль (VII) в другом примере предпочтительный способ получения соединений формулы А, в которой R-із представляет собой Е или F, предусматривает 1) взаимодействие антрациклина формулы А, как указано выше, который имеет только первичную аминогруппу, с галогенацилпроизводным формулы Е1 или F1 ЕІ F1 где R7 имеет указанное выше значение, Hal обозначает атом галогена, и R-I7 является алкоксиостатком, предпочтительно, этокси, и, если желательно, 2) обработку полученного моноаминоацилпроизводного основанием с образованием групп формул Е или F, и, если желательно, превращение полученного указанного соединения формулы А в его фармацевтически приемлемую соль Соединения формулы А, как указано в (і), могут быть получены, как описано в DE-A-2557537, например взаимодействием соединения формулы Н, как указано выше, полученного из соединения G согласно DE-A-1197874, с 1 - 1,2 эквивалентами подходящего амина формулы NHR7R8, где R7 и Rs указаны выше, при условии, что R7 и Rs не являются группой формул CORg, CONR9R10, CONR9COOR10 или SO2R9, как указано выше, в сухом полярном растворителе, таком как ацетон или диметилформамид, при температуре приблизительно 0° - 30°С, предпочтительно при комнатной температуре, в течение 4 - 24 часов, и, если желательно, превращением полученного указанного соединения формулы А в его фармацевтически приемлемую соль, предпочтительно с безводным хлористым водородом в метаноле 61875 16 15 Соединения формулы А, описанные в (м), мотаком как оксид ртути, в присутствии конденсигут быть получены путем взаимодействия соедирующего агента, такого как оксид ртути, бромид нения формулы А, указанного в (і), с ацилпроизртути, и молекулярных сит, описанных в DE-Aводным формулы HalCORg или HalSO2Rg, где Hal 2525633 Альтернативный способ предусматриобозначает галоген, a Rg имеет указанное выше вает конденсацию антрациклинона формулы К с значение, в сухом полярном растворителе, таком производным галогенированного сахара формукак ацетон или диметилформамид, при темпералы L1 или L2, описанным выше, в сухом аполяртуре приблизительно 0° - 30°С, предпочтительно ном растворителе, таком как метиленхлорид, с при комнатной температуре, в течение 4 - 24 чатрифторметансульфонатом серебра, растворенсов ным в этиловом эфире, при температуре 0° 25°С в течение 1 - 6 часов, как описано в ВЕ-АСоединения формулы А, как указано в (ш), 842930 могут быть получены, как описано в Wo 92/10212 и Wo 92/02255, например взаимодействием анСоединения формулы А, описанные в (vn), трациклина, описанного в (ш) (1), с производными могут быть получены взаимодействием антраформулы В1 или С1 в апротонном растворителе, циклина, имеющего только первичную аминотаком как метиленхлорид, в присутствии кислотгруппу, с галогенпроизводным формулы Е1 или ного катализатора, такого как п-толуолсульфонат F1, описанным выше, в органическом растворипиридиния, при температуре 10° - 30°С, предпочтеле, таком как тетрагидрофуран или диметилтительно при комнатной температуре, в течение формамид, при 0°С-комнатной температуре в 3 - 24 часов, и, если желательно, превращением течение 1 - 24 часов Моноацилпроизводное обполученного указанного соединения формулы А рабатывают затем конденсирующим агентом, в фармацевтически приемлемую соль, предпочтаким как тетрабутиламмонийфторид, с получетительно с безводным хлористым водородом в нием(циклический ацил)антрациклина метаноле, или гидролизом эфирного производноДругие антрациклины формулы А можно пого разбавленным водным гидроксидом натрия лучить аналогичным образом, исходя из известных соединений при помощи известных процеСоединения формулы А, описанные в (iv), ДУР могут быть получены восстановлением антрациклинов формулы А, указанных в (iv), в воде Например, следующие соединения известны или в одном или более органических раствории могут быть представлены той же формулой А, телях, в зависимости от природы соединения, в которой X обозначает сахар формулы Х1 или при помощи микробного восстановления даунорубицин (А19 Ri = ОСН3, R2=OH, Например, водорастворимые антрациклины восR3—СОСН3, R11—Ri2~Ri5~H, R13—NH2, Ri4~ОН); станавливают в воде при рН 8-9, предпочтительдоксорубицин (А20 R1 = ОСН3, R =ОН, но при рН 8,5, в присутствии восстановителя, R3=COCH2OH, Rii=Ri2=Ri5=H, Ri 3 =NH 2 , R U =OH) ; такого как боргидрид натрия, при температуре от 4-деметоксидаунорубицин (А21 Ri=H, 0°С до комнатной температуры, в течение 1 - 1 0 R2—OH, R3—COCH3, R11—R12—R15—H, R13— NH2, минут, как описано в Gaz Chim Ital , 114, 185 Ri4=OH; (1984) Нерастворимые в воде антрациклины 4-деметоксидоксорубицин (А22 Ri=H, предпочтительно растворяют в безводном апроR2=OH, R3=COCH2OH, Rii=Ri2=Ris=H, R i3 =NH 2 , тонном органическом растворителе, таком как Ri4=OH), сухой тетрагидрофуран, охлаждают до -50°С, 4'-эпидаунорубицин (А23 R1=OCH3, R2=OH, обрабатывают 1,5 эквивалентами эфирата броR3=COCH3, R11=R12=Ri4=H, Ri 3 =NH 2 , Ri5=OH, мида магния и 1,5 эквивалентами боргидрида 4'-эпидоксорубицин (А24 Ri=OCH3, R2=OH, натрия в течение 5 - 30 минут, затем добавляют R3=COCH2OH, R11=R12=Ri4=H, Ri 3 =NH 2 , Ri5=OH), каплями метанол 13-Дигидропроизводное фор4'-деоксидаунорубицин (А25 Ri=OCH3, мулы А, описанное выше, извлекают из реакциR2—OH, R3—COCH3 R11—Ri2—R14—R15—H, Ri3— NH2), онной смеси экстракцией метиленхлоридом и 4'-деоксидоксорубицин (А26 Ri=OCH3, промыванием водой Микробное восстановление R2—OH, R3—COCH2OH, R11—Ri2—R14—R15—H, антрациклинов, описанных в (iv), можно провоRi 3 =NH 2 ); дить, например, с применением блокированного 4'-иоддаунорубицин (А27 Ri=OCH3, R2=OH, мутанта -Streptomyces peucetius, как описано в Caz Chim Ital , 114, 185, (1984) R3—COCH3, Rn = R1 2 — R 5 H, Ri3— NH2, R14— I), 1— 4'-иоддоксорубицин (А28 Ri=OCH3, R2=OH, Соединения формулы А, описанные в (v), моR3—COCH2OH, R11—Ri2=Ri5—H, RKi3—NH2, R 4 I); 1— гут быть получены, как описано в GB-A-2238540, 9-деоксидаунорубицин (А29 Ri=OCH3, R2=H, например восстановлением производного 13-[(4R3—COCH3, Rn = Ri 2 — R15— H, Ri3— NH2, R14—OH); фтор)бензолсульфонил] гидразона антрациклина 9-деоксидоксорубицин (А30 Ri=OCH3, R2=H, формулы А, описанного в (v) (1), цианоборгидриR3=COCH2OH, R 11 =R 12 =R 15 =H 1 Ri 3 =NH 2 , Ri4=OH), дом натрия в органическом растворителе, таком 9-деацетилдаунорубицин (А31 Ri=OCH3, как толуол или диметилформамид, при темпераR2—OH, R3—H, Rn = Ri 2 — R 5 H, Ri3— NH2, R14—OH), 1— туре 25° - 80°С, в течение 6 - 24 часов 9-деацетил-9-деоксидаунорубицин (А32 Соединения формулы А, описанные в (iv), Ri = OCH 3 , R2—R3—H, R11—Ri2—R15—H, Ri3—NH2, могут быть получены конденсацией антрациклиRi4=OH), нона формулы К, описанного выше, при помощи 9-деацетил-9-гидроксиметилендаунорубицин реакции Кенинга-Кнорра с производным галоге(A33 Ri=OCH3, R2=CH2OH, R3=H, R 11 =R 12 =R 15 =H 1 нированного сахара формулы L1 или L2, описанR i 3 =NH 2 Ri4=OH), ных выше, в сухом аполярном растворителе, 13-дигидродаунорубицин (А34 Ri=OCH3 17 61875 18 Ri 3 =NH2 , i3 R2=OH, R3=CHOHCH3, Rii=Ri2=Ri5 Ri4=0H); 13-дигидродоксорубицин (А35 Ri=0CH3, R2=OH, R3=CHOHCH2OH, Rn=Ri 2 =Ri 5 =H, Ri3=NH2, Ri4=0H), 13-дигидро-4-деметоксидаунорубицин (А36 = Ri H, R2—OH, R3—CHOHCH3, R11—Ri2— R 5 H, 1— Ri3=NH2, Ri4=OH), 13-дигидро-4'-эпидаунорубицин (А37 = Ri OCH3, R2—OH, R3—CHOHCH3, R11—Ri2— R 4 H, 1— 13-дигидро-4'-эпидоксорубицин (А38 Ri=OCH3, R2=OH, R3=CHOHCH2OH, R11—Ri2—R14—H, R 3 NH2, R15—OH); 1— 13-дигидро-4-иоддоксорубицин (А39 Ri=OCH3, R2=OH, R3=CHOHCH2OH, R11-R12-R15-H, Ri3=NH2, Ru=l); 13-деоксодаунорубицин (А40 Ri=OCH3, R2—OH, R3—СН2СНз, Ri і—Ri2— R 5 H, R13— NH2, 1— Ri4=OH), N-трифторацетилдаунорубицин (A41 Ri=OCH3, R2—OH, R3—COCH3, R11—Ri2— R 5 H, 1— Ri3=HCOCF3, Ri4=OH), N-трифторацетилдоксорубицин (A42 Ri=OCH3 R2=OH, R3=COCH2OH, R 11 =R 12 =R 15 =H 1 Ri3=NHCOCF3, Ri4=OH), М-трифторацетил-4-деметоксидаунорубицин (A43 Ri=H, R2=OH, R3=COCH3, Rii=Ri2=Ri5=H, Ri3=NHCOCF3, Ri4=OH), |\1-трифторацетил-4'-эпидаунорубицин (А44 Ri=OCH3, R2—OH, R3—COCH3, R11—Ri2— R 4 H, 1— Ri3=NHCOCF3, Ris=OH М-трифторацетил-4'-иоддаунорубицин (А45 Ri=OCH3, R2=OH, R3=COCH3, Rii=Ri2=Ri5=H, Ri3=NHCOCF3, Ru=l) (CM F Arcamone in "Doxorub" Medicinal Chemistry, vol 17, Academic Press, 1981) или 4'-деокси-4'-метансульфонатдаунорубицин (A46 Ri=OCH3, R2=OH, R3=COCH3 R11—Ri2—R15—H, R13— NH 2 , R14—Оо02СНз), 4'-деокси-4'-метансульфонатдоксорубицин (A47 Ri=OCH3 R2=OH, R3=COCH2OH, Rii=Ri2=Ri5=H 1 Ri3=NH 2 , Ri4=OSO 2 CH 3 ) (см W O 95/16693) Некоторые из вышеупомянутых антрациклинов, в частности 4'-эпидоксорубицин, являются также предпочтительными соединениями в объеме данного изобретения Некоторые агликоны, применяемые для получения антрациклинов формулы А, описанных в (vi ), также известны и могут быть представлены формулой К, описанной выше, например дауномицинон (К1 Ri=OCH3, R2=OH, R3=COCH3, адриамицинон (К2 Ri=OCH3, R2=OH, R3=COCH2OH), 4-деметоксидауномицинон (КЗ Ri=H, R2=OH, R3=COCH3) Известны также некоторые сахара, применяемые для получения антрациклинов формулы А, описанных в (vi), и могут быть представлены формулой М М такие как аминосахара дауносамин, 3-амино2,3,6-тридеокси-І_-ликсо-гексопираноза (М1 Ris=OH, Ri9=R2o=R23=H, R 2i =NH 2 , R 2 2 =OH(CM J Am Chem, Soc , 86, 5334, 1964) или акозамин, 3-амино-2,3,6-тридеокси-І_-арабиногексопираноза (М2 Ris=OH, Rig=R2o-R22-H, R 2i =NH 2 , R23=OH) (см J Med Chem, 18, 703, 1975) или соответствующие 1 -хлор-3,4дитрифторацетилдаунозаминил производные (МЗ Ris=CI, Ri9=R20=R23=H, R2i=NHCOCF3, R22=OCOCF3) или 1-хлор-3,4дитрифторацетилакозаминил производные (МЗ Ri8=CI, R19—R2o~R22~H, R2i~ NHCOCF3, R23=OCOCFs) или диаминосахара, такие как Lфруктоза (М4 Ri8=Ri9=R2i=R22=OH, R20=R23=H) и L-рамноза (М5 Ri8=R2o=R2i=R23=OH, Ri9=R22=H) Соединения по данному изобретению характеризуются высокой активностью ингибирования амилоидоза Термин амилоидоз обозначает многочисленные заболевания, общей чертой которых является склонность к полимеризации и осаждению определенных белков в виде нерастворимых фибрилл во внеклеточном пространстве, что вызывает структурное и функциональное повреждение органа и тканей Классификация амилоида и амилоидоза недавно пересмотрена в Bulletin of the World Health Organization 71(1) 105 (1993) Все разные типы амилоида имеют общую ультраструктурную организацию в виде антипараллельных [3-сложенных слоев, несмотря на тот факт, что они содержат множество сильно отличающихся белковых субъединиц [см Glenner G G New England g Med 302 (23) 1283-8(1980)] AL амилоидоз обусловлен необычными легкими цепями многоклонального иммуноглобулина, которые образуют амилоидные фибриллы Эти моноклональные легкие цепи продуцируются моноклональными клетками плазмы с низким митотическим индексом, что объясняет их хорошо известную нечувствительность к химиотерапии Злокачественность этих клеток состоит в их белоксинтезирующей активности Клиническое течение этого заболевания зависит от селективности поражения органов, прогноз может быть крайне неблагоприятным в случае инфильтрации сердца(среднее выживание менее 12 месяцев) или более обнадеживающим в случае поражения почки(среднее выживание приблизительно 5 лет) Принимая во внимание относительную нечувствительность амилоидогенных отложений к протеолитическому разрушению, можно полагать, что только разработка молекулы, которая может блокировать или замедлять образование амилоида и увеличивать растворимость уже существующих отложений амилоида, дает, повидимому, вероятную надежду в случае больных с AL амилоидозом 61875 20 19 Кроме того, поскольку надмолекулярная орцию р25-35 индуцировало смерть нервных клеток ганизация амилоидных фибрилл одинакова для путем активации механизма запрограммированвсех типов амилоида, наличие лекарственного ной смерти клеток, известной как апоптоз (Forlorn средства, которое препятствует образованию et al , Neuro-Report, 4 523, 1993) В этом случае амилоида и увеличивает растворимость сущестнейротоксичность также ассоциировалась со вующих отложений, делая возможным очищение свойством самоагрегации р25-35 при помощи нормальных механизмов, могло бы Другие нейродегенеративные нарушения, тапривести к большому успеху в случаях всех тикие как губкообразная энцефалопатия(ЭЕ), хапов амилоидоза и, в частности, при лечении борактеризуются смертью нервных клеток и внелезни Альцгеймера клеточным отложением амилоида, в этом случае происходящего из белка Приона(РгР) ПаралДействительно, основной патологической лельно с наблюдением, что р-амилоид является особенностью болезни Альцгеймера(АО), синнейротоксичным, исследовали действие синтедрома Дауна, старческого слабоумия(Оетепйа тических пептидов, гомологичных разным сегpugihstica) и церебральной амилоидной ангиопаментам РгР, на жизнеспособность первичных тии является отложение амилоида в паренхиме нейронов гиппокампа крыс мозга и в стенках сосудов Эти маркеры ассоциированы с потерей нервных клеток в коре гоДлительное применение пептида, соответстловного мозга, лимбических районах и подкорковующего РгР 106-126, вызвало смерть нейронов вых ядрах Некоторые исследования показали, в результате апоптоза, тогда как при тех же усчто селективное повреждение различных нейловиях все другие испытанные пептиды и беспоронных систем и потеря синапса в лобной части рядочно собранная последовательность РгР 106коры головного мозга коррелировали с прогрес126 не снижали жизнеспособность клеток (For сированием ухудшения познавательной способlom et al , Nature 362 543) PrP 106-126 был выности Патогенез и молекулярная основа нейросокофибриллогенным in vitro и при окрашивании дегенеративных процессов в AD неизвестны, по Конго красным пептидный агрегат обнаружил роль р-амилоида, отлагающегося в паренхиме зеленое окрашивание, свидетельствующее о мозга и стенках сосудов, была выдвинута на конформации в виде р-слоев(пластов), характерпервый план недавним сообщением о его нейроной для амилоида токсической активности in vitro и in vivo(Janker et Соединения по данному изобретению можно al , Science, 245 417, 1990 Kowall et al , PNAS, применять для приготовления лекарственных 88 7247, 1991) Кроме того, сегрегация хорошо средств, применимых для предотвращения или знакомой болезни Альцгеймера(АФ) с мутацией остановки прогрессирования заболеваний, вызыгена предшественника белка амилоида(АРР) ваемых амилоидными белками, таких как AL вызвала интерес к потенциальной патогенетичеамилоидоз, синдром Альцгеймера или синдром ской функции р-амилоида в болезни АльцгеймеДауна и т п ра [Mullan M Etal TINS, 16(10) 392(1993)] Данное изобретение также включает в свой объем фармацевтические композиции, содержаНейротоксичность р-амилоида была ассощие одно или более соединений формулы А или циирована с фибриллогенными свойствами белих фармацевтически приемлемые соли в качестка Исследования с гомологичными синтетичеве активных ингредиентов в сочетании с фармаскими пептидами показывают, что клетки цевтически приемлемыми носителями, наполнигиппокампа были нечувствительны к обработке телями и другими добавками, если необходимо свежим раствором [31-42 в течение 24 часов, тогда как их жизнеспособность снижалась при эксФармацевтические композиции, содержащие позиции нервных клеток с [31-42, предварительно соединение формулы А или его соли, могут быть хранившимся в солевом растворе в течение 2 - 4 приготовлены обычным способом с использовадней при 37°С для способствования агрегации нием обычных нетоксичных фармацевтических пептидов Связь между фибриллами и нейротокносителей или разбавителей в виде различных сичностью подтверждается далее недавним релекарственных форм для различных путей ввезультатом, показывающим, что растворимая дения форма р -амилоида продуцируется in vivo и in В частности, соединения формулы А могут vitro во время нормального клеточного метабобыть введены лизма (Hass et al Nature, 359, 322, 1993), и тольА) перорально, например в виде таблеток, ко при агрегации амилоида в конгофильное обпастилок, лепешек, водной или масляной суспенразование он ассоциировался с дистрофическим зии, диспергируемых порошков или гранул, невритом С другой стороны, не-конгофильное эмульсий, твердых или мягких капсул или сиро"преамилоидное" образование, состоящее из пов или эликсиров Композиции, предназначенединственной молекулы р-амилоида, не было ные для перорального введения, могут быть присвязано с изменением нейронов (Tagliavim et al, готовлены согласно любому способу, известному Neurosci Lett 93 191, 1988) в этой области для производства фармацевтических композиций, и такие композиции могут соНейротоксичность р-амилоида также была держать один или несколько агентов из группы, подтверждена с применением пептидного гомосодержащей подслащивающие средства, аромалога р-амилоидного фрагмента 25 - 35(р25-35), тизаторы и консервирующие средства, для обессохраняющего свойства самоагрегации полного печения приятных на вид и съедобных фармар-амилоидного фрагмента [3142 цевтических препаратов Хроническое, но не острое, воздействие нейронов гиппокампа на микромолярную концентра Таблетки содержат активный ингредиент в 61875 22 21 смеси с нетоксичными фармацевтически приемили цетиловый спирт Подслащивающие вещелемыми наполнителями, которые пригодны для ства, такие, которые указаны выше, и ароматизапроизводства таблеток Эти наполнители могут торы могут быть добавлены для придания перопредставлять собой, например, инертные разбаральному препарату вкуса Эти композиции могут вители, такие как карбонат кальция, карбонат содержать консерванты, такие как автооксиданнатрия, лактоза, фосфат кальция или фосфат ты, например аскорбиновую кислоту Диспергинатрия, гранулирующие и разрыхляющие агенты, руемые порошки и гранулы, пригодные для принапример кукурузный крахмал или альгиновую готовления водной суспензии путем добавления кислоту, связующие средства, например кукурузводы, обеспечивают активный ингредиент в сменый крахмал и аравийскую камедь, и смачиваюси с диспергирующим или смачивающим агенщие агенты, например стеарат магния или стетом, суспендирующим агентом, и одним или нериновую кислоту или тальк Таблетки могут не сколькими консервантами Примеры пригодных иметь покрытия или они могут быть покрыты издиспергирующих и смачивающих и суспендивестными способами для замедления разрушерующих агентов приведены выше Могут также ния и поглощения в желудочно-кишечном тракте присутствовать дополнительные наполнители, и, следовательно, обеспечения пролонгированнапример подслащивающие, ароматизирующие ного действия в течение более длительного пеагенты риода Например, можно использовать такой Фармацевтические композиции по изобретематериал для пролонгирования действия, как нию могут быть также в форме эмульсий типа глицерилмоностеарат или глицерилдистеарат масло в воде Масляной фазой может быть расГотовая лекарственная форма для перорального тительное масло, например оливковое масло или применения может быть также представлена в арахисовое масло, или минеральное масло, навиде жесткой желатиновой капсулы, в которой пример жидкий парафин, или их смеси активный ингредиент смешан с инертным тверПодходящие эмульгаторы могут представдым разбавителем, например карбонатом кальлять собой природные камеди, например, такие ция, фосфатом кальция или каолином, или мягкак аравийская камедь или трагакантовая какими желатиновыми капсулами, в которых медь, встречающиеся в природе фосфатиды, активный ингредиент смешан с водой или маснапример лецитин сои, и эфиры или неполные ляной средой, например арахисовым маслом, эфиры, производные жирных кислот и ангидрижидким парафином или оливковым маслом Воддов гексита, например сорбитанмоноолеат, и ные суспензии содержат активные материалы в продукты конденсации неполных эфиров с этисмеси с наполнителями, пригодными для изголеноксидом, например полиоксиэтиленсорбитовления водных суспензий танмоноолеат Эмульсия может также содержать подслащивающие и ароматизирующие вещества Такие наполнители представляют собой сусСиропы и эликсиры могут быть приготовлены с пендирующие агенты, например, такие как карподслащивающими веществами, например глибоксиметилцеллюлоза натрия, метилцеллюлоза, церином, сорбитом или сахарозой Такие формы гид роксипропил метил целлюлоза, альгинат намогут также содержать средство, уменьшающее трия, поливинилпирролидон, смола трагаканта и раздражение, консервант, ароматизаторы и крааравийская камедь, диспергирующие или смачисители вающие агенты могут представлять собой встречающиеся в природе фосфатиды, например леВ) Парентерально, либо подкожно, либо цитин, или продукты конденсации алкиленоксида внутривенно, либо внутримышечно, либо внутрис жирными кислотами, например полиэтиленгрудинно или инфузионным способом, в форме стеарат, или продукты конденсации этиленоксистерильной инъецируемой водной или маслянида с длинноцепочечными алифатическими спирстой суспензии Фармацевтические композиции тами, например гептадекаэтиленоксицетанол, могут быть в форме стерильных инъецируемых или продукты конденсации этиленоксида с неводных или масляных суспензий полными сложными эфирами, производными Эти суспензии могут быть приготовлены изжирных кислот и гексита, например полиоксиэтивестным способом с применением указанных ленсорбитмоноолеат, или продукты конденсации выше диспергирующих или смачивающих агенэтиленоксида с неполными сложными эфирами, тов и суспендирующих агентов Стерильный производными жирных кислот и ангидридов гекинъецируемый препарат может также представсита, например полиоксиэтиленсорбитанмонолять собой стерильные инъецируемые раствор олеат Водные суспензии могут также содержать или суспензию в нетоксичном парентерально один или несколько консервантов, например нприемлемом разбавителе или растворителе, пропил-п-гидроксибензоат, один или более кранапример в виде раствора в 1,3-бутандиоле сителей, один или более ароматизаторов, или Среди приемлемых носителей и растворителей, один или более подслащивающих средств, таких которые можно использовать, можно указать вокак сахароза или сахарин Масляная суспензия ду, раствор Рингера и изотонический раствор может быть получена суспендированием активхлористого натрия Кроме того, стерильные жирного ингредиента в растительном масле, наприные масла(с большим содержанием жира) являмер в арахисовом масле, оливковом масле, кунются обычно используемыми в качестве раствожутном масле или кокосовом масле, или в рителя или суспендирующей среды минеральном масле, таком как жидкий парафин Для этой цели могут использоваться любые Масляные суспензии могут содержать загустимягкие жирные масла, в том числе синтетические тель, например пчелиный воск, твердый парафин моно- или диглицериды Кроме того, такие жир 23 ные кислоты, как олеиновая кислота, находят применение в приготовлении инъецируемых препаратов Еще одним объектом изобретения является способ борьбы со связанными с амилоидозом заболеваниями путем введения терапевтически эффективного количества одного или более активных соединений формулы А людям, нуждающимся в подобном лечении Суточные дозы находятся в диапазоне приблизительно 0,1 - 50мг на кг веса пациента, в зависимости от активности конкретного соединения, возраста, веса и состояния подвергаемого лечению субъекта, типа и тяжести заболевания и частоты и пути введения, предпочтительно уровни суточных доз находятся в диапазоне 5мг - 2г Количество активного ингредиента, которое может быть вместе с материалами-носителями для получения формы разовой дозы, будет изменяться в зависимости от подвергаемого лечению субъекта и конкретного способа введения Например, состав, предназначенный для перорального введения, может содержать 5мг - 2г активного агента вместе с приемлемым и удобным количеством материала-носителя, которое может изменяться от около 5 до около 95% от всей композиции Единичные дозированные формы обычно будут содержать от около 5мг до около 500мг активного ингредиента Следующие примеры иллюстрируют изобретение, но не ограничивают его Пример 1 Получение 14-г\І-(морфолино)-3'-г\Ітрифторацетил-4'-иоддауномицина (А1) Гидрохлорид 4'-иоддаунорубицина(А27, 1,34г, 2ммоль) растворяли в смеси диоксана(ЗОмл) и метанола(20мл) и обрабатывали раствором 10% брома в хлороформе(2мл) при 0°С, как описано в US-A-4438105 Спустя 1 час, к реакционной смеси добавляли этиловый эфир(200мл) и осадок собирали, промывали этиловым эфиром(ЮОмл), вновь растворяли в безводном тетрагидрофуране(80мл) и обрабатывали морфолином(0,25мл) в течение ночи при комнатной температуре После этого реакционную смесь концентрировали до малого объема при пониженном давлении, разбавляли метиленхлоридом, охлаждали до 0°С и обрабатывали раствором трифторуксусного ангидрида(2мл) в метиленхлориде(Юмл) Через 30 минут реакционную смесь промывали водным 5% гидрокарбонатом калия и дважды водой Органическую фазу концентрировали при пониженном давлении и подвергали флаш-хроматографии на силикагеле с применением смеси метиленхлорид/метанол (90 10об/об) в качестве элюирующей системы, получая указанное в заголовке соединение А1, которое превращали в соответствующий гидрохлорид путем добавления стехиометрического количества хлористого водорода с последующим осаждением этиловым эфиром Выход 0,9г Тонкослойная хроматография на Kieselgel F254(Merck), элюирующая система метиленхлорид/метанол (90 Юоб/об) Rf = 0,5 FD-MS m/e 816 [М]+ Пример 2 61875 24 Получение 13-дигидро-14-І\І-(морфолино)-3'|\|-трифторацетил-4'-иоддауномицина (А7) 14-г\1-(морфолино)-3'-г\1-трифторацетил-4'иоддауномицин(А1, 0,4г, 0,05ммоль), полученный, как описано в примере 1, в виде свободного основания растворяли в безводном тетрагидрофуране(20мл) и к раствору добавляли эфират бромида магния(0,7г) Через 10 минут при комнатной температуре, в атмосфере азота, смесь охлаждали до -50°С, добавляли боргидрид натрия(50мг) и затем обрабатывали безводным метанолом(1 х 2мл) в течение 5 минут После этого добавляли ацетон(5мл) Реакционную смесь доводили до температуры 0°С и экстрагировали 0,1 н водной соляной кислотой Водную фазу доводили до рН 8,5 0,1 н гидроксидом натрия и экстрагировали метиленхлоридом, получая указанное в заголовке соединение А7, которое превращали в соответствующий гидрохлорид добавлением стехиометрического количества хлористого водорода с последующим осаждением этиловым эфиром Выход 0,Зг TLC на Kieselqel F254(Merck), система элюирующая метиленхлорид и метанол(90 Юоб/об) Rf = 0,3 FD-MS m/e818[M] + Пример З Получение 14-N-(3,4диметоксибензиламино)-3'-І\І-трифторацетил-4'иоддауномицина (А2) Указанное в заголовке соединение А2 получали взаимодействием 14-бром-4'иоддауномицина(0,65г, 1 ммоль) с 3,4диметоксибензиламином(0,3г, 1 ммоль) в безводном тетрагидрофуране(50мл), как описано в примере 1 Выход 0,Зг TLC на Kiselgel F254(Merck), элюирующая система - метиленхлорид/метанол(90 Юоб /об) Rf = 0,45 FD-MS m/e 797 [М]+ Пример 4 Получение 14-г\1-(морфолино)-3'-г\1-фталоил4'-иоддауномицина (А8) 14-1\1-(морфолино)-4'-иоддауномицин(0,7г, 1ммоль), полученный, как описано в примере 1, подвергали взаимодействию в фталоилхлоридом(0,4г, 2ммоль) в безводном тетрагидрофуране(50мл) при 0°С в течение 4 часов Смесь разбавляли метиленхлоридом(ЮОмл) и промывали водным гидрокарбонатом натрия и водой, затем сушили над безводным сульфатом натрия Растворитель удаляли при пониженном давлении и сырой продукт подвергали флаш-хроматографии на силикагеле с применением смеси метиленхлорид/ацетон(95 5об /об ) в качестве элюирующей системы, получая указанное в заглавии соединение А8(0,5г) TLC на Kieselqel F254(Merck), элюирующая система метиленхлорид/метанол(90 Юоб /об ) Rf = 0,25 FD-MS m/e851[M]+ Пример 5 Получение 3'-І\І-дифенилметилен-4'иоддоксорубицина (А16) Гидрохлорид иоддоксорубицина(А27, 0,65г, 1 ммоль) растворяли втетрагидрофуране(50мл) и обрабатывали бензофенонимином(0,36г, 2ммоля) Смесь выдерживали при комнатной 25 61875 температуре в течение ночи, затем растворитель удаляли при пониженном давлении и сырой продую" подвергали флаш-хроматографии на силикагеле, получая указанное в заголовке соединение А16(0,6г) TLC на Kieselgel F254(Merck), элюирующая система метиленхлорид/ацетон(95 5об /об ) Rf = 0,55 + FD-MS m/e816[M] Пример 6 Получение 14-г\І-(морфолино)-3'-г\Ідифенилметилен-4'-иоддаунорубицина (А17) 14-1\1-(морфолино)-4'-иоддауномицин(0,7г, 1ммоль), полученный, как описано в примере 1, подвергали взаимодействию с бензофенонимином(0,36г, 2ммоля), как описано в примере 5, получая указанное в заголовке соединение А17(0,65г) TLC на Kiselgel F254(Merck), элюирующая система - метиленхлорид/ацетон(95 5об/об) Rf=0,40 FD-MS m/e 885[M]+ Биологическое исследование Производные антрациклина формулы А препятствуют самоагрегирующей активности фрагмента 25-35 р-амилоида и РгР фрагмента 106126 при испытании анализом светорассеяния Комп'ютерна верстка І Вихованець 26 [325-35 (GSNKGAIIGLH) и РгР 106-126 (KTNMKHMA G AAAAGAVVGGLG) синтезировали при помощи твердофазной химии с применением 430А Applied Biosystems Instruments и очищали при помощи НРІ_С(ЖХВР) с обращенной фазой(Весктап Inst mod 243) согласно Forlorn ei al Nature 362 543, 1993 Светорассеяние пептидных растворов оценивали при помощи спектрофлуорометрии (Perkm Elmer LS 50В), возбуждение и эмиссию наблюдали при бООнм р-Амилоидный фрагмент 25-35 и РгР 106-126 растворяли при концентрации 0,5 - 1мг/мл(0,4 - 0,8мМ и 0,2 - 0,4мМ, соответственно) в растворе фосфатного буфера рН 5, 10мм самопроизвольно агрегировали в пределах часа 13-дигидро-4'-иодоксорубицин(А39), растворенный при нескольких концентрациях(0,2 - 2мМ) в Трис буфере 5мМ рН 7,4, добавляли к пептидным растворам в момент их приготовления для оценки процесса фибриллогенеза Соединение А29, добавленное при эквимолярной концентрации с р-амилоидным фрагментом 2535 и РгР 106-126, показало полное предотвращение агрегации Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюA medicament for use in the treatment of amyloidosis, an anthracycline and a pharmaceutical composition
Автори англійськоюBardzhotti Alberto
Назва патенту російськоюЛекарственное средство для лечения амилоидоза, антрациклин и фармацевтическая композиция
Автори російськоюБарджотти Альберто
МПК / Мітки
МПК: A61K 31/70, A61K 31/7034, A61K 31/7028, A61K 31/704, C07H 15/252, A61K 31/7042, A61K 31/7052, C07H 17/02, A61P 25/00, A61P 25/28
Мітки: композиція, фармацевтична, лікарський, засіб, лікування, антрациклін, амілоїдозу
Код посилання
<a href="https://ua.patents.su/13-61875-likarskijj-zasib-dlya-likuvannya-amilodozu-antraciklin-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Лікарський засіб для лікування амілоїдозу, антрациклін та фармацевтична композиція</a>
Попередній патент: Полімер етилена, спосіб його одержання, плівка та інші вироби, що містять полімер етилену
Наступний патент: Композиція інгредієнтів для вермуту сухого або міцного, або десертного червоного “джовані казанова”
Випадковий патент: Спосіб вирощування насіння гречки з урахуванням фону живлення та строку сівби в умовах нестійкого зволоження правобережного лісостепу україни












