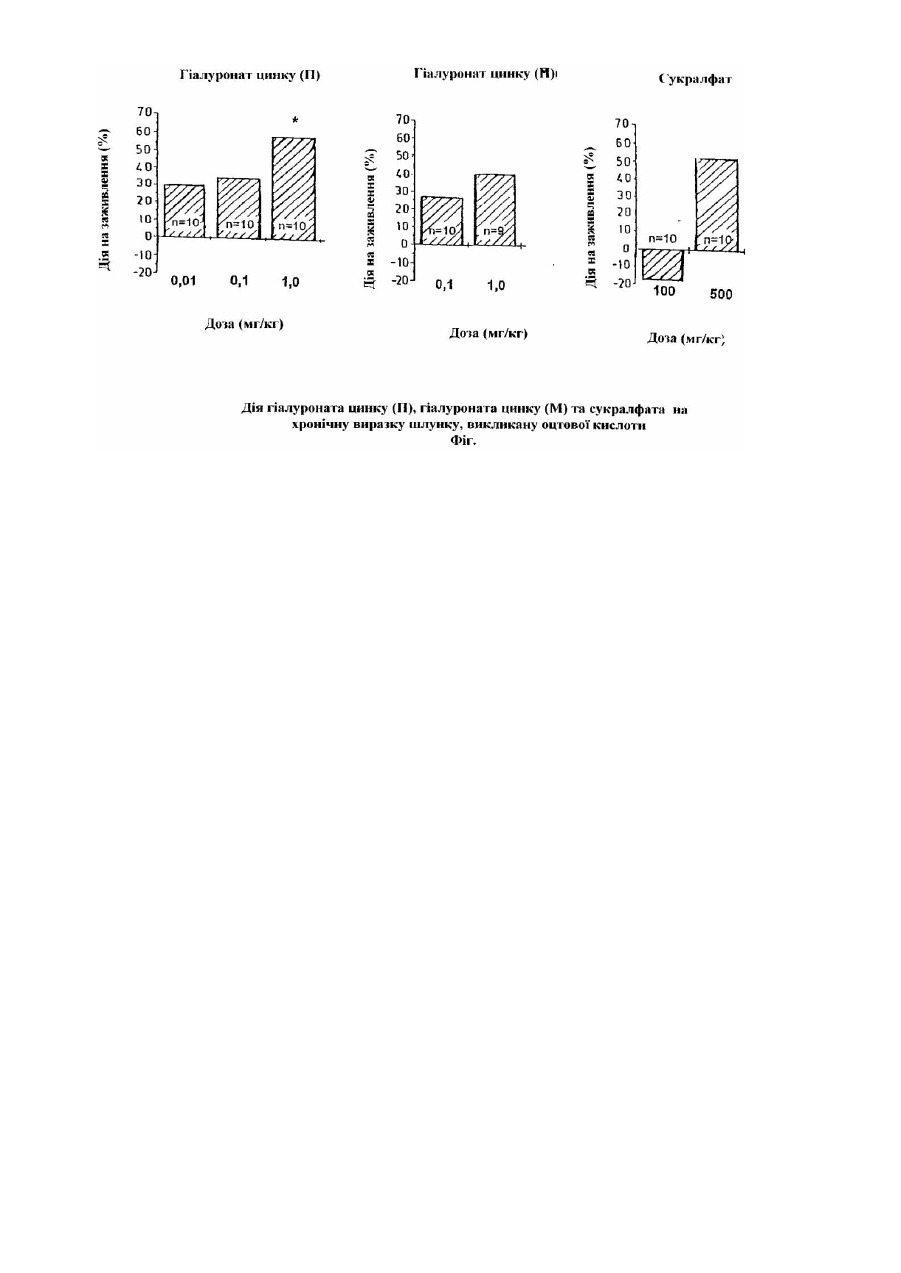
Фармацевтична композиція для лікування та профілактики пептичної виразки, спосіб її отримання та спосіб лікування пептичних виразок
Номер патенту: 62964
Опубліковано: 15.01.2004
Автори: Несмелі Ержебет, Спорні Гуала, Форрай Габорне, Матус Юдіт, Штефко Бела, Іллеш Янош, Шаги Каталін
Формула / Реферат
1. Фармацевтична композиція для лікування та профілактики пептичної виразки для перорального застосування, що містить як активний інгредієнт асоціат (комплекс) гіалуронату цинку, що має молекулярну масу в інтервалі від 500 000 до 1 200 000 дальтон, у суміші з носієм та/або іншими добавками, які звичайно застосовують у фармацевтичних композиціях.
2. Фармацевтична композиція для перорального застосування за п.1, що включає гіалуронат цинку, який має молекулярну масу 900 000 дальтон.
3. Спосіб одержання фармацевтичної композиції для лікування та профілактики пептичної виразки для перорального застосування, при якому змішують асоціат (комплекс) гіалуронату цинку, який має молекулярну масу в інтервалі від 500 000 до 1 200 000 дальтон, як активний інгредієнт, з носієм та/або іншими добавками, що звичайно застосовують у фармацевтичній промисловості та перетворюють суміш у фармацевтичну композицію перорального заcтосування.
4. Спосіб лікування пептичних виразок, а також профілактики утворення виразок, при якому вводять пацієнту, який підлягає лікуванню, терапевтичну кількість асоціату (комплексу) гіалуронату цинку, що має молекулярну масу в інтервалі від 500 000 до 1 200 000 дальтон, окремо або у вигляді фармацевтичної композиції для перорального застосування.
Текст
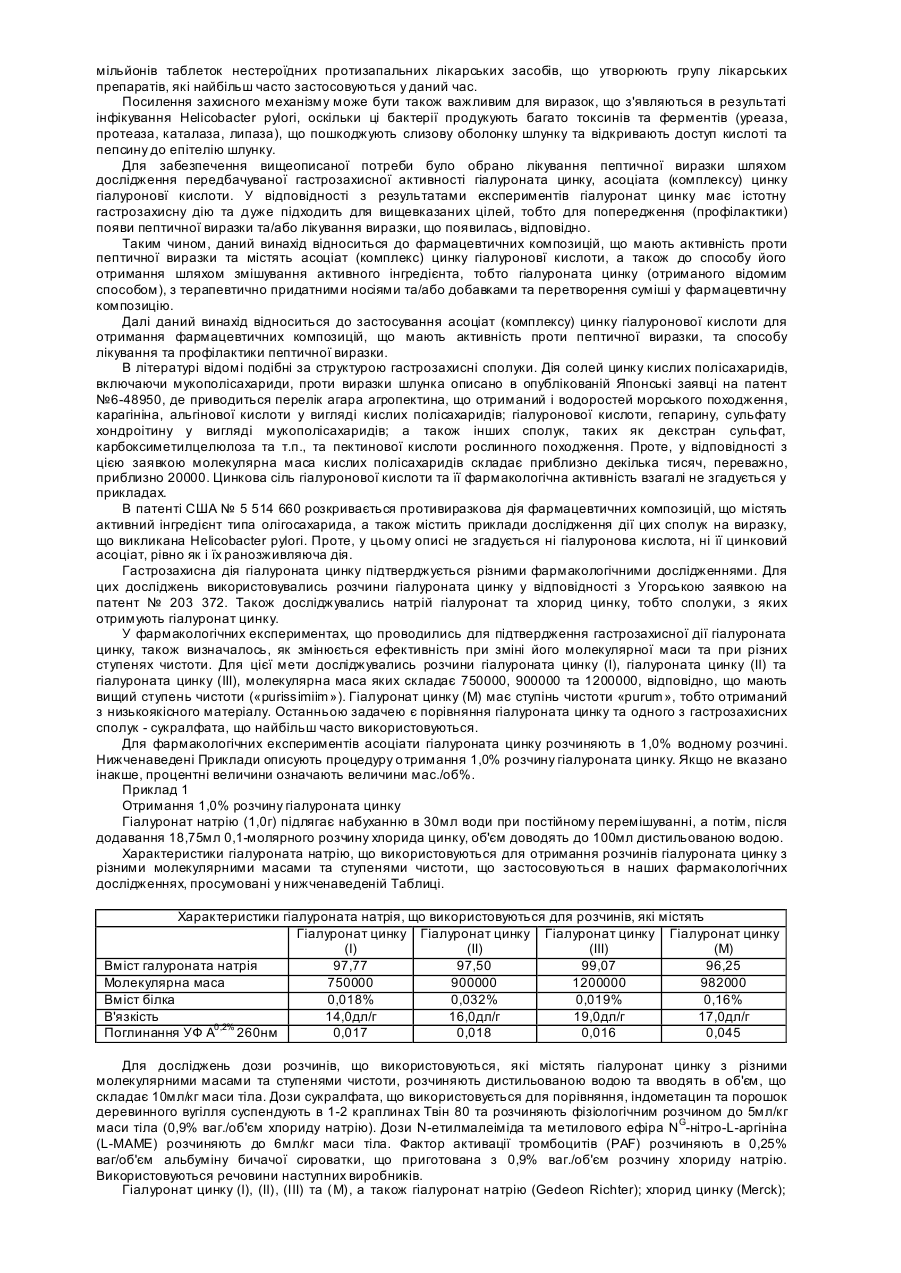
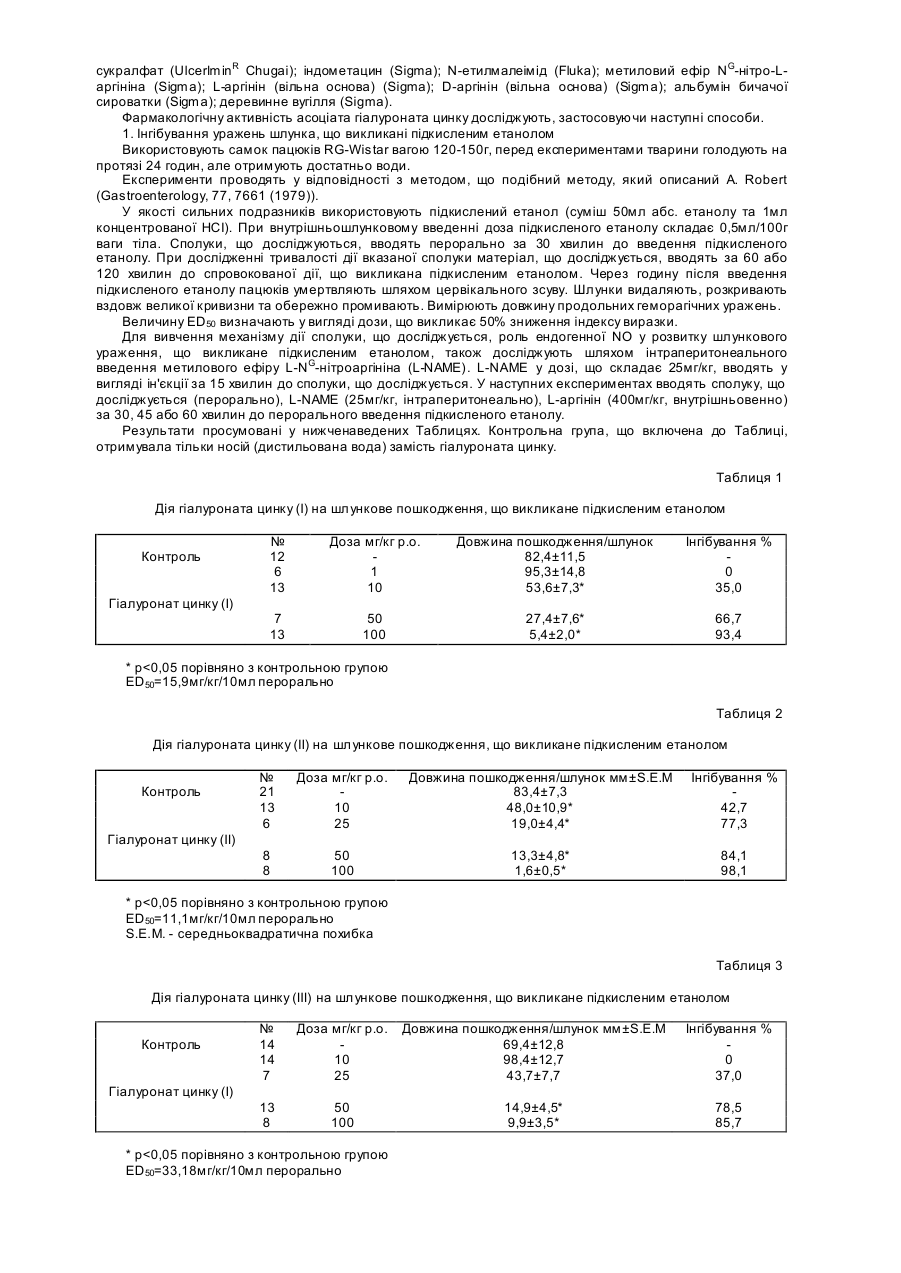
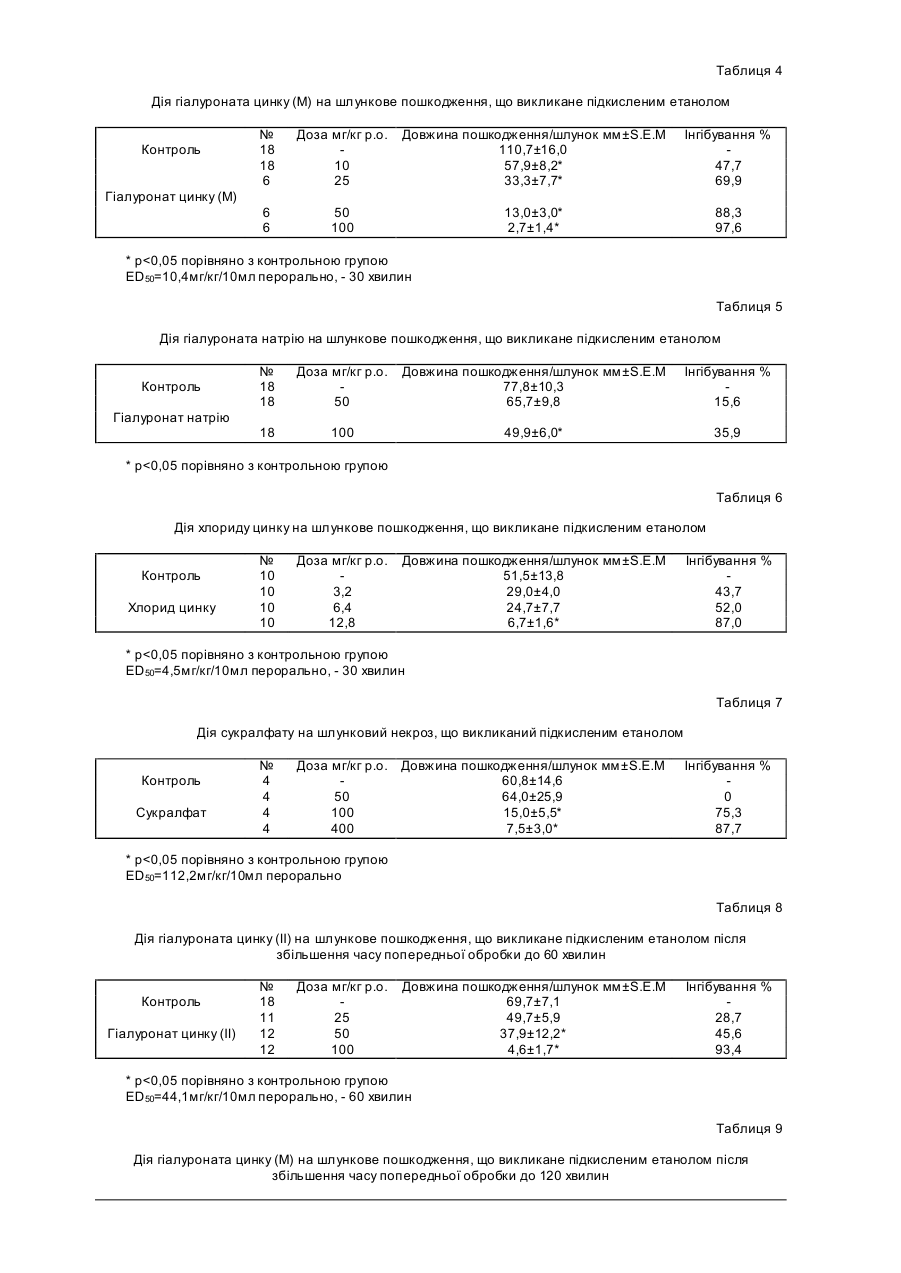
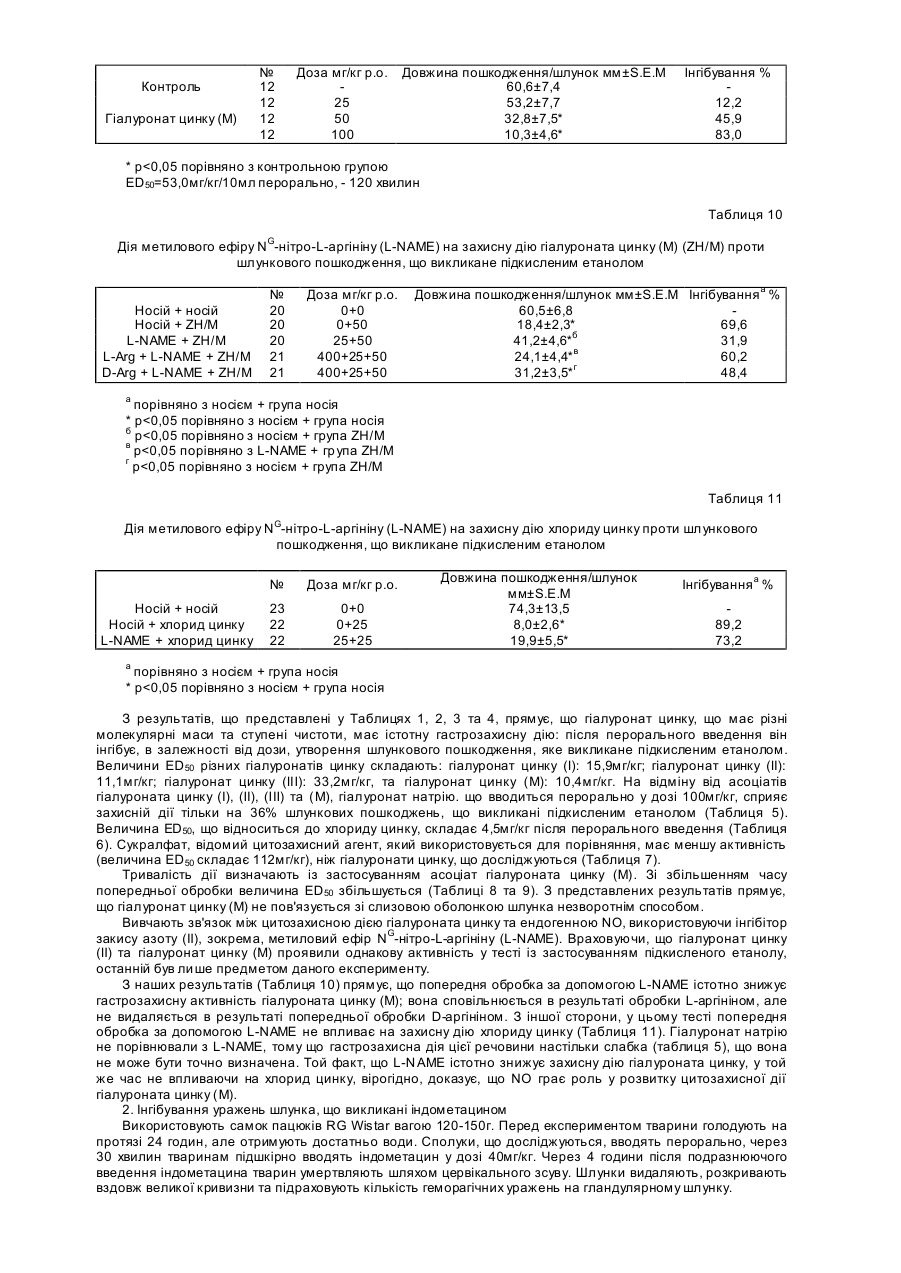
Даний винахід відноситься до фармацевтичних композицій, що мають активність проти пептичної виразки та містять асоціат (комплекс) цинку гіалуронової кислоти, а також до способу їх отримання. Далі даний винахід відноситься до застосування асоціата (комплексу) цинку гіалуронової кислоти, тобто гіалуроната цинку, для отримання фармацевтичних композицій, що мають активність проти пептичної виразки, та до способу їх лікування та профілактики пептичної виразки. Даний винахід також відноситься до застосування гіалуроната цинку для профілактики реінфекції після заживлення пептичної виразки. Макромолекула, що відома як гіалуронова кислота, що звичайно зустрічається у вигляді її натрієвої солі, представляє собою сполуку, яка відома більше 50 років. Meyer et al. (J. Biol. Chem., 107, 629 (1934)) вперше описали, що гіалуронова кислота представляє собою високов'язкий нативний глюкозаміноглікан, що містить почергово b1-3 глюкоронову кислоту та залишки b1-4 глюкозаміна, її молекулярна маса складає від 50000 до декількох мільйонів. Гіалуронова кислота зустрічається у сполучних тканинах всіх ссавців; у найбільшій кількості вона знаходиться у шкірі, скловидному тілі ока, синовіальній рідині, пуповині, а також у хрящовій тканині. До останнього часу гіалуронова кислота застосовувалась у вигляді натрієвої солі для лікування, головним чином в офтальмології, дерматології, хірургії, терапії суглобу, а також у косметиці. Солі гіалуронової кислоти, що утворені з лугом, лужною землею, магнієм, алюмінієм, амонієм та заміщеними іонами амонію, можуть служити як носії для стимулювання абсорбції лікарських засобів (див. Опис до Бельгійського патенту № 904 547). Солі важких металів гіалуронової кислоти, включаючи сіль срібла, застосовують у вигляді фун гіцидів, у той час як солі золота можуть бути використані для лікування ревматоїдного артриту (див. опис до патенту № WO 87/05517). Однак, відомі важкі побічні реакції сполук срібла та золота, тобто їх дія на імунну систему, органи кровообігу та нервову систему (M. Shinogi, S. Maezumi: «Effect of preinduction of metallothionein on tissue distribution of silver & hepatic lipid peroxidation», Biol. Pharm. Bull. (Japan), Apr. 1993, 16 (4), h. 372-374; C. Masson et al.,: Rev. Med. Interne (France), May-June 1992, 13(3), p.225-232 (1992)). Асоціати (комплекси) гіалуронової кислоти з видаленим протоном з іонами металів 3d 4-го періоду Періодичної Таблиці, такі як гіалуронати цинку та кобальту, що мають лікувальну дію, особливо проти виразок на ногах, пролежнів та т. ін., розкриті в описі до Венгерського патенту № 203 372 (якому відповідає WO-A-9010020) з підтвердженням зовнішнього застосування. У даний час було винайдено, що асоціат (комплекс) цинку гіалуронової кислоти, тобто гіалуронат цинку має істотну гастрозахисну активність, тому він може бути використаний для профілактики та лікування пептичних виразок, включаючи виразки, що викликані Helicobacter pylori. Пептична виразка - це складне та багатофакторне захворювання, що спостерігається у більшої частини цивілізованого населення. Багато питань, що стосуються точного патогенезу цього захворювання, чекають своїх відповідей. На протязі останніх п'яти років з'явився новий підхід завдяки «повторному відкриттю» Helicobacter pylori. Загальновідомо, що розвиток пептичної виразки у людей пов'язаний з інфікуванням Helicobacter pylori, проте з іншої сторони, Helicobacter pylori не може відповідати за всі причини появи пептичної виразки. До даного часу лікування пептичної виразки істотно не змінилось: як і раніше, блокатори Н2 та інгібітори протонного насоса є найбільш важливими засобами терапевтичного арсеналу, у той час як в літературі переважають можливі терапевтичні способи умертвіння бактерій Н. pylori. Окрім того, лікування гастродуоденальних пошкоджень, що викликані нестероідними протизапальними лікарськими засобами, зайняло центральне місце. Пептична виразка, що з'явилась за любих обставин, може бути о характеризована порушенням балансу, що існує у здорових умовах між агресивними факторами, що викликають розвиток виразки, та захисними факторами, що захищають шлунок від появи виразки. Таким чином, виразка розвивається у кожному випадку, коли посилення агресивних факторів виходить за певні межі та/або захисні фактори слабшають. Захисні фактори включають такі фактори, як опір слизової оболонки шлунка та утворення слизу (H. Shay: Etiology of peptic ulcer, Am. J. Dig. Dis., 6, 29-49 (1961)). Серед агресивних факторів головними факторами є секреція соляної кислоти та пепсину, а також всі фактори, що стимулюють секрецію любого з цих речовин. Секреція кислоти може бути також посилена патологічним вагусним подразником або підвищеним утворенням гастрина аутоімунним механізмом та, у деяких випадках, гормональною дією. Окрім того, рівновага між агресивними та захисними факторами може бути також порушена пошкодженнями, що відносяться до всього організму. Таким чином, пептична виразка є багатофакторним захворюванням. Засоби, що застосовуються для лікування виразок, призначені для зниження ролі агресивних факторів та/або посилення ролі захисних факторів. До останнього часу фармакологічні дослідження були напрямлені на послаблення дії агресивних факторів, таким чином первинною метою було утримання утворення кислоти та пепсину. Лікарські засоби, що застосовуються для лікування виразок, в першу чергу були напрямлені на нейтралізацію кислоти (антациди, такі як двовуглекислий натрій або гідроокис алюмінію) або на інгібування її секреції (блокатори Н2, наприклад, циметидін, фамотидін, інгібітори протонного насоса, наприклад, омепразол). Тільки в останній час велике значення набуло дослідження агентів, що посилюють роль захисних факторів, окрім розвитку мототерапії, що застосовується для ооооооооооо Helicobacter pylori. Проте, існує обмежена кількість композицій, що посилюють захисні фактори, при цьому вони мають побічні дії. Такими композиціями є колоїдний субцитрат вісмуту (CBS, De-NOL), сукралфат та мізопростол. CBS містить вісмут, що викликає токсикологічні проблеми. Сукралфат, основна сіль алюмінію сульфатованої са харози викликає деякі побічні реакції, наприклад, нудоту, блювання, інтоксикацію алюмінієм та т. ін., а мізопростол, синтетичний аналог простагландіну, викликає посилену інтестинальну активність або нудоту. З вищевказаного видно, що існує подальша потреба в ефективних та безпечних лікарських засобах для лікування виразок, що не викликають підвищену секрецію кислоти. Такі композиції можуть з успіхом застосовуватись у тих випадках, коли метою є попередження уражень шлунка в результаті подразнюючої та пошкоджуючої дії, наприклад, нестероїдних протизапальних лікарських засобів, таких як індометацин, аспірин, шляхом посилення захисного механізму слизової. Кількість пацієнтів, що мають пептичні виразки із-за вживання нестероїдних протизапальних лікарських засобів (NSAID), може у майбутньому підвищитись, якщо прийняти до уваги дані, які демонструють, що щоденно у всьому світі вживається більше десяти мільйонів таблеток нестероїдних протизапальних лікарських засобів, що утворюють групу лікарських препаратів, які найбільш часто застосовуються у даний час. Посилення захисного механізму може бути також важливим для виразок, що з'являються в результаті інфікування Helicobacter pylori, оскільки ці бактерії продукують багато токсинів та ферментів (уреаза, протеаза, каталаза, липаза), що пошкоджують слизову оболонку шлунку та відкривають доступ кислоті та пепсину до епітелію шлунку. Для забезпечення вищеописаної потреби було обрано лікування пептичної виразки шляхом дослідження передбачуваної гастрозахисної активності гіалуроната цинку, асоціата (комплексу) цинку гіалуроновї кислоти. У відповідності з результатами експериментів гіалуронат цинку має істотну гастрозахисну дію та дуже підходить для вищевказаних цілей, тобто для попередження (профілактики) появи пептичної виразки та/або лікування виразки, що появилась, відповідно. Таким чином, даний винахід відноситься до фармацевтичних композицій, що мають активність проти пептичної виразки та містять асоціат (комплекс) цинку гіалуроновї кислоти, а також до способу його отримання шляхом змішування активного інгредієнта, тобто гіалуроната цинку (отриманого відомим способом), з терапевтично придатними носіями та/або добавками та перетворення суміші у фармацевтичну композицію. Далі даний винахід відноситься до застосування асоціат (комплексу) цинку гіалуронової кислоти для отримання фармацевтичних композицій, що мають активність проти пептичної виразки, та способу лікування та профілактики пептичної виразки. В літературі відомі подібні за структурою гастрозахисні сполуки. Дія солей цинку кислих полісахаридів, включаючи мукополісахариди, проти виразки шлунка описано в опублікованій Японські заявці на патент №6-48950, де приводиться перелік агара агропектина, що отриманий і водоростей морського походження, карагініна, альгінової кислоти у вигляді кислих полісахаридів; гіалуронової кислоти, гепарину, сульфату хондроітину у вигляді мукополісахаридів; а також інших сполук, таких як декстран сульфат, карбоксиметилцелюлоза та т.п., та пектинової кислоти рослинного походження. Проте, у відповідності з цією заявкою молекулярна маса кислих полісахаридів складає приблизно декілька тисяч, переважно, приблизно 20000. Цинкова сіль гіалуронової кислоти та її фармакологічна активність взагалі не згадується у прикладах. В патенті США № 5 514 660 розкривається противиразкова дія фармацевтичних композицій, що містять активний інгредієнт типа олігосахарида, а також містить приклади дослідження дії цих сполук на виразку, що викликана Helicobacter pylori. Проте, у цьому описі не згадується ні гіалуронова кислота, ні її цинковий асоціат, рівно як і їх ранозживляюча дія. Гастрозахисна дія гіалуроната цинку підтверджується різними фармакологічними дослідженнями. Для цих досліджень використовувались розчини гіалуроната цинку у відповідності з Угорською заявкою на патент № 203 372. Також досліджувались натрій гіалуронат та хлорид цинку, тобто сполуки, з яких отримують гіалуронат цинку. У фармакологічних експериментах, що проводились для підтвердження гастрозахисної дії гіалуроната цинку, також визначалось, як змінюється ефективність при зміні його молекулярної маси та при різних ступенях чистоти. Для цієї мети досліджувались розчини гіалуроната цинку (І), гіалуроната цинку (ІІ) та гіалуроната цинку (III), молекулярна маса яких складає 750000, 900000 та 1200000, відповідно, що мають вищий ступень чистоти («purissimiim»). Гіалуронат цинку (Μ) має ступінь чистоти «purum», тобто отриманий з низькоякісного матеріалу. Останньою задачею є порівняння гіалуроната цинку та одного з гастрозахисних сполук - сукралфата, що найбільш часто використовуються. Для фармакологічних експериментів асоціати гіалуроната цинку розчиняють в 1,0% водному розчині. Нижченаведені Приклади описують процедуру о тримання 1,0% розчину гіалуроната цинку. Якщо не вказано інакше, процентні величини означають величини мас./об%. Приклад 1 Отримання 1,0% розчину гіалуроната цинку Гіалуронат натрію (1,0г) підлягає набуханню в 30мл води при постійному перемішуванні, а потім, після додавання 18,75мл 0,1-молярного розчину хлорида цинку, об'єм доводять до 100мл дистильованою водою. Характеристики гіалуроната натрію, що використовуються для отримання розчинів гіалуроната цинку з різними молекулярними масами та ступенями чистоти, що застосовуються в наших фармакологічних дослідженнях, просумовані у нижченаведеній Таблиці. Характеристики гіалуроната натрія, що використовуються для розчинів, які містять Гіалуронат цинку Гіалуронат цинку Гіалуронат цинку Гіалуронат цинку (І) (II) (III) (М) Вміст галуроната натрія 97,77 97,50 99,07 96,25 Молекулярна маса 750000 900000 1200000 982000 Вміст білка 0,018% 0,032% 0,019% 0,16% В'язкість 14,0дл/г 16,0дл/г 19,0дл/г 17,0дл/г Поглинання УФ Α0,2% 260нм 0,017 0,018 0,016 0,045 Для досліджень дози розчинів, що використовуються, які містять гіалуронат цинку з різними молекулярними масами та ступенями чистоти, розчиняють дистильованою водою та вводять в об'єм, що складає 10мл/кг маси тіла. Дози сукралфата, що використовується для порівняння, індометацин та порошок деревинного вугілля суспендують в 1-2 краплинах Твін 80 та розчиняють фізіологічним розчином до 5мл/кг маси тіла (0,9% ваг./об'єм хлориду натрію). Дози N-етилмалеіміда та метилового ефіра NG-нітро-L-аргініна (L-MAME) розчиняють до 6мл/кг маси тіла. Фактор активації тромбоцитів (PAF) розчиняють в 0,25% ваг/об'єм альбуміну бичачої сироватки, що приготована з 0,9% ваг./об'єм розчину хлориду натрію. Використовуються речовини наступних виробників. Гіалуронат цинку (І), (II), (III) та (М), а також гіалуронат натрію (Gedeon Richter); хлорид цинку (Merck); сукралфат (Ulcerlmin R Chugai); індометацин (Sigma); N-етилмалеімід (Fluka); метиловий ефір NG-нітро-Lаргініна (Sigma); L-аргінін (вільна ocновa) (Sigma); D-аргінін (вільна основа) (Sigma); альбумін бичачої сироватки (Sigma); деревинне вугілля (Sigma). Фармакологічну активність асоціата гіалуроната цинку досліджують, застосовуючи наступні способи. 1. Інгібування уражень шлунка, що викликані підкисленим етанолом Використовують самок пацюків RG-Wistar вагою 120-150г, перед експериментами тварини голодують на протязі 24 годин, але отримують достатньо води. Експерименти проводять у відповідності з методом, що подібний методу, який описаний A. Robert (Gastroenterology, 77, 7661 (1979)). У якості сильних подразників використовують підкислений етанол (суміш 50мл абс. етанолу та 1мл концентрованої НСІ). При внутрішньошлунковому введенні доза підкисленого етанолу складає 0,5мл/100г ваги тіла. Сполуки, що досліджуються, вводять перорально за 30 хвилин до введення підкисленого етанолу. При дослідженні тривалості дії вказаної сполуки матеріал, що досліджується, вводять за 60 або 120 хвилин до спровокованої дії, що викликана підкисленим етанолом. Через годину після введення підкисленого етанолу пацюків умертвляють шляхом цервікального зсуву. Шлунки видаляють, розкривають вздовж великої кривизни та обережно промивають. Вимірюють довжину продольних геморагічних уражень. Величину ED50 визначають у вигляді дози, що викликає 50% зниження індексу виразки. Для вивчення механізму дії сполуки, що досліджується, роль ендогенної NO у розвитку шлункового ураження, що викликане підкисленим етанолом, також досліджують шляхом інтраперитонеального введення метилового ефіру L-NG-нітроаргініна (L-NAME). L-NAME у дозі, що складає 25мг/кг, вводять у вигляді ін'єкції за 15 хвилин до сполуки, що досліджується. У наступних експериментах вводять сполуку, що досліджується (перорально), L-NAME (25мг/кг, інтраперитонеально), L-аргінін (400мг/кг, внутрішньовенно) за 30, 45 або 60 хвилин до перорального введення підкисленого етанолу. Результати просумовані у нижченаведених Таблицях. Контрольна група, що включена до Таблиці, отримувала тільки носій (дистильована вода) замість гіалуроната цинку. Таблиця 1 Дія гіалуроната цинку (І) на шлункове пошкодження, що викликане підкисленим етанолом Контроль Гіалуронат цинку (І) № 12 6 13 Доза мг/кг р.о. 1 10 Довжина пошкодження/шлунок 82,4±11,5 95,3±14,8 53,6±7,3* Інгібування % 0 35,0 7 13 50 100 27,4±7,6* 5,4±2,0* 66,7 93,4 * р
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical compositions against peptic ulcer, manufacture process, and method for treating peptic ulcer
Автори англійськоюIlles Janos, Stefko Bela
Назва патенту російськоюФармацевтическая композиция для лечения и профилактики пептической язвы, способ ее получения и способ лечения пептической язвы
Автори російськоюИллеш Янош, Штефко Бела
МПК / Мітки
МПК: A61K 31/715, A61P 1/04
Мітки: пептичної, виразок, пептичних, спосіб, виразки, композиція, фармацевтична, профілактики, лікування, отримання
Код посилання
<a href="https://ua.patents.su/13-62964-farmacevtichna-kompoziciya-dlya-likuvannya-ta-profilaktiki-peptichno-virazki-sposib-otrimannya-ta-sposib-likuvannya-peptichnikh-virazok.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція для лікування та профілактики пептичної виразки, спосіб її отримання та спосіб лікування пептичних виразок</a>