Сполуки та композиція для доставки активних агентів
Номер патенту: 80248
Опубліковано: 10.09.2007
Автори: Верайано Брюс Ф., Бханкаркар Сатадж, Бей Уільям Е., Маджуру Шінгай, Шілдс Лінн, Уейднер Джон Дж.
Формула / Реферат
1. Сполука формули
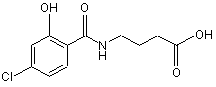
або її сіль.
2. Композиція, що містить
(А) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та
(В) сполуку, що має формулу
 ,
,
її сіль або їх суміш.
3. Композиція за п. 2, яка відрізняється тим, що біологічно активний агент вибраний із групи, яка містить гормони росту, гормони росту людини, рекомбінантні гормони росту людини, гормони росту великої рогатої худоби, гормони росту свині, гормони вивільнення гормонів росту, інтерферони, a-інтерферон, b-інтерферон, g-інтерферон, інтерлейкін-1, інтерлейкін-2, інсулін, інсулін свині, інсулін великої рогатої худоби, інсулін людини, рекомбінантний інсулін людини, інсуліноподібний фактор росту, інсуліноподібний фактор росту-1, кальцитонін, кальцитонін лосося, кальцитонін вугра, кальцитонін людини; еритропоетин (ЕРО), передсердний натрійуретичний фактор, антигени, моноклональні антитіла, соматостатин, адренокортикотропін, гормон вивільнення гонадотропіну, окситоцин, гормон вивільнення лютеїнізуючого гормону, фолікулостимулюючий гормон, глюкоцереброзидазу, тромбопоетин, філграстим, циклоспорин, вазопресин, кромолін натрію, хромоглікат натрію, хромоглікат динатрію, ванкоміцин, паратироїдний гормон, фрагменти паратироїдного гормону; аналоги, фрагменти, міметики та поліетиленглікольмодифіковані похідні цих сполук та будь-яку їх комбінацію.
4. Композиція за п. 3, яка відрізняється тим, що біологічно активний агент вибраний із групи, яка містить інсулін, гормон росту людини, інтерферон, кромолін натрію або їх комбінації.
5. Композиція за п. 3, яка відрізняється тим, що біологічно активним агентом є інсулін.
6. Композиція за п. 3, яка відрізняється тим, що біологічно активним агентом є інтерферон.
7. Композиція за будь-яким з пп. 2-6, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує.
8. Одинична дозована форма, яка містить
(А) композицію, що містить
1) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та
2) сполуку, що має формулу
 ,
,
її сіль або їх суміш та
(В) (a) наповнювач,
(b) розріджувач,
(c) дезінтегратор,
(d) змащувач,
(e) пластифікатор,
(f) барвник,
(g) дозувальний носій або
(h) будь-яку їх комбінацію.
9. Одинична дозована форма за п. 8, яка відрізняється тим, що біологічно активний агент вибирають із групи, яка містить гормони росту, гормони росту людини, рекомбінантні гормони росту людини, гормони росту великої рогатої худоби, гормони росту свині, гормони вивільнення гормонів росту, інтерферони, a-інтерферон, b-інтерферон, g-інтерферон, інтерлейкін-1, інтерлейкін-2, інсулін, інсулін свині, інсулін великої рогатої худоби, інсулін людини, рекомбінантний інсулін людини, інсуліноподібний фактор росту, інсуліноподібний фактор росту-1, кальцитонін, кальцитонін лосося, кальцитонін вугра, кальцитонін людини; еритропоетин (ЕРО), передсердний натрійуретичний фактор, антигени, моноклональні антитіла, соматостатин, адренокортикотропін, гормон вивільнення гонадотропіну, окситоцин, гормон вивільнення лютеїнізуючого гормону, фолікулостимулюючий гормон, глюкоцереброзидазу, тромбопоетин, філграстим, циклоспорин, вазопресин, кромолін натрію, хромоглікат натрію, хромоглікат динатрію, ванкоміцин, паратироїдний гормон, фрагменти паратироїдного гормону; аналоги, фрагменти, міметики та поліетиленглікольмодифіковані похідні цих сполук та будь-яку їх комбінацію.
10. Одинична дозована форма за п. 8, яка відрізняється тим, що біологічно активний агент вибирають із групи, яка містить інсулін, гормон росту людини, інтерферон, кромолін натрію або їх комбінації.
11. Одинична дозована форма за п. 8, яка відрізняється тим, що біологічно активним агентом є інсулін.
12. Одинична дозована форма за п. 8, яка відрізняється тим, що біологічно активним агентом є інтерферон.
13. Одинична дозована форма за п. 8, яка відрізняється тим, що має форму таблетки, капсули, частинок, порошку, саше або рідини.
14. Одинична дозована форма за п. 8, яка відрізняється тим, що дозувальним носієм є рідина, вибрана з групи, яка містить воду, водний розчин пропіленгліколю, фосфатний буфер, 1,2-пропандіол, етанол та будь-яку їх комбінацію.
15. Спосіб одержання композиції, який відрізняється тим, що здійснюють змішування
(А) принаймні одного біологічно активного агента, вибраного із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та
(В) сполуки
 ,
,
її солі або їх суміші; та
(С) необов‘язково, дозувального носія.
16. Спосіб лікування хвороб, які підлягають лікуванню будь-яким з біологічно активних агентів, вибраних з групи, яка містить гормони росту, гормони росту людини, рекомбінантні гормони росту людини, гормони росту великої рогатої худоби, гормони росту свині, гормони вивільнення гормонів росту, інтерферони, a-інтерферон, b-інтерферон, g-інтерферон, інтерлейкін-1, інтерлейкін-2, інсулін, інсулін свині, інсулін великої рогатої худоби, інсулін людини, рекомбінантний інсулін людини, інсуліноподібний фактор росту, інсуліноподібний фактор росту-1, кальцитонін, кальцитонін лосося, кальцитонін вугра, кальцитонін людини; еритропоетин (ЕРО), передсердний натрійуретичний фактор, антигени, моноклональні антитіла, соматостатин, адренокортикотропін, гормон вивільнення гонадотропіну, окситоцин, гормон вивільнення лютеїнізуючого гормону, фолікулостимулюючий гормон, глюкоцереброзидазу, тромбопоетин, філграстим, циклоспорин, вазопресин, кромолін натрію, хромоглікат натрію, хромоглікат динатрію, ванкоміцин, паратироїдний гормон, фрагменти паратироїдного гормону; аналоги, фрагменти, міметики та поліетиленглікольмодифіковані похідні цих сполук та будь-яку їх комбінацію, при якому вводять композицію за п. 3 тварині, що цього потребує.
17. Безводна сполука формули

або її сіль.
18. Сполука за п.17, яка відрізняється тим, що сіль являє собою мононатрієву сіль.
19. Безводний 4-[(4-хлор-2-гідроксибензоїл)аміно]бутаноат натрію.
20. Гідрат 4-[(4-хлор-2-гідроксибензоїл)аміно]бутаноату натрію.
21. Канальний гідрат 4-[(4-хлор-2-гідроксибензоїл)аміно]бутаноату натрію, що має вміст води від 4 до 5,5 %.
22. Фармацевтична композиція, що містить гідрат за п. 20 або 21 та інсулін.
23. Фармацевтична композиція за п. 22, яка відрізняється тим, що вона призначена для перорального застосування.
24. Ізопропанол сольват сполуки формули
 ,
,
або її сіль.
25. Ізопропанол сольват за п. 24, який відрізняється тим, що сіль являє собою мононатрієву сіль.
26. Ізопропанол сольват 4-[(4-хлор-2-гідроксибензоїл)аміно]бутаноату натрію.
27. Композиція, що містить:
(а) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та
(b) безводну сполуку за будь-яким з пп.17-19.
28. Композиція за п. 27, яка відрізняється тим, що активним агентом є інсулін.
29. Композиція за п. 27, яка відрізняється тим, що біологічно активним агентом є гормон росту людини.
30. Композиція за п. 27, яка відрізняється тим, що біологічно активним агентом є рекомбінований гормон росту людини.
31. Композиція за п. 27, яка відрізняється тим, що біологічно активним агентом є кромолін натрію.
32. Композиція за п. 27, яка відрізняється тим, що біологічно активним агентом є гепарин.
33. Композиція за п. 27, яка відрізняється тим, що біологічно активним агентом є кальцитонін.
34. Композиція за п. 27, яка відрізняється тим, що біологічно активним агентом є паратироїдний гормон.
35. Композиція за будь-яким з пп. 27-34, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує.
36. Композиція, що містить:
(а) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та
(b) ізопропанол сольват за будь-яким з пп. 24-26.
37. Композиція за п. 36, яка відрізняється тим, що біологічно активним агентом є інсулін.
38. Композиція за п. 36, яка відрізняється тим, що активним агентом є гормон росту людини.
39. Композиція за п. 36, яка відрізняється тим, що біологічно активним агентом є рекомбінований гормон росту людини.
40. Композиція за п. 36, яка відрізняється тим, що біологічно активним агентом є кромолін натрію.
41. Композиція за п. 36, яка відрізняється тим, що біологічно активним агентом є гепарин.
42. Композиція за п. 36, яка відрізняється тим, що біологічно активним агентом є кальцитонін.
43. Композиція за п. 36, яка відрізняється тим, що біологічно активним агентом є паратироїдний гормон.
44. Композиція за будь-яким з пп. 36-43, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує.
45. Композиція, що містить:
(а) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та
(b) гідрат за будь-яким з пп. 20-21.
46. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є інсулін.
47. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є гормон росту людини.
48. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є рекомбінований гормон росту людини.
49. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є кромолін натрію.
50. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є гепарин.
51. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є кальцитонін.
52. Композиція за п. 45, яка відрізняється тим, що біологічно активним агентом є паратироїдний гормон.
53. Композиція за будь-яким з пп. 45-52, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує.
54. Тверда пероральна дозована форма, яка містить:
(А) композицію, вибрану з групи, що містить композицію за будь-яким з пп. 27-35, композицію за будь-яким з пп. 36-44, композицію за будь-яким з пп. 45-53, та
(В) (а) наповнювач,
(b) розріджувач,
(c) дезінтегратор,
(d) змащувач,
(e) пластифікатор,
(f) барвник,
(g) дозувальний носій, або
(h) будь-яку їх комбінацію.
55. Тверда пероральна дозована форма за п. 54, яка відрізняється тим, що тверда дозована форма являє собою таблетку або капсулу.
56. Тверда пероральна дозована форма за п. 54 або 55, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує.
Текст
1. Сполука формули 2 C2 1 3 80248 роїдний гормон, фрагменти паратироїдного гормону; аналоги, фрагменти, міметики та поліетиленглікольмодифіковані похідні цих сполук та будь-яку їх комбінацію. 4. Композиція за п.3, яка відрізняється тим, що біологічно активний агент вибраний із групи, яка містить інсулін, гормон росту людини, інтерферон, кромолін натрію або їх комбінації. 5. Композиція за п.3, яка відрізняється тим, що біологічно активним агентом є інсулін. 6. Композиція за п.3, яка відрізняється тим, що біологічно активним агентом є інтерферон. 7. Композиція за будь-яким з пп.2-6, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує. 8. Одинична дозована форма, яка містить (А) композицію, що містить 1) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та 2) сполуку, що має формулу OH 11. Одинична дозована форма за п.8, яка відрізняється тим, що біологічно активним агентом є інсулін. 12. Одинична дозована форма за п.8, яка відрізняється тим, що біологічно активним агентом є інтерферон. 13. Одинична дозована форма за п.8, яка відрізняється тим, що має форму таблетки, капсули, частинок, порошку, саше або рідини. 14. Одинична дозована форма за п.8, яка відрізняється тим, що дозувальним носієм є рідина, вибрана з групи, яка містить воду, водний розчин пропіленгліколю, фосфатний буфер, 1,2пропандіол, етанол та будь-яку їх комбінацію. 15. Спосіб одержання композиції, який відрізняється тим, що здійснюють змішування (А) принаймні одного біологічно активного агента, вибраного із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та (В) сполуки O OH O OH N H Cl 4 O OH N H , її сіль або їх суміш та (В) (a) наповнювач, (b) розріджувач, (c) дезінтегратор, (d) змащувач, (e) пластифікатор, (f) барвник, (g) дозувальний носій або (h) будь-яку їх комбінацію. 9. Одинична дозована форма за п.8, яка відрізняється тим, що біологічно активний агент вибирають із групи, яка містить гормони росту, гормони росту людини, рекомбінантні гормони росту людини, гормони росту великої рогатої худоби, гормони росту свині, гормони вивільнення гормонів росту, інтерферони, a-інтерферон, b-інтерферон, gінтерферон, інтерлейкін-1, інтерлейкін-2, інсулін, інсулін свині, інсулін великої рогатої худоби, інсулін людини, рекомбінантний інсулін людини, інсуліноподібний фактор росту, інсуліноподібний фактор росту-1, кальцитонін, кальцитонін лосося, кальцитонін вугра, кальцитонін людини; еритропоетин (ЕРО), передсердний натрійуретичний фактор, антигени, моноклональні антитіла, соматостатин, адренокортикотропін, гормон вивільнення гонадотропіну, окситоцин, гормон вивільнення лютеїнізуючого гормону, фолікулостимулюючий гормон, глюкоцереброзидазу, тромбопоетин, філграстим, циклоспорин, вазопресин, кромолін натрію, хромоглікат натрію, хромоглікат динатрію, ванкоміцин, паратироїдний гормон, фрагменти паратироїдного гормону; аналоги, фрагменти, міметики та поліетиленглікольмодифіковані похідні цих сполук та будь-яку їх комбінацію. 10. Одинична дозована форма за п.8, яка відрізняється тим, що біологічно активний агент вибирають із групи, яка містить інсулін, гормон росту людини, інтерферон, кромолін натрію або їх комбінації. O Cl , її солі або їх суміші; та (С) необов‘язково, дозувального носія. 16. Спосіб лікування хвороб, які підлягають лікуванню будь-яким з біологічно активних агентів, вибраних з групи, яка містить гормони росту, гормони росту людини, рекомбінантні гормони росту людини, гормони росту великої рогатої худоби, гормони росту свині, гормони вивільнення гормонів росту, інтерферони, a-інтерферон, bінтерферон, g-інтерферон, інтерлейкін-1, інтерлейкін-2, інсулін, інсулін свині, інсулін великої рогатої худоби, інсулін людини, рекомбінантний інсулін людини, інсуліноподібний фактор росту, інсуліноподібний фактор росту-1, кальцитонін, кальцитонін лосося, кальцитонін вугра, кальцитонін людини; еритропоетин (ЕРО), передсердний натрійуретичний фактор, антигени, моноклональні антитіла, соматостатин, адренокортикотропін, гормон вивільнення гонадотропіну, окситоцин, гормон вивільнення лютеїнізуючого гормону, фолікулостимулюючий гормон, глюкоцереброзидазу, тромбопоетин, філграстим, циклоспорин, вазопресин, кромолін натрію, хромоглікат натрію, хромоглікат динатрію, ванкоміцин, паратироїдний гормон, фрагменти паратироїдного гормону; аналоги, фрагменти, міметики та поліетиленглікольмодифіковані похідні цих сполук та будь-яку їх комбінацію, при якому вводять композицію за п.3 тварині, що цього потребує. 17. Безводна сполука формули OH O OH N H Cl O або її сіль. 18. Сполука за п.17, яка відрізняється тим, що сіль являє собою мононатрієву сіль. 19. Безводний 4-[(4-хлор-2гідроксибензоїл)аміно]бутаноат натрію. 5 80248 20. Гідрат 4-[(4-хлор-2гідроксибензоїл)аміно]бутаноату натрію. 21. Канальний гідрат 4-[(4-хлор-2гідроксибензоїл)аміно]бутаноату натрію, що має вміст води від 4 до 5,5 %. 22. Фармацевтична композиція, що містить гідрат за п.20 або 21 та інсулін. 23. Фармацевтична композиція за п.22, яка відрізняється тим, що вона призначена для перорального застосування. 24. Ізопропанол сольват сполуки формули 6 , або її сіль. 25. Ізопропанол сольват за п.24, який відрізняється тим, що сіль являє собою мононатрієву сіль. 26. Ізопропанол сольват 4-[(4-хлор-2гідроксибензоїл)аміно]бутаноату натрію. 27. Композиція, що містить: (а) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та (b) безводну сполуку за будь-яким з пп.17-19. 28. Композиція за п.27, яка відрізняється тим, що активним агентом є інсулін. 29. Композиція за п.27, яка відрізняється тим, що біологічно активним агентом є гормон росту людини. 30. Композиція за п.27, яка відрізняється тим, що біологічно активним агентом є рекомбінований гормон росту людини. 31. Композиція за п.27, яка відрізняється тим, що біологічно активним агентом є кромолін натрію. 32. Композиція за п.27, яка відрізняється тим, що біологічно активним агентом є гепарин. 33. Композиція за п.27, яка відрізняється тим, що біологічно активним агентом є кальцитонін. 34. Композиція за п.27, яка відрізняється тим, що біологічно активним агентом є паратироїдний гормон. 35. Композиція за будь-яким з пп.27-34, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує. 36. Композиція, що містить: (а) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та (b) ізопропанол сольват за будь-яким з пп.24-26. 37. Композиція за п.36, яка відрізняється тим, що біологічно активним агентом є інсулін. 38. Композиція за п.36, яка відрізняється тим, що активним агентом є гормон росту людини. 39. Композиція за п.36, яка відрізняється тим, що біологічно активним агентом є рекомбінований гормон росту людини. 40. Композиція за п.36, яка відрізняється тим, що біологічно активним агентом є кромолін натрію. 41. Композиція за п.36, яка відрізняється тим, що біологічно активним агентом є гепарин. 42. Композиція за п.36, яка відрізняється тим, що біологічно активним агентом є кальцитонін. 43. Композиція за п.36, яка відрізняється тим, що біологічно активним агентом є паратироїдний гормон. 44. Композиція за будь-яким з пп.36-43, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує. 45. Композиція, що містить: (а) біологічно активний агент, вибраний із групи, яка містить білки, поліпептиди, пептиди, гормони, кромолін натрію та будь-яку їх комбінацію; та (b) гідрат за будь-яким з пп.20-21. 46. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є інсулін. 47. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є гормон росту людини. 48. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є рекомбінований гормон росту людини. 49. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є кромолін натрію. 50. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є гепарин. 51. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є кальцитонін. 52. Композиція за п.45, яка відрізняється тим, що біологічно активним агентом є паратироїдний гормон. 53. Композиція за будь-яким з пп.45-52, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує. 54. Тверда пероральна дозована форма, яка містить: (А) композицію, вибрану з групи, що містить композицію за будь-яким з пп.27-35, композицію за будь-яким з пп.36-44, композицію за будь-яким з пп.45-53, та (В) (а) наповнювач, (b) розріджувач, (c) дезінтегратор, (d) змащувач, (e) пластифікатор, (f) барвник, (g) дозувальний носій, або (h) будь-яку їх комбінацію. 55. Тверда пероральна дозована форма за п.54, яка відрізняється тим, що тверда дозована форма являє собою таблетку або капсулу. 56. Тверда пероральна дозована форма за п.54 або 55, яка відрізняється тим, що вона призначена для перорального введення тварині, яка цього потребує. Даний винахід стосується сполук для доставки активнихагентів, таких, як біологічно або хімічно активні агенти, до місця призначення. Ці сполуки є добре придатними для утворення нековалентних сумішей з активними агентами для перорального, внутрішньотовстокишкового, пульмонального або інших шляхів введення тваринам. Також описано способи одержання та введення таких композицій. OH O OH N H Cl O 7 80248 Традиційні засоби доставки активних агентів часто бувають жорстко обмежені біологічними, хімічними та фізичними перешкодами. Як правило, ці перешкоди зумовлюються середовищем, через яке відбувається доставка, середовищем об'єкта призначення та/або самим об'єктом призначення. Біологічно та хімічно активні агенти є особливо уразливими до таких перешкод. При введенні тваринам біологічно активних та хімічно активних фармакологічних та терапевтичних агентів перешкоди створюються самим організмом. Прикладами фізичних перешкод є шкіра, ліпідні подвійні шари та мембрани різних органів, які є відносно непроникними для певних активних агентів, але мають бути подолані до досягнення об'єкта призначення, наприклад, кровоносної системи. До хімічних перешкод, крім інших, належать зміни рівня рН у шлунково-кишковому (GI) тракті та ферменти, що розпадаються. На ці перешкоди особливо слід зважати при розробці систем пероральної доставки. Перевагу для введення тваринам багатьох біологічно або хімічно активних агентів віддають пероральному шляхові доставки, якщо це не пов'язано з біологічними, хімічними та фізичними перешкодами. Серед численних агентів, які зазвичай не підлягають пероральному введенню, є біологічно або хімічно активні пептиди, такі, як кальцитонін та інсулін; полісахариди, зокрема, мукополісахариди, включаючи, крім інших, гепарин; гепариноїди; антибіотики; та інші органічні речовини. Ці агенти швидко можуть стати неефективними або бути зруйнованими у шлунково-кишковому тракті через кислотний гідроліз, ферменти і т. ін. Крім того, абсорбції можуть перешкоджати розмір та структура макромолекулярних ліків. Раніше застосовувані способи уразливих при пероральному введенні фармакологічних агентів були пов'язані з паралельним введенням допоміжних засобів (наприклад, резорцинів та неіонних поверхнево-активних речовин, таких, як поліоксіетиленолеїловий етер та nгексадецилполіетиленовий етер) для штучного збільшення проникності стінок кишечника, а також паралельне введення ферментних інгібіторів (наприклад, інгібіторів трипсину підшлункової залози, діізопропілфторофосфату (DFF) та тразинолу) для інгібування ферментного розпаду. Як системи доставки ліків для інсуліну та гепарину, також було описано ліпосоми. Однак широкому застосуванню таких систем доставки ліків перешкоджають такі чинники: (1) ці системи вимагають токсичних кількостей допоміжних засобів або інгібіторів; (2) відсутність придатних вантажів, тобто, активних агентів низькоїмолекулярної маси; (3) системи виявляють погану стійкість і мають недостатній термін зберігання; (4) виробництво систем пов'язане з труднощами; (5) системи не захищають активний агент (вантаж); (6) системи негативним чином змінюють активний агент; або (7) системи не забезпечують або не сприяють абсорбції активного агента. Останнім часом для доставки фармацевтичних препаратів застосовують протеїноїдні мікросфери. [Наприклад, див. US 5,401,516, US 8 5,443,841 та US RE35,862]. Крім того, для доставки фармацевтичних препаратів застосовують деякі модифіковані амінокислоти. [Див., наприклад, US 5,629,020; US 5,643,957; US 5,766,633; US 5,776,888 та US 5,866,536]. Однак і нині відчувається потреба у простих, недорогих системах доставки, які можуть бути легко одержані і які є придатними для доставки широкого кола активних агентів різними шляхами. Пропонуються сполуки та композиції, які є корисними для доставки активних агентів. Даний винахід охоплює сполуки, які мають представлену нижче формулу, або їхні солі, або їхні суміші. Композиції даного винаходу включають принаймні один активний агент, в оптимальному варіанті - біологічно або хімічно активний агент, та принаймні одну зі сполук даного винаходу або їхніх солей. Пропонуються також способи одержання та введення таких композицій. Також пропонуються форми дозованих одиниць, які включають ці композиції. Форма дозованої одиниці може мати тверду форму (наприклад, таблетка, капсула або частинки, наприклад, порошок або саше) або рідку форму. Пропонуються також способи введення біологічно активного агента тварині, яка його потребує, зокрема, пероральним, внутрішньотовстокишковим або пульмональним шляхами, з композиціями даного винаходу, а також способи лікування з застосуванням таких композицій. Пропонується спосіб лікування хвороб тварин, який включає введення композиції даного винаходу тварині, яка цього потребує. Сполуки Сполуки можуть бути у формі карбонової кислоти та/або її солей. Солі можуть бути органічними та неорганічними солями, наприклад, солями лужних металів, таких, як натрій, калій та літій; солі лужноземельних металів, таких, як магній, кальцій або барій; солями амонію; основними амінокислотами, такими, як лізин або аргінін; органічними амінами, такими, як диметиламін або піридин. В оптимальному варіанті солі є солями натрію. Солі можуть бути моно- або багатовалентними солями, такими, як моно- та динатрієві солі. Солі також можуть бути сольватами, включаючи сольвати етанолу. Крім того, застосовують поліамінокислоти та пептиди, які включають одну або кілька з цих сполук. Амінокислота є будь-якою карбоновою кислотою, яка має принаймні одну вільну аміногрупу і може бути як природною, так і синтетичною амінокислотою. Поліамінокислоти є або пептидами (які являють собою дві або кілька амінокислот, з'єднаних пептидним зв'язком) або є двома або кількома амінокислотами, з'єднаними зв'язком, утвореним іншими групами, які можуть бути зв'язані, наприклад, естерним або ангідридним зв'язком. Пептиди можуть мати різну довжину, від дипептидів з дво 9 80248 ма амінокислотами до поліпептидів із кількома сотнями амінокислот. Одна або кілька амінокислот або пептидних ланок можуть бути ацилованими або сульфонованими. Описані нами сполуки можуть походити від амінокислот і легко можуть бути одержані з амінокислот звичними для спеціалістів способами на основі даного опису та способами, [описаними у WO96/30036, WO97/36480, US 5,643,957 та US 5,650,385]. Наприклад, сполуки можуть бути одержані шляхом реакції однієї амінокислоти з відповідним ацилюючим або аміномодифікуючим агентом, який реагує з вільним амінним компонентом, присутнім в амінокислоті, для утворення амідів. Застосовують захисні групи для уникнення небажаних побічних реакцій, які можуть бути відомими спеціалістам. Захисні групи згадуються [в роботі T.W.Greene, Protecting Groups in Organic Synthesis, Wiley, New York (1981)], на зміст якої авторами робиться посилання. Солі даної сполуки одержують відомими спеціалістам способами. Наприклад, солі натрію одержують шляхом розчинення сполуки в етанолі й додавання водного розчину гідроксиду натрію. Сполуку очищають шляхом рекристалізації або фракціонування на одній або кількох твердих хроматографічних основах, розташованих окремо або зв'язаних послідовно. Придатними системами рекристалізаційних розчинників є, крім інших, ацетонітрил, метанол та тетрагідрофуран. Фракціонування здійснюють на відповідній хроматографічній основі, такій як глинозем, з використанням сумішей метанолу / n-пропанолу як рухомої фази; шляхом обернено-фазової хроматографії з використанням сумішей трифторооцтової кислоти/ацетонітрилу як рухомої фази; іонообмінної хроматографії з використанням води або відповідного буфера як рухомої фази. У разі аніонообмінної хроматографії в оптимальному варіанті застосовують градієнт хлорид натрію 0-500мМ. Згідно з одним варіантом втілення, сполуку застосовують у її безводній формі. Активні агенти До активних агентів, придатних для застосування у даному винаході, належать біологічно активні агенти та хімічно активні агенти, включаючи, крім інших, пестициди, фармакологічні агенти та терапевтичні агенти. Наприклад, до біологічно або хімічно активних агентів, придатних для застосування у даному винаході, належать, крім інших, білки, поліпептиди, пептиди, гормони, полісахариди, зокрема, суміші мукополісахаридів, вугле води, ліпіди, інші органічні сполуки, зокрема, сполуки, які самі не проникають (або які проникають лише як частина введеної дози) крізь шлунково-кишкову слизову оболонку і/або є схильними до хімічного розщеплення з боку кислот та ферментів у шлунково-кишковому тракті; або будь-яка їхня комбінація. Іншими прикладами, крім інших, є нижчезазначені, включаючи їхні синтетичні, природні, або рекомбінантні джерела: гормони росту, включаючи гормони росту людини (hGH), рекомбінантні гормони росту людини (rhGH), гормони росту великої рогатої худоби та гормони росту свині; гормони 10 вивільнення гормонів росту, інтер ферони, включаючи a, b та g, інтерлейкін-1; інтерлейкін-2; інсулін, включаючи інсулін свині, великої рогатої худоби, людини та рекомбінантний інсулін людини, які необов'язково мають протиіони, включаючи натрій, цинк, кальцій та амоній; інсуліноподібний фактор росту, включаючи IGF-1; гепарин, включаючи нефракціонований гепарин, гепариноїди, дерматани, хондроїтини, гепарин низькоїмолекулярної маси, гепарин дуже низькоїмолекулярної маси та гепарин наднизькоїмолекулярної маси; кальцитонін, включаючи кальцитонін лосося, вугра, свині та людини; еритропоетин; передсердний натрійуретичний фактор; антигени; моноклональні антитіла; соматостатин; інгібітори протеази; адренокортикотропін, гормон вивільнення гонадотропіну; окситоцин; гормон вивільнення лютеїнізуючого гормону; фолікулостимулюючий гормон; глюкоцереброзидаза; тромбопоетин; філграстим; простагландини; циклоспорин; вазопресин; кромоліннатрій (натрійабо динатрійхромоглікат); ванкоміцин; десферіоксамін (DFO); паратиреоїдний гормон (РТН), включаючи його фрагменти; протимікробні агенти, включаючи протигрибкові агенти; вітаміни; аналоги, фрагменти, міметики або модифіковані поліетиленгліколем (PEG) похідні цих сполук; або будь-яка їхня комбінація. Інші придатні форми інсуліну, включаючи, крім інших, синтетичні форми інсуліну, [описано у патентах США №№4,421,665, 5,474,978 та 5,534,486], на кожен з яких авторами робиться посилання в повному обсязі. Системи доставки Композиції даного винаходу включають агент доставки та один або кілька активних агентів. В одному варіанті втілення одну або кілька сполук агентів доставки, або солей цих сполук, або поліамінокислот чи пептидів, з яких утворюються один або кілька елементів цих сполук або солей, застосовують як агент доставки шляхом змішування з активним агентом до введення. Композиції для введення можуть мати рідку форму. Дозувальним носієм може бути вода (наприклад, для кальцитоніну лосося, паратиреоїдного гормону та еритропоетину), 25% водний розчин пропіленгліколю (наприклад, для гепарину) та фосфатний буфер (наприклад, для rhGH). До інших дозувальних носіїв належать поліетиленгліколі, сорбіт, маніт і цукроза. Дозувальні розчини одержують шляхом змішування розчину сполуки агента доставки з розчином активного агента безпосередньо перед введенням, В альтернативному варіанті розчин агента доставки (або активного агента) змішують із твердою формою активного агента (або агента доставки). Сполука агента доставки та активний агент також можуть бути змішані у вигляді сухи х порошків. Сполука агента доставки та активний агент також можуть бути домішані під час процесу виробництва. Дозувальні розчини необов'язково можуть містити додатки, такі, як фосфатно-буферні солі, лимонна кислота, гліколі або інші диспергатори. До розчину можуть бути включені стабілізуючі додатки, в оптимальному варіанті - у концентрації від приблизно 0,1 до 20% (маса/об'єм). 11 80248 Композиції для введення в альтернативному варіанті можуть бути у формі твердої речовини, наприклад, у вигляді таблетки, капсули або частинок, наприклад, у вигляді порошку або саше. Тверді дозовані форми одержують шляхом змішування твердої форми сполуки з твердою формою активного агента. В альтернативному варіанті тверду речовину одержують із розчину сполуки та активного агента відомими спеціалістам способами, такими, як сублімаційне висушування, осадження, кристалізація та диспергування твердих частинок. Композиції для введення згідно з даним винаходом також можуть включати один або кілька інгібіторів ферментів. До таких інгібіторів ферментів належать, крім інших, такі сполуки, як актинонін або епіактинонін та їхні похідні. Іншими інгібіторами ферментів, крім інших, є апротинін (Тразинол) та інгібітор Боумена-Бірка. Кількість активного агента, який застосовують у композиції для введення згідно з даним винаходом, є кількістю, ефективною для досягнення конкретним активним агентом мети призначення. Кількість активного агента в композиціях, як правило, є фармакологічно, біологічно, терапевтично або хімічно ефективною кількістю. Однак ця кількість може бути меншою за кількість при застосуванні композиції у формі дозованої одиниці, оскільки форма дозованої одиниці може містити багато композицій сполук/активних агентів або може містити розподілену фармакологічно, біологічно, терапевтично або хімічно ефективну кількість. Загальну ефективну кількість вводять у сукупних одиницях, які загалом містять ефективну кількість активного агента. Загальну кількість активного агента, який має бути застосований, визначають відомими спеціалістам способами. Однак, оскільки дані композиції можуть доставляти активні агенти ефективніше, ніж попередні композиції, суб'єктові можна вводити меншу кількість біологічно або хімічно активних агентів порівняно з кількістю, яку застосовували у попередніх формах дозованих одиниць або системах доставки з досягненням такого ж самого рівня в крові та/або терапевтичного ефекту. Описані нами сполуки доставляють біологічно та хімічно активні агенти, зокрема, у пероральних, інтраназальних, під'язикових, інтрадуоденальних, підшкірних, букальних, вн утрішньотовстокишкових, ректальних, вагінальних, мукозальних, пульмональних, крізьшкірних, вн утрішньошкірних, парентеральних, внутрішньовенних, внутрішньом'язових та очних системах, а також при подоланні гематоенцефалічного бар'єру. Форми дозованих одиниць також можуть включати будь-який з наповнювачів, розріджувачів, дезінтеграторів, змащувачів, пластифікаторів, барвників, ароматизаторів, агентів, які коригують смак ліків, цукрів, підсолоджувачів, солей та дозувальних носіїв, або їхню комбінацію, включаючи, крім інших, воду, 1,2-пропандіол, етанол, оливкову олію або будь-яку їхню комбінацію. Сполуки та композиції, які є предметом винаходу, є корисними для введення біологічно або хімічно активних агентів будь-яким тваринам, 12 включаючи, крім інших, крім інших, птахів, таких, як курка; ссавців, таких, як гризуни, корова, свиня, собака, кіт, примати, зокрема, людина, та комах. Ця система є особливо вигідною для доставки хімічно або біологічно активних агентів, які за інших умов були б зруйновані або стали б менш ефективними через умови, з якими активний агент стикається, перш, ніж досягає зони призначення (тобто, ділянки, в якій має вивільнюватись активний агент композиції для доставки) у межах організму тварин, яким вони вводяться. Зокрема, сполуки та композиції даного винаходу є корисними для перорального введення активних агентів, особливо, ти х, які зазвичай не можуть бути доставлені пероральним шляхом, або тих, які вимагають поліпшення доставки. Композиції, які включають сполуки та активні агенти, мають застосування для доставки активних агентів до вибраних біологічних систем та підвищення або поліпшення біоакумуляції активного агента порівняно з введенням активного агента без агента доставки. Доставка може бути поліпшена шляхом доставлення більш активного агента за період часу або при доставленні активного агента у конкретний період часу (наприклад, для здійснення прискореної або уповільненої доставки) або протягом періоду часу (наприклад, при тривалій доставці). Після введення активний агент, присутній у композиції або формі дозованої одиниці, надходить до системи кровообігу. Біоакумуляцію агента можна легко визначити шляхом вимірювання відомої фармакологічної дії в крові, наприклад, збільшення часу згортання крові, викликаного гепарином, або зменшення рівня циркуляції кальцію, викликаного кальцитоніном. В альтернативному варіанті сам рівень циркуляції активного агента може бути виміряний безпосередньо. Нижченаведені приклади пояснюють винахід, не обмежуючи його обсягу. Усі частки представлено за масою, якщо не вказано інше. Приклад 1 - Одержання сполуки 1а. Одержання сполуки 1. 4-хлоросаліцилову кислоту (10,0г, 0,0579моль) додавали в одношийкову 250мл колбу з круглим дном, яка містила приблизно 50мл метиленхлориду. Розпочинали перемішування, яке тривало решту часу реакції. У колбу порціями додавали зв'язувальний агент 1,1-карбонілдіімідазол (9,39г, 0,0579моль) у вигляді твердої речовини. Реакційну суміш перемішували при кімнатній температурі протягом приблизно 20 хвилин після додавання всієї кількості зв'язувального агента, а потім у колбу при перемішуванні додавали етил-4амінобутиратгідрохлорид (9,7г, 0,0579моль). З лійки для додавання по краплях додавали триетиламін (10,49мл, 0,0752моль). Лійку для додавання споліскували метиленхлоридом. Реакційну суміш залишали перемішуватися при кімнатній температурі до наступного дня. Реакційну суміш виливали у ділильну лійку і промивали 2N НСІ з утворенням емульсії. Емульсію залишали стояти протягом двох днів. Після цього емульсію фільтрували крізь целіт у фритованій скляній лійці. Фільтрат повертали до ділиль 13 80248 ної лійки для відокремлення шарів. Органічний шар висушували над сульфатом натрію, який потім відфільтровували, і фільтрат концентрували у роторному випарнику. Одержаний в результаті твердий матеріал піддавали гідролізові за допомогою 2N NaOH, зберігали до наступного дня у замороженому вигляді, а потім гідролізацію відновлювали. Розчин підкислювали за допомогою 2N HCL and і утворені тверді речовини відокремлювали, висушували у вакуумі і двічі рекристалізували, використовуючи метанол/воду. Тверді фази осаджували до наступного дня, відокремлювали й висушували. Тверді фази розчиняли у 2N NaOH і рівень рН зразка доводили до рН5 за допомогою 2N НСІ. Тверді фази збирали, і HPLC виявляла один пік. Ці тверді фази після цього рекристалізували у метанолі/воді, відокремлювали, а потім висушували у вакуумі, одержуючи на виході 4,96г (33,0%) 4-(4 хлоро-2-гідроксибензоїл) аміномасляної кислоти. (C11H12CINO4 ; молекулярна маса 257,67). Точка плавлення: 131-133°С. Органічний елементарний аналіз: %С: 51,27 (розрах.), 51,27 (виявл.); %Н: 4,69 (розрах.), 4,55 (виявл.); %N: 5,44 (розрах.), 5,30 (виявл.). Η ЯМР-аналіз: (d6-DMSO): δ 13,0. s, 1H (СООН); δ 12,1, s, 1Η (ОН); δ 8,9, t, 1Н (ΝΗ); δ 7,86, d, 1Η (Η орто-амід); δ 6,98, d, 1Н (Η орто-фенол ОН); δ 6,96, d, 1Η, (Η мета-амід); δ 3,33, m, 2H (CH2 суміжний з ΝΗ); δ 2,26, t, 2Н (СН2 суміжний з СООН); δ 1,80, m, 2Н (аліфатичн. СН2 бета-NH та СН2 бета-СООН). 1b. Додаткове одержання сполуки 1. 4-хлоросаліцилову кислоту (25,0г, 0,1440моль) додавали в одношийкову 250мл колбу з круглим дном 1, яка містила приблизно 75-100мл метилен хлорид. Розпочинали перемішування, яке тривало решту часу реакції. У колбу порціями додавали зв'язувальний агент 1,1-карбонілдіімідазол (23,5г, 0,1448моль) у вигляді твердої речовини. Реакційну суміш перемішували при кімнатній температурі протягом приблизно 20 хвилин після додавання всієї кількості зв'язувального агента, а потім у колбу при перемішуванні додавали етил-4амінобутират гідрохлорид (24,3г, 0,1448моль). З лійки для додавання по краплях додавали триетиламін (26,0мл, 0,18824моль). Лійку для додавання споліскували метиленхлоридом. Реакційну суміш залишали перемішуватися при кімнатній температурі до наступного дня. Реакційну суміш виливали у а ділильну лійку і промивали 2N НСІ з утворенням емульсії. Емульсію фільтрували крізь целіт у фритованій скляній лійці. Фільтрат повертали до ділильної лійки для відокремлення шарів. Органічний шар промивали водою та розсолом, потім висушували над сульфатом натрію, який потім відфільтровували, і фільтрат концентрували у роторному випарнику. Одержаний в результаті твердий матеріал піддавали гідролізові за допомогою 2N NaOH до наступного дня. Розчин підкислювали за допомогою 2N НСІ, і утворені бурі тверді речовини рекристалізували, використовуючи метанол / воду, відфільтровуючи при високій температурі нерозчинний чорний матеріал. Білі тверді фази осаджували, відокремлювали й висушували, одержуючи на виході 11,68г (37,0%) 4-(4 хлоро-2-гідроксибензоїл) 14 аміномасляної кислоти. (C 11H12CINO4;молекулярна маса 257,67). Точка плавлення: 129-133°С. Органічний елементарний аналіз: %С: 51,27 (розрах.), 51,26 (виявл.); %Н: 4,69 (розрах.), 4,75 (виявл.); %N: 5,44 (розрах.), 5,32 (виявл.). Η ЯМР-аналіз: (d6-DMSO): δ 13,0, s, 1Н (СООН); δ 12,1, s, 1Η (ОН); δ 8,9, t, 1Η (ΝΗ); δ 7,86, d, 1Η (Η орто-амід); δ 6,98, d, 1Н (Η орто-фенол ОН); δ 6,96, d, 1H, (Η мета-амід); δ 3,33, m, 2Η (СН2 суміжний з ΝΗ); δ 2,28, t, 2Н (СН2 суміжний з СООН); δ 1,80, m, 2Н (аліфатичн. СН2 бета-NH та СН2 бета-СООН). 1с. Додаткове одержання сполуки 1 (4-[(4-хлоро-2-гідроксибензоїл)аміно]бутанова кислота) 22л, п'ятишийкову колбу з круглим дном було оснащено насадною мішалкою, 1л пасткою ДінаСтарка з парціальним конденсатором, термоелектричним індикатором температури та нагрівним кожухом. Описану нижче реакцію здійснювали в атмосфері сухого азоту. До реакційної колби завантажували реагент n-бутанол (5000мл) та 4хлоросаліцилову кислоту (2000г, 11,59моль). Пастку Діна-Старка заповнювали n-бутанолом (1000мл). Додавали концентровану сірчану кислоту (50г). Реакційну суміш нагрівали до дефлегмації протягом приблизно 120 годин. За цей час у пастці збиралося приблизно 206мл води. Нагрівний кожух знімали і реакційній суміші давали охолонути до навколишньої температури. Пастку Діна-Старка звільняли від води і знімали. Заливали деіонізовану воду (1000мл). Двофазну суміш перемішували протягом 10 хвилин. Перемішування припиняли і фазам давали розділитись. Нижчу водну фазу відкачували сифоном і зливали. До реакційної суміші додавали 10мас.% водний розчин бікарбонату натрію (1000мл). Суміш перемішували протягом 10 хвилин. Реакційну суміш перевіряли паперовим індикатором рН, щоб пересвідчитись у тому, що рН розчину є більшим за 7. До реакційної суміші додавали воду (500мл). Перемішування припиняли і фазам давали розділитись. Нижчий водний шар відкачували сифоном і зливали. Реакційну суміш промивали ще однією 500мл порцією деіонізованої води. Реактор настроювали на атмосферну дистиляцію у 5л приймач. Суміш відганяли, доки температура у посудині не підніметься до 140150°С. Дистиляцію перемикали з атмосферної дистиляції на вакуумну дистиляцію. Тиск у дистиляційній установці повільно знижували до 100мм рт.ст. Температура у посудині знижувалася, і решту n-бутанолу та n-бутилового етеру (побічний продукт реакції) відганяли. Нагрівання припиняли і реакційній суміші давали охолонути до навколишньої температури. Вакуум порушували сухим азотом. Необроблений бутиловий естер переносили до 5л колби установки для вакуумної дистиляції. Необроблений бутиловий естер відганяли в умовах тиску від 0,2 до 0,5мм рт.ст. Легку фракцію, зібрану при підвищеній температурі
ДивитисяДодаткова інформація
Назва патенту англійськоюCompounds and compositions for delivering active agents
Автори англійськоюWeidner John J., Variano Bruce F., Majuru Shingai, Bhankarkar Sataj, Bay Williame, Shields Lynn
Назва патенту російськоюСоединения и композиция для доставки активных агентов
Автори російськоюУэйднер Джон Дж., Верайано Брюс Ф., Маджуру Шингай, Бханкаркар Сатадж, Бей Уильям Э., Шилдс Линн
МПК / Мітки
МПК: A61K 9/20, A61K 9/08, A61K 47/10, A61K 47/34, A61K 38/28, A61K 9/48, C07C 235/60, C07C 235/52, A61K 38/21, A61K 9/16, A61K 38/27, A61K 47/16, A61K 9/14, A61K 47/04, A61K 31/352, A61K 45/06
Мітки: доставки, сполуки, композиція, агентів, активних
Код посилання
<a href="https://ua.patents.su/13-80248-spoluki-ta-kompoziciya-dlya-dostavki-aktivnikh-agentiv.html" target="_blank" rel="follow" title="База патентів України">Сполуки та композиція для доставки активних агентів</a>
Попередній патент: Напрямний апарат та діафрагма напрямного апарата в газотурбінному двигуні
Наступний патент: Капсуль-детонатор
Випадковий патент: Склоемалева фрита подвійного призначення












