Тверді форми (2s,3r,4r,5s,6r)-2-(4-хлор-3(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2н-піран-3,4,5-тріолу і їх застосування
Номер патенту: 106048
Опубліковано: 25.07.2014
Автори: Перлберг Анетт, Чжао Меттью Манчжу, Поль Сьюзан Маргарет де
Формула / Реферат
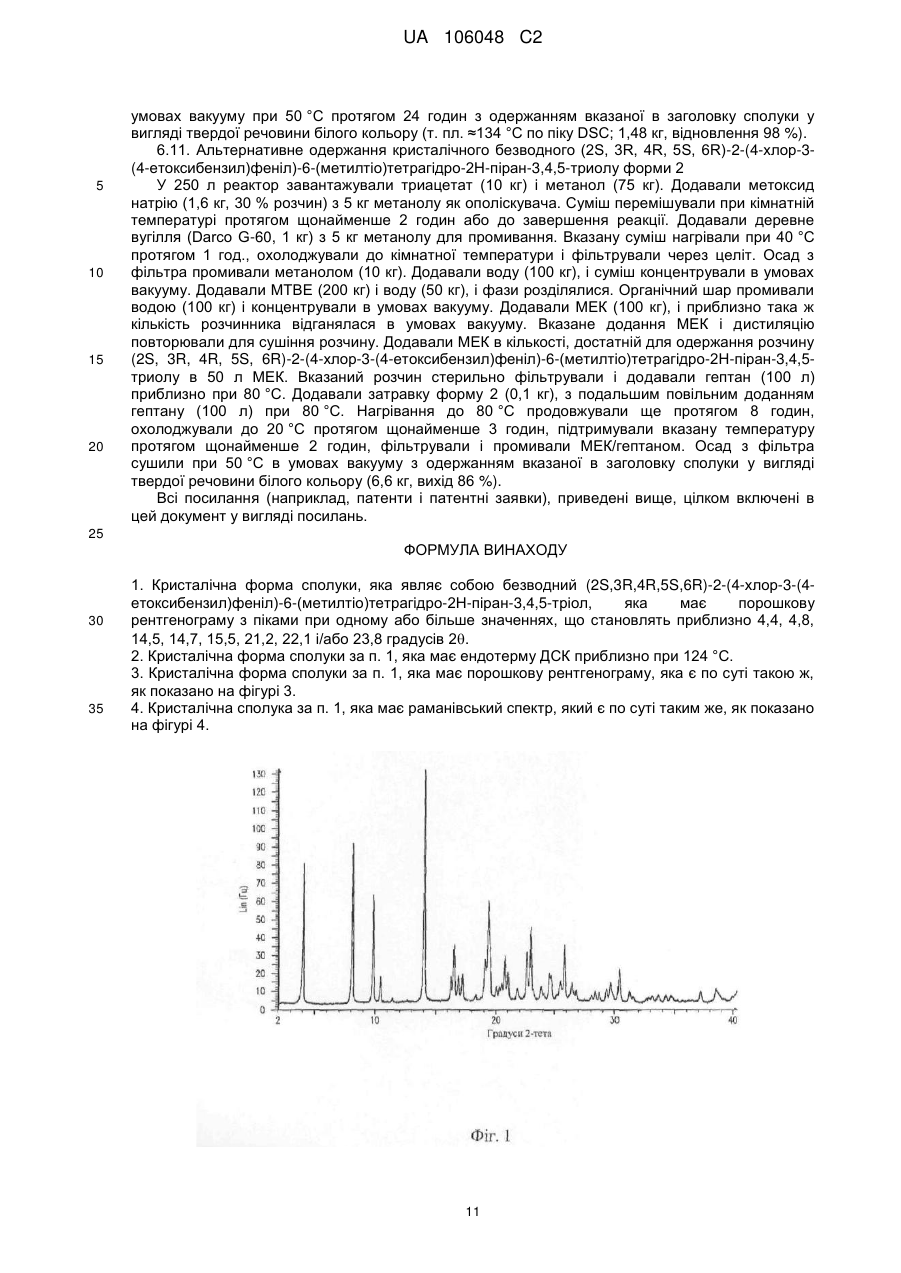
1. Кристалічна форма сполуки, яка являє собою безводний (2S,3R,4R,5S,6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-тріол, яка має порошкову рентгенограму з піками при одному або більше значеннях, що становлять приблизно 4,4, 4,8, 14,5, 14,7, 15,5, 21,2, 22,1 і/або 23,8 градусів 2q.
2. Кристалічна форма сполуки за п. 1, яка має ендотерму ДСК приблизно при 124 °C.
3. Кристалічна форма сполуки за п. 1, яка має порошкову рентгенограму, яка є по суті такою ж, як показано на фігурі 3.
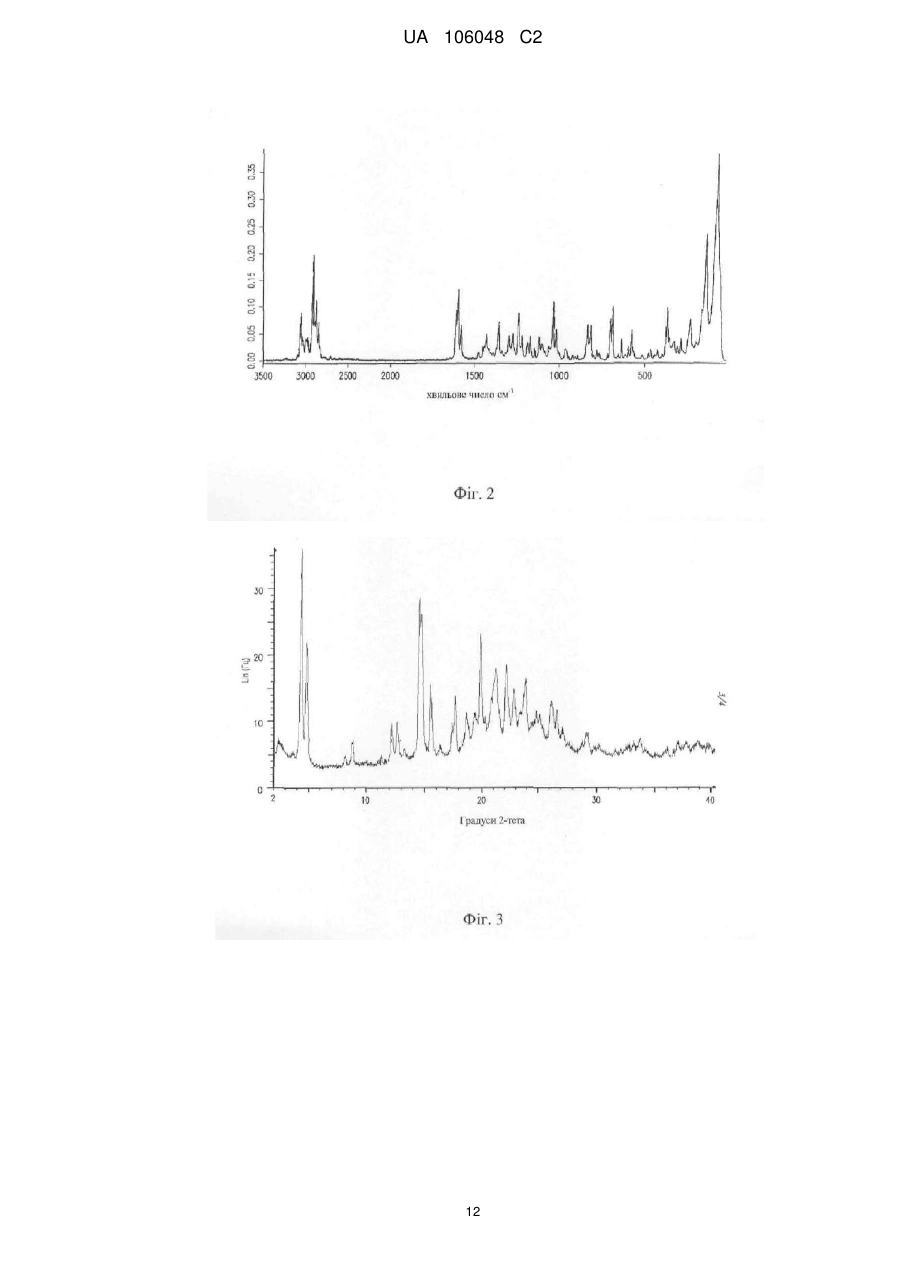
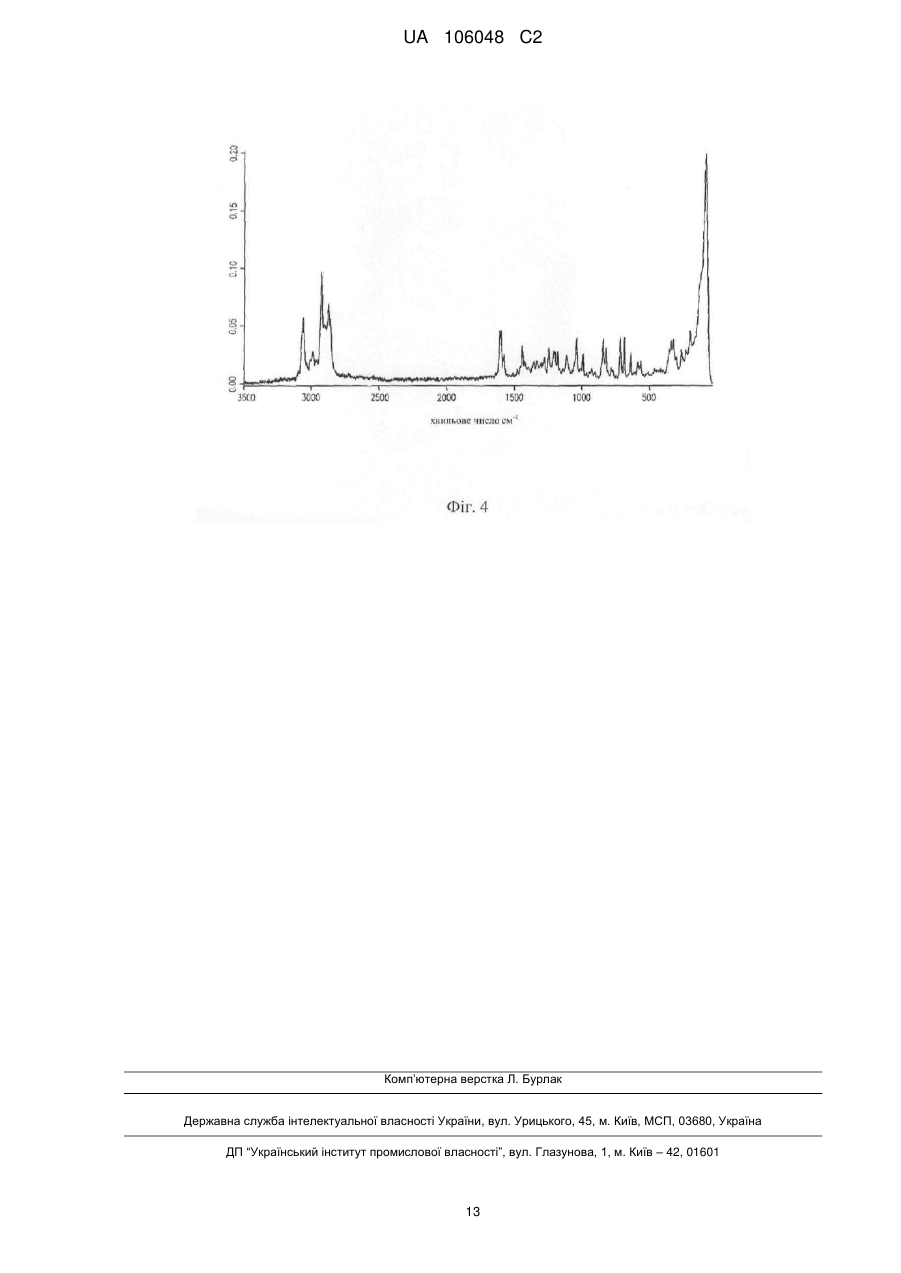
4. Кристалічна сполука за п. 1, яка має раманівський спектр, який є по суті таким же, як показано на фігурі 4.
Текст
Реферат: Винахід стосується кристалічної форми (2S,3R,4R,5S,6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6(метилтіо)тетрагідро-2Н-піран-3,4,5-тріолу, а також її застосування для лікування різних захворювань і розладів. UA 106048 C2 (12) UA 106048 C2 UA 106048 C2 5 10 15 20 25 30 35 40 45 50 ОПИС Дана заявка заявляє пріоритет згідно з попередньою заявкою США № 61/081423, поданою 17 липня 2008 р., яка повністю включена в цей документ шляхом посилання. 1. Галузь ВИНАХОДУ Даний винахід стосується твердих форм (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу і способів їх застосування. 2. РІВЕНЬ ТЕХНІКИ Різні тверді форми однієї і тієї самої сполуки можуть мати властивості, що значно розрізнюються. Наприклад, аморфна форма лікарської речовини може мати властивості розчинності і характеристики біодоступності, відмінні від властивості її кристалічної форми (форм), властивості, які можуть впливати на те, як слід вводити лікарську речовину, щоб одержати оптимальний ефект. Аморфні і кристалічні форми лікарської речовини також можуть мати властивості, що розрізнюються при обробці (наприклад, текучість, стисливість), швидкості розчинення, розчинності і стабільностей, які можуть впливати на виготовлення препаративних форм. Відповідно, одержання різних форм лікарської речовини є бажаним з ряду причин. Крім того, регулюючі органи (наприклад, Управління по нагляду за якістю харчових продуктів і лікарських речовин США) можуть вимагати ідентифікації всіх твердих (наприклад, поліморфних) форм нової лікарської субстанції раніше продуктів, які їх містять. А. Goho, Science News 166(8): 122-123 (2004). Сполуки можуть існувати в одній або більше кристалічних формах, але існування і характеристики вказаних форм не можна передбачити з цілковитою певністю. Крім цього, не існує стандартної процедури для одержання всіх можливих поліморфних форм сполуки. Навіть після ідентифікації одного поліморфа існування і характеристики інших форм можна визначити тільки після додаткового експериментування. 3. СУТЬ ВИНАХОДУ Даний винахід спрямований частково на аморфні і кристалічні форми безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу, який являє собою інгібітор натрій-глюкозного співтранспортера 2. Один варіант здійснення даного винаходу охоплює фармацевтичні композиції, включаючи тверді форми, описані в цьому документі. Інший варіант здійснення даного винаходу охоплює способи інгібування активності SGLT2, а також способи лікування, профілактики і контролю різних захворювань і розладів з використанням твердих форм, описаного в цьому документі. 4. КОРОТКИЙ ОПИС ФІГУР Фігура 1 являє собою порошкову рентгенограму аналізу (XRPD) форми 1 кристалічного безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Нпіран-3,4,5-триолу. Рентгенограму отримували з використанням Bruker D8 Advance System (випромінювання Cu Kα) з детектором VANTEC-1. Фігура 2 являє собою FT-раманівський спектр форми 1 кристалічного безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу. Спектр отримували з використанням Bruker RFS100 із збудженням при 1064 нм. Фігура 3 являє собою рентгенограму XRPD форми 2 кристалічного безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу. Рентгенограму отримували з використанням Bruker D8 Advance System (випромінювання Cu Kα) з детектором VANTEC-1. Фігура 4 являє собою FT-раманівський спектр форми 2 кристалічного безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу. Спектр отримували з використанням Bruker RFS100 із збудженням на 1064 нм. 5. ДОКЛАДНИЙ ОПИС ВИНАХОДУ Даний винахід спрямований частково на тверді (наприклад, кристалічні) форми безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5триолу: 1 UA 106048 C2 5 10 15 20 25 30 35 40 45 50 55 Сполука являє собою інгібітор натрій-глюкозного співтранспортера 2 і може застосовуватися для лікування діабету і ряду інших захворювань і станів. Див. патентну заявку США № 11/862690, подану 28 вересня 2007 р. Даний винахід спрямований також на препаративні форми, що включають в себе тверді форми безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу, і на способи їх застосування. 5.1. Визначення Якщо не вказано інше, терміни "контролювати", "контролювання" і "контроль" означають запобігання рецидивам конкретного захворювання або розладу у пацієнта, який вже страждав вказаним захворюванням або розладом, і/або подовження терміну,протягом якого у пацієнта, який страждав вказаним захворюванням або розладом, зберігається ремісія. Терміни охоплюють модулювання порога, розвитку і/або тривалості захворювання або розладу або зміну характеру реакції пацієнта на захворювання або розлад. Якщо не вказано інше, терміни "запобігати", "запобігання" і "профілактика" мають на увазі дію, яка має місце до того, як пацієнт почне страждати від конкретного захворювання або розладу, яке інгібує або зменшує тяжкість захворювання або розладу. Іншими словами, всі вказані терміни означають профілактику. Якщо не вказано інше, "профілактично ефективна кількість" сполуки являє собою кількість, достатню для запобігання захворюванню або розладу або одного або більше симптомів, пов'язаних із захворюванням або розладом, або для запобігання його рецидиву. Профілактично ефективна кількість сполуки означає таку кількість терапевтичного агента, окремо або в комбінації з іншими агентами, яка забезпечує профілактичну сприятливу дію для запобігання захворюванню або розладу. Термін "профілактично ефективна кількість" може включати в себе кількість, яка поліпшує загальну профілактику або посилює профілактичну ефективність іншого профілактичного агента. Якщо не вказано інше, "терапевтично ефективна кількість" сполуки являє собою кількість, достатню для забезпечення терапевтично сприятливого ефекту для лікування або контролю захворювання або розладу, або для затримки або зведення до мінімуму одного або більше симптомів, пов'язаних із захворюванням або розладом. Терапевтично ефективна кількість сполуки означає таку кількість терапевтичного агента, окремо або в комбінації з іншими агентами, яка забезпечує терапевтичну сприятливу дію для лікування або контролю захворювання або розладу. Термін "терапевтично ефективна кількість" може включати в себе кількість, яка поліпшує загальну терапію, зменшує або допомагає уникнути симптомів або випадків захворювання або розладу або посилює терапевтичну ефективність іншого терапевтичного агента. Якщо не вказано інше, терміни "лікувати", "спосіб лікування" і "лікування" мають на увазі дію, яка має місце під час того, як пацієнт страждає від конкретного захворювання або розладу, який зменшує тяжкість захворювання або розладу або одного або більше з його симптомів, або затримує або сповільнює прогресування захворювання або розладу. Якщо не вказано інше, термін "включають" має те ж значення, що "включають, без обмеження", а термін "включає" має те ж значення, що "включає, без обмеження". Подібно цьому термін "такий як" має те ж значення, що "такий як, без обмеження". Якщо не вказано інше, один або більше прикметників, безпосередньо попередні ряду іменників, потрібно тлумачити як такі, що застосовуються до кожного з іменників. Наприклад, фраза "необов'язково заміщений алкіл, арил або гетероарил" має те ж значення, що "необов'язково заміщений алкіл, необов'язково заміщений арил або необов'язково заміщений гетероарил". Потрібно зазначити також, що будь-який атом, показаний на кресленні, з вільними валентностями передбачає зв'язок з атомами водню в кількості, достатній, щоб зайняти валентності. Крім цього хімічні зв'язки, зображені однією суцільною лінією, паралельною одній пунктирній лінії, охоплюють як одинарний, так і подвійний (наприклад, ароматичний) зв'язки, якщо дозволяють валентності. Структури, які представляють сполуки з одним або більше хіральними центрами, але які не означають стереохімію (наприклад, жирні або пунктирні лінії), охоплюють чисті стереоізомери і їх суміші (наприклад, рацемічні суміші). Подібно цьому назви сполук, що мають один або більше хіральних центрів, які не відображають стереохімію вказаних центрів, охоплюють чисті стереоізомери і їх суміші. 5.2. Тверді форми Даний винахід спрямований на тверді форми безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5-триолу: 2 UA 106048 C2 5 10 15 20 25 30 35 40 45 50 Один варіант здійснення даного винаходу спрямований на тверді аморфні форми. Інший спрямований на тверді кристалічні форми. Окрема кристалічна форма, яка називається в цьому документі формою 1, має ендотерму диференціальної скануючої калориметрії (DSC) приблизно 124 °C. У даному контексті термін "приблизно" означає ±5,0 °C. В одному варіанті здійснення даного винаходу форма дає порошкову рентгенограму (XRPD), яка містить піки при одному або більше значеннях, що становлять приблизно 4,0, 8,1, 9,8, 14,0 і/або 19,3 градусів 2θ. У даному контексті термін "приблизно" означає ±0,3 градуси. Як добре відомофахівцям, відносна інтенсивність піків в картині XRPD може варіюватися в залежності від того, як був виготовлений зразок і як здійснювався збір даних. З урахуванням вищесказаного приклад рентгенограми XRPD вказаної форми приводиться на фігурі 1. В одному варіанті здійснення даного винаходу форма дає раманівський спектр з піками при одному або більше значеннях, що становлять 3068, 2929, 2888, 2881, 1615, 1603, 1244, 1037, -1 -1 692 і/або 372 см . У даному контексті термін "приблизно" означає ±2 см . Як добре відомо фахівцям, відносна інтенсивність піків в раманівському спектрі може варіюватися в залежності від того, як був виготовлений зразок і як здійснювався збір даних. З урахуванням вищесказаного приклад FT-раманівського спектра вказаної форми приводиться на фігурі 2. Окрема кристалічна форма, яка називається в цьому документі формою 2, має ендотерму диференціальної скануючої калориметрії (DSC) приблизно 134 °C. У даному контексті термін "приблизно" означає ±5,0 °C. В одному варіанті здійснення даного винаходу форма дає картину XRPD, яка містить піки при одному або більше значеннях, що становлять 4,4, 4,8, 14,5, 14,7, 15,5, 21,2, 22,1 і/або 23,8 градусах 2θ. У даному контексті термін "приблизно" означає ±0,3 градуси. Приклад картини XRPD вказаної форми приводиться на фігурі 3. В одному варіанті здійснення даного винаходу форма дає раманівський спектр з піками на -1 одному або більше приблизно 3061, 2927, 2877, 2864, 1605, 1038, 842 і/або 719 см . У даному -1 контексті термін "приблизно" означає ±2 см . Приклад FT-раманівського спектра вказаної форми приводиться на фігурі 4. Даний винахід охоплює композиції, що включають в себе різні кристалічні форми безводного (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5триолу. Даний винахід охоплює також тверді речовини, які являють собою суміші як аморфної, так і кристалічної форм сполуки. Деякі вказані тверді речовини включають в себе кристалічний (2S, 3R, 4R, 5S, 6R)-2-(4-хлор-3-(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2Н-піран-3,4,5триол в кількості щонайменше приблизно 50, 75, 80, 85, 90, 95 або 99 масових процентів. 5.3. Способи застосування Даний винахід охоплює спосіб інгібування активності SGLT2, який включає в себе контактування SGLT2 з ефективною кількістю сполуки згідно з даним винаходом (наприклад, сполуки, описаної в цьому документі). В одному варіанті здійснення даного винаходу білок знаходиться in vivo. В іншому він знаходиться ех vivo. Винахід охоплює також спосіб зниження рівня глюкози в крові пацієнта (наприклад, ссавця, такого як людина, собака або кішка), який включає введення пацієнту ефективної кількості сполуки згідно з даним винаходом. Винахід охоплює також спосіб підвищення екскреції глюкози з сечею пацієнта, який включає введення пацієнту ефективної кількості сполуки згідно з даним винаходом. Винахід охоплює також спосіб відновлення або підвищення чутливості до інсуліну у пацієнта, який включає введення пацієнту ефективної кількості сполуки згідно з даним винаходом. Винахід охоплює також спосіб лікування, контролю або запобігання захворюванню або розладу у пацієнта, який включає в себе введення пацієнту терапевтично або профілактично ефективної кількості сполуки згідно з даним винаходом. Приклади захворювань і розладів включають в себе атеросклероз, серцево-судинне захворювання, діабет (1 і 2 типів), гіперглікемію, розлади ліпідного обміну, ожиріння і синдром Х. Особливим захворюванням є діабет 2 типу. 3 UA 106048 C2 5 10 15 20 25 30 35 40 45 50 55 60 Кількість, шлях введення і схема введення сполуки можуть залежати від таких чинників, як конкретне показання для лікування, профілактики або контролю, а також віку, статі і стану пацієнта. Ролі, які грають вказані чинники, добре відомі фахівцям і можуть підбиратися шляхом звичайного експериментування. 5.4. Фармацевтичні композиції Даний винахід охоплює фармацевтичні композиції, що включають в себе одну або більше сполук згідно з даним винаходом. Певні фармацевтичні композиції являють собою препаративні форми, відповідні для перорального, черезслизового (наприклад, назального, сублінгвального, вагінального, букального або ректального), парентерального (наприклад, підшкірного, внутрішньовенного, болюсної ін'єкції, внутрішньом'язового або внутрішньоартеріального) або черезшкірного введення пацієнту. Приклади препаративних форм включають, без обмеження, таблетки, капсули, такі як м'які еластичні желатинові капсули, крохмальні капсули, пастилки, коржики, дисперсії, супозиторії, мазі, припарки, пасти, порошки, пов'язки, креми, пластири, розчини, накладки, аерозолі (наприклад, назальніспреї або інгалятори), гелі, рідкі препаративні форми, відповідні для перорального або черезслизового введення пацієнту, включаючи суспензії (наприклад, водні або неводні рідкі суспензії, емульсії типу "масло у воді" або рідкі емульсії типу "вода в маслі"), розчини і еліксири, рідкі препаративні форми, відповідні для парентерального введення пацієнту, і стерильні тверді речовини (наприклад, кристалічні або аморфні тверді речовини), які можна розчиняти з одержанням рідких препаративних форм, відповідних для парентерального введення пацієнту. Композиція повинна відповідати способу введення. Наприклад, пероральне введення вимагає наявності ентеросолюбільних покриттів, щоб захистити сполуку згідно з даним винаходом від розкладання в шлунково-кишковому тракті. Подібно цьому композиція може містити інгредієнти, які полегшують доставку активного інгредієнта (інгредієнтів) до місця дії. Наприклад, сполуку можна вводити в ліпосомальних композиціях з метою захистити їх від розкладаючих ферментів, полегшити транспорт в кровоносну систему і вплинути на доставку через клітинні мембрани до внутрішніх дільниць клітини. Композиція, форма і тип препаративної форми буде залежати від її застосування. Наприклад, препаративна форма, яку використовують при невідкладному лікуванні захворювання, може містити більш високі кількості одного або більше активних інгредієнтів, ніж ті кількості, які вона містить, коли препаративна форма використовується для постійного лікування того ж захворювання. Подібно цьому парентеральна препаративна форма може містити більш низькі кількості одного або більше активних інгредієнтів, ніж ті кількості, які вона містить, коли пероральна препаративна форма використовується для лікування того ж захворювання. Вказані і інші чинники, внаслідок яких конкретні препаративні форми згідно з даним винаходом будуть відрізнятися одна від одної, будуть очевидними для фахівця. Див., наприклад, Remington's Pharmaceutical Sciences, 18-е вид., Mack Publishing, Easton PA (1990). 5.4.1. Пероральні препаративні форми Фармацевтичні композиції згідно з даним винаходом, придатні для перорального введення, можуть бути представлені у вигляді дискретних препаративних форм, таких як, без обмеження, таблетки (наприклад, жувальні таблетки), таблетки в формі капсул, капсули і рідин (наприклад, сиропи з коригентами). Вказані препаративні форми містять заздалегідь визначені кількості активних інгредієнтів і можуть бути виготовлені способами, добре відомими фахівцям в галузі фармації. Див., наприклад, Remington's Pharmaceutical Sciences, 18-е вид., Mack Publishing, Easton PA (1990). Типові пероральні препаративні форми виготовляють комбінуванням активного інгредієнта (інгредієнтів) в ретельній суміші з щонайменше одним наповнювачем, згідно із звичайними фармацевтичними технологіями виготовлення лікарських речовин. Наповнювачі можуть мати цілий ряд форм в залежності від форми препарату, бажаної для введення. Внаслідок простоти введення таблетки і капсули являють собою найбільш вигідні пероральні дозовані препаративні форми. Якщо це бажано, на таблетки можна наносити покриття з використанням стандартних водних або неводних технологій. Вказані препаративні форми можна виготовляти звичайними фармацевтичними способами. Звичайно фармацевтичні композиції і препаративні форми виготовляють шляхом однорідного і ретельного змішування активних інгредієнтів з рідкими носіями, високодисперсними твердими носіями або і з тими, і з іншими, а потім шляхом надання продукту бажаної форми, якщо це необхідно. Розпушувачі можна включати в тверді препаративні форми для полегшення швидкого розчинення. Змащувальні агенти також можна включати для полегшення виготовлення препаративних форм (наприклад, таблеток). 5.4.2. Парентеральні препаративні форми 4 UA 106048 C2 5 10 15 20 25 30 35 40 45 50 55 60 Парентеральні препаративні форми можна вводити пацієнтам різними шляхами, включаючи, без обмеження, підшкірний, внутрішньовенний (включаючи болюсну ін'єкцію), внутрішньом'язовий і внутрішньоартеріальний. Оскільки їх введення звичайно мине природні захисні бар'єри проти контамінантів, парентеральні препаративні форми спеціально виготовляються стерильними або здатними до стерилізації перед введенням пацієнту. Приклади парентеральних препаративних форм включають в себе, без обмеження, розчини, готові для ін'єкції, сухі продукти, готові для розчинення або суспендування в фармацевтично прийнятному носії для ін'єкції, суспензії, готові для ін'єкції, і емульсії. Відповідні носії, які можна використати для виготовлення парентеральних препаративних форм, добре відомі фахівцям. Приклади включають в себе, без обмеження, воду для ін'єкцій USP; водні носії, такі як, без обмеження, фізіологічний розчин, розчин Рінгера, розчин декстрози, розчин декстрози і хлориду натрію і розчин Рінгера з лактатом; носії, що змішуються з водою, такі як, без обмеження, етиловий спирт, поліетиленгліколь і поліпропіленгліколь; і неводні носії, такі як, без обмеження, кукурудзяна олія, бавовняна олія, арахісова олія, кунжутна олія, етилолеат, ізопропілміристат і бензилбензоат. 5.4.3. Черезшкірне, місцеве і черезслизове введення Черезшкірні, місцеві і черезслизові препаративні форми включають в себе, без обмеження, офтальмологічні розчини, спреї, аерозолі, креми, лосьйони, мазі, гелі, розчини, емульсії, суспензії або інші форми, відомі фахівцям. Див., наприклад, Remington's Pharmaceutical Sciences, 16-е і 18-е вид., Mack Publishing, Easton PA (1980 & 1990) і Introduction to Pharmaceutical Dosage Forms, 4-е вид., Lea & Febiger, Philadelphia (1985). Черезшкірні препаративні форми включають в себе накладки "резервуарного типу" або "матриксного типу", які можна закріпляти на шкірі і носити протягом певного періоду часу, щоб здійснювалося проникнення бажаної кількості активних інгредієнтів. Відповідні наповнювачі (наприклад, носії і розріджувачі) і інші матеріали, які можна використати для виготовлення черезшкірних, місцевих і черезслизових препаративних форм, добре відомі фахівцям в галузі фармацевтики і залежать від конкретної тканини, на яку наносять дану фармацевтичну композицію або препаративну форму. У залежності від конкретної тканини, що піддається лікуванню, можна використати додаткові компоненти до лікування, в поєднанні з лікуванням або після лікування активними інгредієнтами згідно з даним винаходом. Наприклад, підсилювачі проникнення можна використати, щоб сприяти доставці активних інгредієнтів в тканину. рН фармацевтичної композиції або препаративної форми або тканини, на яку наносять фармацевтичну композицію або препаративну форму, також можна підбирати таким чином, щоб поліпшити доставку одного або більше активних інгредієнтів. Подібно цьому полярність розчинника, що служить носієм, його іонну силу або тонічність можна підбирати таким чином, щоб поліпшити доставку. Такі сполуки як стеарати, також можна додавати в фармацевтичні композиції або препаративні форми для зміни у вигідну сторону гідрофільності або ліпофільності одного або більше активних інгредієнтів таким чином, щоб поліпшувати доставку. З цієї точки зору стеарати можуть служити як ліпідний носій для композиції, як емульгуючий агент або поверхнево-активний агент і як агент, поліпшуючий доставку або поліпшуючий проникнення. Різні солі, гідрати або гідрати активних інгредієнтів можна використати для подальшого підбору властивостей композиції, що одержується. 6. ПРИКЛАДИ Особливості даного винаходу можна зрозуміти з наступних прикладів. 6.1. Синтез (3aS, 5R, 6S, 6aS)-6-гідрокси-2,2-диметилтетрагідрофуро[2,3-d][1,3]діоксол-5іл)(морфоліно)метанону У 12 л тригорлу колбу з круглим дном з механічної мішалкою, гумовою пробкою з температурним датчиком і газовим барботером вміщували L-(-)ксилозу (504,40 г, 3,360 моль), ацетон (5 л, реагентний сорт) і порошок безводного MgSO 4 (811,23 г, 6,740 моль/2,0 екв.). Суспензію починали перемішувати при кімнатній температурі, а потім додавали концентровану H2SO4 (50 мл, 0,938 моль/0,28 екв.). Спостерігалася повільна слаба екзотермічна реакція (температура зростала до 24 °C протягом приблизно 1 год.), і реакцію залишали перемішуватися при кімнатній температурі протягом ночі. Через 16,25 години ТШХ показала, що вся L-ксилоза прореагувала, а основним продуктом був біс-ацетонід з деякою кількістю (3aS, 5S, 6R, 6aS)-5-(гідроксиметил)-2,2-диметилтетрагідрофуро[2,3-d][1,3]діоксол-6-ола. Реакційну суміш фільтрували, а зібрані тверді речовини двічі промивали ацетоном (по 500 мл). Фільтрат жовтого кольору, що перемішується, нейтралізували концентрованим розчином NH 4OH (39 мл) до рН=8,7. Після перемішування протягом 10 хв. суспендовані тверді речовини видаляли фільтруванням. Фільтрат концентрували з одержанням сирої проміжної речовини біс-ацетоніду 5 UA 106048 C2 5 10 15 20 25 30 35 40 45 50 55 60 у вигляді масла жовтого кольору (725,23 г). Масло жовтого кольору суспендували в 2,5 л води при перемішуванні в 5 л тригорлій колбі з круглим дном з механічною мішалкою, гумовою пробкою з температурним датчиком і газовим барботером. рН з 9 доводили до 2 з використанням 1Н водної HСl (142 мл) і перемішували при кімнатній температурі протягом 6 год., поки ГХ не показувала достатню конверсію проміжної речовини біс-ацетоніду в (3aS, 5S, 6R, 6aS)-5-(гідроксиметил)-2,2-диметилтетрагідрофуро[2,3-d][1,3]діоксол-6-ол. Реакційну суміш нейтралізували доданням 50 % мас. водного розчину K2HPO4 до рН=7. Розчинник потім випаровували і додавали етилацетат (1,25 л), з одержанням суспензії білого кольору, яку потім фільтрували. Фільтрат концентрували в умовах вакууму, з одержанням масла оранжевого кольору, яке розчиняли в 1 л метилтрет-бутилового ефіру. Вказаний розчин мав KF 0,23 % мас. води і був сконцентрований з одержанням (3aS, 5S, 6R, 6aS)-5-(гідроксиметил)-2,2диметилтетрагідрофуро[2,3-d][1,3]діоксол-6-ола у вигляді масла оранжевого кольору (551,23 г, 1 , вихід 86 %, 96,7 % чистоти по ГХ). H ЯМР (400 МГц, ДМСО-д6) δ 1,22 (с, 3H) 1,37 (с, 3H) 3,51 (дд, J=11,12, 5,81 Гц, 1H), 3,61 (дд, J=11,12, 5,05 Гц, 1H), 3,93-4,00 (м, 1H), 3,96 (с, 1H), 4,36 (д, 13 J=3,79 Гц, 1H), 4,86 (шир.с, 2H), 5,79 (д, J=3,54 Гц, 1H). C ЯМР (101 МГц, ДМСО-d6) δ 26,48, 27,02, 59,30, 73,88, 81,71, 85,48, 104,69, 110,73. До розчину (3aS, 5S, 6R, 6aS)-5-(гідроксиметил)-2,2-диметилтетрагідрофуро[2,3d][1,3]діоксол-6-ола (25,0 г, 131 ммоль) в ацетоні (375 мл, 15Х) і Н2О (125 мл, 5Х) додавали NaHCO3 (33,0 г, 3,0 екв.), NaBr (2,8 г, 20 моль%) і TEMPO (0,40 г, 2 моль%) при 20 °C. Суміш охолоджували до 0-5 °C, а потім по частинах додавали тверду трихлорізоціанурову кислоту (ТССА, 30,5 г, 1,0 екв.). Суспензію перемішували при 20 °C протягом 24 год. Додавали метанол (20 мл) і суміш перемішували при 20 °C протягом 1 год. На даній стадії утворювалася суспензія білого кольору. Суміш фільтрували, промивали ацетоном (50 мл, 2Х). Органічний розчинник видаляли в умовах вакууму, а водний шар екстрагували з використанням EtOAc (300 мл, 12Х×3), і об'єднані органічні шари концентрували з одержанням маслянистої суміші з деякою кількістю твердого залишку. Ацетон (125 мл, 5Х) додавали і суміш перемішували. Розчин в ацетоні потім концентрували з одержанням бажаної кислоти (3aS, 5R, 6S, 6aS)-6-гідрокси-2,2диметилтетрагідрофуро[2,3-d][1,3]диоксол-5-карбонової кислоти у вигляді твердої речовини 1 жовтого кольору (21,0 г, 79 %). H ЯМР (метанол-д4), δ 6,00 (д, J=3,2 Гц, 1H), 4,72 д, J=3,2 Гц, 1H), 4,53 (д, J=3,2 Гц, 1H), 4,38 (д, J=3,2 Гц, 1H), 1,44 (с, 3H), 1,32 (с, 3H). До розчину (3aS, 5R, 6S, 6aS)-6-гідрокси-2,2-диметилтетрагідрофуро[2,3-d][1,3]діоксол-5карбонової кислоти (5,0 г, 24,5 ммоль) в TНF (100 мл, 20Х) додавали ТВТИ (11,8 г, 1,5 екв.), Nметилморфолін (NMM, 4,1 мл, 1,5 екв.), і суміш перемішували при 20 °C протягом 30 хв. Потім додавали морфолін (3,2 мл, 1,5 екв.), і реакційну суміш перемішували при 20 °C ще протягом 6 год. Тверду речовину відфільтровували, а осад, що залишився на фільтрі, промивали з використанням TGF (10 мл 2Х×2). Органічний розчин концентрували в умовах вакууму і залишок очищали з використанням хроматографії на колонці з силікагелем (гексани: EtOAc, від 1:4 до 4:1), з одержанням 4,3 г бажаного морфолінового аміду (64 %) у вигляді твердої речовини 1 , білого кольору. H ЯМР (CDCl3) δ 6,02 (д, J=3,2 Гц, 1H), 5,11 (шир.с, 1H), 4,62 (д, J=3,2 Гц, 1H), 4,58 (д, J=3,2 Гц, 1H), 3,9-3,5 (м, 8H), 1,51 (с, 3H), 1,35 (с, 3H). 6.2. Альтернативний синтез (3aS, 5R, 6S, 6aS)-6-гідрокси-2,2-диметилтетрагідрофуро[2,3d][1,3]діоксол-5-іл)(морфоліно)метанону Розчин діола (3aS, 5S, 6R, 6aS)-5-(гідроксиметил)-2,2-диметилтетрагідрофуро[2,3d][1,3]діоксол-6-ола в ацетонітрилі (5,38 кг, 65 % мас., 3,50 кг активного, 18,40 моль), ацетонітрил (10,5 л) і ТЕМРО (28,4 г, 1 моль%) додавали в розчин К 2НРО4 (0,32 кг, 1,84 моль) і КН2РО4 (1,25 кг, 9,20 моль) у воді (10,5 л). Розчин NaClO2 (3,12 кг, 80 % мас., 27,6 моль, 1,50 екв.) у воді (7,0 л) і розчин K2HPO4 (2,89 кг, 0,90 екв.) у воді (3,0 л) готували при охолоджуванні. Хлорне вапно (3,0 л, приблизно 6 % побутового сорту) змішували з розчином K2HPO4. Додавали приблизно 20 % розчини NaClO2 (1,6 л) і розчину хлорного вапна/K2HPO4 (400 мл, ~1 моль%). Залишки двох розчинів додавали одночасно. Реакційна суміш набувала темного червонокоричневого кольору, і спостерігалася повільна екзотермічна реакція. Швидкість додання розчину NaClO2 становила приблизно 40 мл/хв. (додання протягом 3-4 годин), а швидкість додання розчину хлорного вапна/K2HPO4 становила приблизно 10-12 мл/хв. (додання протягом 10 годин), при підтримці температури реакційної суміші 15-25 °C. Додатково здійснювали додання ТЕМРО (14,3 г, 0,5 моль%) кожні 5-6 годин, аж до закінчення реакції (звичайно досить двох додатків). Заповнювали азотом вільний простір над продуктом з використанням водного газоочисника, щоб запобігти накопиченню газу жовтувато-зеленого кольору в посудині. Реакційну суміш охолоджували до
ДивитисяДодаткова інформація
Назва патенту англійськоюSolid forms of (2s,3r,4r,5s,6r)-2-(4-chloro-3-(4-ethoxybenzyl)phenyl)-6-(methylthio)tetrahydro-2h-pyran-3,4,5-triol and methods of their use
Автори російськоюde Paul, Susan, Margaret, Perlberg, Anett, Zhao, Matthew, Mangzhu
МПК / Мітки
МПК: C07H 5/00, A61P 3/10, A61K 31/70
Мітки: застосування, форми, 2s,3r,4r,5s,6r)-2-(4-хлор-3(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2н-піран-3,4,5-тріолу, тверді
Код посилання
<a href="https://ua.patents.su/15-106048-tverdi-formi-2s3r4r5s6r-2-4-khlor-34-etoksibenzilfenil-6-metiltiotetragidro-2n-piran-345-triolu-i-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Тверді форми (2s,3r,4r,5s,6r)-2-(4-хлор-3(4-етоксибензил)феніл)-6-(метилтіо)тетрагідро-2н-піран-3,4,5-тріолу і їх застосування</a>
Попередній патент: Спосіб отримання високої щільності життєздатних клітин в культурі клітин ссавців
Наступний патент: Спосіб зниження швидкості ферментативного розщеплення гранул крохмалю у їжі та харчових продуктах, до складу яких входить крохмаль
Випадковий патент: Прилад для оберігання взуття від ковзання